文档内容
2025 年重庆市普通高中学业水平选择性考试
高三第一次联合诊断检测 化学参考答案
1~5 DCABD 6~10 DAACB 11~14 DBBC
1.D.解析:A选项,锰钢属于合金材料;B选项,聚乙烯是有机高分子材料;C选项,钢化玻璃是传统无机非
金属材料;D选项,光导纤维属于新型无机非金属材料。
2.C.解析略。
3.A.解析:A 选项,溶有CO 的水溶液中,Al3+、Ba2+、Cl-、I-能大量共存;B 选项,铁氰化钾与Fe2+会生
2
成沉淀;B不能大量共存;C选项,遇紫色石蕊显红色的溶液呈酸性,在酸性溶液中,[Al(OH) ]-、CO2-都要发
4 3
生反应,C不能大量共存;D选项,水电离出的c(H+)=1×10-13 mol·L-1的溶液可能是酸性溶液,也可
能是碱性溶液,NH+会与碱反应,HCO-既可与酸反应又能与碱反应,D不能大量共存。
4 3
4.B.解析:A选项,电负性:O>N>H,A错误;B选项,基态N、S、K原子核外未成对电子数分别是3、2、
1,B正确;C选项,第一电离能:N>O>C,C错误;D选项,K元素在s区,不在p区,D错误。
5.D.解析:A选项,乙酸乙酯与NaOH溶液会发生反应,A错误;B选项,会发生倒吸,正确装置水应在上
层,下层可选择CCl ,B错误;C选项,CO 会与Na CO 溶液反应,C错误。
4 2 2 3
6.D.解析:A选项,Ⅰ中含碳碳双键,Ⅱ中没有碳碳双键,A正确;B选项,Ⅰ的碳碳双键中其中一个碳原子
上连有两个 H 原子,不存在顺反异构,B 正确;C 选项,Ⅰ→Ⅱ属于加聚反应,原子利用率为 100%,C
正确;D选项,Ⅱ中有酯基,在酸或碱的条件下均要发生水解,D错误。
7.A.解析:由题意可知,X是Fe,a是Cl ,b是FeCl ,c是FeCl ,d是Fe O 。A选项,Cl 无漂白性,A错
2 2 3 2 3 2
误;B 选项,Fe 元素是人体必需的微量元素,B 正确;C 选项,Fe 与水蒸气反应可生成 Fe O 和 H ,C
3 4 2
正确;D选项,苯酚遇FeCl 的水溶液显紫色,D正确。
3
8.A.解析:由题意推出 X、Y、Z、W、M、G 分别为元素 H、C、N、O、S、Fe;MW 、X M、X W 分别为
3 2 2
SO 、H S、H O,键角大小为:SO >H O>H S。
3 2 2 3 2 2
9.C.解析:A选项,制取Fe(OH) 胶体需向沸水中滴加几滴饱和FeCl 溶液,题目中的操作得到的是Fe(OH)
3 3 3
沉淀,A错误;B选项,制Cu(OH) 悬浊液是向2mL10%NaOH溶液中滴入5滴5% CuSO 溶液,B错误;
2 4
D选项,如果溶液中有Cl-也会使KMnO 溶液褪色,D错误。
4
10.B.解析:Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ分别代表Cu2+、Cu(NH )2+、Cu(NH )2+、Cu(NH )2+、Cu(NH )2+的变化曲线,
3 3 2 3 3 3 4
A选项, Cu2+在溶液中发生水解反应,CuSO 溶液中,c(Cu2+)<c(SO2-),A错误;B选项,由图可知,
4 4
B正确;C选项,第③步是Cu(NH )2++NH Cu(NH )2+,K=1×102.9,C错误;D选项,溶液中还含有
3 2 3 3 3
其他离子,D错误。
第一次联合诊断检测(化学)第5页 共8页11.D.解析:该晶胞中有8个K+,4个阴离子,阴离子的配位数为8,A、B选项均错误;C选项,两个K+
M
之间的最短距离为0.5anm,C选项错误;D选项,1个晶胞中含有4个X,每个X的质量为 g,
N
A
4M1021
晶胞的密度为 g·cm-3。
N a3
A
12.B.解析: H =3 H - H =(3a-b) kJ·mol-1, H <0,E -E =(b-3a) kJ·mol-1。
1 2 3 1 逆 正
13.B.解析:A△选项,△Mn元△素的化合价发生了变化,发△生了氧化还原反应,A错误;B选项,充电时,发生
反应为:NaMnO +C →Na MnO +Na C ,Mn元素化合价升高,钠离子在锰基材料上脱出,B正确;
2 n 1-x 2 x n
C选项,放电时负极反应为Na C -xe-=xNa++C ,C错误;D选项,充电时,外电路中转移4mol e-,
x n n
锰基材料脱出4mol Na+,质量减少92g,D错误。
14.C.解析:由题可知,Ⅱ是绝热容器,且该反应为放热反应。容器Ⅱ中温度高于容器Ⅰ,则KⅠ >KⅡ ,起始
物质的量相同,则Ⅱ中 A 的平衡转化率小;A、B 选项错误;C 选项,从方程式看,容器减少压强,就
是A减少的压强,故容器Ⅰ中A减少的压强为100-85=15kPa,容器Ⅰ中v(A)=15/8=1.875kPa/min,
C选项正确;D选项,v >v ,D选项错误。
x y
15.(14分)
(1)+6(2分) (2分)
焙烧
(2)2MoS +6Na CO +9O 2Na MoO +4Na SO +6CO (2分) NH (1分)CO (1分)
2 2 3 2 2 4 2 4 2 3 2
(3)增大NH+浓度,促进NH VO 尽可能完全析出(2分)
4 4 3
(4)为使Fe3+、Cu2+、Al3+沉淀完全,Cu2+需要的pH最大,Cu2+沉淀完全需要的pH大于6.5(2分)
(5)22.4n(2分)
解析:(4)为使Fe3+、Cu2+、Al3+沉淀完全,Cu2+需要的pH最大,Cu2+沉淀完全时,
1020
c(OH-)> 107.5,pH>14-7.5=6.5。
1.0105
(5)将离子方程配平得aAl3++bFe3++nHCO-+mSO2-=Al Fe (OH) (SO ) ↓+nCO ↑,生成1mol沉淀,同时
3 4 a b n 4 m 2
生成n mol CO ,在标准状况的体积为22.4n L。
2
16.(15分)
(1)球形冷凝管(1分)检查是否漏液(1分)
(2)高锰酸钾(或次氯酸钠、氯酸钾等,合理答案给分)(2分)
(3)c→d→e→f→g→h(2分)
(4)B(OCH ) +6Cl
65℃75℃
BCl +3CO+9HCl(2分)水浴加热(1分)
3 3 2 3
(5)未处理反应产生的有毒气体CO,会对环境造成污染(2分)
第一次联合诊断检测(化学)第6页 共8页(6)①为了覆盖AgCl,防止AgCl与KSCN反应导致结果偏低(2分)
35.5(cV cV )
② 1 1 2 2 (2分)
a
解析:(6)有关系式:Ag+~Cl-;Ag+~SCN-,n(Ag+) =c ×V ×10-3,n(SCN-)=c ×V ×10-3,
总 1 1 2 2
ag产品中n(Cl)=( c ×V ×10-3-c ×V ×10-3) ×250/25
1 1 2 2
产品中氯元素的质量分数为:
250
(c V 103c V 103) 35.5
1 1 2 2 25 100%= 35.5(c 1 V 1 c 2 V 2 ) %
a a
17.(14分)
(1)①反应Ⅰ=反应Ⅱ+反应Ⅲ,K =K ×K =1.0×2.5=2.5(2分)
1 2 3
3
②CO*(g)+2H (g)→HCO*(g)+ H (g)(2分) 0.94(0.95也给分,2分)
2 2
2
(2)①bc(1分) ②5.75(2分)
(3)①B(1分) ②CO +6e-+6H+=CH OH+H O(2分) ③81(2分)
2 3 2
91
解析:(1)② 6.021023 0.94
1.61022
(2)②平衡时H O(g)的分压为0.25p kPa,n(H O)∶0.25 p =4∶p ,得平衡时n(H O)=1mol,
2 0 2 0 0 2
CH OH(g)2H (g)+CO(g);
3 2
起始(mol) 2
转化(mol) 1.8 3.6 1.8
CO(g)+H O(g)H (g)+CO (g)
2 2 2
起始(mol) 1.8 2 3.6
转化(mol) 1 1 1 1
平衡(mol) 0.8 1 4.6 1
4.6 1
( p)( p)
n n
K = 总 总 =5.75
p 0.8 1
( p)( p)
n n
总 总
(3)电解时阴极反应为CO +6e-+6H+=CH OH+H O,阳极反应为4OH--4e-=2H O+O ↑,48g CH OH
2 3 2 2 2 3
物质的量为1.5mol,电路中转移9mole-,双极膜向阳极室移动9mol OH-,阳极室放出O :9/4=2.25mol,
2
阳极室溶液增加的质量为:9×17-2.25×32=81g。
18.(15分)
(1)15(1分) 醚键、氨基(2分)
(2)取代反应(2分) 还原反应(2分)
第一次联合诊断检测(化学)第7页 共8页(3) (2分,产物写Li CO 、LiHCO 可给分)
2 3 3
(4) (2分)
(5)16(2分)
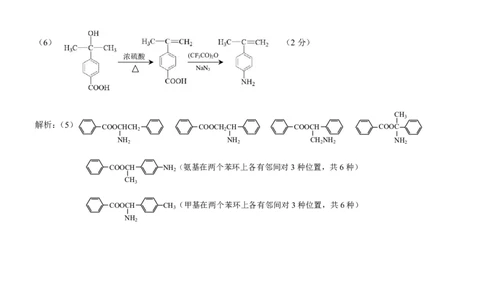
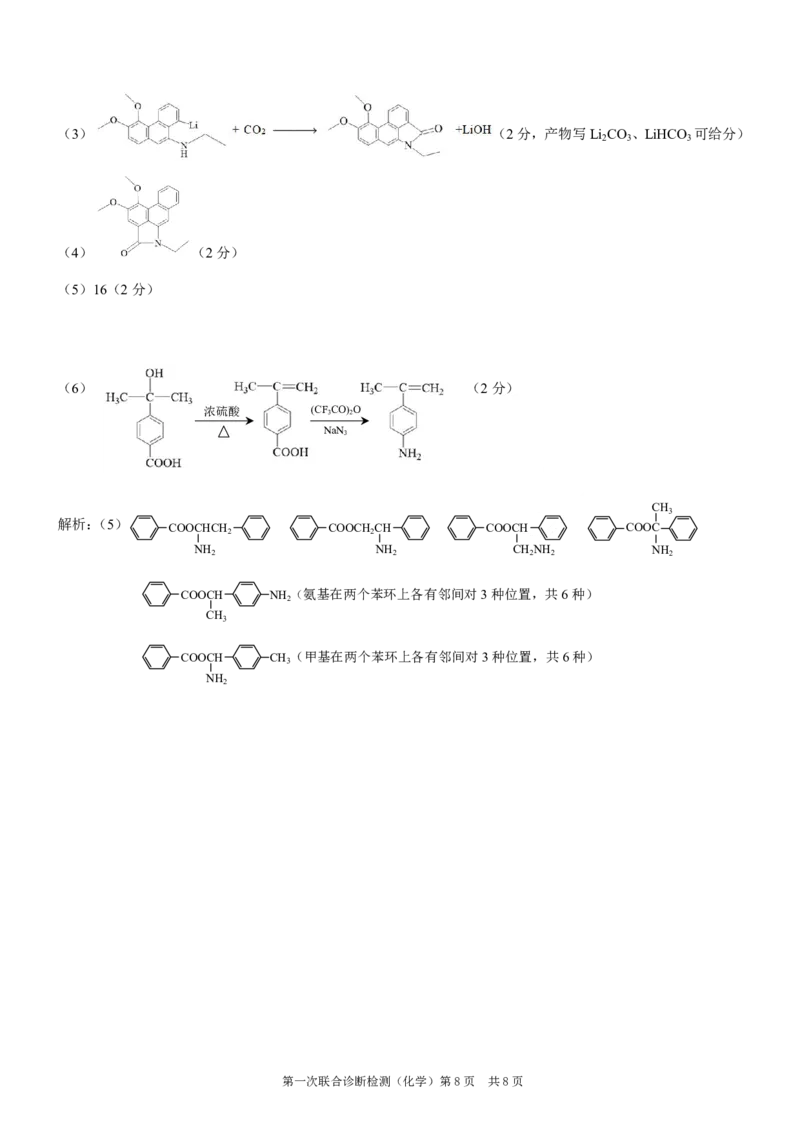
(6) (2分)
浓硫酸 (CF
3
CO)
2
O
NaN
3
CH
3
解析:(5)
COOCHCH COOCHCH COOCH COOC
2 2
NH NH CHNH NH
2 2 2 2 2
COOCH NH(氨基在两个苯环上各有邻间对3种位置,共6种)
2
CH
3
COOCH CH(甲基在两个苯环上各有邻间对3种位置,共6种)
3
NH
2
第一次联合诊断检测(化学)第8页 共8页