文档内容
二、化学选择题(本大题包括12个小题,每小题只有一个选项符合题意, 11~18小题每题1
分,19~22小题每题2分,共16分)
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Fe-56
11.下列属于化学变化的是
A.粗盐提纯 B.葡萄酿酒 C.冰雪融化 D.酒精挥发
12.下列实验操作正确的是
带火星的木条
A.滴加液体 B.测溶液PH C.氧气验满 D.蒸发食盐水
13.下列关于分子、原子的说法正确的是
A.分子可分而原子不可分 B.分子间有间隔而原子间没有间隔
C.分子的质量一定比原子质量大 D.分子、原子都可以直接构成物质
14.下列说法错误的是
A.溶液中溶剂不一定都是水 B.可燃物温度达到着火点一定会燃烧
C.点燃可燃性气体前一定要验纯 D.生成盐和水的反应不一定是中和反应
15.白菜生长过程中不茂盛,叶子发黄,应施加的化肥是
A.CO(NH) B.KSO C.Ca (PO ) D.KH PO
2 2 2 4 3 4 2 2 4
16.下列实验现象描述正确的是
A.二氧化碳通入紫色石蕊试液中,溶液由紫色变为红色
B.铁丝在空气中剧烈燃烧,火星四射
C.红磷在空气中燃烧产生大量白雾
D.涤纶和羊毛点燃时都可闻到烧焦羽毛的气味
17.下列有关化学用语说法正确的是
A.AlO表示氧化铝 B.H 表示两个氢原子
2
C.2Fe2+表示两个铁离子 D.在SO 、S、HS中,硫元素化合价依次降低
2 2
18.食品安全是人类健康永恒的话题,下列做法正确的是
A.用甲醛溶液浸泡海产品 B.烹调食物时不能用亚硝酸钠代替食盐
C.霉变的大米用水清洗后可以食用 D.油炸食品要常吃,以补充能量
19.草莓、香蕉等水果都具有芳香的气味,是因为其中含有乙酸乙酯(C HO)等物质。关于乙
4 8 2
酸乙酯的说法错误的是
A.它是有机物 B.它的一个分子中含有14个原子
C.其中C、H、O元素质量比为2∶4∶1 D.它的相对分子质量为88
20.下列每组中的两种固体物质,只用水做试剂,不能将其鉴别出来的是
A.NaCl、NaSO B.CaCO 、NaCO C.CuSO 、NaSO D.NH NO 、NaCl
2 4 3 2 3 4 2 4 4 3
21.下列各组离子在水中一定能大量共存,并形成无色溶液的是
A.Cu2+、SO 2-、Cl- B.Ca2+ 、CO2-、NO -
4 3 3
1C.NH +、 OH - 、 NO - D.Na+ 、 K+ 、SO 2-
4 3 4
22.下列除去杂质的方法中,正确的是
选项 括号内为杂质 方 法
A CO(HCl气体) 通过足量的NaOH溶液
2
B KCl (KClO) 加入少量MnO 加热
3 2
C NaCl(NaCO) 加入足量的盐酸后蒸干
2 3
D Fe(Cu) 加入足量的稀HSO 后过滤
2 4
化 学 部 分
八、填空题(本大题包括4个小题,共18分)
45. (4分)用化学式填空
(1)生理盐水中的溶质 (2)空气中含量最多的气体
(3)胃液中含有的酸 (4)焙制糕点所用发酵粉的主要成分
46. (4分)用所学的化学知识填空
(1)防毒面具中使用了活性炭,这是利用了活性炭的
(2)洗涤剂能去除油污,是因为它具有 功能
(3)用微粒的观点解释:一氧化碳有毒而二氧化碳无毒的原因是
(4)铝在空气中具有很好耐腐蚀性的原因
47.(5分)饺子是中国传统食品,是吉祥幸运的象征。小明通过妈妈包饺子的过程发现了许多
化学知识。
(1)包饺子所用的原料包括面粉、水、牛肉、芹菜、食盐、植物油等,它们含多种营养素。其
中牛肉富含的营养素是
(2)调馅时使用铁强化酱油,酱油中加铁是为了防止
(3)煮饺子用的炊具是不锈钢锅,不锈钢属于 (填“金属材料”或“合成材料”)
(4)煮饺子过程中发现锅被熏黑,产生这种现象的原因是
(5)饺子煮熟后关闭燃气阀门,此灭火原理是
48.(5分)水是生命之源,为了更好保护我们的鸭绿江水,某小组同学进行了下列有关研究。
(1)鸭绿江水属于 (填“纯净物”或“混合物”);为了检验江水是硬水还是软水,可
向水中加 检验
(2)可采用 来测定江水的酸碱度
(3)为了防止江水污染,下列做法正确的是 (填字母)
A.工业废水处理后再排放 B.农业上合理使用农药化肥
C.不向江中随意倾倒垃圾 D.不使用含磷洗衣粉
(4)小组同学想要证明水的组成,下列实验能达到目的的是 (填字母)
A.水的蒸发 B.水的蒸馏 C.水的电解 D.氢气在氧气中燃烧
2九、简答题(本大题包括4个小题,共20分)
49.(5分)甲、乙、丙三种固体物质在水中的溶解度曲线如右图所示。请回答:
(1)图中P点的意义是
甲
(2)若甲中混有少量的乙,最好采用 的方法提纯甲
溶解度/g
(3)使30℃接近饱和的甲溶液变成该温度下的饱和溶液,
60
可采用的一种方法是
(4)使50℃甲、乙、丙三种物质的饱和溶液降温到10℃,则 40 乙
P
其溶质质量分数不变的是
丙
(5)向100g 50℃的水中加入65g甲固体,发现全部溶解,
一段时间后又有部分甲的晶体析出。你认为“全部 0
10 30 50 温
溶解”的原因可能是 度/℃
50. (6分)能源是国家发展的命脉,与我们的生活息息相关。
(1)当前,南海问题引起我国政府的高度重视,南海蕴藏着丰富的油气资源。请写出天然
气主要成分燃烧的化学方程式
(2)一氧化碳既是一种重要的燃料,又常用于冶炼金属。请写出工业上用一氧化碳还原赤
铁矿(主要成分是氧化铁)的化学方程式
(3)某未知燃料燃烧的化学方程式为2X+5O 点 燃 4CO+2HO,据此可知:X的化学式
2 2 2
为 ,判断的依据是
51.(2分)右图是某原子结构示意图,回答下列问题
该原子最外层电子数为 , +8 2 6
由该数字你能获得的一条信息是
52.(7分)右图中:A、B、C、D、E、F、G是初中化学常见的物质,其中A为单质,B为氧化物,
C是大理石的主要成分,C和F属于不同类别的物
D
质,D 和 E 是配制农药波尔多液的两种原料。“
”表示两端的物质能发生反应,“ ”表示一种 A B C E
物质可转化为另一种物质。
G F
请回答:
(1)D和E发生反应的基本反应类型为
(2)完成下列化学方程式:
① A B的化学方程式
② B C的化学方程式
(3)物质F可以是 或 (具体写两种不同类别的物质)
3十、实验与探究题(本大题包括3个小题,共20分)
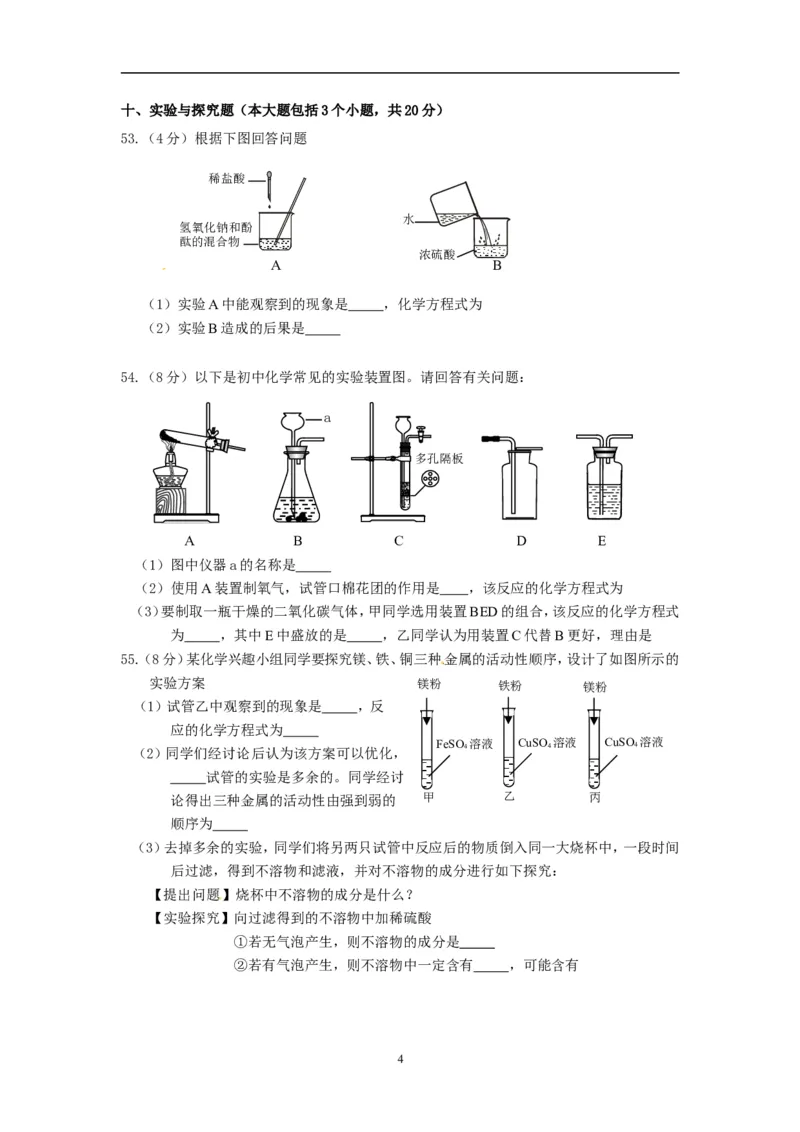
53.(4分)根据下图回答问题
稀盐酸
水
氢氧化钠和酚
酞的混合物
浓硫酸
A B
(1)实验A中能观察到的现象是 ,化学方程式为
(2)实验B造成的后果是
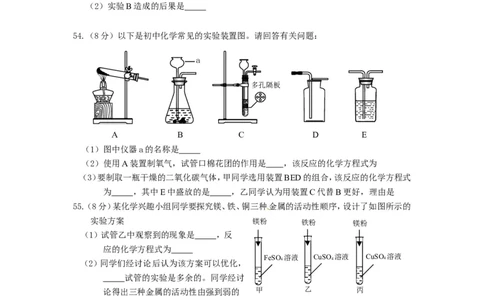
54.(8分)以下是初中化学常见的实验装置图。请回答有关问题:
a
多孔隔板
A B C D E
(1)图中仪器a的名称是
(2)使用A装置制氧气,试管口棉花团的作用是 ,该反应的化学方程式为
(3)要制取一瓶干燥的二氧化碳气体,甲同学选用装置BED的组合,该反应的化学方程式
为 ,其中E中盛放的是 ,乙同学认为用装置C代替B更好,理由是
55.(8分)某化学兴趣小组同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的
实验方案 镁粉 铁粉 镁粉
(1)试管乙中观察到的现象是 ,反
应的化学方程式为
(2)同学们经讨论后认为该方案可以优化, FeSO 4 溶液 CuSO 4 溶液 CuSO 4 溶液
试管的实验是多余的。同学经讨
论得出三种金属的活动性由强到弱的 甲 乙 丙
顺序为
(3)去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间
后过滤,得到不溶物和滤液,并对不溶物的成分进行如下探究:
【提出问题】烧杯中不溶物的成分是什么?
【实验探究】向过滤得到的不溶物中加稀硫酸
①若无气泡产生,则不溶物的成分是
②若有气泡产生,则不溶物中一定含有 ,可能含有
4十一、计算题(共6分)
56. 向20g赤铁矿样品中(样品中杂质不溶于水,也不和酸反应)不断加入稀盐酸至固体量不
再减少为止,共消耗稀盐酸184g,测得剩余固体的质量为4g。请计算:
(1)赤铁矿样品中,氧化铁的质量分数
(2)最后所得溶液中溶质的质量分数
52014年丹东市初中毕业生毕业升学考试化学参考答案
二、化学选择题
11、B; 12、C; 13、D; 14、B; 15、A; 16、A; 17、D; 18、B;
19、C; 20、A; 21、D; 22、C;
(化学方程式评分标准:除计算题外每式全对得2分,化学式书写正确得1分,其它各项全正
确得共1分)
八、填空题
45、(1)NaCl (2)N (3)HCl (4)NaHCO
2 3
46、(1)吸附性 (2)乳化 (3)分子构成不同(只要能体现分子不同,合理即可)
(4)铝能和空气中的氧气反应,表面形成致密的氧化膜,起保护作用。
(强调出形成致密的氧化膜即可)
47、(1)蛋白质 (2)贫血 (3)金属材料
(4)燃料不充分燃烧(或氧气不充足) (5)清除可燃物(合理即可)
48、(1)混合物 肥皂水(2)pH试纸(或pH计)(3)ABCD(漏选不得分)(4)CD(漏选不得分)
九、简答题
49、(1)10℃时,甲乙丙三种物质溶解度相等 (2)冷却热饱和溶液(或降温结晶)
(3)加溶质甲至不再溶解(或加溶质、加甲物质、蒸发溶剂也可。改变温度不得分)
(4)丙 (5)甲溶解时放热
50、(1)CH +2O
点燃
CO +2H O
4 2 2 2
(2)3CO + Fe O
高温
2 Fe + 3 CO
2 3 2
(3)C H 质量守恒定律 (或化学反应前后,原子的种类、数目不变)
2 2
51、 6 该元素是非金属元素
或该元素在化学反应中通常显-2价(元素写成原子不给分)
或该原子在化学反应中易得电子)(原子写成元素不给分)
52、(1)复分解反应 (2)①C +O
点燃
CO
2 2
(只要反应物中有O 或C , 生成物有CO 即可)
2 2
② Ca(OH) + CO == CaCO ↓+ HO
2 2 3 2
(3) Fe NaOH
(可溶性碱和活泼金属,不包括K Ca Na。写名称,化学式均可,顺序可以颠倒。)
十、实验探究题
[来源:Z&xx&k.Com]
53、(1)溶液由红色变为无色(或红色消失) NaOH + HCl == NaCl + H O
2
(2) 液体沸腾而飞溅(沸腾或飞溅都可以)
54、(1)长颈漏斗
△
(2)防止高锰酸钾粉末进入导管 2KMnO KMnO + MnO + O↑
4 2 4 2 2
(3)CaCO + 2HCl == CaCl + CO↑+ HO 浓硫酸(或浓HSO )
3 2 2 2 2 4
该装置能控制反应发生和停止(节约药品也可。控制反应速率不得分)
55、(1)铁表面有红色物质析出,溶液由蓝色变为浅绿色(溶液颜色变化可不答,但只
答溶液颜色变化不得分) Fe + CuSO ==FeSO +Cu
4 4
(2) 丙 Mg>Fe>Cu
(3)①铜(或Cu) ②铜 铁(或Cu Fe)(漏选不得分) 镁(或Mg)
6十一、计算题
56、解:设:略
(1)样品中氧化铁的质量是20g — 4 g == 16 g ……………………………… 1分
样品中,氧化铁的质量分数为 ×100% == 80%…………………… 1分
(2)Fe O + 6HCl===2 FeCl + 3H O ……………………………………… 1分
2 3 3 2
160 325
16g X
16 0 325
16g X
X == 32.5g …………………………………………………… 1分
所得溶液的质量为:184 g + 20 g — 4 g == 200 g …………………………… 1分
所得溶液中溶质的质量分数为 ==16.25% …………………………1分
答:略。
(单位和百分号都不在扣分范围内)
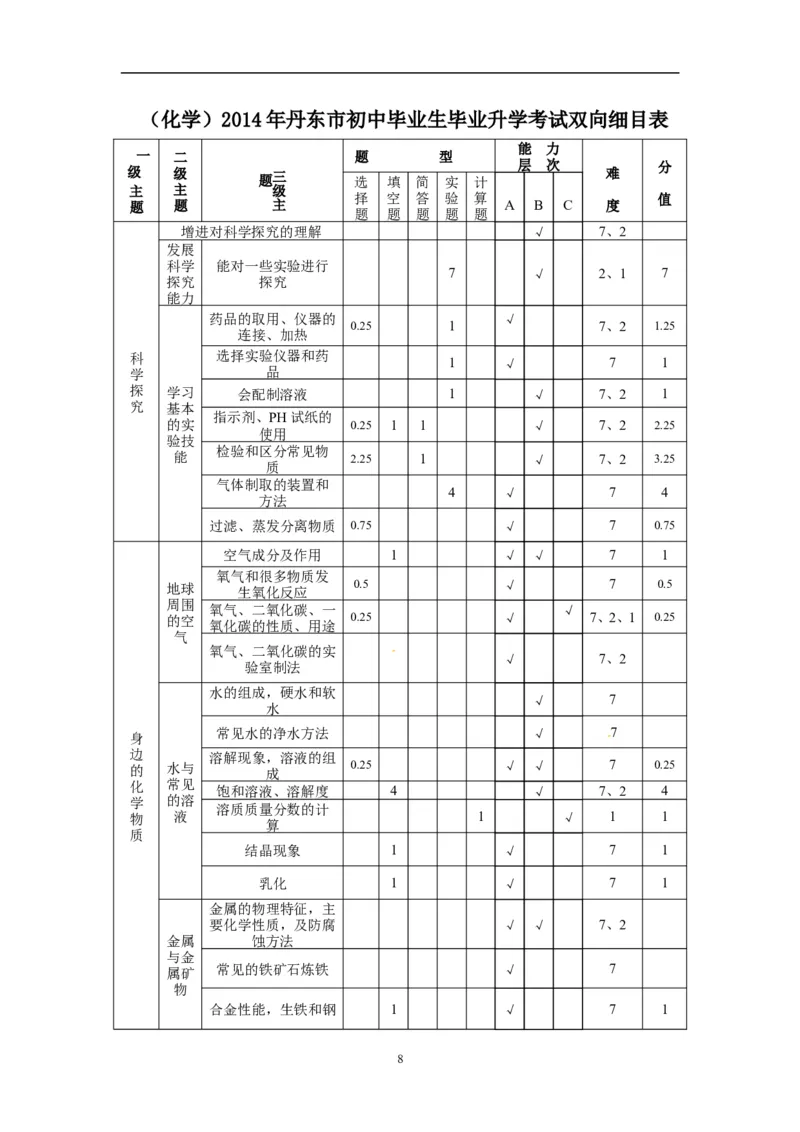
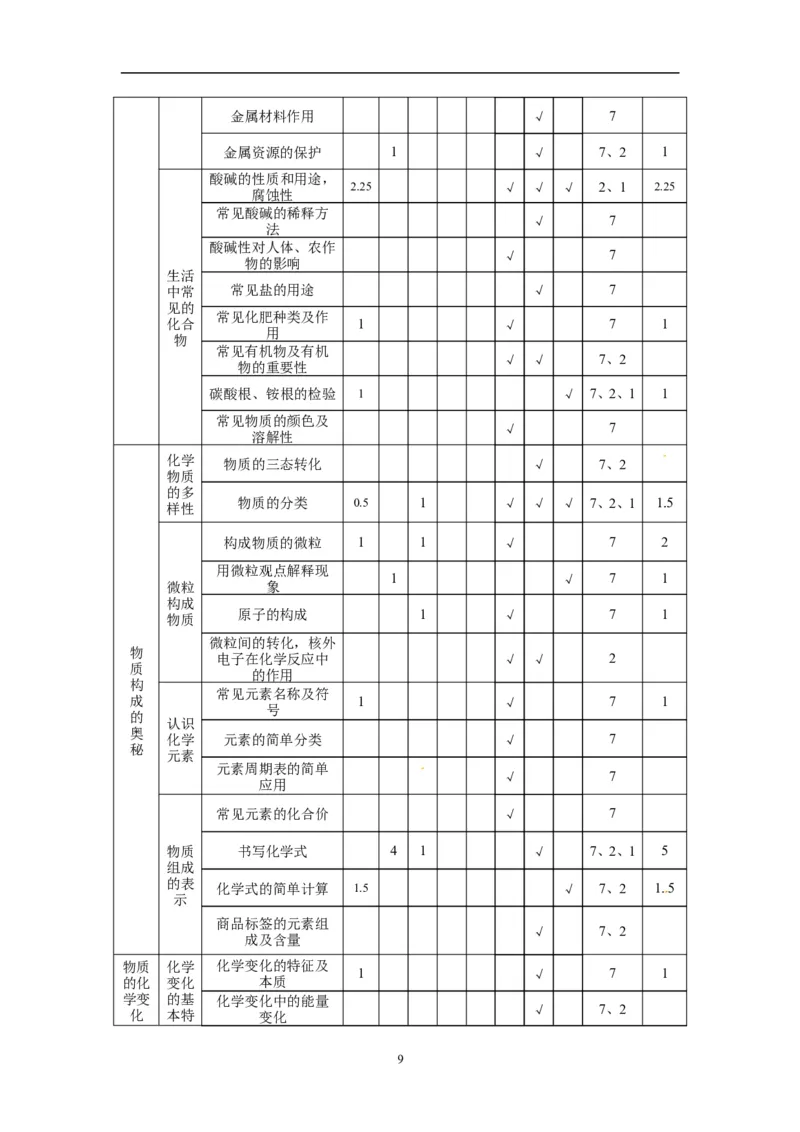
7(化学)2014年丹东市初中毕业生毕业升学考试双向细目表
一 二
级 级
[来
源 主 :Zxxk.Com] 主
题 题
8
[ 来源
:Zxxk.Com]
能 力
题 型
[来源:学*科*网Z*X*X*K] 层 次 [来 分 源:Zxxk.Com]
题三
选 填 简 实 计
难
级
择 空 答 验 算 值
主 A B C 度
题 题 题 题 题
增进对科学探究的理解 √ 7、2
发展
科学 能对一些实验进行
7 √ 2、1 7
探究 探究
能力
药品的取用、仪器的 √
0.25 1 7、2 1.25
连接、加热
科 选择实验仪器和药
1 √ 7 1
学 品
探 学习 会配制溶液 1 √ 7、2 1
究 基本
指示剂、PH试纸的
的实 0.25 1 1 √ 7、2 2.25
使用
验技
检验和区分常见物
能 2.25 1 √ 7、2 3.25
质
气体制取的装置和
4 √ 7 4
方法
过滤、蒸发分离物质 0.75 √ 7 0.75
空气成分及作用 1 √ √ 7 1
氧气和很多物质发
地球 生氧化反应 0.5 √ 7 0.5
周围
氧气、二氧化碳、一 √
的空 0.25 √ 7、2、1 0.25
氧化碳的性质、用途
气
氧气、二氧化碳的实
√ 7、2
验室制法
水的组成,硬水和软
√ 7
水
常见水的净水方法 √ 7
身
边 溶解现象,溶液的组
的 水与 成 0.25 √ √ 7 0.25
化 常见
饱和溶液、溶解度 4 √ 7、2 4
学 的溶
溶质质量分数的计
物 液 1 √ 1 1
算
质
结晶现象 1 √ 7 1
乳化 1 √ 7 1
金属的物理特征,主
要化学性质,及防腐 √ √ 7、2
金属 蚀方法
与金
属矿 常见的铁矿石炼铁 √ 7
物
合金性能,生铁和钢 1 √ 7 1金属材料作用 √ 7
金属资源的保护 1 √ 7、2 1
酸碱的性质和用途,
2.25 √ √ √ 2、1 2.25
腐蚀性
常见酸碱的稀释方
√ 7
法
酸碱性对人体、农作
√ 7
物的影响
生活
中常 常见盐的用途 √ 7
见的
常见化肥种类及作
化合 1 √ 7 1
用
物
常见有机物及有机
√ √ 7、2
物的重要性
碳酸根、铵根的检验 1 √ 7、2、1 1
常见物质的颜色及
√ 7
溶解性
化学 物质的三态转化 √ 7、2
物质
的多
物质的分类 0.5 1 √ √ √ 7、2、1 1.5
样性
构成物质的微粒 1 1 √ 7 2
用微粒观点解释现
1 √ 7 1
微粒 象
构成
原子的构成 1 √ 7 1
物质
微粒间的转化,核外
物
电子在化学反应中 √ √ 2
质
的作用
构
常见元素名称及符
成 1 √ 7 1
号
的
认识
奥
化学 元素的简单分类 √ 7
秘
元素
元素周期表的简单
√ 7
应用
常见元素的化合价 √ 7
物质 书写化学式 4 1 √ 7、2、1 5
组成
的表
化学式的简单计算 1.5 √ 7、2 1.5
示
商品标签的元素组
√ 7、2
成及含量
物质 化学 化学变化的特征及
1 √ 7 1
的化 变化 本质
学变 的基 化学变化中的能量
√ 7、2
化 本特 变化
9催化剂的作用 √ 7
征
化学反应基本类型,
认识 用化学反应解释现 0.5 1 √ √ 7、2 1.5
几种 象
化学
金属活动顺序表的
反应 √ 2、1
应用
质量守恒定律及应
1 1 √ 1 2
用
质量
守恒 书写化学方程式 8 6 √ 7、2 14
定律
根据化学方程式的
4 √ 7、2 4
简单计算
常见燃料的燃烧及
0.25 √ 7 0.25
对环境的影响
化学
与能 燃烧和灭火 0.25 1 √ 7 1.25
源、
资源 水资源的保护 3 √ 7 3
化
利用
学
与 常见的化石燃料 √ 7
社
会 常见的化学合成材料 0.25 √ 7 0.25
发 化学 元素与人体健康
1 √ 7、2 1
展
物质
与健
康 食品中的营养素 1 1 √ 7 2
保护 典型的大气、土壤、
好环 水污染源及危害。形 1 √ 7 1
境 成正确的环保意识
合
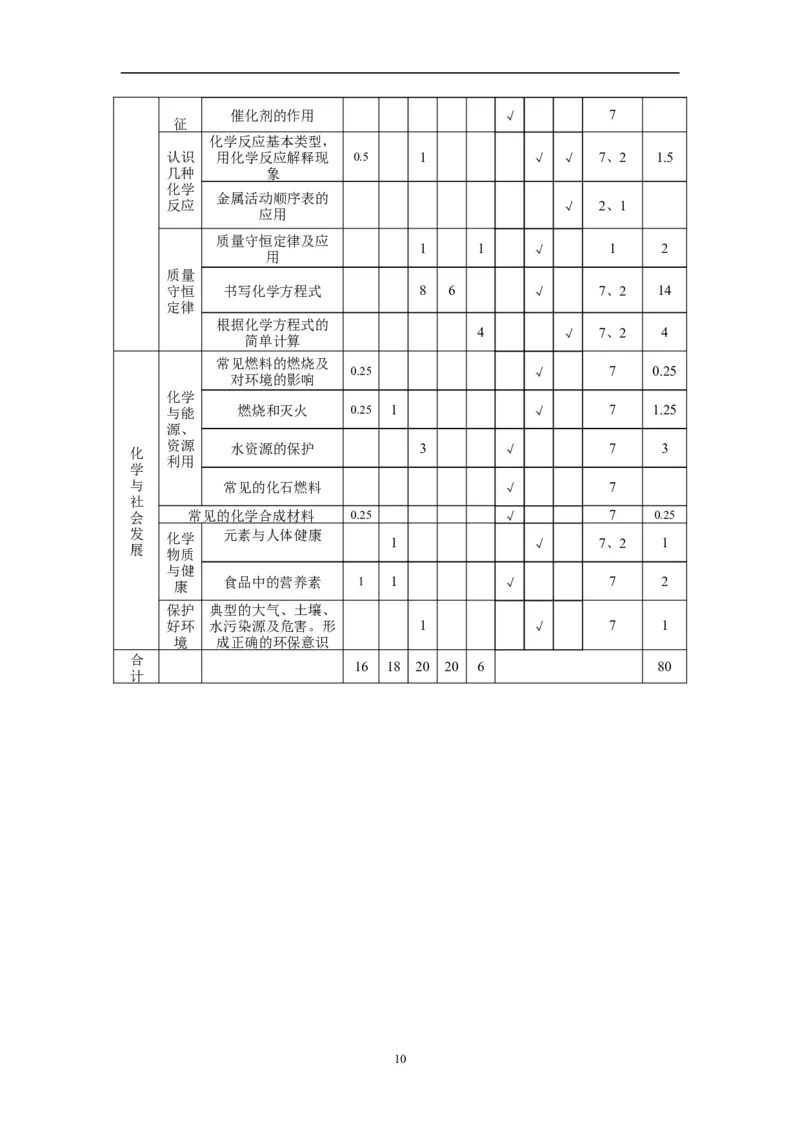
16 18 20 20 6 80
计
10