文档内容
答案与解析
★ ★
大教育山东联盟2025届高三质量检测第二次联考
化学参考答案与评分参考
1 【解析】 “强烧之,紫青烟起”,这是 元素的焰色 、、 的原子序数依次增大,且 原子的价电子数等于
.D K XYZ Y X
反应,故 错;丹砂为 ,加热变为 ,发生了分解反应, 原子的核外电子总数,说明 原子的核外电子数小于 ,所
A HgS Hg X 8
故 错;根据慈石的颜色和可吸连针铁,说明其主要成分为 以 为 , 为 或 ;短周期元素 原子的价电子所在能
B X CY O S Z
, 错误;“蒸令气上”,说明该方法为蒸馏, 正确。 层有 个轨道,则 的价电子位于第 能层,又根据 种元
Fe3O4 C D 9 Z 3 4
2 【解析】 酚醛树脂的单体为苯酚和甲醛,而不是甲 素形成的化合物的结构, 形成 价阳离子,因此 的价电
.D Z +1 Z
醇, 错误;聚氨酯( )材料,具有透气性、热塑性, 错误; 子排布为 1,即 为 ,则 为 ; 的原子序数最小且
A PU B 3s Z Na Y O W
聚酯是通过羟基和羧基缩聚反应形成的, 错误;聚乙烯醇 只能形成 个共价键,因此 为 。电负性: , 错
C 1 W H C>H A
中含有大量的羟基,能与水形成氢键, 正确。 误;基态 原子和基态 原子中,未成对电子数均为 ,故
D C O 2 B
3 【解析】 电器起火,先切断电源,再用二氧化碳灭 正确;基态 原子核外电子共占据 个轨道,即电子空间运
.B O 5
火器灭火,防止触电或电器发生爆炸伤人, 正确。过氧乙 动状态有 种, 错误;碳的氢化物有多种物质,例如辛烷的
A 5 C
酸的结构简式为 ,属于有机过氧化物;过碳酸 沸点高于水的, 错误。
CH3COOOH D
钠的化学式为 · ,属于无机过氧化物, 错 8 【解析】 由配离子的结构推断 为 价, 3+ 的
2Na2CO3 3H2O2 B .D Fe +3 Fe
误。高锰酸钾易分解,应保存在棕色瓶中,固体应保存在广
价电子轨道表示式为 , 正确;据题图
口瓶中, 正确。食盐和苯甲酸在不同温度下的溶解度差异 A
C
较大,可以利用重结晶法将低温下溶解度较小的苯甲酸提纯 所示,每个 3+ 连接 个原子,配位数为 , 正确; 与
Fe 6 6B H2O
出来, 正确。 相邻 之间存在氢键,中心 与 原子之间存在配位键,
D O O Fe C
4
.C
【解析】
NH3
的收集需用向下排空气法,
A
错误; 正确;乙酸根中有两个
C
原子,一个是
sp 2
杂化,另一个是
灼烧海带要在坩埚里进行,
B
错误;分液时,下层液体从下口
sp 3
杂化,
D
错误。
放出,上层液体从上口倒出, C 正确; Br2 易挥发,可随气体进 9 .B 【解析】 该材料具有良好的离子电导率, Li + 的定
入 溶液,同时, 易溶于水,吸收时需要防倒吸, 向移动完成电流的传导, 正确;放电时,负极由 ( )失电
AgNO3 HBr D A TiⅢ
错误。 子变为 ( ),正极由 ( )得电子变为 ( ),正极反应
TiⅣ TiⅢ TiⅡ
5 .B 【解析】 SiH4 中 Si 为 +4 价, H 为 -1 价, SiH4 为 为 Li3TiCl6+Li + +e - Li4TiCl6 , B 错误;充电时,阴极由
还原剂, 为氧化剂, 既是氧化产物又是还原产物,
NH3 H2 A ( )得电子变为 ( ),电极反应为 + -
TiⅣ TiⅢ Li2TiCl6+Li +e
错误; 中 周围有 个 原子, 周围有 个 ,还有
Si3N4 Si 4 N N 3 Si , 正确;电池工作时,负极脱嵌 +,质
Li3TiCl6 C 1molLi
1
个孤电子对,杂化方式均为
sp
3,
B
正确;氮化硅的熔点为
量减小 ,正极嵌入 +,质量增加 ,两极质量变
7g 1molLi 7g
,是共价晶体,不是分子晶体, 错误;第一电离能
1900℃ C 化总和为 , 正确。
14gD
, ,所以 ,故 错误。
N>CC>Si N>Si D 10 【解析】 由图可知,醋酸的超临界水氧化过程分
.D
6 【解析】 中含有饱和碳原子,不可能所有原子共
.B Z 为两步: ,
CH3COOH+O2 2CO+2H2O2CO+O2
平面, 错误;、 均含碳碳双键,均能使酸性高锰酸钾溶液
A YZ ,其中一氧化碳是中间产物,二氧化碳是最终产物。
2CO2
褪色, 正确; 中的官能团有酰胺基、氨基、醚键、酯基、碳
B M x( )曲线中,最高点前v(醋酸氧化) v( 氧化),最高
CO > CO
碳双键,共 种官能团, 错误; 不能发生水解反应,
5 C X D 点后v(醋酸氧化)v( 氧化), 点时x( )已经从最
< CO M CO
错误。
高点降低, 错误;由 点的坐标可知,前 内v(醋酸氧
A M 3s
7 【解析】 短周期元素 原子的最外层 轨道与
.B X s p
轨道上的电子数相同, 可能为 或 ,但短周期元素 、
化)
=
0.38×0.2
mol
·
L
-1·
s
-1,
B
错误;该氧化反应分两
X C Si W 3
1
— —步进行,不同时间段内两个反应进行的速率不同,所以无法
判断, 错误;由第 个图可知,温度升高,x( )峰值出现
C 2 CO
的时间提前且峰值更高,意味着在更短时间内一氧化碳的物
质的量分数达到更高值,说明醋酸快速氧化生成一氧化碳,
即醋酸的氧化速率增长幅度比一氧化碳的氧化速率的增长
幅度更大, 正确。
D
11 【解析】 由相对分子质量可知分子中 、 的相
.BD C H
对质量为 , 除以 的相对原子质量 得 余 ,则
107107 C 12 8 11
分子式为 ,若减 个 则分子式为 ,
C8H11O2N 1 C C7H23O2N H
原子数太多,不符合要求,该有机物的分子式为 ,
C8H11O2N
正确;根据
A
可知,分子中有 种片段,结合题干中物质名称 氰基丙烯
4 α-
酸酯可知,分子中含氰基、碳碳双键、酯基三种官能团, 错 B
误;样品中加入强碱溶液,有能使湿润的红色石蕊试纸变蓝
的气体生成,证明分子中有氰基, 正确;核磁共振氢谱实
C
验,显示 组峰,且峰面积之比为 ,说明分子
5 1∶2∶2∶3∶3
中有 个化学环境不同的甲基, 错误。
2 D
12 【解析】 由图甲知,化合物 、、、 中 均为 .CD 1234 Fe
价,化合价未变, 错误;由图乙可知,化合物 和
+2 A 2 H2O
生成化合物 与 - 的反应是放热反应,反应物的总能
3 HCOO
量大于生成物的总能量,但不能判断化合物 的能量和化合
2
物 的能量的大小关系,所以不能比较二者稳定性的相对大
3
小, 错误;由图甲可知 为 -,物质 与
-
反应生成
B M OH 3 OH
与 , 正确;由图甲知 氢化的总反应为
4 H2O C CO2 CO2+
- - , 正确。 H2+OH HCOO +H2OD
13 【解析】 反应中有极性键的断裂(如 — 键、
.C C N
— 键等),非极性键的生成(如 — 键的生成), 正确;
C H C C A
中 、1、2、3 均为烷基,
Y RR R R
*
成,故 H ,二者均为离子转变为沉淀的反应,故 S ,
Δ <0 Δ <0
所以反应 低温下均可自发进行, 错误;由题目中的
①② A
K 数据可知, 的溶解度远小于 ( )的,所以反应
sp CuS CuOH 2
不能发生,不会出现蓝色沉淀, 错误;由实验 和 可知,
③ B 1 2
反应 的速率大于反应 的, 正确;由实验 可知,增大
① ② C 2
2+
和
2-
浓度可使反应 发生,所以
2+
的氧化性和
2-
Cu S ② Cu S
的还原性与浓度有关, 正确。
D
15 【解析】 由图可知曲线M代表 c( +),曲线N
.A lg H
代表 c( -),曲线X的K -20,曲线Y的K
lg OH sp=1×10 sp=
-15,因为K [ ( )] K [ ( )],所以X代
1×10 sp CoOH 2 > sp PbOH 2
表 c( 2+)与 的关系, 错误。 的电离常数K
lg Pb pH A HR a=
c( H c + ( )c( R ) -) ,当 lgc c ( ( R -) )=-3 时,c( H +) =10 -2 mol · L -1,
HR HR
则K -5;当c(-) c( )时,c( +) -6
a=1×10 R =5 HR H =2×10
· -1,c( -) -9 · -1,K [ ( )]
mol L OH =5×10 mol L sp PbOH 2 =
-20,所以c( 2+) -4 · -1, 正确。 点
1×10 Pb =4×10 mol L B a
时,由K [ ( )] -15 可知,此时c( -)
sp Co OH 2 =1×10 OH =
-4.5 · -1,c( +) -9.5 · -1,代入K
10 mol L H =10 mol L a=
c( H
c
+
(
)c( R
)
-)
=1×10
-5、c(
R
-)
+
c(
HR
)
=0.1 mol
·
L
-1,
HR
可得c( -) · -1 c( 2+),由图像知 点 R ≈0.1mol L > Co a
c( 2+)c( +) c( 2+),所以c( -) c( 2+)
Co > H > Pb R > Co >
c( +)c( 2+), 正确; ( ) 2+
H > Pb C Co OH 2+2HRCo +
- 的 平 衡 常 数 K
c(
Co
2+)c2(
R
-)
2R +2H2O = c2( ) =
HR
c(
Co
2+)c2(
OH
-)c2(
R
-)c2(
H
+) K
sp
[
Co
(
OH
)
2
]K2
a,由 c2( )c2( +)c2( -) = K2
HR H OH w
图像可知K [ ( )] -15,K -5,K -14,代
sp CoOH 2 =10 a=10 w=10
入可得K 3, 正确。
=10 D
16 共 分 .( 12 )
【答案】 分 分 分 离子晶
(1)①5(1 ) ⅡB(1 ) 1(1 ) ②
体 分 分 3 分 (1 ) [(CH3)3S]2[CdBr4](2 ) sp(2 )
分 异硫氰酸
(2)H—NCS(1 ) (H—NCS)
分子间能形成氢键 分子间作用力大 沸点高 分
, , (1 )
硫氰酸 异硫氰酸 氰酸 分
(3) > > (2 )
价层电子对数为 【解析】 () 在元素周期表中与 紧邻的只有左、右、
C 1① Zn
下三个位置,左为 元素,右为 元素,故 只能为同族
Cu Ga Cd
, + 为 原子失去 个电子形成的,价层电子对数为 ,
的下一周期。
②
由图可知,晶胞中[
CdBr4
]m
-
位于顶角和面
4N N 1 4B
正确; 中 原子上无孤电子对,不显碱性,不能与盐酸反应 心,根据均摊法知,[ ]m - 有 1 1 个;
X N CdBr4 8× +6× =4
8 2
生成盐酸盐, 中 原子上有孤电子对,显碱性,能与盐酸
M N [( ) ]n + 有 个在顶角上, 个在面上, 个在晶胞内
反应生成盐酸盐, 错误;由机理可知,上述反应可发生,
CH3 3S 8 4 5
C D
正确。 部,所以根据均摊法[( CH3 ) 3S ]n + 有 8× 1 +4× 1 +5=8
8 2
14 【解析】 反应 均无旧键断裂,只有新键生 个,阴、阳离子的个数比为 ,化学式为
.CD ①② 1∶2
2
— —[(
CH3
)
3S
]
2
[
CdBr4
]。[(
CH3
)
3S
]+ 与(
CH3
)
3N
为等电子
10
n(
AgNO3
)
=10×0.1×10
-3V
1 mol
,
Cl
的质量分数
=
体,所以
S
原子的杂化方式为
sp 3
杂化。
( -3V 35.5) 3.55 V 1 。
()因为异硫氰酸与硫氰酸互为同分异构体,但沸点远高 10×0.1×10 1× a ×100%= a %
2
于硫氰酸,所以存在分子间氢键,结构式为 — 。 铬酸钾指示剂浓度过高时,一是由于颜色太深,会影响
H NCS
()三种酸根中,中心原子 、 、 的半径逐渐减小,负 终点的观察,二是会提前生成 砖红色沉淀,导致终
3 SN O Ag2CrO4
电荷的分散度逐渐减弱,所以酸性逐渐减弱。 点提前到达,使V 变小。
1
17 共 分 V
.( 12 ) 根据表达式3.55 1 ,V 变小,表达式的值变小。
【答案】 恒压滴液漏斗 分 打开 关闭 向 a % 1
(1) (1 ) K1、 K2,
装置中通入氩气 , 排尽装置中的空气 (2 分 ) 18 .( 共 12 分 )
【答案】 分
(2)NO2
-
+Fe
2+
+2H
+
Fe
3+
+NO↑+H2O(2
分
)
(1)SO2(1 )
分 3+ 2+ 分 避免在除去 3+
(3)NO2Cl(2 ) (2)FeS+2Fe 3Fe +S(2 ) Al
中和 水解产生的酸 以免影响滴定 时 3+一并沉淀 分
(4)① NOCl、NO2Cl , Fe (1 )
终点的判断 分 分 分
(2 ) (3)5.2≤pH<7.5(1 ) S、Al(OH)3(2 )
② 3.5 a 5 V 1 %(2 分 ) 偏小 (1 分 ) (4)① 负 (1 分 ) 3Fe2O3+2e - 2Fe3O4+O 2- (2 分 )
分
催化剂 ②11.2L(2 )
【解析】 该实验的原理是 ,实
【解析】 ()硫铁矿煅烧时, 元素被氧化为 ,故气体
Cl2+2NO2NOCl
△ 1 S SO2
验过程中可能存在少量 被氧化为 ,可能存在反应 为 。()“还原”的目的是使
3+
变为 2+,发生的反
NO NO2 X SO2 2 Fe Fe
催化剂
。沸点: 为 ,
应是
3+ 2+
;先“还原”,可使
3+
变为
Cl2+2NO22NO2Cl NOCl -6℃ NO2Cl
FeS+2Fe 3Fe +S Fe
△ 2+,“调 ”除去
3+
时铁元素不会造成损失。()根据
为 , 控制的温度约为 ,故产物 中可能含 Fe pH Al 3
5℃ F -15℃ NOCl
表中数据知,使
3+
沉淀完全且
2+
不能生成沉淀的
有的少量杂质 会冷凝为液体而被收集,未反应的 Al Fe pH
NO2Cl
范围为 ;因“还原”时生成 单质,“调 ”生
、 由于沸点低于 而不会冷凝,以气体形式逸出 5.2≤pH<7.5 S pH
Cl2 NO -15℃
成 ( )沉淀,故滤渣 的成分为 、 ( )。() 由
进行尾气处理。 AlOH 3 2 SAlOH 3 4①
图像知, 在阴极被还原为 ,则 为电源负极,发
()为防止 被氧化,通入 和 前,应排尽装置
Fe2O3 Fe3O4 a
1 NO NO Cl2
中的空气,具体操作:打开 、关闭 ,向装置中通入氩气。 生的电极反应为 - 2-,生成的
K1 K2 3Fe2O3+2e 2Fe3O4+O
()装置 中制取 ,根据装置中给出的反应物:
2 A NO
溶液、稀硫酸和 溶液,分析元素化合价知, O 2-
进入电解质,氯化胆碱( )的
Cl -
在阳极
FeSO4 NaNO2
为氧化剂, 为还原剂,故离子反应为
-
NaNO2 FeSO4 NO2 + 放电生成 , 的物质的量为 ,转移电子
2+ + 3+ 。
Cl2240gFe2O3 1.5mol
Fe +2H Fe +NO↑+H2O 的物质的量为 ,生成 ,标准状况下的体积
()实验过程中产生的少量 会发生反应 1mol 0.5molCl2
3 NO2 Cl2+ 为 。
催化剂 11.2L
。 沸点为 , 中控制的温
2NO2 △ 2NO2Cl NO2Cl 5℃ F 19 .( 共 12 分 )
度约为 ,故产物 中可能含有的少量杂质为
-15℃ NOCl
。 NO2Cl 【答案】
(1)
() 、 水解生成 、 和 ,溶
4①NOClNO2Cl HNO2 HNO3 HCl
液呈酸性,滴入 , + 与 2- 反应,使 2- 浓度 K2CrO4 H CrO4 CrO4
降低,从而无法形成 砖红色沉淀来指示滴定终点,
Ag2CrO4
加入 溶液,中和 、 水解生成的酸,以免影
NaOH NOClNO2Cl
响滴定终点的判断。
和 的水解反应分别为
②NOCl NO2Cl NOCl+H2O
, 。 -
HNO2+HClNO2Cl+H2OHNO3+HCl Cl +
+ 。故 和 的物质的量之和等于
Ag AgCl↓ NOCl NO2Cl
滴定 时 消 耗 标 准 液 的 物 质 的 量。n( )
AgNO3 Cl =
NO2
CH3
分 还原反应 分
(1 ) (1 )
CH2COCl
硝基 羧基 分
(2) 、 (2 )
(3)
NO2
CH3
+ + 2H2O + H →
CH2CN
NO2
CH3
+ 分
+NH4(2 )
CH2COOH
3
— —分
(4) (2 )
(5)
CHO
C COOH 分
(1 )
HO
NH2
金属钠 分
(6) (1 )
H3C 分
(2 )
SO3H
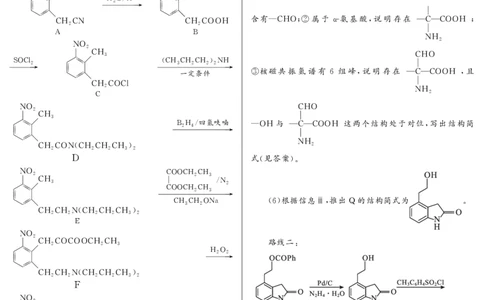
【解析】 根据题干信息和已知流程图综合分析,罗匹尼
罗的合成路线一如下:
NO2
CH3 H2O / H +
→
CH2CN
A
NO2
CH3
CH2COOH
B
SOCl2
→
NO2
CH3 ( )
CH3CH2CH22NH
一定条件 →
CH2COCl
C
NO2
CH3 /四氢呋喃 B2H6
→
( )
CH2CONCH2CH2CH3 2
D
NO2 COOCH2CH3/
CH3 N2
COOCH2CH3
→
( ) CH3CH2ONa
CH2CH2NCH2CH2CH3 2
E
NO2
CH2COCOOCH2CH3
H2O2
→
( )
CH2CH2NCH2CH2CH3 2
F
NO2
CH2COOH / ,
①PdCH2
一定条件→
②
( )
CH2CH2NCH2CH2CH3 2
G
() 发生的是羧基上的— 被— 取代的反应,
1B→C OH Cl
的结构简式为
C
( 分子中 原子数增加, 原子数减少)和已知信息 ,
E H O ⅱ D
为还原反应。
→E
()以 的结构简式为基础,结合反应条件和分子式可
2 A
推出 的结构简式(见上述流程图),则 中含氧官能团的名
B B
称为硝基、羧基。
() 是— 在酸性条件下水解生成— 的
3A→B CN COOH
反应,— 中的 生成 +,离子方程式(见答案)。
CN N NH4
()根据 的结构和信息“罗匹尼罗分子中除苯环外,还
4 G
存在一个五元环”,且罗匹尼罗分子中只有一个 原子,可推
O
知反应 是— 被还原为— ,— 和— 缩
① NO2 NH2 NH2 COOH
水成环,其结构简式(见答案)。
() 的分子式为 , 能与 溶液发生显
5B C9H9NO4 ① FeCl3
色反应,说明苯环与— 直接相连,能发生银镜反应,说明
OH
含有— ; 属于 氨基酸,说明存在 ;
CHO ② α- C COOH
NH2
CHO
核磁共振氢谱有 组峰,说明存在 ,且
③ 6 C COOH
NH2
CHO
— 与 这两个结构处于对位,写出结构简 OH C COOH
NH2
式(见答案)。
()根据信息 ,推出 的结构简式为 。
6 ⅲ Q
路线二:
根据 与 的结构差异, 中存在羟基,可选择金属钠
Q R Q
检验羟基的存在。 生成罗匹尼罗时,还生成对甲基苯磺酸
R
NO2
CH3
;根据 、 分子组成差异
DE
CH2COCl
H3C 。
SO3H
4
— —20 共 分 c() c()
.( 12 ) 内, 的平均反应速率为v( ) Δ X +Δ Y
30s M M = t =
【答案】 分 a b 分 Δ
(1)>(1 ) 10(3 -2)(2 )
(2)0.1(1
分
)
在反应时间较短时分离产物
Y(1
分
)
1.5 mol · L -1 + 1.5 mol · L -1
=0.1 mol
·
L
-1·
s
-1;根据
30s
催化剂 可加快反应 的速率 缩短到达平衡的时间 产物
m, Ⅱ , , 图像,产物 在反应较短时间内浓度达到最大,则为获得产
Y
的浓度峰值点提前 反应 消耗的 减少 体系中 浓度
Y , Ⅰ M , M 物 可采取的措施为在反应时间较短时分离产物 。改换
Y Y
增大 的浓度峰值点增大 分
,Y (2 ) 成催化剂 ,可加快反应 的速率,缩短到达平衡的时间,产
m Ⅱ
5
nα
分 5
α2
分 不变 分 物 的浓度峰值点提前,由于时间缩短,反应 消耗的 减
(3) (2 ) n α3 (2 ) (1 ) Y Ⅰ M
7 28 (1- ) 少,体系中 浓度增大,导致 浓度大于原峰值。()参考
【解析】 ()设反应 的反应热为 H( ),反应 的反 M Y 3
1 Ⅰ Δ Ⅰ Ⅱ ()中数据,达到平衡时,c( ) · -1,c( )
应热为 H( ),根据盖斯定律,则反应 的焓变 H( ) 2 X =2.5mol L Y =
Δ Ⅱ ③ Δ Ⅲ = · -1,向某反应容器中加入n 、n ,
H( ) H( ),根据题意,分别以 的 和 1.0mol L molM2 molH2
Δ Ⅱ -Δ Ⅰ 0.5mol M 控制温度为T ,测得 的平衡转化率为 ,则平衡时
的 为原料进行上述反应,当产物 和产物 的产 0 M α
1mol H2 X Y
n( )n( α) ,n( ) n( α) ,n( )
率均为 时,体系放热a ;当产物 产率为 和产物 M = 1- mol H2 =2 1- mol X +
10% kJ X 15% n()n( )αn ,由图中平衡 、 的浓度可求得反
的产率为 时,体系放热b ,则可列: Y = H2O = mol XY
Y 25% kJ 0.5× 应 的K ,将该式代入上式可以求出平衡体系中
H( ) H( ) a , Ⅲ =0.4
10%Δ Ⅰ +0.5×10%Δ Ⅱ = - kJ0.5×
nα nα
H( ) H( ) b ,根据题意,a n() 2 ,n() 5 ,容器容积为 ,反应 的
15%Δ Ⅰ +0.5×25%Δ Ⅱ =- kJ 2 > Y = mol X = mol 1L Ⅰ
7 7
b,则 a b ,根据上述两个式子可得 H( )
2 - >0 0.5×5%Δ Ⅰ -
5nα
H( ) ,即 H( ) H( ),则 H( ) nα
0.5×5%Δ Ⅱ <0 Δ Ⅰ <Δ Ⅱ Δ Ⅲ = 7
Δ
H(
Ⅱ
)
-Δ
H(
Ⅰ
)
>0
。 平衡常数K
=n( 1- α)
1
[2
×
n
1
( 1- α) ]2 = 28 n
5
( 1
α
-
2
α)3
。反应
根据 H( ) H( )
1
×
1
①0.5×10%Δ Ⅰ +0.5×10%Δ Ⅱ =
a , H( ) H( )
开始短时间内,反应
Ⅱ
得到的产物
Y
比反应
Ⅰ
得到的产物
X
- kJ②0.5×15%Δ Ⅰ +0.5×25%Δ Ⅱ =
b ,将 ,与 联立,消去 H( ),解得 H( )
多,说明反应
Ⅱ
的速率比反应
Ⅰ
的速率大,速率越大,其活化
- kJ ①×1.5 ② Δ Ⅰ Δ Ⅱ
= ( 3 a -2 b) ×10 kJ · mol -1。 能越小,则反应活化能:E a1> E a2 ;增加 H2 的量,K Ⅲ =
() 、 反应中 、 、 的化学计量数均为 ,则 c( Y ) ,温度不变,平衡常数不变,则 c( Y ) 的值不变。
2Ⅰ Ⅱ M X Y 1 0~ c() c()
X X
5
— —