文档内容
2025 届高三一模
化学
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息。
2.请将答案正确填写在答题卡上。
一、单选题(共42分)
1. 若配合物中心离子含有单电子,则配合物为顺磁性物质,将顺磁性物质置于外磁场中,会使磁场强度增
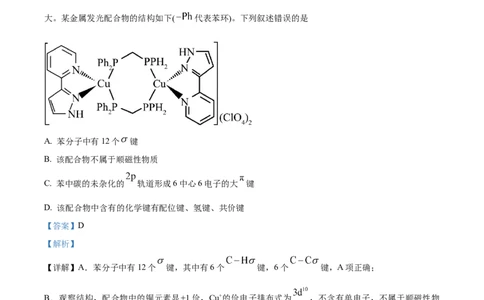
大。某金属发光配合物的结构如下( 代表苯环)。下列叙述错误的是
A. 苯分子中有12个 键
B. 该配合物不属于顺磁性物质
C. 苯中碳的未杂化的 轨道形成6中心6电子的大 键
D. 该配合物中含有的化学键有配位键、氢键、共价键
【答案】D
【解析】
【详解】A.苯分子中有12个 键,其中有6个 键,6个 键,A项正确;
B.观察结构,配合物中的铜元素显+1价,Cu+的价电子排布式为 ,不含有单电子,不属于顺磁性物
质,B项正确;
C.苯中环上的每个碳原子存在一个未杂化的 2p轨道,每个轨道中含1个电子,碳的未杂化的 轨道形
成6中心6电子的大 键,C项正确;
D.氢键不属于化学键,D项错误;
故选:D。2. 某学习研究小组为了测定一定质量的 和 混合物中 的质量百分含量,设计了如下实
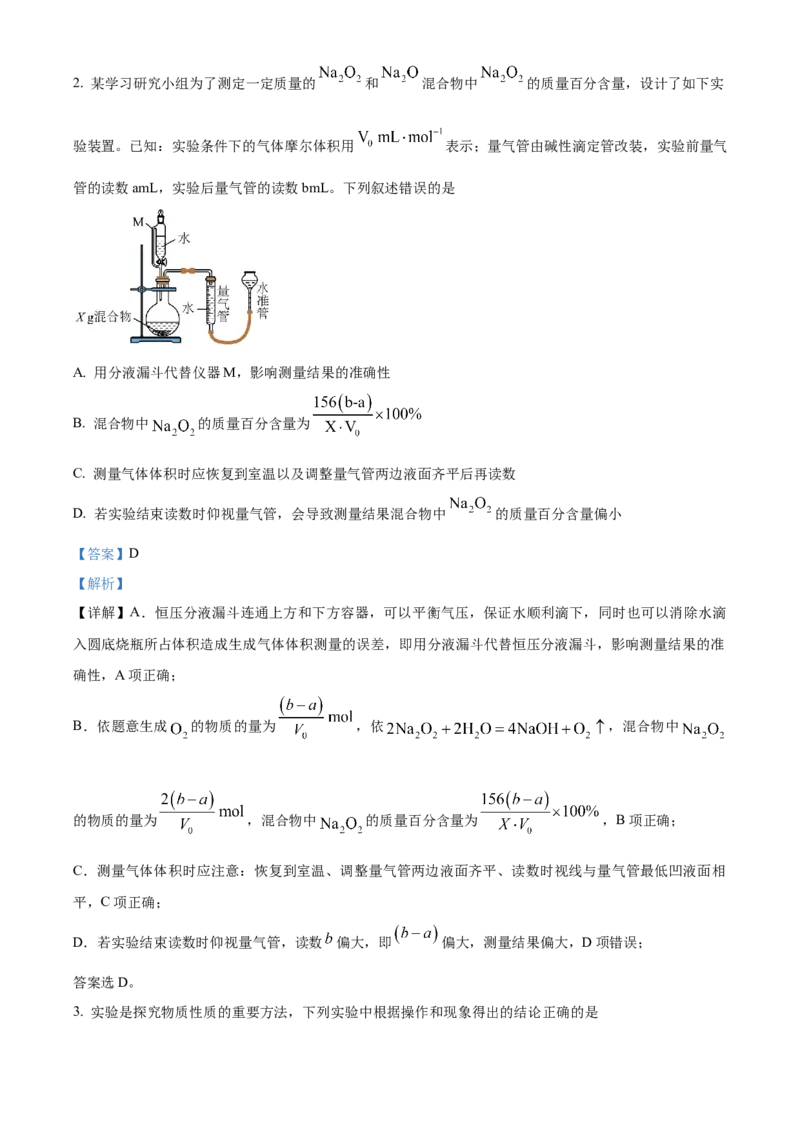
验装置。已知:实验条件下的气体摩尔体积用 表示;量气管由碱性滴定管改装,实验前量气
管的读数amL,实验后量气管的读数bmL。下列叙述错误的是
A. 用分液漏斗代替仪器M,影响测量结果的准确性
B. 混合物中 的质量百分含量为
C. 测量气体体积时应恢复到室温以及调整量气管两边液面齐平后再读数
D. 若实验结束读数时仰视量气管,会导致测量结果混合物中 的质量百分含量偏小
【答案】D
【解析】
【详解】A.恒压分液漏斗连通上方和下方容器,可以平衡气压,保证水顺利滴下,同时也可以消除水滴
入圆底烧瓶所占体积造成生成气体体积测量的误差,即用分液漏斗代替恒压分液漏斗,影响测量结果的准
确性,A项正确;
B.依题意生成 的物质的量为 ,依 ,混合物中
的物质的量为 ,混合物中 的质量百分含量为 ,B项正确;
C.测量气体体积时应注意:恢复到室温、调整量气管两边液面齐平、读数时视线与量气管最低凹液面相
平,C项正确;
D.若实验结束读数时仰视量气管,读数 偏大,即 偏大,测量结果偏大,D项错误;
答案选D。
3. 实验是探究物质性质的重要方法,下列实验中根据操作和现象得出的结论正确的是选
操作 现象 结论
项
向麦芽糖溶液中加少量稀硫酸,加热一段时间,冷却后加过量 出现银 麦芽糖的水解产物
A
NaOH溶液至碱性,再加银氨溶液,水浴加热 镜 具有还原性
出现红 木炭具有还原性,
B 在烧瓶中加入木炭颗粒与浓硝酸,然后加热 棕色气
能还原
体
有气泡 证明非金属性
C 向 溶液中加入过量盐酸振荡、静置
产生 Cl>C
将Zn与Fe用导线相连,插入稀硫酸酸化的3%NaCl溶液,一段时间
无明显 Zn可以保护Fe不
D
后,从Fe电极区取出少量溶液,滴入2滴 溶液 现象 被腐蚀
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.麦芽糖、葡萄糖都能和银氨溶液发生银镜反应,故实验现象不能说明麦芽糖的水解产物具有
还原性,故A错误;
B.在烧瓶中加入木炭颗粒与浓硝酸,然后加热,出现红棕色气体,可能是木条还原浓硝酸,生成了
NO ,也可能是浓硝酸受热分解,生成了NO ,故B错误;
2 2
C.盐酸为无氧酸,不能比较Cl、C的非金属性,故C错误;
D.将Zn与Fe用导线相连,插入稀硫酸酸化的3%NaCl溶液,一段时间后,从Fe电极区取出少量溶液,
滴入2滴K[Fe(CN) ]溶液,无明显现象,即Fe没有失去电子,生成Fe2+,故Zn可以保护Fe不被腐蚀,故
3 6
D正确;
答案选D。
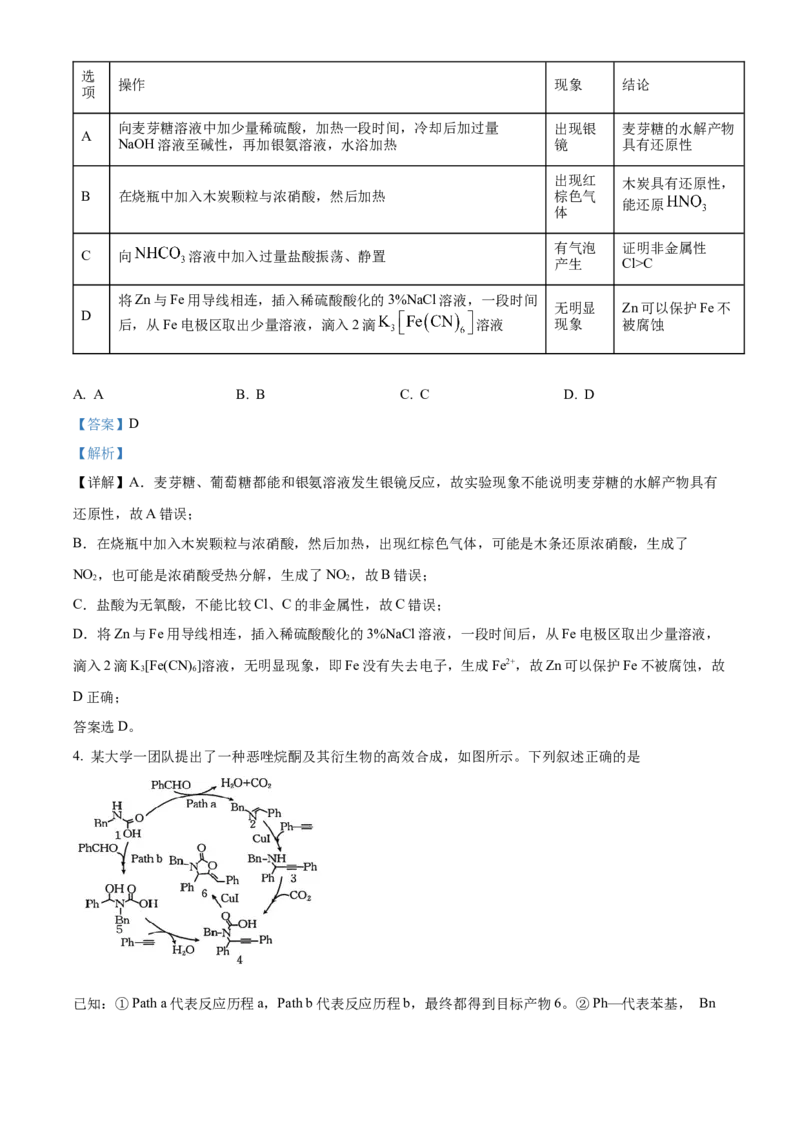
4. 某大学一团队提出了一种恶唑烷酮及其衍生物的高效合成,如图所示。下列叙述正确的是
已知:①Path a代表反应历程a,Path b代表反应历程b,最终都得到目标产物6。②Ph—代表苯基, Bn—代表苯甲基。
A. Path a和Path b的产物不完全相同
B. 4→6和5→4的反应类型相同
C. 上述循环中,只断裂了极性键
D. 1、4、5都具有亲水性
【答案】D
【解析】
【详解】A.Path a与Path b的产物均为化合物6和HO,A错误;
2
B.4→6是加成反应,5→4是取代反应,B错误;
C.4→6时断裂了碳碳三键中的1个非极性键,C错误;
D.有机物含氨基、羟基、羧基等与水形成氢键,有亲水性,D正确;
故选D。
5. 下列说法正确的是
A. 用电子式表示MgCl 的形成过程:
2
B. 四氯化碳分子的空间填充模型:
C. 的名称:乙二酸二乙酯
D. 质子数为58、中子数为80的Ce的核素符号:
【答案】C
【解析】
【详解】A.MgCl 是离子化合物,镁失电子,氯得电子,形成过程:
2
,A错误;
B.CCl 为正四面体结构,C原子位于四面体的中心,但C原子半径小于Cl,其空间填充模型不是
4
,B错误;C.酯的命名是某酸某酯,观察该物质可知名称为乙二酸二乙酯,C正确;
D.质子数为58、中子数为80的Ce质量数为58+80=138,表示为 ,D错误;
故答案选C。
6. 为阿伏加德罗常数的值。下列说法正确的是
A. 32g ( )中S原子形成共价键的数目为
B. 1mol 与足量的水充分反应转移的电子数为
C. 在1mol 中存在的配位键数目为
D. 铅酸蓄电池的正极质量增加3.2g时,电路中通过的电子数目为
【答案】A
【解析】
【详解】A.根据分子结构可知一个S 分子含有8个共价键,32g S 的物质的量为 ,共
8 8
价键数目为N ,故A正确;
A
B.氯气与水反应为可逆反应,不能进行到底,所以1molCl 与足量的水充分反应转移的电子数小于N ,
2 A
故B错误;
C.1个[Co(NH )Cl]Cl中,4个氨气、2个氯离子为配体子,则1mol[Co(NH)Cl]Cl中存在的配位键数目
3 4 2 3 4 2
为6N ,故C错误;
A
D.铅蓄电池中,正极电极反应为PbO +2e-+4H++ =PbSO+2H O,正极由PbO →PbSO ,每增重64g
2 4 2 2 4
转移2mol电子,当正极增加3.2g时,电路中通过的电子数目为0.1N ,故D错误;
A
故选A。
7. 青霉素是一种高效、低毒的抗生素,青霉素的使用增强了人类抵抗细菌性感染的能力。青霉素结构如图
所示,下列关于青霉素的说法中正确的是A. 1个青霉素分子中有4个手性C原子 B. 青霉素分子与水分子之间能形成氢键
C. 青霉素分子中的 原子的杂化类型是 D. 青霉素最多能与 反应
【答案】B
【解析】
【详解】A. ,1个青霉素分子中有3个手性C原子,A错误;
B.酰胺基和水之间可以形成氢键,青霉素分子与水分子之间能形成氢键,B正确;
C.青霉素分子中的 原子的杂化类型是 ,C错误;
D. 青霉素最多能与 反应,苯环与氢气发生加成反应消耗3mol,羧基与酰胺基不能与氢气反
应,D错误;
故选B。
8. 取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度相同),反应现象没有明显差别的
是
选项 试剂① 试剂②
A 溶液 HCl溶液
B 溶液 溶液
C 氨水 溶液
D 溶液 溶液
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.将 溶液加入HCl溶液中,先发生反应 ,
无明显现象,后发生反应 ,产生白色沉淀;将 HCl 溶液加入溶液中,先发生反应 ,产生白色沉淀,后发生
反应 ,白色沉淀溶解,现象不同,A项不选;
B.将 溶液加入 溶液中,发生反应 ,产生无色气体;将
溶液加入 溶液中,先发生反应 ,无明显现象,后发生反应
,产生无色气体,现象不同,B项不选;
C.将氨水加入 溶液中,先发生反应 ,生成蓝色沉淀,
后发生反应 ,蓝色沉淀溶解形成深蓝色溶液;
将 溶液加入氨水中,发生反应 ,溶液变为深蓝色,
现象不同,C项不选;
D.无论如何滴加,均产生白色沉淀,现象相同,D项选;
答案选D。
9. 可用作理离子电池的电解质。以LiF、HF和 为原料制备 的某工艺流程如图所示:
已知:HF的沸点为19.5℃, 极易水解。下列说法错误的是
A. “反应I”中HF既作反应物又作溶剂 B. “反应Ⅱ”结束后,可使用玻璃漏斗过滤得到
C. 物质a可在该流程中循环使用 D. 整个制备过程需要在低温、干燥条件下进行
【答案】B
【解析】【详解】A.“反应I”为LiF和HF反应生成 ,HF既作反应物又作溶剂,A项正确;
B.根据原子守恒可知a为HF,故“反应Ⅱ”结束后,不能使用玻璃漏斗过滤,因为玻璃中的二氧化硅可
以和HF发生反应,B项错误;
C.物质a为HF,可返回“反应I”中循环使用,C项正确;
D.整个制备过程需要在低温、干燥条件下进行,一方面防止 HF挥发,另一方面防止 水解,从而提高
原料利用率,D项正确;
答案选B。
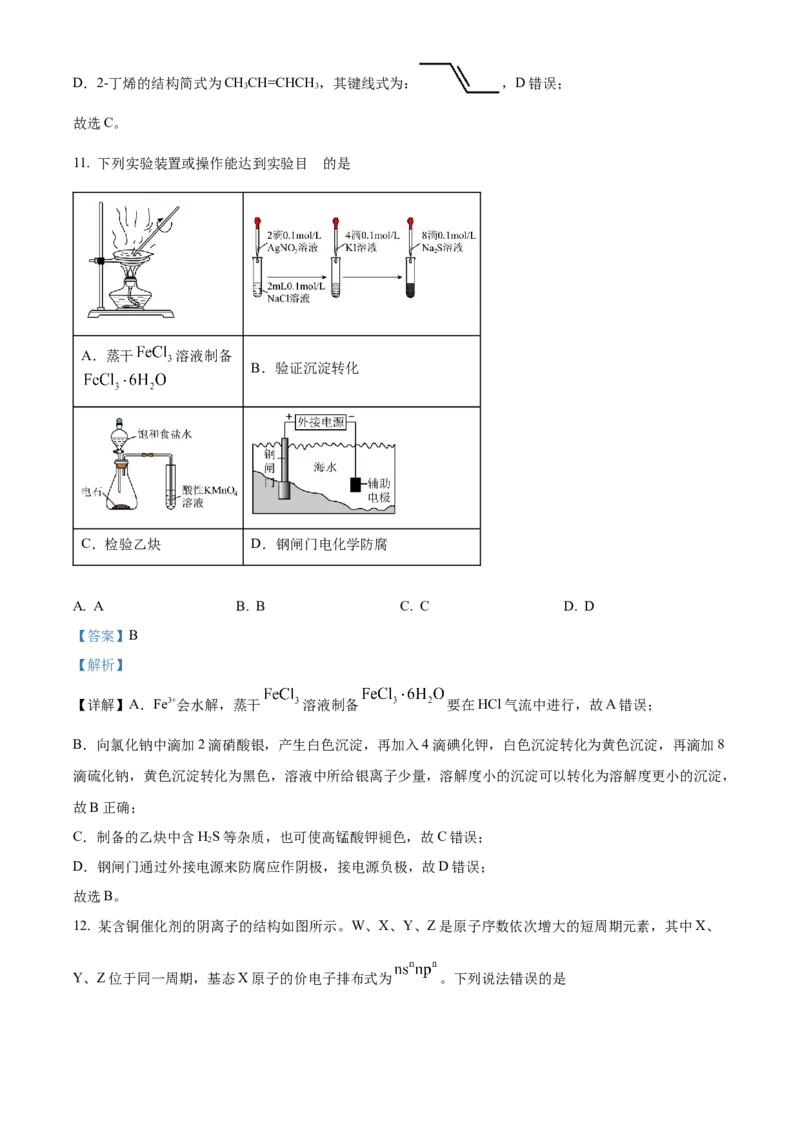
10. 下列化学用语使用正确的是
A. NaCl晶体 晶胞: B. 的化学名称:N-二甲基甲酰胺
的
C. 的电子云图: D. 丁二烯的键线式:
【答案】C
【解析】
【详解】A.NaCl晶体的晶胞为: ,A错误;
B. 的化学名称为:N,N—二甲基甲酰胺,B错误;
C.2p 的电子云图: ,C正确;
zD.2-丁烯的结构简式为CHCH=CHCH ,其键线式为: ,D错误;
3 3
故选C。
的
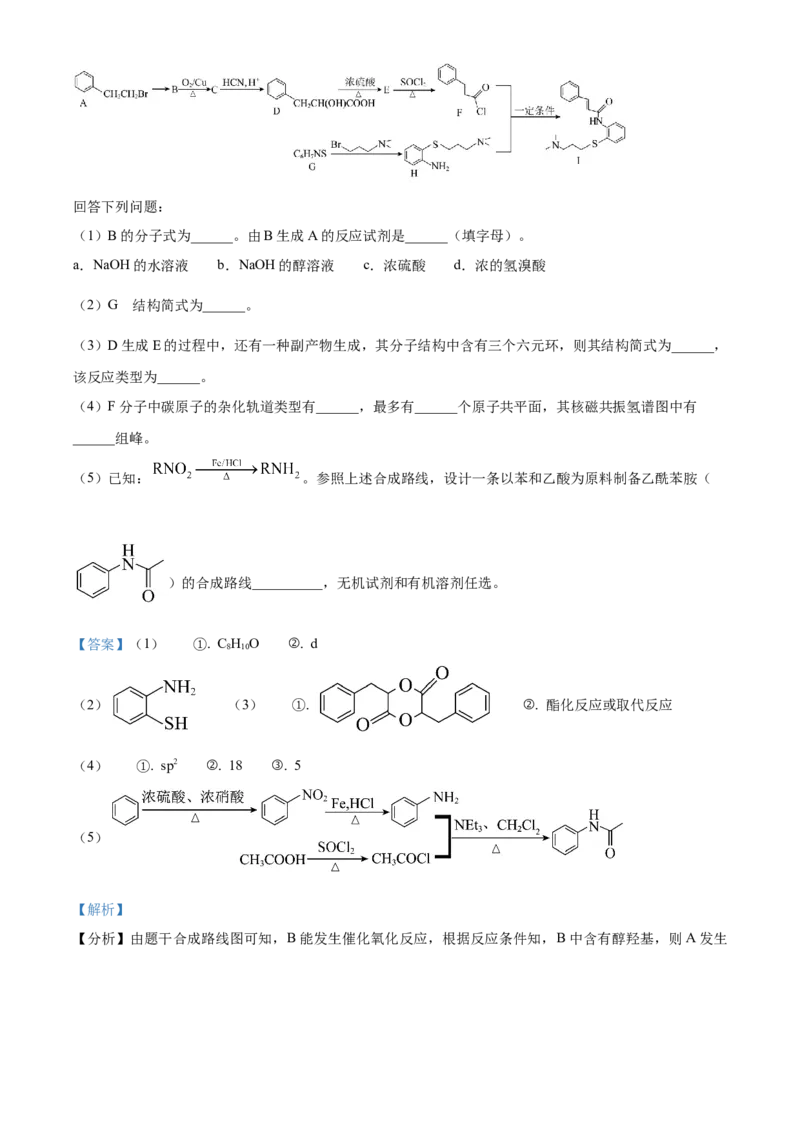
11. 下列实验装置或操作能达到实验目 的是
A.蒸干 溶液制备
B.验证沉淀转化
C.检验乙炔 D.钢闸门电化学防腐
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.Fe3+会水解,蒸干 溶液制备 要在HCl气流中进行,故A错误;
B.向氯化钠中滴加2滴硝酸银,产生白色沉淀,再加入4滴碘化钾,白色沉淀转化为黄色沉淀,再滴加8
滴硫化钠,黄色沉淀转化为黑色,溶液中所给银离子少量,溶解度小的沉淀可以转化为溶解度更小的沉淀,
故B正确;
C.制备的乙炔中含HS等杂质,也可使高锰酸钾褪色,故C错误;
2
D.钢闸门通过外接电源来防腐应作阴极,接电源负极,故D错误;
故选B。
12. 某含铜催化剂的阴离子的结构如图所示。W、X、Y、Z是原子序数依次增大的短周期元素,其中X、
Y、Z位于同一周期,基态X原子的价电子排布式为 。下列说法错误的是A. 该阴离子中铜元素的化合价为+3 B. 由W和Y构成的化合物不可能为离子化合物
C. 电负性:Z>Y>X>W D. X、Y、Z均位于元素周期表的p区
【答案】B
【解析】
【分析】基态X原子的价电子排布式为nsnnpn,基态X原子的价电子排布式为2s22p2,X为C元素,W、
X、Y、Z是原子序数依次增大的短周期元素,结合含铜催化剂阴离子的结构知,W为H,Y为N,Z为
F。
【详解】A.该阴离子为[Cu(CF)(CHCN)]-,其中铜元素的化合价为+3价,A项正确;
3 3 2
B.H和N构成的化合物NH H为离子化合物,B项错误;
4
C.同周期从左到右主族元素的电负性逐渐增大,元素的非金属性越强、电负性越大,则电负性:Z>Y>
X>W,C项正确;
D.C、N、F均位于元素周期表的p区,D项正确;
答案选B。
13. 为阿伏加德罗常数的值。下列叙述正确的是
A. 标准状况下, 溶于水,溶液中 、 和 的微粒数之和小于
B. 溶液中含有 数目小于
C. 与 完全反应,反应中转移的电子数介于 和 之间
D. 苯乙烯中含有碳碳双键数为
【答案】A
【解析】
【详解】A.氯气与水反应为可逆反应,不能进行到底,依据氯原子个数守恒可知,标准状况下11.2LCl
2
溶于水,氯气物质的量n= =0.5mol,溶液中Cl-、ClO-、HClO的微粒数之和小于N ,故A正确;
AB.0.1mol/LNH NO 溶液体积不知,不能计算溶液中含有 数目,故B错误;
4 3
C.2.3gNa物质的量n= =0.1mol,与O 完全反应,反应中转移的电子数为0.1N ,故C错误;
2 A
D.苯环中不存在碳碳双键,1mol苯乙烯中含有碳碳双键数为N ,故D错误;
A
故选:A。
14. 设 为阿伏加德罗常数的值。工业上制备硫酸涉及 、 、 、 等物质。下列说法正确
的是
A. 分子中含有的质子数为
B. 和 充分反应后分子总数为
C. 标准状况下, 中分子的数目为
D. 的 溶液中 数目为
【答案】D
【解析】
【详解】A.一个S原子有16个质子, 的物质的量为 ,则 所含质子数
的数目为0.125×8×16N =16N ,故A错误;
A A
B.SO 和氧气的反应为可逆反应,则 和 充分反应后分子总数大于 ,故B错误;
2
C.标准状况下, 为固体,不能用气体摩尔体积公式进行计算,故C错误;
D.pH=2的硫酸溶液中c(H+)=0.01mol/L,则1LpH=2的硫酸溶液中 数目为 ,故D正确;
故选D。
二、解答题(共58分)
15. 由我国两位院士领衔的联合课题组,综合利用虚拟筛选和酶学测试相结合的策略进行药物筛选,发现
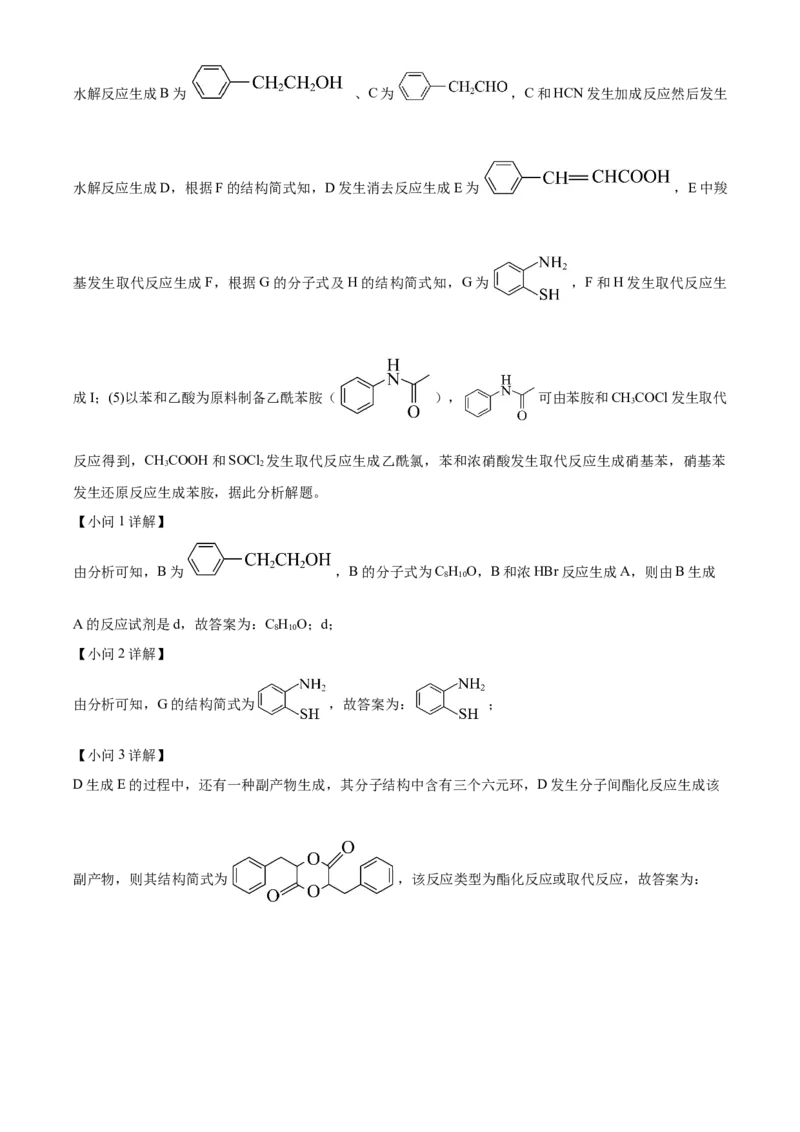
肉桂硫胺是抗击病毒的潜在用药。肉桂硫胺(I)的一种合成路线如下:回答下列问题:
(1)B的分子式为______。由B生成A的反应试剂是______(填字母)。
a.NaOH的水溶液 b.NaOH的醇溶液 c.浓硫酸 d.浓的氢溴酸
的
(2)G 结构简式为______。
(3)D生成E的过程中,还有一种副产物生成,其分子结构中含有三个六元环,则其结构简式为______,
该反应类型为______。
(4)F分子中碳原子的杂化轨道类型有______,最多有______个原子共平面,其核磁共振氢谱图中有
______组峰。
(5)已知: 。参照上述合成路线,设计一条以苯和乙酸为原料制备乙酰苯胺(
)的合成路线__________,无机试剂和有机溶剂任选。
【答案】(1) ①. C H O ②. d
8 10
(2) (3) ①. ②. 酯化反应或取代反应
(4) ①. sp2 ②. 18 ③. 5
(5)
【解析】
【分析】由题干合成路线图可知,B能发生催化氧化反应,根据反应条件知,B中含有醇羟基,则A发生水解反应生成B为 、C为 ,C和HCN发生加成反应然后发生
水解反应生成D,根据F的结构简式知,D发生消去反应生成E为 ,E中羧
基发生取代反应生成F,根据G的分子式及H的结构简式知,G为 ,F和H发生取代反应生
成I;(5)以苯和乙酸为原料制备乙酰苯胺( ), 可由苯胺和CHCOCl发生取代
3
反应得到,CHCOOH和SOCl 发生取代反应生成乙酰氯,苯和浓硝酸发生取代反应生成硝基苯,硝基苯
3 2
发生还原反应生成苯胺,据此分析解题。
【小问1详解】
由分析可知,B为 ,B的分子式为C H O,B和浓HBr反应生成A,则由B生成
8 10
A的反应试剂是d,故答案为:C H O;d;
8 10
【小问2详解】
由分析可知,G的结构简式为 ,故答案为: ;
【小问3详解】
D生成E的过程中,还有一种副产物生成,其分子结构中含有三个六元环,D发生分子间酯化反应生成该
副产物,则其结构简式为 ,该反应类型为酯化反应或取代反应,故答案为:;酯化反应或取代反应;
【小问4详解】
由题干流程图中F的结构简式可知,F分子中碳原子的杂化轨道类型有sp2,F分子中所有原子都可以共平
面,最多有18个原子共平面,分子中存在一根对称轴,根据等效氢原理可知,分子含有5种不同环境的H
原子,其核磁共振氢谱图中有5组峰,故答案为:sp2;18;5;
【小问5详解】
以苯和乙酸为原料制备乙酰苯胺( ), 可由苯胺和CHCOCl发生取代反应得到,
3
CHCOOH和SOCl 发生取代反应生成乙酰氯,苯和浓硝酸发生取代反应生成硝基苯,硝基苯发生还原反
3 2
应生成苯胺,合成路线为:
故答案为:
。
16. 扁桃酸衍生物是重要的医药中间体,以 和 为原料合成扁桃酸衍生物 的路线如下:
(1) 的分子式为 ,可发生银镜反应,且具有酸性, 所含官能团的名称为_______。
已知: 为加成反应,则 的结构简式为_______。(2)C( )中①、②、③三个 电离出 的能力由强到弱的顺序是_______。
(3)E是由2分子 生成的含有3个六元环的化合物, 分子中不同化学环境的氢原子有_______种。
(4) 的反应类型是_______反应(填“取代”或“加成”)。
(5)写出符合下列条件的 的所有同分异构体(不考虑立体异构)的结构简式:_______。
①属于一元酸类化合物
②苯环上只有2个取代基且处于对位,其中一个是羟基
(6)已知:
试写出由乙酸为原料制备 的合成路线_______(无机试剂任选)。(合成路线常用的表示
)
【答案】(1) ①. 醛基、羧基 ②.
(2)③>①>② (3)4
( 4 ) 取 代 ( 5 ) 、 、 、
( 6 )
【解析】
【分析】A的分子式为C HO ,A可发生银镜反应,且具有酸性,则A中含有醛基和羧基,其结构简式为
2 2 3
HOOCCHO,对比A、C的结构且A+B→C为加成反应可知B为苯酚,由C→D的反应条件可看出该反应
为酯化反应,C中有羧基和醇羟基,两个C分子可以发生酯化反应生成含有3个六元环的化合物E,D→F的反应为醇羟基与HBr发生的取代反应,据此分析回答问题。
【小问1详解】
A的结构简式为HOOCCHO,则A中含有醛基和羧基;对比A、C的结构且A+B→C为加成反应可知B
为苯酚,其结构简式为: ;
【小问2详解】
①②③分别对应的是酚羟基、醇羟基、羧基,其-OH上氢原子的活泼性顺序为羧基>酚羟基>醇羟基,则3
个-OH的酸性由强到弱的顺序是③>①>②;
【小问3详解】
C中有羧基和醇羟基,两个C分子可以发生酯化反应生成含有3个六元环的化合物,其结构为:
,左右对称,分子中不同化学环境的氢原子有4种;
【小问4详解】
对比D、F的结构简式可知,D→F为溴原子取代了羟基,所以D→F的反应类型是取代反应;
【小问5详解】
F中含有酯基、溴原子和酚羟基,三种基团均能与NaOH溶液反应,故1molF在一定条件下最多消耗
3molNaOH。由条件①可知F的同分异构体中含有-COOH,由条件②可知结构中含有,则剩余的只有两个
碳原子、一个溴原子和三个氢原子,可通过移动-COOH与-Br书写出符合要求的F的同分异构体为:
、 、 、 ;
【小问6详解】
根据信息可知,羧酸在PCl 和加热的条件下可在与羧基相连的碳原子上引入一个氯原子,而氯原子水解即
3
可生成羟基,醇羟基发生催化氧化转化成—CHO,据此即可写出由乙酸合成A的路线流程图:
。
17. 我国力争于2030年前做到碳达峰,2060年前实现碳中和。以生物材质(以C计)与水蒸气反应制取H 是
2
一种低耗能,高效率的制H 方法。该方法由气化炉制造H 和燃烧炉再生CaO两步构成。气化炉中涉及到
2 2的反应如下:
Ⅰ.
Ⅱ.
Ⅲ.
Ⅳ.
(1)已知反应Ⅱ的 , 、 、 的键能分别为803kJ/mol、464kJ/mol、
436kJ/mol,则 中碳氧键的键能为_____kJ/mol
(2)绝热条件下,将 、 以体积比2:1充入恒容密闭容器中,若只发生反应Ⅱ,下列可作为反应Ⅱ
达到平衡的判据是_____。
.
A 与 比值不变 B. 容器内气体密度不变
C. 容器内气体压强不变 D. 不变
(3)反应Ⅱ: 的速率方程为 ,
。( 、 为速率常数,与温度、催化剂、接触面积有关,与浓度无关)。净反
应速率( )等于正、逆反应速率之差。平衡时, _____ (填“>”“<”或“=”)。
(4)对于反应Ⅲ,若平衡时保持温度不变,再充入 ,使其浓度增大到原来的2倍,则平衡移动方向
为_____(填“向左移动”“向右移动”或“不移动”);当重新平衡后, 浓度_____(填“变大”“变小”或“不变”)。
(5)一定条件下, 与 反应可合成 ,
,该反应分两步进行:ⅰ.
ⅱ.
T℃,压强恒定为100kPa时,将 的混合气体和催化剂投入反应器中,达平衡时,部
分组分的物质的量分数如表所示。
组分
物 质 的 量 分 数
(%)
的平衡转化率为_____,反应ⅰ的平衡常数 _____( 是以分压表示的平衡常数,分压=总压×物质
的量分数)。
【答案】(1)1073.0 (2)CD
(3)= (4) ①. 向左移动 ②. 不变
(5) ①. 90% ②. 3.4
【解析】
【小问1详解】
反应Ⅱ. 的 , 、 、 的键
能分别为803kJ/mol、464kJ/mol、436kJ/mol,则有:2E(C=O)+E(H-H)-E(C≡O)-2E(H-O)=2×803+436-
E(C≡O)-2×464=+41,解得:E(C≡O)=1073kJ/mol,即 中碳氧键的键能为1073kJ/mol,故答案为:
1073;
【小问2详解】
A. 化学平衡的特征之一为各组分的浓度保持不变,而不是相对或成比例,故 与 比值不变,
不能说明反应达到化学平衡,A不合题意;
B. 已知反应Ⅱ前后气体的质量不变,容器为恒容密闭容器,即反应过程中容器内气体的密度一直不变,故
容器内气体密度不变不能说明反应达到化学平衡,B不合题意;
C. 反应Ⅱ前后气体的物质的量虽然保持不变,容器的体积保持不变,但为绝热容器,故反应过程中容器的
温度一直在改变,即容器的压强一直在改变,即容器内气体压强不变说明反应达到化学平衡,C符合题意;D. 即为浓度熵或平衡常数,反应过程中一直在改变,且平衡常数仅仅是温度的函数,温
度一直在改变, 也一直在变, 保持不变可以说明反应达到化学平衡,D
符合题意;
故答案为:CD;
【小问3详解】
已知化学平衡的本质特征为正、逆反应速率相等,即任何平衡状态下,净反应速率( )等于正、逆反应速
率之差均为0,故有平衡时, = ,故答案为:=;
【小问4详解】
对于反应Ⅲ. ,若平衡时保持温度不变,再充入 ,使其浓度增大
到原来的2倍,则增大生成物浓度,化学平衡移动方向为向逆反应方向即向左移动;根据平衡常数
K=c(CO)仅仅是温度的函数可知,当重新平衡后,CO 浓度不变,故答案为:向左移动;不变;
2 2
【小问5详解】
令CO 的初始物质的量为1mol,H 的初始物质的量为3mol,设平衡气中CO 为xmol,CO为ymol,HO
2 2 2 2
(g)为zmol,则平衡时气体的总物质的量为 y÷ %= %ymol,平衡时H 的物质的量为 %ymol×
2
%=5ymol,平衡时CH=CH 的物质的量为 %ymol× %=4ymol,由碳原子守恒:x+y+8y=1;由
2 2
氧原子守恒:2x+y+z=2;由氢原子守恒:2x+10y+16y=6;联合解得x=0.1,y=0.1,z=1.7;CO 的平衡转化
2
率为 ×100%=90%,CO 、HO 的物质量分数为 、 ,反应ⅰ的平衡常数 K=
2 2 p= =3.4,故答案为:90%;3.4。
18. 酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所示:
(1)A的化学名称为___________。
(2)酮基布洛芬官能团的名称为___________,D→E的反应类型为___________。
(3)写出C的结构简式:___________;A~G中含有手性碳原子的物质有___________种。
(4)请写出B在NaOH水溶液中加热的化学方程式:___________。
(5)H为酮基布洛芬的同分异构体,则符合下列条件的H有___________种。
①含 的酯类化合物
②两个苯环上还有一个取代基
(6)以 、苯和 为原料(无机试剂任选),设计制
的一种合成路线____。
【答案】(1)间甲基苯甲酸(3-甲基苯甲酸)
(2) ①. 羧基、酮羰基 ②. 取代反应
(3) ①. ②. 2(4) (5)18
( 6 )
【解析】
【分析】B和NaCN反应生成C,C和SOCl 发生取代反应生成D,由B、D的结构简式及C的分子式可推
2
测出,C为 ;D和苯在AlCl 的作用下发生取代反应生成E和HCl,根据D、F的结构简
3
式及E的分子式可推测出,E为 。
【小问1详解】
由A的结构简式可知,A的名称为间甲基苯甲酸(3-甲基苯甲酸);
【小问2详解】
由酮基布洛芬的结构简式可知,其官能团为羧基、酮羰基;D和苯在AlCl 的作用下反应生成E,该反应为
3
取代反应;
【小问3详解】由分析可知,C的结构简式为 ;由A~G的结构简式可知,F、G中含有手性碳原子,共2
种;
【小问4详解】
B中含有羧基能和NaOH反应,含有Cl原子,能在NaOH水溶液加热的条件下发生水解反应,则B在
NaOH水溶液中加热的化学方程式为 ;
【小问5详解】
H为酮基布洛芬的同分异构体,①含 的酯类化合物;②两个苯环上还有一个取代基;H
的取代基可能为:—CHCHOOCH、—CHOOCCH 、—OOCCH CH、 、—CHCOOCH 、
2 2 2 3 2 3 2 3
—COOCH CH, 上含有3种不同环境的氢原子( ),则符合条件的H
2 3
的结构简式共有18种;
【小问6详解】
被酸性KMnO 溶液氧化生成 ,
4和SOCl 发生取代反应生成 ,
2
和苯在AlCl 的作用下发生取代反应生成
3
, 和H 发生加成
2
反应生成 ,则合成路线为
。