文档内容
衡阳县四中 2025 届高三第一学期期末考试 A.实验室中金属钠着火时,可以用泡沫灭火器灭火
B. 等钡的化合物均有毒,相关废弃物应进行无害化处理
化 学
C.浓硫酸不慎溅到皮肤上,应立即用大量水冲洗,然后再涂上 3%~5%的碳酸氢钠溶
液
注意事项:
D.实验室制乙酸乙酯时,应将导管直接插入饱和碳酸钠溶液中收集产物
1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证
4.设 为阿伏加德罗常数的值。下列叙述正确的是( )
号条形码粘贴在答题卡上的指定位置。
A.一定条件下, 分解得到气体产物的分子总数为
2.选择题的作答:每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案
标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。 B. 由 和 组成的混合气体含有的原子总数为
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。写在试题
C.标准状况下, 与水完全反应生成 和 时转移的电子数为
卷、草稿纸和答题卡上的非答题区域均无效。
D.在核反应 中, 含有的中子数为
4.考试结束后,请将本试题卷和答题卡一并上交。
5.对于下列过程中发生的化学反应,相应离子方程式正确的是( )
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 Si 28 P 31 S 32
Cl 35.5 Cr 52 Cu 64 Zn 65 A.用硫酸铜溶液除去电石气中的 :
一、单选题(每题3分,共42分)
B.将 通入84消毒液中(有效成分 ):
1.科技创新是推动社会进步和经济发展的关键因素。下列说法正确的是( )
C . 将 铝 屑 与 烧 碱 溶 液 混 合 放 入 管 道 , 疏 通 管 道 :
A.“深地一号”制造钻头用的金刚石为共价晶体
B.实施 海底封存,减少温室气体的排放, 液化时破坏了共价键
D.用稀硝酸清洗试管壁上的银镜:
C.量子通信技术中作为传输介质的光导纤维,其主要成分为晶体
6.下列对物质的性质描述与化学实验不具有对应关系的是( )
D.“华龙一号”核电项目中,所用轴棒中含有的 和 互为同素异形体
选
2.某化学兴趣小组进行 相关实验,下列实验装置可以达到预期实验目的的是 物质 性质 化学实验
项
( )
A 密度大于空气 向上排空气法收集
B 浓溶液具有强氧化性 铁、铝插入浓硝酸中钝化
C 水溶液呈碱性 与澄清石灰水混合有白色沉淀产生
D 漂白性 溶液使品红溶液褪色
A.制备 气体 B.干燥 气体
7.某化合物由原子序数依次增大的短周期主族元素 W、X、Y、Z、Q组成(结构如
图)。X的核外电子数是其最外层电子数的2倍,Y是构成有机物的主要元素,Q和W
能形成两种室温下常见的液态化合物,下列说法正确的是( )
C.验证 是酸性氧化物 D.收集 气体
3.下列有关化学实验安全的必备知识,说法正确的是( )A.W存在两种核素 B.Q的氢化物中Q的化合价均为 价
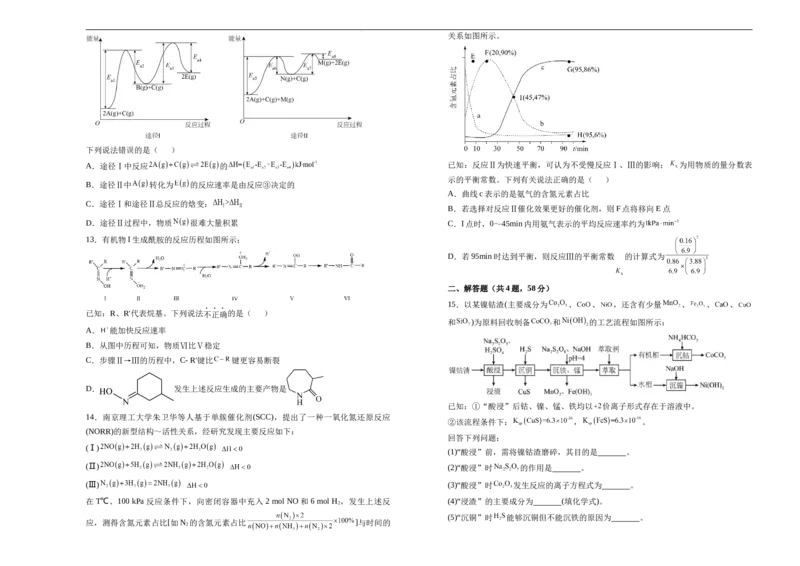
A.将硼镁矿研磨成粉末可以加快浸取速率
C. 为离子化合物 D.简单氢化物的沸点:
B. 溶液中的杂质主要是 和
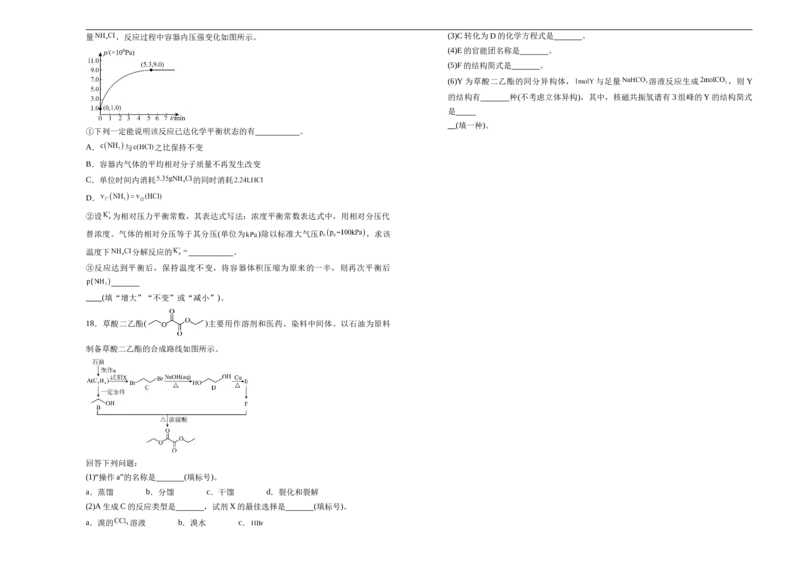
8.中药密蒙花具有抗氧化应激、肝脏保护作用、抗炎和神经保护功能,在临床被广泛
用于治疗各类眼科疾病,其中一种活性成分的结构简式如图,下列说法正确的是 C.一系列操作主要包括冷却结晶、过滤、洗涤、干燥
( )
D.硼砂溶液与硫酸反应的离子方程式为
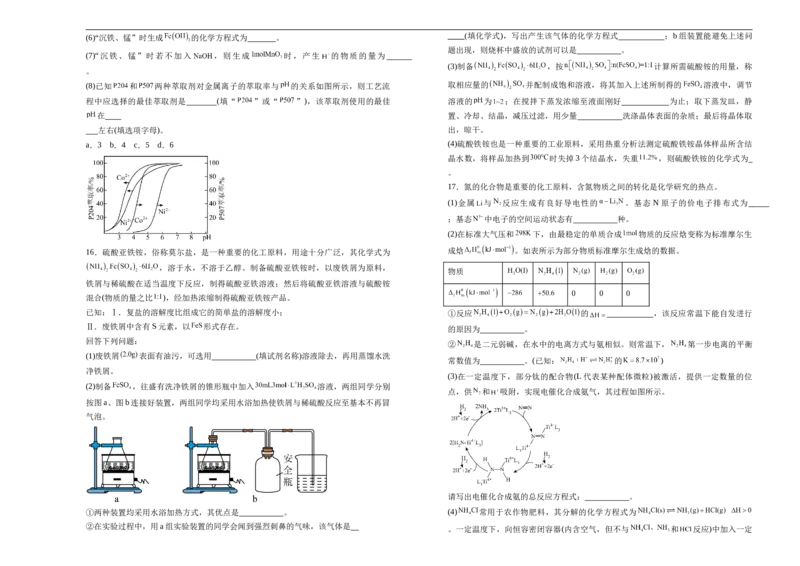
11.朱砂(硫化汞)在众多先秦考古遗址中均有发现,其立方晶系β型晶胞如下图所示,
晶胞参数为anm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为N ,下列说
A
法正确的是( )
A.该分子不能与酸反应
B.可能发生取代反应,加成反应、缩聚反应
C.一定条件下,与足量Na反应,1mol该分子最多消耗4mol Na
D.分子中所有碳原子可能共平面
9.电催化含氮废水合成尿素 ,有助于实现碳中和及解决水污染问题。利用
A.S原子的配位数是8 B.晶胞中B原子分数坐标为
如下图所示装置可合成尿素。该装置工作时,下列说法不正确的是( )
C.该晶体的密度是ρ= D.相邻两个Hg的最短距离为 anm
12.已知 和 经过两种途径转化为 的反应如下:途径Ⅰ:①
; ② ; 途 径 Ⅱ : ③ ; ④
。其反应过程的能量变化如图所示,已知 的单位为
A.电源B极为正极
。
B.该装置采用质子交换膜
C.a电极上发生反应:
D.理论上,每生成 ,阳极区质量减少32g
10.硼酸 是重要的化工原料,一种以硼镁矿(含 及少量
)为原料生产硼酸的工艺流程如图所示,下列说法错误的是( )
[已知:硼酸和硼砂 均易溶于热水,在冷水中溶解度小]关系如图所示。
下列说法错误的是( )
A.途径Ⅰ中反应 的 已知:反应Ⅱ为快速平衡,可认为不受慢反应Ⅰ、Ⅲ的影响; 为用物质的量分数表
示的平衡常数。下列有关说法正确的是( )
B.途径Ⅱ中 转化为 的反应速率是由反应③决定的
A.曲线c表示的是氨气的含氮元素占比
C.途径Ⅰ和途径Ⅱ总反应的焓变:
B.若选择对反应Ⅱ催化效果更好的催化剂,则F点将移向E点
D.途径Ⅱ过程中,物质 很难大量积累 C.I点时,0~45min内用氨气表示的平均反应速率约为
13.有机物I生成酰胺的反应历程如图所示:
D.若95min时达到平衡,则反应Ⅲ的平衡常数 的计算式为
二、解答题(共4题,58分)
15.以某镍钴渣(主要成分为 、 、 ,还含有少量 、 、 、
已知:R、R′代表烷基。下列说法不正确的是( )
和 )为原料回收制备 和 的工艺流程如图所示:
A. 能加快反应速率
B.从图中历程可知,物质Ⅵ比Ⅴ稳定
C.步骤Ⅱ→Ⅲ的历程中,C- R′键比 键更容易断裂
D. 发生上述反应生成的主要产物是
已知:①“酸浸”后钴、镍、锰、铁均以 价离子形式存在于溶液中。
14.南京理工大学朱卫华等人基于单簇催化剂(SCC),提出了一种一氧化氮还原反应
②该流程条件下: , 。
(NORR)的新型结构~活性关系,经研究发现主要反应如下:
回答下列问题:
(Ⅰ)
(1)“酸浸”前,需将镍钴渣磨碎,其目的是 。
(Ⅱ) (2)“酸浸”时 的作用是 。
(Ⅲ) (3)“酸浸”时 发生反应的离子方程式为 。
在T℃、100 kPa 反应条件下,向密闭容器中充入 2 mol NO 和6 mol H ,发生上述反 (4)“浸渣”的主要成分为 (填化学式)。
2
(5)“沉铜”时 能够沉铜但不能沉铁的原因为 。
应,测得含氮元素占比[如N 的含氮元素占比 ]与时间的
2(6)“沉铁、锰”时生成 的化学方程式为 。 (填化学式),写出产生该气体的化学方程式 ;b组装置能避免上述问
题出现,则烧杯中盛放的试剂可以是 。
(7)“沉铁、锰”时若不加入 ,则生成 时,产生 的物质的量为
(3)制备 ,按 计算所需硫酸铵的用量,称
。
(8)已知 和 两种萃取剂对金属离子的萃取率与 的关系如图所示,则工艺流 取相应量的 并配制成饱和溶液,将其加入上述所制得的 溶液中,调节
程中应选择的最佳萃取剂是 (填“ ”或“ ”),该萃取剂使用的最佳 溶液的 为 ;在搅拌下蒸发浓缩至液面刚好 为止;取下蒸发皿,静
在 置、冷却、结晶,减压过滤,用少量 洗涤晶体表面的杂质;最后将晶体取
左右(填选项字母)。 出,晾干。
a.3 b.4 c.5 d.6 (4)硫酸铁铵也是一种重要的工业原料,采用热重分析法测定硫酸铁铵晶体样品所含结
晶水数,将样品加热到 时失掉3个结晶水,失重 ,则硫酸铁铵的化学式为
。
17.氮的化合物是重要的化工原料,含氮物质之间的转化是化学研究的热点。
(1)金属 与 反应生成有良好导电性的 。基态 N 原子的价电子排布式为
;基态 中电子的空间运动状态有 种。
(2)在标准大气压和 下,由最稳定的单质合成 物质的反应焓变称为标准摩尔生
16.硫酸亚铁铵,俗称莫尔盐,是一种重要的化工原料,用途十分广泛,其化学式为 成焓 。如表所示为部分物质标准摩尔生成焓的数据。
,溶于水,不溶于乙醇。制备硫酸亚铁铵时,以废铁屑为原料,
物质
铁屑与稀硫酸在适当温度下反应,制得硫酸亚铁溶液;然后将硫酸亚铁溶液与硫酸铵
0 0 0
混合(物质的量之比 ),经加热浓缩制得硫酸亚铁铵产品。
已知:Ⅰ.复盐的溶解度比组成它的简单盐的溶解度小; ①反应 的 ,该反应常温下能自发进行
Ⅱ.废铁屑中含有S元素,以 形式存在。
的原因为 。
回答下列问题:
② 是二元弱碱,在水中的电离方式与氨相似。则常温下, 第一步电离的平衡
(1)废铁屑 表面有油污,可选用 (填试剂名称)溶液除去,再用蒸馏水洗
常数值为 。(已知: 的 )
净铁屑。
(3)在一定温度下,部分钛的配合物(L代表某种配体微粒)被激活,提供一定数量的位
(2)制备 ,往盛有洗净铁屑的锥形瓶中加入 溶液,两组同学分别
点,供 和 吸附,实现电催化合成氨气,其过程如图所示。
按图a、图b连接好装置,两组同学均采用水浴加热使铁屑与稀硫酸反应至基本不再冒
气泡。
请写出电催化合成氨的总反应方程式: 。
①两种装置均采用水浴加热方式,其优点是 。 (4) 常用于农作物肥料,其分解的化学方程式为
②在实验过程中,用a组实验装置的同学会闻到强烈刺鼻的气味,该气体是
。一定温度下,向恒容密闭容器(内含空气,但不与 和 反应)中加入一定量 ,反应过程中容器内压强变化如图所示。 (3)C转化为D的化学方程式是 。
(4)E的官能团名称是 。
(5)F的结构简式是 。
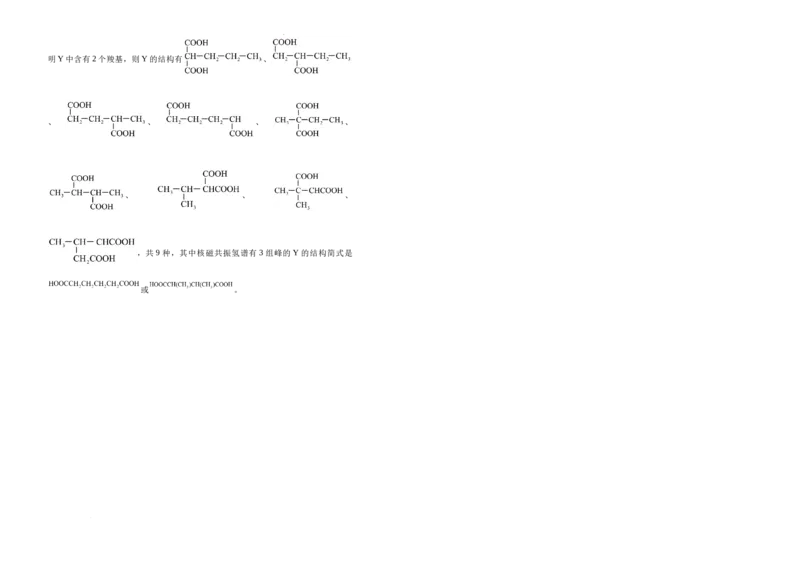
(6)Y为草酸二乙酯的同分异构体, 与足量 溶液反应生成 ,则Y
的结构有 种(不考虑立体异构),其中,核磁共振氢谱有3组峰的Y的结构简式
是
(填一种)。
①下列一定能说明该反应已达化学平衡状态的有 。
A. 与 之比保持不变
B.容器内气体的平均相对分子质量不再发生改变
C.单位时间内消耗 的同时消耗
D.
②设 为相对压力平衡常数,其表达式写法:浓度平衡常数表达式中,用相对分压代
替浓度。气体的相对分压等于其分压(单位为 )除以标准大气压 ,求该
温度下 分解反应的 。
③反应达到平衡后,保持温度不变,将容器体积压缩为原来的一半,则再次平衡后
(填“增大”“不变”或“减小”)。
18.草酸二乙酯( )主要用作溶剂和医药、染料中间体。以石油为原料
制备草酸二乙酯的合成路线如图所示。
回答下列问题:
(1)“操作a”的名称是 (填标号)。
a.蒸馏 b.分馏 c.干馏 d.裂化和裂解
(2)A生成C的反应类型是 ,试剂X的最佳选择是 (填标号)。
a.溴的 溶液 b.溴水 c.化学参考答案
总数为 = ,B正确;C. 中,H、F的化合价不
1.【答案】A
变, 价的 O 和 价的 O 发生归中反应生成 , 完全反应时转移 1mol 电
【解析】A.金刚石结构中碳原子与周围的四个碳原子以单键结合,形成立体网状结
子 , C 项 错 误 ; D . 根 据 质 量 守 恒 和 质 子 守 恒 知 , 含 中 子 数 :
构,为共价晶体,故A正确;B. 是分子晶体,液化时破坏的是分子间作用力,不
,D项错误;答案选B。
破坏共价键,故B错误;C.光导纤维主要成分为 ,故C错误;D. 和 互
5.【答案】C
为同位素,故D错误;答案选A。
2.【答案】B 【 解 析 】 A . 硫 化 氢 为 弱 电 解 质 , 不 能 拆 开 , 反 应 的 离 子 方 程 式 为 :
【解析】A.铜与浓硫酸反应需要加热,A错误;B.浓硫酸不能氧化二氧化硫,可以
,故A错误;B.次氯酸钠具有强氧化性,将二氧化硫氧化为硫酸
用来干燥二氧化硫,B正确;C.二氧化硫能使品红褪色,验证的是漂白性,不能验证
酸性氧化物,C错误;D.二氧化硫与水反应不能用排水法收集,D错误;故选B。 根,因此反应的离子方程式为: ,故B错误;C.铝屑与
3.【答案】C 烧 碱 溶 液 反 应 生 成 Na[Al(OH)
4
] 和 氢 气 , 离 子 方 程 式 为 :
【解析】A.金属钠着火时,与空气中的氧气反应生成过氧化钠,过氧化钠与水,二氧 ,故C正确;D.试管壁上的银镜用稀硝酸清洗:
化碳反应,而干冰灭火器和泡沫灭火器都生成二氧化碳,只能用干燥沙土盖灭,A错
,故D错误;故答案选C。
误;B. 难溶于水,且性质稳定,不溶于水和酸,因此可以用作“钡餐”来诊断
6.【答案】C
消化道疾病,这说明它对人体无害,无毒性 ,B错误;C.浓硫酸溅到皮肤上时,先用
大量的水冲洗,然后再涂上 3%~5%的碳酸氢钠溶液,C正确;D.实验室制乙酸乙酯 【解析】A.NO 2 的密度大于空气,可以用向上排空气法收集 NO 2 ,A不符合题意;
时,应将导管末端应该在饱和碳酸钠溶液液面上,收集产物,D错误;故选C。
B.浓硝酸具有强氧化性,可以使铁铝发生钝化,B不符合题意;C.NaHCO 水溶液
3
4.【答案】B
呈碱性,说明 发生水解,NaHCO 与澄清石灰水混合有白色沉淀产生,是因为
3
【解析】A.HI的分解反应是可逆反应,1molHI生成 和 的总物质的量小于1mol,
与 OH-、Ca2+发生反应生成了CaCO 沉淀,与 的水解没有对应关系,C符
3
A项错误;B. 和 最简式相同, 由 和 组成的混合气体含有的原子
合题意;D.NaClO具有强氧化性、漂白性,能够使品红溶液褪色,D不符合题意;答
案选B。
学科网(北京)股份有限公司7.【答案】D 10.【答案】B
【解析】A.W为氢,存在 、 、 三种核素,A错误;B.Q的氢化物有两种, 【解析】A.硼镁矿研磨成粉末可以增大固体的表面积,有利于增大反应物的接触面
积,加快浸取速率,故A正确;B.由分析可知,硼酸钠溶液中的主要杂质为硅酸钠和
分别是 、 ,其中的Q元素化合价分别为 和 价,B错误;C. 和 处在
四羟基合铝酸钠,故B错误;C.由分析可知,得到硼酸的一系列操作为冷却结晶、过
滤、洗涤、干燥,故C正确;D.由分析可知,加入热水和稀硫酸调节溶液pH为2的
元素周期表的对角线上,具有相似的化学性质,如 和 都属于共价化合物,C
目的是将硼砂转化为硼酸,反应的离子方程式为 ,故D正
错误;D.常温水为液态、氨气和甲烷为气体,水沸点最高;氨气分子能形成氢键且相
确;故选B。
对分子质量大于甲烷,故其沸点高于甲烷,则简单氢化物的沸点: ,D
11.【答案】C
正确;故选D。
【解析】A.由晶胞图知,S原子周围距离最近的Hg原子有4个,S的配位数是4,故
8.【答案】B
A错误;B.由 A原子的分数坐标为(0,0,0),结合投影图知,晶胞中 B 原子位于
【解析】A.该活性成分中含有醇羟基,能与酸发生酯化反应,A项错误;B.该分子
“左上前”的小四面体体心,其分数坐标为( , , ),故B错误;C.由晶胞图可
含有羟基,能发生取代反应,能与醛发生缩聚反应,含有苯环,能发生加成反应,B
项正确;C.羟基能与 Na 反应,1mol 该分子含 5mol 羟基,则 1mol 最多消耗 5mol 知,S原子位于体内,含S原子=4×1=4个,Hg原子位于8个顶角和6个面心,共含Hg
Na,C项错误;D.由题干有机物的结构简式可知,分子中左侧环上的碳原子均采用
sp3杂化,则所有碳原子不可能共平面,D项错误;故选B。
原子数=6× +8× =4,故该晶体的密度是 ,故 C 正
9.【答案】D
确;D.相邻两个 Hg的最短距离为面对角线的一半,为 anm,故D错误;故选:
【解析】A.b是阳极,所以电源B极为正极,故A正确;B.b是阳极,阳极反应式
C。
为 2H O-4e-=O +4H+ ; a 是 阴 极 , 阴 极 反 应 式 为
2 2
12.【答案】C
,阳极生成氢离子、阴极消耗氢离子,所以该
【解析】A.由图可知,反应 的 ,A 正
装置采用质子交换膜,故B正确;C.a是阴极,硝酸根离子得电子生成CO(NH ) ,a
2 2
确;B.由图可知,反应③的活化能大于反应④的活化能,活化能越大反应速率越慢,
电极上发生反应: ,故C正确;D.理论上,
决速步骤由最慢的步骤决定,故途径Ⅱ中A(g)转化为E(g)的反应速率是由反应③决定
每生成 ,电路中转移4mol电子,阳极放出1mol氧气,同时有4molH+移入 的,B正确;C.根据盖斯定律,途径I和途径Ⅱ总反应的焓变相等,即 ,C
阴极区,所以阳极区质量减少36g,故D错误;选D。 错误;D.由图可知,途径Ⅱ中反应④的活化能低于反应③的活化能,活化能越低反应
学科网(北京)股份有限公司速率越快,故反应④的反应速率大于反应③的反应速率,物质 N(g)很难大量积累,D
【解析】A.反应 ii 为快反应,曲线 a表示物质快速减少,故表示 NO,NH 快速增
3
正确;故选C。
加,故曲线b表示氨气,曲线表示c氮气,A错误;B.若选择对反应Ⅱ催化效果更好
13.【答案】D
的催化剂,反应Ⅱ会更快,生成NH 达到最高点所用时间短,NH 的占比更大,因此F
3 3
点可能移向E点上方的某个点,B错误;C.起始时,压强为100kPa、2mol NO、6mol
【解析】A.由图可知,氢离子是反应的催化剂,能降低反应的活化能,加快反应速
H ,Ⅰ点时,由图知,NO的氮含量为6%,n(NO)=2mol×6%=0.12mol,NH 的氮含量
2 3
为 47%,n(NH )=2mol×47%=0.94mol,N 的氮含量为 47%,n(N )=
率,故A正确;B.由结构简式可知, 分子中羟基直接连在不饱和碳 3 2 2
, 由 氧 守 恒 得 , n(H O)=2mol-0.12mol=1.88mol , 由 氢 守 恒 得 , n(H )=
2 2
原子上,结构不稳定,会转化为结构稳定的 ,所以物质Ⅵ比Ⅴ稳
, 此 时 的 总 压 为 P =
总
=76.5kPa , 氨 气 的 分 压 为 P(NH )=
3
定,故 B 正确;C.由结构简式可知, 发生 C- R′键断裂转化为
,则0~45min内用氨气表示的平均反应速率
约为 ,C错误;D.起始时,2mol NO、6mol H ,若95min时达
2
,说明 C- R′键比 键更容易断裂,故C正确;D.由图可知, 到平衡,则由图知,NO 的氮含量为 6%,n(NO)=2mol×6%=0.12mol,N 的氮含量为
2
86% , n(N )= , NH 的 氮 含 量 为 100%-6%-86%=8% ,
2 3
n(NH )=2mol×8%=0.16mol,由氧守恒得,n(H O)=2mol-0.12mol=1.88mol,由氢守恒
3 2
发生上述反应生成的主要产物是 或 ,不能
得 , n(H )= , 此 时 总 物 质 的 量 为
2
转化为 ,故D错误;故选D。 (0.12+0.86+0.16+1.88+3.88)=6.9mol,N 的物质的量分数为 ,H 的物质的量分数
2 2
14.【答案】D
学科网(北京)股份有限公司16.【答案】(1)碳酸钠溶液或氢氧化钠溶液(2分)
为: ,NH 的物质的量分数为: ,则反应Ⅲ的平衡常数Kx= ,D
3 (2) 使 反 应 物 受 热 均 匀 , 反 应 温 度 易 于 控 制 ( 2 分 ) H S ( 2 分 )
2
(2分) 溶液或 溶液(2分)
正确;故选D。
(3)出现晶膜(2分) 乙醇(1分)
15.【答案】(1)增大固体与溶液的接触面积,加快反应速率,提高浸出效率(2分)
(4) (2分)
(2)作还原剂,还原+3价钴、+4价锰和+3价铁(2分)
(3)2Co O +S +6H+=4Co2++ 2 +3H O(2分) 【解析】(1)油脂在碱性条件下能完全水解生成可溶性物质,所以可以选用热的碳酸
2 3 2 2
(4)CaSO 、SiO (2分) 钠溶液或氢氧化钠溶液除去铁屑表面的油污,故答案为:热的碳酸钠溶液或氢氧化钠
4 2
(5)CuS的溶解度非常小,且不溶于一般稀酸,而FeS能够溶于强酸(2分) 溶液;(2)①水浴加热可以使反应物受热均匀,反应温度易于控制,所以,故答案
(6)2FeSO +Na S O +6NaOH=2Fe(OH) ↓+4Na SO (2分) 为:使反应物受热均匀,反应温度易于控制;②由题意可知,废铁屑中含有硫化亚
4 2 2 8 3 2 4
(7)4mol(1分) 铁,用a组实验装置的同学会闻到强烈刺鼻的气味是因为废铁屑与稀硫酸反应时,硫
(8)P507(1分) c(1分) 化亚铁会与稀硫酸反应生成硫酸亚铁和硫化氢气体,反应的化学方程式为
【解析】镍钴渣酸浸并用 Na S O 还原;浸渣为 SiO 和 CaSO ,浸出液中有 Cu2+、
2 2 5 2 4
;硫化氢能与氢氧化钠溶液反应生成硫化钠和水,也能与硫
Co2+、Ni2+、Mn2+、Fe2+,通入H S气体生成CuS沉淀除去Cu2+,加入Na S O 和NaOH
2 2 2 8
酸铜溶液反应生成硫化铜沉淀和硫酸,所以b组装置的烧杯中盛放的试剂是可以吸收
除去Mn2+和Fe2+,形成MnO 和Fe(OH) 沉淀,加萃取剂在有机相萃取出Co2+离子,有
2 3
硫化氢气体,防止污染环境的氢氧化钠溶液或硫酸铜溶液,故答案为:H S ;
2
机相加入NH HCO 沉淀出Co2+,水相中加入NaOH得到Ni(OH) 沉淀;(1)“酸浸”
4 3 2
前,需将镍钴渣磨碎,其目的是增大固体与溶液的接触面积,加快反应速率,提高浸 ; 溶液或 溶液;(3)硫酸亚铁铵溶于水、不溶于
出效率;(2)由已知信息可知,“酸浸”时 Na S O 的作用是作还原剂,还原+3价
2 2 5
乙醇,由题意可知,制备硫酸亚铁铵晶体的操作为将硫酸铵饱和溶液加入硫酸亚铁溶
钴、+4价锰和+3价铁;(3)“酸浸”时 Co O 发生反应的离子方程式为 2Co O +S
2 3 2 3 2
液中,调节溶液的pH为1~2,在搅拌下蒸发浓缩至液面刚好出现晶膜为止,取下蒸发
皿,静置、冷却、结晶,减压过滤,用少量乙醇洗涤表面的杂质,最后将晶体取出,
+6H+=4Co2++ 2 +3H O;(4)“浸渣”的主要成分为 CaSO 和 SiO ;(5)
2 4 2
“沉铜”时生成CuS,CuS的溶解度非常小,且不溶于一般稀酸,而FeS能够溶于强 晾干,故答案为:出现晶膜;乙醇;(4)设结晶水合物的化学式为
酸 ; ( 6 ) “ 沉 铁 、 锰 ” 时 生 成 Fe(OH) 的 化 学 方 程 式 为
3
2FeSO 4 +Na 2 S 2 O 8 +6NaOH=2Fe(OH) 3 ↓+4Na 2 SO 4 ;(7)“沉铁、锰”时,若不加入 ,由题意可得: %=11.2%,解得 ,则硫酸铁铵的化学式为
NaOH,Mn2+发生反应Mn2++S +2H O=MnO ↓+2S +4H+,则生成1mol MnO 时,
2 2 2 2
,故答案为: 。
产生 H+的物质的量为4mol;(8)P507能够将两种金属离子分离开,则工艺流程中应
17.【答案】(1)2s22p3(1分) 5(1分)(2) -622.6kJ/mol (2分) 该反
选择的最佳萃取剂是P507,其使用的最佳pH 在5左右。
学科网(北京)股份有限公司应为放热反应,反应的熵变ΔS基本不变,常温下反应ΔH—TΔS<0,能自发进行(2 正逆反应速率相等,反应已达到平衡,故正确;故选BD;②由图可知,起始空气的压
分) 8.7×10—7(2分) 强为1.0×103kPa,平衡时混合气体的总压为9.0×103kPa,则由方程式可知,氯化氢和氨
(3)N +3H 2NH (2分)
2 2 3
气的平衡分压都为 =4.0×103kPa,则氯化铵分解反应的
(4)BD(2分) 1600(1分) 不变(1分)
【解析】(1)氮元素的原子序数为7,基态原子的价电子排布式为2s22p3,基态氮离
子的电子排布式为 1s22s22p6,电子的空间运动状态有 5 种,故答案为:2s22p3;5; × =1600,故答案为:1600;③平衡常数为温度函数,温度不变,
(2)①由△H=生成物的标准摩尔生成焓之和—反应物的标准摩尔生成焓之和可得:反
平衡常数不变,则反应达到平衡后,保持温度不变,将容器体积压缩为原来的一半,
应△H=(−286 kJ/mol×2+0)-(+50.6 kJ/mol+0)=-622.6kJ/mol;该反应为放热反应,反应的
再次平衡后氨气和氯化氢的分压均不变,故答案为:不变。
熵变ΔS基本不变,常温下反应ΔH-TΔS<0,能自发进行,故答案为:-622.6kJ/mol;
该反应为放热反应,反应的熵变ΔS基本不变,常温下反应ΔH-TΔS<0,能自发进行; 18.【答案】(1)d(2分)
(2)加成反应(1分) a(2分)
②由题意可知,肼在溶液中的第一步电离的电离方程式为 N H +H O N H + OH—,
2 4 2 2
(3) (2分)
(4)醛基(1分)
电离常数 K = ,由方程式可得,反应平衡常数 K= =
b1
(5) (2分)
(6)9(2分) 或 (2分)
= =8.7×107,解得K =8.7×10—7,故答案为:8.7×10—7;(3)由
b1
【解析】石油裂解得到乙烯,乙烯和溴发生加成反应生成1,2-二溴乙烷,1,2-二溴乙烷
图可知,电催化合成氨的总反应为Ti3+L 做催化剂条件下氮气与氢气反应生成氨气,反
3 水解为乙二醇,乙二醇发生催化氧化生成乙二醛(E),乙二醛氧化为乙二酸(F);乙烯和
水发生加成反应生成乙醇,乙醇和乙二酸发生酯化反应生成草酸二乙酯。(1)石油发
应的化学方程式为 N +3H 2NH ,故答案为:N +3H 2NH ;(4)
2 2 3 2 2 3
生裂化、裂解得到乙烯,“操作a”的名称是裂化和裂解,选d。(2)乙烯和溴发生加
①A.由方程式可知,氨气的浓度与氯化氢的浓度之比始终保持不变,则氨气的浓度
与氯化氢的浓度之比保持不变不能说明正逆反应速率相等,无法判断反应是否达到平 成反应生成1,2-二溴乙烷,溴易溶于四氯化碳,所以试剂 X的最佳选择是溴的 溶
衡,故错误;B.由质量守恒定律可知,容器内反应中气体的质量增大,由方程式可
液,选a。(3)1,2-二溴乙烷在氢氧化钠水溶液中发生水解反应生成乙二醇和溴化钠,
知,容器内气体的物质的量增大,由于装置内初始存在空气,则容器内气体的平均相
对分子质量减小,容器内气体的平均相对分子质量不再发生改变说明正逆反应速率相 化学方程式是 ;(4)E是乙二醛,结构简式
等,反应已达到平衡,故正确;C.缺标准状况下,无法计算 2.24L氯化氢的物质的
为 OHC-CHO,官能团名称是醛基;(5)F 是乙二酸,结构简式为 HOOCCOOH;
量,则单位时间内消耗5.35g氯化铵的同时消耗2.24L氯化氢不能说明正逆反应速率相
(6)Y为草酸二乙酯的同分异构体, 与足量 溶液反应生成 ,说
等,无法判断反应是否达到平衡,故错误;D.由方程式可知, 说明
学科网(北京)股份有限公司明Y中含有2个羧基,则Y的结构有 、
、 、 、 、
、 、 、
,共 9 种,其中核磁共振氢谱有 3 组峰的 Y 的结构简式是
或 。
学科网(北京)股份有限公司