文档内容
云南省 2025 年普通高校招生适应性测式
化学
注意事项:
1.答卷前、考生务必用黑色碳素笔将自己的姓名、准考证号、考场号、座位号填写在答题卡
上,并认真核准条形码上的姓名、准考证号、考场号、座位号及科目,在规定的位置贴好条
形码。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,用黑色碳素笔将答案写在
答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 云南传统工艺是各民族的智慧结晶。下列说法错误的是
A. “乌铜走银”中的铜合金硬度比纯铜的大
B. “银胎掐丝珐琅”用到的硅酸盐珐琅化学性质稳定
C. “手工造纸”中加入草木灰(含 )可以降低纸浆的
D. “户撒刀”锻制中将红热铁制刀具浸入水中,表面有 生成
【答案】C
【解析】
【详解】A.合金的硬度比形成合金的纯金属的硬度大,故铜合金硬度比纯铜的大,A项不符合题意;
B.硅酸盐珐琅具有良好的耐火性和化学稳定性,B项不符合题意;
C. 水溶液呈碱性,“手工造纸”中加入草木灰(含 )可以增大纸浆的 ,C项符合题意;
D.红热的铁与水蒸气反应,生成 ,D项不符合题意错误;
答案选C。
2. 科学使用化学品可提升人们生产生活质量。下列说法正确的是
第1页/共25页
学科网(北京)股份有限公司A. 有机氯农药防虫害效率高,可大量使用
B. 可用于中和过多的胃酸,缓解胃部不适
C. 苯甲酸钠是一种常用的增味剂,能增加食品的鲜味
D. 卤水能使豆浆中的蛋白质聚沉,是制作豆腐常用的凝固剂
【答案】D
【解析】
【详解】A.有机氯农药防虫害效率高,但有机氯有毒,危害人体健康,应该合理使用有机氯农药,不能
大量使用,故A错误;
B. 溶于盐酸,钡离子能使蛋白质变性,引起人体中毒,不能用 中和过多的胃酸,故B错
误;
C.苯甲酸钠是一种防腐剂,可以抑制细菌的滋生,防止食品变质,不是增味剂,不能增加食品的鲜味,
故C错误;
D.卤水中含电解质,在豆浆中加入卤水能使蛋白质发生聚沉,从而使豆浆凝固,是制作豆腐常用的凝固
剂,故D正确;
故答案为:D。
3. 下列反应方程式错误的是
A. B.
C. D.
【答案】A
【解析】
【详解】A.HClO为弱电解质,不能拆成离子,正确的离子方程式为: ,
A项符合题意;
B.Al与 发生铝热反应,生成Fe和 ,B项不符合题意;
C.HS与SO 发生归中反应生成S单质,C项不符合题意;
2 2
D.Na与HO反应生成NaOH和H,D项不符合题意;
2 2
答案选A。
4. 下列化学用语或图示表达正确的是
第2页/共25页
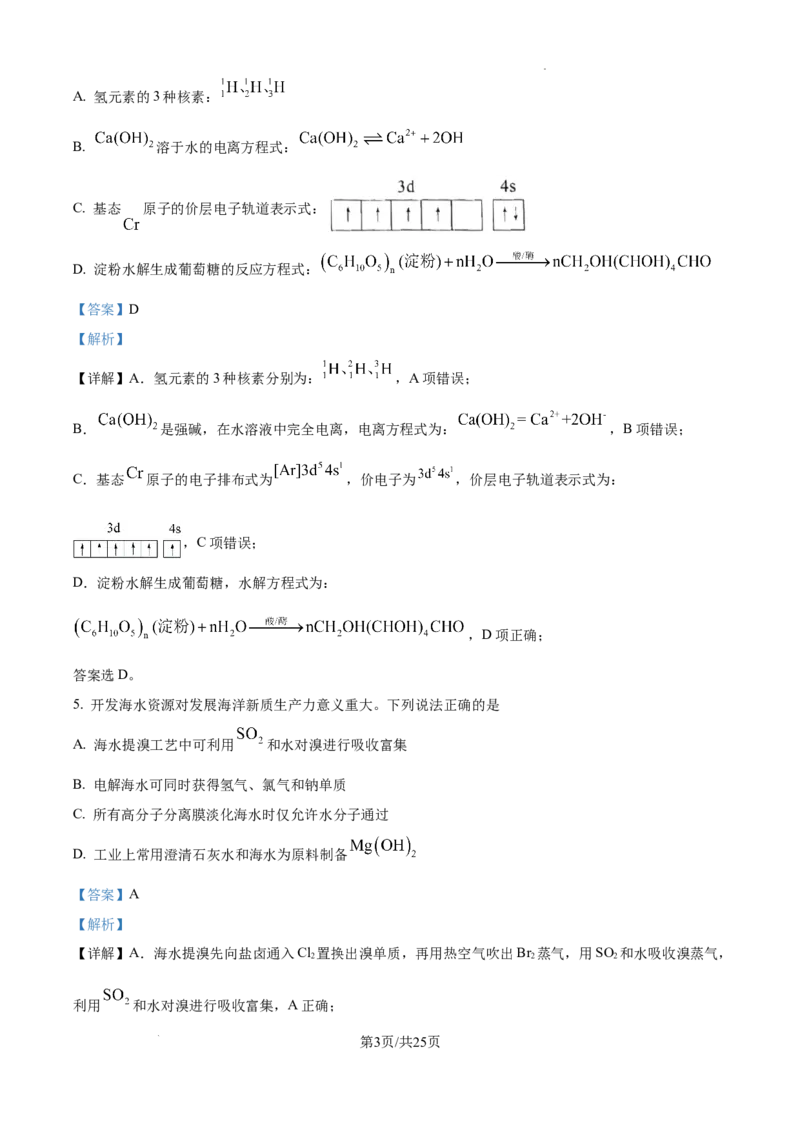
学科网(北京)股份有限公司A. 氢元素的3种核素:
B. 溶于水的电离方程式:
C. 基态 原子的价层电子轨道表示式:
D. 淀粉水解生成葡萄糖的反应方程式:
【答案】D
【解析】
【详解】A.氢元素的3种核素分别为: ,A项错误;
B. 是强碱,在水溶液中完全电离,电离方程式为: ,B项错误;
C.基态 原子的电子排布式为 ,价电子为 ,价层电子轨道表示式为:
,C项错误;
D.淀粉水解生成葡萄糖,水解方程式为:
,D项正确;
答案选D。
5. 开发海水资源对发展海洋新质生产力意义重大。下列说法正确的是
A. 海水提溴工艺中可利用 和水对溴进行吸收富集
B. 电解海水可同时获得氢气、氯气和钠单质
C. 所有高分子分离膜淡化海水时仅允许水分子通过
D. 工业上常用澄清石灰水和海水为原料制备
【答案】A
【解析】
【详解】A.海水提溴先向盐卤通入Cl 置换出溴单质,再用热空气吹出Br 蒸气,用SO 和水吸收溴蒸气,
2 2 2
利用 和水对溴进行吸收富集,A正确;
第3页/共25页
学科网(北京)股份有限公司B.电解海水可同时获得氢气、氯气和氢氧化钠,B错误;
C.所有高分子分离膜淡化海水时仅允许离子通过,C错误;
D.工业上常用石灰乳和海水为原料制备 ,D错误;
答案选A。
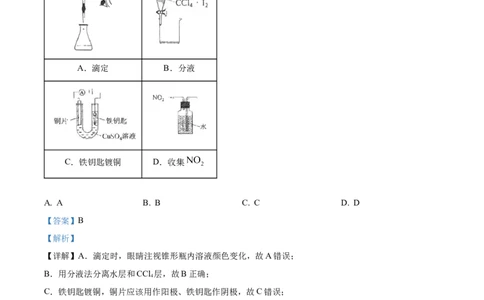
6. 下列操作及装置(夹持装置省略)能达到实验目的的是
A.滴定 B.分液
C.铁钥匙镀铜 D.收集
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.滴定时,眼睛注视锥形瓶内溶液颜色变化,故A错误;
B.用分液法分离水层和CCl 层,故B正确;
4
C.铁钥匙镀铜,铜片应该用作阳极、铁钥匙作阴极,故C错误;
D.NO 能与水反应,不能用排水法收集NO ,故D错误;
2 2
选B。
7. 制备 的化学方程式为: ,设 为阿
伏伽德罗常数的值。下列说法正确的是
A. 中原子总数为
第4页/共25页
学科网(北京)股份有限公司B. 中 键的数目为
C. 每消耗 ,转移电子数为
D. 溶液中 的数目等于
【答案】B
【解析】
【详解】A.没有注明标准状况,无法计算气体的物质的量,A错误;
B.1个 中有3个 键, 键的数目为 ,B正确;
C.根据方程式 可知,2molCl 参加反应,电子转
2
移的物质的量为2mol,电子转移数目为2N ,C错误;
A
D.没有给出溶液的体积,无法计算NaHCO 的物质的量,D错误;
3
答案选B。
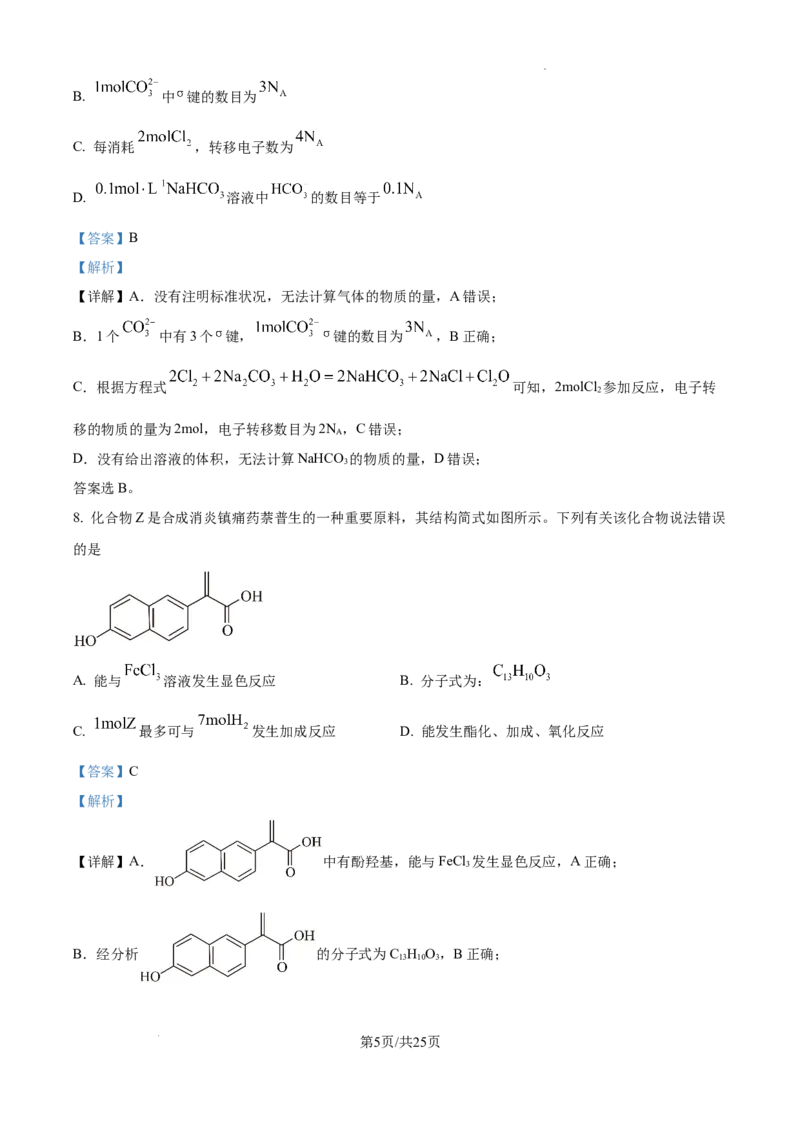
8. 化合物Z是合成消炎镇痛药萘普生的一种重要原料,其结构简式如图所示。下列有关该化合物说法错误
的是
A. 能与 溶液发生显色反应 B. 分子式为:
C. 最多可与 发生加成反应 D. 能发生酯化、加成、氧化反应
【答案】C
【解析】
【详解】A. 中有酚羟基,能与FeCl 发生显色反应,A正确;
3
B.经分析 的分子式为C H O,B正确;
13 10 3
第5页/共25页
学科网(北京)股份有限公司C. 最多可与6molH 发生加成反应,C错误;
2
D. 结构中有羧基可以发生酯化反应,有碳碳双键和苯环,可以发生加成反应,
酚羟基和碳碳双键可以发生氧化反应,D正确;
答案选C。
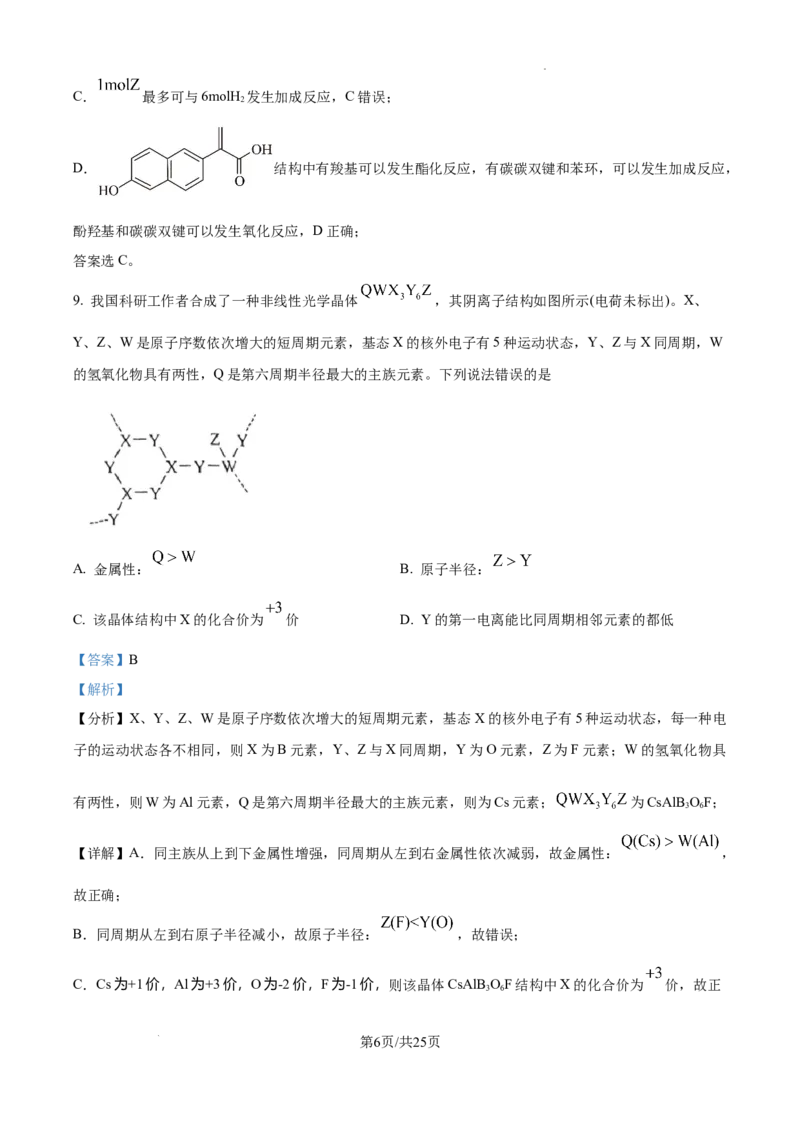
9. 我国科研工作者合成了一种非线性光学晶体 ,其阴离子结构如图所示(电荷未标出)。X、
Y、Z、W是原子序数依次增大的短周期元素,基态X的核外电子有5种运动状态,Y、Z与X同周期,W
的氢氧化物具有两性,Q是第六周期半径最大的主族元素。下列说法错误的是
A. 金属性: B. 原子半径:
C. 该晶体结构中X的化合价为 价 D. Y的第一电离能比同周期相邻元素的都低
【答案】B
【解析】
【分析】X、Y、Z、W是原子序数依次增大的短周期元素,基态X的核外电子有5种运动状态,每一种电
子的运动状态各不相同,则X为B元素,Y、Z与X同周期,Y为O元素,Z为F元素;W的氢氧化物具
有两性,则W为Al元素,Q是第六周期半径最大的主族元素,则为Cs元素; 为CsAlB OF;
3 6
【详解】A.同主族从上到下金属性增强,同周期从左到右金属性依次减弱,故金属性: ,
故正确;
B.同周期从左到右原子半径减小,故原子半径: ,故错误;
C.Cs为+1价,Al为+3价,O为-2价,F为-1价,则该晶体CsAlB OF结构中X的化合价为 价,故正
3 6
第6页/共25页
学科网(北京)股份有限公司确;
D.同周期元素由左向右元素原子的第一电离能呈递增趋势,但O原子的价电子排布式为2s22p4,N原子
的价电子排布式为2s22p3,p轨道为半充满状态较为稳定,故N、O、F三种元素第一电离能由大到小顺序
为F> N>O,Y的第一电离能比同周期相邻元素的都低,故正确;
答案选B。
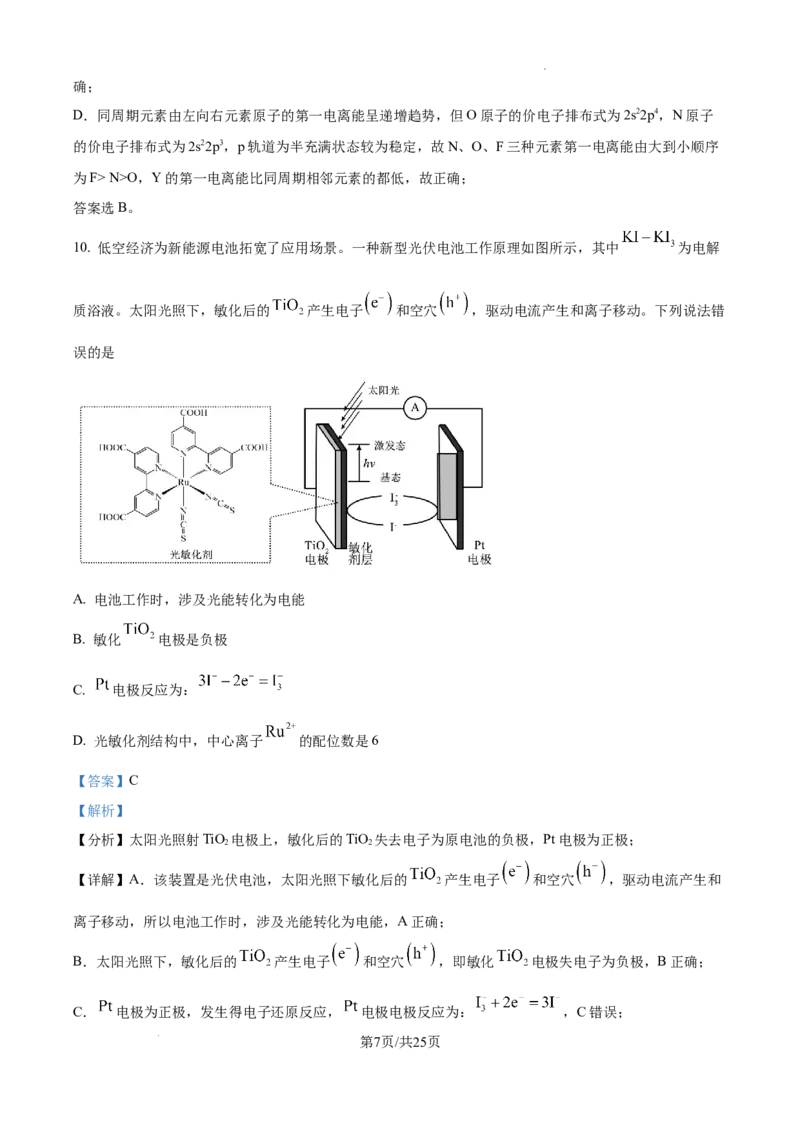
10. 低空经济为新能源电池拓宽了应用场景。一种新型光伏电池工作原理如图所示,其中 为电解
质浴液。太阳光照下,敏化后的 产生电子 和空穴 ,驱动电流产生和离子移动。下列说法错
误的是
A. 电池工作时,涉及光能转化为电能
B. 敏化 电极是负极
C. 电极反应为:
D. 光敏化剂结构中,中心离子 的配位数是6
【答案】C
【解析】
【分析】太阳光照射TiO 电极上,敏化后的TiO 失去电子为原电池的负极,Pt电极为正极;
2 2
【详解】A.该装置是光伏电池,太阳光照下敏化后的 产生电子 和空穴 ,驱动电流产生和
离子移动,所以电池工作时,涉及光能转化为电能,A正确;
B.太阳光照下,敏化后的 产生电子 和空穴 ,即敏化 电极失电子为负极,B正确;
C. 电极为正极,发生得电子还原反应, 电极电极反应为: ,C错误;
第7页/共25页
学科网(北京)股份有限公司D.由图可知,光敏化剂结构中,中心离子 与6个N原子成键,配位数是6,D正确;
答案选C。
11. 根据下列实验操作和现象所得结论错误的是
选项 实验操作和现象 结论
用激光笔照射某有色玻璃,看到一条光亮的
A 该有色玻璃是胶体
“通路”
用铂丝蘸取溶液在酒精灯外焰上灼烧,观察
B 溶液中有钠盐
到黄色
用惰性电极电解 溶液,将湿润的淀粉
C 阳极有 生成
试纸靠近阳极,试纸变蓝
向 溶液中滴加 溶液,一段时间
D 被氧化为
后溶液变红
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.胶体具有丁达尔效应,用激光笔照射某有色玻璃,看到一条光亮的“通路”, 有色玻璃属于固
溶胶,是胶体,A正确;
B.用铂丝蘸取溶液在酒精灯外焰上灼烧,观察到黄色,该溶液中含有Na元素,不一定是钠盐,B错误;
C.惰性电极电解 溶液,阳极上发生氧化反应,2Cl—-2e-=Cl↑,Cl 能使湿润的淀粉碘化钾试纸变蓝
2 2
色,C正确;
D.Fe3+遇到KSCN溶液变红色,向 溶液中滴加 溶液,一段时间后溶液变红,说明 被氧
化为 ,D正确;
答案选B。
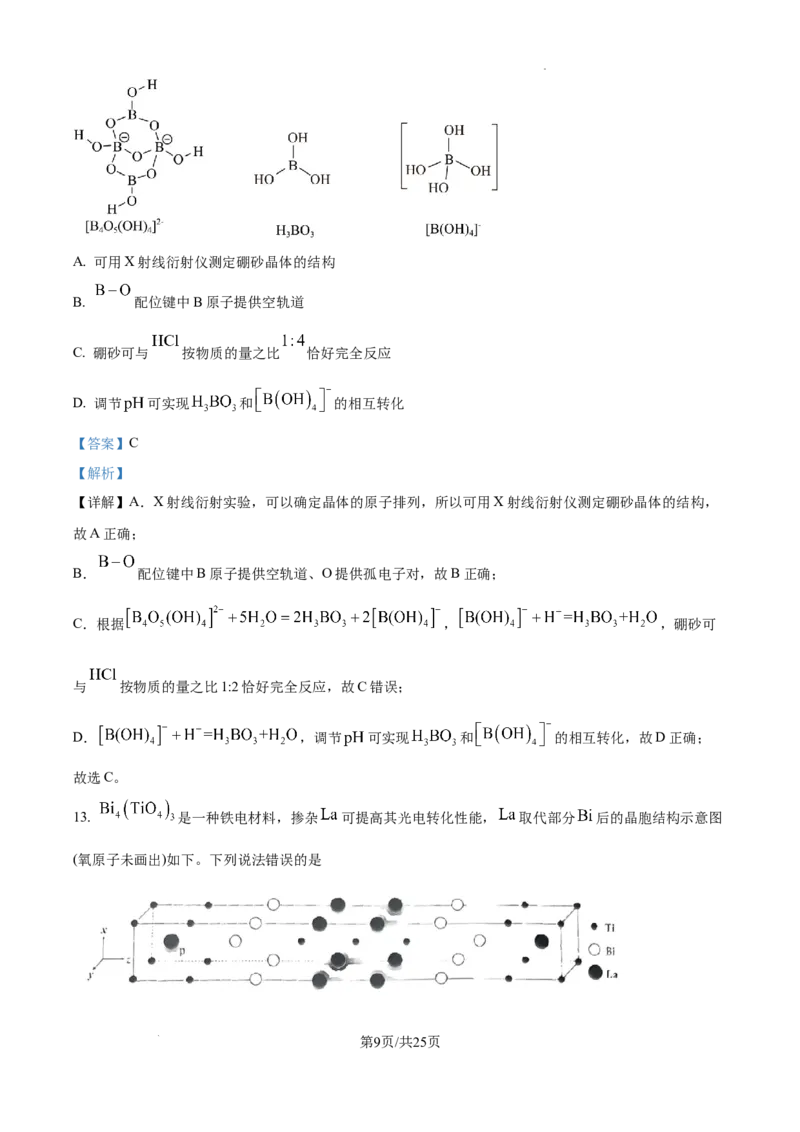
12. 硼砂的化学式可表示为 ,其水解反应的离子方程式为:
,三种含硼微粒结构示意图如下。下列说法错误的是
第8页/共25页
学科网(北京)股份有限公司A. 可用X射线衍射仪测定硼砂晶体的结构
B. 配位键中B原子提供空轨道
C. 硼砂可与 按物质的量之比 恰好完全反应
D. 调节 可实现 和 的相互转化
【答案】C
【解析】
【详解】A.X射线衍射实验,可以确定晶体的原子排列,所以可用X射线衍射仪测定硼砂晶体的结构,
故A正确;
B. 配位键中B原子提供空轨道、O提供孤电子对,故B正确;
C.根据 , ,硼砂可
与 按物质的量之比1:2恰好完全反应,故C错误;
D. ,调节 可实现 和 的相互转化,故D正确;
故选C。
13. 是一种铁电材料,掺杂 可提高其光电转化性能, 取代部分 后的晶胞结构示意图
(氧原子未画出)如下。下列说法错误的是
第9页/共25页
学科网(北京)股份有限公司A. 填充在 形成的六面体空隙中
B. 该晶体的化学式为
C. 该晶胞在 平面的投影为
D. 若p点 平移至晶胞体心,则 位于晶胞顶点
【答案】D
【解析】
【详解】A.由图可知,最左/右侧两端,La替代了Bi,Bi在正方体体心,是六面体结构,A正确;
B.由均摊法可知,Ti的数目为 ,Bi的数目为 ,La的数目为
,该晶体的化学式为 ,B正确;
C.该晶胞在 平面的投影,棱上为Ti、Bi、La,投在四个角,La、Bi、Ti,投在面心, ,C
正确;
D.若p点 平移至晶胞体心,则La位于晶胞顶点,D错误;
故选D;
14. 盐酸羟胺 是一种分析试剂。用 溶液滴定
和 的混合溶液以测定 的含量,待
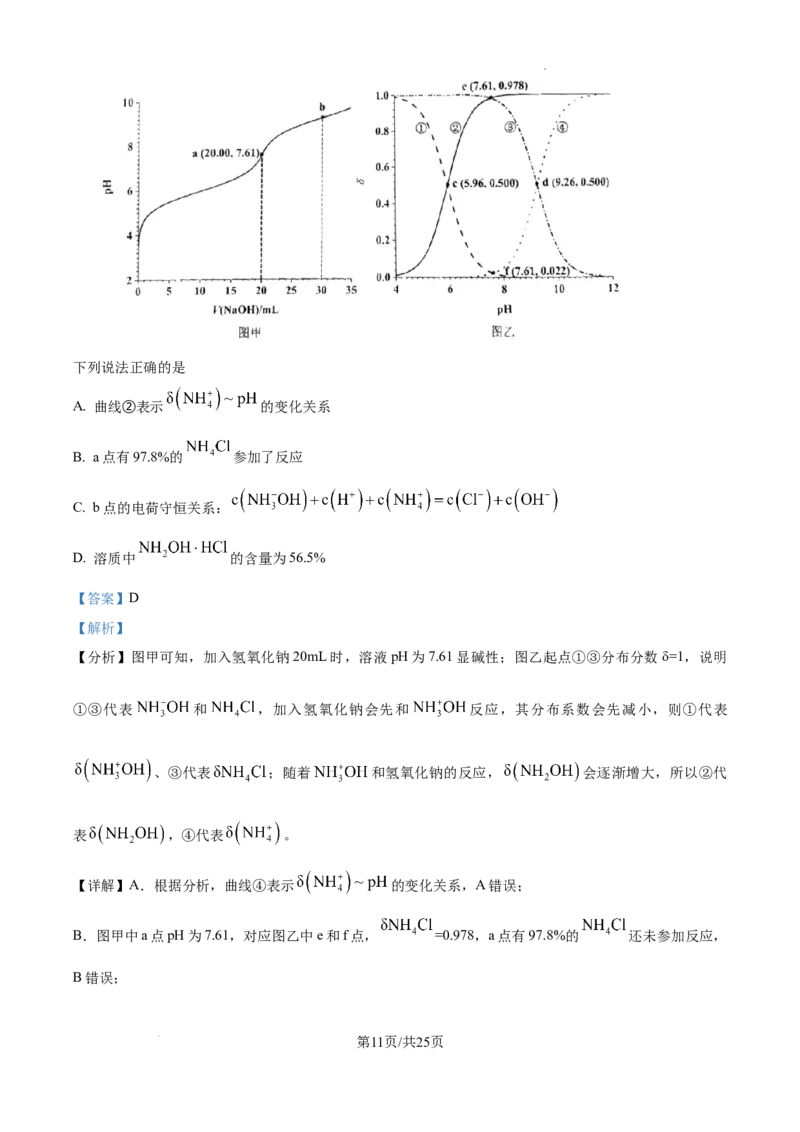
测液中溶质总质量为 ,滴定曲线如图甲所示,四种含氮物质分布分数δ与 关系如图乙所示[如:
]。
第10页/共25页
学科网(北京)股份有限公司下列说法正确的是
A. 曲线②表示 的变化关系
B. a点有97.8%的 参加了反应
C. b点的电荷守恒关系:
D. 溶质中 的含量为56.5%
【答案】D
【解析】
【分析】图甲可知,加入氢氧化钠20mL时,溶液pH为7.61显碱性;图乙起点①③分布分数δ=1,说明
①③代表 和 ,加入氢氧化钠会先和 反应,其分布系数会先减小,则①代表
、③代表 ;随着 和氢氧化钠的反应, 会逐渐增大,所以②代
表 ,④代表 。
【详解】A.根据分析,曲线④表示 的变化关系,A错误;
B.图甲中a点pH为7.61,对应图乙中e和f点, =0.978,a点有97.8%的 还未参加反应,
B错误;
第11页/共25页
学科网(北京)股份有限公司C.b点的pH在8~10,从图乙可看出此时是 与氢氧化钠反应,根据溶液中的阴阳离子列出电荷守
恒关系有 ,C错误;
D.加入氢氧化钠20mL时,即加入 ,设 ,根据反应列三段式分
析 ,则
, ,所以 的含
量为: ,D正确;
故选D。
二、非选择题:本题共4小题,共58分。
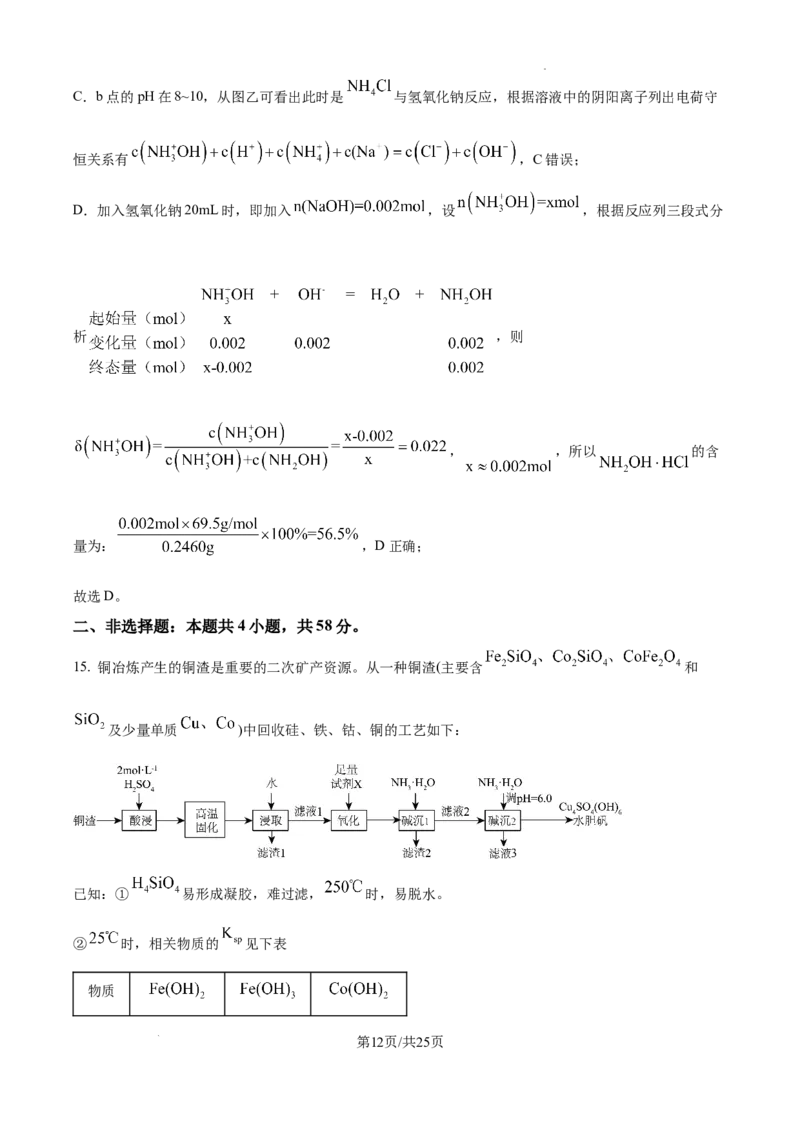
15. 铜冶炼产生的铜渣是重要的二次矿产资源。从一种铜渣(主要含 和
及少量单质 )中回收硅、铁、钴、铜的工艺如下:
已知:① 易形成凝胶,难过滤, 时,易脱水。
② 时,相关物质的 见下表
物质
第12页/共25页
学科网(北京)股份有限公司回答下列问题:
(1)“酸浸”前,采用_______方法可提高酸浸效率(填一条即可)。
(2)“酸浸”时,有空气参与反应, 溶解的化学方程式为_______。从环保角度考虑,不使用
酸浸的原因可能是_______(填一条即可)。
(3)“高温固化”的作用是_______。
(4)“氧化”中可选用的最佳试剂X为_______(填标号)。
A. B. C.
(5) “碱沉1”中, _______时, 沉淀完全 。
(6)“滤液3”中可回收的盐主要有 和_______。
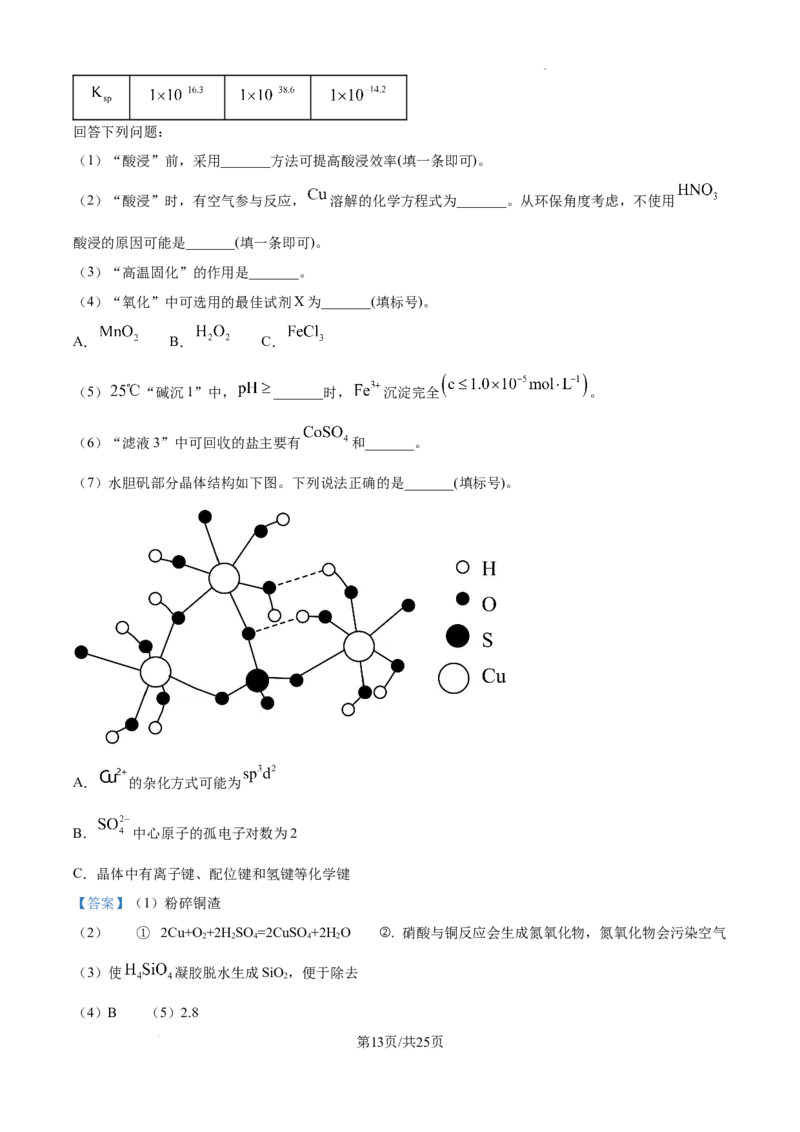
(7)水胆矾部分晶体结构如下图。下列说法正确的是_______(填标号)。
A. 的杂化方式可能为
B. 中心原子的孤电子对数为2
C.晶体中有离子键、配位键和氢键等化学键
【答案】(1)粉碎铜渣
.
(2) ① 2Cu+O +2H SO =2CuSO+2H O ②. 硝酸与铜反应会生成氮氧化物,氮氧化物会污染空气
2 2 4 4 2
(3)使 凝胶脱水生成SiO,便于除去
2
(4)B (5)2.8
第13页/共25页
学科网(北京)股份有限公司(6)(NH )SO
4 2 4
(7)A
【解析】
【分析】铜渣加入稀硫酸酸浸,再高温固化将HSiO 脱水生成SiO 便于除去,加水浸取,滤液中有Fe2+、
4 4 2
Cu2+、Co2+等离子,滤渣为SiO,,加入氧化剂氧化将Fe2+氧化为Fe3+离子氧化剂选择HO,不会引入杂
2 2 2
质,加入氨水调节pH值使Fe3+离子沉淀除去,滤渣2为Fe(OH) ,滤液中再加入氨水,使Cu2+转化为水胆
3
矾,滤液3中有CoSO 和(NH )SO 。
4 4 2 4
【小问1详解】
“酸浸”前,采用将铜渣粉碎,可以增大与酸的接触面积,从而提高酸浸效率;
【小问2详解】
“酸浸”时,有空气参与反应, 与O 和HSO 反应生成硫酸铜和水,反应的化学方程式为:
2 2 4
2Cu+O +2H SO =2CuSO+2H O;从环保角度考虑,不使用 酸浸的原因可能是硝酸与铜反应会生成
2 2 4 4 2
氮氧化物污染空气;
【小问3详解】
易形成凝胶,难过滤, 时,易脱水,高温固化的作用是将HSiO 脱水形成SiO,易于分离
4 4 2
除去;
【小问4详解】
“氧化”的目的是将Fe2+氧化为Fe3+,不能引入杂质,可选用的最佳试剂为HO,答案选B;
2 2
【小问5详解】
根据K [Fe(OH) ]=c(Fe3+)×c3(OH-)=1×10-38.6,c(Fe3+)=1×10-5mol·L-1,得出c(OH-)=10-11.2mol·L-1,
sp 3
c(H+)=10-2.8mol·L-1,pH=2.8, 2.8时, 沉淀完全;
【小问6详解】
经过分析,滤液3中有CoSO 和(NH )SO ;
4 4 2 4
【小问7详解】
由图可知,水胆矾中Cu2+的配位数为6,应该形成6个杂化轨道,杂化方式sp3d2为6个杂化轨道,A正确;
中心原子的孤电子对数为 ,B错误;
氢键不是化学键,C错误;
答案选A。
第14页/共25页
学科网(北京)股份有限公司16. 二苯乙醇酸是一种皮肤再生调节剂。由二苯乙二酮制备二苯乙醇酸的反应原理为:
实验步骤如下:
Ⅰ.在圆底烧瓶中加入 水、 二苯乙二酮和 95%乙醇溶液、水浴加热回流
(装置如图,加热及夹持装置省略)。
Ⅱ.将Ⅰ中所得混合物转入烧杯中,冰水浴冷却结晶,过滤、洗涤。将晶体溶于 蒸馏水中,调节
至少量胶状物(未反应的二苯乙二酮)浮于液面,加入活性炭,搅拌、过滤。
Ⅲ.向滤液中缓慢滴加5.0%盐酸,调节 (用刚果红试纸检测)。冰水浴冷却,有大量晶体析出。过
滤、冰水洗涤,得粗产品。
Ⅳ.将粗产品加热水溶解,冷却结晶,过滤、冰水洗涤、干燥,得 产品。
已知:①相关物质的信息见下表
物质 性质 熔点/℃ 溶解性
不溶于水,溶于
二苯乙二酮 210 淡黄色固体 95 —
乙醇、苯
易溶于热水或
二苯乙醇酸 228 无色晶体 150 3.06
苯,难溶于冰水
第15页/共25页
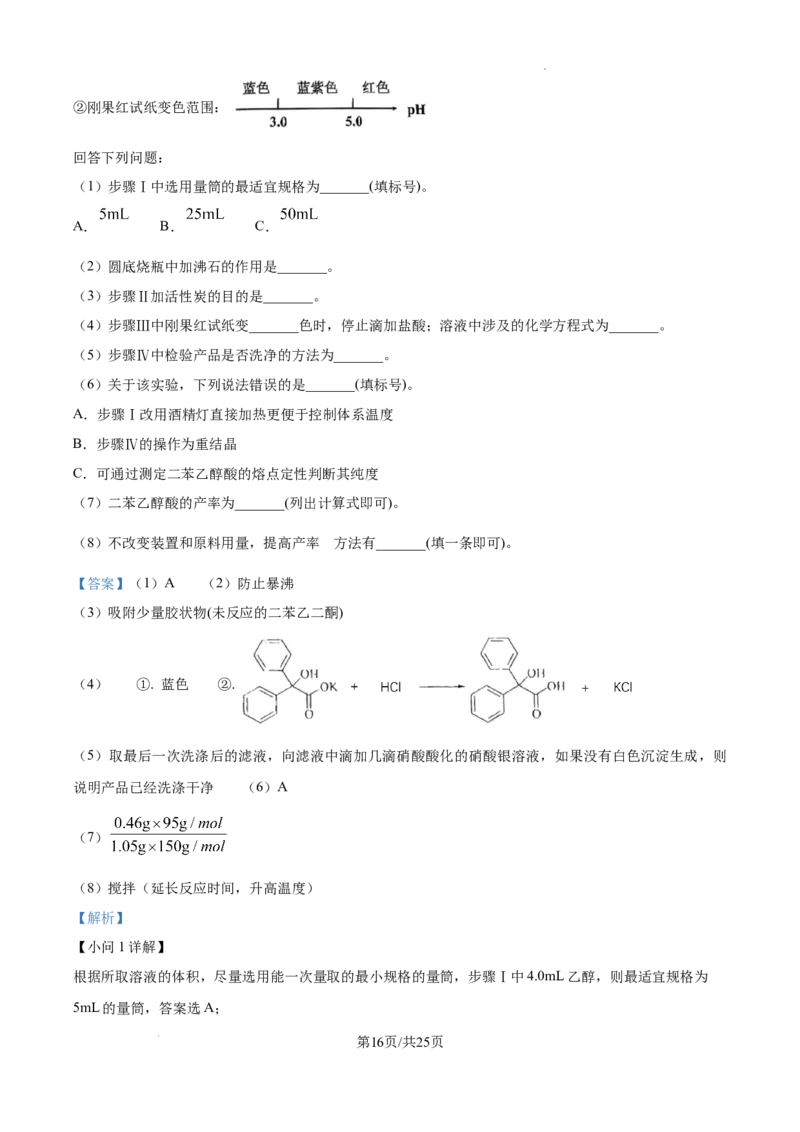
学科网(北京)股份有限公司②刚果红试纸变色范围:
回答下列问题:
(1)步骤Ⅰ中选用量筒的最适宜规格为_______(填标号)。
A. B. C.
(2)圆底烧瓶中加沸石的作用是_______。
(3)步骤Ⅱ加活性炭的目的是_______。
(4)步骤Ⅲ中刚果红试纸变_______色时,停止滴加盐酸;溶液中涉及的化学方程式为_______。
(5)步骤Ⅳ中检验产品是否洗净的方法为_______。
(6)关于该实验,下列说法错误的是_______(填标号)。
A.步骤Ⅰ改用酒精灯直接加热更便于控制体系温度
B.步骤Ⅳ的操作为重结晶
C.可通过测定二苯乙醇酸的熔点定性判断其纯度
(7)二苯乙醇酸的产率为_______(列出计算式即可)。
的
(8)不改变装置和原料用量,提高产率 方法有_______(填一条即可)。
【答案】(1)A (2)防止暴沸
(3)吸附少量胶状物(未反应的二苯乙二酮)
(4) ①. 蓝色 ②.
(5)取最后一次洗涤后的滤液,向滤液中滴加几滴硝酸酸化的硝酸银溶液,如果没有白色沉淀生成,则
说明产品已经洗涤干净 (6)A
(7)
(8)搅拌(延长反应时间,升高温度)
【解析】
【小问1详解】
根据所取溶液的体积,尽量选用能一次量取的最小规格的量筒,步骤Ⅰ中4.0mL乙醇,则最适宜规格为
5mL的量筒,答案选A;
第16页/共25页
学科网(北京)股份有限公司【
小问2详解】
圆底烧瓶中加沸石的作用是防止加热时液体暴沸;
【小问3详解】
步骤Ⅱ中调节 后产生少量胶状物(未反应的二苯乙二酮)浮于液面,加入活性炭,搅拌可吸附少量的胶
状物(未反应的二苯乙二酮);
【小问4详解】
由刚果红试纸变色范围可知,当 时刚果红试纸会变成蓝色,则当刚果红试纸变成蓝色时,停止滴
加盐酸;滴加盐酸的作用是酸化 ,化学方程式为
;
【小问5详解】
粗产品中可能含有KCl,则检验方法为:取最后一次洗涤后的滤液,向滤液中滴加几滴硝酸酸化的硝酸银
溶液,如果没有白色沉淀生成,则说明产品已经洗涤干净;
【小问6详解】
与酒精灯相比,水浴加热的温度控制相对容易且稳定,加热均匀,更便于控制温度,A错误;步骤Ⅳ将粗
产品加热水溶解,冷却结晶,过滤、冰水洗涤、干燥,这种操作为重结晶,B正确;纯物质的熔点是固定
的,如果化合物中含有杂质,其熔点通常会发生变化,若二苯乙醇酸的熔点为105℃左右,则二苯乙醇酸
较纯,C正确;答案选A;
【小问7详解】
, ,则二
第17页/共25页
学科网(北京)股份有限公司苯乙醇酸 产率 ;
的
【小问8详解】
适当的搅拌速度可以确保反应物充分混合,提高反应效率,提高产率;延长反应时间可以使反应更充分或
适当的升高反应温度;
17. 氮化钒 广泛用于钢铁产业、储能、工业催化等领域。工业上可采用碳热还原氮化法制备
时热化学方程式及平衡常数如下:
Ⅰ.
回答下列问题:
(1)钒元素在元素周期表中属于_______区。
(2)反应Ⅰ分两步进行:
Ⅱ.
Ⅲ.
①反应Ⅰ的 _______ , _______(用 和 表示)。
②升温有利于提高 产率,从平衡移动角度解释_______。
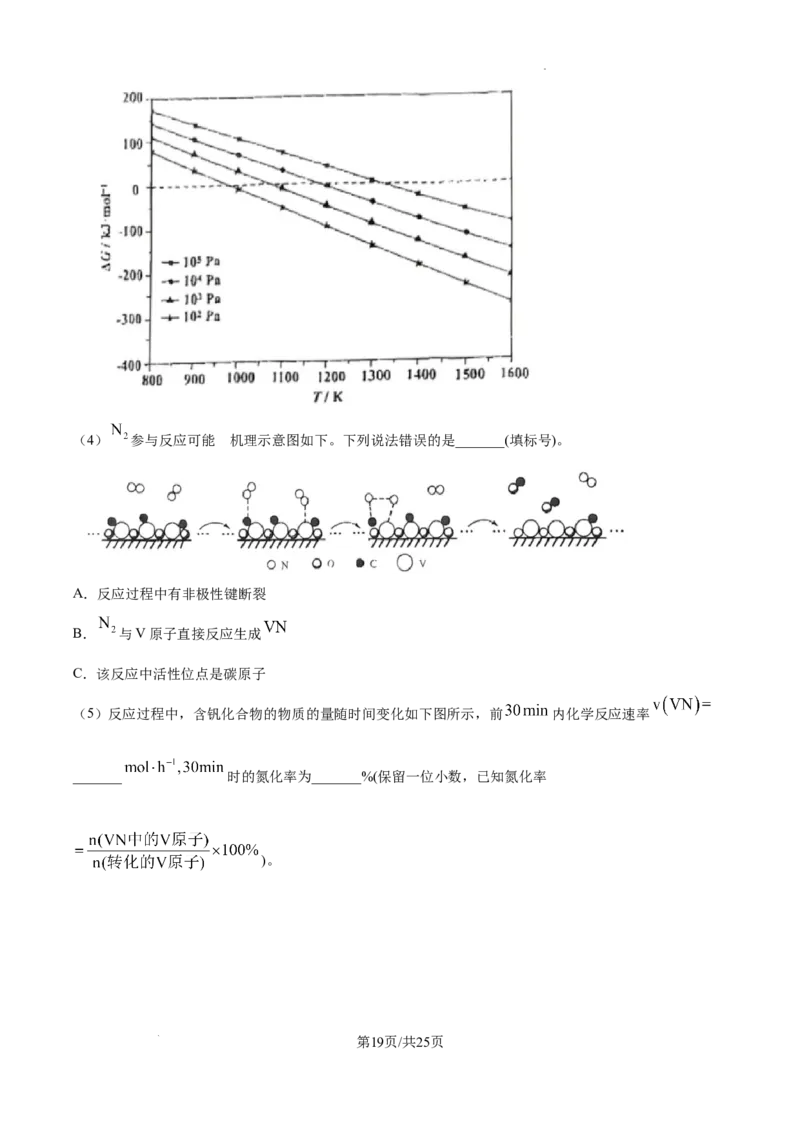
(3)通过热力学计算,不同压强下反应Ⅰ的 随T变化如图所示,_______(填“高温低压”或“低温高
压”)有利于该反应自发进行(已知 时,反应可自发进行)。
第18页/共25页
学科网(北京)股份有限公司的
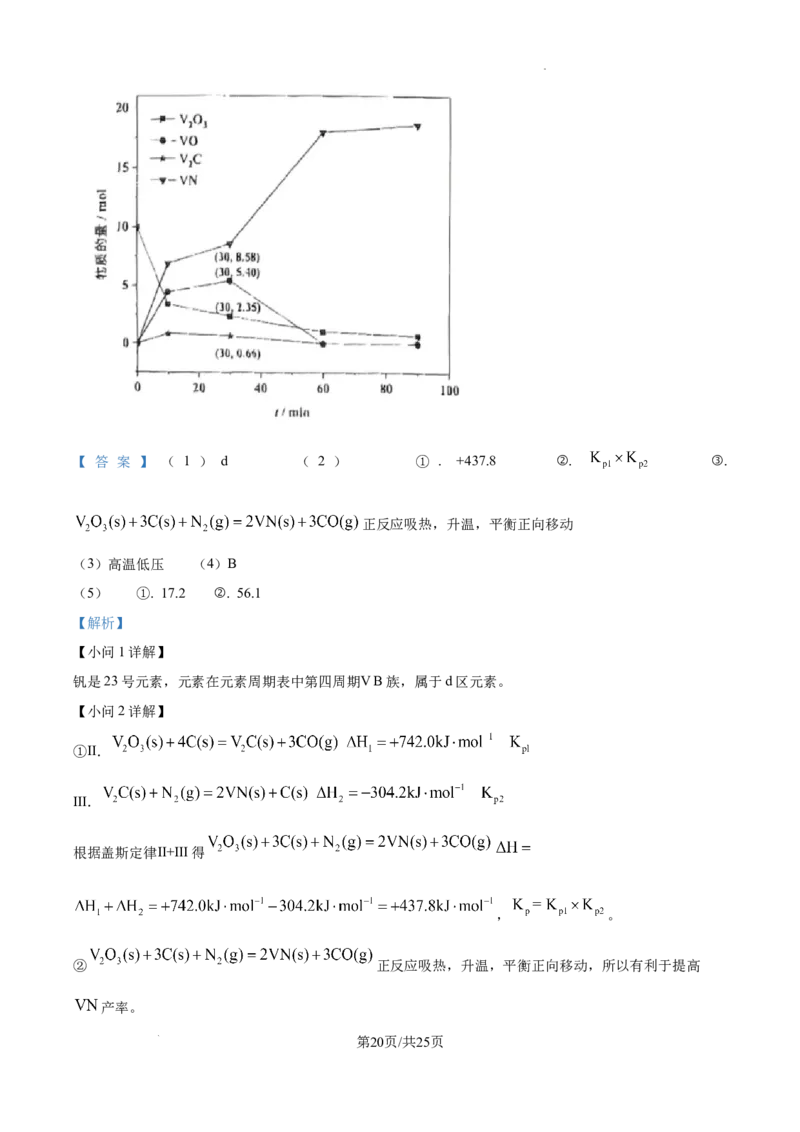
(4) 参与反应可能 机理示意图如下。下列说法错误的是_______(填标号)。
A.反应过程中有非极性键断裂
B. 与V原子直接反应生成
C.该反应中活性位点是碳原子
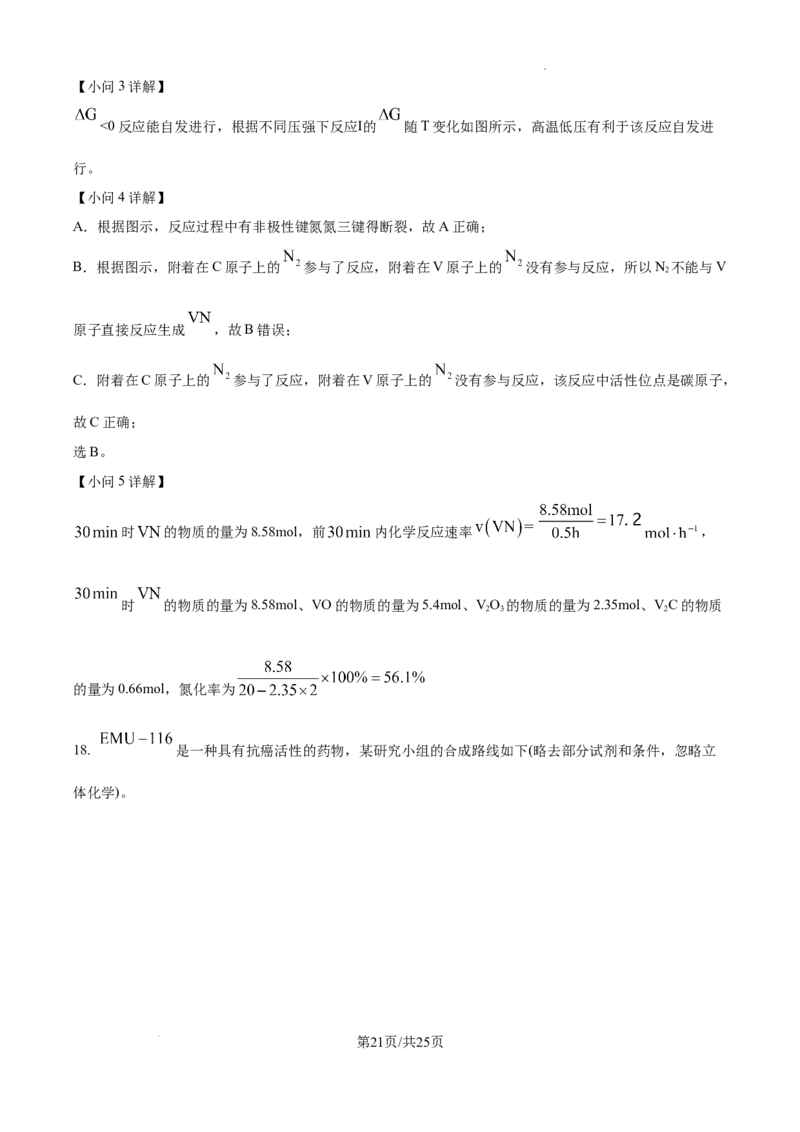
(5)反应过程中,含钒化合物的物质的量随时间变化如下图所示,前 内化学反应速率
_______ 时的氮化率为_______%(保留一位小数,已知氮化率
)。
第19页/共25页
学科网(北京)股份有限公司【 答 案 】 ( 1 ) d ( 2 ) ① . +437.8 ②. ③.
正反应吸热,升温,平衡正向移动
(3)高温低压 (4)B
(5) ①. 17.2 ②. 56.1
【解析】
【小问1详解】
钒是23号元素,元素在元素周期表中第四周期ⅤB族,属于d区元素。
【小问2详解】
①Ⅱ.
Ⅲ.
根据盖斯定律Ⅱ+Ⅲ得
, 。
② 正反应吸热,升温,平衡正向移动,所以有利于提高
产率。
第20页/共25页
学科网(北京)股份有限公司【小问3详解】
<0反应能自发进行,根据不同压强下反应Ⅰ的 随T变化如图所示,高温低压有利于该反应自发进
行。
【小问4详解】
A.根据图示,反应过程中有非极性键氮氮三键得断裂,故A正确;
B.根据图示,附着在C原子上的 参与了反应,附着在V原子上的 没有参与反应,所以N 不能与V
2
原子直接反应生成 ,故B错误;
C.附着在C原子上的 参与了反应,附着在V原子上的 没有参与反应,该反应中活性位点是碳原子,
故C正确;
选B。
【小问5详解】
时 的物质的量为8.58mol,前 内化学反应速率 ,
时 的物质的量为8.58mol、VO的物质的量为5.4mol、VO 的物质的量为2.35mol、VC的物质
2 3 2
的量为0.66mol,氮化率为
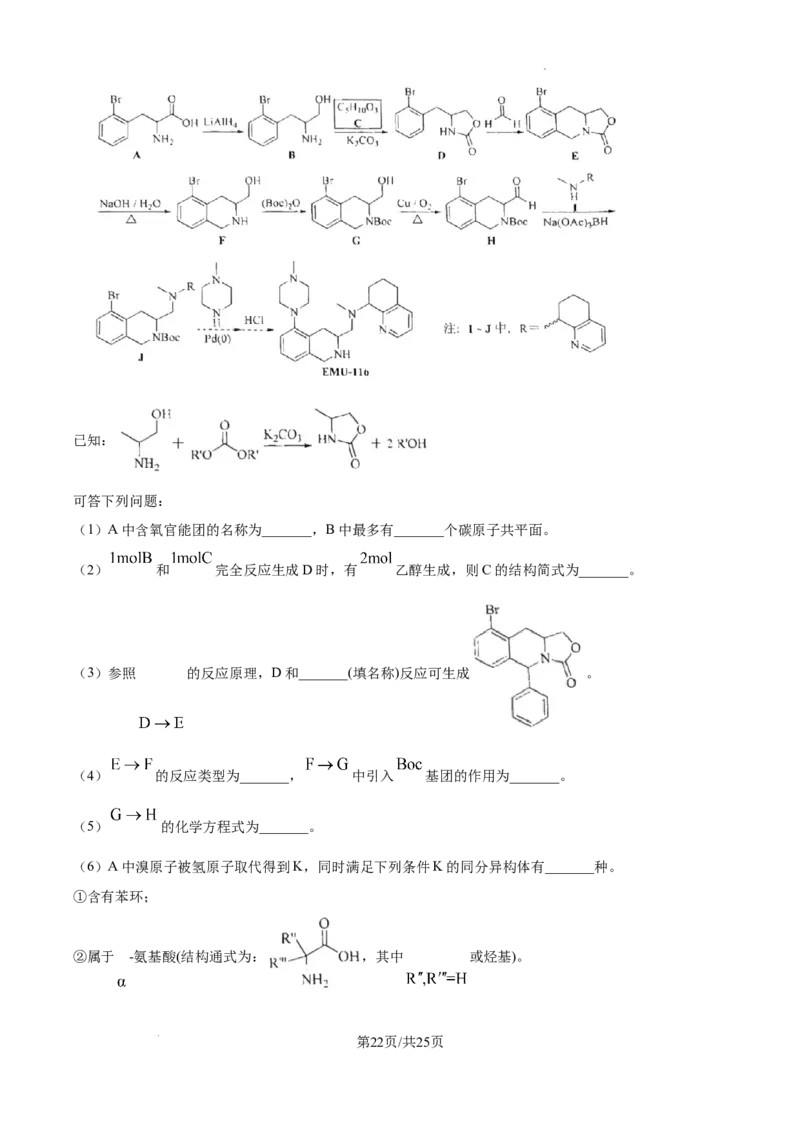
18. 是一种具有抗癌活性的药物,某研究小组的合成路线如下(略去部分试剂和条件,忽略立
体化学)。
第21页/共25页
学科网(北京)股份有限公司已知:
可答下列问题:
(1)A中含氧官能团的名称为_______,B中最多有_______个碳原子共平面。
(2) 和 完全反应生成D时,有 乙醇生成,则C的结构简式为_______。
(3)参照 的反应原理,D和_______(填名称)反应可生成 。
(4) 的反应类型为_______, 中引入 基团的作用为_______。
(5) 的化学方程式为_______。
(6)A中溴原子被氢原子取代得到K,同时满足下列条件K的同分异构体有_______种。
①含有苯环;
②属于 -氨基酸(结构通式为: ,其中 或烃基)。
第22页/共25页
学科网(北京)股份有限公司(7)用“*”标出 中的手性碳原子_______。
【答案】(1) ①. 羧基 ②. 9
(2) (3)苯甲醛
(4) ①. 水解反应(取代反应) ②. 保护氨基
(5) (6)5
(7)
【解析】
【分析】A到B发生还原反应,羧基转化为-OH,B到C形成环状结构,根据已知信息和 和
完全反应生成D时,有 乙醇生成,则C的结构简式为: ,D与甲醛反应生成E发
生先加成后脱水形成环状结构,E到F发生在碱性条件下水解,酯基和酰胺基均发生水解,F到G保护-
NH-防止被氧化,G到H发生醇羟基氧化生成醛基,H到J发生加成反应,最后J到产物发生取代反应,同
时把-NH-还原出来。
【小问1详解】
A中含氧官能团的名称为羧基;苯环上碳原子共面,C-C单键可以旋转,B最多有9个碳原子共面;
【小问2详解】
由分析可知, 完全反应生成D时,有 乙醇生成,则C的结构简式为: ;
【小问3详解】
第23页/共25页
学科网(北京)股份有限公司D到E发生先加成后脱水成环,参照 的反应原理,D和苯甲醛反应可生成 ;
【小问4详解】
E到F发生酯基和酰胺基水解反应,也是取代反应;F到G引入 基团的作用为保护-NH-,防止被氧化;
【小问5详解】
G到H发生醇羟基氧化为醛基的反应,反应的化学方程式为:
;
【小问6详解】
A的结构简式为: ,A中溴原子被氢原子取代得到K,K的同分异构体中含有
苯环,属于α-氨基酸的有 、 、 (邻间
对三种),共5种结构;
【小问7详解】
一个碳原子周围连接四个不同原子或原子团称为手性碳原子,EMU-116结构中,有2个手性碳原子,手性
第24页/共25页
学科网(北京)股份有限公司碳原子位置如图: 。
第25页/共25页
学科网(北京)股份有限公司