文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(浙江专用)
黄金卷 06
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35.5 K
39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Br 80 Ag 108 Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.下列物质属于电解质,且在熔融状态下能导电的是( )
A.水银 B.生石灰 C.硝酸 D.二氧化硅
2.下列化学用语表示正确的是( )
A.中子数为16的磷原子:16P
15
B.NH 分子的VSEPR模型:
3
C.CaCl 的电子式:
2
D.顺-2-丁烯的结构简式:
3.下列关于铝及其化合物说法不正确的是( )
A.铝元素位于周期表的p区
B.明矾溶液呈酸性
C.常温下,可用铝制容器盛装浓硝酸
D.工业上常用电解熔融AlCl 制备金属铝
3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx0024.下列说法不正确的是( )
A.钠是一种强还原剂,可以将钛等金属从其熔融的氯化物中置换出来
B.可以用黄铁矿制备硫酸,而不能用黄铜矿制备硫酸
C.二氧化硅是共价晶体,可直接用于制造光导纤维而不能直接做芯片
D.镁燃烧发出耀眼的白光,常用于制造信号弹和焰火,镁还能在CO 或SO 或NO 中剧烈燃烧
2 2 2
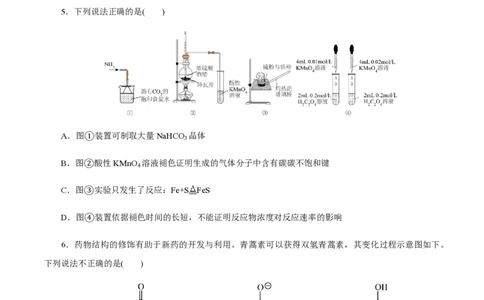
5.下列说法正确的是( )
A.图①装置可制取大量NaHCO 晶体
3
B.图②酸性KMnO 溶液褪色证明生成的气体分子中含有碳碳不饱和键
4
C.图③实验只发生了反应:Fe+S FeS
D.图④装置依据褪色时间的长短,不能证明反应物浓度对反应速率的影响
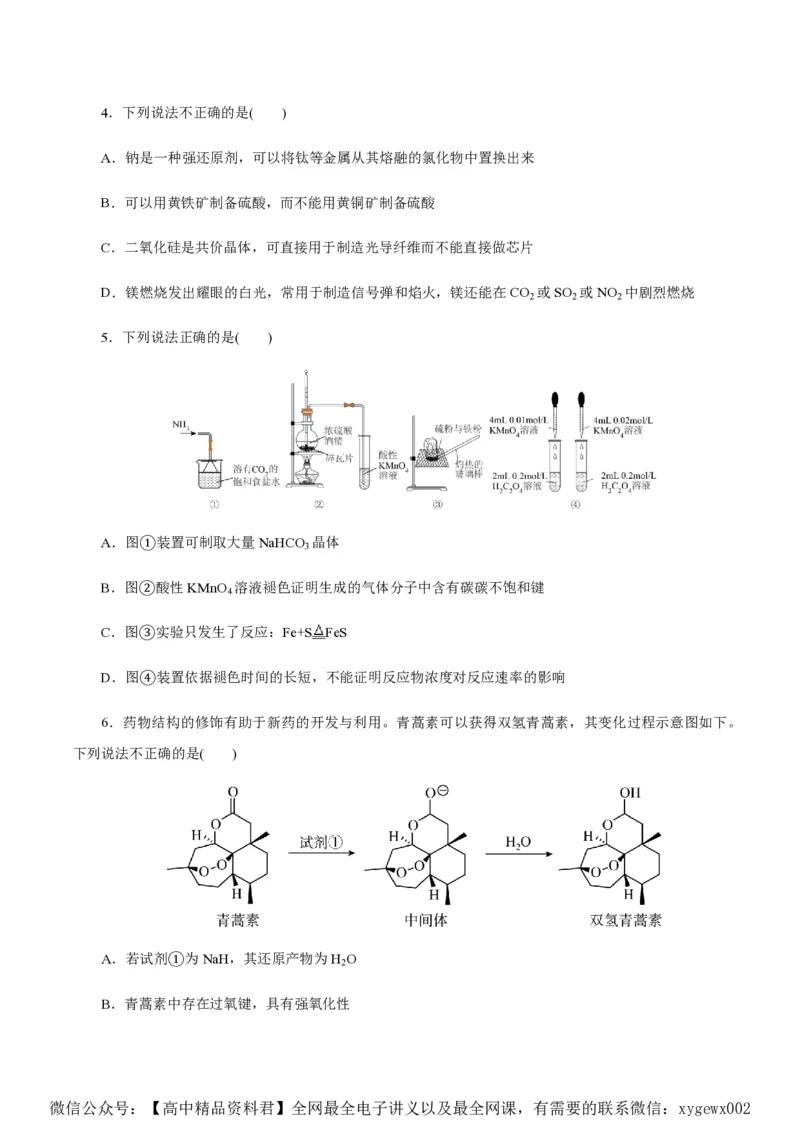
6.药物结构的修饰有助于新药的开发与利用。青蒿素可以获得双氢青蒿素,其变化过程示意图如下。
下列说法不正确的是( )
A.若试剂①为NaH,其还原产物为H O
2
B.青蒿素中存在过氧键,具有强氧化性
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C.该过程若有1mol青蒿素完全转化,则转移2mol电子
D.羟基的引入使得双氢青蒿素分子拥有更多修饰与改造的可能
7.膦(PH )可用白磷(P )与过量碱液反应制备,反应方程式:P +3KOH+3H O=PH ↑+3KH PO ,下列说
3 4 4 2 3 2 2
法不正确的是( )
A.1mol P 含σ键数目为6 N
4 A
B.KH PO 为酸式盐
2 2
C.氧化剂与还原剂的物质的量之比为1∶3
D.生成1molPH 转移的电子数为3 N
3 A
8.下列说法正确的是( )
A.油脂在酸性溶液中的水解反应可称为皂化反应
B.苯中含少量苯酚,可加入浓溴水,充分反应后过滤除去
C.氨基酸既能与HCl反应,也能与NaOH反应,产物均为盐和水
D.乙醛和氢气混合气体通过热的镍催化剂,乙醛发生还原反应
9.下列反应的方程式不正确的是( )
A.将碳酸氢钙溶液与过量的澄清石灰水混合:HCO - +Ca2++OH-=CaCO ↓+H O
3 3 2
B.将稀硫酸加入硫代硫酸钠溶液:S O 2-+SO 2-+4H+=2SO ↑+S↓+2H O
2 3 4 2 2
C.CuSO 溶液与闪锌矿(ZnS)反应生成铜蓝(CuS):ZnS(s)+Cu2+(aq) CuS(s)+ Zn2+(aq)
4
D.向银氨溶液中滴加乙醛,水浴加热,析出光亮银镜:CH CHO+2Ag(NH)OH
3 32
CHCOONH+2Ag↓+3NH+HO
3 4 3 2
10.肉桂醛可利用苯甲醛、乙醛通过如下途径合成。下列说法不正确的是( )
+CH CHONaOH水溶液 +H O
3 Δ 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.上述反应依次经历了加成、消去的过程
B.肉桂醛与足量溴水反应生成
C.产物中可能存在副产物CH₃CH=CHCHO
D.肉桂醛分子的碳原子具有相同的杂化方式
11.Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是同周期元素,位于s区,Y的s能
级电子数等于p能级的电子数,五种元素中Q的未成对电子数最多。W、Z最外层电子数相同,Z的核电荷
数是W的2倍。则下列说法正确的是( )
A.离子半径:XZW
B.化合物ZW 和ZW 中Z杂化不同
2 3
C.简单氢化物的稳定性:QW
D.Z和X可形成原子个数比为1:1和1:2的化合物
12.高铁酸钾(K FeO )具有杀菌消毒及净水作用,某实验小组在碱性条件下制备K FeO 流程如图所示:
2 4 2 4
下列说法不正确的是( )
A.1molK FeO 消毒能力相当于1.5mol HClO
2 4
B.氧化反应:3NaClO+2Fe(NO ) +10 NaOH=2Na FeO +3NaCl+6 NaNO +5H O
3 3 2 4 3 2
C.同温度时高铁酸钠溶解度大于高铁酸钾
D.提纯时,应用到的玻璃仪器有蒸发皿、玻璃棒、烧杯、酒精灯
13.一种检测空气中甲醛含量的电化学传感器的工作原理如图所示。下列说法正确的是( )
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.工作时,电能转化为化学能
B.工作时,工作电极电势低,发生还原反应
C.工作时,电子由工作电极通过导线转移到对电极,再经过电解质溶液回到工作电极
D.工作时,对电极区的电极反应为O +4H++4e-=2H O
2 2
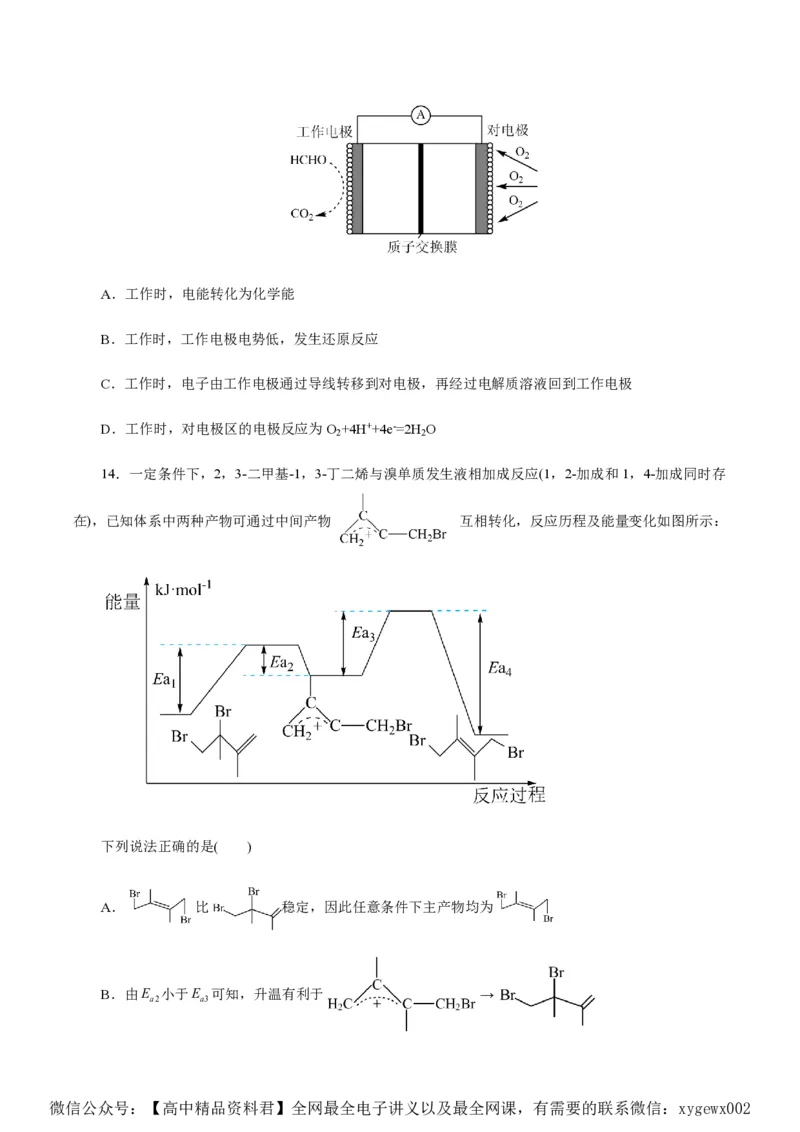
14.一定条件下,2,3-二甲基-1,3-丁二烯与溴单质发生液相加成反应(1,2-加成和1,4-加成同时存
在),已知体系中两种产物可通过中间产物 互相转化,反应历程及能量变化如图所示:
下列说法正确的是( )
A. 比 稳定,因此任意条件下主产物均为
B.由E 小于E 可知,升温有利于 →
a2 a3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002C. H E E E E kJ/mol
a1 a3 a2 a4
D.由反应历程及能量变化图可知,该加成反应为放热反应
15.H S是常见的二元弱酸(电离常数K (H S)=1.1×10-7,K (H S)=1.3×10-13)。氢氧化铁[K = 2.8×10-
2 a1 2 a2 2 sp
39]、氢氧化锌[K = 3.0×10-17]均为难溶多元弱碱,硫化锌[K = 1.6×10-24]为难溶盐。所有数据均为25℃的
sp sp
值。下列有关说法不正确的是( )
A.因为H S的K >>K ,所以c(S2-)≈K =1.3×10-13mol/L
2 a1 a2 a2
B.Fe(OH) 饱和溶液中的c(Fe3+)≈1×10-10mol/L
3
C.分别向等体积等浓度的(CH COO) Zn、ZnSO 溶液中通入等物质的量的H S沉淀ZnS后,前者c(Zn2+)
3 2 4 2
更小
D.pH=13的Na S溶液与相同物质的量的ZnSO 反应,只沉淀ZnS
2 4
16.下列方案设计、现象和结论都正确的是( )
实验目的 实验设计 现象和结论
检验某固体化合物样品中是否存 取少量固体样品完全溶于盐酸,在滴 若出现血红色,则该固体化
A
在Fe3 加KSCN溶液 合物中存在Fe3
若产生白色沉淀,则说明酸
B 探究H SO 和HClO的酸性强弱 将SO 气体通入Ca(ClO) 溶液中
2 3 2 2
性:H SO >HClO
2 3
探究常温下同浓度的CH COOH 常温下,分别测0.1mol/L的 若两者的pH之和等于14,
3
C
和NH ·H O的电离能力 CH COONa和NH Cl溶液的pH 则两者的电离程度相同
3 2 3 4
若溶液变蓝,则说明气体为
D 验证某红棕色气体是否为NO 将气体通入淀粉碘化钾溶液
2
NO
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002第Ⅱ卷
二、非选择题:共5题,共52分。
17.(10分)铂及其配合物在生活中有重要应用。
(1)顺铂有抗癌作用。机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH ) (OH)Cl
3 2
与DNA结合,破坏DNA的结构,阻止癌细胞增殖。如:
①基态Cu原子价层电子排布式为_______。
②鸟嘌呤与Pt(NH ) (OH)Cl反应的产物中包含的化学键_______。
3 2
A氢键 B.离子键 C.共价键 D.配位键
③在Pt(NH ) Cl ,配体与铂(Ⅱ)的结合能力:Cl -_______(NH 填“>”或“<”)。
3 2 2 3
(2)顺铂和反铂互为同分异构体,两者的结构和性质如下。
顺铂 反铂
空间结构
25℃时溶解度/g 0.2577 0.0366
①推测Pt(NH ) Cl 的结构是_______(填“平面四边形”或“四面体形”)。
3 2 2
②顺铂在水中的溶解度大于反铂的原因是_______。
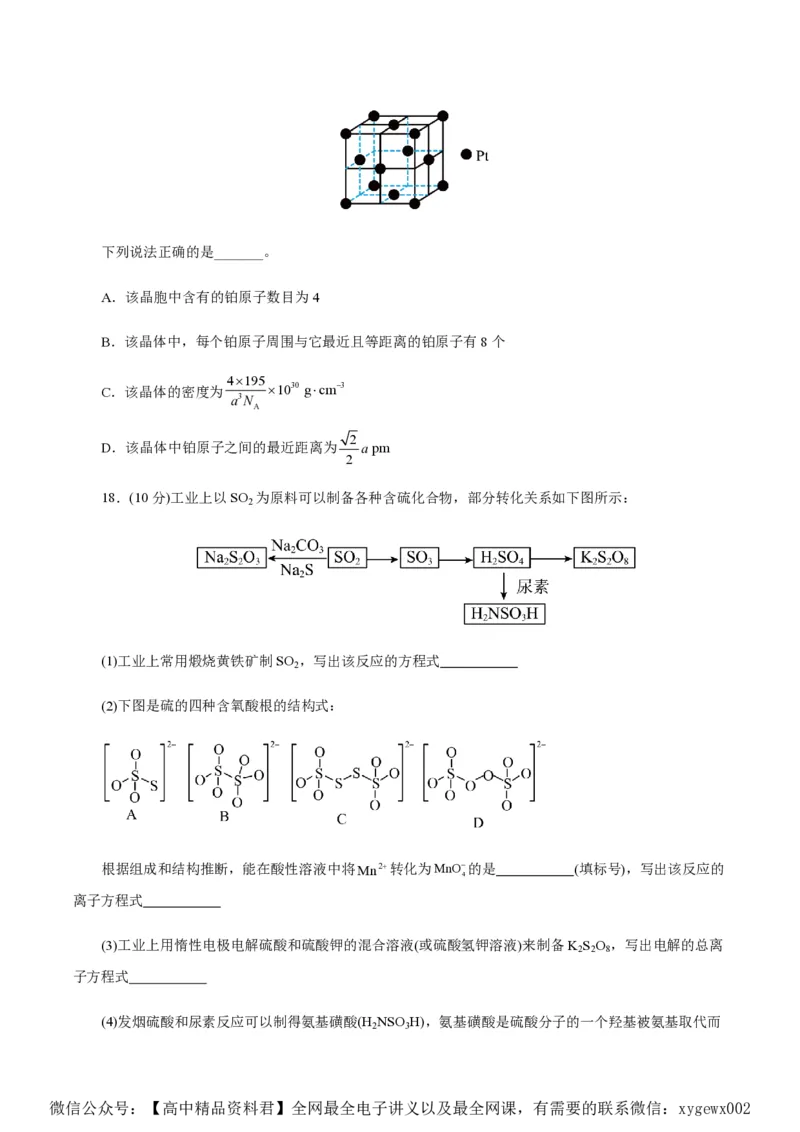
(3)铂晶胞为立方体,边长为a pm,结构如图:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002下列说法正确的是_______。
A.该晶胞中含有的铂原子数目为4
B.该晶体中,每个铂原子周围与它最近且等距离的铂原子有8个
4195
C.该晶体的密度为 1030 gcm3
a3N
A
2
D.该晶体中铂原子之间的最近距离为 apm
2
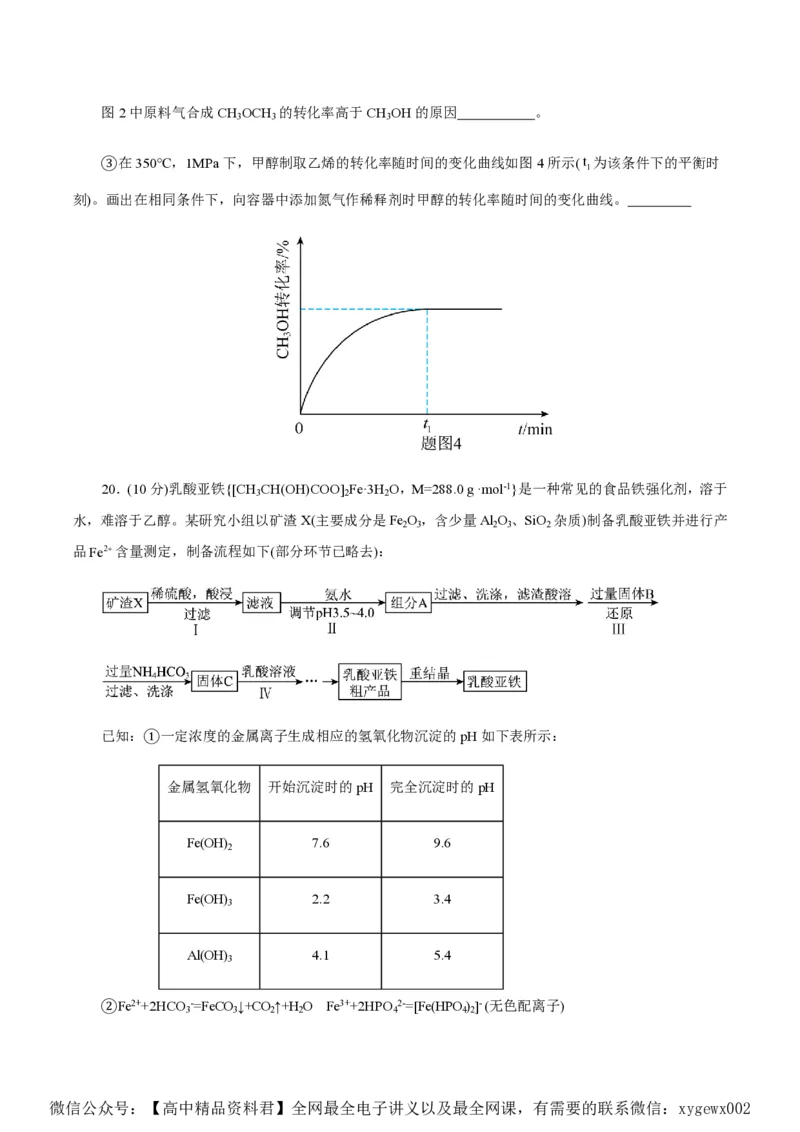
18.(10分)工业上以SO 为原料可以制备各种含硫化合物,部分转化关系如下图所示:
2
(1)工业上常用煅烧黄铁矿制SO ,写出该反应的方程式
2
(2)下图是硫的四种含氧酸根的结构式:
根据组成和结构推断,能在酸性溶液中将Mn2转化为MnO的是 (填标号),写出该反应的
4
离子方程式
(3)工业上用惰性电极电解硫酸和硫酸钾的混合溶液(或硫酸氢钾溶液)来制备K S O ,写出电解的总离
2 2 8
子方程式
(4)发烟硫酸和尿素反应可以制得氨基磺酸(H NSO H),氨基磺酸是硫酸分子的一个羟基被氨基取代而
2 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002形成的无机固体酸,是一种常见的化工原料。下列说法不正确的是___________
A.氨基磺酸能与醇反应
B.氨基磺酸能与活泼金属反应产生氢气
C.氨基磺酸的实际存在形式可能为+H NSO -
3 3
D.氨基磺酸与硝酸只能发生非氧化还原反应
(5)设计实验检验氨基磺酸(H NSO H)中的N元素
2 3
(6)硫代硫酸钠有较强的配位能力,不溶于水的AgBr可以溶解在Na S O 溶液中,生成和银氨溶液类似
2 2 3
的物质,写出该反应的离子方程式 ,和Ag+成键的原子是
A.氧原子 B.端基硫原子 C.中心硫原子
19.(10分)以煤为原料,经由甲醇可制取甲醚,也可以制取烯烃并可以此取代传统的以石油为原料制
取烯烃的路线。
(1)已知:在25℃和101kPa条件下,甲醇的燃烧热为-726.5 kJ·mol-1,乙烯的燃烧热为-1411 kJ·mol-1,
E
Rlnk a C(E 为活化能,R、C为常数,k为平衡常数)。则:
T a
①CH OH(l)脱水生成C H 的热化学方程式是 ,该反应自发进行的条件是 (填“较
3 2 4
低”、“较高”或“任意”)温度。
②甲醇脱水生成乙烯的温度与平衡常数的实验数据图如图1所示,该反应的正反应的活化能为
kJmol1。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(2)以煤为原料气化产生的原料气可以用来合成CH OH和CH OCH ,合成气平衡转化率随氢碳比
3 3 3
nH
( 2 )的变化如图2所示:甲醇制取烃的过程中,会发生多种反应,可以生成CH 、C H 、C H 等,一
nCO 4 2 4 4 8
定条件下,测得各烃的质量分数、CH OH转化率随温度变化情况如图3所示。
3
①下列叙述不正确的是 。
A.合成CH OCH 的最佳氢碳比为1.0
3 3
B.甲醇制取烃的过程中,相同条件下,温度越高越有利于CH 的生成
4
C.甲醇制取乙烯的过程中,一般控制在350℃~400℃比较合适
D.甲醇制取烃的过程中,CH OH的平衡转化率随温度升高先增大后减少
3
②原料气合成CH OH、CH OCH 过程有如下反应发生:
3 3 3
反应Ⅰ CO(g)+ 2H (g) CH OH(g) ΔH=-91 kJ·mol-1
2 3
反应Ⅱ CO(g)+ H O(g) CO (g)+H (g) ΔH=-41 kJ·mol-1
2 2 2
反应Ⅲ 2 CH OH(g) CH OCH (g)+H O(g) ΔH=-24kJ·mol-1
3 3 3 2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002图2中原料气合成CH OCH 的转化率高于CH OH的原因 。
3 3 3
③在350℃,1MPa下,甲醇制取乙烯的转化率随时间的变化曲线如图4所示(t 为该条件下的平衡时
1
刻)。画出在相同条件下,向容器中添加氮气作稀释剂时甲醇的转化率随时间的变化曲线。
20.(10分)乳酸亚铁{[CH CH(OH)COO] Fe·3H O,M=288.0 g ·mol-1}是一种常见的食品铁强化剂,溶于
3 2 2
水,难溶于乙醇。某研究小组以矿渣X(主要成分是FeO,含少量AlO、SiO 杂质)制备乳酸亚铁并进行产
2 3 2 3 2
品Fe2含量测定,制备流程如下(部分环节已略去):
已知:①一定浓度的金属离子生成相应的氢氧化物沉淀的pH如下表所示:
金属氢氧化物 开始沉淀时的pH 完全沉淀时的pH
Fe(OH) 7.6 9.6
2
Fe(OH) 2.2 3.4
3
Al(OH) 4.1 5.4
3
②Fe2++2HCO -=FeCO↓+CO↑+HO Fe3++2HPO 2-=[Fe(HPO)]- (无色配离子)
3 3 2 2 4 42
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002请回答:
(1)步骤Ⅳ,转化时使用如图装置,仪器A的名称是___________。
(2)下列有关说法不正确的是___________。
A.步骤Ⅱ,加入氨水调节pH后,组分A中主要含铁成分为Fe2+、Fe(OH)
3
B.步骤Ⅲ,固体B为铁
C.固体C为FeCO 和Fe
3
D.重结晶后可选择乙醇洗涤晶体
E.为得到干燥的乳酸亚铁晶体,采用高温烘干的方式
(3)实验室常用已知浓度的重铬酸钾标准溶液滴定Fe2。
①从下列选项中选择合理的仪器和操作,补全如下步骤[“___________”上填写一件最关键仪器,
“( )”内填写一种操作,均用字母表示]___________
蒸馏水洗涤______→润洗→( )→装液→( )→( )→用_________(量取一定体积的Fe2)→加指
示剂,准备开始滴定。
仪器:a.烧杯;b.酸式滴定管;c.碱式滴定管;d.锥形瓶
操作:e.调整液面至“0”或“0”刻度以下,记录读数
f.橡皮管向上弯曲,挤压玻璃球,放液
g.打开活塞快速放液
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002h.控制活塞,将洗涤液从滴定管下部放出
i.将洗涤液从滴定管上口倒出
②滴定曲线如下图所示(曲线a未加磷酸,曲线b加磷酸)。滴定操作中向溶液中加入磷酸溶液的原因是:
溶液酸化抑制Fe2水解、___________(写出两个理由)。
(4)研究小组为了测定乳酸亚铁产品中的Fe2含量,称取5.600 g乳酸亚铁产品溶于蒸馏水,定容至250
mL,进行如下实验。
【实验一】铈量法测定Fe2+含量。
取25.00 mL试液,用0.1000 mol/L的Ce(SO ) 标准溶液滴定至终点。滴定反应为:Ce4++Fe2+=
4 2
Ce34++Fe3+,4次滴定消耗Ce(SO ) 溶液的体积如下:
4 2
实验次数 1 2 3 4
消耗Ce(SO ) 溶液的体积/mL 18.75 20.05 18.70 18.65
4 2
①则该产品中Fe2+含量为___________%(保留四位有效数字)。
【实验二】高锰酸钾法测定Fe2+含量。
取25.00 mL试液,加入适量硫酸,用0.0200 mol/L的高锰酸钾标准溶液滴定至终点。4次滴定测得的Fe2+
含量如下:
实验次数 1 2 3 4
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002Fe2含量(%) 19.61 20.17 21.26 19.46
②比较实验一、二测得的产品中Fe2+含量,认为铈量法适合于乳酸亚铁中Fe2+含量的测定,原因是
___________。
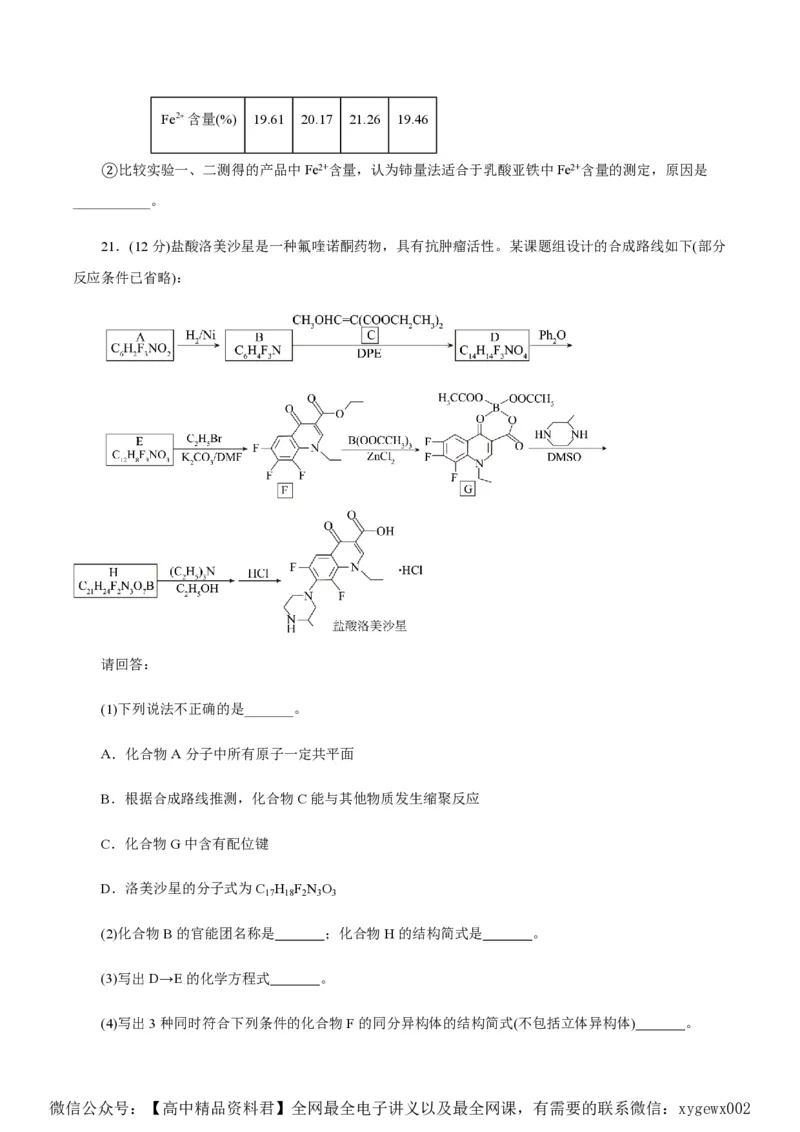
21.(12分)盐酸洛美沙星是一种氟喹诺酮药物,具有抗肿瘤活性。某课题组设计的合成路线如下(部分
反应条件已省略):
请回答:
(1)下列说法不正确的是_______。
A.化合物A分子中所有原子一定共平面
B.根据合成路线推测,化合物C能与其他物质发生缩聚反应
C.化合物G中含有配位键
D.洛美沙星的分子式为C H F N O
17 18 2 3 3
(2)化合物B的官能团名称是 ;化合物H的结构简式是 。
(3)写出D→E的化学方程式 。
(4)写出3种同时符合下列条件的化合物F的同分异构体的结构简式(不包括立体异构体) 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002①1HNMR谱表明:分子中共有3种不同化学环境的氢原子;
②IR谱检测表明:苯环上有多酚羟基且相邻,且分子不含-CN,含-N=O;
③分子中还有一个五元碳环。
(5)以苯胺( )和甲氧亚甲基丙二酸二甲酯[CH OCH=C(COOCH ) ]为原料,设计合成如下图所示化合
3 3 2
物的合成路线(用流程图表示,无机试剂、有机溶剂任选) 。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002