文档内容
阿伏加德罗常数的应用
N 应用常设陷阱
A
常设陷阱 应用举例(判断正误)
1.溶液体积未知 (1)在pH=13的NaOH溶液中,OH-的数目为0.1×6.02×1023(
溶液的体积未知,溶质的物质的量无法 )
计算,所以微粒数也无法计算 (2)0.1 mol·L-1 FeCl 溶液中所含Fe3+的数目小于0.1N ( )
3 A
2.标准状况下与非标准状况下的陷阱
(1)常温常压下,22.4 L氯气与足量的镁粉充分反应,转移的
气体若在非标准状况下,气体摩尔体积
电子数为2N ( )
A
不能用22.4 L·mol-1计算;标准状况下为
(2)标准状况下,22.4 L苯中含有6N 个碳原子( )
A
非气体的物质:SO 、CH OH、HF等
3 3
3.不能完全反应的陷阱 (1)密闭容器中,1 mol N 与3 mol H 充分反应,生成2 mol
2 2
可逆反应不能进行到底,如加热条件 NH ( )
3
下,一定量的浓盐酸(浓硫酸)与足量的 (2)50 mL 12 mol·L-1盐酸与足量MnO 共热,转移的电子数为
2
MnO (金属铜)不能反应完全 0.3N ( )
2 A
4.弱电解质的电离、盐类水解 (1)1 L 0.1 mol·L-1 CH
3
COOH溶液中所含H+的数目为0.1N
A
(
弱电解质仅部分电离;注意盐类水解引 )
起的粒子数目变化 (2)1 L 0.1 mol·L-1 NH
Cl溶液中,NH+
的数目为0.1N ( )
4 4 A
5.存在自由基连锁反应
1.0 mol CH 与Cl 在光照下反应生成的CH Cl分子数为N (
4 2 3 A
氯气与CH 反应同时生成CH Cl、
4 3
)
CH Cl 、CHCl 、CCl 四种氯代物
2 2 3 4
对点训练
1.求粒子数
(1)1 mol Na O (或CaC )中含有的阴离子数为2N ( )
2 2 2 A
(2)1 mol —OH中含有的电子数为10N ( )
A
(3)18 g H O、D O组成的物质中含有的质子数为10N ( )
2 2 A
(4)28 g 乙烯和环丁烷(C H )的混合气体中含有的碳原子数为2N ( )
4 8 A
(5)1 mol Na O 和Na S的混合物中含有的离子总数为3N ( )
2 2 2 A
特别提醒 ①因同位素而造成的摩尔质量不同的物质(如H O、D O组成的物质)需分别计算。
2 2
②对最简式相同的混合物,按最简式来计算(如乙烯、丙烯和环丁烷,它们的最简式都是CH )。
2
③最简式不同的物质要分别计算。2.求化学键数目或电子对数目
(1)1 mol金刚石(或晶体硅)中含有C—C(或Si—Si)的数目为4N ( )
A
(2)0.1 mol 肼(N H )含有的孤电子对数为0.2N ( )
2 4 A
(3)34 g呋喃( )中含有的极性键数目为3N ( )
A
(4)1 mol [Cu(H O) ]2+中含有的σ键的数目为12N ( )
2 4 A
特别提醒 ①苯环中不含碳碳双键。
②1 mol白磷(P )中含有6N P—P。
4 A
③1 mol金刚石(晶体硅)中含有2N C—C(Si—Si)。
A
④1 mol S 中含有8N S—S。
8 A
⑤1 mol SiO 中含有4N Si—O。
2 A
⑥单键为σ键,双键中有一个σ键、一个π键,三键中有两个π键、一个σ键。如在H—C≡N中含有2个σ
键、2个π键、1个孤电子对。
3.N 在电子转移数目中的应用
A
(1)过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.4N ( )
A
(2)1 mol氯气与足量的水反应,转移的电子数为N ( )
A
(3)标准状况下,6.72 L NO 溶于足量的水中,转移的电子数为0.3N ( )
2 A
(4)反应KIO +6HI===KI+3H O+3I 中,生成1 mol I 转移电子的总数为2N ( )
3 2 2 2 A
特别提醒 ①注意特殊物质,如由过氧化钠、过氧化氢制取1 mol氧气转移2 mol电子。
②铁与单质硫、单质碘、非氧化性酸反应,1 mol铁参与反应转移2 mol电子。
③1 mol铁与足量的氯气、稀硝酸反应,转移3 mol电子。
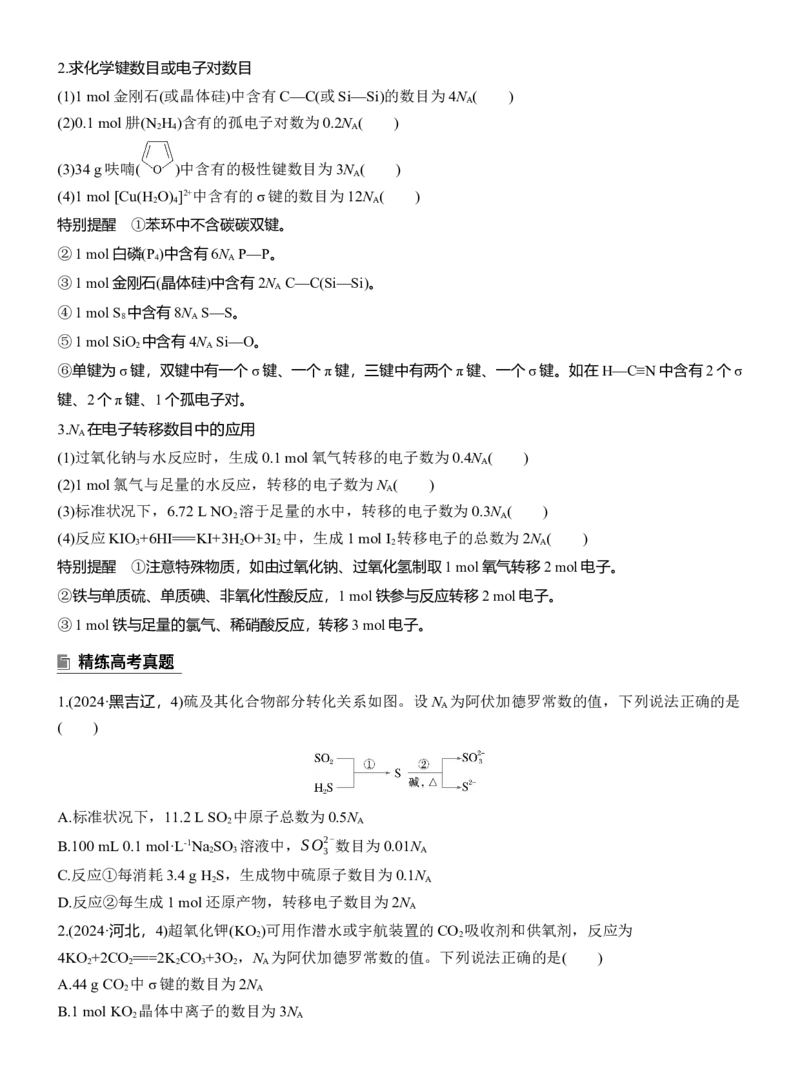
1.(2024·黑吉辽,4)硫及其化合物部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是
A
( )
A.标准状况下,11.2 L SO 中原子总数为0.5N
2 A
B.100 mL 0.1 mol·L-1Na SO
溶液中,SO2-数目为0.01N
2 3 3 A
C.反应①每消耗3.4 g H S,生成物中硫原子数目为0.1N
2 A
D.反应②每生成1 mol还原产物,转移电子数目为2N
A
2.(2024·河北,4)超氧化钾(KO )可用作潜水或宇航装置的CO 吸收剂和供氧剂,反应为
2 2
4KO +2CO ===2K CO +3O ,N 为阿伏加德罗常数的值。下列说法正确的是( )
2 2 2 3 2 A
A.44 g CO 中σ键的数目为2N
2 A
B.1 mol KO 晶体中离子的数目为3N
2 AC.1 L 1 mol·L-1 K CO
溶液中CO2-的数目为N
2 3 3 A
D.该反应中每转移1 mol电子生成O 的数目为1.5N
2 A
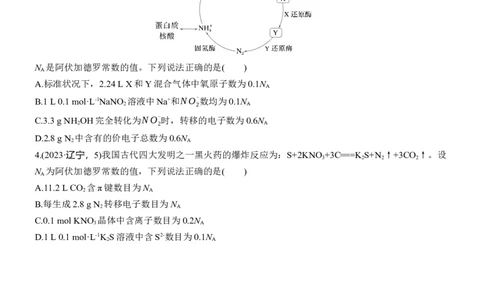
3.(2024·安徽,6)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化
物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反
2
应的产物盐酸羟胺([NH OH]Cl)广泛用于药品、香料等的合成。
3
已知25 ℃时,K(HNO )=7.2×10-4,K (NH ·H O)=1.8×10-5,K (NH OH)=7.7×10-9。
a 2 b 3 2 b 2
N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24 L X和Y混合气体中氧原子数为0.1N
A
B.1 L 0.1 mol·L-1NaNO
溶液中Na+和NO-
数均为0.1N
2 2 A
C.3.3 g NH
OH完全转化为NO-
时,转移的电子数为0.6N
2 2 A
D.2.8 g N 中含有的价电子总数为0.6N
2 A
4.(2023·辽宁,5)我国古代四大发明之一黑火药的爆炸反应为:S+2KNO +3C===K S+N ↑+3CO ↑。设
3 2 2 2
N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.11.2 L CO 含π键数目为N
2 A
B.每生成2.8 g N 转移电子数目为N
2 A
C.0.1 mol KNO 晶体中含离子数目为0.2N
3 A
D.1 L 0.1 mol·L-1K S溶液中含S2-数目为0.1N
2 A答案精析
盘点核心知识
1.(1)× (2)×
2.(1)× (2)×
3.(1)× (2)×
4.(1)× (2)×
5.×
对点训练
1.(1)× (2)× (3)× (4)√ (5)√
2.(1)× (2)√ (3)√ (4)√
3.(1)× (2)× (3)× (4)×
精练高考真题
1.D [标准状况下SO 为气体,11.2 L SO 的物质的量为0.5 mol,共含有1.5 mol原子,原子总数为
2 2
1.5N
,A项错误;SO2-
为弱酸阴离子,其在水中易发生水解,100 mL 0.1 mol·L-1 Na SO
溶液中SO2-
数目
A 3 2 3 3
小于0.01N ,B项错误;反应①的化学方程式为SO +2H S===3S↓+2H O,3.4 g H S的物质的量为0.1
A 2 2 2 2
mol,完全反应生成0.15 mol S,生成物中S原子数目为0.15N ,C项错误;反应②的离子方程式为
A
3S+6OH- S O 3 2- +2S2-+3H 2 O,还原产物为S2-,S→S2-,S化合价降低2,故每生成1 mol S2-,转移2 mol电
子,转移电子数目为2N ,D项正确。]
A
2.A [CO 的结构式为O C O,1个CO 分子中含有2个σ键,44 g即1 mol CO 中σ键的数目为2N ,
2 2 2 A
A正确;KO
由K+和O-
构成,1 mol KO 晶体中离子的数目为2N
,B错误;CO2-
在水溶液中会发生水解:
2 2 2 A 3
CO2- +H O HCO- +OH-,故1 L 1 mol·L-1K CO 溶液中CO2- 的数目小于N ,C错误;该反应中部分氧
3 2 3 2 3 3 A
1 1
元素化合价由- 价升至0价,部分氧元素化合价由- 价降至-2价,每4 mol KO 参加反应转移3 mol电子,
2 2 2
生成3 mol O ,则每转移1 mol电子生成O 的数目为N ,D错误。]
2 2 A
3.A
[NO-
在亚硝酸盐还原酶的作用下转化为X,X在X还原酶的作用下转化为Y,X、Y均为氮氧化物,
2
即X为NO,Y为N O。标准状况下,2.24 L NO和N O混合气体的物质的量为0.1 mol,氧原子数为
2 2
0.1N ,A项正确;HNO
为弱酸,NO-
能够水解为HNO ,1 L 0.1 mol·L-1 NaNO
溶液中NO-
的数目小于
A 2 2 2 2 2
0.1N ,B项错误;NH
OH完全转化为NO-
时,N元素的化合价由-1价升高到+3价,3.3 g NH OH的物质
A 2 2 2
的量为0.1 mol,转移的电子数为0.4N ,C项错误;2.8 g N 的物质的量为0.1 mol,N的价电子数为5,故
A 2
2.8 g N 含有的价电子总数为N ,D项错误。]
2 A4.C [题中没有说是标况条件下,气体摩尔体积未知,无法计算π键个数,A项错误;2.8 g N 的物质的量
2
为0.1 mol,生成1 mol N 转移的电子数为12N ,则生成0.1 mol N 转移的电子数为1.2N ,B项错误;因
2 A 2 A
为S2-水解使溶液中S2-的数目小于0.1N ,D项错误。]
A