文档内容
阿伏加德罗常数的应用
N 应用常设陷阱
A
常设陷阱 应用举例(判断正误)
1.溶液体积未知 (1)在pH=13的NaOH溶液中,OH-的数目为0.1×6.02×1023( ×
溶液的体积未知,溶质的物质的量无法 )
计算,所以微粒数也无法计算 (2)0.1 mol·L-1 FeCl 溶液中所含Fe3+的数目小于0.1N ( × )
3 A
2.标准状况下与非标准状况下的陷阱
(1)常温常压下,22.4 L氯气与足量的镁粉充分反应,转移的
气体若在非标准状况下,气体摩尔体积
电子数为2N ( × )
A
不能用22.4 L·mol-1计算;标准状况下为
(2)标准状况下,22.4 L苯中含有6N 个碳原子( × )
A
非气体的物质:SO 、CH OH、HF等
3 3
3.不能完全反应的陷阱 (1)密闭容器中,1 mol N 与3 mol H 充分反应,生成2 mol
2 2
可逆反应不能进行到底,如加热条件 NH ( × )
3
下,一定量的浓盐酸(浓硫酸)与足量的 (2)50 mL 12 mol·L-1盐酸与足量MnO 共热,转移的电子数为
2
MnO (金属铜)不能反应完全 0.3N ( × )
2 A
4.弱电解质的电离、盐类水解 (1)1 L 0.1 mol·L-1 CH
3
COOH溶液中所含H+的数目为0.1N
A
(
弱电解质仅部分电离;注意盐类水解引 × )
起的粒子数目变化 (2)1 L 0.1 mol·L-1 NH
Cl溶液中,NH+
的数目为0.1N ( × )
4 4 A
5.存在自由基连锁反应
1.0 mol CH 与Cl 在光照下反应生成的CH Cl分子数为N ( ×
4 2 3 A
氯气与CH 反应同时生成CH Cl、
4 3
)
CH Cl 、CHCl 、CCl 四种氯代物
2 2 3 4
对点训练
1.求粒子数
(1)1 mol Na O (或CaC )中含有的阴离子数为2N ( )
2 2 2 A
(2)1 mol —OH中含有的电子数为10N ( )
A
(3)18 g H O、D O组成的物质中含有的质子数为10N ( )
2 2 A
(4)28 g 乙烯和环丁烷(C H )的混合气体中含有的碳原子数为2N ( )
4 8 A
(5)1 mol Na O 和Na S的混合物中含有的离子总数为3N ( )
2 2 2 A
答案 (1)× (2)× (3)× (4)√ (5)√
特别提醒 ①因同位素而造成的摩尔质量不同的物质(如H O、D O组成的物质)需分别计算。
2 2
②对最简式相同的混合物,按最简式来计算(如乙烯、丙烯和环丁烷,它们的最简式都是CH )。
2③最简式不同的物质要分别计算。
2.求化学键数目或电子对数目
(1)1 mol金刚石(或晶体硅)中含有C—C(或Si—Si)的数目为4N ( )
A
(2)0.1 mol 肼(N H )含有的孤电子对数为0.2N ( )
2 4 A
(3)34 g呋喃( )中含有的极性键数目为3N ( )
A
(4)1 mol [Cu(H O) ]2+中含有的σ键的数目为12N ( )
2 4 A
答案 (1)× (2)√ (3)√ (4)√
特别提醒 ①苯环中不含碳碳双键。
②1 mol白磷(P )中含有6N P—P。
4 A
③1 mol金刚石(晶体硅)中含有2N C—C(Si—Si)。
A
④1 mol S 中含有8N S—S。
8 A
⑤1 mol SiO 中含有4N Si—O。
2 A
⑥单键为σ键,双键中有一个σ键、一个π键,三键中有两个π键、一个σ键。如在H—C≡N中含有2个σ
键、2个π键、1个孤电子对。
3.N 在电子转移数目中的应用
A
(1)过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.4N ( )
A
(2)1 mol氯气与足量的水反应,转移的电子数为N ( )
A
(3)标准状况下,6.72 L NO 溶于足量的水中,转移的电子数为0.3N ( )
2 A
(4)反应KIO +6HI===KI+3H O+3I 中,生成1 mol I 转移电子的总数为2N ( )
3 2 2 2 A
答案 (1)× (2)× (3)× (4)×
特别提醒 ①注意特殊物质,如由过氧化钠、过氧化氢制取1 mol氧气转移2 mol电子。
②铁与单质硫、单质碘、非氧化性酸反应,1 mol铁参与反应转移2 mol电子。
③1 mol铁与足量的氯气、稀硝酸反应,转移3 mol电子。
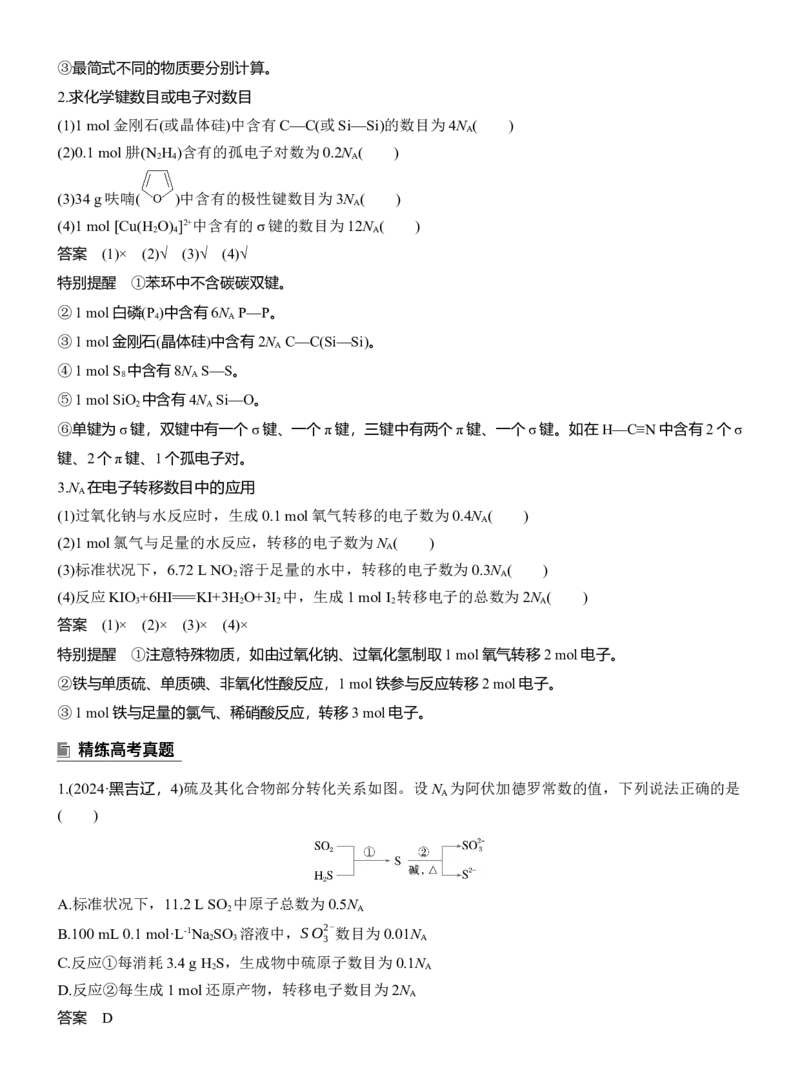
1.(2024·黑吉辽,4)硫及其化合物部分转化关系如图。设N 为阿伏加德罗常数的值,下列说法正确的是
A
( )
A.标准状况下,11.2 L SO 中原子总数为0.5N
2 A
B.100 mL 0.1 mol·L-1Na SO
溶液中,SO2-数目为0.01N
2 3 3 A
C.反应①每消耗3.4 g H S,生成物中硫原子数目为0.1N
2 A
D.反应②每生成1 mol还原产物,转移电子数目为2N
A
答案 D解析 标准状况下SO 为气体,11.2 L SO 的物质的量为0.5 mol,共含有1.5 mol原子,原子总数为
2 2
1.5N
,A项错误;SO2-
为弱酸阴离子,其在水中易发生水解,100 mL 0.1 mol·L-1 Na SO
溶液中SO2-
数目
A 3 2 3 3
小于0.01N ,B项错误;反应①的化学方程式为SO +2H S===3S↓+2H O,3.4 g H S的物质的量为0.1
A 2 2 2 2
mol,完全反应生成0.15 mol S,生成物中S原子数目为0.15N ,C项错误;反应②的离子方程式为
A
O2-
3S+6OH- S 3 +2S2-+3H O,还原产物为S2-,S→S2-,S化合价降低2,故每生成1 mol S2-,转移2 mol
2
电子,转移电子数目为2N ,D项正确。
A
2.(2024·河北,4)超氧化钾(KO )可用作潜水或宇航装置的CO 吸收剂和供氧剂,反应为
2 2
4KO +2CO ===2K CO +3O ,N 为阿伏加德罗常数的值。下列说法正确的是( )
2 2 2 3 2 A
A.44 g CO 中σ键的数目为2N
2 A
B.1 mol KO 晶体中离子的数目为3N
2 A
C.1 L 1 mol·L-1 K CO
溶液中CO2-的数目为N
2 3 3 A
D.该反应中每转移1 mol电子生成O 的数目为1.5N
2 A
答案 A
解析 CO 的结构式为O==C==O,1个CO 分子中含有2个σ键,44 g即1 mol CO 中σ键的数目为2N ,
2 2 2 A
A正确;KO
由K+和O-
构成,1 mol KO 晶体中离子的数目为2N
,B错误;CO2-
在水溶液中会发生水解:
2 2 2 A 3
CO2-
+H O
HCO-
+OH-,故1 L 1 mol·L-1K CO
溶液中CO2-
的数目小于N ,C错误;该反应中部分氧
3 2 3 2 3 3 A
1 1
元素化合价由- 价升至0价,部分氧元素化合价由- 价降至-2价,每4 mol KO 参加反应转移3 mol电子,
2 2 2
生成3 mol O ,则每转移1 mol电子生成O 的数目为N ,D错误。
2 2 A
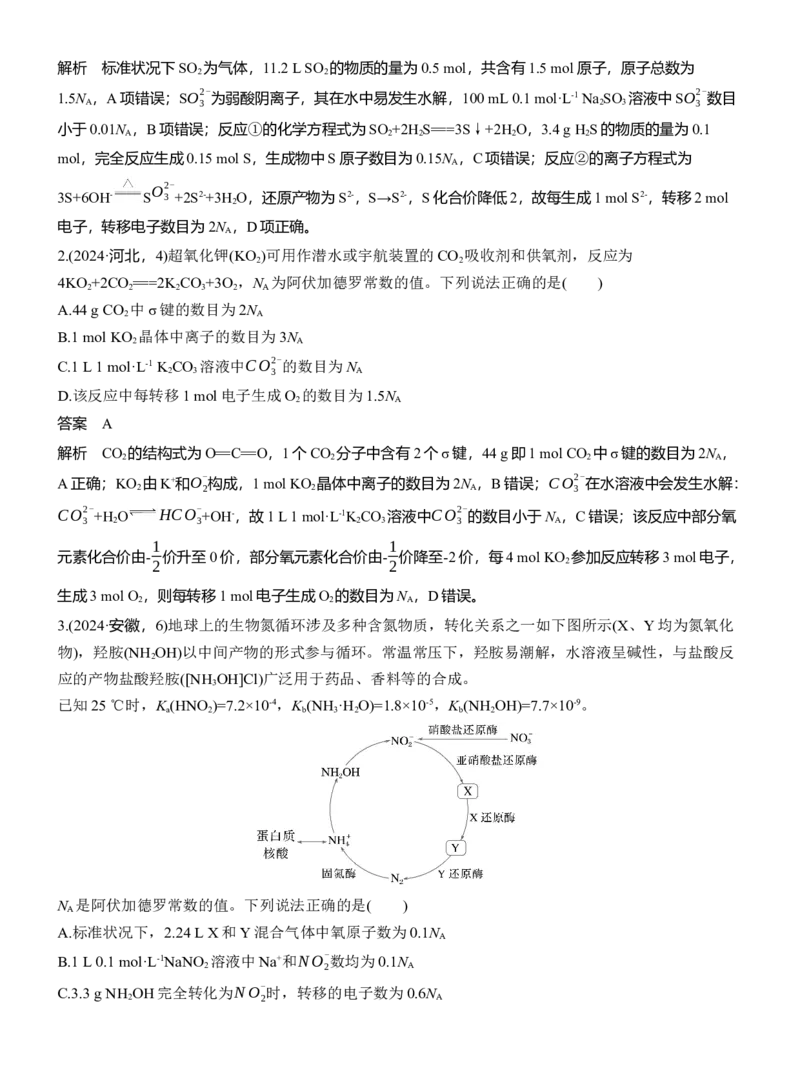
3.(2024·安徽,6)地球上的生物氮循环涉及多种含氮物质,转化关系之一如下图所示(X、Y均为氮氧化
物),羟胺(NH OH)以中间产物的形式参与循环。常温常压下,羟胺易潮解,水溶液呈碱性,与盐酸反
2
应的产物盐酸羟胺([NH OH]Cl)广泛用于药品、香料等的合成。
3
已知25 ℃时,K(HNO )=7.2×10-4,K (NH ·H O)=1.8×10-5,K (NH OH)=7.7×10-9。
a 2 b 3 2 b 2
N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,2.24 L X和Y混合气体中氧原子数为0.1N
A
B.1 L 0.1 mol·L-1NaNO
溶液中Na+和NO-
数均为0.1N
2 2 A
C.3.3 g NH
OH完全转化为NO-
时,转移的电子数为0.6N
2 2 AD.2.8 g N 中含有的价电子总数为0.6N
2 A
答案 A
解析
NO-
在亚硝酸盐还原酶的作用下转化为X,X在X还原酶的作用下转化为Y,X、Y均为氮氧化物,
2
即X为NO,Y为N O。标准状况下,2.24 L NO和N O混合气体的物质的量为0.1 mol,氧原子数为
2 2
0.1N ,A项正确;HNO
为弱酸,NO-
能够水解为HNO ,1 L 0.1 mol·L-1 NaNO
溶液中NO-
的数目小于
A 2 2 2 2 2
0.1N ,B项错误;NH
OH完全转化为NO-
时,N元素的化合价由-1价升高到+3价,3.3 g NH OH的物质
A 2 2 2
的量为0.1 mol,转移的电子数为0.4N ,C项错误;2.8 g N 的物质的量为0.1 mol,N的价电子数为5,故
A 2
2.8 g N 含有的价电子总数为N ,D项错误。
2 A
4.(2023·辽宁,5)我国古代四大发明之一黑火药的爆炸反应为:S+2KNO +3C===K S+N ↑+3CO ↑。设
3 2 2 2
N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.11.2 L CO 含π键数目为N
2 A
B.每生成2.8 g N 转移电子数目为N
2 A
C.0.1 mol KNO 晶体中含离子数目为0.2N
3 A
D.1 L 0.1 mol·L-1K S溶液中含S2-数目为0.1N
2 A
答案 C
解析 题中没有说是标况条件下,气体摩尔体积未知,无法计算π键个数,A项错误;2.8 g N 的物质的量
2
为0.1 mol,生成1 mol N 转移的电子数为12N ,则生成0.1 mol N 转移的电子数为1.2N ,B项错误;因
2 A 2 A
为S2-水解使溶液中S2-的数目小于0.1N ,D项错误。
A
题型突破练 [分值:100 分]
(选择题1~6题,每小题5分,7~16题,每小题7分,共100分)
1.(2024·黑龙江部分学校高三模拟)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1.8 g由H 18 O与D 16 O组成的混合物中所含中子、电子数目均为N
2 2 A
B.100 g质量分数为17%的H O 溶液中O原子数约为5.6N
2 2 A
C.常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
D.22.4 L CO
与NaOH溶液完全反应,则n(CO2- )+n(HCO-
)+n(H CO )=1 mol
2 3 3 2 3
答案 B
解析 1.8 g由H 18 O与D 16 O组成的混合物中所含中子、电子数目均为0.9N ,A错误;100 g质量分数为
2 2 A
17%的H O 溶液中含17 g H O 和83 g H O,O原子数约为5.6N ,B正确;常温下,铝片投入足量的浓硫
2 2 2 2 2 A
酸中发生钝化,生成致密的氧化膜会阻止内部的铝与浓硫酸反应,C错误;气体所处状况未知,无法通过
气体体积计算物质的量,D错误。
2.(2024·贵州六校联盟联考)设N 为阿伏加德罗常数的值。下列叙述正确的是( )
AA.1 mol NH F晶体中含有共价键的数目为5N
4 A
B.标准状况下,33.6 L SO 中含有分子的数目为1.5N
3 A
C.1 mol
CH+中含有的电子数为10N
3 A
D.在电解精炼粗铜的过程中,当阴极质量增重32 g时转移的电子数为N
A
答案 D
解析 1 mol NH F晶体中含有共价键的数目为4N ,故A错误;SO 在标准状况下不是气态,不能用气体
4 A 3
摩尔体积计算,故B错误;1 mol
CH+
中含有的电子数为(6+3-1)N =8N ,故C错误;在电解精炼粗铜的过
3 A A
程中,阴极:1 mol Cu2+~2N e-~64 g Cu,当阴极质量增重32 g时转移的电子数为N ,故D正确。
A A
3.(2024·东北三省三校高三模拟)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,11.2 L环庚烷中氢原子数目为7N
A
B.13 g苯、乙炔的混合物中所含氢原子数目为N
A
C.2.4 g Mg在空气中燃烧生成MgO和 Mg N ,转移电子数目为0.1N
3 2 A
D.1 mol NH+中含有完全相同的N—H 共价键的数目为3N
4 A
答案 B
解析 标准状况下,环庚烷不是气体,11.2 L环庚烷中氢原子数目不是7N ,A错误;苯和乙炔的最简式
A
相同,为CH,13 g苯、乙炔的混合物中所含氢原子数目为N ,B正确;2.4 g Mg在空气中燃烧生成MgO
A
和 Mg N ,镁由0价升高到+2价,转移电子数目为0.2N ,C错误;铵根离子中4个N—H 共价键完全相同,
3 2 A
所以1 mol
NH+
中含有完全相同的N—H共价键的数目为4N ,D错误。
4 A
4.(2024·东北三省高三模拟)羰基硫(COS)是一种粮食熏蒸剂,能防止某些害虫和真菌的危害。CO与H S反
2
应可以制得COS,其化学方程式为CO(g)+H S(g)===COS(g)+H (g)。N 为阿伏加德罗常数的值,下列有关
2 2 A
说法正确的是( )
A.2.8 g C18O含中子数为1.6N
A
B.4.8 g COS中π键数目为0.16N
A
C.pH=2的H S溶液中H+的数目为0.01N
2 A
D.生成2.24 L H ,转移电子数目为0.2N
2 A
答案 B
2.8 g
解析 2.8 g C18O的物质的量为 <0.1 mol,1个C18O分子中含16个中子,0.1 mol C18O分子中
30 g·mol-1
含中子数为1.6N ,故2.8 g C18O含中子数小于1.6N ,A错误;4.8 g COS的物质的量为0.08 mol,1个
A A
COS分子中有2个π键,0.08 mol COS中π键数目为0.16N ,B正确;溶液的体积未知,无法求出H+的数
A
目,C错误;未注明“标准状况”,无法计算2.24 L H 的物质的量,不能得出反应转移的电子数,D错误。
2
5.(2024·黑龙江绥化高三联考)用N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol乙烷中含有sp3杂化的原子数目为N
AC.46 g C H O分子中含极性键数目一定是7N
2 6 A
D.标准状况下,22.4 L CH Cl 中C—Cl的数目为2N
2 2 A
答案 B
解析 溶液的体积未知,无法计算pH=3的甲酸溶液中氢离子的数目,故A错误;乙烷分子中碳原子的杂
化方式都为sp3杂化,则0.5 mol乙烷中含有sp3杂化的原子数目为N ,故B正确;分子式为C H O的有机
A 2 6
物可能是极性键数目为7的乙醇,或极性键数目为8的甲醚,或是两者的混合物,所以46 g C H O分子中
2 6
含极性键数目不一定是7N ,故C错误;标准状况下,二氯甲烷为液态,无法计算22.4 L二氯甲烷含有的
A
C—Cl的数目,故D错误。
6.(2024·贵阳高三下学期适应性测试)丙烯不溶于H O,能与Cl 、HCl反应。设N 为阿伏加德罗常数的值。
2 2 A
下列叙述正确的是( )
A.21 g丙烯所含共用电子对数为4N
A
B.1.5 mol D O所含中子数为15N
2 A
C.22.4 L Cl 溶于水转移的电子数为N
2 A
D.2 mol·L-1HCl溶液中Cl-数为2N
A
答案 B
21 g
解析 1个丙烯(CH ==CHCH )分子中含有9个共用电子对,21 g丙烯的物质的量为 =0.5
2 3 42 g·mol-1
mol,则所含共用电子对数为4.5N ,A不正确;1个D O中含有10个中子,则1.5 mol D O所含中子数为
A 2 2
15N ,B正确;温度、压强未知,无法求出22.4 L Cl 的物质的量,且溶于水的Cl 只有部分与水发生反应,
A 2 2
所以无法求出转移的电子数,C不正确;2 mol·L-1HCl溶液的体积未知,无法求出其含有的Cl-数目,D不
正确。
7.(2024·南宁高三毕业班第一次适应性测试)一种电化学还原制氨气的反应为2N +6H O 4NH +3O ,
2 2 3 2
N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.常温常压下,28 g N 中含有的N≡N数目为N
2 A
B.标准状况下,22.4 L H O中氢原子的数目为2N
2 A
C.1 L 0.1 mol·L-1NH ·H O溶液的pH为13
3 2
D.每生成3 mol O ,理论上转移电子的数目为6N
2 A
答案 A
28 g
解析 28 g N 的物质的量为 =1 mol,其含有的N≡N数目为N ,故A正确;标准状况下,
2 28 g·mol-1 A
H O不是气态,22.4 L H O的物质的量不为1 mol,故B错误;NH ·H O为弱电解质, 0.1 mol·L-1NH ·H O
2 2 3 2 3 2
电离出的OH-浓度小于0.1 mol·L-1,故C错误;O的化合价由-2价上升到0价,每生成3 mol O ,理论上转
2
移电子的数目为12N ,故D错误。
A8.(2024·广西模拟)为处理制硝酸过程中产生的尾气NO ,可用具有碱性的Na CO 溶液进行吸收,反应方程
2 2 3
式为2NO +Na CO ===NaNO +NaNO +CO 。设N 为阿伏加德罗常数的值,下列说法正确的是( )
2 2 3 2 3 2 A
A.常温下,22.4 L NO 气体所含分子数为N
2 A
B.1 mol·L-1 NaNO
溶液中,NO-
的数目小于N
2 2 A
C.Na CO 溶液中含有1 mol CO2-,则Na+的数目大于2N
2 3 3 A
D.每生成22 g CO 反应转移的电子数为N
2 A
答案 C
解析 没有明确溶液体积,不能计算NaNO
溶液中含NO-
的数目,B错误;Na CO 溶液中含有1 mol
2 2 2 3
CO2- ,因为CO2- 水解,则Na CO 的物质的量大于1 mol,则Na+的数目大于2N ,C正确;根据反应
3 3 2 3 A
2NO +Na CO ===NaNO +NaNO +CO ,N元素由+4价变为+3价和+5价,转移电子数为1,每生成22 g
2 2 3 2 3 2
CO (即0.5 mol),反应转移的电子数为0.5N ,D错误。
2 A
9.(2024·皖豫名校高三模拟)设N 表示阿伏加德罗常数的值。下列说法错误的是( )
A
A.12 g NaHSO 固体中含有的阳离子数目为0.1N
4 A
B.18 g重水(D O)中含有的质子数为9N
2 A
C.1 mol 中含σ键的数目为5N
A
D.0.1 mol Fe和0.1 mol Cl 充分反应,转移的电子数为0.2N
2 A
答案 C
解析 12 g NaHSO 固体的物质的量为0.1 mol,其中含有的阳离子为钠离子,数目为0.1N ,A项正确;每
4 A
个D O中含质子数为10,D O的相对分子质量为20,18 g重水中含有的质子数为9N ,B项正确;1个分
2 2 A
子中,C—C和C—O σ键共5个,C—H σ键共4个,故1 mol 中含σ键的数目为9N ,C项错误;0.1
A
mol Fe和0.1 mol Cl 充分反应生成FeCl ,Fe过量,因此按Cl 计算,转移的电子数为0.2N ,D项正确。
2 3 2 A
10.(2024·安徽淮北高三调研)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.常温下,pH为13的Ba(OH) 溶液中含有OH-的数目为0.2N
2 A
B.2 L 0.1 mol·L-1 NaCN溶液中含N的粒子数目为0.2N
A
C.粗铜精炼时,若阳极材料减少6.4 g,电路中通过电子数一定是0.2N
A
D.100 g 46%的甲酸水溶液中,含有的氧原子数为2N
A
答案 B
解析 溶液体积未知,无法确定OH-的数目,A错误;根据元素守恒可知:c(HCN)+c(CN-)=0.1 mol·L-1,溶
液体积为2 L,则HCN与CN-的总数目为0.2N ,B正确;阳极多种金属参与反应,无法计算电路中通过的
A
电子数,C错误;100 g 46%的甲酸水溶液中,甲酸的质量为46 g,物质的量为1 mol,故含2 mol氧原子;
水的质量为54 g,物质的量为3 mol,故含3 mol氧原子,则此溶液中含有的氧原子的物质的量为5 mol,
即个数为5N ,D错误。
A11.(2023·广东名校联盟联考)设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1 L 0.1 mol·L-1 Ca(ClO) 溶液中含ClO-的数目为0.2N
2 A
B.12 g质量分数为25%的甲醛水溶液中含0.1N 个O原子
A
C.已知核反应:235U+1 n―→ 144Ba+AM+31 n,则0.1 mol M中含中子的数目为5.3N
92 0 56 Z 0 A
D.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO 分子的数目为0.46N
2 A
答案 C
解析 次氯酸根离子发生水解,导致其数目小于0.2N ,A错误;12 g质量分数为25%的甲醛水溶液中的
A
水中也含有氧原子,故含有的O原子数大于0.1N ,B错误;A=235+1-144-3×1=89,Z=92-56=36,M中含
A
有的中子数为89-36=53,故0.1 mol M中含中子的数目为5.3N ,C正确;随着反应进行,硫酸浓度减小,
A
稀硫酸和铜不反应,生成SO 分子的数目小于0.46N ,D错误。
2 A
12.(2024·浙江金丽衢十二校高三模拟)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.6 g石英晶体中含有的Si—O的数目是0.2N
A
B.18 g氨基(—NH )中含有的电子数为10N
2 A
C.4.4 g C H O中含σ键的数目最多为0.7N
2 4 A
D.1 L 0.1 mol·L-1的CH COONH
溶液中,含有NH+
的数目为0.1N
3 4 4 A
答案 C
解析 1 mol SiO 中含4 mol Si—O,则6 g石英晶体即0.1 mol SiO 中含有的Si—O的数目是0.4N ,A错误;
2 2 A
9 81
1个氨基(—NH )中含9个电子,则18 g氨基(—NH )即 mol氨基中含有的电子数为 N ,B错误;当
2 2 8 8 A
C H O表示环氧乙烷( )时,1个环氧乙烷分子中含7个σ键,则4.4 g即0.1 mol环氧乙烷中含σ键的数
2 4
目为0.7N ,当C H O表示CH CHO时,4.4 g CH CHO中含σ键的数目为6N ,C正确;CH COONH 溶液
A 2 4 3 3 A 3 4
中N H+ 会水解,则1 L 0.1 mol·L-1的CH COONH 溶液中,含有N H+ 的数目小于0.1N ,D错误。
4 3 4 4 A
13.(2024·江西重点中学协作体高三联考)设N 为阿伏加德罗常数的值,下列叙述不正确的是( )
A
A.常温下,1 L 0.1 mol·L-1的NH
Cl溶液中滴入氨水至pH=7,NH+
的数目为0.1N
4 4 A
B.100 g质量分数为46%的C H O水溶液中O原子数为4N
2 6 A
C.标准状况下,2.24 L一氯甲烷中含sp3⁃s型σ键数目为0.1N
A
D.常温下,1 L pH=5的NH Cl溶液中,水电离出的OH-数目为10-5N
4 A
答案 C
100 g×46%
解析 100 g质量分数为46%的C H O水溶液中,n(C H O)= =1 mol,n(H O)=
2 6 2 6 46 g·mol-1 2
100 g×(1-46%)
=3 mol,则共含氧原子的物质的量为1 mol+3 mol=4 mol,数目为4N ,B不符合题意;
18 g·mol-1 A
标准状况下,2.24 L一氯甲烷为0.1 mol,一分子一氯甲烷中含三个C—H和一个C—Cl,C—H属于sp3⁃sσ
键,其数目为0.3N ,C符合题意;NH Cl属于强酸弱碱盐,能促进水的电离,常温下,1 L pH=5的NH Cl
A 4 4溶液中,由水电离出的c(H+)=10-5 mol·L-1,那么由水电离出的c(OH-)=10-5 mol·L-1,对应的OH-的数目为10-
5N ,D不符合题意。
A
14.(2024·湖南邵阳高三模拟)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.标准状况下,11.2 L Cl 溶于水,溶液中Cl-、ClO-和HClO的微粒数之和小于N
2 A
B.0.1 mol·L-1NH NO 溶液中含有N H+ 数目小于0.1N
4 3 4 A
C.2.3 g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N 之间
2 A A
D.1 mol 苯乙烯中含有碳碳双键数为4N
A
答案 A
解析 氯气与水的反应为可逆反应,不能进行到底,依据氯原子个数守恒可知,标准状况下,11.2 L 氯气
11.2 L
的物质的量为 =0.5 mol,则溶液中Cl-、ClO-、HClO的微粒数之和小于N ,故A正确;溶
22.4 L·mol-1 A
液体积未知,不能计算溶液中含有N H+ 的数目,故B错误;2.3 g Na物质的量为0.1 mol,与O 完全反应,
4 2
反应中转移的电子数为0.1N ,故C错误;苯环中不存在碳碳双键,1 mol苯乙烯中含有碳碳双键数为N ,
A A
故D错误。
15.(2024·湖北省部分高中高三模拟)硫酸铵主要用作肥料,还可用于纺织、皮革、医药等方面。其加热分解
的方程式为(N H ) SO ―→NH ↑+N ↑+H O+SO ↑(未配平)。设N 为阿伏加德罗常数的值,下列说法正
4 2 4 3 2 2 2 A
确的是( )
A.0.5 mol·L-1的(N H ) SO 溶液中N H+ 的数目小于N
4 2 4 4 A
B.每生成1 mol NH ,反应中转移1.5N 电子
3 A
C.标准状况下,22.4 L H O中含有的原子数为3N
2 A
D.6.4 g SO 分子中中心原子上的孤电子对数为0.2N
2 A
答案 B
N H+
解析 溶液的体积未知,无法计算溶液中 4的数目,故A错误;配平方程式为3(NH
4
)
2
SO
4
4NH ↑+N ↑+6H O+3SO ↑,每生成1 mol NH ,反应中转移1.5N 电子,故B正确;标准状况下,H O不
3 2 2 2 3 A 2
是气体,22.4 L H O中含有的原子数大于3N ,故C错误;SO 中心原子上的孤电子对数为1,故6.4 g SO
2 A 2 2
分子中中心原子上的孤电子对数为0.1N ,故D错误。
A
16.(2024·湖北省八市高三联考)纳米球状红磷可提高钠离子电池的性能,可由PCl (易水解)和NaN 制备:
5 3
2PCl +10NaN ===2P+15N ↑+10NaCl。设N 为阿伏加德罗常数的值,下列说法正确的是( )
5 3 2 A
A.11.2 L N 含π键数目为N
2 A
B.每生成3.1 g P转移电子数目为N
A
C.0.1 mol NaN 晶体中含离子数目为0.2N
3 A
D.0.1 mol PCl 与足量水反应,所得溶液中H+的数目为0.8N
5 A
答案 C解析 未说明N 所处的温度和压强,无法计算11.2 L N 含π键的数目,故A错误;
2 2
2PCl +10NaN ===2P+15N ↑+10NaCl中P元素由+5价下降到0价,3.1 g P的物质的量为0.1 mol,则每生
5 3 2
成3.1 g P转移电子数目为0.5N ,故B错误;NaN 晶体中含有Na+和N3-,0.1 mol NaN 晶体中含离子数目
A 3 3
为0.2N ,故C正确;PCl 与水发生反应:PCl +4H O===5HCl+H PO ,0.1 mol PCl 与足量水反应生成0.5
A 5 5 2 3 4 5
mol HCl和0.1 mol H PO ,H PO 是弱电解质,在水溶液中不能完全电离,所得溶液中H+的数目小于
3 4 3 4
0.8N ,故D错误。
A