文档内容
西安中学 2026 届高三质量检测考试(一)
化学试题
时间:75 分钟 满分:100 分
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Si-28 S –32 Cu-64 Zn-65
Pb -207
一、选择题(本题共 14 个小题,每小题 4 分,共 56 分。在每小题只有一项符合题目要求)
1. 下列说法错误的是( )
A. 乙烯的产量经常作为衡量一个国家石油化工水平的高低
B. 乙烯可用作植物果实生长的催化剂和调节剂
C. 苯、己烷、甲苯、环己烷、硝基苯均不溶于水且密度小于水
D.石油裂解和煤的气化都是化学变化
2. 以甲烷为燃料,KOH 溶液为导电介质组成燃料电池,以下叙述错误的是( )
A. 负极反应式为:CH -8e-+10OH-===CO 2-+7H O
4 3 2
B. 可以将燃料和氧化剂由电池外部连续供给并在电极上反应,生成物被排出,可连续
不断的提供电能
C. CH 和 CO 2-中碳原子的杂化方式分别为 sp3 和 sp2 杂化
4 3
D. 该电池的总反应为: CH + 2O = CO +2H O。
4 2 2 2
3. 某有机化合物的结构简式为: ,下列说法不正确的是( )
A. 能被银氨溶液氧化
B. 能使酸性高锰酸钾溶液褪色
C. 向该物质中加入溴水后振荡,溴水褪色,说明该化合物中存在碳碳双键
D. 该化合物可以发生氧化、还原、加聚等反应
4. 石墨烯电池是利用锂离子在石墨烯表面和电极之间快速大量穿梭运动的特性而研发的新
型可充放电电池,其反应式为 Li C +Li CoO C +LiCoO ,其工作原理如下图所示。
x 6 1-x 2 6 2
下列关于该电池的说法正确的是( )
A.充电时,Li+嵌入 LiCoO 中
2
高三年级化学试题第1页共6页B.放电时,LiCoO 极发生的电极反应为:
2
LiCoO -xe-===Li CoO +xLi+
2 1-x 2
C.放电时负极反应可表示为:Li C -ye-===yLi+ + Li C
x 6 (x-y) 6
D.充电时,若转移 x mol e-,石墨烯电极增重 7 g
5. 利用生物燃料电池原理研究室温下氨的合成,电池工作时 MV2+/MV+ 在电极与酶之间传
递电子,示意图如下所示。下列说法错误的是( )
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应 H
2
+2MV2+===2H++2MV+
C.正极区,固氮酶为催化剂,N 发生还原反应生成 NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
6. 回收利用工业废气中的 CO 和 SO ,实验原理示意图如下。
2 2
下列说法不正确的是( )
A.装置 a 的作用是吸收 SO 并分离出 CO
2 2
B. 该离子交换膜为阳离子交换膜
C. 阳极的电极反应式为:
SO 2- - 2e- + 2HCO - = SO 2- + H O + 2CO
3 3 4 2 2
D.装置 b 中的总反应为 +CO +H O HCOOH+
2 2
7. 下列热化学方程式正确的是( )
A. 2NO ===O +2NO ΔH=+116.2 kJ·mol-1
2 2
B. 3.2 g CH (g)完全燃烧生成 CO (g)和 H O(l)时放出 178 kJ 的热量,其热化学方程式
4 2 2
为 CH (g)+2O (g)===CO (g)+2H O(l) ΔH=-890 kJ
4 2 2 2
C. 已知 N (g)+3H (g) 2NH (g) ΔH=-92 kJ·mol-1,
2 2 3
则 NH (g) N (g)+ H (g) ΔH=+46 kJ·mol-1
3 2 2
D. 1 mol 液态肼在足量氧气中完全燃烧生成水蒸气,放出 642 kJ 的热量,则
N H (l)+O (g)===N (g)+2H O(g) ΔH=+642 kJ·mol-1
2 4 2 2 2
8. “千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH ) SO 的离子键强弱,设计如
4 2 4
高三年级化学试题第2页共6页图所示的循环过程,可得ΔH /(kJ· mol-1)为( )
4
A.+533 B.+838 C.+686 D.+1 143
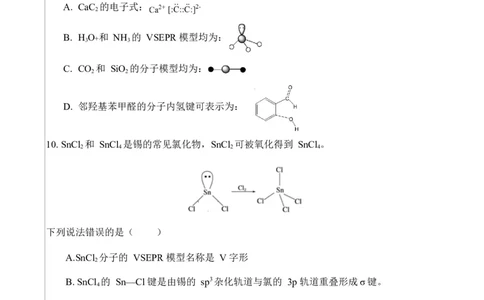
9. 下列化学用语正确的是( )
A. CaC 的电子式:
2
B. H
3
O+ 和 NH
3
的 VSEPR 模型均为:
C. CO 和 SiO 的分子模型均为:
2 2
D. 邻羟基苯甲醛的分子内氢键可表示为:
10. SnCl 和 SnCl 是锡的常见氯化物,SnCl 可被氧化得到 SnCl 。
2 4 2 4
下列说法错误的是( )
A.SnCl 分子的 VSEPR 模型名称是 V 字形
2
B. SnCl 的 Sn—Cl 键是由锡的 sp3 杂化轨道与氯的 3p 轨道重叠形成σ键。
4
C.分子中 Cl—Sn—Cl 键角:SnCl >SnCl
2 4
D. 分子的极性:SnCl > SnCl
2 4
11. 一种高聚物(XYZ ) 被称为“无机橡胶”,可由如图所示的环状三聚体制备。X 、Y 和 Z 都
2 n
是短周期元素,X、Y 价电子数相等,X、Z 电子层数相同,基态 Y 的 2p 轨道半充满,Z 的
最外层只有 1 个未成对电 子,下列说法正确的是( )
高三年级化学试题第3页共6页A. X、Z 的第一电离能:X>Z
B. X、Y 的简单氢化物的键角:X>Y
C. 最高价含氧酸的酸性:Z>X>Y
D. X、Y、Z 均有多种含氧酸
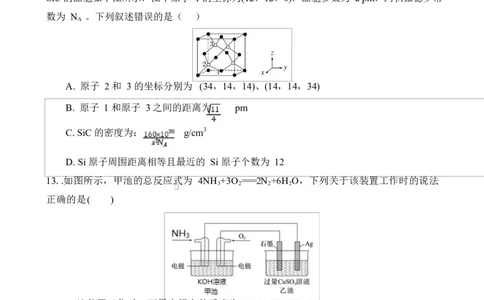
12. 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,
SiC 的晶胞如下图所示,图中原子 1 的坐标为(12,12,0),晶胞参数为 a pm,阿伏伽德罗常
数为 N 。下列叙述错误的是( )
A
A. 原子 2 和 3 的坐标分别为 (34,14,14)、(14,14,34)
B. 原子 1 和原子 3 之间的距离为 pm
C. SiC 的密度为: g/cm3
D. Si 原子周围距离相等且最近的 Si 原子个数为 12
13. .如图所示,甲池的总反应式为 4NH +3O ===2N +6H O,下列关于该装置工作时的说法
3 2 2 2
正确的是( )
A.该装置工作时,石墨电极上的反应为:4OH- - 4e- = O + 2H O
2 2
B. 甲池和乙池中溶液的 pH 均减小
C. 甲池中负极反应式为 2NH
3
-6e-===N
2
+6H+
D.当甲池中消耗 1.7 g NH 时,乙池中理论上最多产生 6.4g 固体
3
14. 海港、码头的钢制管桩会受到海水的长期侵袭,常用外加电流法对其进行保护(如下图
所示,其中高硅铸铁为惰性辅助阳极)。下列有关叙述中错误的是( )。
高三年级化学试题第4页共6页A. 高硅铸铁是作为损耗阳极材料发挥作用的
B. 通电后外电路的电子被强制流向钢制管桩
C. 保护电流应该根据环境条件变化进行调整
D. 通电后使钢制管桩表面的腐蚀电流接近零
二、非选择题(共 44 分)
15.(12 分)长征系列部分火箭采用了肼(N H )作燃料,N H 与 NH 有相似的化学性质,回答下
2 4 2 4 3
列问题:
(1)已知肼(N H )分子中所有原子最外层都满足稀有气体原子结构,则肼分子的结构式
2 4
为 。
(2)下表是常见的键能数据:
化学键 N—H N—N N≡N H—H
键能/(kJ·mol-1) 386 167 946 a
已知合成氨反应 N (g)+3H (g) 2NH (g) ΔH=-92 kJ·mol-1,则 a 为 。
2 2 3
(3)以肼为燃料,KOH 溶液为导电介质,O 为氧化剂,金属铂为电极组成燃料电池,写
2
出负极的电极反应式: 。
(4) 肼(N H )和乙烷(C H )的相对分子质量接近,但通常状况下,肼为液态而乙烷
2 4 2 6
为气态,原因是 。
(5) H O 、 N H 、C H ,三个分子中均含非极性共价键,其中属于非极性分子的是
2 2 2 4 2 6
(填分子式)
(6)向硫酸铜溶液中加入肼,可形成配体与中心离子物质的量比为 2:1 的配合物离子,用
“ ”表示配位键,写出该配合物离子的结构简式 。
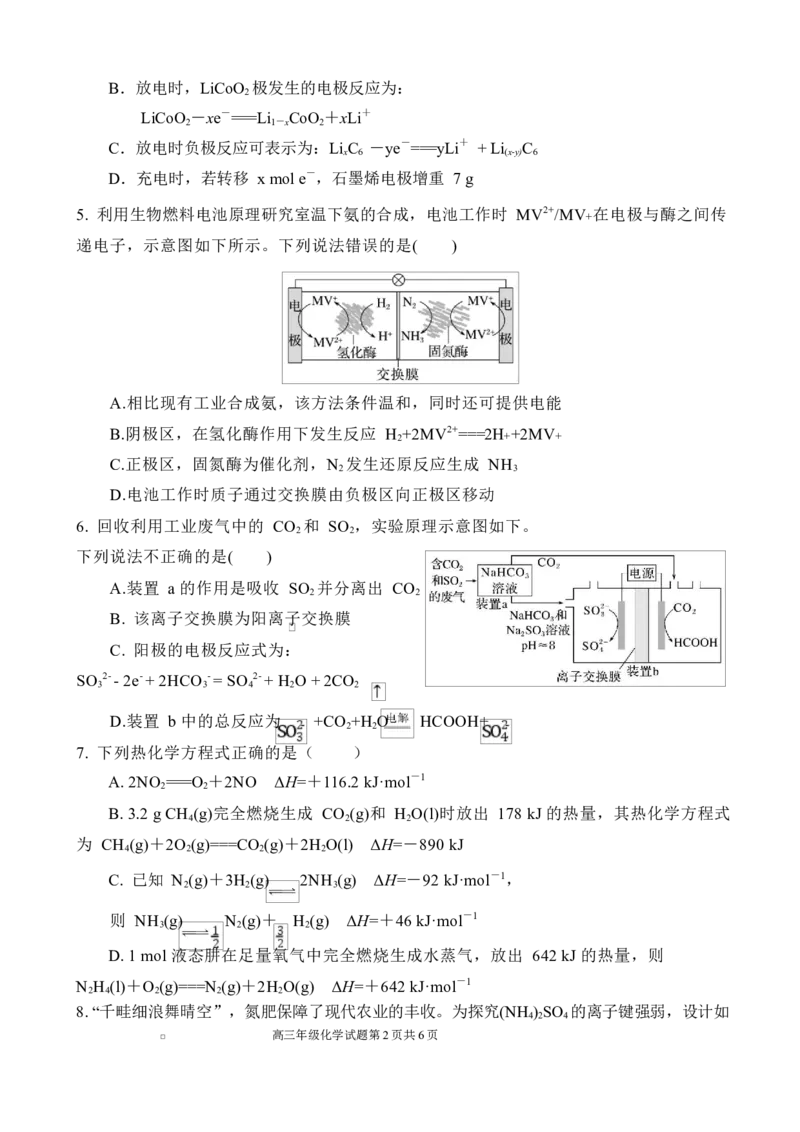
16.(10 分)为增强铝的耐腐蚀性,现以铅酸蓄电池为外电源,以 Al 作阳极、Pb 作阴极,
高三年级化学试题第5页共6页电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
原电池:Pb(s)+PbO (s)+2H SO (aq)===2PbSO (s)+2H O(l)
2 2 4 4 2
电解池:2Al+3H O ==Al O +3H ↑
2 2 3 2
电解过程中,填写以下空白
原电池 电解池
(1) 每消耗 3 mol Pb 生成 mol Al O
2 3
(2) 正极电极反应式: 阳极电极反应式:
(3) 正极电极质量增加 6.4g 生成标况下 H 的体积 L
2
(4)
(画出对应曲线)
17(10 分)回答下列问题:
(1)气态氢化物热稳定性:HF 大于 HCl 的主要原因是__________。
(2)CaCN 是离子化合物,各原子均满足 8 电子稳定结构,CaCN 的电子式是_______。
2 2
(3)已知硝基(-NO )是吸电子基,甲基(-CH )是推电子基,则酸性强弱:
2 3
(填“>”,“<”或“=”)。
(4)已知 K+ 能和某冠醚形成超分子,结构如图所示,下列说法错误的是( )
a. K+ 和冠醚分子之间以配位键结合
b. 在烯烃中加入该冠醚,可提高 KMnO 溶液对烯烃的氧化速率
4
c.在烯烃中加入该冠醚,可提高 Na Cr O 溶液对烯烃的氧化速率
2 2 7
(5)NO -离子中的大 键为 (用 的形式表示,“n”为参与形成大 键的原子数
2
目,“m”为共享的电子数目),
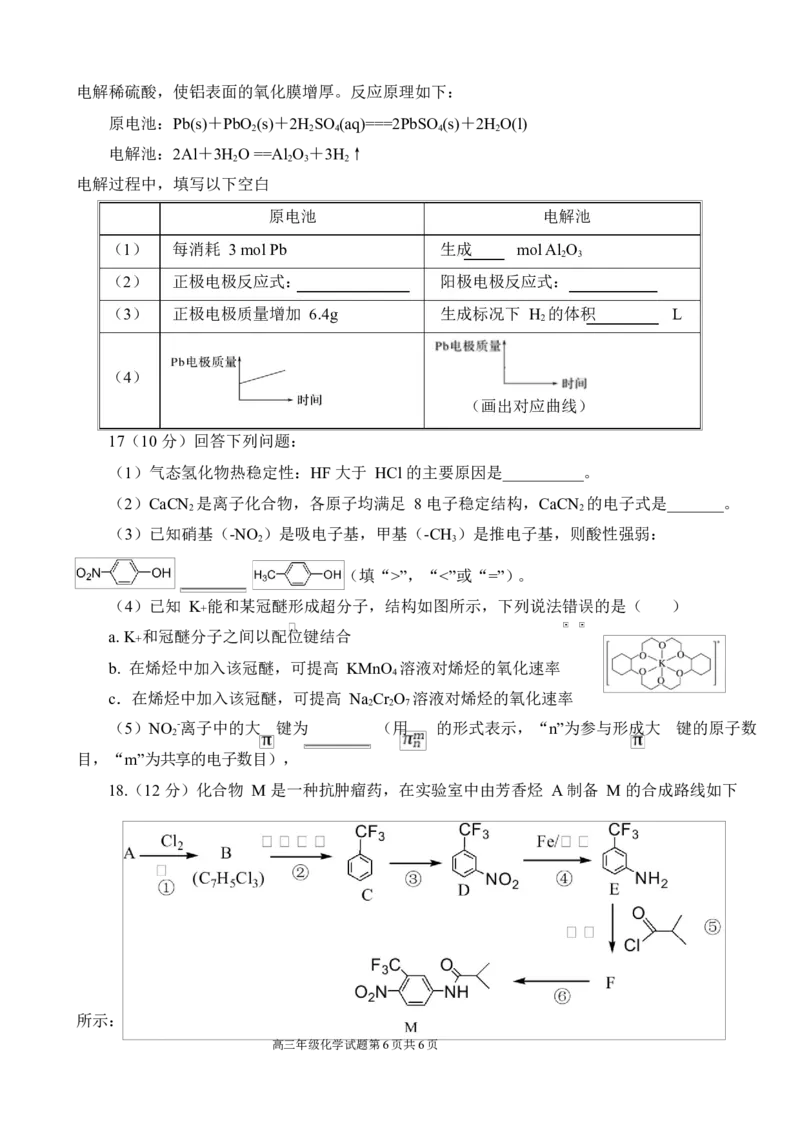
18.(12 分)化合物 M 是一种抗肿瘤药,在实验室中由芳香烃 A 制备 M 的合成路线如下
所示:
高三年级化学试题第6页共6页(1)芳香烃 A 的名称是 ,反应③和④的反应分别是 、 。
(2)请写出反应⑤的化学方程式 。吡啶是一种有机碱,请推测其在反应⑤中的作
用 。
(3)异丁酰氯( )的同分异构体中能发生银镜反应,核磁共振氢谱有四组峰且峰面
积比为 3:2:1:1 的同分异构体共有 种。
(4)对甲氧基乙酰苯胺( )是合成染料和药物的中间体,请写出由苯
甲醚( )制备对甲氧基乙酰苯胺的合成路线(其它试剂任选)。
高三年级化学试题第7页共6页