文档内容
曲靖一中 2026 届高三年级教学质量检测四
化 学 试 卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Pd-106 I-127 Cs-133
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与生活、科技、社会发展息息相关。下列说法正确的是( )
A.光导纤维不属于新型无机非金属材料
B.“神舟飞船”返回舱外层材料的酚醛树脂有固定熔点
C.加工馒头、面包时,可加入一些膨松剂如NH HCO ,使面团疏松多孔
4 3
D.“长征七号”采用液氧、煤油等作为推进剂,液氧、煤油都是纯净物
2.下列化学用语或图示表示错误的是( )
A.气态二聚氟化氢分子[(HF) ]: B.H BO 的球棍模型:
2 3 3
C.2-甲基-3-乙基戊烷的键线式: D.CaO 的电子式:
2
3.依据下列实验现象或实验目的,对应离子反应方程式正确的是( )
H O
CH CH Br + OH - 2 CH CH OH + Br -
A. 溴乙烷在热烧碱溶液中水解: 3 3 3 2
△
B.证明NH 对Cu2+的配位能力强于H O:
3 2
C.H C O 使酸性高锰酸钾溶液褪色:
2 2 4
D.联氨(N H )是一种二元弱碱, 在水溶液中发生水解的离子方程式:
2 4
4.设N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,4.48L HF中含有的电子数目为2N
A
B.镁铝合金与盐酸反应时,当生成4g H 时转移的电子数目为2N
2 A
C.标准状况下,11.2L Cl 溶于水,所得溶液中Cl-、ClO-、HClO的微粒数之和小于N
2 A
D.CO (g)通过足量Na O (s)充分反应,固体增重14g时,反应中转移的电子数为N
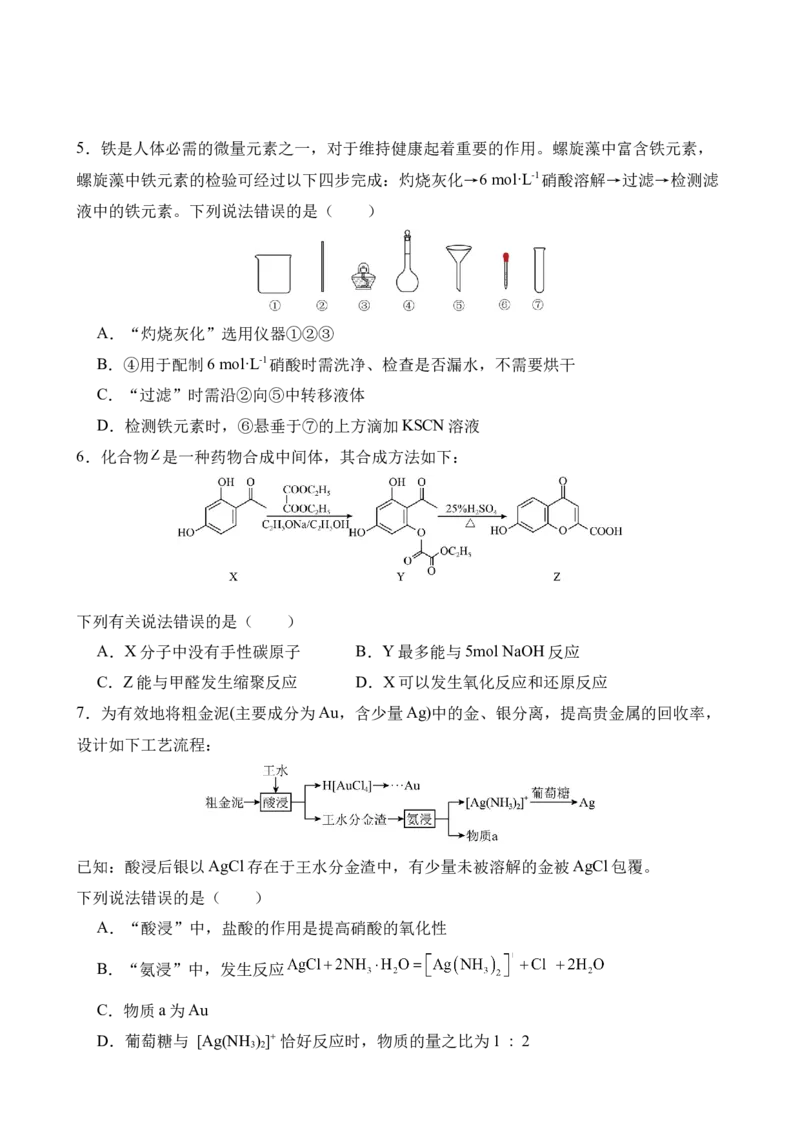
2 2 2 A5.铁是人体必需的微量元素之一,对于维持健康起着重要的作用。螺旋藻中富含铁元素,
螺旋藻中铁元素的检验可经过以下四步完成:灼烧灰化→6 mol·L-1硝酸溶解→过滤→检测滤
液中的铁元素。下列说法错误的是( )
A.“灼烧灰化”选用仪器①②③
B.④用于配制6 mol·L-1硝酸时需洗净、检查是否漏水,不需要烘干
C.“过滤”时需沿②向⑤中转移液体
D.检测铁元素时,⑥悬垂于⑦的上方滴加KSCN溶液
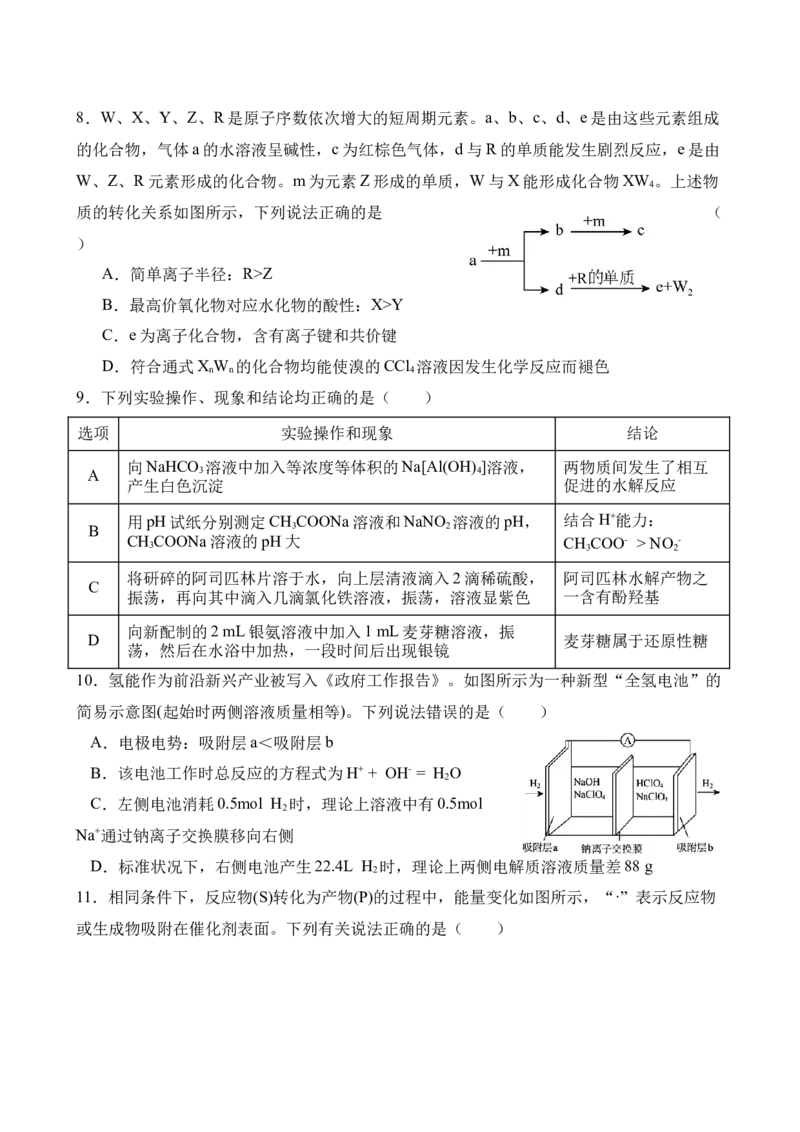
6.化合物 是一种药物合成中间体,其合成方法如下:
下列有关说法错误的是( )
A.X分子中没有手性碳原子 B.Y最多能与5mol NaOH反应
C.Z能与甲醛发生缩聚反应 D.X可以发生氧化反应和还原反应
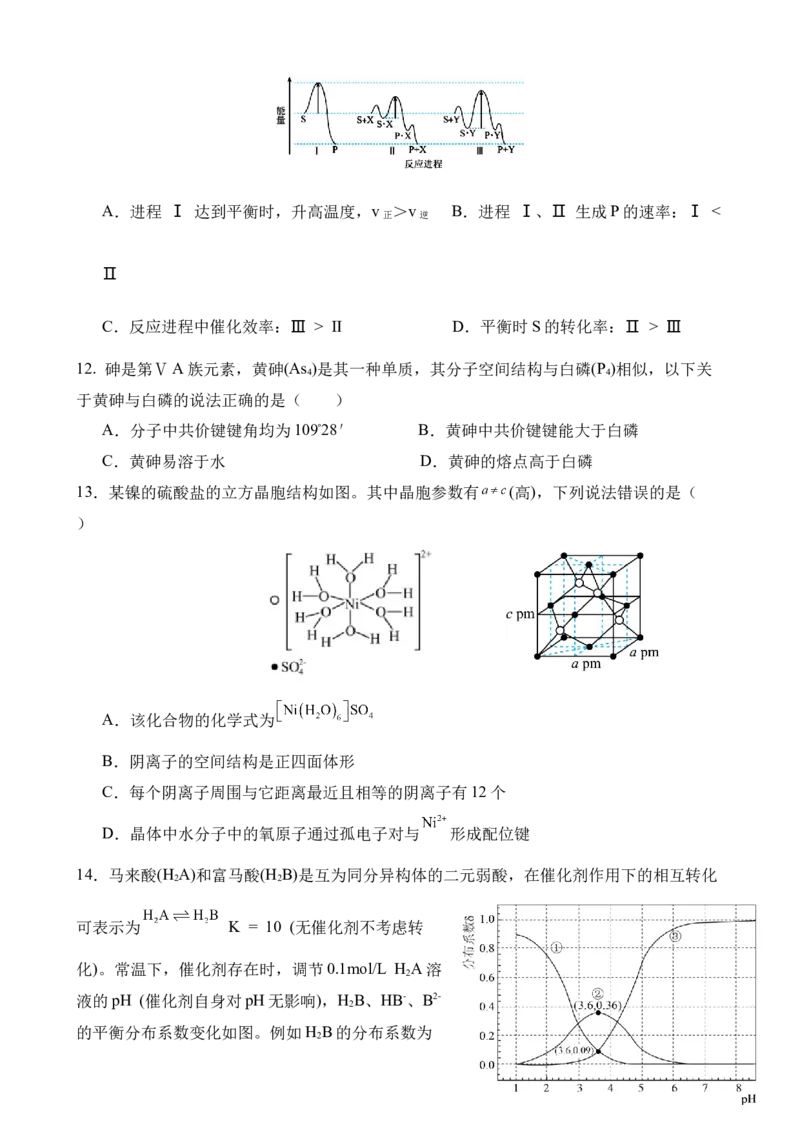
7.为有效地将粗金泥(主要成分为Au,含少量Ag)中的金、银分离,提高贵金属的回收率,
设计如下工艺流程:
已知:酸浸后银以AgCl存在于王水分金渣中,有少量未被溶解的金被AgCl包覆。
下列说法错误的是( )
A.“酸浸”中,盐酸的作用是提高硝酸的氧化性
B.“氨浸”中,发生反应
C.物质a为Au
D.葡萄糖与 [Ag(NH ) ]+ 恰好反应时,物质的量之比为1 : 2
3 28.W、X、Y、Z、R是原子序数依次增大的短周期元素。a、b、c、d、e是由这些元素组成
的化合物,气体a的水溶液呈碱性,c为红棕色气体,d与R的单质能发生剧烈反应,e是由
W、Z、R元素形成的化合物。m为元素Z形成的单质,W与X能形成化合物XW 。上述物
4
质的转化关系如图所示,下列说法正确的是 (
)
A.简单离子半径:R>Z
B.最高价氧化物对应水化物的酸性:X>Y
C.e为离子化合物,含有离子键和共价键
D.符合通式X W 的化合物均能使溴的CCl 溶液因发生化学反应而褪色
n n 4
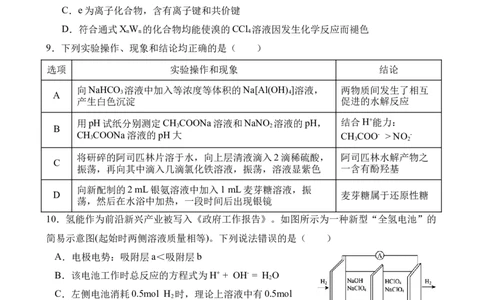
9.下列实验操作、现象和结论均正确的是( )
选项 实验操作和现象 结论
向NaHCO 溶液中加入等浓度等体积的Na[Al(OH) ]溶液, 两物质间发生了相互
A 3 4
产生白色沉淀 促进的水解反应
用pH试纸分别测定CH COONa溶液和NaNO 溶液的pH, 结合H+能力:
B 3 2
CH COONa溶液的pH大 CH COO- > NO -
3 3 2
将研碎的阿司匹林片溶于水,向上层清液滴入2滴稀硫酸, 阿司匹林水解产物之
C
振荡,再向其中滴入几滴氯化铁溶液,振荡,溶液显紫色 一含有酚羟基
向新配制的2 mL银氨溶液中加入1 mL麦芽糖溶液,振
D 麦芽糖属于还原性糖
荡,然后在水浴中加热,一段时间后出现银镜
10.氢能作为前沿新兴产业被写入《政府工作报告》。如图所示为一种新型“全氢电池”的
简易示意图(起始时两侧溶液质量相等)。下列说法错误的是( )
A.电极电势:吸附层a<吸附层b
B.该电池工作时总反应的方程式为H+ + OH- = H O
2
C.左侧电池消耗0.5mol H 时,理论上溶液中有0.5mol
2
Na+通过钠离子交换膜移向右侧
D.标准状况下,右侧电池产生22.4L H 时,理论上两侧电解质溶液质量差88 g
2
11.相同条件下,反应物(S)转化为产物(P)的过程中,能量变化如图所示,“·” 表示反应物
或生成物吸附在催化剂表面。下列有关说法正确的是( )A.进程 Ⅰ 达到平衡时,升高温度,v >v B.进程 Ⅰ、Ⅱ 生成P的速率:Ⅰ <
正 逆
Ⅱ
C.反应进程中催化效率:Ⅲ > Ⅱ D.平衡时S的转化率:Ⅱ > Ⅲ
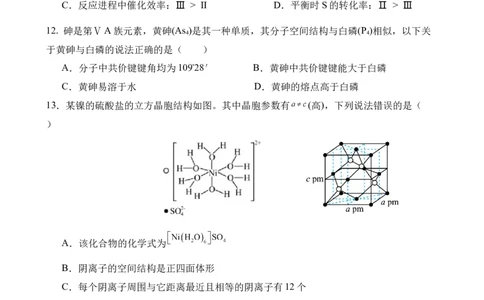
12. 砷是第ⅤA族元素,黄砷(As )是其一种单质,其分子空间结构与白磷(P )相似,以下关
4 4
于黄砷与白磷的说法正确的是( )
A.分子中共价键键角均为109º28′ B.黄砷中共价键键能大于白磷
C.黄砷易溶于水 D.黄砷的熔点高于白磷
13.某镍的硫酸盐的立方晶胞结构如图。其中晶胞参数有 (高),下列说法错误的是(
)
A.该化合物的化学式为
B.阴离子的空间结构是正四面体形
C.每个阴离子周围与它距离最近且相等的阴离子有12个
D.晶体中水分子中的氧原子通过孤电子对与 形成配位键
14.马来酸(H A)和富马酸(H B)是互为同分异构体的二元弱酸,在催化剂作用下的相互转化
2 2
可表示为 K = 10 (无催化剂不考虑转
化)。常温下,催化剂存在时,调节0.1mol/L H A溶
2
液的pH (催化剂自身对pH无影响),H B、HB-、B2-
2
的平衡分布系数变化如图。例如H B的分布系数为
2。下列说法错误的是( )
A.
B.无催化剂存在时,NaHB溶液显酸性
C.常温下,有催化剂存在时,任意 下 、 都为定值
D.Na A溶液中加入催化剂后,溶液碱性减弱
2
二、非选择题:本题共4小题,共58分。
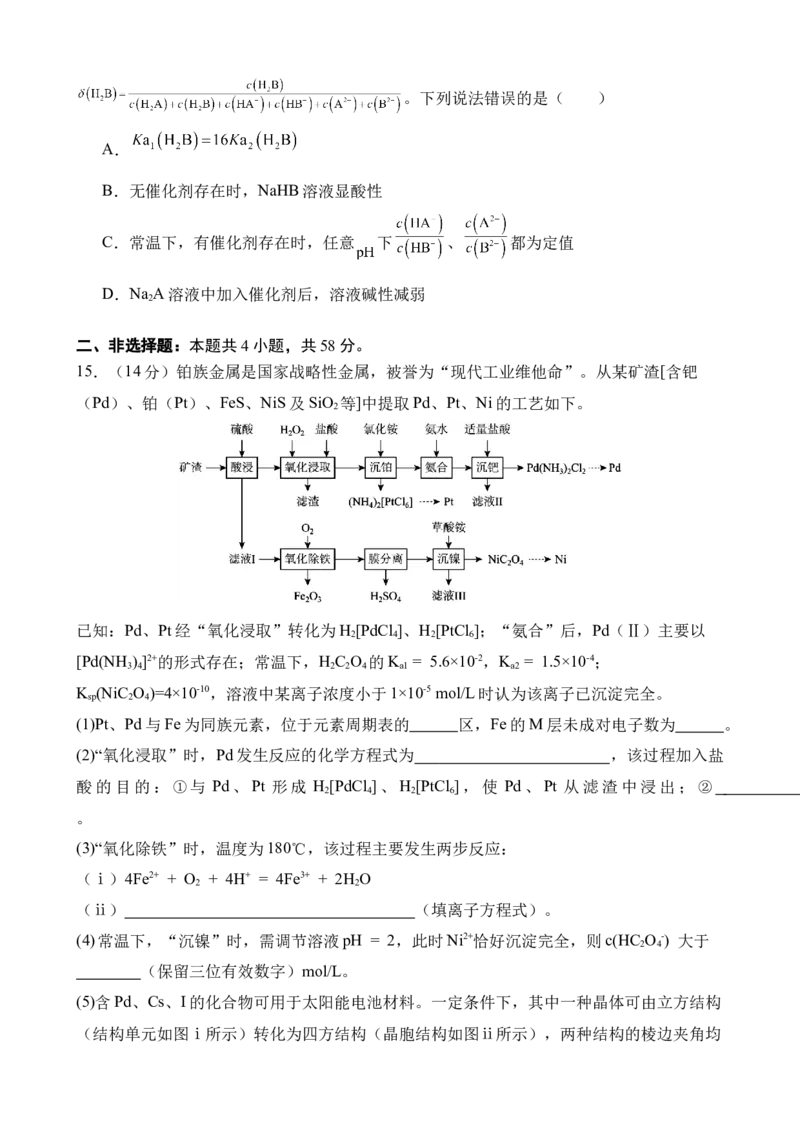
15.(14分)铂族金属是国家战略性金属,被誉为“现代工业维他命”。从某矿渣[含钯
(Pd)、铂(Pt)、FeS、NiS及SiO 等]中提取Pd、Pt、Ni的工艺如下。
2
已知:Pd、Pt经“氧化浸取”转化为H [PdCl ]、H [PtCl ];“氨合”后,Pd(Ⅱ)主要以
2 4 2 6
[Pd(NH ) ]2+的形式存在;常温下,H C O 的K = 5.6×10-2,K = 1.5×10-4;
3 4 2 2 4 a1 a2
K (NiC O )=4×10-10,溶液中某离子浓度小于1×10-5 mol/L时认为该离子已沉淀完全。
sp 2 4
(1)Pt、Pd与Fe为同族元素,位于元素周期表的 区,Fe的M层未成对电子数为 。
(2)“氧化浸取”时,Pd发生反应的化学方程式为 ,该过程加入盐
酸的目的:①与 Pd、Pt 形成 H [PdCl ]、H [PtCl ],使 Pd、Pt 从滤渣中浸出;②
2 4 2 6
。
(3)“氧化除铁”时,温度为180℃,该过程主要发生两步反应:
(ⅰ)4Fe2+ + O + 4H+ = 4Fe3+ + 2H O
2 2
(ⅱ) (填离子方程式)。
(4)常温下,“沉镍”时,需调节溶液pH = 2,此时Ni2+恰好沉淀完全,则c(HC O -) 大于
2 4
(保留三位有效数字)mol/L。
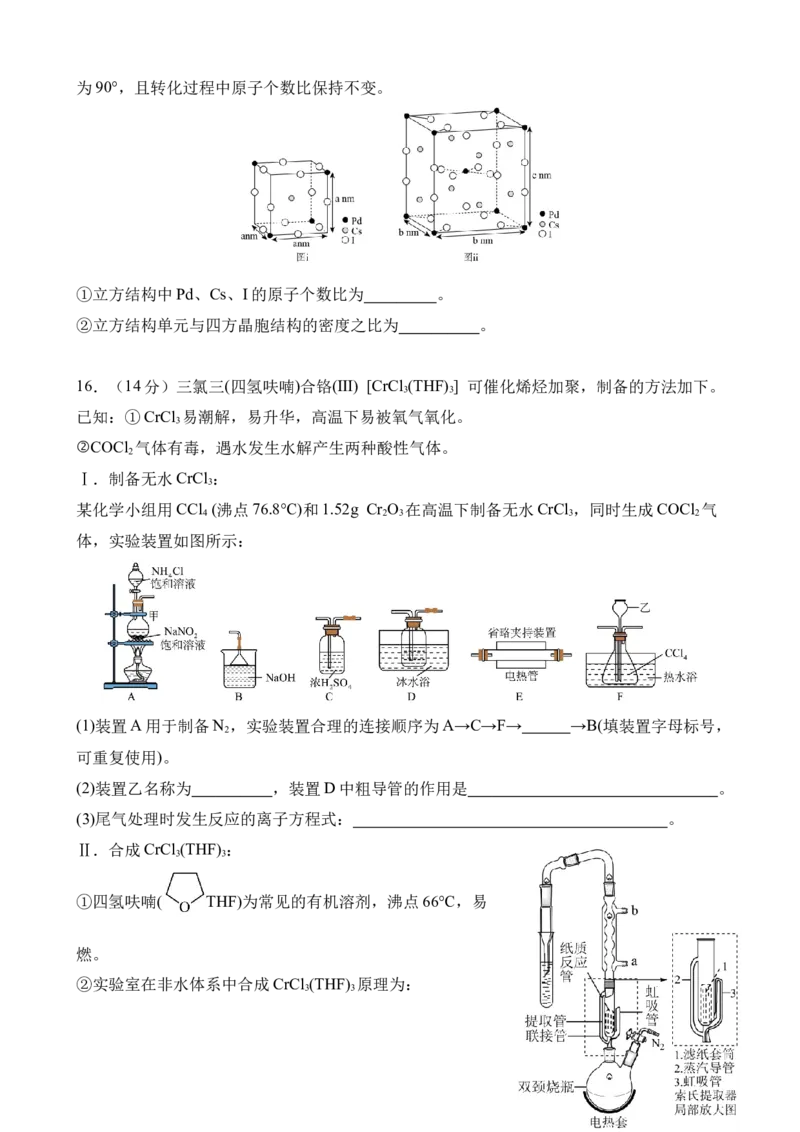
(5)含Pd、Cs、I的化合物可用于太阳能电池材料。一定条件下,其中一种晶体可由立方结构
(结构单元如图ⅰ所示)转化为四方结构(晶胞结构如图ⅱ所示),两种结构的棱边夹角均为90°,且转化过程中原子个数比保持不变。
①立方结构中Pd、Cs、I的原子个数比为 。
②立方结构单元与四方晶胞结构的密度之比为 。
16.(14分)三氯三(四氢呋喃)合铬(Ⅲ) [CrCl (THF) ] 可催化烯烃加聚,制备的方法加下。
3 3
已知:①CrCl 易潮解,易升华,高温下易被氧气氧化。
3
②COCl 气体有毒,遇水发生水解产生两种酸性气体。
2
Ⅰ.制备无水CrCl :
3
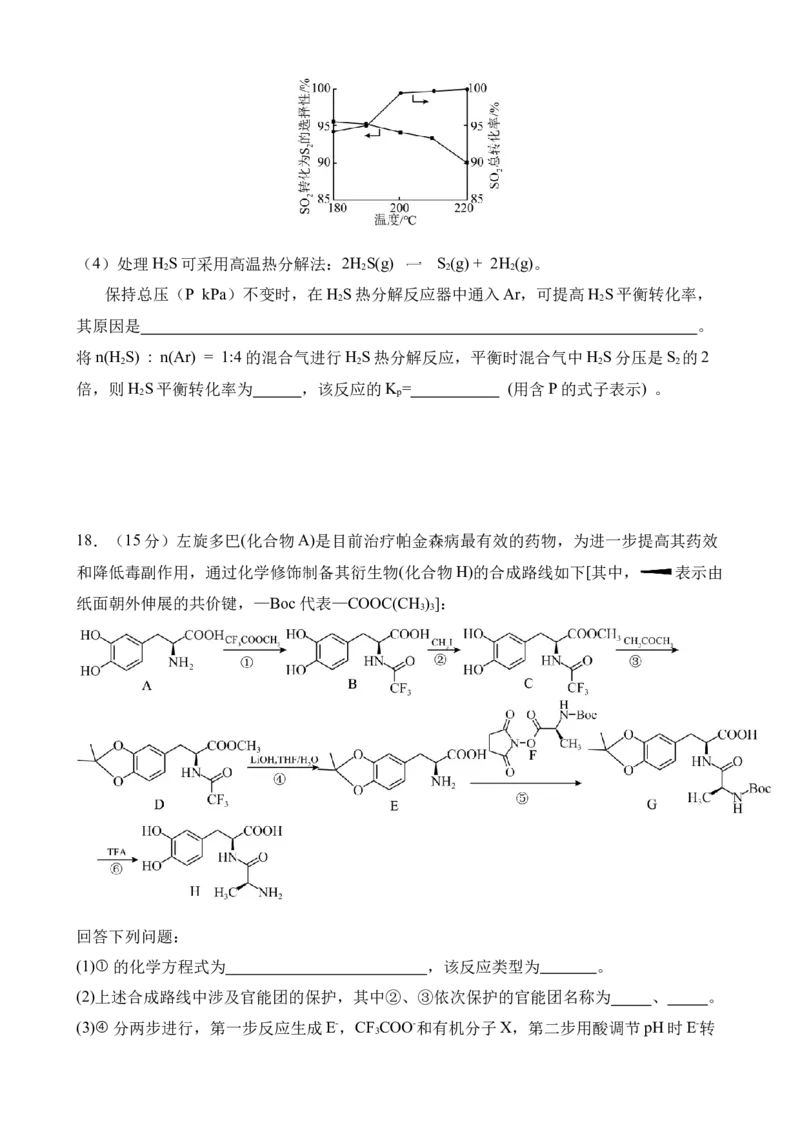
某化学小组用CCl (沸点76.8℃)和1.52g Cr O 在高温下制备无水CrCl ,同时生成COCl 气
4 2 3 3 2
体,实验装置如图所示:
(1)装置A用于制备N ,实验装置合理的连接顺序为A→C→F→ →B(填装置字母标号,
2
可重复使用)。
(2)装置乙名称为 ,装置D中粗导管的作用是 。
(3)尾气处理时发生反应的离子方程式: 。
Ⅱ.合成CrCl (THF) :
3 3
①四氢呋喃( THF)为常见的有机溶剂,沸点66℃,易
燃。
②实验室在非水体系中合成CrCl (THF) 原理为:
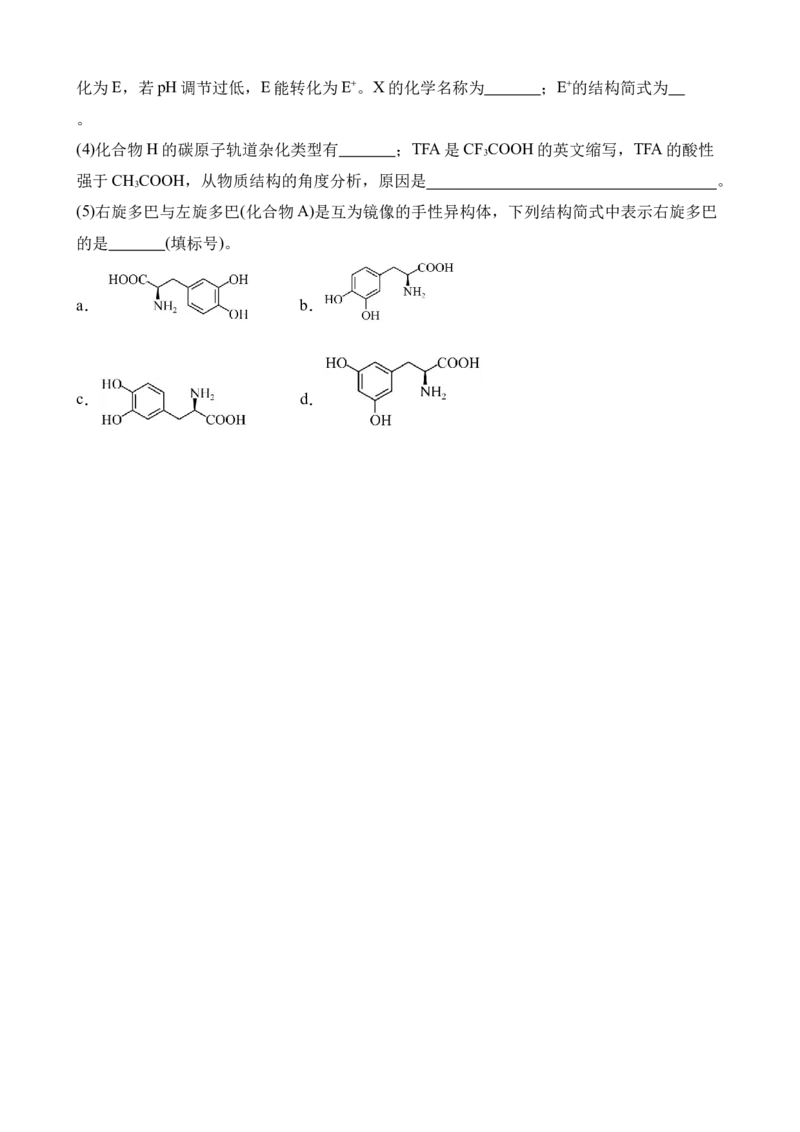
3 3实验操作:按如图组装仪器,将步骤 Ⅰ 所得无水CrCl 和0.15g锌粉放入滤纸套筒内,双
3
颈烧瓶中加入100mL无水四氢呋喃(THF),通N 5min后关闭,接通冷却水,加热四氢呋喃
2
至沸腾,在索氏提取器中发生反应,回流2.5h后再通入N 冷却至室温;取下双颈烧瓶,在
2
通风橱中蒸发至有较多固体析出,冷却、抽滤、干燥后称量即得产品4.50g。
(4)该反应不能使用明火加热的原因 。
(5)产品沿索氏提取器的管 (2或3) 流回双颈烧瓶。
(6)实验所用的四氢呋喃需进行无水处理,下列可以除去四氢呋喃中少量水分的试剂是 。
A.金属钠 B.浓硫酸 C.具有吸水能力的分子筛
(7)产品产率为 %(结果保留整数)[已知:Cr O 的摩尔质量为152 g/mol;
2 3
CrCl (THF) 的摩尔质量为374.5 g/mol]。
3 3
17.(15分)天然气净化厂和石油化工厂均需要处理过程气中的SO 、H S,以实现硫资源
2 2
的高效回收和含硫污染物的减排。
(1)一般采用选择性加氢催化剂处理SO ,将其转化为单质硫,主要发生以下反应:
2
反应Ⅰ:2SO (g) + 4H (g) S (g) + 4H O(g)
2 2 2 2
反应Ⅱ:SO (g) + 3H (g) H S(g) + 2H O(g) , ∆S = - 58 J/(mol·K)
2 2 2 2
则反应Ⅲ:2SO (g) + 4H S(g) 3S (g) + 4H O(g) 的 ,反应Ⅱ自发进行的
2 2 2 2
温度范围是 K。(结果保留整数)
(2)理论上分析,用反应Ⅰ、Ⅱ处理SO 时,下列措施中能提高SO 的平衡转化率,同时
2 2
加快反应速率的是 。
A.升高温度 B.降低温度 C.增大压强 D.增大H 的浓度
2
(3)下图表示反应温度对选择性加氢催化剂活性的影响判断SO 加氢转化为S 的最佳温度
2 2
为 ,理由是 。(4)处理H S可采用高温热分解法:2H S(g) S (g) + 2H (g)。
2 2 2 2
保持总压(P kPa)不变时,在H S热分解反应器中通入Ar,可提高H S平衡转化率,
2 2
其原因是 。
将n(H S) : n(Ar) = 1:4的混合气进行H S热分解反应,平衡时混合气中H S分压是S 的2
2 2 2 2
倍,则H S平衡转化率为 ,该反应的K = (用含P的式子表示) 。
2 p
18.(15分)左旋多巴(化合物A)是目前治疗帕金森病最有效的药物,为进一步提高其药效
和降低毒副作用,通过化学修饰制备其衍生物(化合物H)的合成路线如下[其中, 表示由
纸面朝外伸展的共价键,—Boc代表—COOC(CH ) ]:
3 3
回答下列问题:
(1)①的化学方程式为 ,该反应类型为 。
(2)上述合成路线中涉及官能团的保护,其中②、③依次保护的官能团名称为 、 。
(3)④分两步进行,第一步反应生成E-,CF COO-和有机分子X,第二步用酸调节pH时E-转
3化为E,若pH调节过低,E能转化为E+。X的化学名称为 ;E+的结构简式为
。
(4)化合物H的碳原子轨道杂化类型有 ;TFA是CF COOH的英文缩写,TFA的酸性
3
强于CH COOH,从物质结构的角度分析,原因是 。
3
(5)右旋多巴与左旋多巴(化合物A)是互为镜像的手性异构体,下列结构简式中表示右旋多巴
的是 (填标号)。
a. b.
c. d.