文档内容
2025届第一次联合模拟考试
参加学校: 京师荟成学校 燕岭学校
化学 ����答案
【答案】
1. 2. 3. 4. 5. 6. 7.
8. 9. 10. 11. 12. 13. 14.
𝐵𝐵 𝐵𝐵 𝐶𝐶 𝐵𝐵 𝐵𝐵 𝐵𝐵 𝐴𝐴
15. 16.
𝐶𝐶 𝐶𝐶 𝐶𝐶 𝐶𝐶 𝐶𝐶 𝐵𝐵 𝐴𝐴
17. 三颈烧瓶 或三口烧瓶
𝐴𝐴 𝐵𝐵
(1) ( )
(2)𝐵𝐵
、
(3)5
重结晶
(4)𝐶𝐶𝑙𝑙2 𝐶𝐶𝑂𝑂2
(5)①𝐶𝐶 ②
(6)80%
18. 搅拌、适当增加硫酸浓度、适当加热等;
、 ; ;温度过低,硫的溶解速率小,温
(1)
度过高, 易挥发;
(2)𝑆𝑆𝑆𝑆𝑂𝑂2 𝑆𝑆 𝐶𝐶𝑢𝑢2𝑆𝑆+2𝑀𝑀𝑀𝑀𝑂𝑂2+4𝐻𝐻2𝑆𝑆𝑂𝑂4 =2𝑀𝑀𝑀𝑀𝑆𝑆𝑂𝑂4+2𝐶𝐶𝑢𝑢𝑆𝑆𝑂𝑂4+4𝐻𝐻2𝑂𝑂+𝑆𝑆
; ;
𝐶𝐶𝑆𝑆2
−11 ;
(3)3.7⩽𝑝𝑝𝐻𝐻 <5.6 4.0×10 𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿
2+ −~ 都对 ; +
(4)𝑀𝑀𝑀𝑀 +𝐻𝐻𝐶𝐶𝑂𝑂3 +𝑁𝑁𝐻𝐻3 =𝑀𝑀𝑀𝑀𝐶𝐶𝑂𝑂3 ↓+𝑁𝑁𝐻𝐻4
1(59). 96.6%(9 6 . 5% 9 6.6 % ) 变小
0.4
20. −31羟7基.1乙酸24 0 𝐶𝐶 𝑎𝑎𝑎𝑎 𝑚𝑚𝑚𝑚𝑙𝑙/(𝐿𝐿⋅𝑠𝑠) 0.7𝑎𝑎
(1)
(2)
加成反应、还原反应
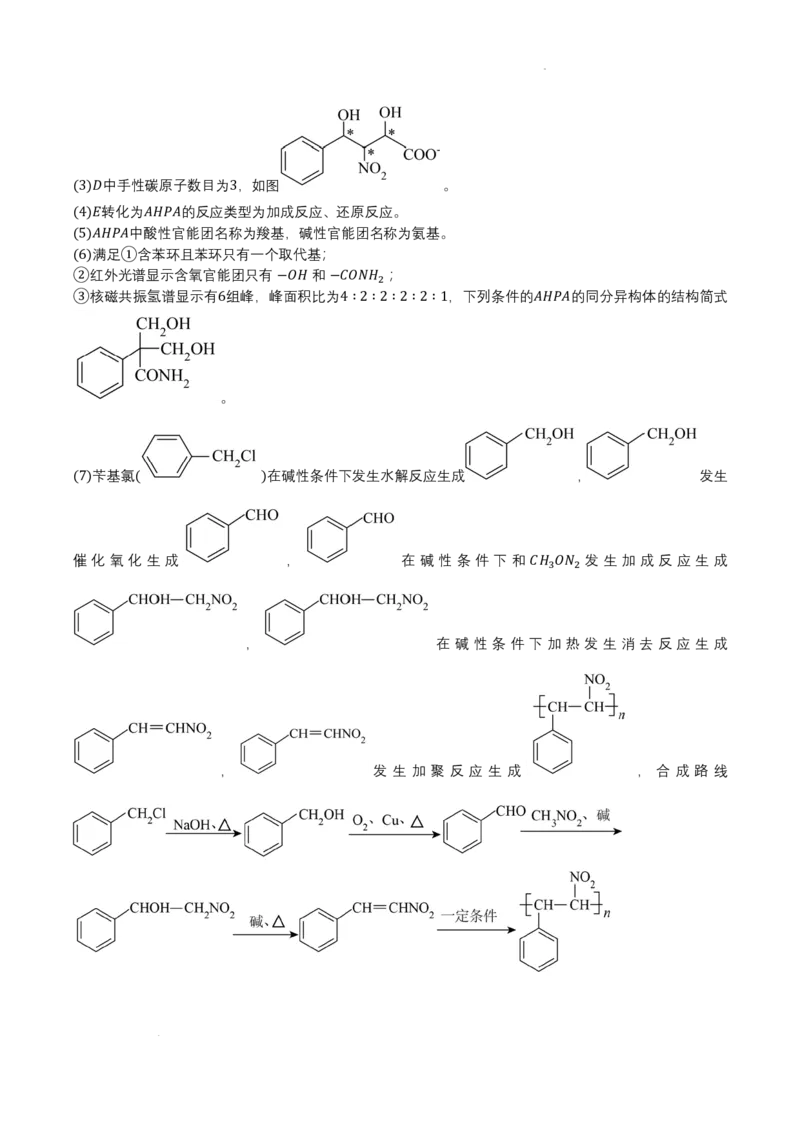
(3)3
羧基;氨基
(4)
(5)
(6)
(7)
学科网(北京)股份有限公司【解析】
1. 解: 皇后之玺玉印,玉的主要成分为硅酸盐,故A错误;
B.青铜为铜与锡等的合金,故B正确;
𝐴𝐴.
C.端砚的主要成分是水云母石,还含有少量石英颗粒,不属于合金,故C错误;
D.素纱禅衣中莎主要成分为蚕丝,属于有机高分子化合物,不是合金,故D错误;
故选: 。
由两种或两种以上的金属 或金属与非金属 熔合而成的具有金属特性的物质为合金。
𝐵𝐵
本题考查了物质的组成,熟悉合金的概念即可解答,题目简单。
( )
2. A.尼龙是聚酰胺纤维 锦纶 ,是有机合成高分子材料,A正确;
B.光伏发电是将太阳能转变为电能,B错误;
( )
C.石墨烯为碳的同素异形体,是新型无机非金属材料,C正确;
D.在出火口格栅涂碱金属,可看到黄色火焰,利用的是焰色反应原理让火焰可视化,D正确;
故选B。
3. A.铝热反应焊接铁轨是铝与氧化铁反应生成铁和氧化铝,发生了置换反应,选项A错误;
B.在钢铁部件表面进行钝化处理过程中生成新物质,属于化学变化,选项B错误;
C.在木材上雕刻花纹的过程主要发生物理变化,没有新物质生成,不是化学变化,选项C正确;
D.杂草腐烂属于化学变化,选项D错误;
答案选C。
4. 解: 是 号元素,位于元素周期表第四周期第Ⅷ族,故A正确;
B.由富马酸分子的比例模型可知,富马酸的结构简式为 ,单键为 键,双键含有 个 键、
𝐴𝐴.𝐹𝐹𝐹𝐹 26
个 键,分子中 键有 个、 键有 个,则分子中 键和 键的数目比为 : ,故B错误;
𝐻𝐻𝑂𝑂𝑂𝑂𝐶𝐶𝐶𝐶𝐻𝐻 =𝐶𝐶𝐻𝐻𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝜎𝜎 1 𝜎𝜎
C.元素的非金属性越强电负性越大,即电负性大小顺序为 ,故C正确;
1 𝜋𝜋 𝜎𝜎 11 𝜋𝜋 3 𝜎𝜎 𝜋𝜋 11 3
D.分子中 个羧基与 溶液反应生成 , 富马酸与足量 溶液反应可生成 ,故D
𝑂𝑂 >𝐶𝐶 >𝐻𝐻
正确;
2 𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 𝐶𝐶𝑂𝑂2 1𝑚𝑚𝑚𝑚𝑙𝑙 𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 2𝑚𝑚𝑚𝑚𝑙𝑙𝐶𝐶𝑂𝑂2
故选: 。
A. 是 号元素;
𝐵𝐵
B.富马酸的结构简式为 ,单键为 键,双键含有 个 键、 个 键;
𝐹𝐹𝐹𝐹 26
C.元素的非金属性越强,其电负性越大;
𝐻𝐻𝑂𝑂𝑂𝑂𝐶𝐶𝐻𝐻=𝐻𝐻𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝜎𝜎 1 𝜎𝜎 1 𝜋𝜋
D.分子中羧基与 溶液反应生成 。
本题以富马酸的结构模型为载体,考查有机物的结构与性质、元素周期律、化学键等,关键是明确富马酸的
𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 𝐶𝐶𝑂𝑂2
结构简式,题目侧重考查学生对基础知识的掌握情况。
5. 解: 该分子中 、 、 、 原子个数依次是 、 、 、 ,分子式为 ,故A错误;
B.醇羟基和氨基都是亲水基,该物质可以溶于水,故B正确;
𝐴𝐴. 𝐶𝐶 𝐻𝐻 𝑁𝑁 𝑂𝑂 9 11 3 5 𝐶𝐶9𝐻𝐻11𝑁𝑁3𝑂𝑂5
C.含氧官能团有羟基、醚键、酰胺基,不含羰基,故C错误;
D.连接 个原子或原子团的碳原子为手性碳原子,五元环中 个碳原子是手性碳原子,故D错误;
故选: 。
4 4
A.该分子中 、 、 、 原子个数依次是 、 、 、 ;
𝐵𝐵
B.醇羟基和氨基都是亲水基;
𝐶𝐶 𝐻𝐻 𝑁𝑁 𝑂𝑂 9 11 3 5
C.含氧官能团有羟基、醚键、酰胺基;
D.连接 个原子或原子团的碳原子为手性碳原子。
本题考查有机物的结构和性质,侧重考查基础知识的掌握和灵活运用能力,明确官能团及其性质的关系是
4
解本题关键,题目难度不大。
6. A.向 溶液中滴加 的浓氨水形成难溶物氢氧化铜,继续滴加至刚开始产生的沉
淀溶解生成四氨合铜离子,再加入极性较小的溶剂,并用玻璃棒摩擦试管壁,析出深蓝色的晶体,其成分是
4𝑚𝑚𝐿𝐿 0.1𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿 𝐶𝐶𝑢𝑢𝑆𝑆𝑂𝑂4 1𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿
学科网(北京)股份有限公司,A正确;
B.钠的焰色呈黄色,可能为氢氧化钠,不能确定该溶液一定是钠盐,B错误;
[𝐶𝐶𝑢𝑢(𝑁𝑁𝐻𝐻3)4]𝑆𝑆𝑂𝑂4·𝐻𝐻2𝑂𝑂
C.取两支试管,分别加入 溶液,将其中的一支试管先加热,加热后溶液变为黄绿色,
2 𝑚𝑚𝐿𝐿 0.5𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿 𝐶𝐶𝑢𝑢𝐶𝐶𝑙𝑙2
放入冷水中,又变为蓝绿色,说明 ,C正确;
D.酯可以在酸性和碱性条件下发生水解反应, 溶液的试管中酯层消失的时间更短,说明碱性条件下氢
氧化钠中和了水解反应生成的酸,使平衡正向移动,乙酸乙酯在碱性条件下水解速率更快,D正确;
𝑁𝑁𝑎𝑎𝑂𝑂𝐻𝐻
故选B。
7. 【分析】
本题考查化学平衡,题目难度中等,掌握外界条件改变对化学平衡的影响是解题的关键。
【解答】
A. 时, 选择性和 选择性均接近 ,则副反应Ⅱ 进行程度很小,故A
正确;
800℃ 𝐻𝐻2 𝐶𝐶𝑂𝑂 100% 𝐶𝐶𝐻𝐻4+2𝑂𝑂2 ⇌𝐶𝐶𝑂𝑂2+2𝐻𝐻2𝑂𝑂
B.在 时,甲烷的转化率为 ,即 , 的选择性为 ,即 ,
𝑛𝑛(𝐶𝐶𝐶𝐶)+𝑛𝑛(𝐶𝐶𝐶𝐶2) 𝑛𝑛(𝐶𝐶𝐶𝐶)
700℃, ,0故.8 B错误;2𝑚𝑚 𝑚𝑚𝑚𝑚 =0.8 𝐶𝐶𝑂𝑂 0.9 𝑛𝑛(𝐶𝐶𝐶𝐶)+𝑛𝑛(𝐶𝐶𝐶𝐶2)=0.9 𝑀𝑀(𝐶𝐶𝑂𝑂)=
C. 、 的选择性随温度升高而增大,则反应Ⅰ的 ,又因为反应Ⅰ的 ,反应Ⅰ在高温下自发,
1.44𝑚𝑚𝑚𝑚𝑙𝑙 𝑀𝑀(𝐶𝐶𝑂𝑂2)=0.16𝑚𝑚𝑚𝑚𝑙𝑙
故C错误;
𝐻𝐻2 𝐶𝐶𝑂𝑂 𝛥𝛥𝐻𝐻 >0 𝛥𝛥𝑆𝑆 >0
D.反应Ⅰ的 ,升高温度,平衡正向移动,有利于合成气的生成,故D错误。
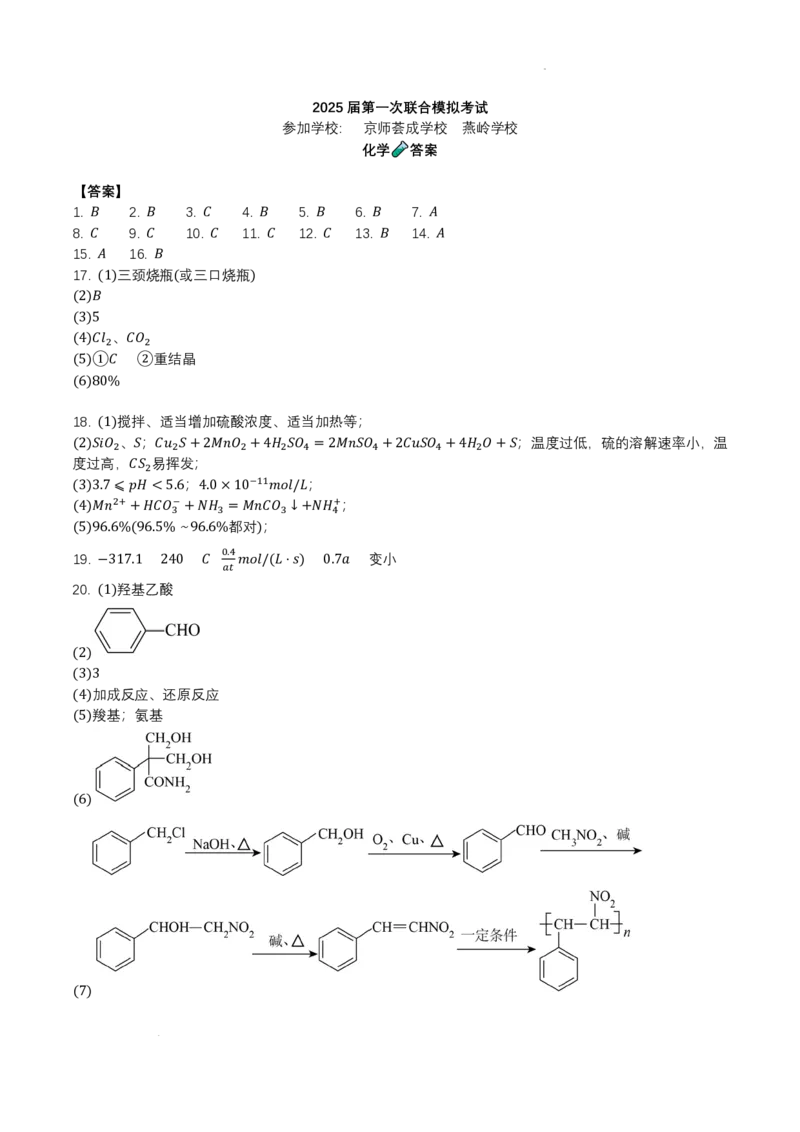
8. 每个 原子只能形成最多四个共价键,根据某烯烃分子中含有一个碳碳双键,一定条件下与氢气加成所得
𝛥𝛥𝐻𝐻 >0
𝐶𝐶
产物的结构式 可知,该烯烃可能的双键的位置有 ;共五种,
故选C。
9. A. 是固体,不能用 的浓度变化表示化学反应速率,故A错误;
B.根据表格数据, 下,可能在 内某一时刻反应刚好达到平衡状态,故B错误;
𝐵𝐵 𝐵𝐵
C.从表中可以看出 反应速率大于 ,所以 ,故C正确;
𝑇𝑇℃ 4∼6𝑚𝑚𝑆𝑆𝑀𝑀
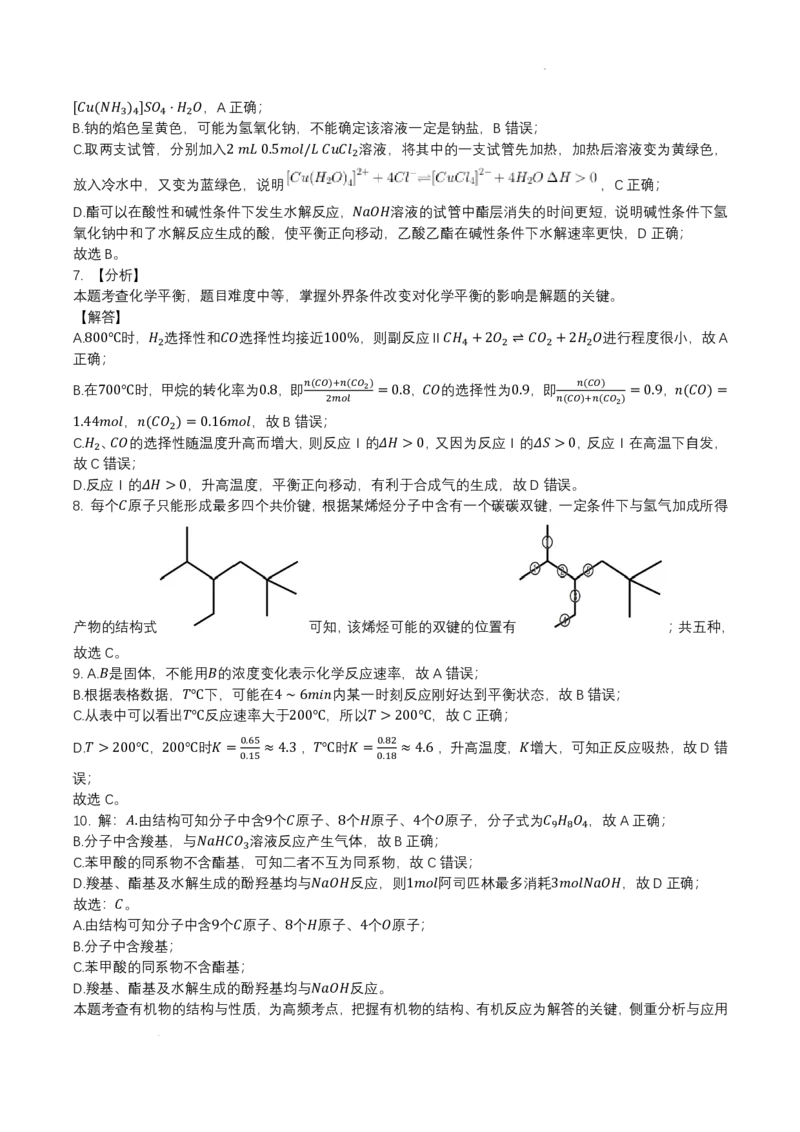
D. , 𝑇𝑇℃时 2 0,0℃ 时 𝑇𝑇 >200℃ ,升高温度, 增大,可知正反应吸热,故D错
0.65 0.82
误𝑇𝑇;> 200℃ 200℃ 𝐾𝐾 =0.15≈4.3 𝑇𝑇℃ 𝐾𝐾 =0.18≈4.6 𝐾𝐾
故选C。
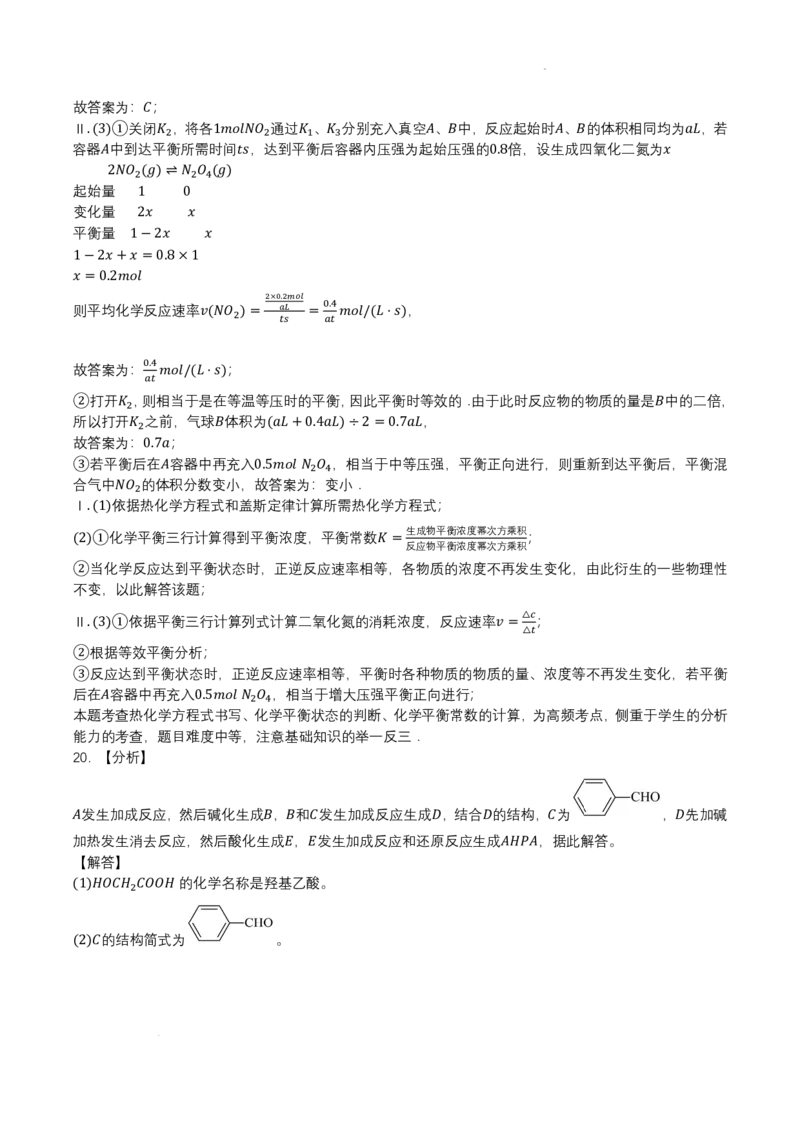
10. 解: 由结构可知分子中含 个 原子、 个 原子、 个 原子,分子式为 ,故A正确;
B.分子中含羧基,与 溶液反应产生气体,故B正确;
𝐴𝐴. 9 𝐶𝐶 8 𝐻𝐻 4 𝑂𝑂 𝐶𝐶9𝐻𝐻8𝑂𝑂4
C.苯甲酸的同系物不含酯基,可知二者不互为同系物,故C错误;
𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3
D.羧基、酯基及水解生成的酚羟基均与 反应,则 阿司匹林最多消耗 ,故D正确;
故选: 。
𝑁𝑁𝑎𝑎𝑂𝑂𝐻𝐻 1𝑚𝑚𝑚𝑚𝑙𝑙 3𝑚𝑚𝑚𝑚𝑙𝑙𝑁𝑁𝑎𝑎𝑂𝑂𝐻𝐻
A.由结构可知分子中含 个 原子、 个 原子、 个 原子;
𝐶𝐶
B.分子中含羧基;
9 𝐶𝐶 8 𝐻𝐻 4 𝑂𝑂
C.苯甲酸的同系物不含酯基;
D.羧基、酯基及水解生成的酚羟基均与 反应。
本题考查有机物的结构与性质,为高频考点,把握有机物的结构、有机反应为解答的关键,侧重分析与应用
𝑁𝑁𝑎𝑎𝑂𝑂𝐻𝐻
学科网(北京)股份有限公司能力的考查,注意选项D为解答的易错点,题目难度不大。
11. 解: 由分析可知, 气体为氢气、 气体为氯气,故A错误;
B.由分析可知,食盐水电解槽内发生的反应为电解饱和食盐水得到氯酸钠和氢气,氢由 价降低为 价,则
𝐴𝐴. 𝑎𝑎 𝑏𝑏
电解槽内每生成 氢气,转移电子的物质的量为 ,故B错误;
+1 0
C.由分析可知,氯酸钠溶液和盐酸在二氧化氯发生器中电解得到氯化钠、氯气、二氧化氯气体,阴极的电极
1𝑚𝑚𝑚𝑚𝑙𝑙 2𝑚𝑚𝑚𝑚𝑙𝑙
反应式为 ,故C正确;
D.没给具体的−温度压+强,无− 法计算氯气的体积,故D错误;
𝐶𝐶𝑙𝑙𝑂𝑂3 +2𝐻𝐻 +𝐹𝐹 =𝐶𝐶𝑙𝑙𝑂𝑂2 ↑+𝐻𝐻2𝑂𝑂
故选: 。
由题给流程可知,电解食盐水得到氯酸钠和氢气,则 为氢气;氯酸钠溶液和盐酸在二氧化氯发生器中电解
𝐶𝐶
得到氯化钠、氯气、二氧化氯气体,则 为氯气;氯气与氢气反应生成氯化氢;发生器中得到的氯化钠可与
𝑎𝑎
循环使用,提高原料的利用率。
𝑏𝑏
本题考查了电解池原理,为高频考点,侧重于学生的分析能力的考查,明确电解池阴阳极上的反应以及电子
守恒即可解答,注意电极反应式的书写,题目难度中等。
12. 解: 鸢尾酮中含 和 ,不饱和度为 ,其同分异构体可含苯环和酚 ,即 鸢尾酮可与某
种酚互为同分异构体,故A正确;
𝐴𝐴.𝛼𝛼 𝐶𝐶 =𝐶𝐶 𝐶𝐶 =𝑂𝑂 4 −𝑂𝑂𝐻𝐻 𝛼𝛼
B. 和 ,均与氢气发生加成反应,则 鸢尾酮最多可与 加成,故B正确;
C.不含 ,则不能发生银镜反应,故C错误;
𝐶𝐶 =𝐶𝐶 𝐶𝐶 =𝑂𝑂 1𝑚𝑚𝑚𝑚𝑙𝑙 𝛼𝛼 3𝑚𝑚𝑚𝑚𝑙𝑙 𝐻𝐻2
D. 加成为饱和烃结构, 加成生成醇,消去转化为烯烃再与氢气加成转化为饱和烃结构,碳链骨
−𝐶𝐶𝐻𝐻𝑂𝑂
𝐶𝐶 =𝐶𝐶 𝐶𝐶 =𝑂𝑂
架不变,则 鸢尾酮经加氢 消去 加氢可转变为 ,故D正确;
故选: 。 𝛼𝛼 → →
鸢尾酮中含 和 ,不饱和度为 ,结合烯烃、酮的性质来解答.
𝐶𝐶
本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酮、醛性
𝛼𝛼 𝐶𝐶 =𝐶𝐶 𝐶𝐶 =𝑂𝑂 4
质的考查,选项A为解答的难点,题目难度不大。
13. 【分析】
向 浓度均 的 逐滴加入浓度均为 的 , 不断减小, 不断增大,
−1 −1 −
20 𝑚𝑚𝐿𝐿 不1断.0 增𝑚𝑚𝑚𝑚大𝑙𝑙,⋅𝐿𝐿则对𝐻𝐻应𝐴𝐴曲线为 ;向 1.浓0 𝑚𝑚度𝑚𝑚均𝑙𝑙⋅𝐿𝐿 𝑁𝑁𝑎𝑎𝑂𝑂𝐻𝐻的𝑐𝑐(𝐻𝐻𝐴𝐴逐) 滴加入浓度𝑐𝑐(均𝐴𝐴为)
−
𝑐𝑐(𝐴𝐴 ) −1
𝑙𝑙𝑙𝑙𝑙𝑙=lg𝑐𝑐(𝐻𝐻𝐴𝐴) ① 20 𝑚𝑚𝐿𝐿 1.0 𝑚𝑚𝑚𝑚𝑙𝑙⋅𝐿𝐿 𝑁𝑁𝑎𝑎𝐴𝐴 1.0 𝑚𝑚𝑚𝑚𝑙𝑙⋅
的 , 不断增大, 不断减小, 不断增大,则对应曲线为 。
−1 − 𝑐𝑐(𝐻𝐻𝐴𝐴)
−
𝐿𝐿【解答𝐻𝐻】𝐶𝐶𝑙𝑙 𝑐𝑐(𝐻𝐻𝐴𝐴) 𝑐𝑐(𝐴𝐴 ) 𝑙𝑙𝑙𝑙𝑙𝑙=lg 𝑐𝑐(𝐴𝐴 ) ②
A. 时,在曲线 、 的交叉点, , , ,
− − +
𝑐𝑐(𝐴𝐴 ) 𝑐𝑐(𝐻𝐻𝐴𝐴) − 𝑐𝑐(𝐴𝐴 )⋅𝑐𝑐(𝐻𝐻 ) + −4.74
则2 5℃ 的数量①级为② ,A正确𝑐𝑐(𝐻𝐻;𝐴𝐴) = 𝑐𝑐(𝐴𝐴 − ) 𝑐𝑐(𝐻𝐻𝐴𝐴)=𝑐𝑐(𝐴𝐴 ) 𝐾𝐾𝑎𝑎(𝐻𝐻𝐴𝐴)= 𝑐𝑐(𝐻𝐻𝐴𝐴) =𝑐𝑐(𝐻𝐻 )=10
B.当 时, −5 ,对于曲线 : ,
𝐾𝐾𝑎𝑎(𝐻𝐻𝐴𝐴) 10
对于曲线 : − + + − − , 不−正确;
𝑝𝑝𝐻𝐻 =4.74 𝑐𝑐(𝐻𝐻𝐴𝐴)=𝑐𝑐(𝐴𝐴 ) ① 𝑐𝑐(𝐻𝐻 )+𝑐𝑐(𝑁𝑁𝑎𝑎 )=𝑐𝑐(𝑂𝑂𝐻𝐻 )+𝑐𝑐(𝐴𝐴 )=𝑐𝑐(𝑂𝑂𝐻𝐻 )+𝑐𝑐(𝐻𝐻𝐴𝐴)
C.由分析可知,曲线+ 表示向+ 浓度−均 − 的− 逐滴加−入浓度均为 − 的 ,则
② 𝑐𝑐(𝐻𝐻 )+𝑐𝑐(𝑁𝑁𝑎𝑎 )=𝑐𝑐(𝑂𝑂𝐻𝐻 )+𝑐𝑐(𝐴𝐴 )+𝑐𝑐(𝐶𝐶𝑙𝑙 )=𝑐𝑐(𝑂𝑂𝐻𝐻 )+𝑐𝑐(𝐻𝐻𝐴𝐴)+𝑐𝑐(𝐶𝐶𝑙𝑙 ) 𝐵𝐵
−1 −1
,C正确; ② 20 𝑚𝑚𝐿𝐿 1.0 𝑚𝑚𝑚𝑚𝑙𝑙⋅𝐿𝐿 𝑁𝑁𝑎𝑎𝐴𝐴 1.0 𝑚𝑚𝑚𝑚𝑙𝑙⋅𝐿𝐿 𝐻𝐻𝐶𝐶𝑙𝑙 𝑙𝑙 =
𝑐𝑐(𝐻𝐻𝐴𝐴)
−
𝑐𝑐(𝐴𝐴 )
D.当滴入体积 时, , ,所以 继续发生电离,此
−
𝐾𝐾𝑊𝑊
−9.26 −4.74
𝑉𝑉 =10𝑚𝑚𝐿𝐿 𝑐𝑐(𝐻𝐻𝐴𝐴)=𝑐𝑐(𝐴𝐴 ) 𝐾𝐾ℎ = 𝐾𝐾𝑎𝑎 =10 <𝐾𝐾𝑎𝑎 =10 𝐻𝐻𝐴𝐴
时 ,溶液 ,D正确;
−
𝑐𝑐(𝐴𝐴 )
lg𝑐𝑐(𝐻𝐻𝐴𝐴)>0 𝑝𝑝𝐻𝐻 >4.74
学科网(北京)股份有限公司故选B。
14. A.若用实验 和 ,若 , ,为保证总体积不变, ,除了温度不同,硫酸浓度也不
同,不能探究温度对反应速率的影响,A错误;
1 2 V1 =10.0 V3 =6.0 V3 =4.0
B.设计该实验的基本原理为在其他条件不变时,一个因素对反应速率的影响,即为控制变量法探究反应速率
的影响因素,B正确;
C.实验 和 ,温度相同,加入的硫代硫酸钠相同,硫酸不同,可探究稀硫酸浓度对该反应速率的影响,C正
确;
1 3
D. 对该反应不影响,所以若将水更换为 溶液,对实验结果无影响,D正确;
故选A。
Na2SO4 Na2SO4
15. 解:有机物和足量的钠反应生成氢气,该有机物中至少含有 、 中的一种,该有机物与
溶液反应生成 气体,说明该有机物一定含有 ,生成二氧化碳的体积与氢气的体积相等,根据
−𝑂𝑂𝐻𝐻 −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3
~ 、 ~ 、 ~ ~ ,可知 或 均与钠反
𝐶𝐶𝑂𝑂2 −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 2−
应可产生 , 与 反应可产生 ,故分子中 与 数目相等,选项
𝑂𝑂𝐻𝐻 𝐻𝐻2 ↑ 2−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝐻𝐻2 ↑ 2−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 2𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 2𝐶𝐶𝑂𝑂2 ↑ 2𝑚𝑚𝑚𝑚𝑙𝑙−𝑂𝑂𝐻𝐻 2𝑚𝑚𝑚𝑚𝑙𝑙−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻
中 符合,
1𝑚𝑚𝑚𝑚𝑙𝑙𝐻𝐻2 2𝑚𝑚𝑚𝑚𝑙𝑙−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 2𝑚𝑚𝑚𝑚𝑙𝑙𝐶𝐶𝑂𝑂2 −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 −𝑂𝑂𝐻𝐻
故选: 。
𝐶𝐶𝐻𝐻3𝐶𝐶𝐻𝐻(𝑂𝑂𝐻𝐻)𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻
有机物和足量的钠反应生成氢气,该有机物中至少含有 、 中的一种,该有机物与 溶液
𝐴𝐴
反应生成 气体,说明该有机物一定含有 ,生成二氧化碳的体积与氢气的体积相等,根据 ~
−𝑂𝑂𝐻𝐻 −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3
、 ~ 、 ~ ~ ,可知有机物只含有的 、 数目相等。
𝐶𝐶𝑂𝑂2 −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 2−𝑂𝑂𝐻𝐻
本题考查有机物的推断,关键是确定官能团的种类与数目,熟练掌握官能团的性质与转化,题目更适合利用
𝐻𝐻2 ↑ 2−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 𝐻𝐻2 ↑ 2−𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 2𝑁𝑁𝑎𝑎𝐻𝐻𝐶𝐶𝑂𝑂3 2𝐶𝐶𝑂𝑂2 ↑ −𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻 −𝑂𝑂𝐻𝐻
验证法进行解答,题目侧重考查学生分析推理能力、灵活运用知识的能力。
16. 【分析】
由电池放电时的反应可知, 化合价由 价变成 价,故是原电池的负极,复杂材料电极是正极。
【解答】
𝐿𝐿𝑆𝑆 0 +1
A.由以上分析可知,放电时, 电极作电池负极,有电子经导线流出,A正确;
B.充电时,阳极 变成二氧化碳,阴极 变成 ,故每转移 电子,消耗 质量为 ,生成
𝐿𝐿𝑆𝑆
质量为 ,故两电极的质量变化差值为+ ,B错误;
𝐶𝐶 𝐿𝐿𝑆𝑆 𝐿𝐿𝑆𝑆 1𝑚𝑚𝑚𝑚𝑙𝑙 0.25𝑚𝑚𝑚𝑚𝑙𝑙𝐶𝐶 3𝑙𝑙 1𝑚𝑚𝑚𝑚𝑙𝑙𝐿𝐿𝑆𝑆
C.充电时,阳极上 失电子变成二氧化碳,故阳极的电极反应式为 ,C正
7𝑙𝑙 3𝑙𝑙+7𝑙𝑙 =10𝑙𝑙
确; − +
𝐶𝐶 𝐶𝐶−4𝐹𝐹 +2𝐿𝐿𝑆𝑆2𝐶𝐶𝑂𝑂3 =3𝐶𝐶𝑂𝑂2 ↑+4𝐿𝐿𝑆𝑆
D. 碳纳米管是一种电导率高、比表面积大、通道和孔隙率丰富的导电基底,增加二氧化碳的吸收效率,
故可使该电池表现出优异的电化学性能,D正确;
𝐶𝐶𝑁𝑁𝑇𝑇𝑠𝑠
故选B。
17. 【分析】
环己醇加入高锰酸钾、碳酸钠水浴加热生成 和二氧化锰,过滤滤液加入盐酸酸化后、蒸
发浓缩、冷却结晶、减压过滤、洗涤干燥得到己二酸;
𝐾𝐾𝑂𝑂𝑂𝑂𝐶𝐶(𝐶𝐶𝐻𝐻2)4𝐶𝐶𝑂𝑂𝑂𝑂𝐾𝐾
【解答】
装置图中仪器 的名称为三颈烧瓶 或三口烧瓶 ;
“氧化”过程需要加热的温度低于 ,低于水的沸点,故选择水浴加热,选B;
(1) 𝐴𝐴 ( )
由图可知,实验过程中应选择的环己醇滴速为 滴 ,此时反应速率较平和,反应温度低于要求温度
(2) 50℃
;
(3) 5 /𝑚𝑚𝑆𝑆𝑀𝑀
“氧化液”含有碳酸钠、高锰酸钾,加浓盐酸酸化时,碳酸钠和盐酸生成二氧化碳、高锰酸钾和盐酸发生氧
50℃
化还原反应生产氯气,故推测该气体的成分有 、 ;
(4)
由图可知,己二酸晶体在低温时溶解度较小,此时洗涤损失较小,故“洗涤”的方法为 用冷水洗涤;
𝐶𝐶𝑙𝑙2 𝐶𝐶𝑂𝑂2
利用两者的溶解度不同,除去己二酸晶体中含有的氯化钠杂质通常采取的实验方法为重结晶法;
(5)① 𝐶𝐶.
②
学科网(北京)股份有限公司实验时称取 环己醇 ,最终得到纯净的己二酸 晶体 ,则该实
(验6)中己二酸的产10率.0为𝑙𝑙 (𝑀𝑀 =100𝑙𝑙/𝑚𝑚𝑚𝑚𝑙𝑙) 。 (𝑀𝑀 =146𝑙𝑙/𝑚𝑚𝑚𝑚𝑙𝑙) 11.68𝑙𝑙
11.68𝑔𝑔
10.0𝑔𝑔
100𝑔𝑔/𝑚𝑚𝑚𝑚𝑚𝑚×146𝑔𝑔/𝑚𝑚𝑚𝑚𝑚𝑚×100%=80%
18. 【分析】
本题考查物质的制备流程,侧重考查实验操作和原理,离子方程式书写, 计算和物质含量的计算,难度
一般,分析物质转化流程为解题关键。
𝐾𝐾𝑠𝑠𝑠𝑠
【解答】
根据影响化学反应速率的因素可知,为加快反应速度,可采取的方法有搅拌、适当增加硫酸浓度、适当
加热等;
(1)
二氧化锰有较强的氧化性,可将辉铜矿中的硫元素氧化为单质硫,单质硫易溶于二硫化碳,则滤渣 的主
要成分为 、 ,“浸取”过程中 被氧化的化学方程式为:
(2) 𝐼𝐼
,温度过低,硫的溶解速率小,温度过高, 易挥发;
𝑆𝑆𝑆𝑆𝑂𝑂2 𝑆𝑆 𝐶𝐶𝑢𝑢2𝑆𝑆 𝐶𝐶𝑢𝑢2𝑆𝑆+2𝑀𝑀𝑀𝑀𝑂𝑂2+4𝐻𝐻2𝑆𝑆𝑂𝑂4 =2𝑀𝑀𝑀𝑀𝑆𝑆𝑂𝑂4+
加入氧化铜,消耗酸, 升高,使溶液中 沉淀完全,而铜离子不沉淀,则 范围是 ,
2𝐶𝐶𝑢𝑢𝑆𝑆𝑂𝑂4+4𝐻𝐻2𝑂𝑂+𝑆𝑆 𝐶𝐶𝑆𝑆2
3+
(将3)溶液的 调为 ,则溶𝑝𝑝𝐻𝐻液中 𝐹𝐹𝐹𝐹 , ,𝑝𝑝𝐻𝐻 3.7≤𝑝𝑝𝐻𝐻 <5.6
−38
+ −5 − −9 3+ 4.0×10
−9 3
𝑝𝑝𝐻𝐻; 5 𝑐𝑐(𝐻𝐻 )=10 𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿 𝑐𝑐(𝑂𝑂𝐻𝐻 )=10 𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿 𝑐𝑐(𝐹𝐹𝐹𝐹 )= (10 ) =4.0×
−沉11锰阶段,加入了碳酸氢铵和氨气,生成了碳酸根离子,进而生成碳酸锰沉淀,离子方程式为:
10 𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿
; 2+
(4) 𝑀𝑀𝑀𝑀 +
− 沉淀为硫酸钡,物质的+ 量为 ,则 溶液中含有 ,样品中含有
𝐻𝐻𝐶𝐶𝑂𝑂3 +𝑁𝑁𝐻𝐻3 =𝑀𝑀𝑀𝑀𝐶𝐶𝑂𝑂3 ↓+𝑁𝑁𝐻𝐻4
(5)4.66 𝑙𝑙 ,则此样品的纯0度.0为2𝑚𝑚𝑚𝑚𝑙𝑙 25.00𝑚𝑚𝐿𝐿 % 𝑀𝑀𝑀𝑀%𝑆𝑆𝑂𝑂。4 ·𝐻𝐻2𝑂𝑂 0.02𝑚𝑚𝑚𝑚𝑙𝑙
0.08𝑚𝑚𝑚𝑚𝑚𝑚×169𝑔𝑔/𝑚𝑚𝑚𝑚𝑚𝑚
1𝑀𝑀9𝑀𝑀. 𝑆𝑆解𝑂𝑂4:·𝐻𝐻Ⅰ2𝑂𝑂 0.08𝑚𝑚𝑚𝑚𝑙𝑙 14.00𝑔𝑔 ×100 ≈96.6
−1
.(1)①𝑁𝑁𝑂𝑂(𝑙𝑙)+𝑂𝑂3(𝑙𝑙)⇌𝑁𝑁𝑂𝑂2(𝑙𝑙)+𝑂𝑂2(𝑙𝑙)△𝐻𝐻 =−200.9𝑘𝑘𝑘𝑘.𝑚𝑚𝑚𝑚𝑙𝑙
得到 时,反应 −1的 ,
②2𝑁𝑁𝑂𝑂(𝑙𝑙)+𝑂𝑂2(𝑙𝑙)⇌2𝑁𝑁𝑂𝑂2(𝑙𝑙)△𝐻𝐻 =−116.2𝑘𝑘𝑘𝑘.𝑚𝑚𝑚𝑚𝑙𝑙
故答案为: ;
①+② 𝑇𝑇℃ 3𝑁𝑁𝑂𝑂 (𝑙𝑙)+𝑂𝑂3(𝑙𝑙)⇌3𝑁𝑁𝑂𝑂2(𝑙𝑙) △𝐻𝐻 =−317.1𝐾𝐾𝑘𝑘/𝑚𝑚𝑚𝑚𝑙𝑙
时,将 和 气体充入到 固定容积的恒温密闭容器中,图象分析可知平衡状态
−317.1
浓度为 , 达到平衡,
(2)①𝑇𝑇℃ 0.6𝑚𝑚𝑚𝑚𝑙𝑙 𝑁𝑁𝑂𝑂 0.2𝑚𝑚𝑚𝑚𝑙𝑙𝑂𝑂3 2𝐿𝐿
𝑁𝑁𝑂𝑂 0.1𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿 10𝑚𝑚𝑆𝑆𝑀𝑀
起始量
3𝑁𝑁𝑂𝑂(𝑙𝑙)+𝑂𝑂3(𝑙𝑙)⇌3𝑁𝑁𝑂𝑂2(𝑙𝑙)
变化量(𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿) 0.3 0 . 1 0
0.2
(𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿) 0.2 3 0.2
平衡量
0.1
.(𝑚𝑚𝑚𝑚𝑙𝑙/𝐿𝐿) 0.1 3 0.2
,
. 3
0 2
故𝐾𝐾 答=案0 为1 3 ×: 0 3 .1 =2;40
反应 的 ,反应是气体体积减小的放热反应,
240
A.气体颜色不再改变,说明二氧化氮浓度不变,反应达到平衡状态,故A不符合;
② 3𝑁𝑁𝑂𝑂 (𝑙𝑙)+𝑂𝑂3(𝑙𝑙)⇌3𝑁𝑁𝑂𝑂2(𝑙𝑙) △𝐻𝐻 =−317.1𝐾𝐾𝑘𝑘/𝑚𝑚𝑚𝑚𝑙𝑙
B.反应前后气体质量不变,物质的量变化,当气体的平均摩尔质量不再改变说明反应达到平衡状态,故B不
符合;
C.气体质量和体积不变,气体的密度始终不改变,不能说明反应达到平衡状态,故C符合;
D.反应速率之比等于化学方程式计量数之比为正反应速率之比,当单位时间内生成 和 物质的量之比
为 : ,表明正逆反应速率相同,反应达到平衡状态,故D不符合;
𝑂𝑂3 𝑁𝑁𝑂𝑂2
1 3
学科网(北京)股份有限公司故答案为: ;
Ⅱ 关闭 ,将各 通过 、 分别充入真空 、 中,反应起始时 、 的体积相同均为 ,若
𝐶𝐶
容器 中到达平衡所需时间 ,达到平衡后容器内压强为起始压强的 倍,设生成四氧化二氮为
.(3)① 𝐾𝐾2 1𝑚𝑚𝑚𝑚𝑙𝑙𝑁𝑁𝑂𝑂2 𝐾𝐾1 𝐾𝐾3 𝐴𝐴 𝐵𝐵 𝐴𝐴 𝐵𝐵 𝑎𝑎𝐿𝐿
𝐴𝐴 𝑡𝑡𝑠𝑠 0.8 𝑥𝑥
起始量
2𝑁𝑁𝑂𝑂2(𝑙𝑙)⇌𝑁𝑁2𝑂𝑂4(𝑙𝑙)
变化量
1 0
平衡量
2𝑥𝑥 𝑥𝑥
1−2𝑥𝑥 𝑥𝑥
1−2𝑥𝑥+𝑥𝑥 =0.8×1
则𝑥𝑥 =平0均.2化𝑚𝑚学𝑚𝑚𝑙𝑙 反应速率 ,
2×0.2𝑚𝑚𝑚𝑚𝑚𝑚
𝑎𝑎𝑎𝑎 0.4
𝑣𝑣(𝑁𝑁𝑂𝑂2)= 𝑎𝑎𝑠𝑠 = 𝑎𝑎𝑎𝑎 𝑚𝑚𝑚𝑚𝑙𝑙/(𝐿𝐿⋅𝑠𝑠)
故答案为: ;
0.4
打开 ,则𝑎𝑎𝑎𝑎相𝑚𝑚当𝑚𝑚𝑙𝑙/于(𝐿𝐿是⋅在𝑠𝑠)等温等压时的平衡,因此平衡时等效的.由于此时反应物的物质的量是 中的二倍,
所以打开 之前,气球 体积为 ,
② 𝐾𝐾2 𝐵𝐵
故答案为: ;
𝐾𝐾2 𝐵𝐵 (𝑎𝑎𝐿𝐿+0.4𝑎𝑎𝐿𝐿)÷2=0.7𝑎𝑎𝐿𝐿
若平衡后在 容器中再充入 ,相当于中等压强,平衡正向进行,则重新到达平衡后,平衡混
0.7𝑎𝑎
合气中 的体积分数变小,故答案为:变小.
③ 𝐴𝐴 0.5𝑚𝑚𝑚𝑚𝑙𝑙 𝑁𝑁2𝑂𝑂4
Ⅰ 依据热化学方程式和盖斯定律计算所需热化学方程式;
𝑁𝑁𝑂𝑂2
生成物平衡浓度幂次方乘积
.(1)化学平衡三行计算得到平衡浓度,平衡常数 ;
反应物平衡浓度幂次方乘积
(2)当①化学反应达到平衡状态时,正逆反应速率相等𝐾𝐾,=各物质的浓度不再发生变化,由此衍生的一些物理性
不变,以此解答该题;
②
Ⅱ 依据平衡三行计算列式计算二氧化氮的消耗浓度,反应速率 ;
△𝑐𝑐
.根(3据)①等效平衡分析; 𝑣𝑣 = △𝑎𝑎
反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,若平衡
②
后在 容器中再充入 ,相当于增大压强平衡正向进行;
③
本题考查热化学方程式书写、化学平衡状态的判断、化学平衡常数的计算,为高频考点,侧重于学生的分析
𝐴𝐴 0.5𝑚𝑚𝑚𝑚𝑙𝑙 𝑁𝑁2𝑂𝑂4
能力的考查,题目难度中等,注意基础知识的举一反三.
20. 【分析】
发生加成反应,然后碱化生成 , 和 发生加成反应生成 ,结合 的结构, 为 , 先加碱
加热发生消去反应,然后酸化生成 , 发生加成反应和还原反应生成 ,据此解答。
𝐴𝐴 𝐵𝐵 𝐵𝐵 𝐶𝐶 𝐷𝐷 𝐷𝐷 𝐶𝐶 𝐷𝐷
【解答】
𝐸𝐸 𝐸𝐸 𝐴𝐴𝐻𝐻𝐴𝐴𝐴𝐴
的化学名称是羟基乙酸。
(1)𝐻𝐻𝑂𝑂𝐶𝐶𝐻𝐻2𝐶𝐶𝑂𝑂𝑂𝑂𝐻𝐻
的结构简式为 。
(2)𝐶𝐶
学科网(北京)股份有限公司中手性碳原子数目为 ,如图 。
转化为 的反应类型为加成反应、还原反应。
(3)𝐷𝐷 3
中酸性官能团名称为羧基,碱性官能团名称为氨基。
(4)𝐸𝐸 𝐴𝐴𝐻𝐻𝐴𝐴𝐴𝐴
满足 含苯环且苯环只有一个取代基;
(5)𝐴𝐴𝐻𝐻𝐴𝐴𝐴𝐴
红外光谱显示含氧官能团只有 和 ;
(6) ①
核磁共振氢谱显示有 组峰,峰面积比为 ,下列条件的 的同分异构体的结构简式
② −𝑂𝑂𝐻𝐻 −𝐶𝐶𝑂𝑂𝑁𝑁𝐻𝐻2
③ 6 4∶2∶2∶2∶2∶1 𝐴𝐴𝐻𝐻𝐴𝐴𝐴𝐴
。
苄基氯 在碱性条件下发生水解反应生成 , 发生
(7) ( )
催 化 氧 化 生 成 , 在 碱 性 条 件 下 和 发 生 加 成 反 应 生 成
𝐶𝐶 𝐻𝐻3𝑂𝑂𝑁𝑁2
, 在 碱 性 条 件 下 加 热 发 生 消 去 反 应 生 成
, 发 生 加 聚 反 应 生 成 , 合 成 路 线
学科网(北京)股份有限公司