文档内容
第四课时 化学平衡图像基础练习题
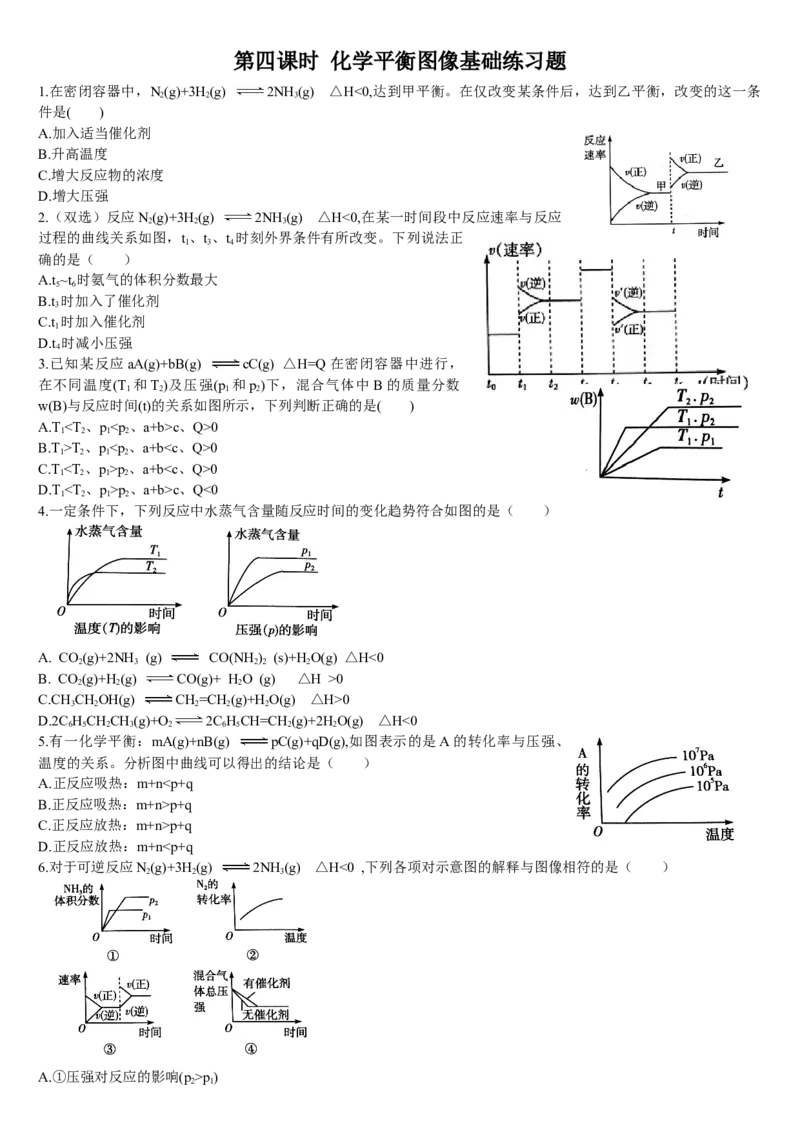
1.在密闭容器中,N(g)+3H(g) 2NH (g) △H<0,达到甲平衡。在仅改变某条件后,达到乙平衡,改变的这一条
2 2 3
件是( )
A.加入适当催化剂
B.升高温度
C.增大反应物的浓度
D.增大压强
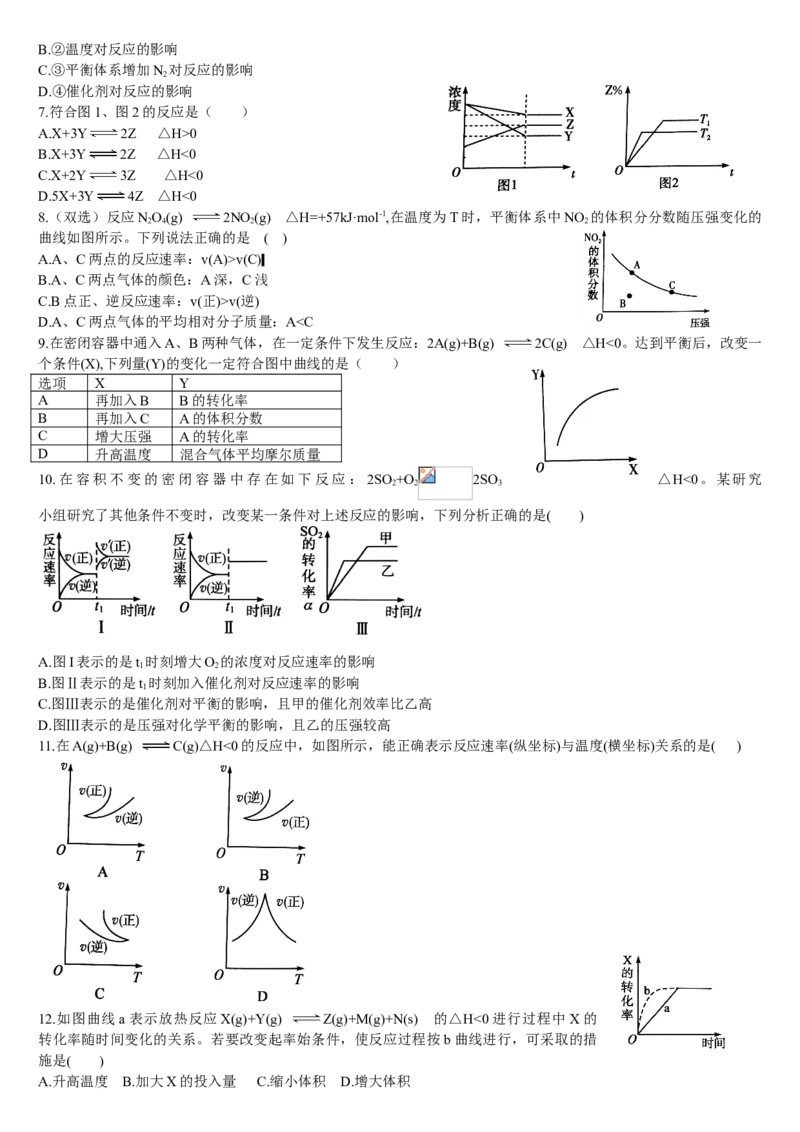
2.(双选)反应N(g)+3H(g) 2NH (g) △H<0,在某一时间段中反应速率与反应
2 2 3
过程的曲线关系如图,t 、t 、t 时刻外界条件有所改变。下列说法正
1 3 4
确的是( )
A.t ~t 时氨气的体积分数最大
5 6
B.t 时加入了催化剂
3
C.t 时加入催化剂
1
D.t 时减小压强
4
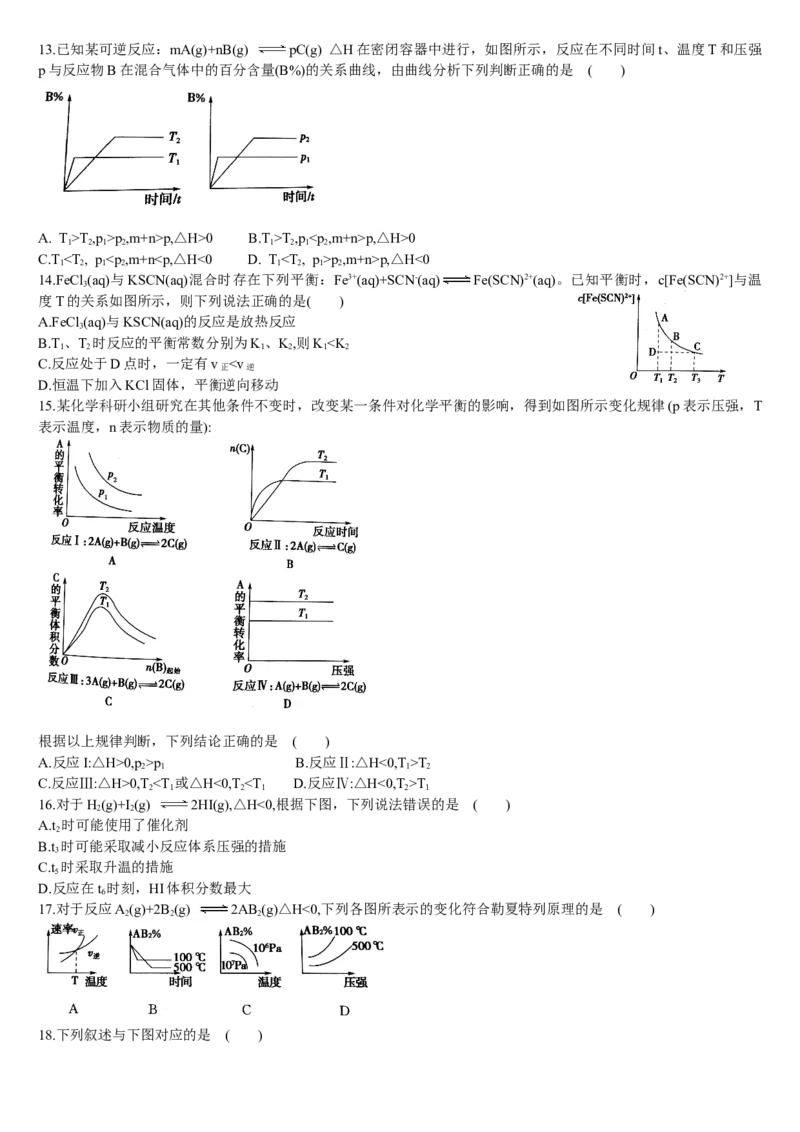
3.已知某反应aA(g)+bB(g) cC(g) △H=Q在密闭容器中进行,
在不同温度(T 和T)及压强(p 和p)下,混合气体中B的质量分数
1 2 1 2
w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
A.T c、Q>0
1 2 1 2
B.T>T、p0
1 2 1 2
C.Tp、a+b0
1 2 1 2
D.T p、a+b>c、Q<0
1 2 1 2
4.一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合如图的是( )
A. CO(g)+2NH (g) CO(NH) (s)+HO(g) △H<0
2 3 2 2 2
B. CO(g)+H(g) CO(g)+ HO (g) △H >0
2 2 2
C.CH CHOH(g) CH=CH (g)+HO(g) △H>0
3 2 2 2 2
D.2C HCHCH(g)+O 2C HCH=CH(g)+2HO(g) △H<0
6 5 2 3 2 6 5 2 2
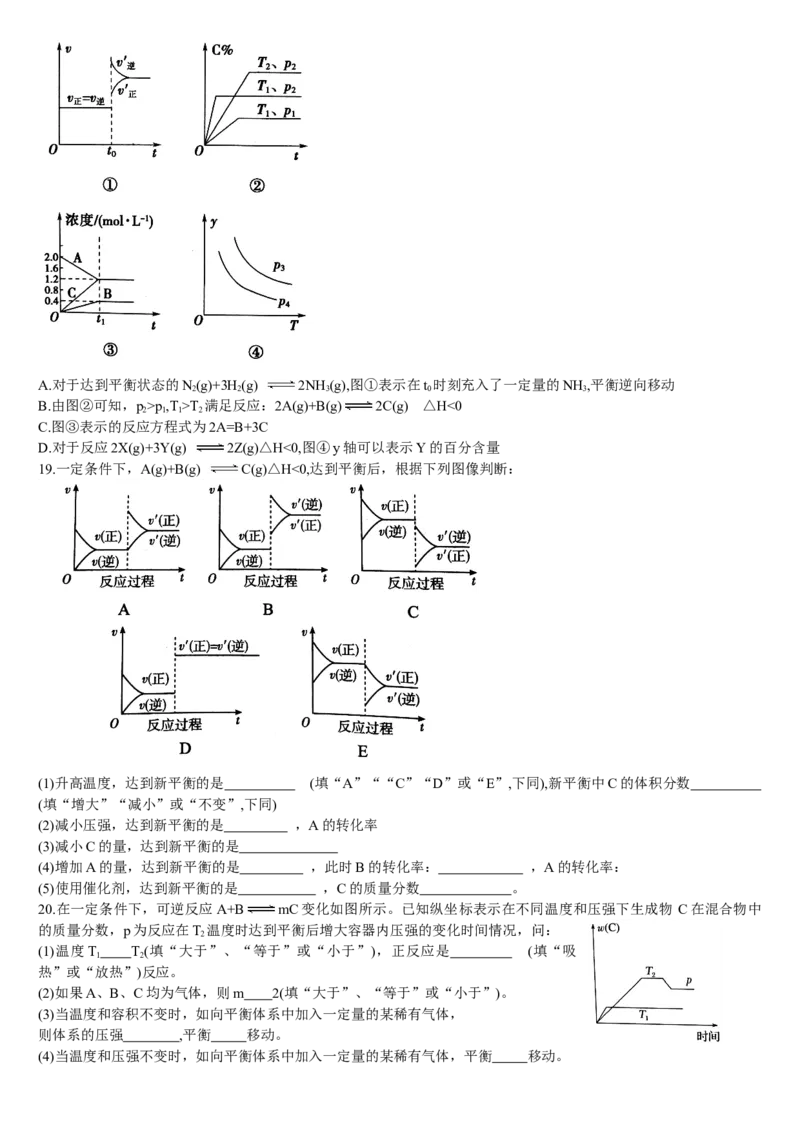
5.有一化学平衡:mA(g)+nB(g) pC(g)+qD(g),如图表示的是A的转化率与压强、
温度的关系。分析图中曲线可以得出的结论是( )
A.正反应吸热:m+np+q
C.正反应放热:m+n>p+q
D.正反应放热:m+np)
2 1B.②温度对反应的影响
C.③平衡体系增加N 对反应的影响
2
D.④催化剂对反应的影响
7.符合图1、图2的反应是( )
A.X+3Y 2Z △H>0
B.X+3Y 2Z △H<0
C.X+2Y 3Z △H<0
D.5X+3Y 4Z △H<0
8.(双选)反应NO(g) 2NO (g) △H=+57kJ·mol-1,在温度为T时,平衡体系中NO 的体积分分数随压强变化的
2 4 2 2
曲线如图所示。下列说法正确的是 ( )
A.A、C两点的反应速率:v(A)>v(C)
B.A、C两点气体的颜色:A深,C浅
C.B点正、逆反应速率:v(正)>v(逆)
D.A、C两点气体的平均相对分子质量:AT,p>p,m+n>p,△H>0 B.T>T,pp,△H>0
1 2 1 2 1 2 1 2
C.Tp,m+n>p,△H<0
1 2 1 2 1 2 1 2
14.FeCl (aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq) Fe(SCN)2+(aq)。已知平衡时,c[Fe(SCN)2+]与温
3
度T的关系如图所示,则下列说法正确的是( )
A.FeCl (aq)与KSCN(aq)的反应是放热反应
3
B.T、T 时反应的平衡常数分别为K、K,则K0,p >p B.反应Ⅱ:△H<0,T>T
2 1 1 2
C.反应Ⅲ:△H>0,TT
2 1 2 1 2 1
16.对于H(g)+I (g) 2HI(g),△H<0,根据下图,下列说法错误的是 ( )
2 2
A.t 时可能使用了催化剂
2
B.t 时可能采取减小反应体系压强的措施
3
C.t 时采取升温的措施
5
D.反应在t 时刻,HI体积分数最大
6
17.对于反应A(g)+2B (g) 2AB (g)△H<0,下列各图所表示的变化符合勒夏特列原理的是 ( )
2 2 2
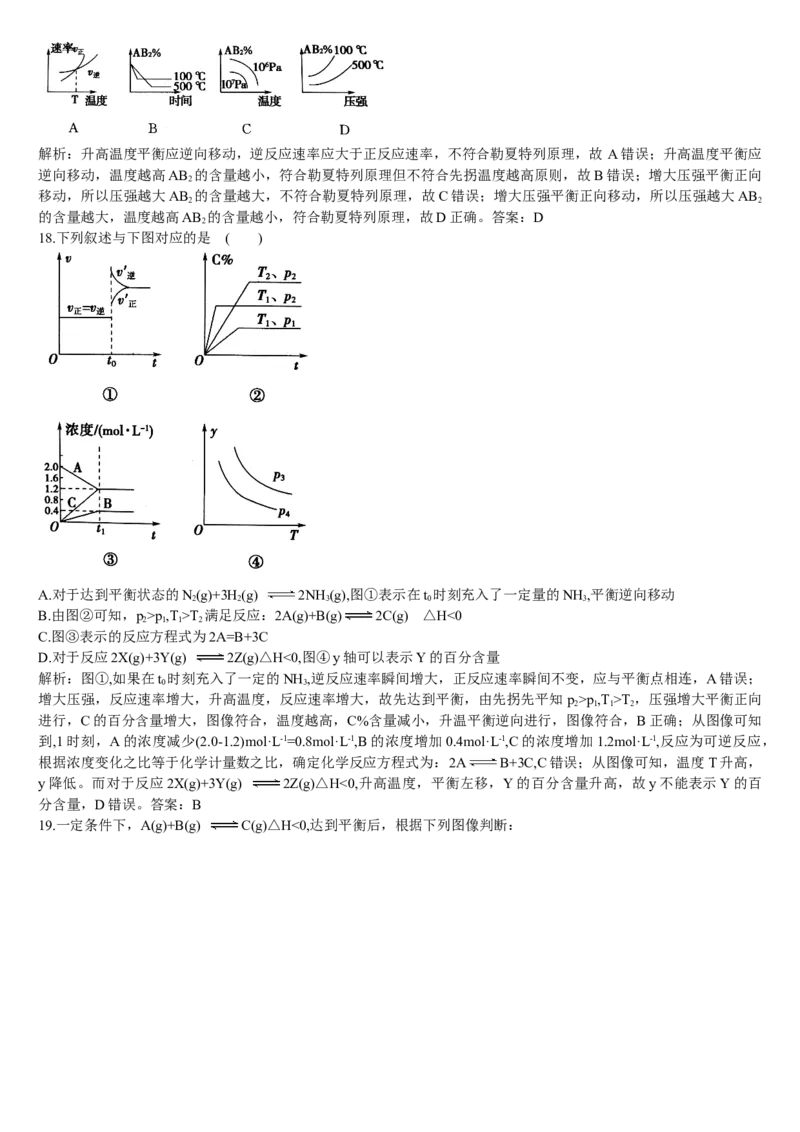
18.下列叙述与下图对应的是 ( )A.对于达到平衡状态的N(g)+3H(g) 2NH (g),图①表示在t 时刻充入了一定量的NH ,平衡逆向移动
2 2 3 0 3
B.由图②可知,p>p,T>T 满足反应:2A(g)+B(g) 2C(g) △H<0
2 1 1 2
C.图③表示的反应方程式为2A=B+3C
D.对于反应2X(g)+3Y(g) 2Z(g)△H<0,图④y轴可以表示Y的百分含量
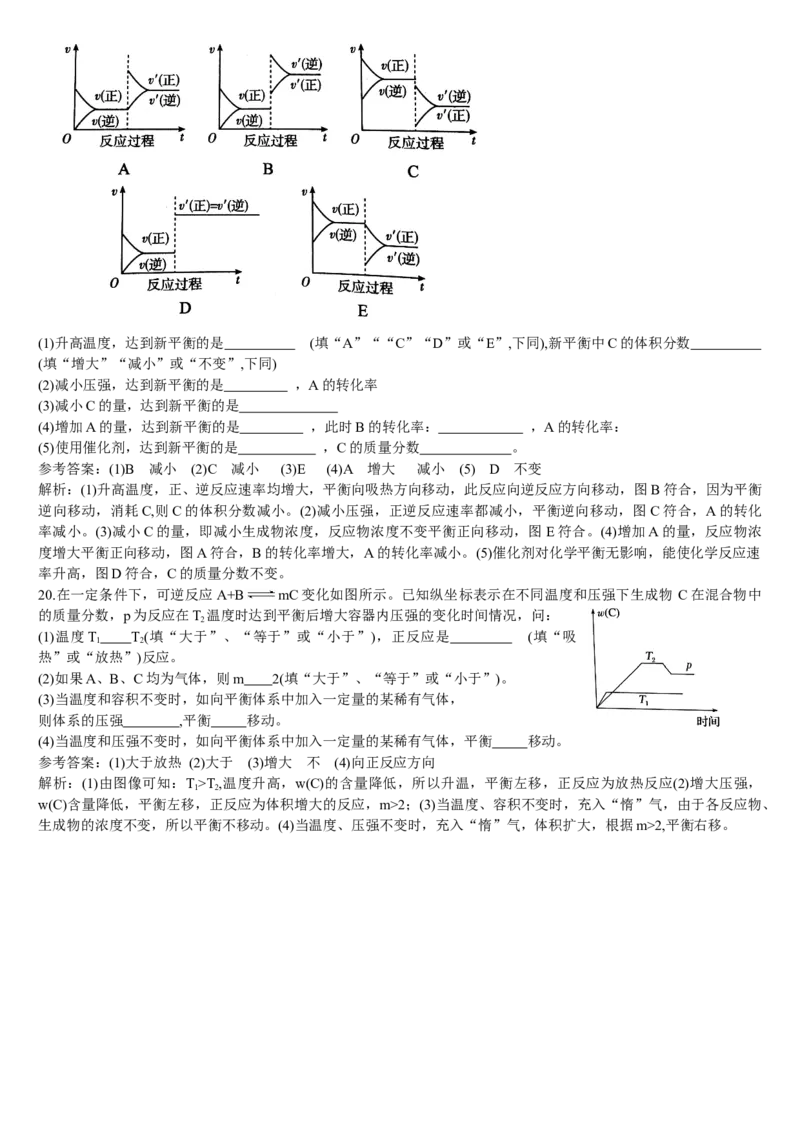
19.一定条件下,A(g)+B(g) C(g)△H<0,达到平衡后,根据下列图像判断:
(1)升高温度,达到新平衡的是 (填“A”““C”“D”或“E”,下同),新平衡中C的体积分数
(填“增大”“减小”或“不变”,下同)
(2)减小压强,达到新平衡的是 ,A的转化率
(3)减小C的量,达到新平衡的是
(4)增加A的量,达到新平衡的是 ,此时B的转化率: ,A的转化率:
(5)使用催化剂,达到新平衡的是 ,C的质量分数 。
20.在一定条件下,可逆反应A+B mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物 C在混合物中
的质量分数,p为反应在T 温度时达到平衡后增大容器内压强的变化时间情况,问:
2
(1)温度T T(填“大于”、“等于”或“小于”),正反应是 (填“吸
1 2
热”或“放热”)反应。
(2)如果A、B、C均为气体,则m 2(填“大于”、“等于”或“小于”)。
(3)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,
则体系的压强 ,平衡 移动。
(4)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡 移动。第四课时 化学平衡图像基础练习题解析版
1.在密闭容器中,N(g)+3H(g) 2NH (g) △H<0,达到甲平衡。在仅改变某条件后,达到乙平衡,改变的这一条
2 2 3
件是( )
A.加入适当催化剂
B.升高温度
C.增大反应物的浓度
D.增大压强
解析:改变条件后正、逆反应速率均加快,可能是升高温度或增大压强,再结合
v(正)>v(逆)可知平衡正向移动,结合N(g)+3H(g) 2NH (g) △H<0可知,t时
2 2 3
刻是增大了压强,D项正确;若升高温度平衡将逆向移动。答案:D
2.(双选)反应N(g)+3H(g) 2NH (g) △H<0,在某一时间段中反应速率与反应过程的曲线关系如图,t 、t 、t
2 2 3 1 3 4
时刻外界条件有所改变。下列说法正确的是( )
A.t ~t 时氨气的体积分数最大
5 6
B.t 时加入了催化剂
3
C.t 时加入催化剂
1
D.t 时减小压强
4
解析:t~t 、t~t 时反应向逆反应方向进行,消耗NH ,因此NH 体积
1 2 4 5 3 3
分数最大的是t~t,A项错误;t 时刻正逆反应速率都增大,且平衡不
0 1 3
移动,是使用了催化剂的缘故,B项正确;使用催化剂对化学平衡无
影响,根据图像变化可知t 时是升高了温度,C项错误;t 时刻,正、逆反应速率都减小且平衡逆向移动,即t 时减小
1 4 4
了体系压强,D项正确。答案:BD
3.已知某反应aA(g)+bB(g) cC(g) △H=Q在密闭容器中进行,在不同温度(T 和T)及压强(p 和p)下,混合气体
1 2 1 2
中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
A.T c、Q>0
1 2 1 2
B.T>T、p0
1 2 1 2
C.Tp、a+b0
1 2 1 2
D.T p、a+b>c、Q<0
1 2 1 2
解析:根据该图可知,温度为 T 时,由到达平衡的时间可判断:p>p,根据增大压
1 2 1
强,平衡逆向移动,即逆向气体总体积小于正向气体总体积,可知a+bT;再结合温度越高,B的含量越低,可知平衡正向移动,即正向为吸热反应,即Q>0,
2 1 1 2
综上分析可知,B项正确。答案:B
4.一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合如图的是( )
A. CO(g)+2NH (g) CO(NH) (s)+HO(g) △H<0
2 3 2 2 2
B. CO(g)+H(g) CO(g)+ HO (g) △H >0
2 2 2
C.CH CHOH(g) CH=CH (g)+HO(g) △H>0
3 2 2 2 2
D.2C HCHCH(g)+O 2C HCH=CH(g)+2HO(g) △H<0
6 5 2 3 2 6 5 2 2
解析:根据两图像和先拐先平可知温度:T>T,压强:p>p 。A项,降温和加压均能增大水蒸气含量,正确;B项,
2 1 1 2
降温平衡逆向移动,水蒸气含量减小,压强对水蒸气含量无影响,错误;C项,降温和加压平衡均逆向移动,水蒸气
含量减小,错误;D项,降温平衡正向移动,水蒸气含量增加,加压平衡逆向移动,水蒸气含量减小,错误。答案:
A
5.有一化学平衡:mA(g)+nB(g) pC(g)+qD(g),如图表示的是A的转化率与压强、
温度的关系。分析图中曲线可以得出的结论是( )
A.正反应吸热:m+np+q
C.正反应放热:m+n>p+q
D.正反应放热:m+np+q。故选B。
答案:B
6.对于可逆反应N(g)+3H(g) 2NH (g) △H<0 ,下列各项对示意图的解释与图像相符的是( )
2 2 3
A.①压强对反应的影响(p>p)
2 1
B.②温度对反应的影响
C.③平衡体系增加N 对反应的影响
2
D.④催化剂对反应的影响
解析:由图①可知压强p>p 增大压强NH 的体积分数应增大,与图像不符;图②温度升高平衡应逆向移动,N 的转
1 2 3 2
化率应降低,与图像不符;图③中v(正)>v(逆),可能是增大N 或H 浓度产生的影响;图④使用催化剂能缩短达到平衡
2 2
的时间,与图像不符。综上分析C项正确。答案:C
7.符合图1、图2的反应是( )
A.X+3Y 2Z △H>0
B.X+3Y 2Z △H<0
C.X+2Y 3Z △H<0
D.5X+3Y 4Z △H<0
解析:结合图1可知,X、Y为反应物,Z为生成物,三者物质量变
化之比为1:3:2,即该反应为X+3Y 2Z;由图2可知温度T>T,即升温Z%减小,平衡逆向移动,则正向为放热反应,
2 1
△H<0。综上分析B项正确。答案:B
8.反应NO(g) 2NO (g) △H=+57kJ·mol-1,在温度为T时,平衡体系中NO 的体积分分数随压强变化的曲线如图
2 4 2 2
所示。下列说法正确的是 ( )
A.A、C两点的反应速率:v(A)>v(C)
B.A、C两点气体的颜色:A深,C浅
C.B点正、逆反应速率:v(正)>v(逆)
D.A、C两点气体的平均相对分子质量:AA点,压强越大,反应速率越快,即v(A)v(正)。答案:B
12.如图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s) 的△H<0进行过程中X的转化率随时间变化的关系。
若要改变起率始条件,使反应过程按b曲线进行,可采取的措施是( )
A.升高温度 B.加大X的投入量 C.缩小体积 D.增大体积
解析:由于该反应是气体分子数不变的反应,缩小体积时压强增大,平衡不移动,反应速率
增大能缩短达到平衡的时间。答案:C
13.已知某可逆反应:mA(g)+nB(g) pC(g) △H在密闭容器中进行,如图所示,反应在
不同时间t、温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是 (
)
A. T>T,p>p,m+n>p,△H>0 B.T>T,pp,△H>0
1 2 1 2 1 2 1 2
C.Tp,m+n>p,△H<0
1 2 1 2 1 2 1 2
解析:由“先拐先平数值大”可知T>T ,p>p ,温度越高B%越小,说明升温平衡正向(吸热方向)动,△H>0,压强越
1 2 1 2大,B%越小,说明增大压强平衡正向移动,m+n>p。答案:A
14.FeCl (aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq) Fe(SCN)2+(aq)。已知平衡时,c[Fe(SCN)2+]与温
3
度T的关系如图所示,则下列说法正确的是( )
A.FeCl (aq)与KSCN(aq)的反应是放热反应
3
B.T、T 时反应的平衡常数分别为K、K,则KK ,B错误;D在曲线下方,未处于平衡状态,c[Fe(SCN)2+]比平衡状态小,应向正反应方
1 2, 1 2
向移动,v >v ,C错误;恒温下加入KCl固体,由于钾离子、氯离子不参与反应,则平衡不移动,D错误。答案:
正 逆
A
15.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示变化规律(p表示压强,T
表示温度,n表示物质的量):
根据以上规律判断,下列结论正确的是 ( )
A.反应I:△H>0,p >p B.反应Ⅱ:△H<0,T>T
2 1 1 2
C.反应Ⅲ:△H>0,TT
2 1 2 1 2 1
解析:由反应I的图可知,温度升高,A的转化率减小,说明该反应的正反应是放热反应,△H<0,由反应式得:压强
越大,A的转化率越大,故p>p,A不正确;由反应Ⅱ的图得:先达平衡对应的温度高,即T>T ,温度越高时n(C)越
2 1 1 2
小,说明该反应的正反应是放热反应,即△H<0,B选项正确;反应Ⅲ由于没有其他限制条件和提示,能从两方面进行
讨论,一方面若该反应的正反应是吸热反应,△H>0,则有T>T 的关系,若该反应的正反应是放热反应,△H<0,则可
2 1
推出TT,则该反应的正反应是吸热反应,即△H>0,D错误。答案:B
2 1 2 1
16.对于H(g)+I (g) 2HI(g),△H<0,根据下图,下列说法错误的是 ( )
2 2
A.t 时可能使用了催化剂
2
B.t 时可能采取减小反应体系压强的措施
3
C.t 时采取升温的措施
5
D.反应在t 时刻,HI体积分数最大
6
解析:改变压强、使用催化剂,平衡均不移动,可能增大压强或使用催化剂,A正确;
t 时正逆反应速率同等程度减小,可能为减小压强,B正确;t 时正逆反应速率增大,
3 5
且逆反应速率大于正反应速率,改变条件为升高温度,C正确;平衡逆向移动,HI的体积分数减小,t 时HI的体积分
1
数最大,D错误。答案:D
17.对于反应A(g)+2B (g) 2AB (g)△H<0,下列各图所表示的变化符合勒夏特列原理的是 ( )
2 2 2解析:升高温度平衡应逆向移动,逆反应速率应大于正反应速率,不符合勒夏特列原理,故 A错误;升高温度平衡应
逆向移动,温度越高AB 的含量越小,符合勒夏特列原理但不符合先拐温度越高原则,故B错误;增大压强平衡正向
2
移动,所以压强越大AB 的含量越大,不符合勒夏特列原理,故C错误;增大压强平衡正向移动,所以压强越大AB
2 2
的含量越大,温度越高AB 的含量越小,符合勒夏特列原理,故D正确。答案:D
2
18.下列叙述与下图对应的是 ( )
A.对于达到平衡状态的N(g)+3H(g) 2NH (g),图①表示在t 时刻充入了一定量的NH ,平衡逆向移动
2 2 3 0 3
B.由图②可知,p>p,T>T 满足反应:2A(g)+B(g) 2C(g) △H<0
2 1 1 2
C.图③表示的反应方程式为2A=B+3C
D.对于反应2X(g)+3Y(g) 2Z(g)△H<0,图④y轴可以表示Y的百分含量
解析:图①,如果在t 时刻充入了一定的NH ,逆反应速率瞬间增大,正反应速率瞬间不变,应与平衡点相连,A错误;
0 3
增大压强,反应速率增大,升高温度,反应速率增大,故先达到平衡,由先拐先平知 p>p,T>T ,压强增大平衡正向
2 1 1 2
进行,C的百分含量增大,图像符合,温度越高,C%含量减小,升温平衡逆向进行,图像符合,B正确;从图像可知
到,1时刻,A的浓度减少(2.0-1.2)mol·L-1=0.8mol·L-1,B的浓度增加0.4mol·L-1,C的浓度增加1.2mol·L-1,反应为可逆反应,
根据浓度变化之比等于化学计量数之比,确定化学反应方程式为:2A B+3C,C错误;从图像可知,温度T升高,
y降低。而对于反应2X(g)+3Y(g) 2Z(g)△H<0,升高温度,平衡左移,Y的百分含量升高,故y不能表示Y的百
分含量,D错误。答案:B
19.一定条件下,A(g)+B(g) C(g)△H<0,达到平衡后,根据下列图像判断:(1)升高温度,达到新平衡的是 (填“A”““C”“D”或“E”,下同),新平衡中C的体积分数
(填“增大”“减小”或“不变”,下同)
(2)减小压强,达到新平衡的是 ,A的转化率
(3)减小C的量,达到新平衡的是
(4)增加A的量,达到新平衡的是 ,此时B的转化率: ,A的转化率:
(5)使用催化剂,达到新平衡的是 ,C的质量分数 。
参考答案:(1)B 减小 (2)C 减小 (3)E (4)A 增大 减小 (5) D 不变
解析:(1)升高温度,正、逆反应速率均增大,平衡向吸热方向移动,此反应向逆反应方向移动,图B符合,因为平衡
逆向移动,消耗C,则C的体积分数减小。(2)减小压强,正逆反应速率都减小,平衡逆向移动,图C符合,A的转化
率减小。(3)减小C的量,即减小生成物浓度,反应物浓度不变平衡正向移动,图E符合。(4)增加A的量,反应物浓
度增大平衡正向移动,图A符合,B的转化率增大,A的转化率减小。(5)催化剂对化学平衡无影响,能使化学反应速
率升高,图D符合,C的质量分数不变。
20.在一定条件下,可逆反应A+B mC变化如图所示。已知纵坐标表示在不同温度和压强下生成物 C在混合物中
的质量分数,p为反应在T 温度时达到平衡后增大容器内压强的变化时间情况,问:
2
(1)温度T T(填“大于”、“等于”或“小于”),正反应是 (填“吸
1 2
热”或“放热”)反应。
(2)如果A、B、C均为气体,则m 2(填“大于”、“等于”或“小于”)。
(3)当温度和容积不变时,如向平衡体系中加入一定量的某稀有气体,
则体系的压强 ,平衡 移动。
(4)当温度和压强不变时,如向平衡体系中加入一定量的某稀有气体,平衡 移动。
参考答案:(1)大于放热 (2)大于 (3)增大 不 (4)向正反应方向
解析:(1)由图像可知:T>T,温度升高,w(C)的含量降低,所以升温,平衡左移,正反应为放热反应(2)增大压强,
1 2
w(C)含量降低,平衡左移,正反应为体积增大的反应,m>2;(3)当温度、容积不变时,充入“惰”气,由于各反应物、
生成物的浓度不变,所以平衡不移动。(4)当温度、压强不变时,充入“惰”气,体积扩大,根据m>2,平衡右移。