文档内容
理科综合考试时间共150分钟。试卷满分300分,其中物理110分,化学100分,生物90分。
化学试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)。第Ⅰ卷5至6页,第Ⅱ卷7至8页,共4页。
考生作答时,需将答案答在答题卡上,在本卷第Ⅱ卷、草稿纸上答题无效。考试结束后,将本试
题卷和答题卡一并交回。
可能用到的相对原子质量:H 1 N 14 O 16 Mg 24 Al 27 S 32 K 39 Cu 64
第Ⅰ卷(选择题 共 42分)
注惹事项:
必须使用 2B 铅笔将答题卡上将所选答案对应的标号涂黑。
Ⅰ卷共 7题,每题 6分。在每题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法不正确的是
A.二氧化硫可广泛用于食品的漂白
B.葡萄糖可用于补钙药物的合成
C.聚乙烯塑料制品可用于食品的包装
D.次氯酸钠溶液可用于环境的消毒杀菌
2.下列物质分类正确的是
A.SO 、SiO 、CO均为酸性氧化物
2 2
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.福尔马林、水玻璃、氨水均为混合物
4.同周期元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4︰3,
Z原子比X原子的核外电子数多4。下列说法正确的是
A.W、Y、Z的电负性大小顺序一定是Z>Y>W
第1页 | 共5页B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子的空间构型可能是正四面体
D.WY 分子中σ键与π键的数目之比是2:1
2
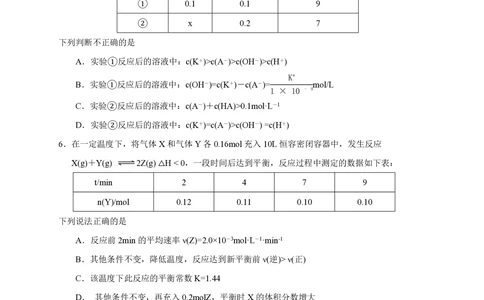
5.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
起始浓度/(mol·L-1)
实验编号 反应后溶液的pH
c(HA) c(KOH)
① 0.1 0.1 9
② x 0.2 7
下列判断不正确的是
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
Kw
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol/L
1 × 10 - 9
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1mol·L-1
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-) =c(H+)
6.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
7.1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO 和
2
N O 的混合气体1120mL (标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子
2 4
全部沉淀时,得到2.54g沉淀,下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2 ︰1
B.该浓硝酸中HNO 的物质的量浓度是14.0mol/L
3
C.NO 和N O 的混合气体中,NO 的体积分数是80%
2 2 4 2
第2页 | 共5页D.得到2.54沉淀时,加入NaOH溶液的体积是600mL
【本解析为学科网名师解析团队原创,授权学科网独家使用,如有盗用,依法追责!】
第Ⅱ卷(非选择题 共 58分)
注意事项:
必须使用 0.5毫米黑色墨迹签字笔在答题卡上题目所指示的答题区域内作答,答在
试题卷上、草稿纸上无效。
Ⅱ卷共 4题
8.(11分)X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与氢气可以化合生成气体
G,其水溶液pH>7;Y单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3
倍。Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO 溶液反应可生成不溶于
3
稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。
请回答下列问题:
(1)M固体的晶体类型是 。
(2)Y基态原子的核外电子排布式是 ① ;G分子中X原子的杂化轨道的类型是 ② 。
(3)L的悬浊液加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是 。
(4)R的一种含氧酸根RO 2-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无
4
色气体产生,该反应的离子方程式是 。
9.(15分)
为了探究AgNO 的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
3
Ⅰ.AgNO 的氧化性
3
将光亮的铁丝伸入AgNO 溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将
3
溶液中的Ag+除尽后,进行了如下实验。可选用第试剂KSCN溶液、K [Fe(CN) ]溶液、氯水。
3 6
(1)请完成下表:
操作 现象 结论
取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 ① 存在Fe3+
取少量除尽Ag+后的溶液于试管中,加入 ② ,振荡 ③ 存在Fe2+
【实验结论】Fe的氧化产物为存在Fe2+和Fe3+
Ⅱ. AgNO 的热稳定性性
3
第3页 | 共5页用下图所示的实验装置A加热AgNO 固体,产生红棕色气体,在装置D中收集到无色气体。当
3
反应结束以后,试管中残留固体为黑色。
(2)装置B的作用是 。
(3)经小组讨论并验证该无色气体为O ,其验证方法是 。
2
(4)【查阅资料】Ag O和粉末的Ag均为黑色;Ag O可溶于氨水。
2 2
【提出假设】试管中残留的黑色固体可能是:ⅰAg;ⅱ.Ag O;ⅲ.Ag和Ag O
2 2
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
实验编号 操作 现象
a 加入足量氨水,振荡 黑色固体不溶解
b 加入足量稀硫酸,振荡 黑色固体溶解,并有气体产生
【实验评价】根据上述实验,不能确定固体产物成分的实验是 ① (填实验编号)。
【实验结论】根据上述实验结果,该小组得出的AgNO 固体热分解的产物有 ② 。
3
10.(17分) 有机化合物G是合成维生素类药物的中间体,其结构简式为:
G的合成线路如下:
其中A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:
请回答下列问题:
(1)G的分子式是 ① ;G中官能团的名称是 ② 。
(2)第①步反应的化学方程式是 。
(3)B的名称(系统命名)是 。
(4)第②~⑥步中属于取代反应的有 (填步骤编号)。
(5)第④步反应的化学方程式是 。
(6)写出同时满足下列条件的E的所有同分异构体的结构简式 。
第4页 | 共5页①只含有一种官能团;②链状结构且无—O—O—;③核磁共振氢谱只有2种峰。
11.(15分)
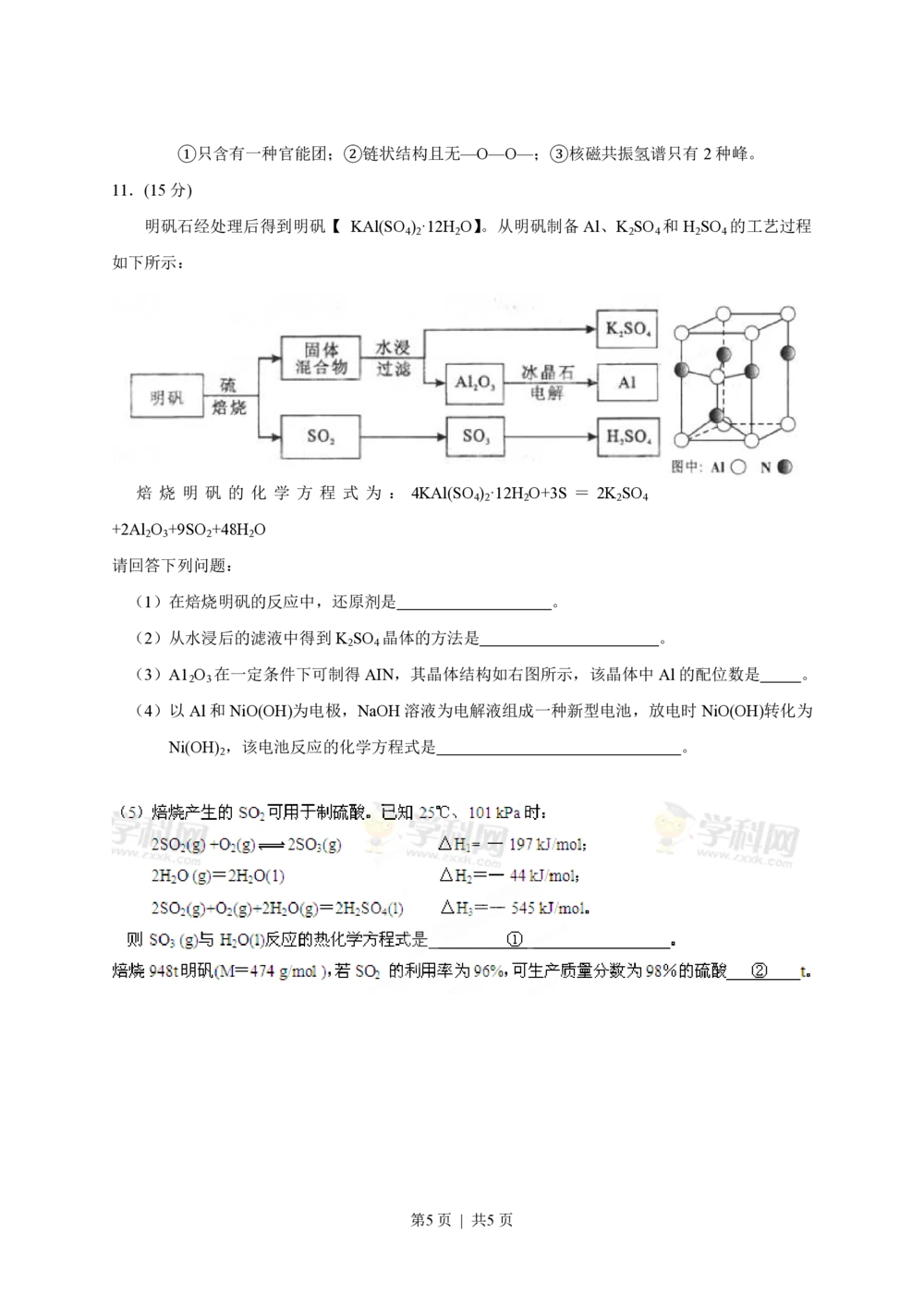
明矾石经处理后得到明矾【 KAl(SO ) ·12H O】。从明矾制备Al、K SO 和H SO 的工艺过程
4 2 2 2 4 2 4
如下所示:
焙 烧 明 矾 的 化 学 方 程 式 为 : 4KAl(SO ) ·12H O+3S = 2K SO
4 2 2 2 4
+2Al O +9SO +48H O
2 3 2 2
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 。
(2)从水浸后的滤液中得到K SO 晶体的方法是 。
2 4
(3)A1 O 在一定条件下可制得AIN,其晶体结构如右图所示,该晶体中Al的配位数是 。
2 3
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为
Ni(OH) ,该电池反应的化学方程式是 。
2
第5页 | 共5页