文档内容
课时分层作业(九) 卤代烃
(建议用时:40分钟)
[合格过关练]
1.氟利昂是一种氟氯代烷,曾被广泛用作制冷剂,但现在国际上已禁止、限制其使用,主
要原因是( )
A.氟利昂有剧毒
B.氟利昂会产生温室效应
C.氟利昂会破坏臭氧层
D.氟利昂会形成酸雨
C [氟利昂性质稳定,无毒,具有易挥发、易液化等特性,曾被广泛用作制冷剂,但其挥发
到大气中,在强烈的紫外线照射下会分解产生起催化作用的氯原子,引发损耗臭氧的反应,对
臭氧层起破坏作用,形成臭氧空洞,危害地球上的生物,应禁止使用。]
2.下列关于卤代烃的叙述错误的是 ( )
A.随着碳原子数的增多,一氯代烃的沸点逐渐升高
B.随着碳原子数的增多,一氯代烃的密度逐渐增大
C.等碳原子数的一氯代烃,支链越多,沸点越低
D.等碳原子数的一卤代烃,卤素的原子序数越大,沸点越高
B [随着碳原子数的增多,一氯代烃的沸点逐渐升高,A项正确;随着碳原子数的增多,一
氯代烃的密度逐渐减小,B项错误;等碳原子数的一氯代烃,支链越多,分子间距离越大,分子
间作用力越小,沸点越低,C项正确;等碳原子数的一卤代烃,卤素的原子序数越大,分子间作
用力越大,沸点越高,D项正确。]
3.下列关于溴乙烷的叙述中,正确的是( )
A.溴乙烷难溶于水,能溶于大多数有机溶剂
B.溴乙烷与NaOH的醇溶液共热可生成乙醇
C.在溴乙烷溶液中滴入AgNO 溶液,立即有淡黄色沉淀生成
3
D.溴乙烷通常用乙烷与溴蒸气直接反应来制取
A [溴乙烷能溶于大多数有机溶剂,难溶于水,也不能在水中电离出Br-,因而不能与
AgNO 反应生成淡黄色AgBr沉淀,A项正确,C项错误;溴乙烷与NaOH的醇溶液共热发生消去反
3
应,生成乙烯,溴乙烷与NaOH的水溶液共热发生取代反应(水解反应),生成乙醇,二者反应的
条件不同,其反应的类型和产物也不相同,B项错误;由于乙烷与溴蒸气发生取代反应是逐步进
行的,反应生成的各种溴代物中溴乙烷的量很少,且不易分离,因此不采用乙烷的溴代反应来
制取溴乙烷,一般用乙烯与溴化氢的加成反应来制取溴乙烷,D项错误。]
4.要检验卤代烃中是否含有溴元素,正确的实验方法是( )
A.加入氯水振荡,观察上层是否有红棕色
B.滴加稀硝酸酸化的硝酸银溶液,观察有无淡黄色沉淀生成
C.滴加NaOH溶液共热,然后加入稀硝酸酸化,最后滴加硝酸银溶液,观察有无淡黄色沉
淀生成
1D.滴加NaOH溶液共热,冷却后滴加硝酸银溶液,观察有无淡黄色沉淀生成
C [忽略卤代烃为非电解质,无法电离出卤素离子而错选B;忽略用稀硝酸酸化,而错选
D,因为卤代烃水解后的溶液呈碱性,而在碱性环境下不能用AgNO 直接检验卤素离子,故检验
3
卤代烃中卤素种类的正确方法为先通过水解产生卤素离子,再加入稀硝酸酸化,最后加入硝酸
银溶液。]
5.下列关于甲、乙、丙、丁四种有机物的说法正确的是( )
A.分别向甲、乙、丙、丁中加入NaOH的醇溶液共热,然后加入稀硝酸至溶液呈酸性,再滴
入AgNO 溶液,均有沉淀生成
3
B.向甲中加入NaOH的水溶液共热,再滴入AgNO 溶液,可检验该物质中含有的卤素原子
3
C.乙发生消去反应得到两种烯烃
D.丙与NaOH的水溶液共热,可生成醇
D [A项,甲、丙、丁不能发生消去反应,所以甲、丙、丁中无沉淀生成,错误;B项,卤代烃
和NaOH的水溶液发生取代反应生成NaX,检验卤素离子,应在酸性条件下,错误;C项,乙发生
消去反应生成一种烯烃,为丙烯,错误;D项,丙与NaOH的水溶液共热生成C(CH)CHOH,正
3 3 2
确。]
6.卤代烃RCHCHX中的化学键如图所示,则下列说法中正确的是 ( )
2 2
A.当该卤代烃发生水解反应时,被破坏的键是①和③
B.当该卤代烃发生水解反应时,被破坏的键是①
C.当该卤代烃发生消去反应时,被破坏的键是①和④
D.当该卤代烃发生消去反应时,被破坏的键是①和②
B [本题考查了卤代烃RCHCHX发生水解反应和消去反应时断键的位置。发生水解反应
2 2
时,只断开C—X键。发生消去反应时,要断开C—X键和与卤素原子所连碳原子的相邻碳原子
上的C—H键(即③)。]
7.某物质 是药品的中间体。下列针对该有机物的描述中,正确的是
( )
①能使溴的CCl 溶液褪色
4
②能使KMnO 酸性溶液褪色
4
2③在一定条件下可以聚合成
④在NaOH水溶液中加热可以生成不饱和醇类
⑤在NaOH醇溶液中加热,可发生消去反应
⑥与AgNO 溶液反应生成白色沉淀
3
A.①②③④ B.①③⑤⑥
C.①②④⑤ D.②④⑤⑥
A [该有机物中因含有 ,所以可以发生反应①②③;因含有—Cl,所以可以
发生反应④;它不能发生消去反应,⑤不正确;氯代烃中不含Cl-,所以加AgNO 溶液,没有AgCl
3
白色沉淀生成,⑥不正确。]
8.以溴乙烷为原料制取1,2二溴乙烷,下列方案最合理的是( )
A.CHCHBr―――→CHCHOH――――→CH===CH――→BrCHCHBr
3 2 3 2 2 2 2 2
B.CHCHBr――→BrCHCHBr
3 2 2 2
C.CHCHBr―――→CH===CH――→CHBrCH――→CHBrCHBr
3 2 2 2 2 3 2 2
D.CHCHBr―――→CH===CH――→CHBrCHBr
3 2 2 2 2 2
D [本题考查有机合成方案的设计与评价。A项,将CHCHBr转化为CH===CH,通过卤代
3 2 2 2
烃的消去反应一步就可以完成,不需要经过两步来实现,A项不合理。B项,该取代反应有多种
溴代物生成,B项不合理。C项,最后一步的取代过程有多种溴代物生成,C项不合理。]
9.某液态卤代烃RX(R是烷基,X是某种卤素原子)的密度是a g·cm-3,该RX可以跟稀碱
发生水解反应生成ROH(能跟水互溶)和X-。为了测定RX的相对分子质量,拟定的实验步骤如
下:
①准确量取该卤代烃b mL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀HNO 酸化,滴加过量AgNO 溶液得到白色沉淀。
3 3
④过滤、洗涤,干燥后称重,得到固体c g。
回答下面问题:
(1)装置中长玻璃管的作用是________________________。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的________(填离子符号)。
(3)该卤代烃中所含卤素的名称是________,判断的依据是
_____________________________________________________。
(4)假设RX完全反应,则该卤代烃的相对分子质量是________(列出算式)。
(5)如果在步骤③中,所加HNO 的量不足,没有将溶液酸化,则步骤④中测得的c值
3
________(填下列选项代码)。
A.偏大 B.偏小
3C.不变 D.大小不定
[解析] 本实验的反应原理是:
R—X+NaOH――→R—OH+NaX,
NaX+AgNO===AgX↓+NaNO。
3 3
(1)因R—X的熔、沸点较低,加热时易挥发,所以装置中的长玻璃管的作用是防止卤代烃
挥发。
(2)R—OH虽然能与水互溶,但难以电离,所以沉淀AgX吸附的离子只能是Na+、NO和过量
的Ag+。
(3)因所得卤化银AgX沉淀是白色的,所以该卤代烃中所含的卤素是氯。
(4)R—Cl ~ AgCl
M 143.5
r
a g·cm-3·b mL c g
=
M=。
r
(5)若加入的酸不足,则步骤④所得的固体还会混有AgO,使其质量c偏大。
2
[答案] (1)防止卤代烃挥发(或冷凝回流)
(2)Ag+、Na+和NO
(3)氯 得到的卤化银沉淀是白色的
(4) (5)A
[素养培优练]
10.(素养题)以环戊烷为原料制备环戊二烯的合成路线如图所示,下列叙述正确的是(
)
A.M的结构简式是
B.①②的反应类型分别为取代反应、消去反应
C.反应②的反应条件是浓硫酸、加热
D.利用酸性KMnO 溶液褪色可证明 已完全转化为
4
B [题述合成路线可表示为 。可知M为氯代环
戊烷,A项错误;反应①为取代反应,反应②为消去反应,B项正确;反应②的反应条件为氢氧化
钠的醇溶液、加热,C项错误;N为环戊烯,环戊烯和环戊二烯中均含碳碳双键,都能使酸性高锰
酸钾溶液褪色,故酸性KMnO 溶液褪色不能证明环戊烷已完全转化为环戊二烯,D项错误。]
4
11.某有机化合物X的分子式为CH Cl,用强碱的醇溶液处理X,可得到分子式为CH 的
5 11 5 10
2种产物Y、Z;Y、Z经催化加氢都可得到2甲基丁烷。则X的结构简式可能为( )
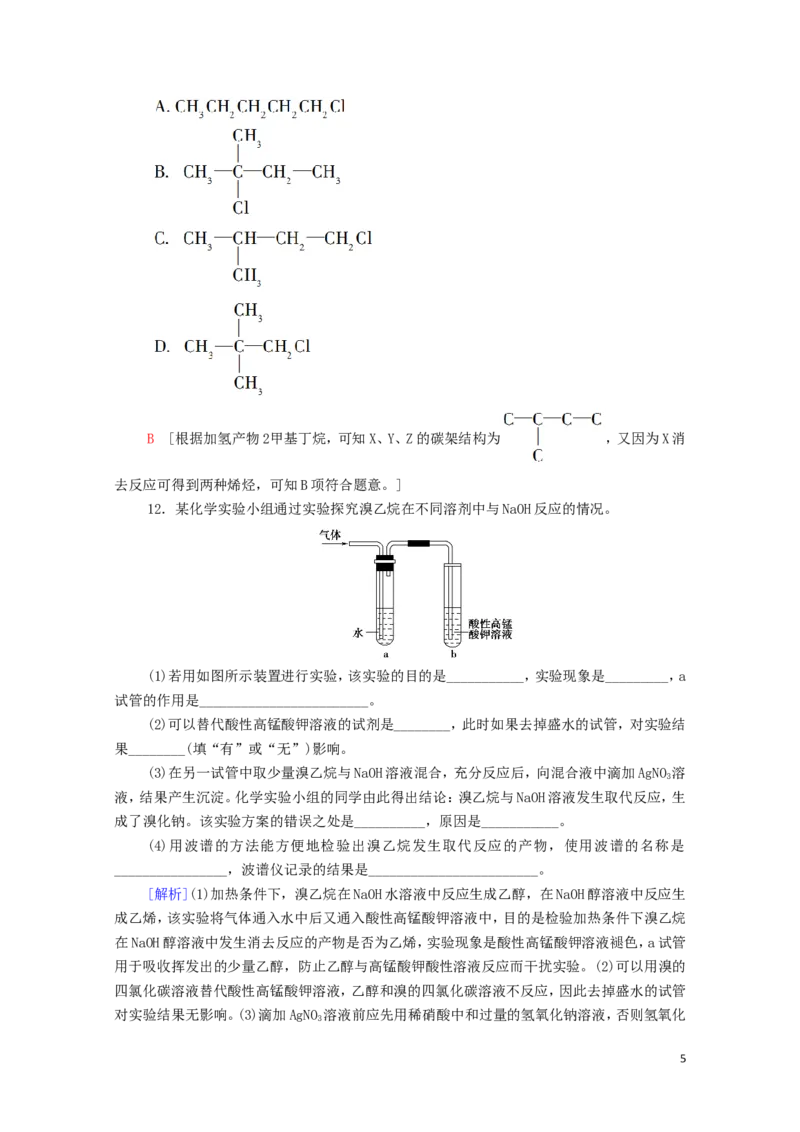
4B [根据加氢产物2甲基丁烷,可知X、Y、Z的碳架结构为 ,又因为X消
去反应可得到两种烯烃,可知B项符合题意。]
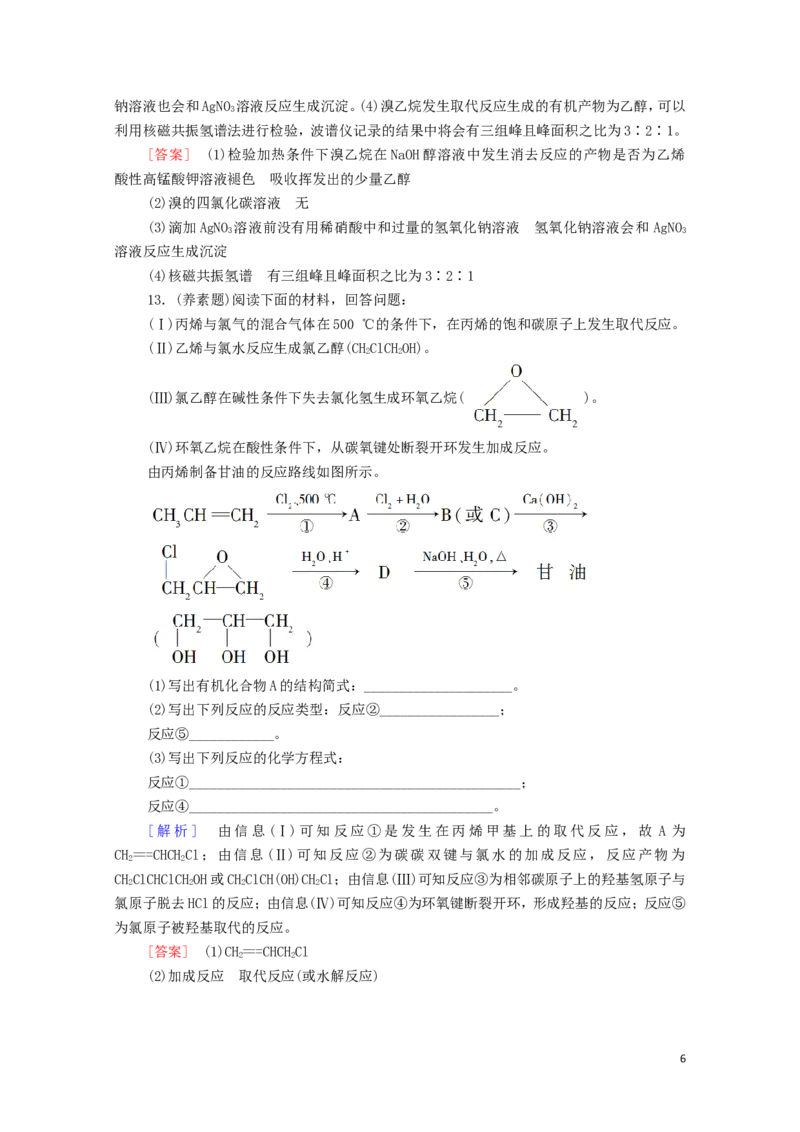
12.某化学实验小组通过实验探究溴乙烷在不同溶剂中与NaOH反应的情况。
(1)若用如图所示装置进行实验,该实验的目的是___________,实验现象是_________,a
试管的作用是________________________。
(2)可以替代酸性高锰酸钾溶液的试剂是________,此时如果去掉盛水的试管,对实验结
果________(填“有”或“无”)影响。
(3)在另一试管中取少量溴乙烷与NaOH溶液混合,充分反应后,向混合液中滴加AgNO 溶
3
液,结果产生沉淀。化学实验小组的同学由此得出结论:溴乙烷与NaOH溶液发生取代反应,生
成了溴化钠。该实验方案的错误之处是__________,原因是___________。
(4)用波谱的方法能方便地检验出溴乙烷发生取代反应的产物,使用波谱的名称是
________________,波谱仪记录的结果是________________________。
[解析](1)加热条件下,溴乙烷在NaOH水溶液中反应生成乙醇,在NaOH醇溶液中反应生
成乙烯,该实验将气体通入水中后又通入酸性高锰酸钾溶液中,目的是检验加热条件下溴乙烷
在NaOH醇溶液中发生消去反应的产物是否为乙烯,实验现象是酸性高锰酸钾溶液褪色,a试管
用于吸收挥发出的少量乙醇,防止乙醇与高锰酸钾酸性溶液反应而干扰实验。(2)可以用溴的
四氯化碳溶液替代酸性高锰酸钾溶液,乙醇和溴的四氯化碳溶液不反应,因此去掉盛水的试管
对实验结果无影响。(3)滴加AgNO 溶液前应先用稀硝酸中和过量的氢氧化钠溶液,否则氢氧化
3
5钠溶液也会和AgNO 溶液反应生成沉淀。(4)溴乙烷发生取代反应生成的有机产物为乙醇,可以
3
利用核磁共振氢谱法进行检验,波谱仪记录的结果中将会有三组峰且峰面积之比为3∶2∶1。
[答案] (1)检验加热条件下溴乙烷在 NaOH醇溶液中发生消去反应的产物是否为乙烯
酸性高锰酸钾溶液褪色 吸收挥发出的少量乙醇
(2)溴的四氯化碳溶液 无
(3)滴加AgNO 溶液前没有用稀硝酸中和过量的氢氧化钠溶液 氢氧化钠溶液会和 AgNO
3 3
溶液反应生成沉淀
(4)核磁共振氢谱 有三组峰且峰面积之比为3∶2∶1
13.(养素题)阅读下面的材料,回答问题:
(Ⅰ)丙烯与氯气的混合气体在500 ℃的条件下,在丙烯的饱和碳原子上发生取代反应。
(Ⅱ)乙烯与氯水反应生成氯乙醇(CHClCHOH)。
2 2
(Ⅲ)氯乙醇在碱性条件下失去氯化氢生成环氧乙烷( )。
(Ⅳ)环氧乙烷在酸性条件下,从碳氧键处断裂开环发生加成反应。
由丙烯制备甘油的反应路线如图所示。
(1)写出有机化合物A的结构简式:_____________________。
(2)写出下列反应的反应类型:反应②_________________;
反应⑤____________。
(3)写出下列反应的化学方程式:
反应①_______________________________________________;
反应④___________________________________________。
[解析] 由信息(Ⅰ)可知反应①是发生在丙烯甲基上的取代反应,故 A 为
CH===CHCHCl;由信息(Ⅱ)可知反应②为碳碳双键与氯水的加成反应,反应产物为
2 2
CHClCHClCHOH或CHClCH(OH)CHCl;由信息(Ⅲ)可知反应③为相邻碳原子上的羟基氢原子与
2 2 2 2
氯原子脱去HCl的反应;由信息(Ⅳ)可知反应④为环氧键断裂开环,形成羟基的反应;反应⑤
为氯原子被羟基取代的反应。
[答案] (1)CH===CHCHCl
2 2
(2)加成反应 取代反应(或水解反应)
67