文档内容
2023~2024 学年度下学期期末质量检测
高一化学
全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上
的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答
题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与生产、生活息息相关,下列叙述错误的是
A. 灿烂美丽的烟花是某些金属的焰色,焰色试验属于物理变化
B. 导光能力强,可用来生产光导纤维,是现代信息技术的基础材料
C. 生活中常用聚乙烯制成的薄膜来包装水果、蔬菜等食物
D. 北京冬奥会火炬燃烧时化学能只转化为热能
2. 下列化学用语表示正确的是
A. 的电子式为
B. 中含有的官能团为碳碳双键和醛基
C. 乙醇的空间填充模型为
D. 聚丙烯的结构简式为
3. 下列有关有机物的说法正确的是
第1页/共14页
学科网(北京)股份有限公司A. 塑料、棉花、羊毛等属于合成有机高分子材料
B. 淀粉和纤维素的分子式均为 ,二者互为同分异构体
C. 所有蛋白质与浓硝酸作用时均呈黄色
D. 加热条件下,淀粉水解的最终产物能与新制 ,反应产生砖红色沉淀
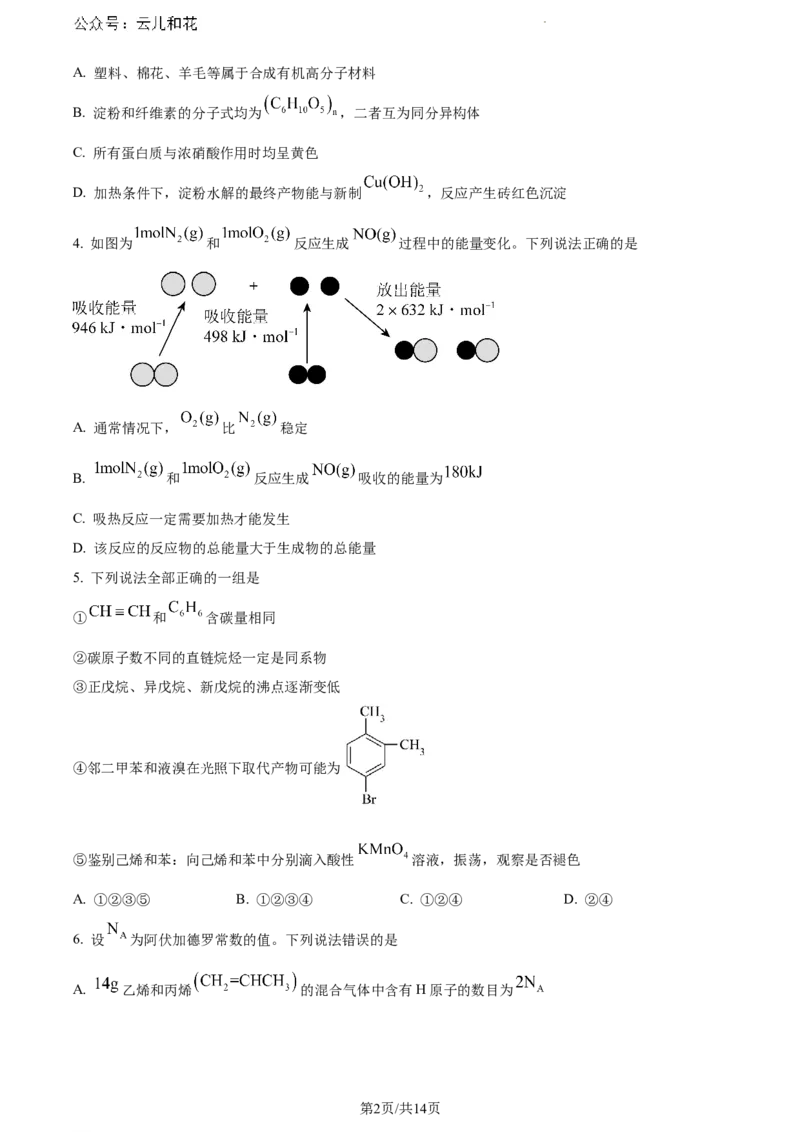
4. 如图为 和 反应生成 过程中的能量变化。下列说法正确的是
A. 通常情况下, 比 稳定
B. 和 反应生成 吸收的能量为
C. 吸热反应一定需要加热才能发生
D. 该反应的反应物的总能量大于生成物的总能量
5. 下列说法全部正确的一组是
① 和 含碳量相同
②碳原子数不同的直链烷烃一定是同系物
③正戊烷、异戊烷、新戊烷的沸点逐渐变低
④邻二甲苯和液溴在光照下取代产物可能为
⑤鉴别己烯和苯:向己烯和苯中分别滴入酸性 溶液,振荡,观察是否褪色
A. ①②③⑤ B. ①②③④ C. ①②④ D. ②④
6. 设 为阿伏加德罗常数的值。下列说法错误的是
A. 乙烯和丙烯 的混合气体中含有H原子的数目为
第2页/共14页
学科网(北京)股份有限公司B. 中L层的电子数目为
C. 中含有的阴、阳离子总数目为
D. 和足量氧气反应转移的电子数目小于
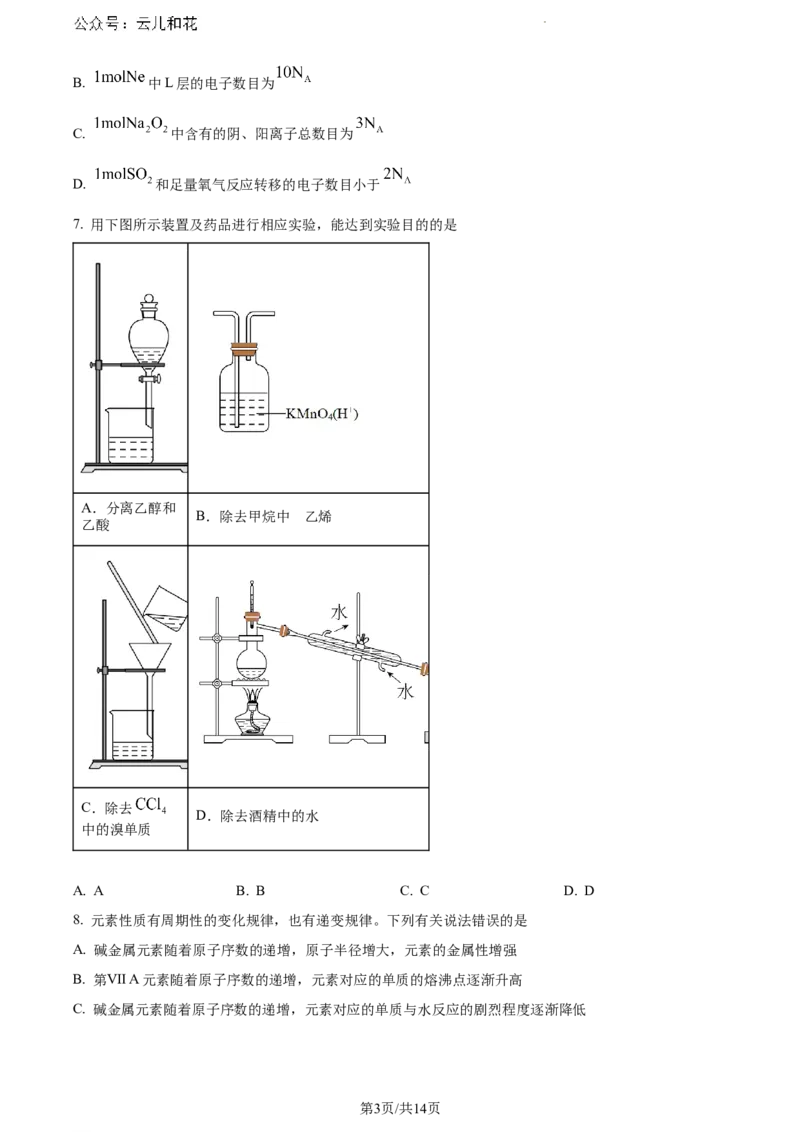
7. 用下图所示装置及药品进行相应实验,能达到实验目的的是
A.分离乙醇和
B.除去甲烷中 的乙烯
乙酸
C.除去
D.除去酒精中的水
中的溴单质
A. A B. B C. C D. D
8. 元素性质有周期性的变化规律,也有递变规律。下列有关说法错误的是
A. 碱金属元素随着原子序数的递增,原子半径增大,元素的金属性增强
B. 第ⅦA元素随着原子序数的递增,元素对应的单质的熔沸点逐渐升高
C. 碱金属元素随着原子序数的递增,元素对应的单质与水反应的剧烈程度逐渐降低
第3页/共14页
学科网(北京)股份有限公司D. 第ⅦA元素随着原子序数的递增,元素对应的单质与氢气化合越来越困难
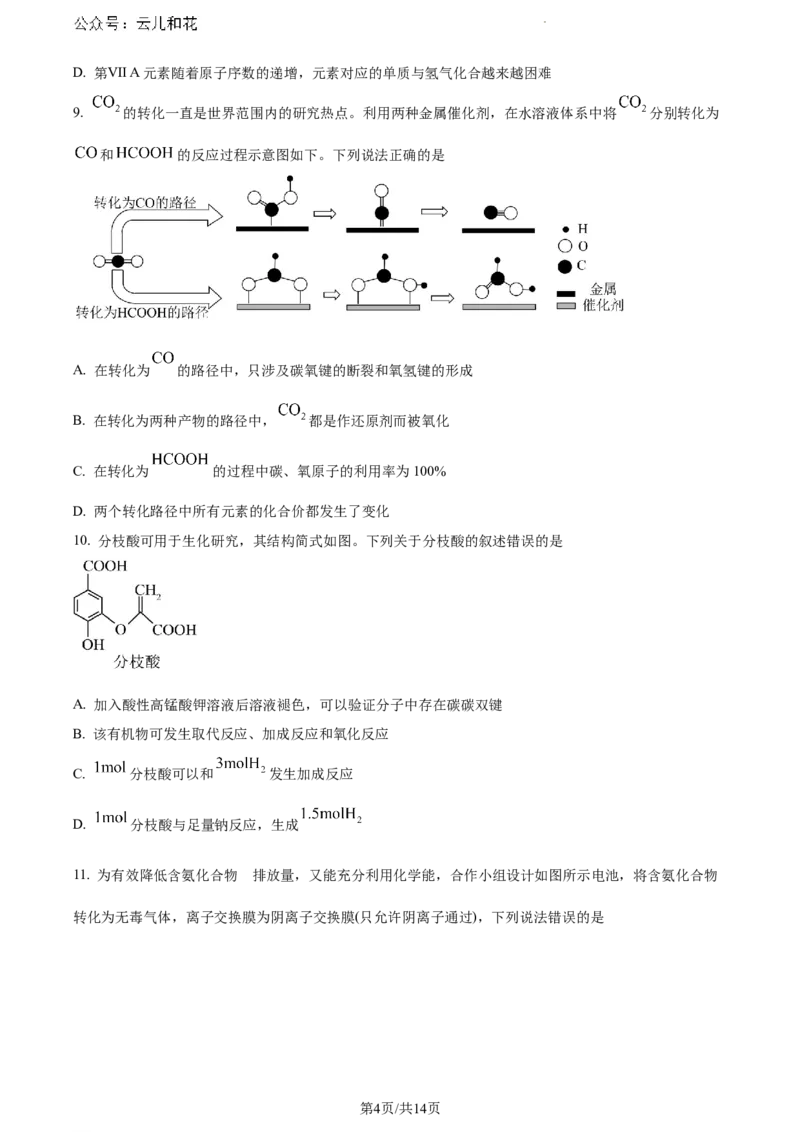
9. 的转化一直是世界范围内的研究热点。利用两种金属催化剂,在水溶液体系中将 分别转化为
和 的反应过程示意图如下。下列说法正确的是
A. 在转化为 的路径中,只涉及碳氧键的断裂和氧氢键的形成
B. 在转化为两种产物的路径中, 都是作还原剂而被氧化
C. 在转化为 的过程中碳、氧原子的利用率为100%
D. 两个转化路径中所有元素的化合价都发生了变化
10. 分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述错误的是
A. 加入酸性高锰酸钾溶液后溶液褪色,可以验证分子中存在碳碳双键
B. 该有机物可发生取代反应、加成反应和氧化反应
C. 分枝酸可以和 发生加成反应
D. 分枝酸与足量钠反应,生成
的
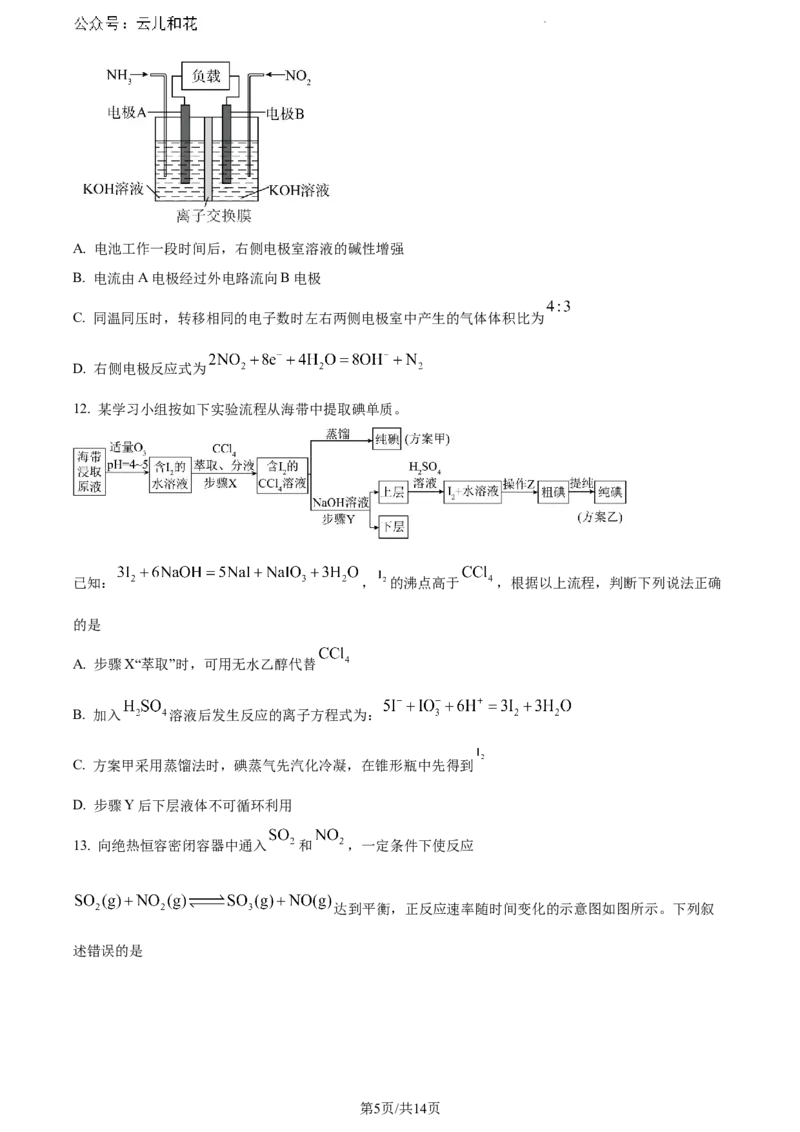
11. 为有效降低含氨化合物 排放量,又能充分利用化学能,合作小组设计如图所示电池,将含氨化合物
转化为无毒气体,离子交换膜为阴离子交换膜(只允许阴离子通过),下列说法错误的是
第4页/共14页
学科网(北京)股份有限公司A. 电池工作一段时间后,右侧电极室溶液的碱性增强
B. 电流由A电极经过外电路流向B电极
C. 同温同压时,转移相同的电子数时左右两侧电极室中产生的气体体积比为
D. 右侧电极反应式为
12. 某学习小组按如下实验流程从海带中提取碘单质。
已知: , 的沸点高于 ,根据以上流程,判断下列说法正确
的是
A. 步骤X“萃取”时,可用无水乙醇代替
B. 加入 溶液后发生反应的离子方程式为:
C. 方案甲采用蒸馏法时,碘蒸气先汽化冷凝,在锥形瓶中先得到
D. 步骤Y后下层液体不可循环利用
13. 向绝热恒容密闭容器中通入 和 ,一定条件下使反应
达到平衡,正反应速率随时间变化的示意图如图所示。下列叙
述错误的是
第5页/共14页
学科网(北京)股份有限公司A. 反应在c点 均达到最大值
B. 反应物浓度:c点小于b点
C. 段速率增大的原因是该反应放热,温度升高
D. 时, 的转化率: 段小于 段
14. 短周期主族元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁与庚的连线上),
戊、己元素在空气中含量分别为第一、第二,辛是比乙的原子序数小的同周期主族元素。下列判断错误的
是
A. 金属性:辛>乙>丙
B. 简单气态氢化物的稳定性:庚>己>戊
C. 辛、丙、戊三种元素的最高价氧化物对应的水化物之间可以相互反应
D. 元素甲的单质一定可以和元素己的单质反应生成过氧化物
15. 下列实验方案能达到相应实验目的的是
选
实验目的 实验方案
项
取 溶液,滴加 溶液 ,充分反
A 探究化学反应的限度
应,根据溶液中既含 又含 的实验事实判断该反应是可逆反应
探究 溶液对
相同条件下,向一支试管中加入 的 和 ,一支试管
B
分解速率的影
中加入 的 和 溶液,观察并比较实验现象
响
将石蜡油蒸气通过炽热的碎瓷片,石蜡油分解,产生的气体通入酸性高锰
验证石蜡油分解产物
C
中含有乙烯 酸钾溶液,观察酸性 溶液是否褪色
第6页/共14页
学科网(北京)股份有限公司比较S和 的非金属
D 向 溶液中通入 ,观察溶液中的现象
性强弱
A. A B. B C. C D. D
二、非选择题:本题共4小题,共55分。
16. 现有部分从上到下原子序数依次增大的短周期主族元素,它们的元素性质或原子结构如下表所示:
元
信息
素
Q 周期表中原子半径最小
W 最外层电子数是次外层电子数的2倍
X 常温下单质 为双原子分子,其简单氢化物水溶液呈碱性
Y 一种单质可用于供给呼吸
元素的最高价氧化物对应的水化物在第三周期中碱性最
Z
强
M 单质是一种银白色金属,其氢氧化物表现出两性
L M层电子数是电子层数的2倍
J 元素的最高化合价为 价
请按要求回答下列问题:
(1)金属性最强的元素是_______(填元素符号)。
(2)Y、Z、L对应简单离子的半径最大的是_______(填微粒符号)。
(3)元素L的气态氢化物比元素J的气态氢化物的稳定性_______(填“强”或“弱”)。
的
(4)用电子式表示由Z和J两种元素组成 化合物的形成过程:_______。
(5)元素Z的最高价氧化物对应的水化物的水溶液与元素M的最高价氧化物对应的水化物能发生化学反
应,其离子方程式为_______。
(6)由14个Q的原子和6个W的原子构成的分子有_______种同分异构体。
(7)与元素X同主族且处于第5周期的元素原子序数为_______。
17. 乙醇在一定条件下可以转化为乙醛。为揭示该变化过程,某实验小组开展了以下探究活动:
【资料查询】I.乙醇的沸点为78.5℃;II.乙醛有刺激性气味,沸点为20.8℃。
【实验探究】
(1)把一端弯成螺旋状的光亮铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有少量乙醇
的试管里,铜丝表面由黑色变为红色,反复操作几次,试管中有刺激性气味物质产生。写出上述过程中发
第7页/共14页
学科网(北京)股份有限公司生反应的总化学方程式:____。
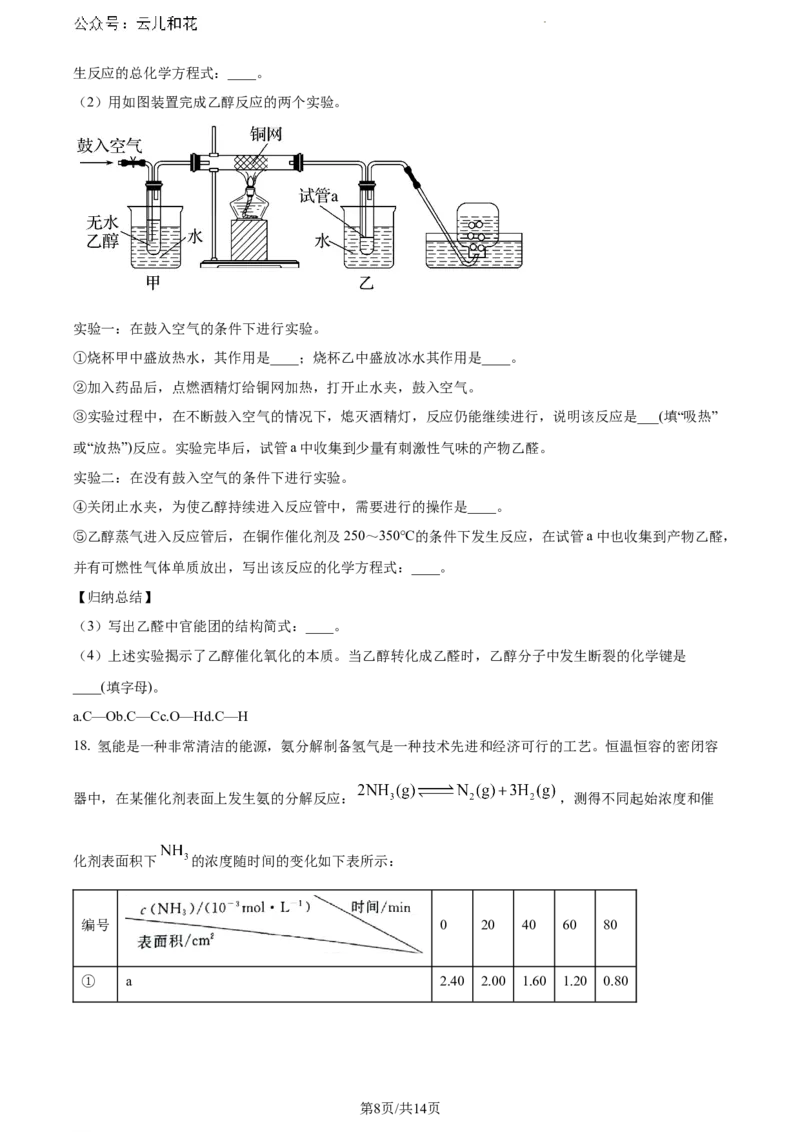
(2)用如图装置完成乙醇反应的两个实验。
实验一:在鼓入空气的条件下进行实验。
①烧杯甲中盛放热水,其作用是____;烧杯乙中盛放冰水其作用是____。
②加入药品后,点燃酒精灯给铜网加热,打开止水夹,鼓入空气。
③实验过程中,在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是___(填“吸热”
或“放热”)反应。实验完毕后,试管a中收集到少量有刺激性气味的产物乙醛。
实验二:在没有鼓入空气的条件下进行实验。
④关闭止水夹,为使乙醇持续进入反应管中,需要进行的操作是____。
⑤乙醇蒸气进入反应管后,在铜作催化剂及250~350℃的条件下发生反应,在试管a中也收集到产物乙醛,
并有可燃性气体单质放出,写出该反应的化学方程式:____。
【归纳总结】
(3)写出乙醛中官能团的结构简式:____。
(4)上述实验揭示了乙醇催化氧化的本质。当乙醇转化成乙醛时,乙醇分子中发生断裂的化学键是
____(填字母)。
a.C—Ob.C—Cc.O—Hd.C—H
18. 氢能是一种非常清洁的能源,氨分解制备氢气是一种技术先进和经济可行的工艺。恒温恒容的密闭容
器中,在某催化剂表面上发生氨的分解反应: ,测得不同起始浓度和催
化剂表面积下 的浓度随时间的变化如下表所示:
编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
第8页/共14页
学科网(北京)股份有限公司.
② a 1.20 0.80 040 x
③ 2.40 1.60 0.80 0.40 0.40
回答下列问题:
(1)关于上述实验,下列说法正确的是_____(填字母)。
A.实验②中,x的数值可能为0
B.相同条件下,增加氨气的浓度,反应速率增大
C.相同条件下,增加催化剂的表面积,反应速率增大
(2)根据上述实验和所学知识,为提高该反应的速率,下列措施可行的是_____(填字母)。
A.适当提高反应的温度
B.恒温恒压充入
C.恒温恒容充入 使压强增大
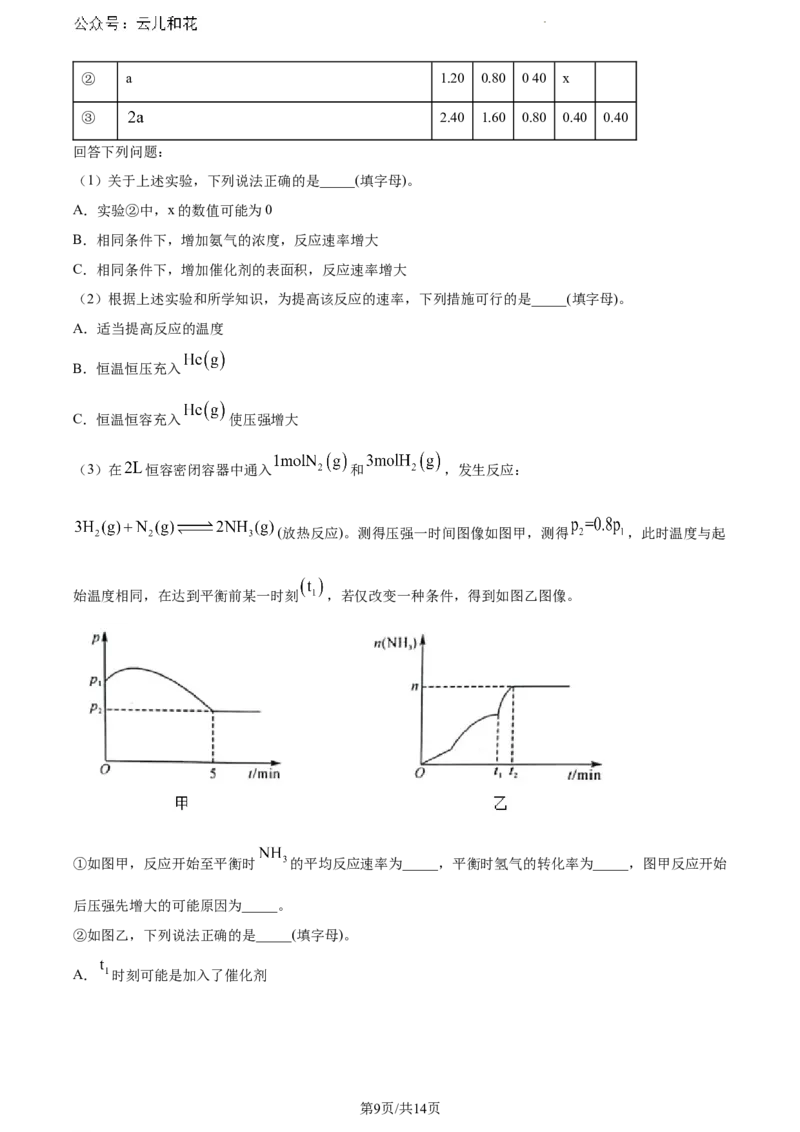
(3)在 恒容密闭容器中通入 和 ,发生反应:
(放热反应)。测得压强一时间图像如图甲,测得 ,此时温度与起
始温度相同,在达到平衡前某一时刻 ,若仅改变一种条件,得到如图乙图像。
①如图甲,反应开始至平衡时 的平均反应速率为_____,平衡时氢气的转化率为_____,图甲反应开始
后压强先增大的可能原因为_____。
②如图乙,下列说法正确的是_____(填字母)。
A. 时刻可能是加入了催化剂
第9页/共14页
学科网(北京)股份有限公司B.改变条件可以使 转化为
C. 时刻正逆反应速率均为0
D. 时刻, 的浓度与 的浓度之比为
(4) 还原 电化学法制备甲醇 的工作原理如图所示:
通入 的一端是电池的_____极(填“正”或“负”),电池工作过程中 通过质子膜向_____(填“左”
或者“右”)移动,通入 的一端发生的电极反应式为_____。
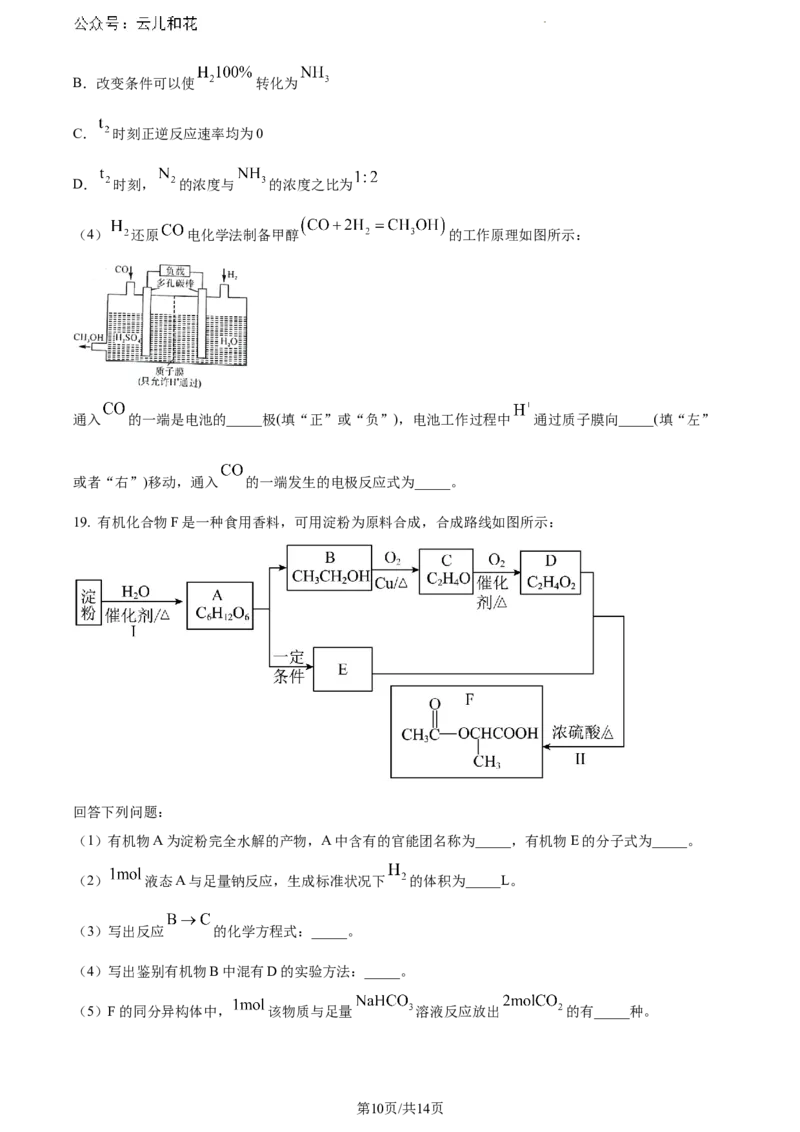
19. 有机化合物F是一种食用香料,可用淀粉为原料合成,合成路线如图所示:
回答下列问题:
(1)有机物A为淀粉完全水解的产物,A中含有的官能团名称为_____,有机物E的分子式为_____。
(2) 液态A与足量钠反应,生成标准状况下 的体积为_____L。
(3)写出反应 的化学方程式:_____。
(4)写出鉴别有机物B中混有D的实验方法:_____。
(5)F的同分异构体中, 该物质与足量 溶液反应放出 的有_____种。
第10页/共14页
学科网(北京)股份有限公司(6)下列说法错误的是_____(填字母)。
a.反应Ⅱ为取代反应
b.等物质的量的E分别与足量的 和 反应,消耗的 和 的物质的量相等
c.D、E互为同系物
(7)淀粉在酸性条件下可发生水解反应生成A,要证明淀粉已经水解完全。需要向水解后的溶液中加入
_____(填试剂名称),完全水解的实验现象为_____。
第11页/共14页
学科网(北京)股份有限公司2023~2024 学年度下学期期末质量检测
高一化学
全卷满分100分,考试时间75分钟。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将条形码粘贴在答题卡上
的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答
题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作
答;字体工整,笔迹清楚。
4.考试结束后,请将试卷和答题卡一并上交。
可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
【1题答案】
【答案】D
【2题答案】
【答案】A
【3题答案】
【答案】D
【4题答案】
【答案】B
【5题答案】
【答案】A
【6题答案】
【答案】B
【7题答案】
【答案】D
【8题答案】
【答案】C
第12页/共14页
学科网(北京)股份有限公司【9题答案】
【答案】C
【10题答案】
【答案】A
【11题答案】
【答案】B
【12题答案】
【答案】B
【13题答案】
【答案】A
【14题答案】
【答案】D
【15题答案】
【答案】B
二、非选择题:本题共4小题,共55分。
【16题答案】
【答案】(1)
(2)
(3)弱 (4)
(5)
(6)5 (7)51
【17题答案】
【答案】(1)2CHCHOH+O 2CHCHO+2H O
3 2 2 3 2
(2) ①. 使乙醇汽化 ②. 使乙醛液化 ③. 放热 ④. 加热烧杯甲 ⑤. CHCHOH
3 2
CHCHO+H
3 2
(3)—CHO (4)cd
【18题答案】
第13页/共14页
学科网(北京)股份有限公司【答案】(1)C (2)A
(3) ①. ②. 40% ③. 反应放热,温度升高的程度大于气体分子数减少的
程度,压强增大 ④. A
(4) ①. 正 ②. 左 ③.
【19题答案】
【答案】(1) ①. 羟基、醛基 ②.
(2)56 (3)
(4)取少量样品于试管中,加入少量碳酸氢钠溶液,产生气泡,证明 中混有 ;
(5)4 (6)bc
(7) ①. 碘水 ②. 加入碘水,溶液不变蓝色
第14页/共14页
学科网(北京)股份有限公司