文档内容
第一节 物质的分类及转化
【学习目标】
1.能从元素组成的角度分析认识物质,根据物质的组成和性质对物质进行分类。
2.熟知溶液、浊液、胶体三种分散系的本质区别。
3.了解胶体的性质及其应用,会鉴别胶体和溶液。
4.熟知酸、碱、盐的性质,会写相关反应的化学方程式,并判断其反应类型。
5.认识同类物质具有相似性,学会分析研究物质性质与相互转化的方法,促进“证据推理
与模型认知”化学核心素养的发展。
【基础知识】
一、物质的分类
1、元素:元素是具有相同 核电荷数 (即质子数)的一类原子的总称。
2、分子:能够独立存在并保持物质化学性质的最小微粒,由原子构成,呈电中性,具有一
定的物理化学性
3、同素异形体:同种元素形成的不同 单质 叫同素异形体。
形成方式:①原子个数不同 ,如O 和O ;② 原子排列方式不同 ,如金
2 3
刚石和石墨。
4、纯净物:由同种 单质或化合物 组成的物质。
5、混合物:由几种不同的单质或化合物组成的物质。
6、单质:由同种元素组成的纯净物 称为单质,包括金属单质和非金属单质。
7、化合物:由两种或两种以上元素 组成的纯净物称为化合物,包括酸、碱、盐、氧化物
等。
注意:常见的混合物举例:
①气体混合物
水煤气 爆鸣气 天然气 焦炉气 高炉煤气 石油气
主要成分 CO、H H 、O CH H 、CH 等 CO、CO 、N 等 丙烷、H 等
2 2 2 4 2 4 2 2 2
②液体混合物
氨水 王水 硬水 水玻璃 福尔马林 汽油
NH 3 ·H 2 O 盐酸、 含Ca2+、Mg2+ Na 2 SiO 3 、 甲醛、 C 5 ~C 11
主要成分
NH 、H O 硝酸 较多的水 H O H O 的烃
3 2 2 2
③固体混合物
碱石灰 漂白粉 玻璃 水泥 铝热剂3CaO·SiO 、
2
CaO、 Ca(ClO) 、 Na O·CaO· Al、金属
2 2
主要成分 2CaO·SiO 、
2
NaOH CaCl 6SiO 氧化物
2 2
3CaO·Al O
2 3
8、分类的方法
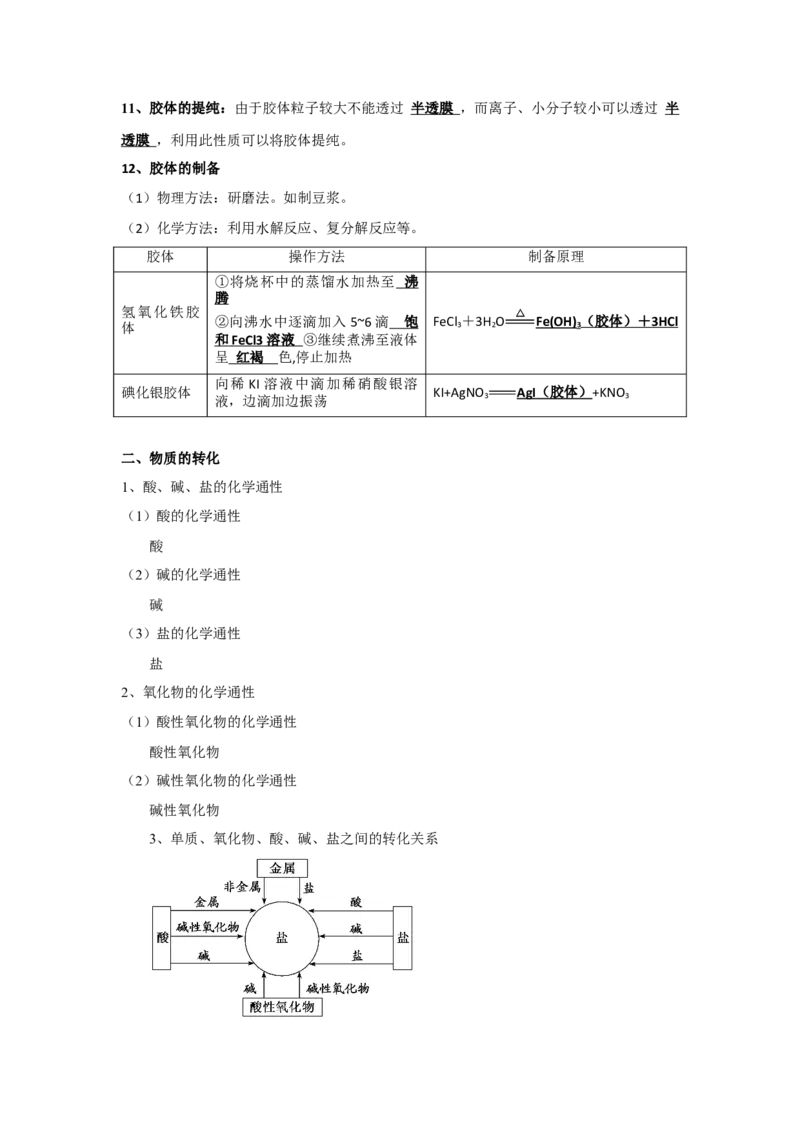
(1)树状分类法:根据对象的共同点和差异,将对象分为不同的种类,而且形成具有一定
从属关系的不同等级系统的一种分类方法。应用树状分类法可以对同类事物进行再分类。
(2)交叉分类法:根据不同的分类标准对同一物质进行分类的一种方法。在对物质进行分
类时,采用交叉分类法能从不同角度对物质进行较全面的分析。
9、分散系:一种(或多种)物质分散到另一种(或多种)物质中所得到的体系,叫做分散
系。被分散的物质称为 分散质 ,起容纳分散质作用的物质称为 分散剂 。
10、分散系的分类
溶液、胶体、浊液的比较
浊液
分散系 溶液 胶体
悬浊液 乳浊液
分散质粒子直径 小于1 nm 1~100 nm 大于100 nm 大于100 nm
稳定性 稳定 介稳体系 不稳定 不稳定
能透过滤纸,
分散质粒子能否透
均能透过 不能透过 半透 均不能透过 均不能透过
过半透膜或滤纸
膜
实例 食盐水 淀粉胶体 泥浆水 植物油和水的混合物11、胶体的提纯:由于胶体粒子较大不能透过 半透膜 ,而离子、小分子较小可以透过 半
透膜 ,利用此性质可以将胶体提纯。
12、胶体的制备
(1)物理方法:研磨法。如制豆浆。
(2)化学方法:利用水解反应、复分解反应等。
胶体 操作方法 制备原理
①将烧杯中的蒸馏水加热至 沸
腾
氢氧化铁胶
②向沸水中逐滴加入5~6滴 饱 FeCl +3H O Fe(OH) (胶体)+ 3HC l
体 3 2 3
和 FeCl3 溶液 ③继续煮沸至液体
呈 红褐 色,停止加热
向稀 KI 溶液中滴加稀硝酸银溶
碘化银胶体 KI+AgNO AgI (胶体) +KNO
液,边滴加边振荡 3 3
二、物质的转化
1、酸、碱、盐的化学通性
(1)酸的化学通性
酸
(2)碱的化学通性
碱
(3)盐的化学通性
盐
2、氧化物的化学通性
(1)酸性氧化物的化学通性
酸性氧化物
(2)碱性氧化物的化学通性
碱性氧化物
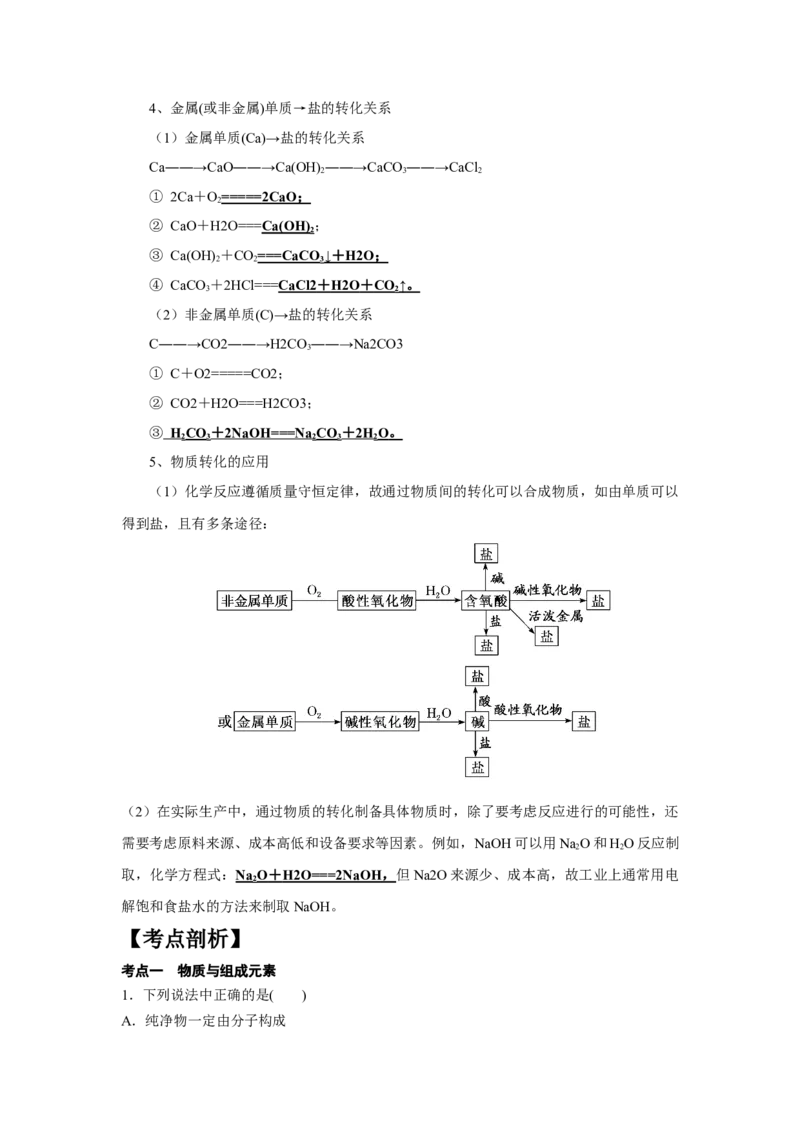
3、单质、氧化物、酸、碱、盐之间的转化关系4、金属(或非金属)单质→盐的转化关系
(1)金属单质(Ca)→盐的转化关系
Ca――→CaO――→Ca(OH) ――→CaCO ――→CaCl
2 3 2
① 2Ca+O ===== 2CaO ;
2
② CaO+H2O===Ca(OH) ;
2
③ Ca(OH) +CO===CaCO ↓ + H2O ;
2 2 3
④ CaCO +2HCl=== CaCl2 + H2O + CO ↑ 。
3 2
(2)非金属单质(C)→盐的转化关系
C――→CO2――→H2CO ――→Na2CO3
3
① C+O2=====CO2;
② CO2+H2O===H2CO3;
③ H CO + 2NaOH===N a CO + 2H O 。
2 3 2 3 2
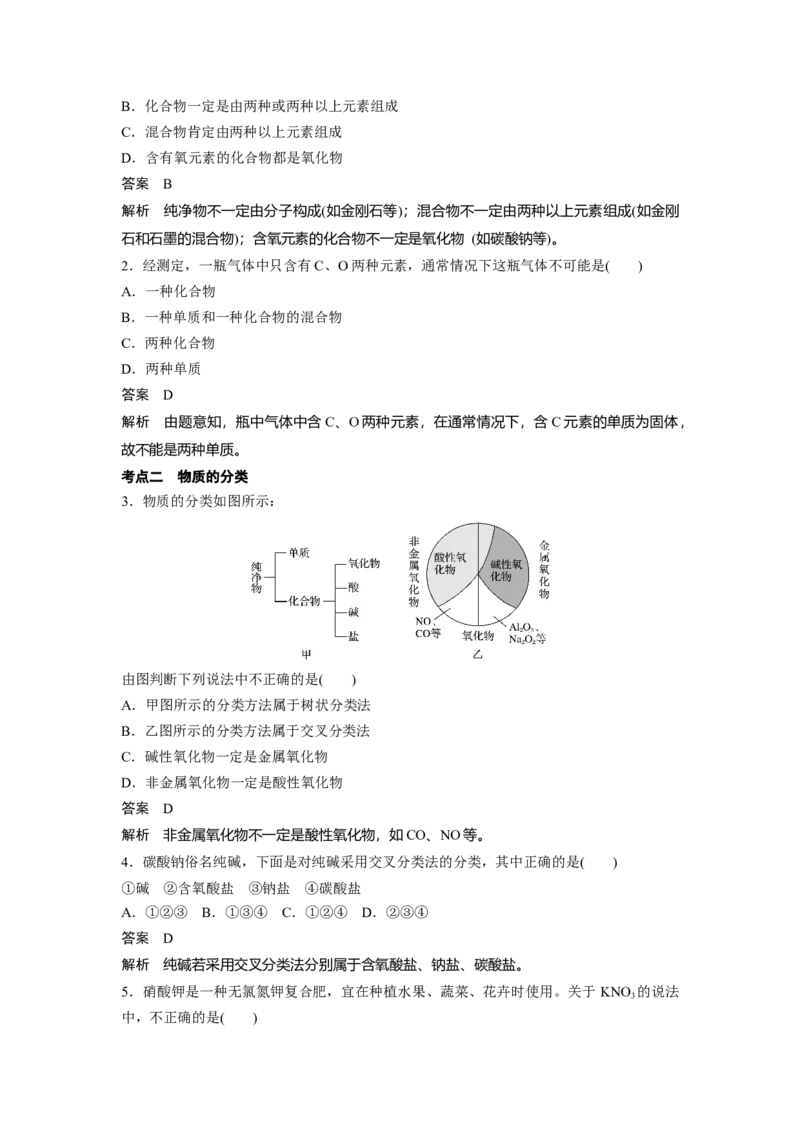
5、物质转化的应用
(1)化学反应遵循质量守恒定律,故通过物质间的转化可以合成物质,如由单质可以
得到盐,且有多条途径:
(2)在实际生产中,通过物质的转化制备具体物质时,除了要考虑反应进行的可能性,还
需要考虑原料来源、成本高低和设备要求等因素。例如,NaOH可以用NaO和HO反应制
2 2
取,化学方程式:Na O + H2O===2NaOH , 但Na2O来源少、成本高,故工业上通常用电
2
解饱和食盐水的方法来制取NaOH。
【考点剖析】
考点一 物质与组成元素
1.下列说法中正确的是( )
A.纯净物一定由分子构成B.化合物一定是由两种或两种以上元素组成
C.混合物肯定由两种以上元素组成
D.含有氧元素的化合物都是氧化物
答案 B
解析 纯净物不一定由分子构成(如金刚石等);混合物不一定由两种以上元素组成(如金刚
石和石墨的混合物);含氧元素的化合物不一定是氧化物 (如碳酸钠等)。
2.经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是( )
A.一种化合物
B.一种单质和一种化合物的混合物
C.两种化合物
D.两种单质
答案 D
解析 由题意知,瓶中气体中含C、O两种元素,在通常情况下,含C元素的单质为固体,
故不能是两种单质。
考点二 物质的分类
3.物质的分类如图所示:
由图判断下列说法中不正确的是( )
A.甲图所示的分类方法属于树状分类法
B.乙图所示的分类方法属于交叉分类法
C.碱性氧化物一定是金属氧化物
D.非金属氧化物一定是酸性氧化物
答案 D
解析 非金属氧化物不一定是酸性氧化物,如CO、NO等。
4.碳酸钠俗名纯碱,下面是对纯碱采用交叉分类法的分类,其中正确的是( )
①碱 ②含氧酸盐 ③钠盐 ④碳酸盐
A.①②③ B.①③④ C.①②④ D.②③④
答案 D
解析 纯碱若采用交叉分类法分别属于含氧酸盐、钠盐、碳酸盐。
5.硝酸钾是一种无氯氮钾复合肥,宜在种植水果、蔬菜、花卉时使用。关于 KNO 的说法
3
中,不正确的是( )A.从其阳离子看,属于钾盐
B.从其阴离子看,属于硝酸盐
C.它属于纯净物中的无机化合物
D.因为含有氧元素,故它属于氧化物
答案 D
解析 氧化物必须是只含有两种元素,且其中一种是氧元素。
考点三 分散系、胶体
6.春秋季节常出现大雾天气,对于这种现象下列说法正确的是( )
A.大雾是由于空气中的SO 超标造成的
2
B.大雾可看作是一种分散剂为水的分散系
C.大雾可看作是一种胶体
D.大雾是由于空气中的粉尘超标造成的
答案 C
解析 雾是由悬浮在大气中的微小液滴构成的气溶胶。
7.胶体区别于其他分散系的本质特征是( )
A.胶体的分散质能通过滤纸空隙,而浊液的分散质不能
B.产生丁达尔现象
C.分散质粒子直径在1~100 nm
D.胶体在一定条件下能稳定存在
答案 C
解析 三种分散系的本质区别是分散质粒子的直径大小不同,胶体区别于其他分散系的本
质特征是胶体粒子直径在1~100 nm,选C。
8.下列关于Fe(OH) 胶体的说法中,不正确的是( )
3
A.分散质粒子直径在10-9~10-7m
B.是一种纯净物
C.具有丁达尔效应
D.具有净水作用
答案 B
解析 氢氧化铁胶体胶粒的直径在10-9~10-7m,A正确; 氢氧化铁胶体是氢氧化铁和水
的混合物,B错误;胶体具有丁达尔效应,C正确;氢氧化铁胶粒能吸附水中的杂质颗粒,
有净水的作用,D正确。
9.某同学在实验室进行了如图所示的实验,下列说法中错误的是( )A.X、Z烧杯中分散质相同
B.利用过滤的方法,可将Z中固体与液体分离
C.Y中产生的气体为CO
2
D.Z中分散系能产生丁达尔效应
答案 A
解析 X是氯化铁溶液,分散质是氯离子和三价铁离子,Z是氢氧化铁胶体,分散质是氢
氧化铁胶粒,故A错误。
10.无机化合物可根据其组成和性质进行分类,
(1)如图所示的物质分类方法名称是 。
(2)以Na、K、H、O、C、S、N中任意两种或三种元素组成合适的物质,分别填写在下表
中的②③⑥后面的横线上。
物质类别 酸 碱 盐 氧化物 氢化物
①HCl ③ ⑤NaCO ⑦CO ⑨NH
2 3 2 3
化学式
② ④Ba(OH) ⑥ ⑧NaO ⑩HO
2 2 2 2
(3)写出⑦转化为⑤的化学方程式: 。
(4)写出实验室由⑩制备O 的化学方程式: 。
2
(5)实验室制备⑦常用 和 反应,检验该气体的方法是 。
答案 (1)树状分类法 (2)②HSO (或HNO 或HCO) ③NaOH(或KOH) ⑥NaSO (或
2 4 3 2 3 2 4
KCO 或 NaSO 或 NaNO 或 KNO 或 KSO ) (3)CO + 2NaOH===NaCO + HO
2 3 2 3 3 3 2 3 2 2 3 2
(4)2H O=====2HO+O↑ (5)稀盐酸 大理石(或石灰石) 将气体通入澄清石灰水中,若
2 2 2 2
石灰水变浑浊,证明气体是CO
2
解析 (2)常见的酸有HSO 、HNO 、HCl;碱有NaOH、KOH、Ba(OH) ;盐有NaCl、
2 4 3 2
NaSO 、NaCO 、NaNO 、NaSO 等。(3)酸、碱、盐、氧化物之间可以相互转化,如:
2 4 2 3 3 2 3
CO(少量)+2NaOH===NaCO +HO。(4)实验室制O 常利用HO 在催化剂作用下的分解
2 2 3 2 2 2 2
反应:2HO=====2HO+O↑。(5)制备CO 常利用大理石或石灰石(CaCO)与稀盐酸反
2 2 2 2 2 3
应:CaCO +2HCl===CaCl +CO↑+HO,将产生的气体通入澄清石灰水,若石灰水变浑
3 2 2 2
浊,即可证明气体是CO。
2
考点四 酸、碱、盐的性质
11.小明知道蛋壳的主要成分是碳酸钙,愚人节这天决定送妈妈一个“无壳鸡蛋”。他从
厨房中取来一个鸡蛋及一杯物质,将蛋泡在其中,只见蛋的表面冒出大量气泡,两天后就
得到了一个没有壳的蛋。他应取下列哪一种物质( )A.醋 B.高粱酒
C.酱油 D.食盐水
答案 A
解析 同类别的物质具有相似的性质。碳酸钙能与酸反应生成钙盐和二氧化碳气体。小明
的实验中产生大量的气泡,选用的应该是酸,醋的主要成分为醋酸。
12.在一定条件下,跟酸、碱、盐都能反应的物质是( )
A.CaO B.NaCO
2 3
C.CaCO D.CO
3 2
答案 B
解析 CaO是碱性氧化物,与碱不发生反应;CO 是酸性氧化物,与酸不发生反应;
2
NaCO 和CaCO 都是盐,但后者难溶于水,不与碱、盐发生反应,前者可以,如可分别与
2 3 3
盐酸、氢氧化钙、氯化钙等发生反应。
13.下列有关物质用途正确的是( )
A.氢氧化钠降低土壤酸性
B.用BaCl 处理大量泄漏的浓硫酸
2
C.氢氧化钙用于治疗胃酸过多
D.熟石灰配制农药波尔多液
答案 D
解析 氢氧化钠具有极强的腐蚀性,不能用于降低土壤的酸性,A错误;氯化钡是有剧毒
的物质,不能用于处理泄露的浓硫酸,B错误;氢氧化钙不能用于治疗胃酸过多,C错误;
熟石灰氢氧化钙可以用于配制农药波尔多液,D正确。
14.无色溶液X是下列四种物质中的一种。将其分成等量的三份,向其中分别加入少量
AgNO 溶液、CuO固体、NaOH溶液,产生的现象如下表。则物质X是下列选项中的(
3
)
AgNO 溶液 CuO固体 NaOH溶液
3
现象 白色沉淀 溶解,溶液变蓝 无明显现象
A.NaCl溶液 B.Ca(OH) 溶液
2
C.稀硝酸 D.稀盐酸
答案 D
解析 能使CuO固体溶解的物质为酸,稀硝酸、稀盐酸均可,能与AgNO 溶液反应生成白
3
色沉淀的为稀盐酸。
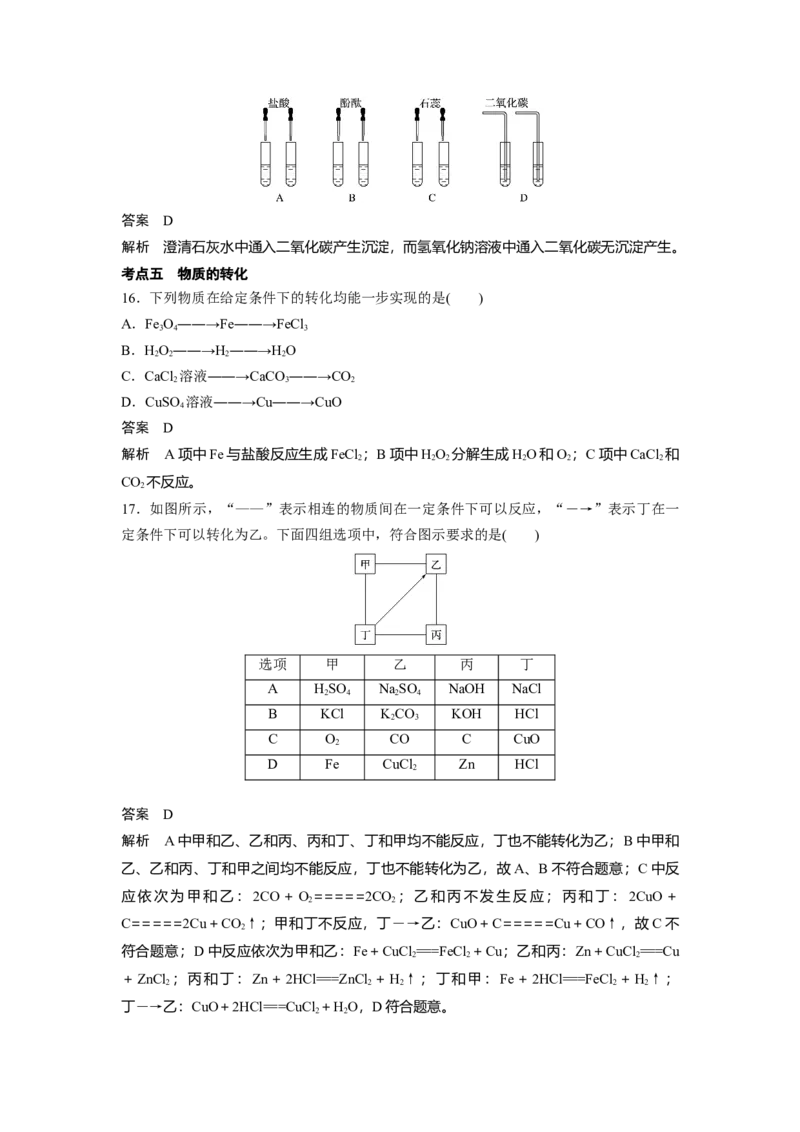
15.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如图所示的四组实验方案,其中
能达到目的的是( )答案 D
解析 澄清石灰水中通入二氧化碳产生沉淀,而氢氧化钠溶液中通入二氧化碳无沉淀产生。
考点五 物质的转化
16.下列物质在给定条件下的转化均能一步实现的是( )
A.Fe O――→Fe――→FeCl
3 4 3
B.HO――→H――→HO
2 2 2 2
C.CaCl 溶液――→CaCO ――→CO
2 3 2
D.CuSO 溶液――→Cu――→CuO
4
答案 D
解析 A项中Fe与盐酸反应生成FeCl ;B项中HO 分解生成HO和O ;C项中CaCl 和
2 2 2 2 2 2
CO 不反应。
2
17.如图所示,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一
定条件下可以转化为乙。下面四组选项中,符合图示要求的是( )
选项 甲 乙 丙 丁
A HSO NaSO NaOH NaCl
2 4 2 4
B KCl KCO KOH HCl
2 3
C O CO C CuO
2
D Fe CuCl Zn HCl
2
答案 D
解析 A中甲和乙、乙和丙、丙和丁、丁和甲均不能反应,丁也不能转化为乙;B中甲和
乙、乙和丙、丁和甲之间均不能反应,丁也不能转化为乙,故A、B不符合题意;C中反
应依次为甲和乙:2CO+O=====2CO ;乙和丙不发生反应;丙和丁:2CuO+
2 2
C=====2Cu+CO↑;甲和丁不反应,丁―→乙:CuO+C=====Cu+CO↑,故C不
2
符合题意;D中反应依次为甲和乙:Fe+CuCl ===FeCl +Cu;乙和丙:Zn+CuCl ===Cu
2 2 2
+ZnCl ;丙和丁:Zn+2HCl===ZnCl +H↑;丁和甲:Fe+2HCl===FeCl +H↑;
2 2 2 2 2
丁―→乙:CuO+2HCl===CuCl +HO,D符合题意。
2 218.现有A、B、C、D四种物质,它们分别是Fe、HCl(稀)、NaOH(溶液)、AgNO(溶液)
3
四种物质中的一种,它们之间的反应关系及所发生反应的反应类型如图:
则物质B为( )
A.Fe B.HCl(稀)
C.NaOH(溶液) D.AgNO(溶液)
3
答案 B
解析 物质B与A发生中和反应,则B为酸或碱,又由于B与C可发生置换反应,可判断
B为HCl(稀)。
19.下列物质间的转化能一步实现的是( )
A.NaCO―→NaOH B.CaCO ―→Ca(OH)
2 3 3 2
C.NaNO ―→NaCl D.FeSO ―→CuSO
3 4 4
答案 A
解析 碳酸钠可以与氢氧化钙反应生成氢氧化钠和碳酸钙,能一步实现,故 A正确;
CaCO 不溶于水,所以不能与碱溶液反应,因此CaCO 不能一步得到Ca(OH) ,故B错误;
3 3 2
NaNO 因不能与其他任何物质反应生成沉淀、气体和水,所以NaNO 不能通过一步反应制
3 3
得NaCl,故C错误;铜的金属活动性比铁弱,FeSO 不能通过一步反应制得硫酸铜,故D
4
错误。
20.对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
X牙膏 Y牙膏
摩擦剂 碳酸钙 二氧化硅
摩擦剂的物质类别(指酸、碱、盐、氧化物)
(2)根据你的推测,牙膏摩擦剂在水中的溶解性是 (填“易溶”或“难溶”)。
(3)X牙膏中的摩擦剂——碳酸钙,可以用石灰石来制备。某学生设计了一种实验室制备碳
酸钙的实验方案,其流程如图所示:
――→―――→――――――→
请写出上述方案中有关反应的化学方程式:
① ;
② ;
③ 。
答案 (1)盐 氧化物 (2)难溶 (3)①CaCO =====CaO+CO↑ ②CaO+HO===Ca(OH)
3 2 2 2③Ca(OH) +NaCO===CaCO ↓+2NaOH
2 2 3 3
解析 (1)碳酸钙属于盐,二氧化硅属于氧化物。(2)摩擦剂的作用是除去牙齿上残留的食物,
联系日常生活中用砂纸来摩擦金属以除去金属表面的锈迹,可知摩擦剂应为坚硬难溶的物
质。