文档内容
高二考试化学试卷
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第二册,选择性必修1第一章至第二章。
5.可能用到的相对原子质量:
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1.化学与生产、生活具有紧密的联系。下列说法正确的是( )。
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.二氧化硫具有抗氧化性,可大量用作葡萄酒的添加剂
C.含自然铜成分的中成药大七厘散(处方药),其包装上有“OTC”标识
D.富勒烯、碳纳米管、石墨烯都属于新型无机非金属材料
2.下列变化过程的 、 的是( )。
A. B.
C. D.
3.下列措施能提高合成氨反应速率的是( )。
A.降低温度 B.恒容条件下加入惰性气体
C.增大氮气的浓度 D.恒压条件下加入惰性气体
4.物质a和物质b在图甲装置中发生反应,一段时间后,U形管内红墨水的液面高度如图乙所示,则物质
a和物质b可能是( )。
选项 物质a 物质b
A 水 生石灰
B 稀盐酸 固体C 稀硫酸 锌粉
D 稀盐酸 小苏打
5.下列关于中和反应反应热测定实验的说法错误的是( )。
A.可以用铁棒代替玻璃搅拌器
B.用同一支温度计测量温度可减小实验误差
C.反应物应一次性加入,且不能有液体溅出
D.稀溶液中, 与 完全反应放出的热量等于
6.下列对活化分子的理解正确的是( )。
A.能发生碰撞的分子是活化分子 B.能发生有效碰撞的分子是活化分子
C.能量较低的分子是活化分子 D.能量高于普通分子的分子是活化分子
7.乙烯是一种重要的基本化工原料,主要用于制造塑料、合成橡胶、合成纤维等。利用 氧化乙烷制
备乙烯的反应为 ,该反应达到平衡后,
下列措施不能提高 平衡产率的是( )。
A.升高温度 B.移除部分
C.压缩容器体积 D.增大 的浓度
8.下列事实能用勒夏特列原理解释的是( )。
A.打开冰镇啤酒,有大量气泡冒出 B.利用铝热反应焊接铁轨
C.利用干冰进行灭火 D.工业生产硫酸的过程中将黄铁矿粉碎后加入沸腾炉
9.某温度下,在密闭容器中充入一定量的 ,发生反应:① ;②
。已知:反应①的反应速率大于反应②。下列反应进程示意图符合题意的是(
)。
A. B. C. D.
10.向 的恒容密闭容器中加入一定量的 和 ,发生反应:
, 后C的浓度增加了 ,下列说法正确的是( )。
A.向容器中充入惰性气体可以加快化学反应速率B. 内,
C. 时,D的物质的量为
D.当 时,反应达到平衡状态
11.下列数据表示反应 在四种不同条件下的化学反应速率,其中化学
反应速率最快的是( )。
A. B.
C. D.
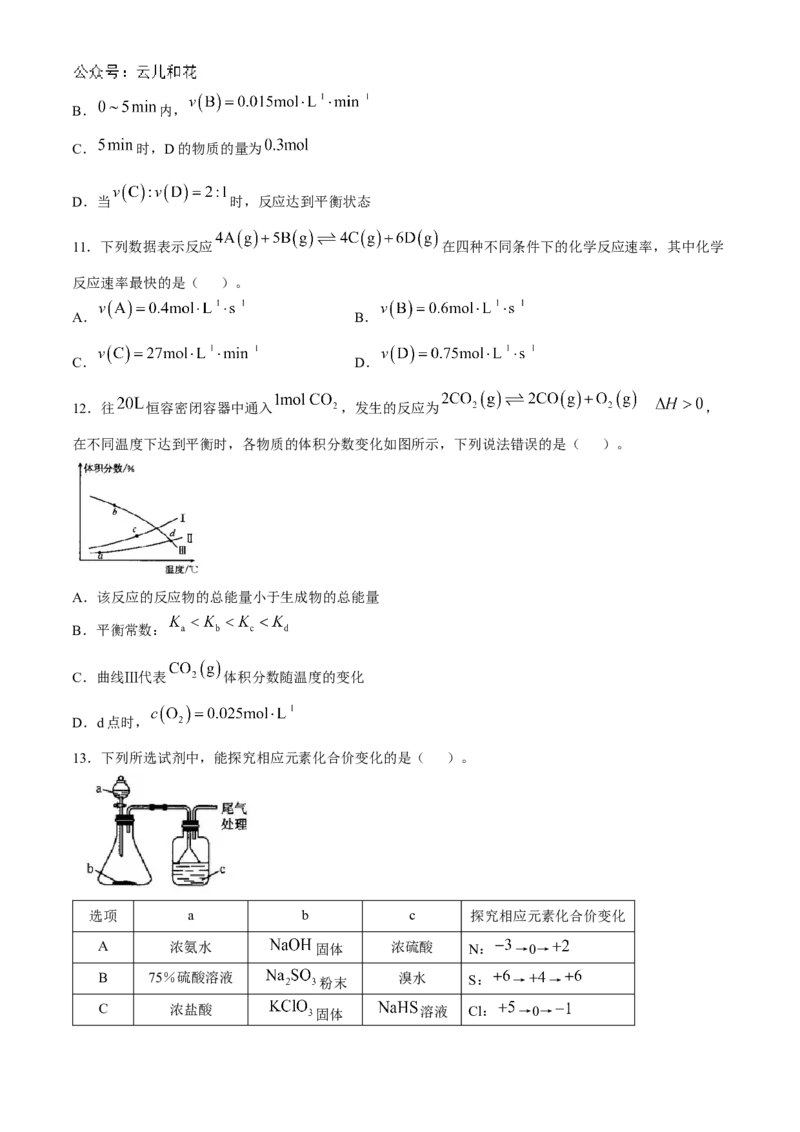
12.往 恒容密闭容器中通入 ,发生的反应为 ,
在不同温度下达到平衡时,各物质的体积分数变化如图所示,下列说法错误的是( )。
A.该反应的反应物的总能量小于生成物的总能量
B.平衡常数:
C.曲线Ⅲ代表 体积分数随温度的变化
D.d点时,
13.下列所选试剂中,能探究相应元素化合价变化的是( )。
选项 a b c 探究相应元素化合价变化
A 浓氨水 固体 浓硫酸 N: →0→
B 75%硫酸溶液 粉末 溴水 S: → →
C 浓盐酸 固体 溶液 Cl: →0→D 稀硫酸 固体 溶液 Fe: → →
14.在 的密闭容器中进行如下反应: 。 内用X表示的平均反应
速率为 ,则 内,物质Z的物质的量的变化量( )。
A.等于 B.小于
C.等于 D.大于 ,小于
15.对于反应 ,根据下列图示信息得到的结论正确的是( )。
A.甲图: B.乙图:
C.丙图:点1对应的 D.丁图:Ⅰ对应的反应温度大于Ⅱ对应的
二、非选择题:本题共4小题,共55分。
16.(14分)丙烷 是一种重要的化工原料和能源产品,具有广泛的用途。
(1)①已知:在25℃、 下, 燃烧生成 和 时放出 热量。
的物质的量为__________mol; 燃烧热的热化学方程式为__________。
②已知 ,该反应中,反应物的总键能__________
(填“>”或“<”)生成物的总键能。
③根据①②计算: 在适量 中完全反应生成 、 和 ,共放出
热量,则反应过程中共生成了__________mol CO。
(2)T℃,向 的密闭容器中充入 和 ,仅发生反应
,充分反应达到平衡状态时放出 热量,则 的平衡转化率为__________;下列措施中,能加快反应速率且能提高
平衡转化率的为__________(填标号)。
a.压缩容器体积 b.加入催化剂 c.降低温度 d.增大 的浓度
(3) 可以制备丙烯和氢气,发生的反应为
,该反应中,正反应的活化能__________(填“>”“<”或“=”)逆反应的活
化能。
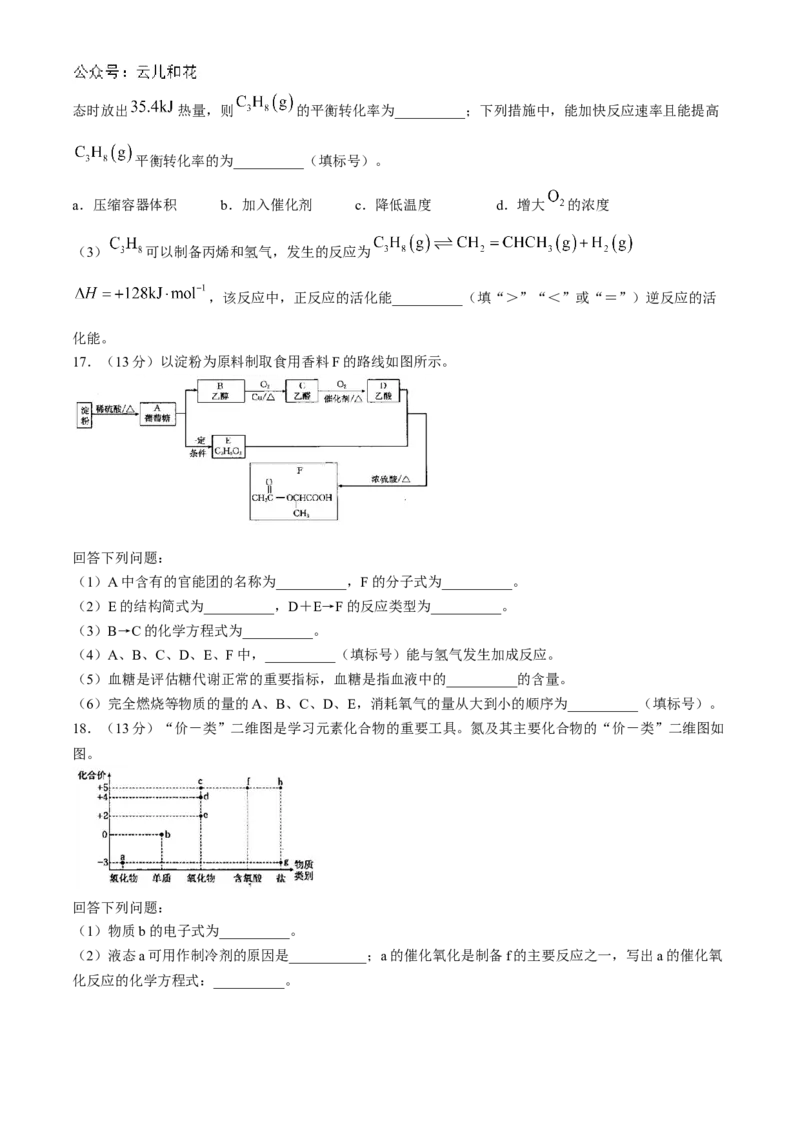
17.(13分)以淀粉为原料制取食用香料F的路线如图所示。
回答下列问题:
(1)A中含有的官能团的名称为__________,F的分子式为__________。
(2)E的结构简式为__________,D+E→F的反应类型为__________。
(3)B→C的化学方程式为__________。
(4)A、B、C、D、E、F中,__________(填标号)能与氢气发生加成反应。
(5)血糖是评估糖代谢正常的重要指标,血糖是指血液中的__________的含量。
(6)完全燃烧等物质的量的A、B、C、D、E,消耗氧气的量从大到小的顺序为__________(填标号)。
18.(13分)“价-类”二维图是学习元素化合物的重要工具。氮及其主要化合物的“价-类”二维图如
图。
回答下列问题:
(1)物质b的电子式为__________。
(2)液态a可用作制冷剂的原因是___________;a的催化氧化是制备f的主要反应之一,写出a的催化氧
化反应的化学方程式:__________。(3)为提高氮元索的原子利用率,并减少环境污染,工业上用废铜屑、 溶液和f的稀溶液制备
,该反应的离子方程式为__________。
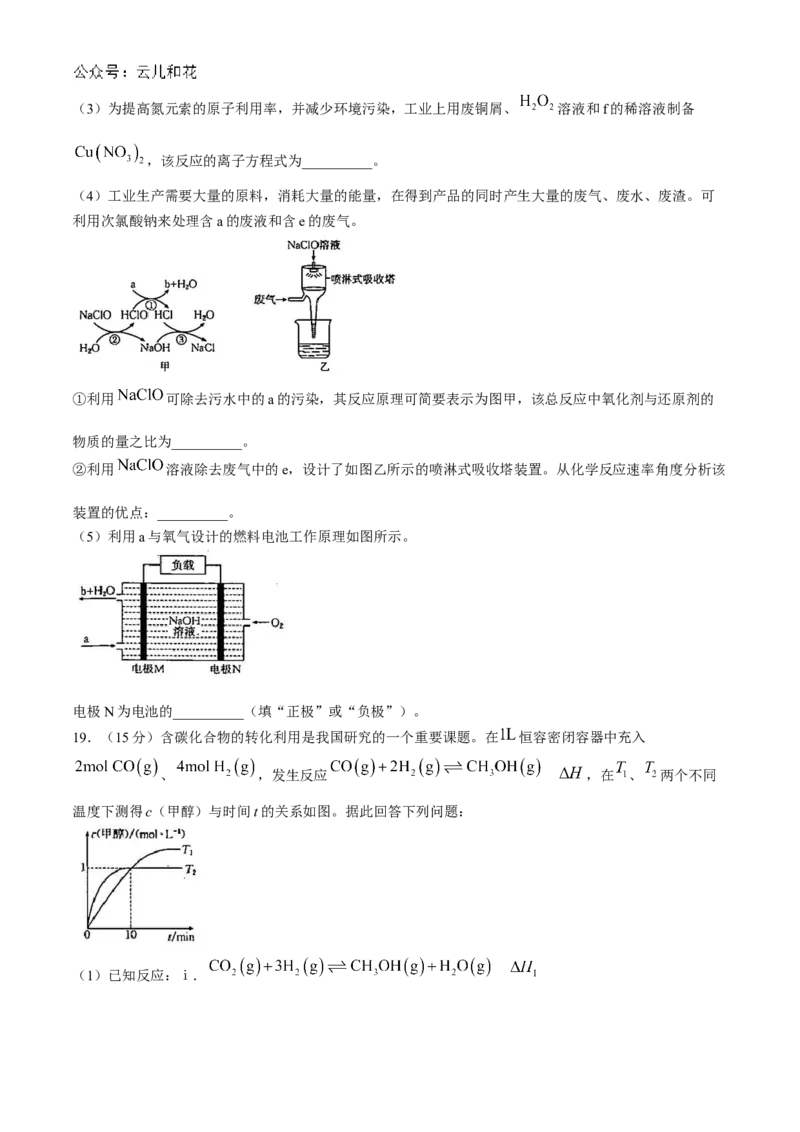
(4)工业生产需要大量的原料,消耗大量的能量,在得到产品的同时产生大量的废气、废水、废渣。可
利用次氯酸钠来处理含a的废液和含e的废气。
①利用 可除去污水中的a的污染,其反应原理可简要表示为图甲,该总反应中氧化剂与还原剂的
物质的量之比为__________。
②利用 溶液除去废气中的e,设计了如图乙所示的喷淋式吸收塔装置。从化学反应速率角度分析该
装置的优点:__________。
(5)利用a与氧气设计的燃料电池工作原理如图所示。
电极N为电池的__________(填“正极”或“负极”)。
19.(15分)含碳化合物的转化利用是我国研究的一个重要课题。在 恒容密闭容器中充入
、 ,发生反应 ,在 、 两个不同
温度下测得c(甲醇)与时间t的关系如图。据此回答下列问题:
(1)已知反应:ⅰ.ⅱ.
则 __________(填含 、 的表达式)。
(2)在 温度下, 内用 表示的反应速率 __________ ; 时,
CO的转化率为__________。
(3)图中反应温度: __________ (填“>”“=”或“<”,下同), __________0,反应
在__________(填“高温”“低温”或“任意温度”)下能自发进行。
(4)在 温度下,该反应的平衡常数为__________(不写单位),达到平衡后向容器中再充入CO、
、 各 ,此时反应速率: __________ (填“>”“=”或“<”)。高二考试化学试卷参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
D B C D A B C A A C D D C B C
16.(1)
①0.25(2分); (2分)
②<(2分)
③1(2分)
(2)30%(2分);d(2分)
(3)>(2分)
17.(1)羟基、醛基(2分); (1分)
(2) (2分);酯化反应(或取代反应,1分)
(3) (2分)
(4)A、C(2分)
(5)葡萄糖(1分)
(6)A>B=E>C>D(2分)
18.(1) (2分)
(2)液氨汽化时吸收大量的热,使周围温度急剧降低(2分); (2
分)
(3) (2分)
(4)① (2分)
②气液逆流法使得反应物充分接触,增大接触面积,反应速率加快(2分)
(5)正极(1分)
19.(1) (2分)
(2)0.2(2分);50%(2分)
(3)<(2分);<(2分);低温(1分)
(4)0.25(2分);>(2分)