文档内容
2025-2026 学年上学期高二期中考试
化学
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.本试卷主要考试内容:人教版必修第一册、必修第二册、选择性必修1第一章至第三章第
二节。
5.可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与生产、生活密切相关。下列物质的主要成分属于金属的是
A.《论语》书本 B.玉手镯
C.一次性塑料碗 D.铜鼎
A. A B. B C. C D. D
2. 下列变化中没有发生熵增的是
第1页/共7页
学科网(北京)股份有限公司A. 气态水变成冰 B. 煅烧石灰石
C. 蔗糖溶解在水中 D. 氯化铵固体受热分解成氯化氢和氨气
3. 催化加氢可制取乙烯: 。反应过程中, (g)与
(g)的反应速率之比为
A. 1:3 B. 2:1 C. 3:2 D. 1:4
4. 下列物质属于非电解质的是
A. Cu B. C. KOH D.
5. 盐酸和醋酸是生活中经常用到的酸。下列说法错误的是
A. 盐酸和醋酸溶液均不属于电解质
B. 适当升高温度有利于 增大
C. HCl在水溶液中的电离方程式为:
D. 浓度均为0.1 的盐酸和醋酸溶液中,所含的 均为0.1
6. 下列说法正确的是
的
A. 所有放热 自发过程均为熵减过程
B. 常温常压下 大于0的反应一定不能自发进行
C. 其他条件不变,升高温度,吸热反应的反应速率加快,放热反应的反应速率减慢
D. (g)与 (g)生成 (g)的反应中,催化剂能减小该反应的焓变
7. 下列有关氢硫酸( )的说法正确的是
A. 氢硫酸溶液中,不存在 分子
B. 25℃时,电离平衡常数:
C. 的第二步电离平衡常数
D. 由反应 可知,酸性:
第2页/共7页
学科网(北京)股份有限公司8. 在某恒温恒压密闭容器中,当反应 , 达到平衡时,下列措施不能
的
提高 平衡转化率 是(每次仅改变一个条件)
的
A. 充入少量 He B. 适当降低温度 C. 及时抽走部分 (g) D. 增大 (g)的浓度
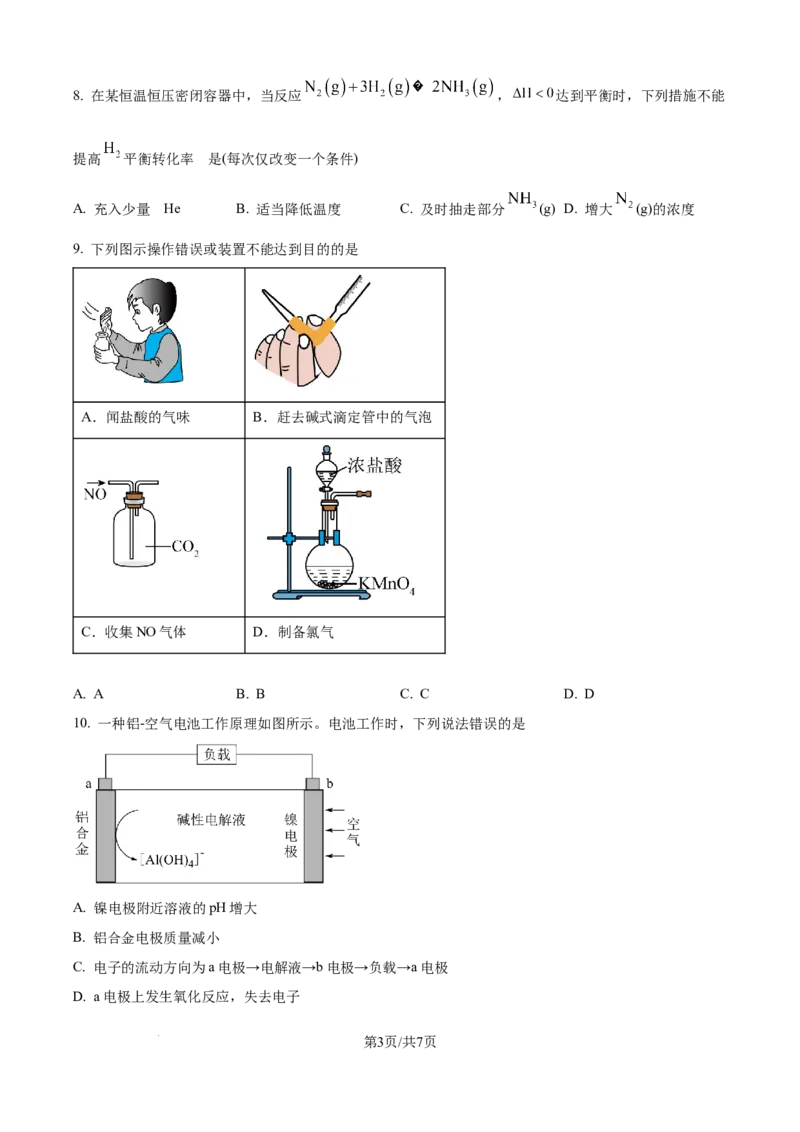
9. 下列图示操作错误或装置不能达到目的的是
A.闻盐酸的气味 B.赶去碱式滴定管中的气泡
C.收集NO气体 D.制备氯气
A. A B. B C. C D. D
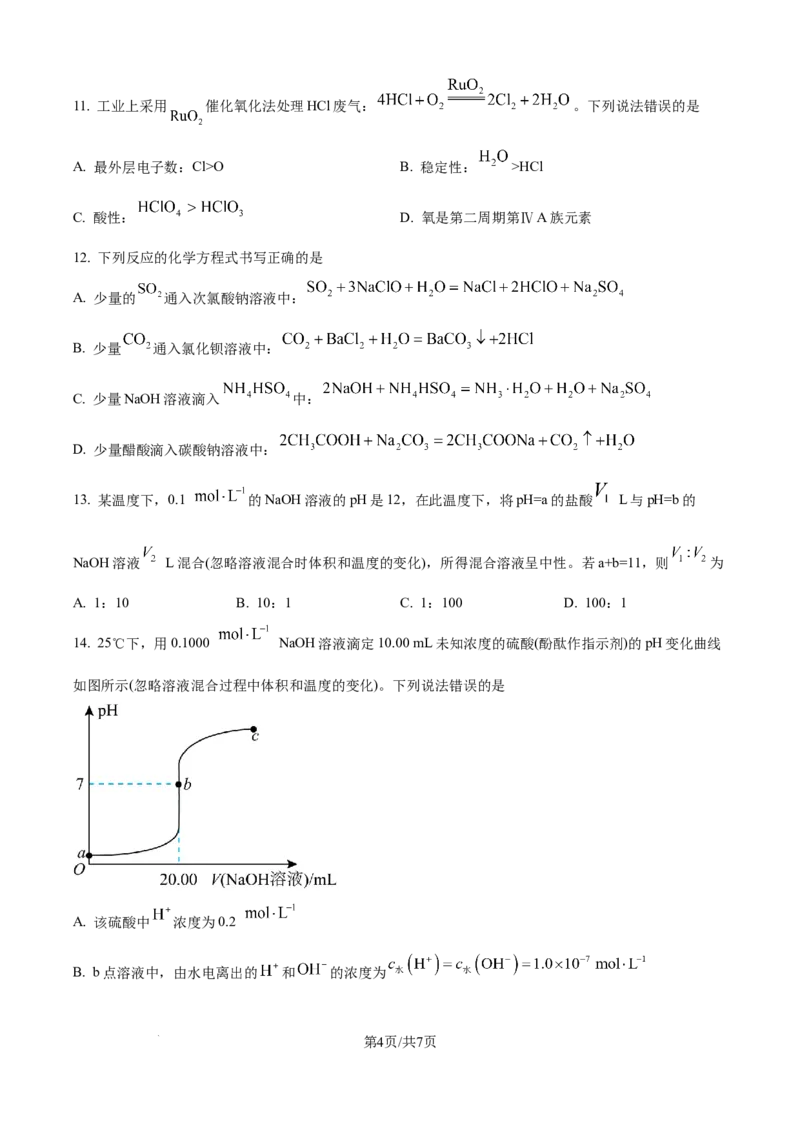
10. 一种铝-空气电池工作原理如图所示。电池工作时,下列说法错误的是
A. 镍电极附近溶液的pH增大
B. 铝合金电极质量减小
C. 电子的流动方向为a电极→电解液→b电极→负载→a电极
D. a电极上发生氧化反应,失去电子
第3页/共7页
学科网(北京)股份有限公司11. 工业上采用 催化氧化法处理HCl废气: 。下列说法错误的是
A. 最外层电子数:Cl>O B. 稳定性: >HCl
C. 酸性: D. 氧是第二周期第ⅣA族元素
12. 下列反应的化学方程式书写正确的是
A. 少量的 通入次氯酸钠溶液中:
B. 少量 通入氯化钡溶液中:
C. 少量NaOH溶液滴入 中:
D. 少量醋酸滴入碳酸钠溶液中:
13. 某温度下,0.1 的NaOH溶液的pH是12,在此温度下,将pH=a的盐酸 L与pH=b的
NaOH溶液 L混合(忽略溶液混合时体积和温度的变化),所得混合溶液呈中性。若a+b=11,则 为
A. 1:10 B. 10:1 C. 1:100 D. 100:1
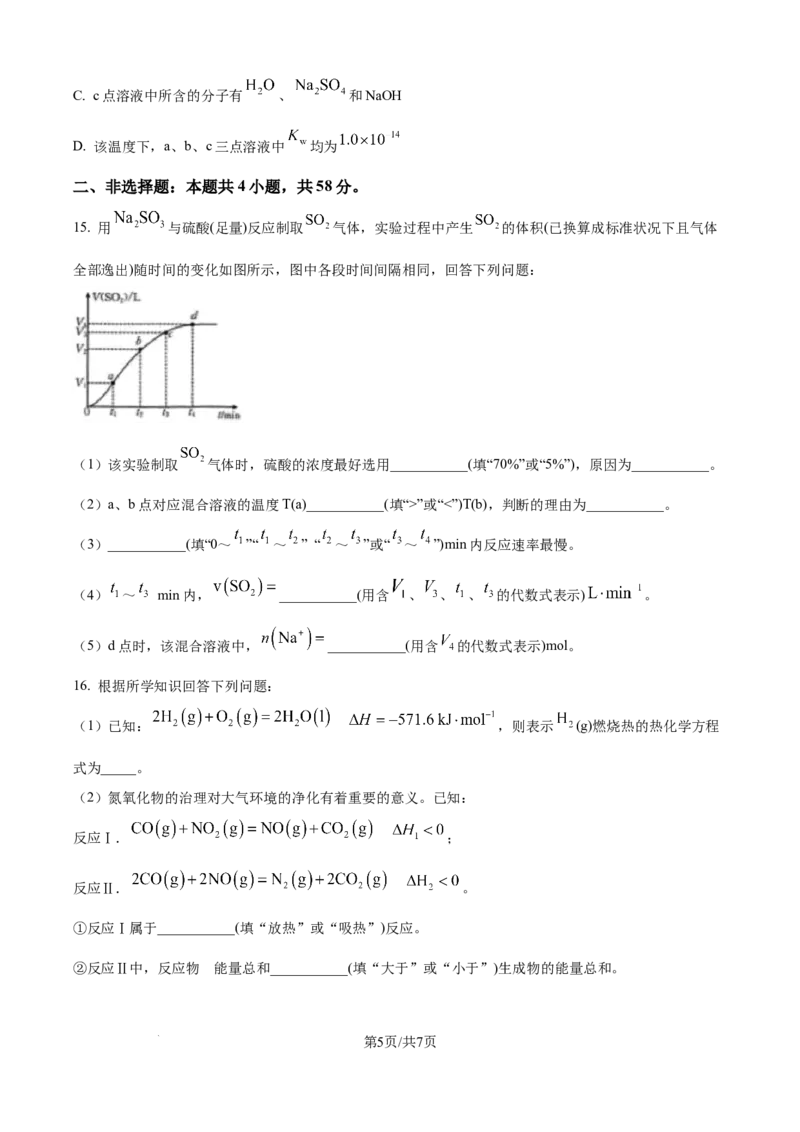
14. 25℃下,用0.1000 NaOH溶液滴定10.00 mL未知浓度的硫酸(酚酞作指示剂)的pH变化曲线
如图所示(忽略溶液混合过程中体积和温度的变化)。下列说法错误的是
A. 该硫酸中 浓度为0.2
B. b点溶液中,由水电离出的 和 的浓度为
第4页/共7页
学科网(北京)股份有限公司C. c点溶液中所含的分子有 、 和NaOH
D. 该温度下,a、b、c三点溶液中 均为
二、非选择题:本题共4小题,共58分。
15. 用 与硫酸(足量)反应制取 气体,实验过程中产生 的体积(已换算成标准状况下且气体
全部逸出)随时间的变化如图所示,图中各段时间间隔相同,回答下列问题:
(1)该实验制取 气体时,硫酸的浓度最好选用___________(填“70%”或“5%”),原因为___________。
(2)a、b点对应混合溶液的温度T(a)___________(填“>”或“<”)T(b),判断的理由为___________。
(3)___________(填“0~ ”“ ~ ” “ ~ ”或“ ~ ”)min内反应速率最慢。
(4) ~ min内, ___________(用含 、 、 、 的代数式表示) 。
(5)d点时,该混合溶液中, ___________(用含 的代数式表示)mol。
16. 根据所学知识回答下列问题:
(1)已知: ,则表示 (g)燃烧热的热化学方程
式为_____。
(2)氮氧化物的治理对大气环境的净化有着重要的意义。已知:
反应Ⅰ. ;
反应Ⅱ. 。
①反应Ⅰ属于___________(填“放热”或“吸热”)反应。
的
②反应Ⅱ中,反应物 能量总和___________(填“大于”或“小于”)生成物的能量总和。
第5页/共7页
学科网(北京)股份有限公司③反应Ⅲ. 的 ___________(填“>”或“<”)0。
④下列反应的能量变化与反应Ⅲ的能量变化相符的是___________(填标号)。
a.生石灰溶于水 b.金属钠溶于水
c.稀盐酸与碳酸氢钠的反应 d.氯化铵固体与 的反应
(3)已知反应: 。相关化学键键能数据如表所示。
化学键 C-H C-F H-F F-F
键能/( ) x y z q
① ___________(用含x、y、z、q的代数式表示) 。
②该反应中,每生成0.2 mol HF(g),转移电子的数目为___________ 。
17. 某温度下,向2L的某恒容密闭容器中仅充入 气体 和 气体 ,在一定条件下发生反应:
。反应 时,测得 的物质的量减少了 ,B的物质的量减少
了 ,有 生成,平均反应速率 。回答下列问题:
(1) 时, _______(用含 、 的代数式表示) ,D的物质的量分数为_______(用含
、 的代数式表示)。
(2)若 为 ,B为 ,D为 ,则上述反应的化学方程式为_______。该反应中,每转移
电子,生成 的体积为_______ (标准状况下)。
(3) 时,该反应达到平衡,此时测得 的物质的量为 。
①B的平衡转化率为_______%(用含 、 的代数式表示,写出计算式即可)。
第6页/共7页
学科网(北京)股份有限公司② 内, _______(用含 的代数式表示) 。
③该反应的平衡常数为_______(用含 、 的代数式表示,写出计算式即可)。
④保持其他条件不变,仅增大压强,此时该反应的平衡常数将_______(填“增大”“减小”或“不变”)。
18. 氨水为实验室常用的化学试剂,回答下列问题:
(1) 的电离方程式为 。
① ___________(填“>”或“<”)0。
②适当升高温度, ___________(填“增大”“减小”或“不变”)。
(2)25℃时,将0.2 氨水加水稀释至0.02 。
①稀释过程中, ___________(填“增大”“减小”或“不变”,下同)。
②稀释过程中,所含氮元素的质量___________。
(3)已知:25℃下, 。
①查阅资料可知,25℃下, 溶液呈中性。 ___________(填“>”“<”或
“=”) 。
②0.2 的氨水中, 约为___________ 。
(4)将3.36 L(标准状况下)氨气溶于水配制成1 L溶液,则溶液中_________。
+___________+___________=0.15 mol。
第7页/共7页
学科网(北京)股份有限公司