文档内容
余姚中学 2024 学年第二学期期中检测高二化学试卷
出卷:张丽丽 审卷:潘爱萍
可能用到的相对原子质量:H-1C-12N-14O-16Na-23S-32Ga-70I-127
一、选择题(本大题共16小题,每小题3分,共48分,每小题列出的四个备选
项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.下列物质属于强电解质的是
A.邻羟基苯甲酸 B.SO C.C H NH Cl D.Mg(OH)
3 2 5 3 2
2.化学与人类社会可持续发展息息相关。下列说法不正确的是
A.乙酸甘油酯在碱性条件下水解,该反应可用于肥皂的生产
B.天然气作为化工原料主要用于合成氨和生产甲醇等
C.制作豆腐时加入氯化镁、硫酸钙等凝固剂,可使豆浆中的蛋白质聚沉
D.工业上,可经过原子利用率都是100%的两步反应,实现由乙烯合成乙二醇
3.下列说法不正确的是
A.乙炔燃烧放出大量的热,常用于焊接和切割金属,平时用丙酮溶解储存在钢瓶中
B.蛋白质遇酶能发生水解,用加酶洗衣粉洗涤真丝织品可快速去污
C.工业上常用硫与橡胶作用,使其硫化,从而增强其强度和韧性
D.聚丙烯酸钠是一种吸水性很强的功能高分子材料
4.下列说法不正确的是
A.可用CO 气体鉴别Na SiO 溶液和澄清石灰水
2 2 3
B.锂和钠同主族,在过量氧气中燃烧均生成正常氧化物
C.为配制较高浓度的碘水,通常将碘单质溶于一定浓度的KI溶液中
D.氢硫酸中通入SO 气体会出现浑浊
2
5.下列表达正确的是
A. 硬脂酸的分子式:C H O
18 34 2
B. 用电子式表示HCl的形成过程:
C.H 的共价键电子云轮廓图:
2
D.NH 分子的球棍模型:
3
6.短周期元素X、Y、Z、Q的原子序数依次增大,X原子的价层电子数是电子层数的2倍,
Y的基态原子s能级与p能级电子数相等,Z是地壳中含量最多的金属元素,Q与Y同主族,
下列说法不正确的是
A.分子的极性:XY >QY
2 2
B.最简单氢化物的热稳定性:Y>Q
C.沸点:XQ >XY
2 2
D.离子键成分的百分数:Z Y >Z Q
2 3 2 3
7.下列说法不
.
正
.
确
.
的是
A. 可用饱和碳酸钠提纯制得的乙酸乙酯
B. 通过X射线法衍射可获得青蒿素的分子结构
C.1mol葡萄糖可水解生成2mol乳糖
D. 由于F-C的极性大于Cl-C,则可知三氟乙酸(CF COOH)的酸性大于三氯乙酸(CCl COOH)
3 3
第 1 页 共 8 页8.下列化学反应与方程式不
.
相
.
符
.
的是
A.少量FeCl 固体加入到KI浓溶液中:2Fe3++3I-=2Fe2++I -
3 3
B.Cu和浓HNO 反应:Cu+4H++2NO -=Cu2++2NO ↑+2H O
3 3 2 2
C.Al (SO ) 溶液与Na[Al(OH) ]溶液反应:Al (SO ) +6Na[Al(OH) ]=3Na SO +8Al(OH) ↓
2 4 3 4 2 4 3 4 2 4 3
D.少量甲醛与新制Cu(OH) 反应:HCHO+2Cu(OH)+NaOH HCOONa+CuO↓+3HO
2 2 2 2
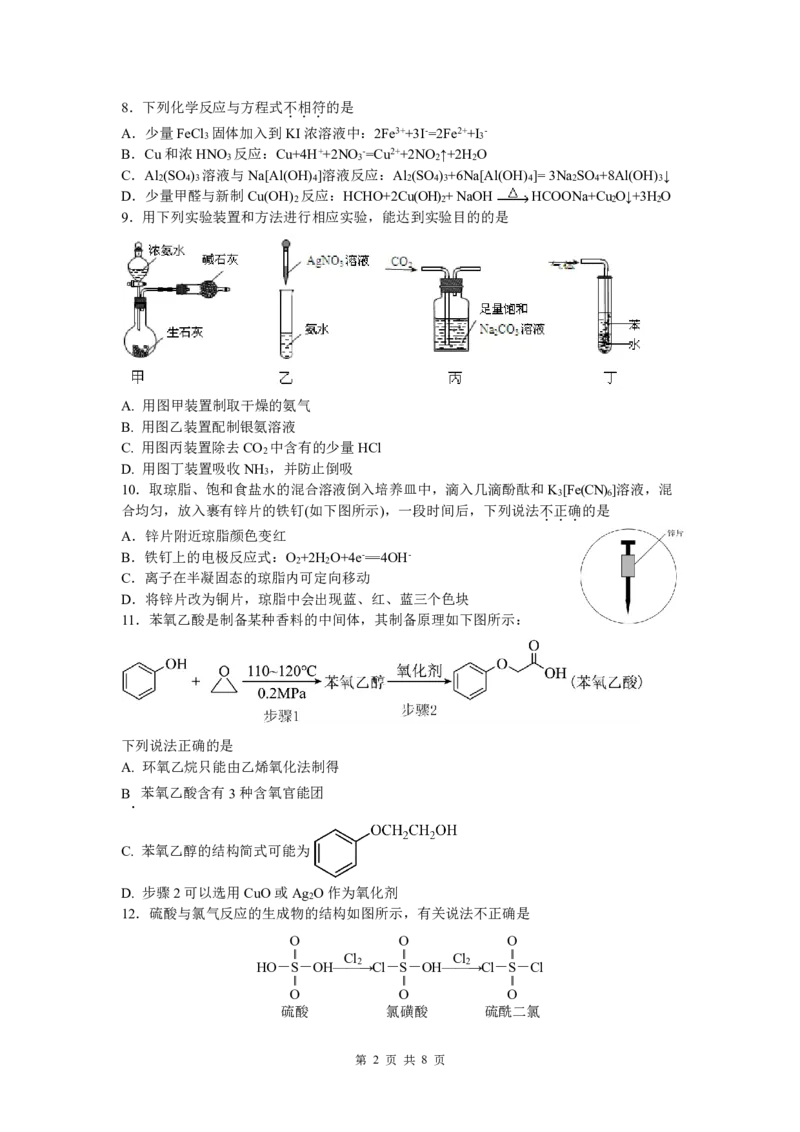
9.用下列实验装置和方法进行相应实验,能达到实验目的的是
A. 用图甲装置制取干燥的氨气
B. 用图乙装置配制银氨溶液
C. 用图丙装置除去CO 中含有的少量HCl
2
D. 用图丁装置吸收NH ,并防止倒吸
3
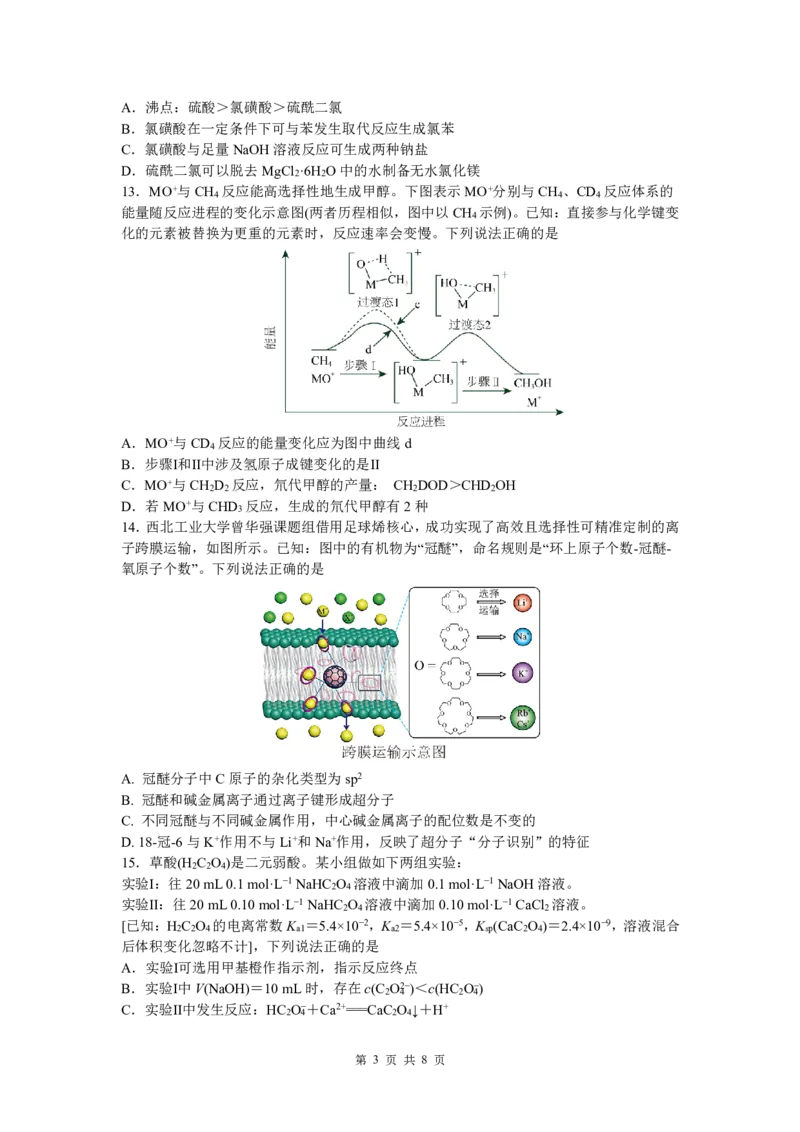
10.取琼脂、饱和食盐水的混合溶液倒入培养皿中,滴入几滴酚酞和K [Fe(CN)]溶液,混
3 6
合均匀,放入裹有锌片的铁钉(如下图所示),一段时间后,下列说法不
.
正
.
确
.
的是
A.锌片附近琼脂颜色变红
B.铁钉上的电极反应式:O +2H O+4e-=4OH-
2 2
C.离子在半凝固态的琼脂内可定向移动
D.将锌片改为铜片,琼脂中会出现蓝、红、蓝三个色块
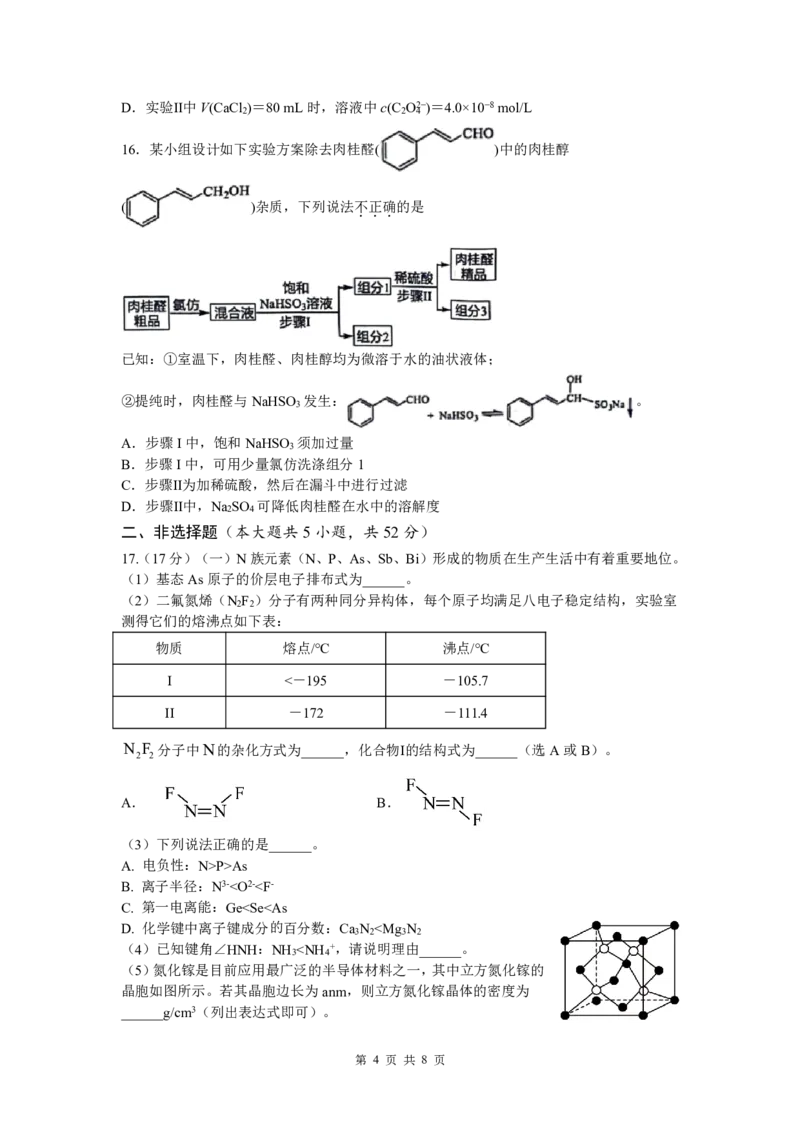
11.苯氧乙酸是制备某种香料的中间体,其制备原理如下图所示:
下列说法正确的是
A. 环氧乙烷只能由乙烯氧化法制得
B 苯氧乙酸含有3种含氧官能团
.
C. 苯氧乙醇的结构简式可能为
D. 步骤2可以选用CuO或Ag O作为氧化剂
2
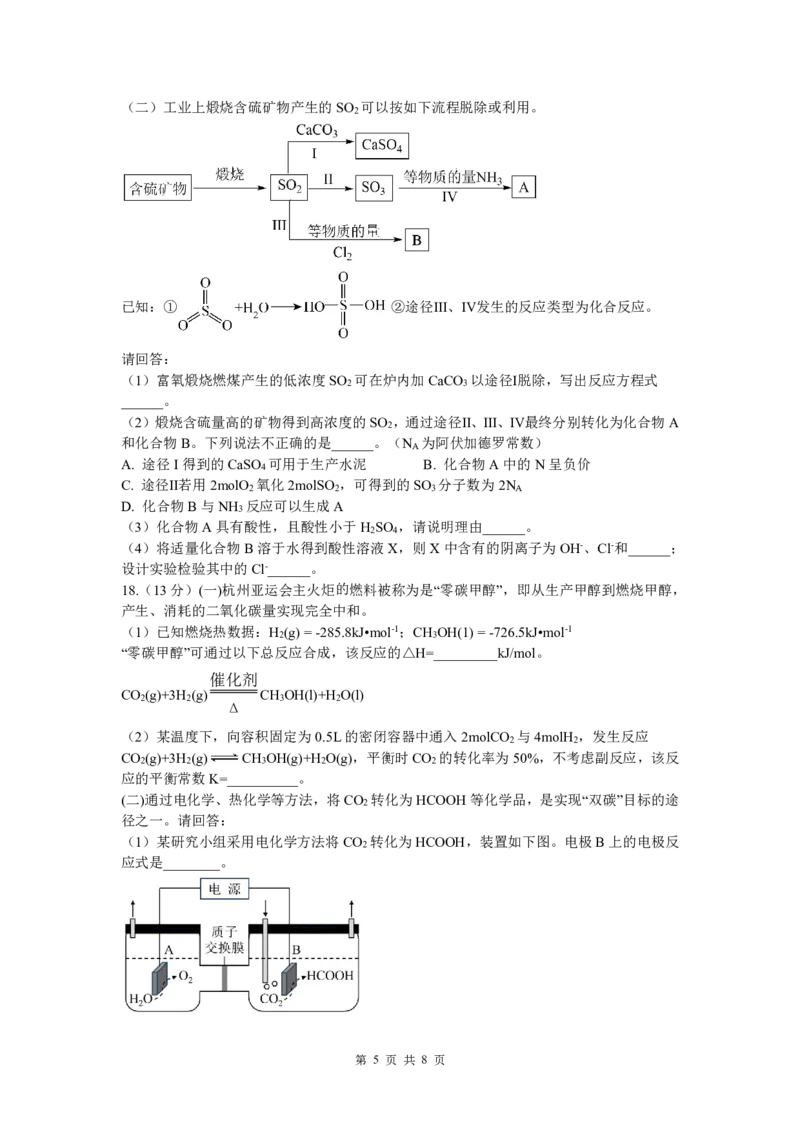
12.硫酸与氯气反应的生成物的结构如图所示,有关说法不正确是
O O O
‖ Cl ‖ Cl ‖
HO-S-OH—— 2 →Cl-S-OH—— 2 →Cl-S-Cl
‖ ‖ ‖
O O O
硫酸 氯磺酸 硫酰二氯
第 2 页 共 8 页A.沸点:硫酸>氯磺酸>硫酰二氯
B.氯磺酸在一定条件下可与苯发生取代反应生成氯苯
C.氯磺酸与足量NaOH溶液反应可生成两种钠盐
D.硫酰二氯可以脱去MgCl ·6H O中的水制备无水氯化镁
2 2
13.MO+与CH 反应能高选择性地生成甲醇。下图表示MO+分别与CH 、CD 反应体系的
4 4 4
能量随反应进程的变化示意图(两者历程相似,图中以CH 示例)。已知:直接参与化学键变
4
化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
A.MO+与CD 反应的能量变化应为图中曲线d
4
B.步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是Ⅱ
C.MO+与CH D 反应,氘代甲醇的产量: CH DOD>CHD OH
2 2 2 2
D.若MO+与CHD 反应,生成的氘代甲醇有2种
3
14.西北工业大学曾华强课题组借用足球烯核心,成功实现了高效且选择性可精准定制的离
子跨膜运输,如图所示。已知:图中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-
氧原子个数”。下列说法正确的是
A. 冠醚分子中C原子的杂化类型为sp2
B. 冠醚和碱金属离子通过离子键形成超分子
C. 不同冠醚与不同碱金属作用,中心碱金属离子的配位数是不变的
D.18-冠-6与K+作用不与Li+和Na+作用,反映了超分子“分子识别”的特征
15.草酸(H C O )是二元弱酸。某小组做如下两组实验:
2 2 4
实验Ⅰ:往20mL0.1mol·L−1NaHC O 溶液中滴加0.1mol·L−1NaOH溶液。
2 4
实验Ⅱ:往20mL0.10mol·L−1NaHC O 溶液中滴加0.10mol·L−1CaCl 溶液。
2 4 2
[已知:H C O 的电离常数K =5.4×10−2,K =5.4×10−5,K (CaC O )=2.4×10−9,溶液混合
2 2 4 a1 a2 sp 2 4
后体积变化忽略不计],下列说法正确的是
A.实验Ⅰ可选用甲基橙作指示剂,指示反应终点
B.实验Ⅰ中V(NaOH)=10mL时,存在c(C O2−)<c(HC O−)
2 4 2 4
C.实验Ⅱ中发生反应:HC O−+Ca2+===CaC O ↓+H+
2 4 2 4
第 3 页 共 8 页D.实验Ⅱ中V(CaCl )=80mL时,溶液中c(C O2−)=4.0×10−8mol/L
2 2 4
16.某小组设计如下实验方案除去肉桂醛( )中的肉桂醇
( )杂质,下列说法不 . 正 . 确 . 的是
已知:①室温下,肉桂醛、肉桂醇均为微溶于水的油状液体;
②提纯时,肉桂醛与NaHSO 发生: 。
3
A.步骤I中,饱和NaHSO 须加过量
3
B.步骤I中,可用少量氯仿洗涤组分1
C.步骤Ⅱ为加稀硫酸,然后在漏斗中进行过滤
D.步骤Ⅱ中,Na SO 可降低肉桂醛在水中的溶解度
2 4
二、非选择题(本大题共5小题,共52分)
17.(17分)(一)N族元素(N、P、As、Sb、Bi)形成的物质在生产生活中有着重要地位。
(1)基态As原子的价层电子排布式为______。
(2)二氟氮烯(N F )分子有两种同分异构体,每个原子均满足八电子稳定结构,实验室
2 2
测得它们的熔沸点如下表:
物质 熔点/℃ 沸点/℃
I <-195 -105.7
II -172 -111.4
N F 分子中N的杂化方式为______,化合物Ⅰ的结构式为______(选A或B)。
2 2
A. B.
(3)下列说法正确的是______。
A. 电负性:N>P>As
B. 离子半径:N3-