文档内容
西安中学 2023-2024 学年度第二学期期末考试
高二化学试题
(时间:75分钟 满分:100分) 命题人:徐君镕
可能用到的相对原子质量:H-1 C-12 Fe-56 Al-27 Na-23 O-16 S-32 N-14
Mg-24 Cl-35.5
一、单选题(本大题共 16小题,每题 3分,共 48分)
1. 下列说法正确的是( )
A.X 射线衍射可测定 CH COOH 的相对分子质量
3
B.有机物燃烧后只生成 CO 和H O 的物质一定只含有碳、氢两种元素
2 2
C.通过红外光谱仪可区分 HCOOCH 和CH COOH
3 3
D.通过质谱分析可获得 CH COOH 的键长、键角等信息
3
2. 布洛芬( )的一种合成路线片段如下:
下列说法不正确的是( )
A.布洛芬属于羧酸,不与乙酸互为同系物
B.乙、丙均能发生取代反应,均能使酸性 KMnO 溶液褪色
4
C.可以用碳酸氢钠溶液区分乙和丙
D.甲分子中所有碳原子有可能共平面
3. 下列物质分类组合正确的是( )
选项 碱 电解质 混合物 碱性氧化物
A 苛性钠 乙醇 胆矾 CaO
B 纯碱 小苏打 液氯 K O
2
C 烧碱 H O Fe(OH) 胶体 MgO
2 3
D 火碱 CaCO 水煤气 Na O
3 2 2
西安中学 高二年级 化学试题 第1页 共8页
学科网(北京)股份有限公司4. 制作豆腐过程一般有如图操作,其中操作⑤中往往用卤水或石膏作凝固剂,下列
说法不正确的是( )
A.操作①与操作②的目的是为了更多的蛋白质溶解于水
B.操作③可使用半透膜进行固液分离,将所得液体进行操作④
C.操作③所得分散系的分散质直径为 10-9至10-7 m
D.在适宜温度下,操作⑤可用MgCl 作凝固剂使蛋白质聚沉
2
5. 常温下,下列各组离子一定能大量共存的是( )
A.pH=1 的溶液中:I-、Mg2+、
西安中学 高二年级 化学试题 第2页 共8页
学科网(北京)股份有限公司
S O 24 、 N O 3
B.滴加几滴 K S C N 溶液显红色的溶液中:K+、Na+、 S O 24 、 H C O 3
C.水电离的 c(H+)=1×10-12 mol·L-1的溶液:K+、 N H +4 、S2-、Cl-
D.能使紫色石蕊试液变蓝的溶液中:K+、Na+、 N O 3 、 C O 23
6. 下列化学反应的离子方程式书写正确的是( )
A.向 Ba(HCO ) 溶液中加入少量 NaOH 溶液:Ba2+ +
3 2
H C O 3 + OH- = BaCO ↓+ H O
3 2
B.向 NH Al(SO ) 溶液中滴加少量 NaOH 稀溶液:NH + OH- = NH ·H O
4 4 2 4 3 2
C.向H C O 中加酸性KMnO 溶液:2MnO+ 5C O2+16H+ = 2Mn2+ +10CO ↑+ 8H O
2 2 4 4 4 2 4 2 2
D.工业制取漂白粉:Cl + 2OH- = Cl- + ClO- + H O
2 2
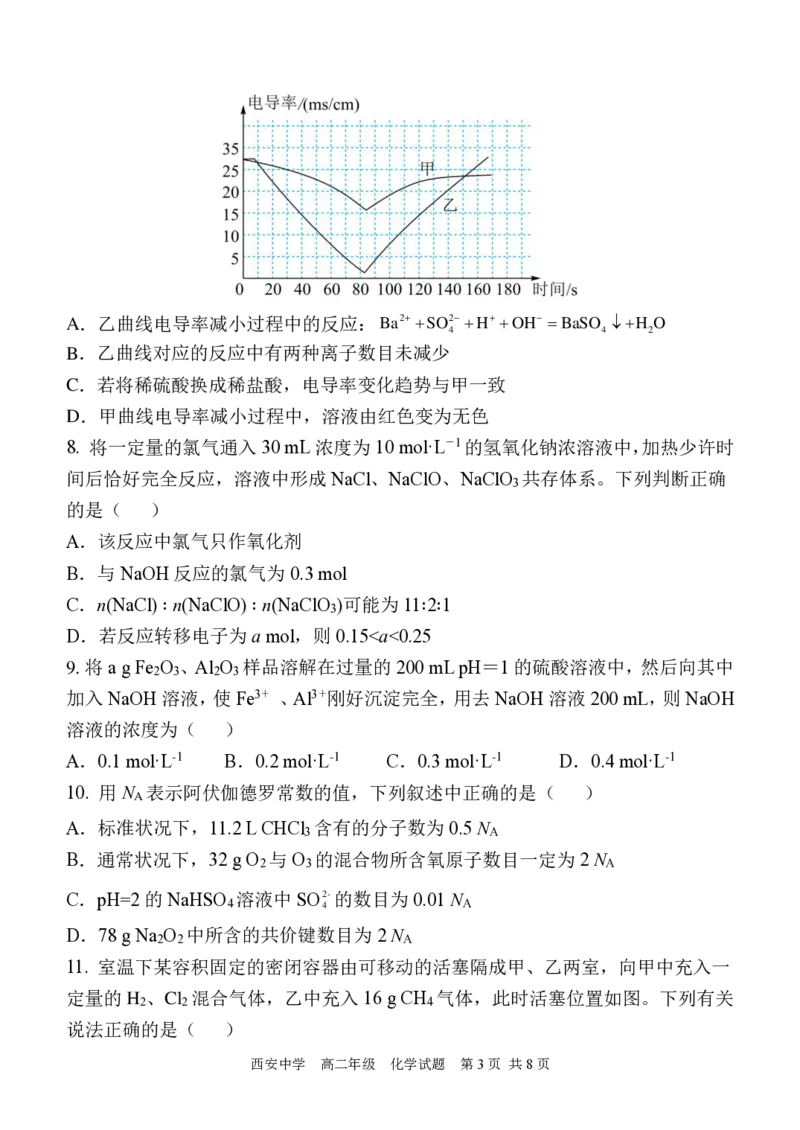
7. 电导率传感器可辅助探究复分解反应的实质。将含有酚酞的 Ba(OH) 溶液平均分
2
成两份并置于两个烧杯中,插入电导率传感器,往其中一份滴加稀硫酸,往另一份
滴加硫酸钠溶液,滴加过程中,这两份溶液的滴加速率始终相同,测得溶液的电导
率变化如图所示。下列说法正确的是( )A.乙曲线电导率减小过程中的反应:
西安中学 高二年级 化学试题 第3页 共8页
学科网(北京)股份有限公司
B a 2 S O 24 H O H B a S O
4
H
2
O
B.乙曲线对应的反应中有两种离子数目未减少
C.若将稀硫酸换成稀盐酸,电导率变化趋势与甲一致
D.甲曲线电导率减小过程中,溶液由红色变为无色
8. 将一定量的氯气通入 30 mL浓度为 10 mol·L-1的氢氧化钠浓溶液中,加热少许时
间后恰好完全反应,溶液中形成 NaCl、NaClO、NaClO 共存体系。下列判断正确
3
的是( )
A.该反应中氯气只作氧化剂
B.与 NaOH 反应的氯气为 0.3 mol
C.n(NaCl) ∶ n(NaClO) ∶ n(NaClO )可能为 11∶2∶1
3
D.若反应转移电子为 a mol,则0.15 Fe2+
13. 已知反应: P
4
2 I
2
8 H
2
O = 2 P H
4
I 2 H
3
P O
4
2 H I ,N 为阿伏加德罗常数的值,
A
若消耗 36 g H O,P 的结构如图所示,下列叙述的错误的是( )
2 4
A.将生成物配制成 1 L水溶液,溶液中 c(H+)= 2 mol·L-1
B.转移电子数为 2.5 N
A
C.还原产物比氧化产物多 0.5 mol
D.断裂的 P-P 键数为 1.5 N
A
14. 在 V L Fe (SO ) 溶液中,含有 W g Fe3+,取 L该溶液稀释到 L,稀释后SO2
2 4 3 4
的物质的量浓度是( )
W W 3W 3W
A. molL1 B. molL1 C. molL1 D. molL1
112V 56V 56V 112V
15.下列实验操作或实验仪器使用正确的是( )
A. 测“84”消毒液的 pH,用洁净玻璃棒蘸取少许“84”消毒液滴在 pH 试纸上
B. 容量瓶、滴定管使用前均需用蒸馏水洗净、烘干,并检查是否漏水C. 硝酸、次氯酸见光易分解,一般将其存放在棕色细口瓶当中,并放置在阴凉处
D.可用碱式滴定管量取 25.00 mL KMnO 标准溶液置于锥形瓶中
4
16. 对固体 NaHCO 充分加热,产生的气体先通过足量浓硫酸,再通过足量 Na O ,
3 2 2
Na O 增重 0.28 g,则固体 NaHCO 的质量为
2 2 3
A.0.42 g B.1.68 g C.0.84 g D.3.36 g
二、非选择题(共 4题,共 52分)
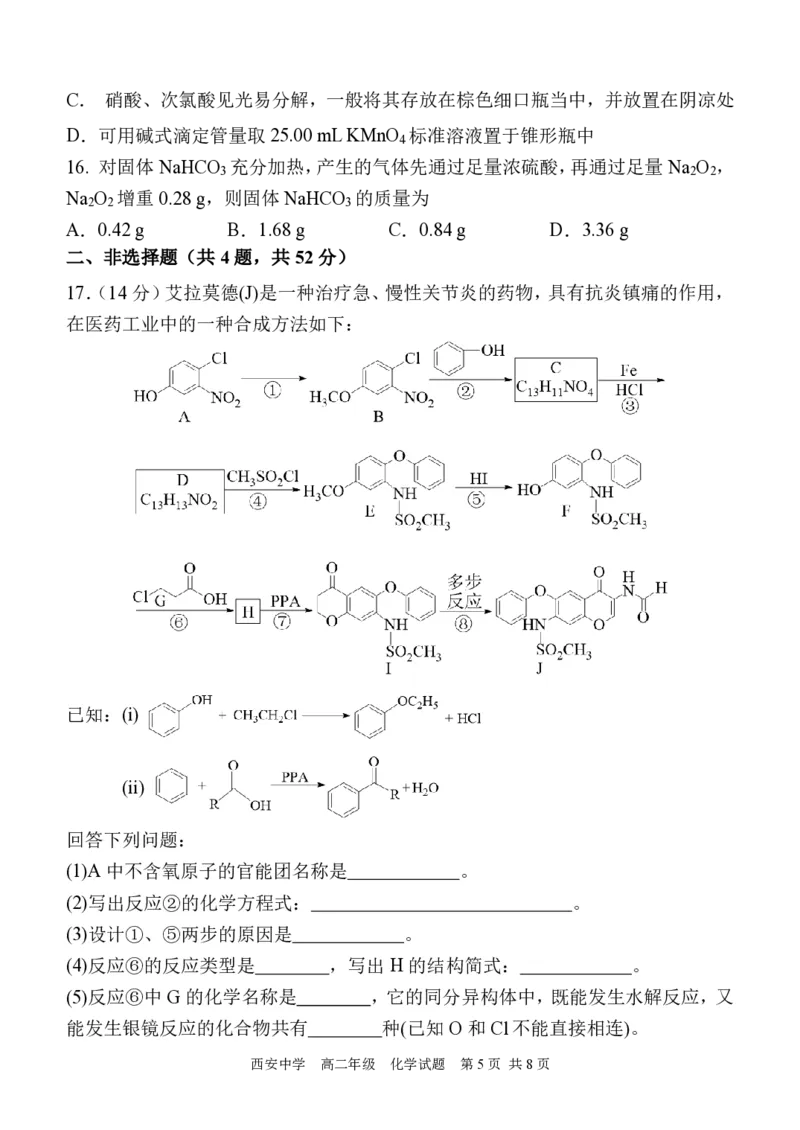
17.(14 分)艾拉莫德(J)是一种治疗急、慢性关节炎的药物,具有抗炎镇痛的作用,
在医药工业中的一种合成方法如下:
已知:(i)
(ii)
回答下列问题:
(1)A中不含氧原子的官能团名称是 。
(2)写出反应②的化学方程式: 。
(3)设计①、⑤两步的原因是 。
(4)反应⑥的反应类型是 ,写出 H 的结构简式: 。
(5)反应⑥中G 的化学名称是 ,它的同分异构体中,既能发生水解反应,又
能发生银镜反应的化合物共有 种(已知 O 和Cl不能直接相连)。
西安中学 高二年级 化学试题 第5页 共8页
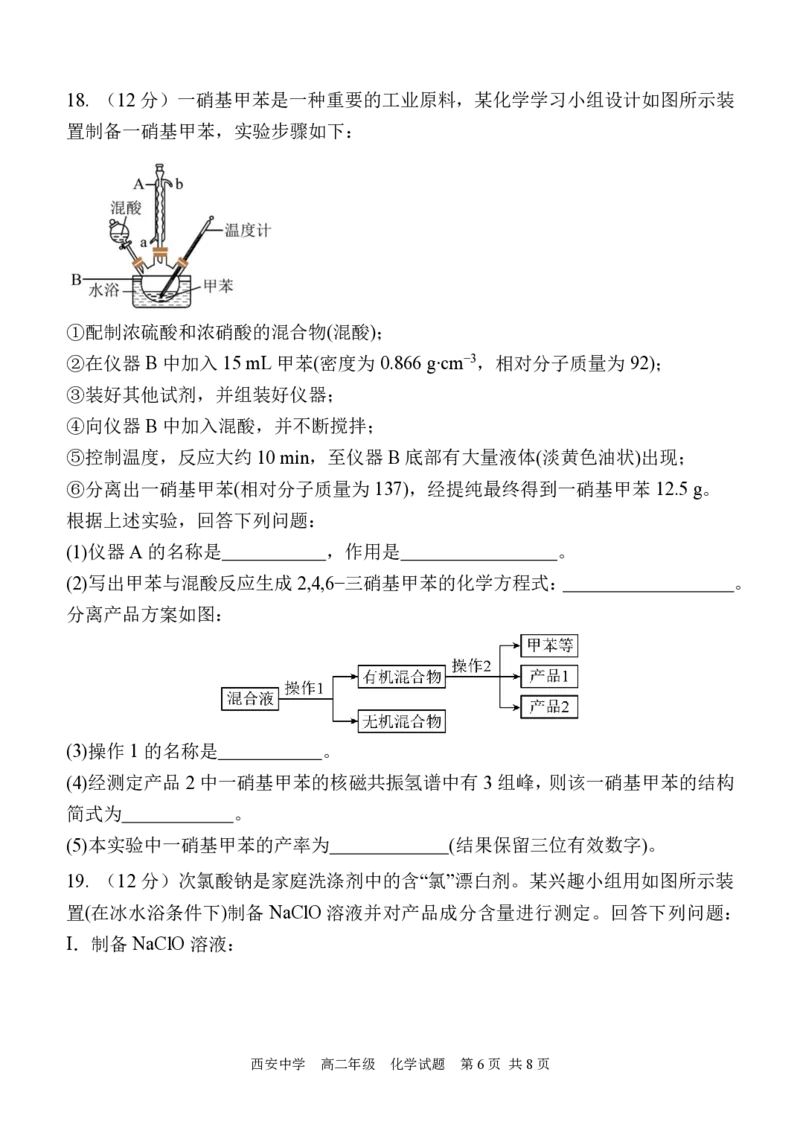
学科网(北京)股份有限公司18. (12 分)一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装
置制备一硝基甲苯,实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在仪器 B中加入 15 mL甲苯(密度为 0.866 g∙cm−3,相对分子质量为 92);
③装好其他试剂,并组装好仪器;
④向仪器 B中加入混酸,并不断搅拌;
⑤控制温度,反应大约 10 min,至仪器 B底部有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯(相对分子质量为 137),经提纯最终得到一硝基甲苯 12.5 g。
根据上述实验,回答下列问题:
(1)仪器 A的名称是 ,作用是 。
(2)写出甲苯与混酸反应生成 2,4,6−三硝基甲苯的化学方程式: 。
分离产品方案如图:
(3)操作 1的名称是 。
(4)经测定产品 2 中一硝基甲苯的核磁共振氢谱中有 3组峰,则该一硝基甲苯的结构
简式为 。
(5)本实验中一硝基甲苯的产率为 (结果保留三位有效数字)。
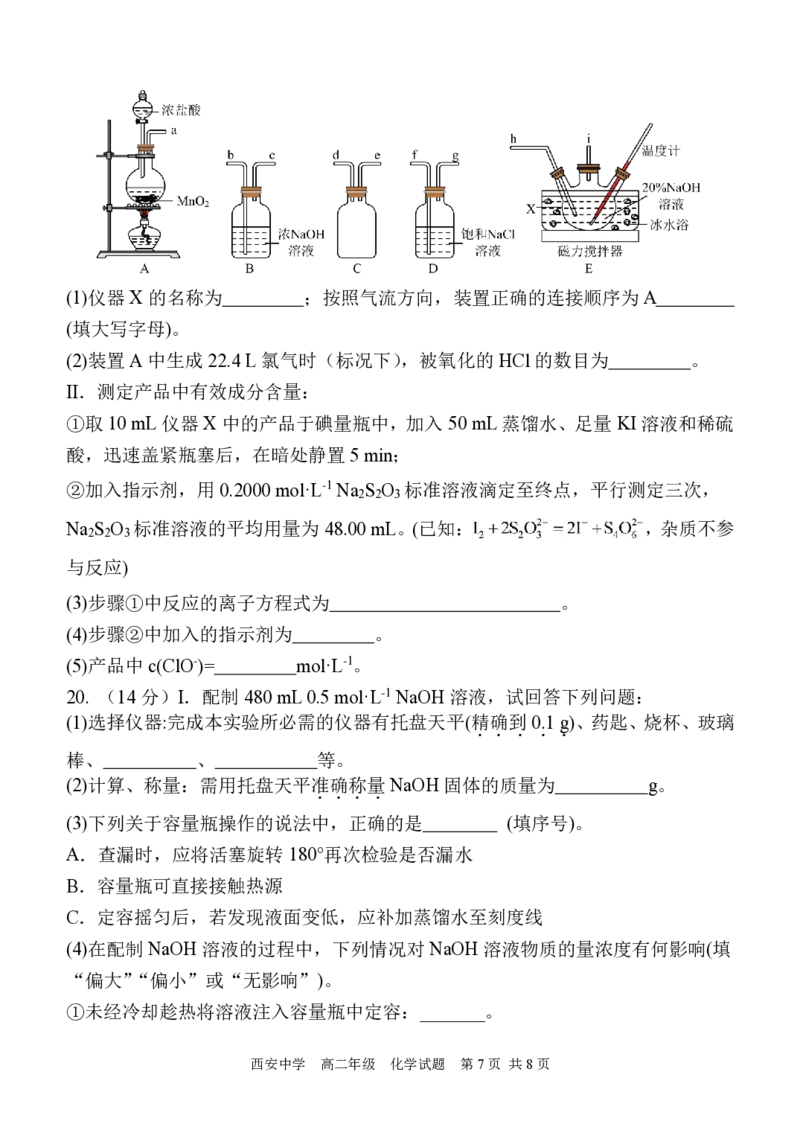
19. (12 分)次氯酸钠是家庭洗涤剂中的含“氯”漂白剂。某兴趣小组用如图所示装
置(在冰水浴条件下)制备NaClO 溶液并对产品成分含量进行测定。回答下列问题:
Ⅰ.制备 NaClO 溶液:
西安中学 高二年级 化学试题 第6页 共8页
学科网(北京)股份有限公司(1)仪器 X 的名称为 ;按照气流方向,装置正确的连接顺序为 A
(填大写字母)。
(2)装置 A中生成 22.4 L氯气时(标况下),被氧化的 HCl的数目为 。
Ⅱ.测定产品中有效成分含量:
①取10 mL仪器 X 中的产品于碘量瓶中,加入 50 mL蒸馏水、足量 KI溶液和稀硫
酸,迅速盖紧瓶塞后,在暗处静置 5 min;
②加入指示剂,用 0.2000 mol·L-1 Na S O 标准溶液滴定至终点,平行测定三次,
2 2 3
Na S O 标准溶液的平均用量为 48.00 mL。(已知: ,杂质不参
2 2 3
与反应)
(3)步骤①中反应的离子方程式为 。
(4)步骤②中加入的指示剂为 。
(5)产品中 c(ClO-)= mol·L-1。
20. (14 分)I.配制 480 mL 0.5 mol·L-1 NaOH 溶液,试回答下列问题:
(1)选择仪器:完成本实验所必需的仪器有托盘天平(精确到 0.1 g)、药匙、烧杯、玻璃
... ..
棒、 、 等。
(2)计算、称量:需用托盘天平准确称量 NaOH 固体的质量为 g。
....
(3)下列关于容量瓶操作的说法中,正确的是 (填序号)。
A.查漏时,应将活塞旋转 180°再次检验是否漏水
B.容量瓶可直接接触热源
C.定容摇匀后,若发现液面变低,应补加蒸馏水至刻度线
(4)在配制 NaOH 溶液的过程中,下列情况对 NaOH 溶液物质的量浓度有何影响(填
“偏大”“偏小”或“无影响”)。
①未经冷却趁热将溶液注入容量瓶中定容:_______。
西安中学 高二年级 化学试题 第7页 共8页
学科网(北京)股份有限公司②定容时仰视观察液面: _______。
II.MgCl ·6H O、AlCl ·6H O、FeCl ·4H O 等结晶水合氯化物在空气中受热脱水易
2 2 3 2 2 2
发生水解反应。
(5)MgCl ·6H O 在空气中受热脱水过程中,热重分析测得剩余固体质量占初始固体
2 2
质量的百分含量随温度变化的曲线如图所示,试判断A点固体的化学式: 。
西安中学 高二年级 化学试题 第8页 共8页
学科网(北京)股份有限公司