文档内容
五年(2021-2025)高考化学真题分类汇编
专题15 化学反应中的能量变化及反应机理
考向 五年考情(2021-2025) 命题趋势
2025·河南卷、2025·北京卷、2025·
浙江1月卷、2024·全国甲卷、2024· 本专题主要分两个大的考查方向,一是
化学反应中的能量变化,常见命题形式
考点一 化学反应中的能 甘肃卷、2024·安徽卷、2023·湖北
多以化学反应与能量的基本概念命题,
量变化 卷、2023·广东卷、2022·天津卷、
考査化学反应中能量转化的形式和反应
2023·海南卷、2022·浙江卷、2022·
热的有关计算。二是反应历程、机理图
重庆卷、2021·广东卷
分析,新高考强调素养为本的情境化命
2025·江苏卷、2025·河北卷、2025·
题,高考通过真实情境的创设,考查学
河南卷、2025·黑吉辽蒙卷、2025·湖
生的信息获取能力和迁移应用能力。近
北卷、2025·云南卷、2025·北京卷、
几年高考常以催化剂的催化反应机理和
考点二 反应历程、机理 2024·贵州卷、2024·河北卷、2024·
能垒图像为情境载体进行命题。这两类
图分析 浙江6月卷、2023·新课标卷、2023·
命题,由于陌生度高,思维转化大,且
江苏卷、2023·湖南卷、2022·湖南
命题视角在不断地发展和创新,成为大
卷、2022·山东卷、2021·山东卷、 多数考生高分路上的“拦路虎”。
2021·湖南卷
考点一 化学反应中的能量变化
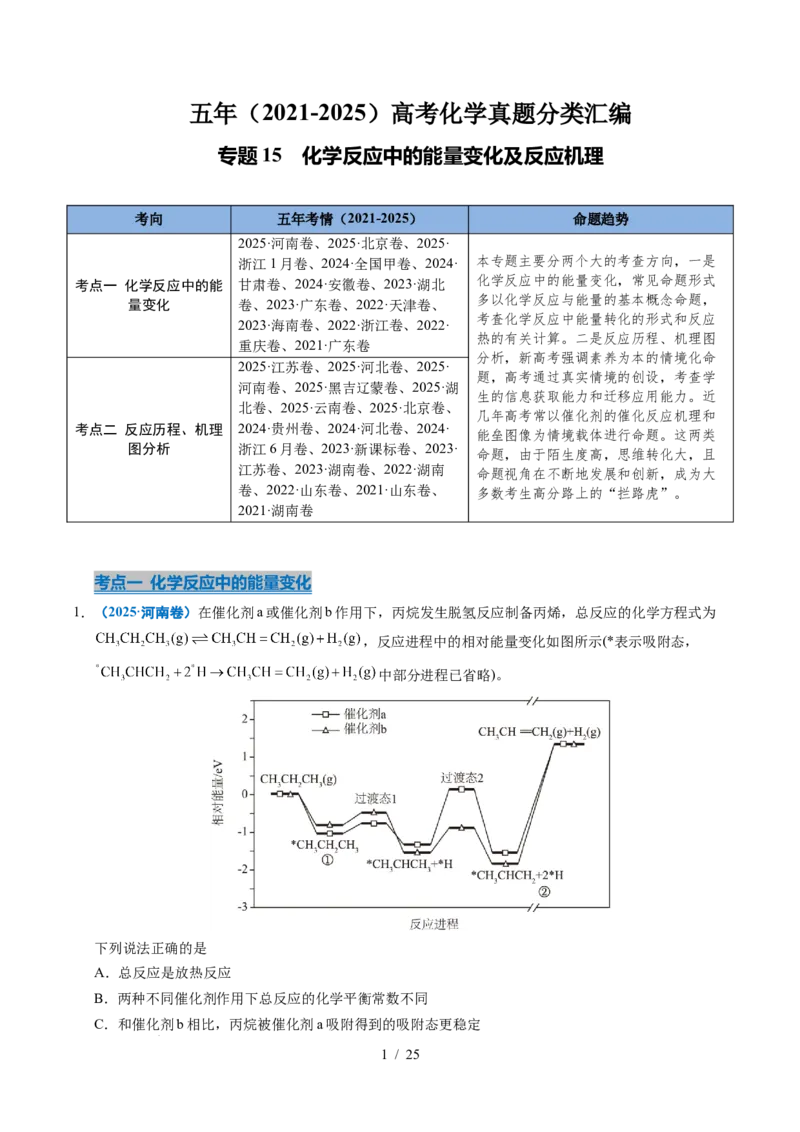
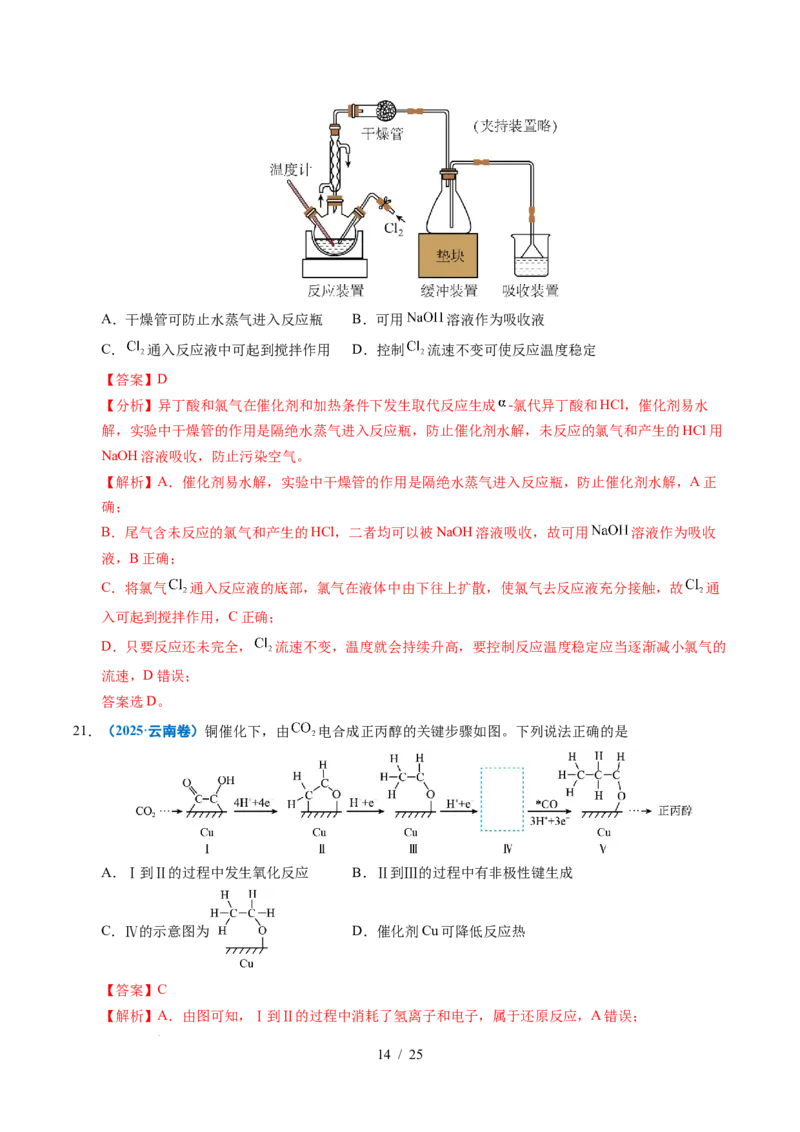
1.(2025·河南卷)在催化剂a或催化剂b作用下,丙烷发生脱氢反应制备丙烯,总反应的化学方程式为
,反应进程中的相对能量变化如图所示(*表示吸附态,
中部分进程已省略)。
下列说法正确的是
A.总反应是放热反应
B.两种不同催化剂作用下总反应的化学平衡常数不同
C.和催化剂b相比,丙烷被催化剂a吸附得到的吸附态更稳定
1 / 25
学学科科网网((北北京京))股股份份有有限限公公司司D.①转化为②的进程中,决速步骤为
【答案】C
【解析】A.由图可知,生成物能量高,总反应为吸热反应,A错误;
B.平衡常数只和温度有关,与催化剂无关,B错误;
C.由图可知,丙烷被催化剂a吸附后能量更低,则被催化剂a吸附后得到的吸附态更稳定, C正确;
D.活化能高的反应速率慢,是反应的决速步骤,故决速步骤为*CHCHCH →*CHCHCH +*H或
3 3 3 2
*CHCHCH +*H→*CHCHCH +2*H,D错误;
3 3 3 2
故选C。
2.(2025·北京卷)为理解离子化合物溶解过程的能量变化,可设想 固体溶于水的过程分两步实现,
示意图如下。
下列说法不正确的是
A. 固体溶解是吸热过程
B.根据盖斯定律可知:
C.根据各微粒的状态,可判断 ,
D.溶解过程的能量变化,与 固体和 溶液中微粒间作用力的强弱有关
【答案】C
【分析】由图可知, 固体溶于水的过程分两步实现,第一步为NaCl固体变为Na+和Cl-,此过程
离子键发生断裂,为吸热过程;第二步为Na+和Cl-与水结合形成水合钠离子和水合氯离子的过程,此
过程为成键过程,为放热过程。
【解析】A.由图可知, 固体溶解过程的焓变为 ,为吸热过程,A正确;
B.由图可知, 固体溶于水的过程分两步实现,由盖斯定律可知 ,即 ,
B正确;
C.由分析可知,第一步为NaCl固体变为Na+和Cl-,此过程离子键发生断裂,为吸热过程,a>0;第
二步为Na+和Cl-与水结合形成水合钠离子和水合氯离子的过程,此过程为成键过程,为放热过程,b<
0,C错误;
D.由分析可知,溶解过程的能量变化,却决于 固体断键吸收的热量及Na+和Cl-水合过程放出的
热量有关,即与 固体和 溶液中微粒间作用力的强弱有关,D正确;
2 / 25
学学科科网网((北北京京))股股份份有有限限公公司司故选C。
3.(2025·浙江1月卷)下列说法正确的是
A.常温常压下 和 混合无明显现象,则反应 在该条件下不自发
B. ,升高温度,平衡逆移,则反应的平衡常数减小
C. ,则正反应的活化能大于逆反应的活化能
D. ,则
【答案】B
【解析】A.根据复合判据ΔG=ΔH-TΔS,该反应ΔH<0、ΔS<0,温度较低时ΔG<0,故低温能自发
进行,A错误;
B.该反应为放热反应,升高温度,平衡逆移,平衡常数减小,B正确;
C.该反应为放热反应,则 ,则正反应的活化能小于逆反应的活化能,C错误;
D. ,根据盖斯定
律,反应①-反应②得到目标反应Na(s)+ Cl(g)=Na+(g)+Cl−(g),则ΔH= ,由于不能明确
2
相对大小,则ΔH不能确定,D错误;
故选B。
4.(2024·全国甲卷)人类对能源的利用经历了柴薪、煤炭和石油时期,现正向新能源方向高质量发展。
下列有关能源的叙述错误的是
A.木材与煤均含有碳元素 B.石油裂化可生产汽油
C.燃料电池将热能转化为电能 D.太阳能光解水可制氢
【答案】C
【解析】A.木材的主要成分为纤维素,纤维素中含碳、氢、氧三种元素,煤是古代植物埋藏在地下经
历了复杂的变化逐渐形成的固体,是有机物和无机物组成的复杂混合物,主要含碳元素,A正确;
B.石油裂化是将相对分子质量较大、沸点较高的烃断裂为相对分子质量较小、沸点较低的烃的过程,
汽油的相对分子质量较小,可以通过石油裂化的方式得到,B正确;
C.燃料电池是将燃料的化学能变成电能的装置,不是将热能转化为电能,C错误;
D.在催化剂作用下,利用太阳能光解水可以生成氢气和氧气,D正确;
故答案选C。
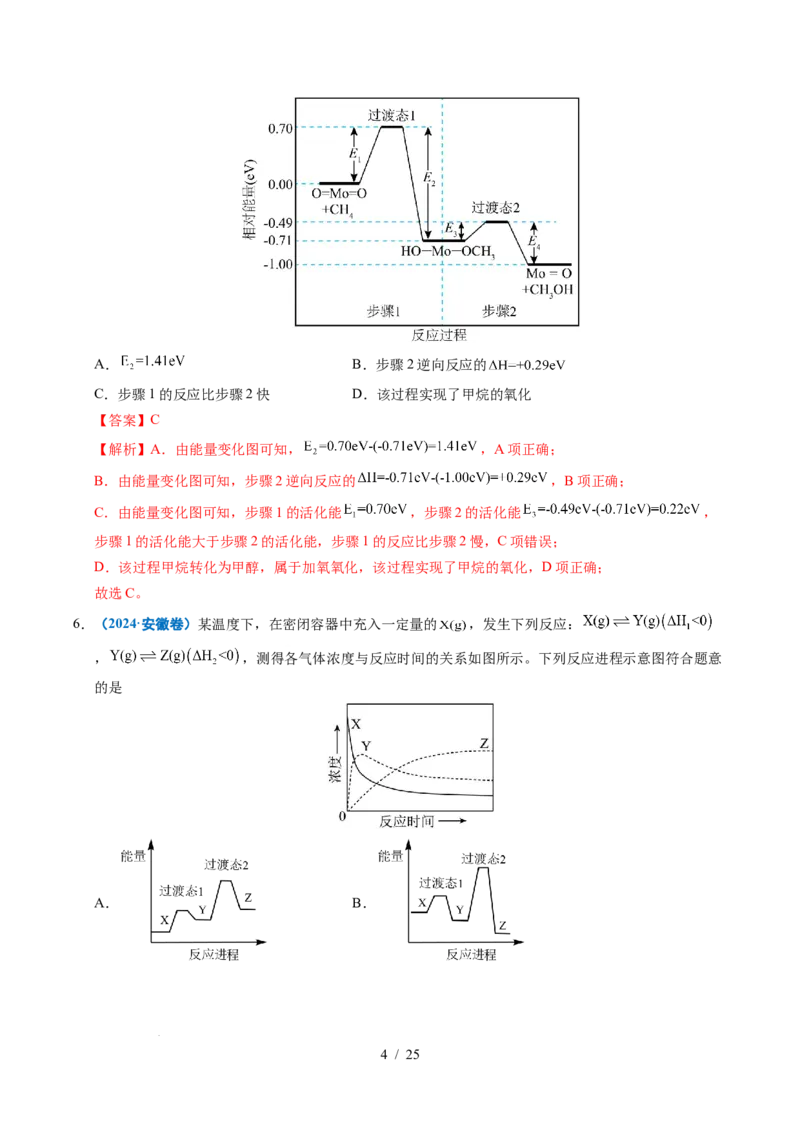
5.(2024·甘肃卷)甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的是
3 / 25
学学科科网网((北北京京))股股份份有有限限公公司司A. B.步骤2逆向反应的
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
【答案】C
【解析】A.由能量变化图可知, ,A项正确;
B.由能量变化图可知,步骤2逆向反应的 ,B项正确;
C.由能量变化图可知,步骤1的活化能 ,步骤2的活化能 ,
步骤1的活化能大于步骤2的活化能,步骤1的反应比步骤2慢,C项错误;
D.该过程甲烷转化为甲醇,属于加氧氧化,该过程实现了甲烷的氧化,D项正确;
故选C。
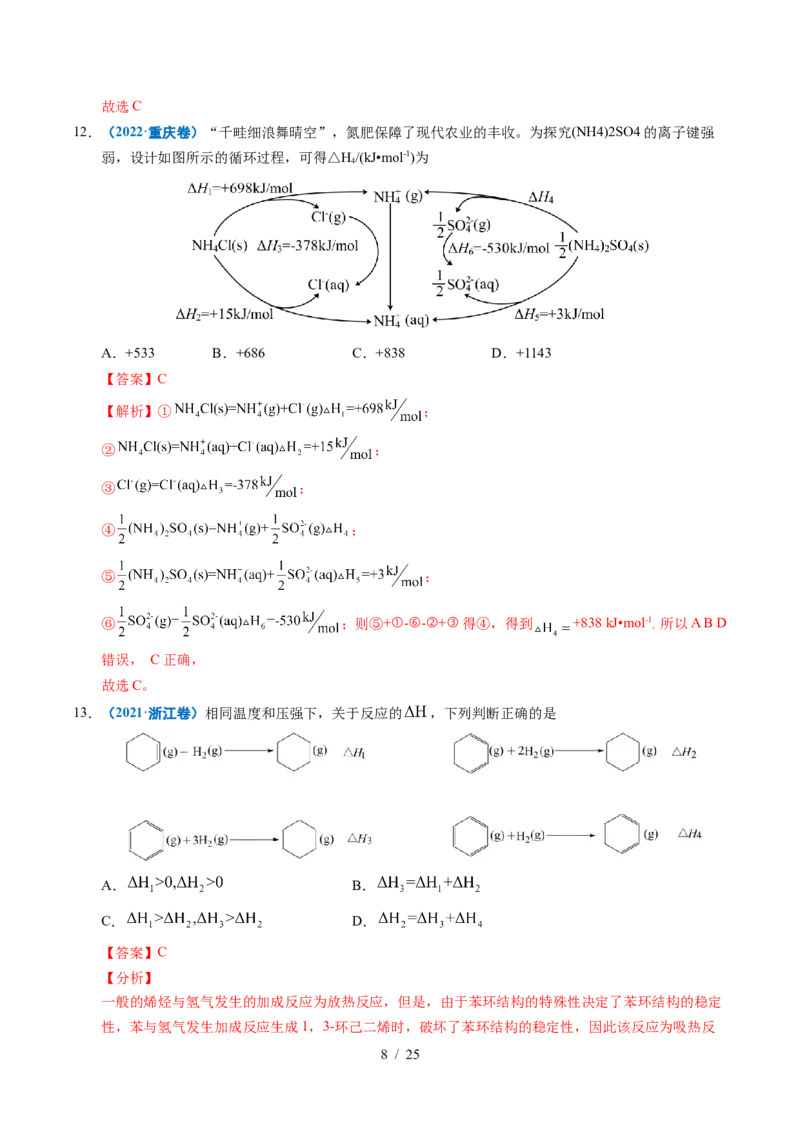
6.(2024·安徽卷)某温度下,在密闭容器中充入一定量的 ,发生下列反应:
, ,测得各气体浓度与反应时间的关系如图所示。下列反应进程示意图符合题意
的是
A. B.
4 / 25
学学科科网网((北北京京))股股份份有有限限公公司司C. D.
【答案】B
【分析】由图可知,反应初期随着时间的推移X的浓度逐渐减小、Y和Z的浓度逐渐增大,后来随着
时间的推移X和Y的浓度逐渐减小、Z的浓度继续逐渐增大,说明X(g) Y(g)的反应速率大于Y(g)
Z(g)的反应速率,则反应X(g) Y(g)的活化能小于反应Y(g) Z(g)的活化能。
【解析】A.X(g) Y(g)和Y(g) Z(g)的∆H都小于0,而图像显示Y的能量高于X,即图像显示X(g)
Y(g)为吸热反应,A项不符合题意;
B.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,且X(g) Y(g)的活化能小于Y(g) Z(g)的活
化能,B项符合题意;
C.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都小于0,但图像上X(g) Y(g)的活化能大于Y(g)
Z(g)的活化能,C项不符合题意;
D.图像显示X(g) Y(g)和Y(g) Z(g)的∆H都大于0,且X(g) Y(g)的活化能大于Y(g) Z(g)的活
化能,D项不符合题意;
选B。
7.(2023·湖北卷)2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量发
展新阶段。下列不能作为火箭推进剂的是
A.液氮-液氢 B.液氧-液氢 C.液态 -肼 D.液氧-煤油
【答案】A
【解析】A.虽然氮气在一定的条件下可以与氢气反应,而且是放热反应,但是,由于 键能很
大,该反应的速率很慢,氢气不能在氮气中燃烧,在短时间内不能产生大量的热量和大量的气体,因
此,液氮-液氢不能作为火箭推进剂,A符合题意;
B.氢气可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-液氢能作为
火箭推进剂,B不符合题意;
C.肼和 在一定的条件下可以发生剧烈反应,该反应放出大量的热,且生成大量气体,因此,液态
-肼能作为火箭推进剂,C不符合题意;
D.煤油可以在氧气中燃烧,反应速率很快且放出大量的热、生成大量气体,因此,液氧-煤油能作为
火箭推进剂,D不符合题意;
综上所述,本题选A。
8.(2023·广东卷)下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
选 陈述Ⅰ 陈述Ⅱ
5 / 25
学学科科网网((北北京京))股股份份有有限限公公司司项
A 将浓硫酸加入蔗糖中形成多孔炭 浓硫酸具有氧化性和脱水性
B 装有 的密闭烧瓶冷却后颜色变浅 转化为 的反应吸热
C 久置空气中的漂白粉遇盐酸产生 漂白粉的有效成分是
D 溶液导电性比同浓度醋酸强 溶液的 比醋酸的高
【答案】A
【解析】A.蔗糖在浓硫酸作用下形成多孔炭主要是蔗糖在浓硫酸作用下脱水,得到碳和浓硫酸反应生
成二氧化碳、二氧化硫和水,体现浓硫酸具有氧化性和脱水性,故A符合题意;
B.装有 的密闭烧瓶冷却后颜色变浅,降低温度,平衡向生成 方向移动,则 转化为
的反应为放热,故B不符合题意;
C.久置空气中的漂白粉遇盐酸产生 是由于次氯酸钙变质,次氯酸钙和空气中二氧化碳、水反应生
成碳酸钙,碳酸钙和盐酸反应生成二氧化碳,故C不符合题意;
D. 溶液导电性比同浓度醋酸强,氯化钠是强电解质,醋酸是弱电解质,导电性强弱与
溶液的 比醋酸的高无关系,故D不符合题意。
综上所述,答案为A。
9.(2022·天津卷)一定条件下,石墨转化为金刚石吸收能量。下列关于石墨和金刚石的说法正确的是
A.金刚石比石墨稳定
B.两物质的碳碳 键的键角相同
C.等质量的石墨和金刚石中,碳碳 键数目之比为4∶3
D.可以用X射线衍射仪鉴别金刚石和石墨
【答案】D
【解析】A.石墨转化为金刚石吸收能量,则石墨能量低,根据能量越低越稳定,因此石墨比金刚石稳
定,故A错误;
B.金刚石是空间网状正四面体形,键角为109°28′,石墨是层内正六边形,键角为120°,因此碳碳
键的键角不相同,故B错误;
C.金刚石是空间网状正四面体形,石墨是层内正六边形,层与层之间通过范德华力连接,1mol金刚
石有2mol碳碳 键,1mol石墨有1.5mol碳碳 键,因此等质量的石墨和金刚石中,碳碳 键数目之比
为3∶4,故C错误;
D.金刚石和石墨是两种不同的晶体类型,因此可用X射线衍射仪鉴别,故D正确。
综上所述,答案为D。
10.(2023·海南卷)各相关物质的燃烧热数据如下表。下列热化学方程式正确的是
物质
6 / 25
学学科科网网((北北京京))股股份份有有限限公公司司A.
B.
C.
D.
【答案】D
【分析】1mol纯物质完全燃烧生成指定的物质放出的热量称为燃烧热。
【解析】A.HO应该为液态,A错误;
2
B. ,B错误;
C.氢气的燃烧热为285.8kJ/mol,则 ,C错误;
D. ,D正确;
故选D。
11.(2022·浙江卷)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
21
能量/kJmol-1 249 39 10 0 0 136 242
8
可根据HO(g)+HO(g)=H O (g)计算出H O 中氧氧单键的键能为214kJmol-1。下列说法不正确的是
2 2 2 2
A.H 的键能为436kJmol-1
2
B.O 的键能大于H O 中氧氧单键的键能的两倍
2 2 2
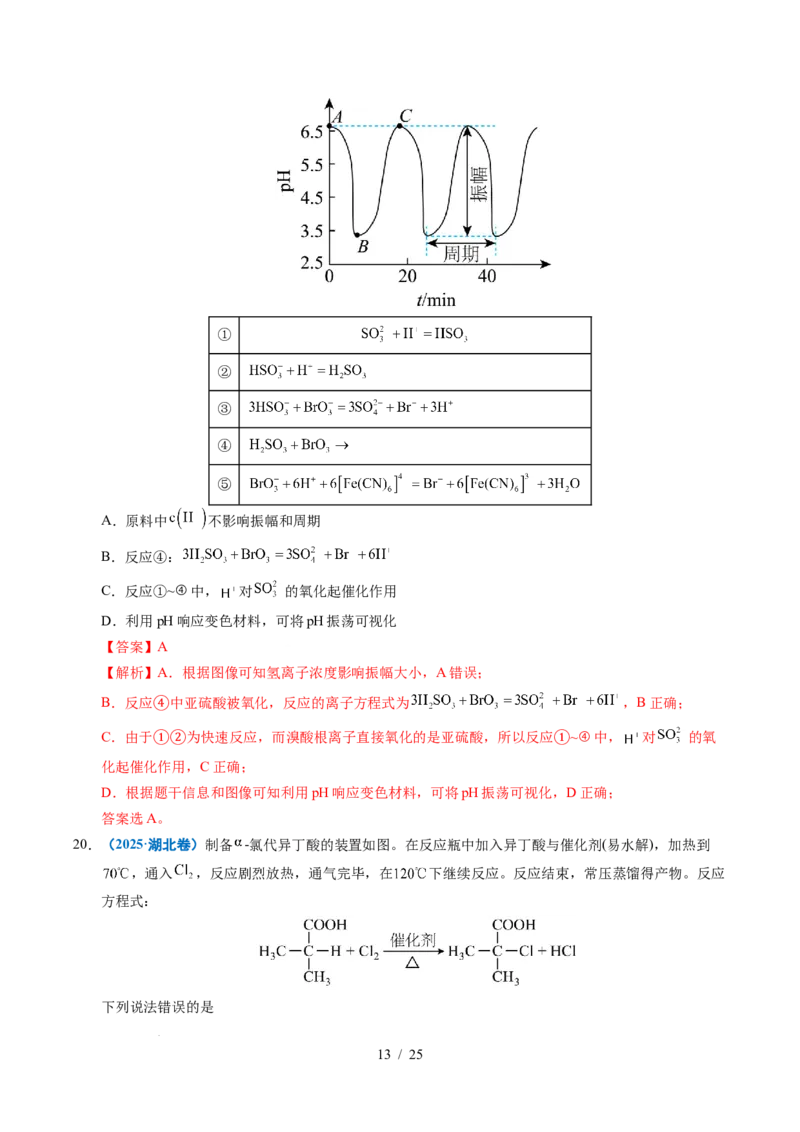
C.解离氧氧单键所需能量:HOOⅠ
C.生成P的速率:Ⅲ>Ⅱ D.进程Ⅳ中,Z没有催化作用
【答案】AD
【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A
说法正确;
B.进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相
同,B说法不正确;
C.进程Ⅲ中由S•Y转化为P•Y的活化能高于进程Ⅱ中由S•X转化为P•X的活化能,由于这两步反应
分别是两个进程的决速步骤,因此生成P的速率为Ⅲ<Ⅱ,C说法不正确;
D.由图中信息可知,进程Ⅳ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转
化为P+Z,因此,Z没有表现出催化作用,D说法正确;
综上所述,本题选AD。
21 / 25
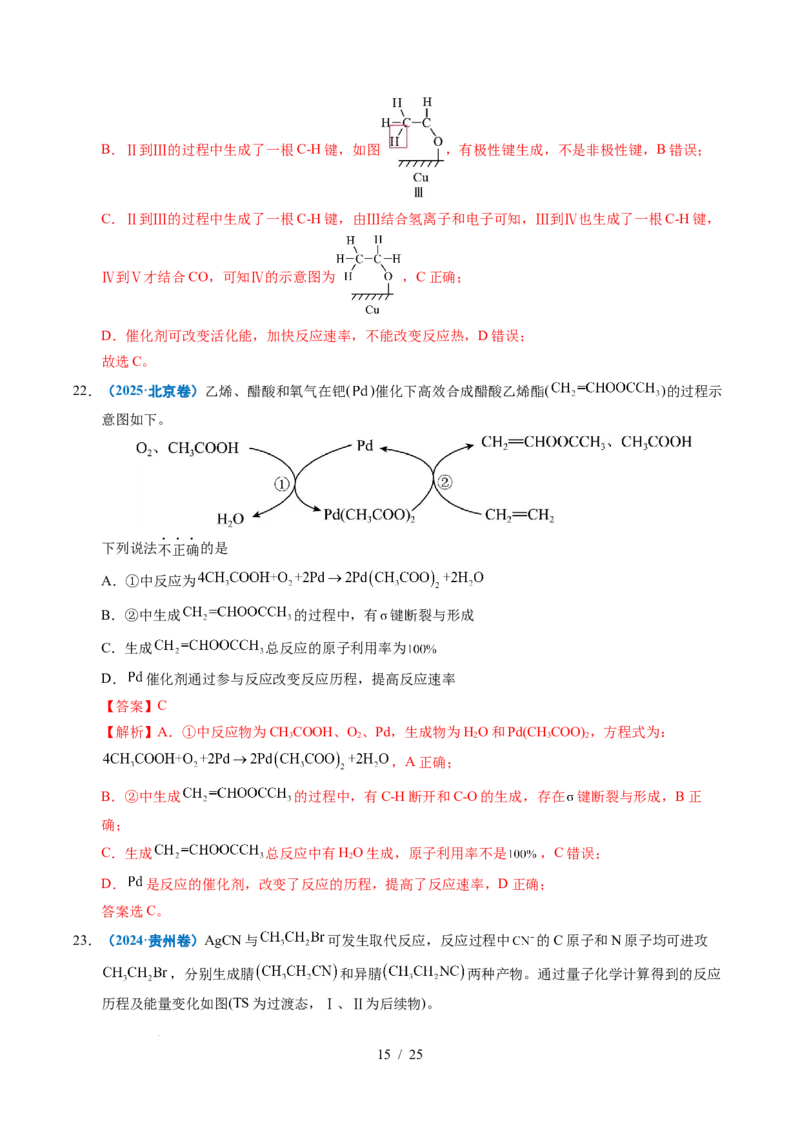
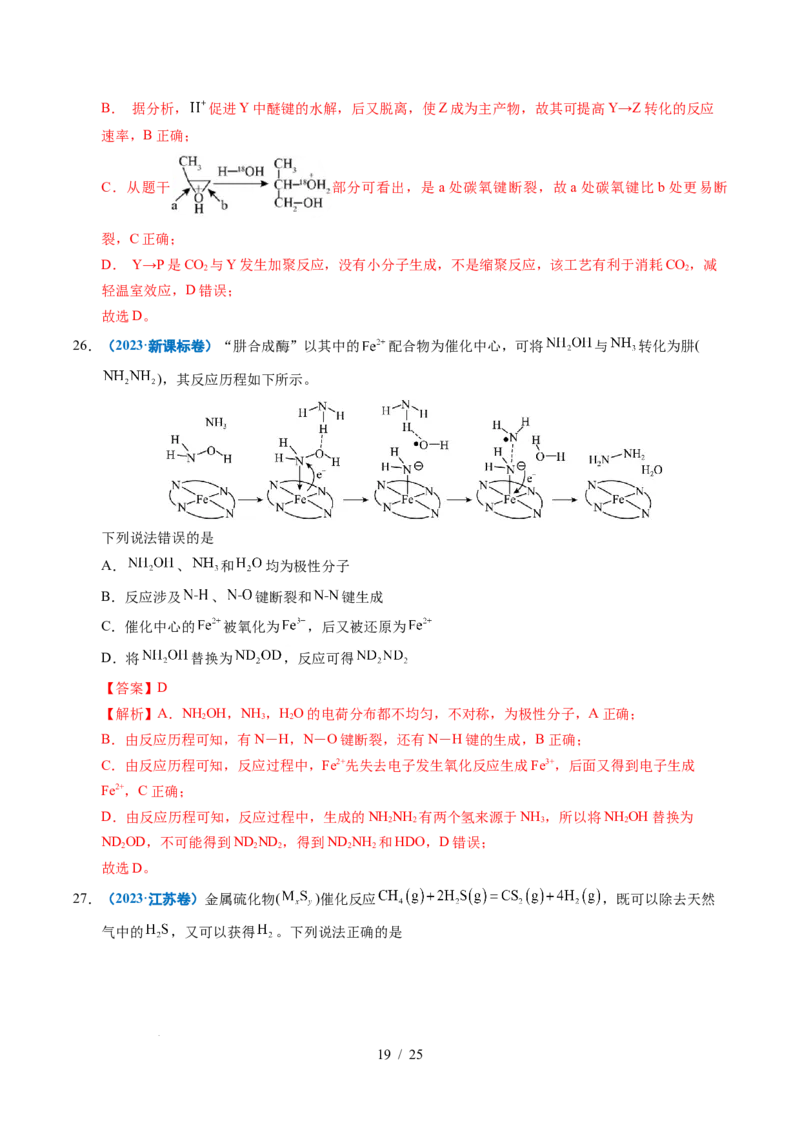
学学科科网网((北北京京))股股份份有有限限公公司司30.(2022·山东卷)在NO催化下,丙烷与氧气反应制备丙烯的部分反应机理如图所示。下列说法错误的
是
A.含N分子参与的反应一定有电子转移
B.由NO生成 的反应历程有2种
C.增大NO的量, 的平衡转化率不变
D.当主要发生包含②的历程时,最终生成的水减少
【答案】D
【解析】A.根据反应机理的图示知,含N分子发生的反应有NO+∙OOH=NO+∙OH、
2
NO+NO +H O=2HONO、NO +∙C H=C H+HONO、HONO=NO+∙OH,含N分子NO、NO 、HONO中
2 2 2 3 7 3 6 2
N元素的化合价依次为+2价、+4价、+3价,上述反应中均有元素化合价的升降,都为氧化还原反
应,一定有电子转移,A项正确;
B.根据图示,由NO生成HONO的反应历程有2种,B项正确;
C.NO是催化剂,增大NO的量,C H 的平衡转化率不变,C项正确;
3 8
D.无论反应历程如何,在NO催化下丙烷与O 反应制备丙烯的总反应都为2C H+O
2 3 8 2
2C H+2H O,当主要发生包含②的历程时,最终生成的水不变,D项错误;
3 6 2
答案选D。
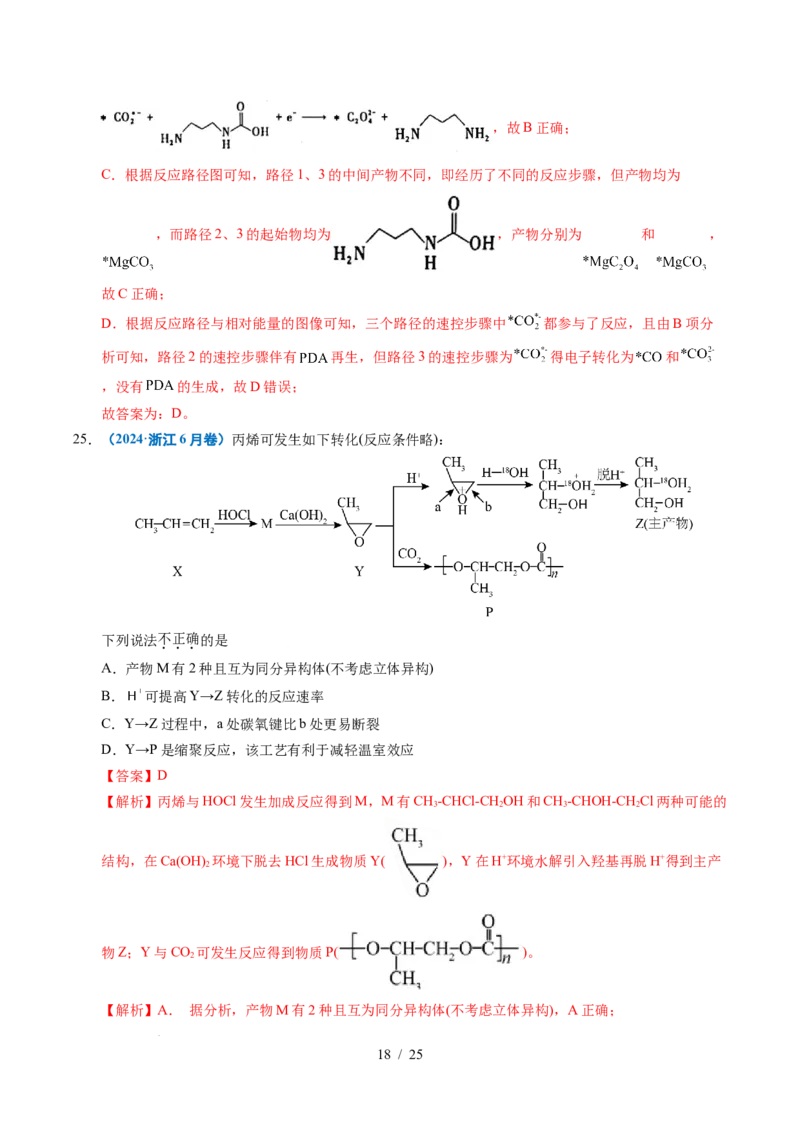
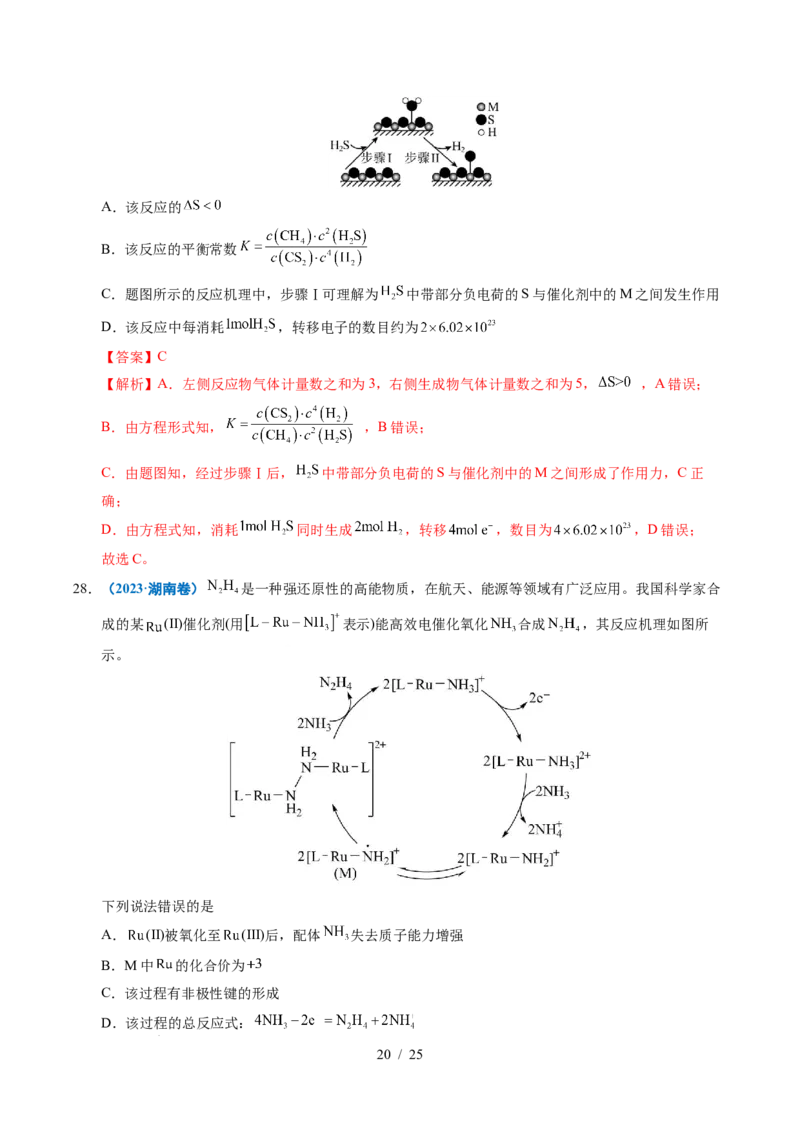
31.(2021·山东卷)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH- +CH O-能量变
3
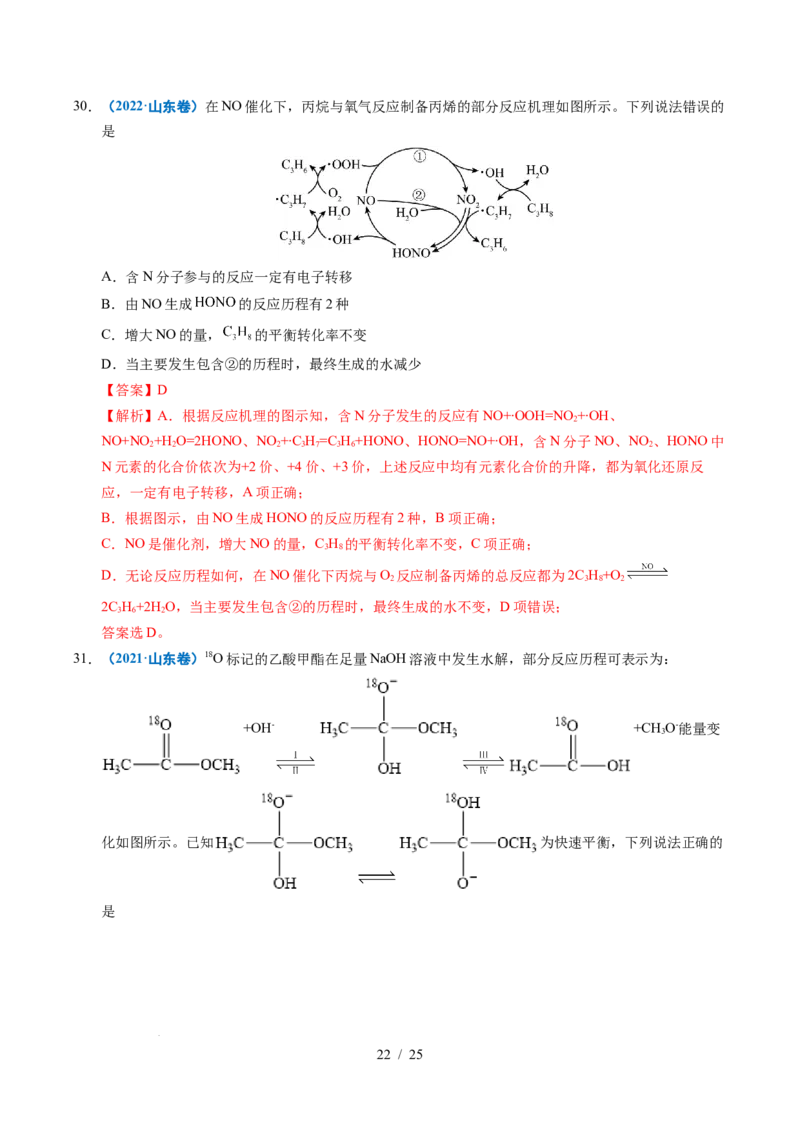
化如图所示。已知 为快速平衡,下列说法正确的
是
22 / 25
学学科科网网((北北京京))股股份份有有限限公公司司A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在CH18OH
3
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
【答案】B
【解析】A.一般来说,反应的活化能越高,反应速率越慢,由图可知,反应I和反应IV的活化能较
高,因此反应的决速步为反应I、IV,故A错误;
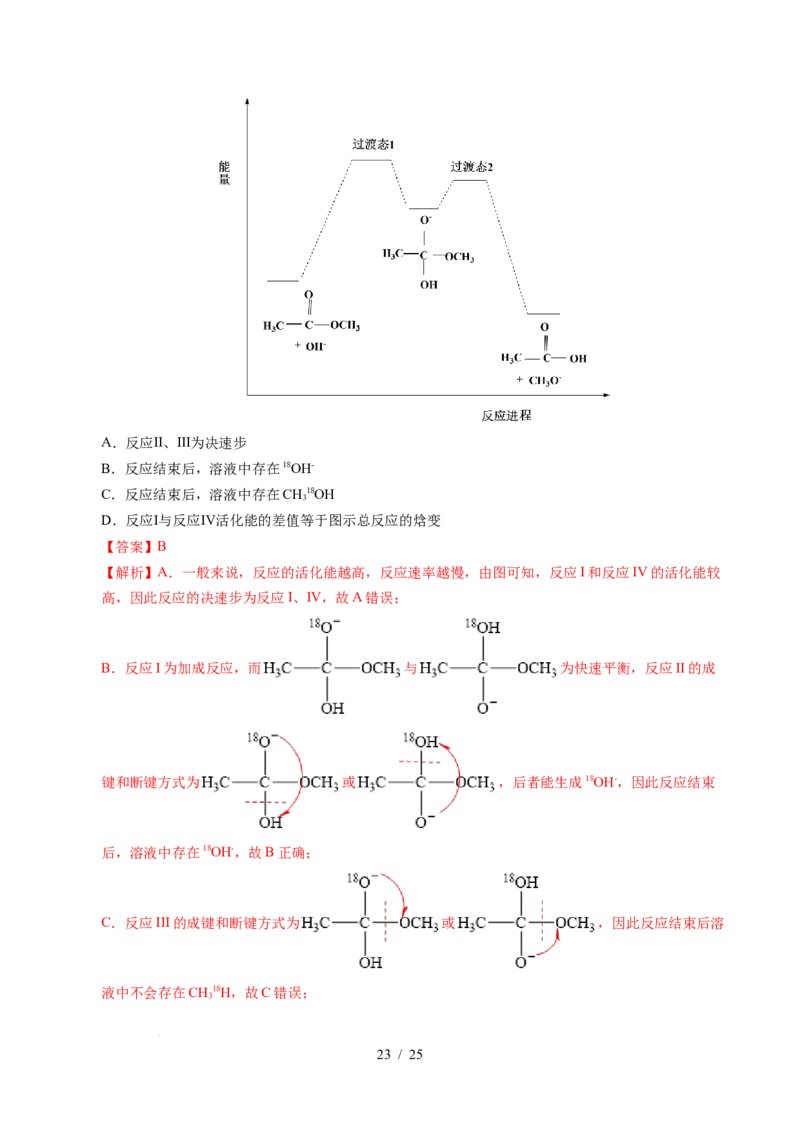
B.反应I为加成反应,而 与 为快速平衡,反应II的成
键和断键方式为 或 ,后者能生成18OH-,因此反应结束
后,溶液中存在18OH-,故B正确;
C.反应III的成键和断键方式为 或 ,因此反应结束后溶
液中不会存在CH18H,故C错误;
3
23 / 25
学学科科网网((北北京京))股股份份有有限限公公司司D.该总反应对应反应物的总能量高于生成物总能量,总反应为放热反应,因此
和CHO-的总能量与 和OH-的总能量之差等于图示总反应的焓变,故D错误;
3
综上所述,正确的是B项,故答案为B。
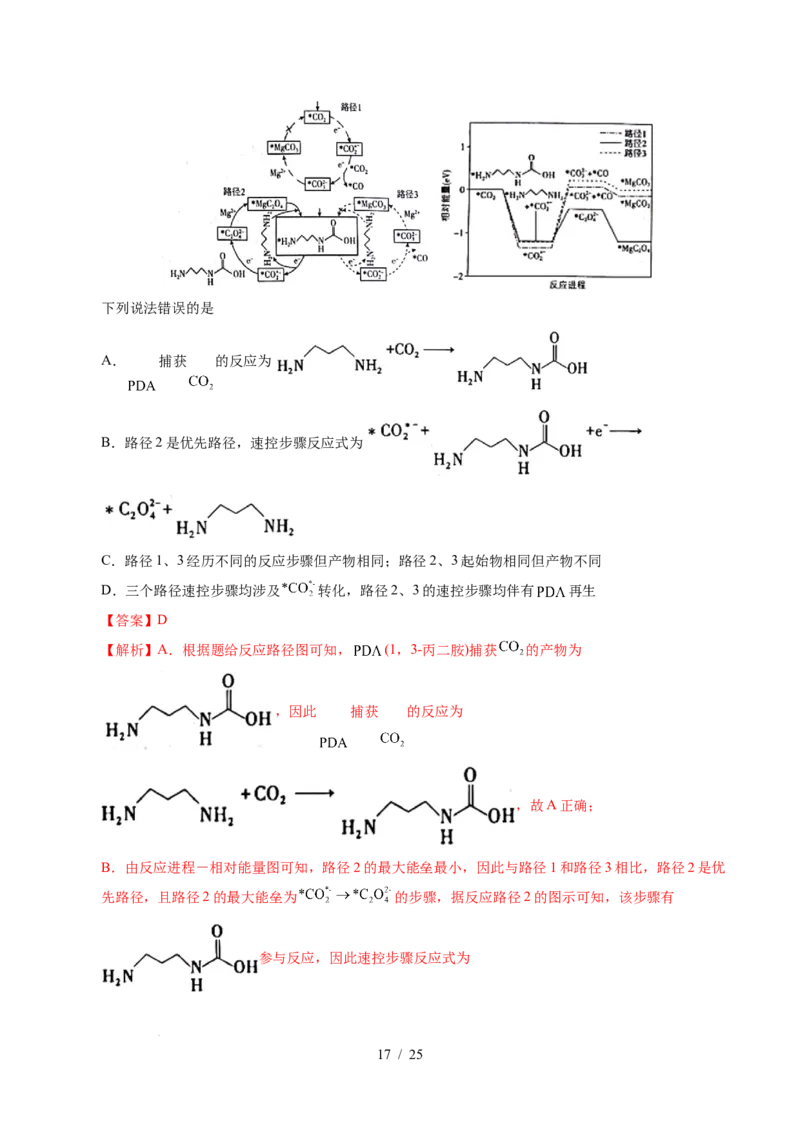
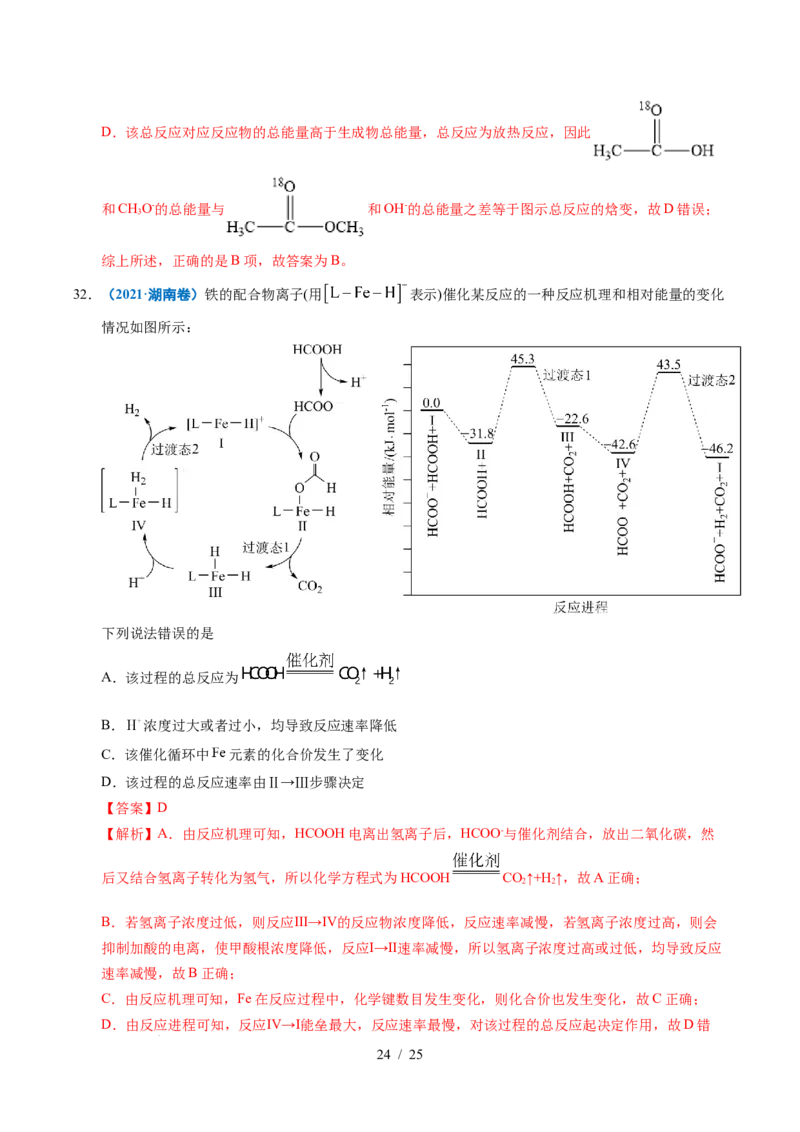
32.(2021·湖南卷)铁的配合物离子(用 表示)催化某反应的一种反应机理和相对能量的变化
情况如图所示:
下列说法错误的是
A.该过程的总反应为
B. 浓度过大或者过小,均导致反应速率降低
C.该催化循环中 元素的化合价发生了变化
D.该过程的总反应速率由Ⅱ→Ⅲ步骤决定
【答案】D
【解析】A.由反应机理可知,HCOOH电离出氢离子后,HCOO-与催化剂结合,放出二氧化碳,然
后又结合氢离子转化为氢气,所以化学方程式为HCOOH CO↑+H ↑,故A正确;
2 2
B.若氢离子浓度过低,则反应Ⅲ→Ⅳ的反应物浓度降低,反应速率减慢,若氢离子浓度过高,则会
抑制加酸的电离,使甲酸根浓度降低,反应Ⅰ→Ⅱ速率减慢,所以氢离子浓度过高或过低,均导致反应
速率减慢,故B正确;
C.由反应机理可知,Fe在反应过程中,化学键数目发生变化,则化合价也发生变化,故C正确;
D.由反应进程可知,反应Ⅳ→Ⅰ能垒最大,反应速率最慢,对该过程的总反应起决定作用,故D错
24 / 25
学学科科网网((北北京京))股股份份有有限限公公司司误;
故选D。
25 / 25
学学科科网网((北北京京))股股份份有有限限公公司司