文档内容
第 09 讲 氯气的实验室制法及氯离子的检验
模块一 思维导图串知识 1.掌握氯气的实验室制备原理及装置,培养科学探
模块二 基础知识全梳理(吃透教材) 究与创新意识,提升实验能力。
模块三 教材习题学解题 2.能结合实验室制取氯气的装置特点设计制备其他
模块四 核心考点精准练(6大考点) 气体的实验装置,培养科学探究与创新意识,提升
模块五 小试牛刀过关测 实验能力。
(基础练10题) 3.通过对比实验掌握氯离子的检验方法,培养证据
(提升练6题) 推理与科学探究能力。
一、氯气的实验室制法
1.反应原理
(1)在实验室中,通常用浓盐酸与二氧化锰反应来制取氯气,反应的化学方程式: ,
离子方程式: 。
(2)该反应的氧化剂是 ,浓盐酸既表现 性,又表现 性。
2.制备装置
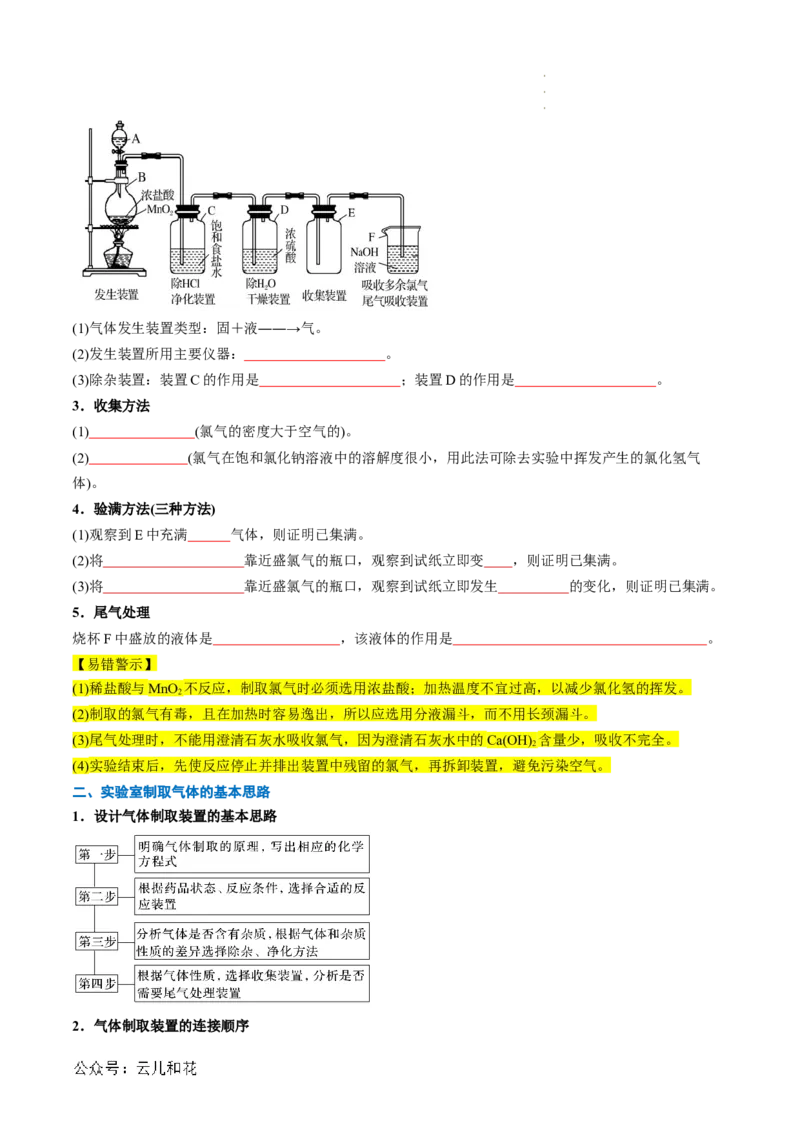
学科网(北京)股份有限公司(1)气体发生装置类型:固+液――→气。
(2)发生装置所用主要仪器: 。
(3)除杂装置:装置C的作用是 ;装置D的作用是 。
3.收集方法
(1) (氯气的密度大于空气的)。
(2) (氯气在饱和氯化钠溶液中的溶解度很小,用此法可除去实验中挥发产生的氯化氢气
体)。
4.验满方法(三种方法)
(1)观察到E中充满 气体,则证明已集满。
(2)将 靠近盛氯气的瓶口,观察到试纸立即变 ,则证明已集满。
(3)将 靠近盛氯气的瓶口,观察到试纸立即发生 的变化,则证明已集满。
5.尾气处理
烧杯F中盛放的液体是 ,该液体的作用是 。
【易错警示】
(1)稀盐酸与MnO 不反应,制取氯气时必须选用浓盐酸;加热温度不宜过高,以减少氯化氢的挥发。
2
(2)制取的氯气有毒,且在加热时容易逸出,所以应选用分液漏斗,而不用长颈漏斗。
(3)尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中的Ca(OH) 含量少,吸收不完全。
2
(4)实验结束后,先使反应停止并排出装置中残留的氯气,再拆卸装置,避免污染空气。
二、实验室制取气体的基本思路
1.设计气体制取装置的基本思路
2.气体制取装置的连接顺序
学科网(北京)股份有限公司3.各种装置的选择
(1)实验室制取气体的发生装置的选择
①选择依据
反应原理、反应物的状态、反应条件等。
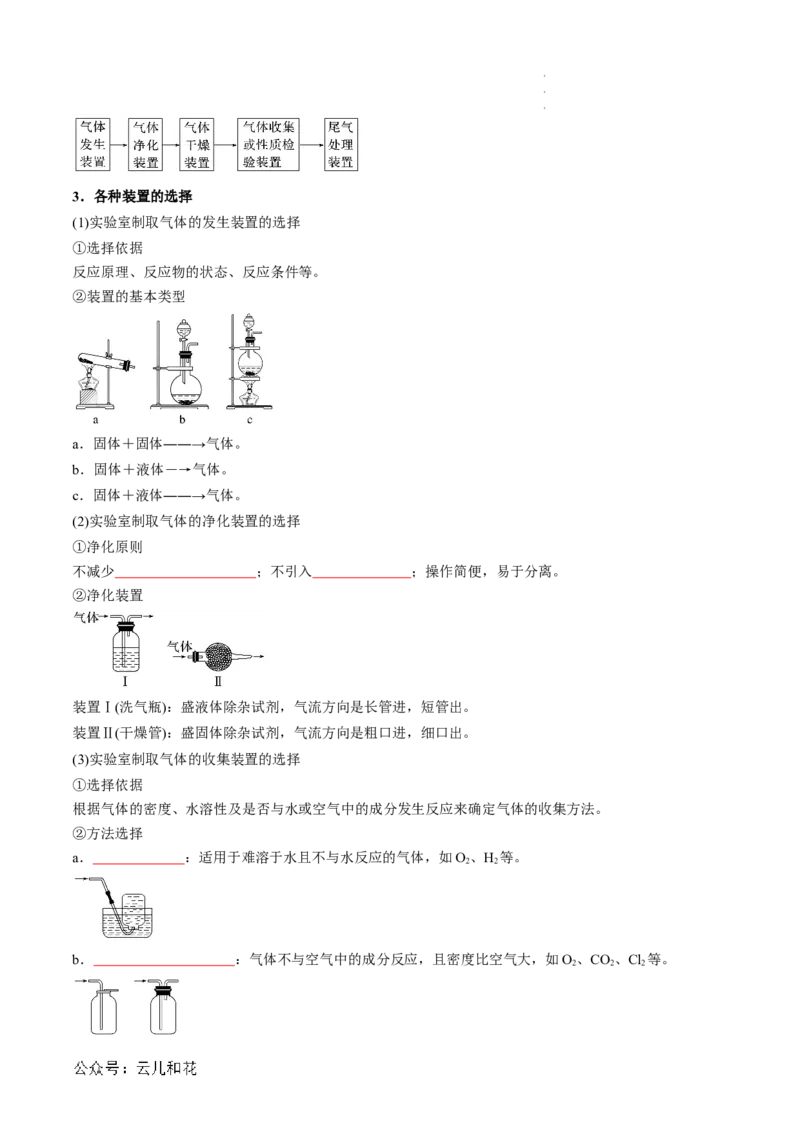
②装置的基本类型
a.固体+固体――→气体。
b.固体+液体―→气体。
c.固体+液体――→气体。
(2)实验室制取气体的净化装置的选择
①净化原则
不减少 ;不引入 ;操作简便,易于分离。
②净化装置
装置Ⅰ(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
装置Ⅱ(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
(3)实验室制取气体的收集装置的选择
①选择依据
根据气体的密度、水溶性及是否与水或空气中的成分发生反应来确定气体的收集方法。
②方法选择
a. :适用于难溶于水且不与水反应的气体,如O、H 等。
2 2
b. :气体不与空气中的成分反应,且密度比空气大,如O、CO、Cl 等。
2 2 2
学科网(北京)股份有限公司c. :气体不与空气中的成分反应,且密度比空气小,如H、CH 等。
2 4
(4)实验室制取气体的尾气处理装置的选择
①
a可用于NaOH溶液吸收Cl、CO(气体溶解或反应速率不快,不易引起倒吸)。b、c可用于收集极易溶且
2 2
溶解速率很快的气体,如HCl等。
②
可用于处理难以吸收且可燃的气体,如H、CO等。如图 ,但点燃前必须对气体进行验纯。
2
③
将气体用气球收集,然后处理,如图 。
三、氯离子的检验
1.氯离子的检验实验
实验现象
试液2~3 mL 离子方程式
滴入几滴硝酸银溶液 加入少量稀硝酸
①稀盐酸
②氯化钠溶液
③碳酸钠溶液
2.氯离子检验方法
(1)试剂: 、 。
(2)方法:先加稀硝酸,再加AgNO 溶液。
3
(3)现象:产生白色沉淀。
(4)原理: 。
【易错警示】氯离子的检验
取少量被检测溶液于试管中,滴加适量稀硝酸,然后滴入AgNO 溶液,若产生白色沉淀则被检测溶液中含
3
有Cl-,若不产生白色沉淀则无Cl-。
学科网(北京)股份有限公司教材习题01 解题思路
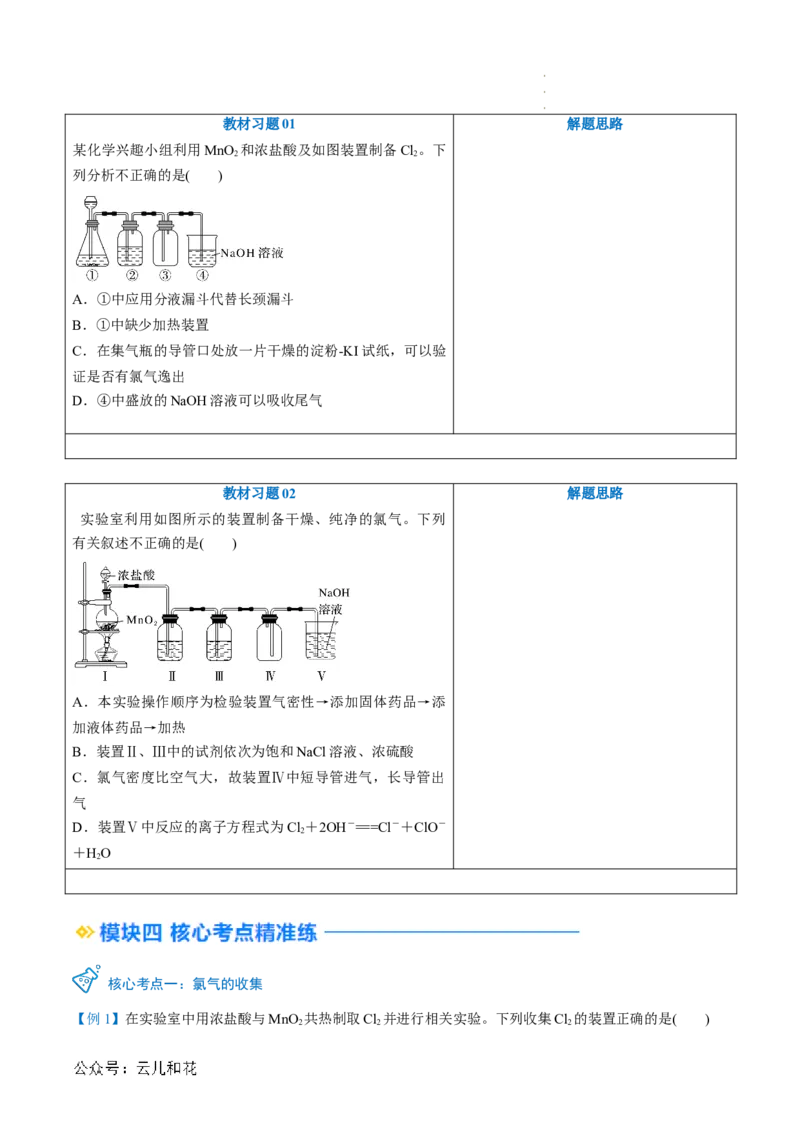
某化学兴趣小组利用MnO 和浓盐酸及如图装置制备Cl 。下
2 2
列分析不正确的是( )
A.①中应用分液漏斗代替长颈漏斗
B.①中缺少加热装置
C.在集气瓶的导管口处放一片干燥的淀粉-KI试纸,可以验
证是否有氯气逸出
D.④中盛放的NaOH溶液可以吸收尾气
教材习题02 解题思路
实验室利用如图所示的装置制备干燥、纯净的氯气。下列
有关叙述不正确的是( )
A.本实验操作顺序为检验装置气密性→添加固体药品→添
加液体药品→加热
B.装置Ⅱ、Ⅲ中的试剂依次为饱和NaCl溶液、浓硫酸
C.氯气密度比空气大,故装置Ⅳ中短导管进气,长导管出
气
D.装置Ⅴ中反应的离子方程式为Cl +2OH-===Cl-+ClO-
2
+HO
2
核心考点一:氯气的收集
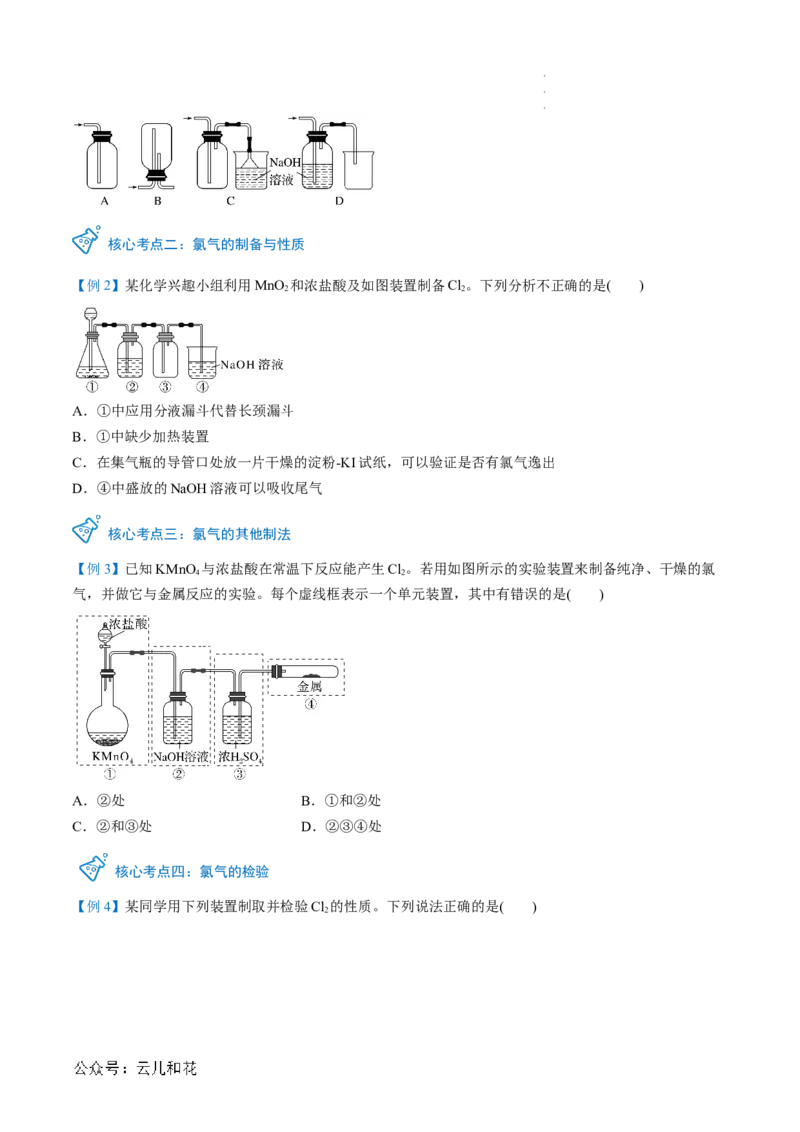
【例1】在实验室中用浓盐酸与MnO 共热制取Cl 并进行相关实验。下列收集Cl 的装置正确的是( )
2 2 2
学科网(北京)股份有限公司核心考点二:氯气的制备与性质
【例2】某化学兴趣小组利用MnO 和浓盐酸及如图装置制备Cl。下列分析不正确的是( )
2 2
A.①中应用分液漏斗代替长颈漏斗
B.①中缺少加热装置
C.在集气瓶的导管口处放一片干燥的淀粉-KI试纸,可以验证是否有氯气逸出
D.④中盛放的NaOH溶液可以吸收尾气
核心考点三:氯气的其他制法
【例3】已知KMnO 与浓盐酸在常温下反应能产生Cl。若用如图所示的实验装置来制备纯净、干燥的氯
4 2
气,并做它与金属反应的实验。每个虚线框表示一个单元装置,其中有错误的是( )
A.②处 B.①和②处
C.②和③处 D.②③④处
核心考点四:氯气的检验
【例4】某同学用下列装置制取并检验Cl 的性质。下列说法正确的是( )
2
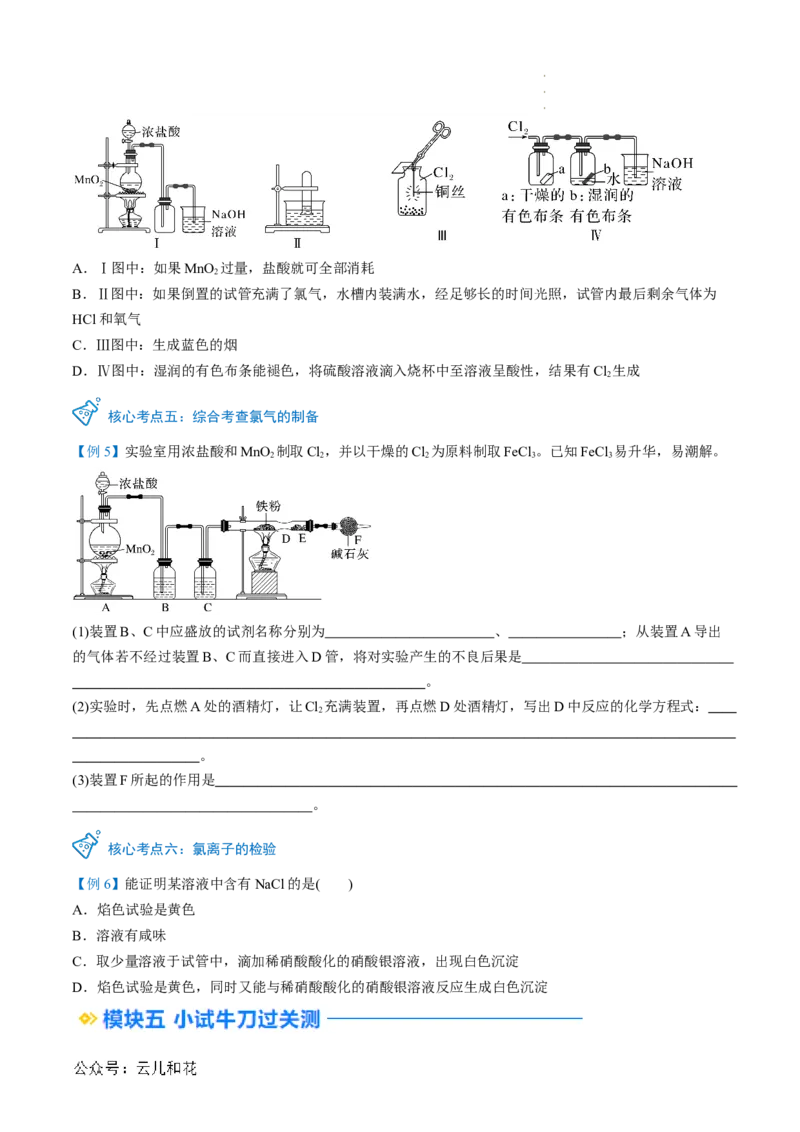
学科网(北京)股份有限公司A.Ⅰ图中:如果MnO 过量,盐酸就可全部消耗
2
B.Ⅱ图中:如果倒置的试管充满了氯气,水槽内装满水,经足够长的时间光照,试管内最后剩余气体为
HCl和氧气
C.Ⅲ图中:生成蓝色的烟
D.Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中至溶液呈酸性,结果有Cl 生成
2
核心考点五:综合考查氯气的制备
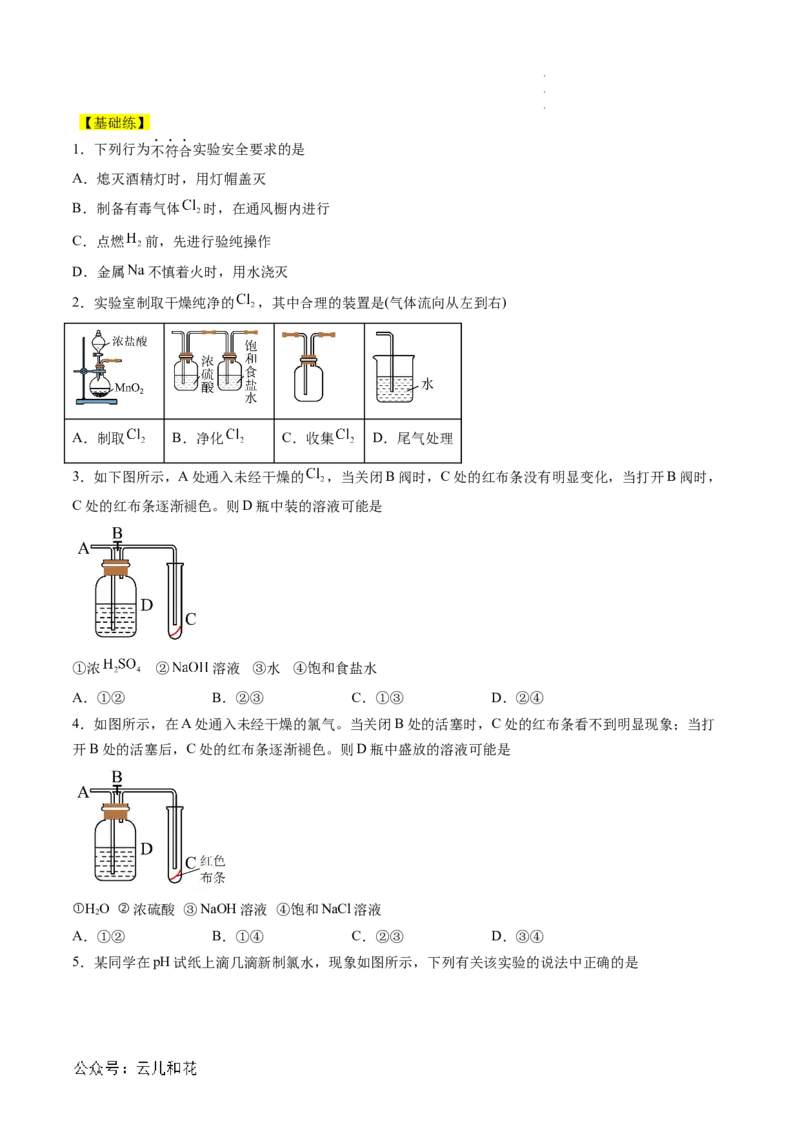
【例5】实验室用浓盐酸和MnO 制取Cl,并以干燥的Cl 为原料制取FeCl 。已知FeCl 易升华,易潮解。
2 2 2 3 3
(1)装置B、C中应盛放的试剂名称分别为 、 ;从装置A导出
的气体若不经过装置B、C而直接进入D管,将对实验产生的不良后果是
。
(2)实验时,先点燃A处的酒精灯,让Cl 充满装置,再点燃D处酒精灯,写出D中反应的化学方程式:
2
。
(3)装置F所起的作用是
。
核心考点六:氯离子的检验
【例6】能证明某溶液中含有NaCl的是( )
A.焰色试验是黄色
B.溶液有咸味
C.取少量溶液于试管中,滴加稀硝酸酸化的硝酸银溶液,出现白色沉淀
D.焰色试验是黄色,同时又能与稀硝酸酸化的硝酸银溶液反应生成白色沉淀
学科网(北京)股份有限公司【基础练】
1.下列行为不符合实验安全要求的是
A.熄灭酒精灯时,用灯帽盖灭
B.制备有毒气体 时,在通风橱内进行
C.点燃 前,先进行验纯操作
D.金属 不慎着火时,用水浇灭
2.实验室制取干燥纯净的 ,其中合理的装置是(气体流向从左到右)
A.制取 B.净化 C.收集 D.尾气处理
3.如下图所示,A处通入未经干燥的 ,当关闭B阀时,C处的红布条没有明显变化,当打开B阀时,
C处的红布条逐渐褪色。则D瓶中装的溶液可能是
①浓 ② 溶液 ③水 ④饱和食盐水
A.①② B.②③ C.①③ D.②④
4.如图所示,在A处通入未经干燥的氯气。当关闭B处的活塞时,C处的红布条看不到明显现象;当打
开B处的活塞后,C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是
①HO ②浓硫酸 ③NaOH溶液 ④饱和NaCl溶液
2
A.①② B.①④ C.②③ D.③④
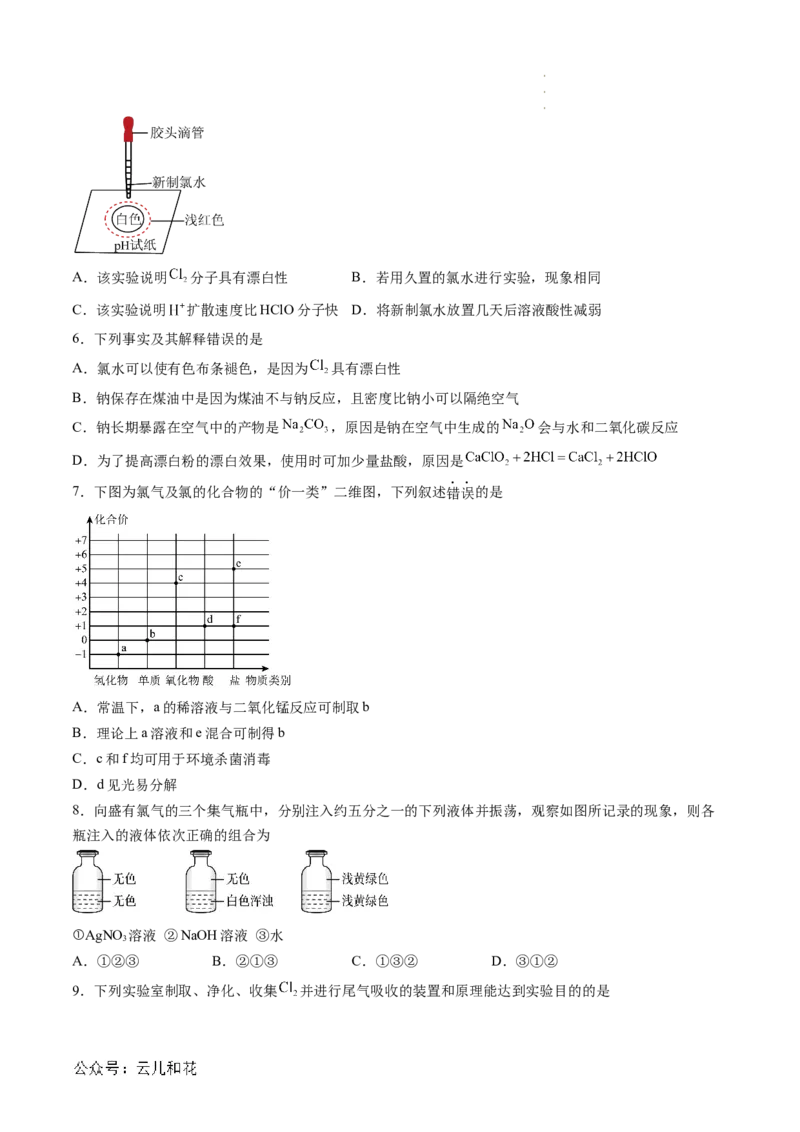
5.某同学在pH试纸上滴几滴新制氯水,现象如图所示,下列有关该实验的说法中正确的是
学科网(北京)股份有限公司A.该实验说明 分子具有漂白性 B.若用久置的氯水进行实验,现象相同
C.该实验说明 扩散速度比HClO分子快 D.将新制氯水放置几天后溶液酸性减弱
6.下列事实及其解释错误的是
A.氯水可以使有色布条褪色,是因为 具有漂白性
B.钠保存在煤油中是因为煤油不与钠反应,且密度比钠小可以隔绝空气
C.钠长期暴露在空气中的产物是 ,原因是钠在空气中生成的 会与水和二氧化碳反应
D.为了提高漂白粉的漂白效果,使用时可加少量盐酸,原因是
7.下图为氯气及氯的化合物的“价一类”二维图,下列叙述错误的是
A.常温下,a的稀溶液与二氧化锰反应可制取b
B.理论上a溶液和e混合可制得b
C.c和f均可用于环境杀菌消毒
D.d见光易分解
8.向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,则各
瓶注入的液体依次正确的组合为
①AgNO 溶液 ②NaOH溶液 ③水
3
A.①②③ B.②①③ C.①③② D.③①②
9.下列实验室制取、净化、收集 并进行尾气吸收的装置和原理能达到实验目的的是
学科网(北京)股份有限公司A.制备 B.净化 C.收集 D.尾气处理
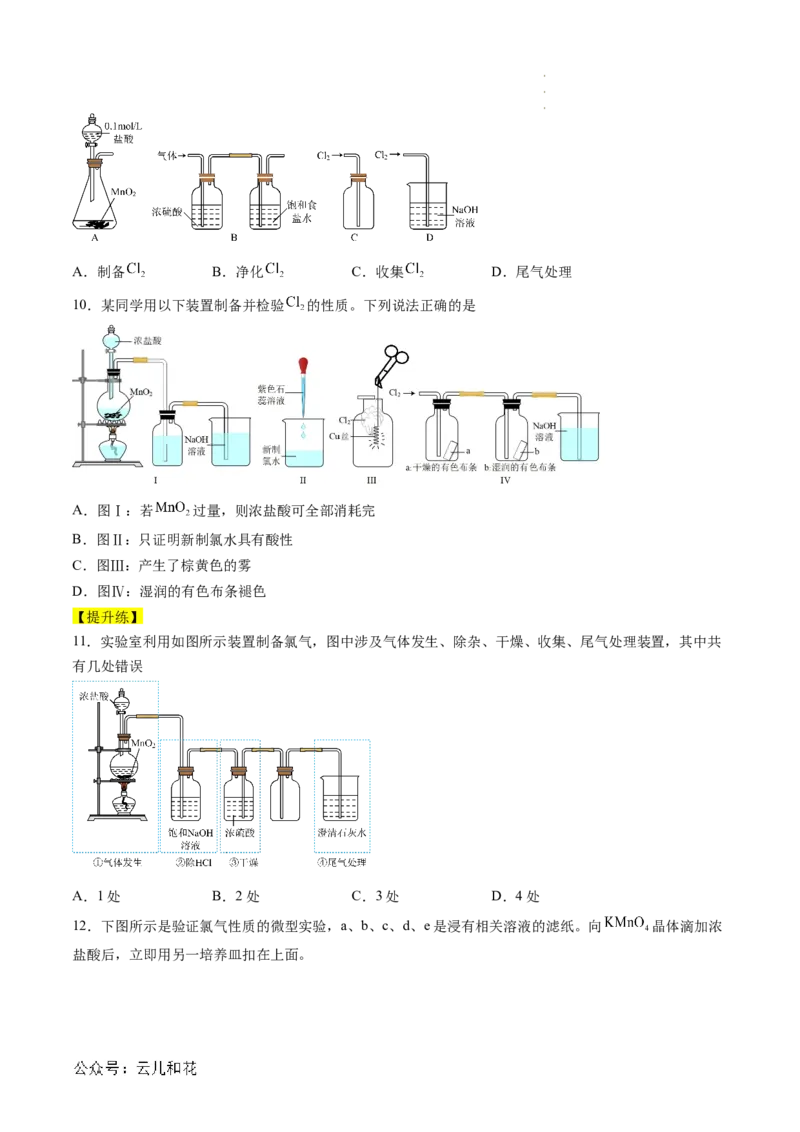
10.某同学用以下装置制备并检验 的性质。下列说法正确的是
A.图Ⅰ:若 过量,则浓盐酸可全部消耗完
B.图Ⅱ:只证明新制氯水具有酸性
C.图Ⅲ:产生了棕黄色的雾
D.图Ⅳ:湿润的有色布条褪色
【提升练】
11.实验室利用如图所示装置制备氯气,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中共
有几处错误
A.1处 B.2处 C.3处 D.4处
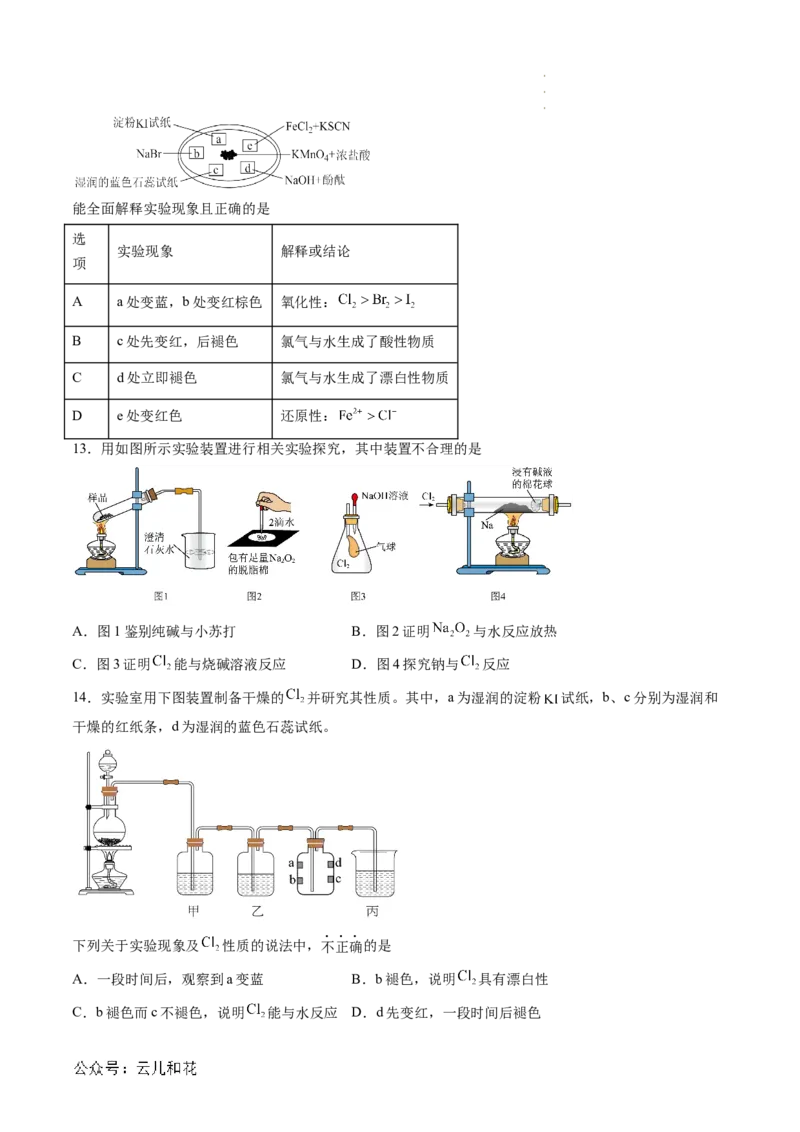
12.下图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向 晶体滴加浓
盐酸后,立即用另一培养皿扣在上面。
学科网(北京)股份有限公司能全面解释实验现象且正确的是
选
实验现象 解释或结论
项
A a处变蓝,b处变红棕色 氧化性:
B c处先变红,后褪色 氯气与水生成了酸性物质
C d处立即褪色 氯气与水生成了漂白性物质
D e处变红色 还原性:
13.用如图所示实验装置进行相关实验探究,其中装置不合理的是
A.图1鉴别纯碱与小苏打 B.图2证明 与水反应放热
C.图3证明 能与烧碱溶液反应 D.图4探究钠与 反应
14.实验室用下图装置制备干燥的 并研究其性质。其中,a为湿润的淀粉 试纸,b、c分别为湿润和
干燥的红纸条,d为湿润的蓝色石蕊试纸。
下列关于实验现象及 性质的说法中,不正确的是
A.一段时间后,观察到a变蓝 B.b褪色,说明 具有漂白性
C.b褪色而c不褪色,说明 能与水反应 D.d先变红,一段时间后褪色
学科网(北京)股份有限公司15.下列实验操作,现象及结论都正确的是
选
实验操作和现象 结论
项
A 向某溶液中加入稀盐酸至溶液呈酸性,产生使澄清石灰水变浑浊的气体 该溶液中含有
B 对某碱性溶液进行焰色试验,火焰颜色为黄色 该溶液为 溶液
C 向某溶液中加入氯化钡溶液有白色沉淀产生,再加过量稀盐酸,沉淀不消失 该溶液中含有
D 向某溶液中加入过量硝酸酸化的 溶液,有白色沉淀生成 该溶液中含有
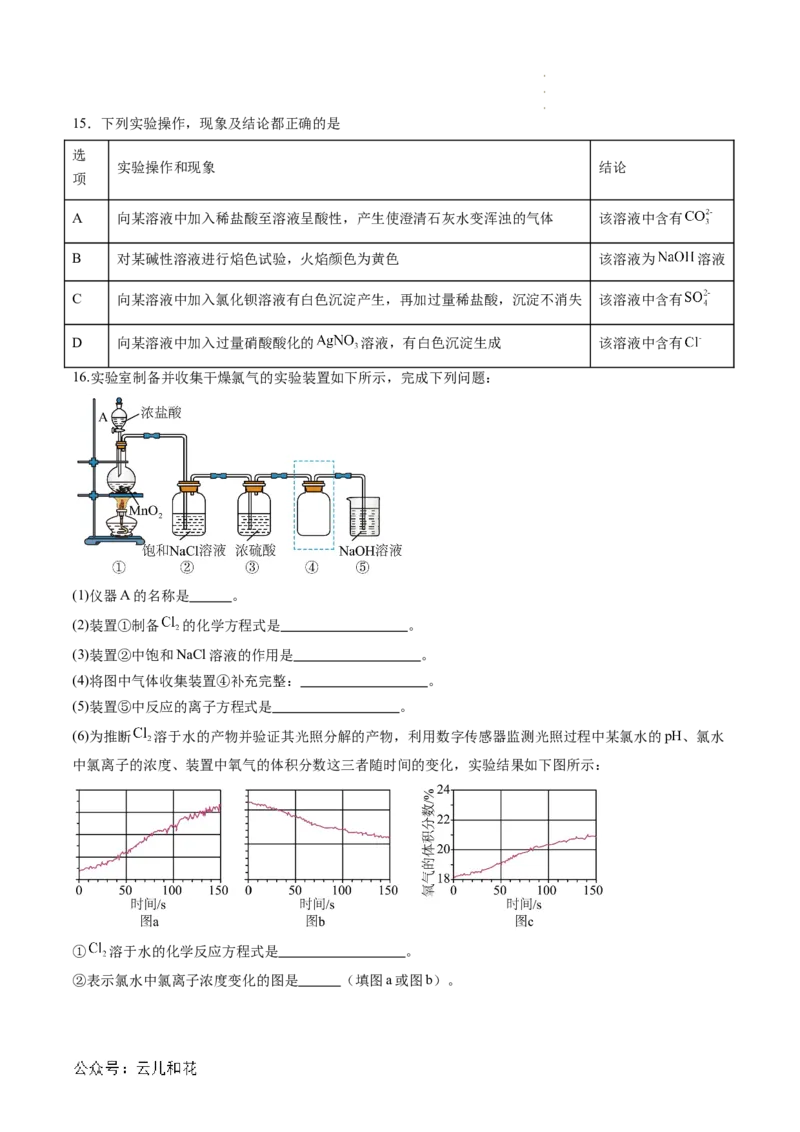
16.实验室制备并收集干燥氯气的实验装置如下所示,完成下列问题:
(1)仪器A的名称是 。
(2)装置①制备 的化学方程式是 。
(3)装置②中饱和NaCl溶液的作用是 。
(4)将图中气体收集装置④补充完整: 。
(5)装置⑤中反应的离子方程式是 。
(6)为推断 溶于水的产物并验证其光照分解的产物,利用数字传感器监测光照过程中某氯水的pH、氯水
中氯离子的浓度、装置中氧气的体积分数这三者随时间的变化,实验结果如下图所示:
① 溶于水的化学反应方程式是 。
②表示氯水中氯离子浓度变化的图是 (填图a或图b)。
学科网(北京)股份有限公司