文档内容
2014 年高考试卷和答案(安徽卷)化学 word 板
可能用到的相对原子量:li 7 O 16 F 19 P 31 S 32 Fe 56
第Ⅰ卷 (选择题 共120分)
每小题6分.在每题给出的四个选项中,只有一项是最符合题目要求的。
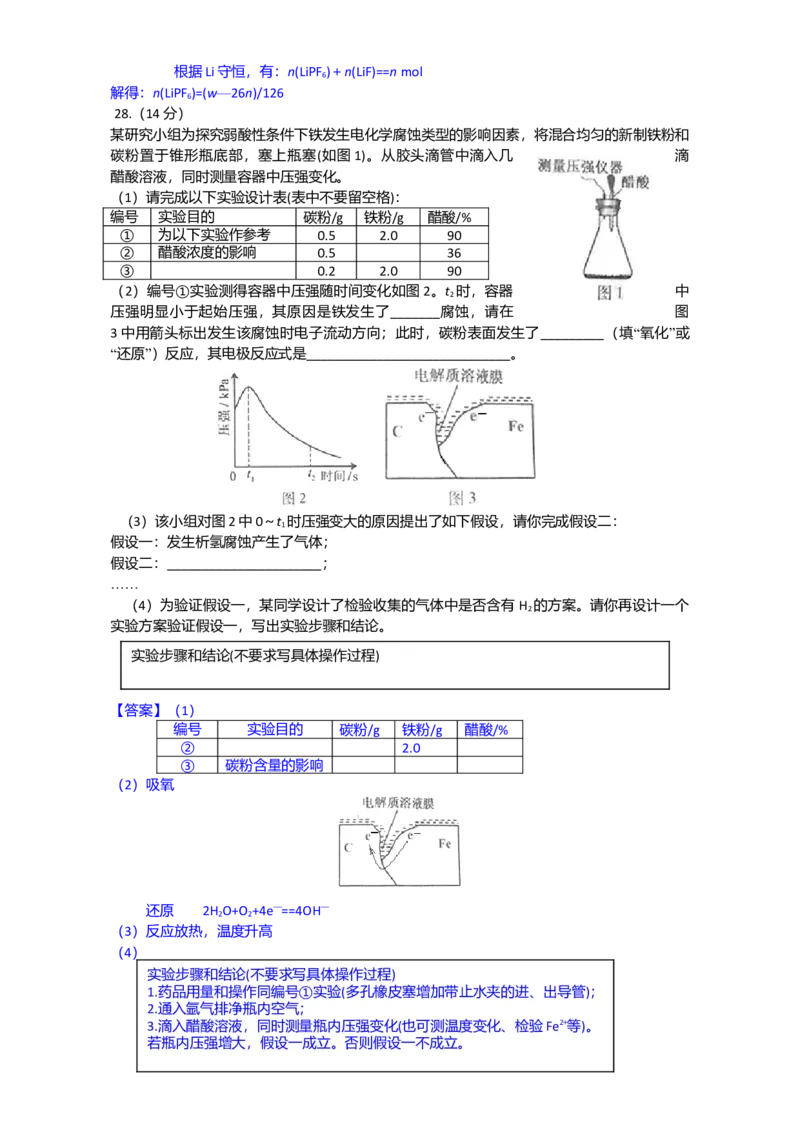
7.CO 的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH 捕获CO 生成重
2 3 2
要化工产品三聚氰酸的反应:
下列有关三聚氰酸的说法正确的是
A.分子式为C H N O B.分子中既含极性键,又含非极性键
3 6 3 3
C.属于共价化合物 D.生成该物质的上述反应为中和反应
8.下列有关Fe (SO ) ,溶液的叙述正确的是
2 4 3
A.该溶液中,K+、Fe2+、C H OH、Br-可以大量共存
6 5
B.和KI溶液反应的离子方程式:Fe3++2I-=Fe2++I
2
C.和Ba(OH) 溶液反应的离子方程式:Fe3++SO 2-+Ba2++3OH-=Fe(OH) ↓+BaSO ↓
2 4 3 4
D.1L0.1mol/L该溶液和足量的Zn充分反应,生成11.2gFe
9.为实现下列实验目的,依据下表提供的主要仪器,所用试剂合理的是
选 实验目的 主要仪器 试剂
项
A 分离Br 和CCl 混合物 分液漏斗、烧杯 Br 和CCl 混合物、蒸馏水
2 4 2 4
B 鉴别葡萄糖和蔗糖 试管、烧杯、酒精灯 葡萄糖溶液、蔗糖溶液、银氨溶液
C 实验室制取H 试管、带导管的橡皮塞 锌粒、稀HNO
2 3
D 测定NaOH溶液浓度 滴定管、锥形瓶、烧杯 NaOH溶液、0.1000mol/L盐酸
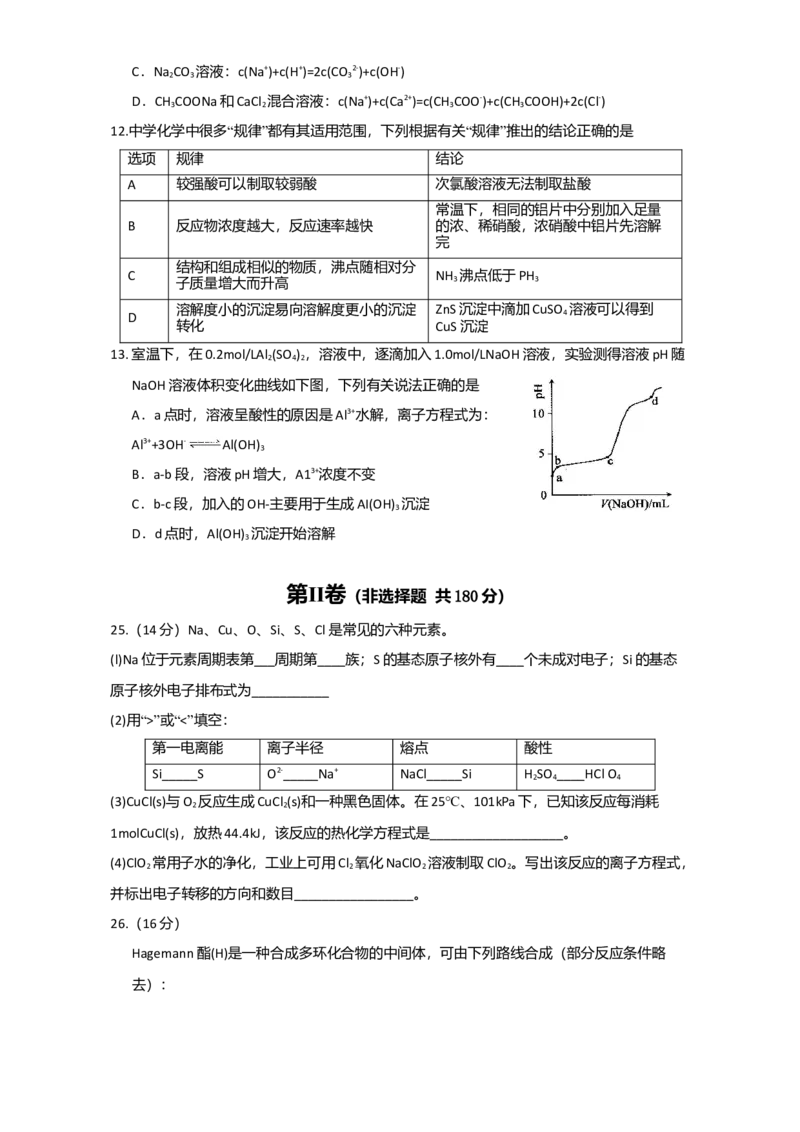
10.臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO (g)+O (g) N O (g)+O (g),若反应在
2 3 2 5 2
恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
11. 室温下,下列溶液中粒子浓度关系正确的是
A.Na S溶液:c(Na+)>c(HS-)>c(OH-)>c(H S)
2 2
B.Na C O 溶液:c(OH-)=c(H+)+c(HC O )+2c(H C O )
2 2 4 2 4 2 2 4C.Na CO 溶液:c(Na+)+c(H+)=2c(CO 2-)+c(OH-)
2 3 3
D.CH COONa和CaCl 混合溶液:c(Na+)+c(Ca2+)=c(CH COO-)+c(CH COOH)+2c(Cl-)
3 2 3 3
12.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是
选项 规律 结论
A 较强酸可以制取较弱酸 次氯酸溶液无法制取盐酸
常温下,相同的铝片中分别加入足量
B 反应物浓度越大,反应速率越快 的浓、稀硝酸,浓硝酸中铝片先溶解
完
结构和组成相似的物质,沸点随相对分
C NH 沸点低于PH
子质量增大而升高 3 3
溶解度小的沉淀易向溶解度更小的沉淀 ZnS沉淀中滴加CuSO 溶液可以得到
D 4
转化 CuS沉淀
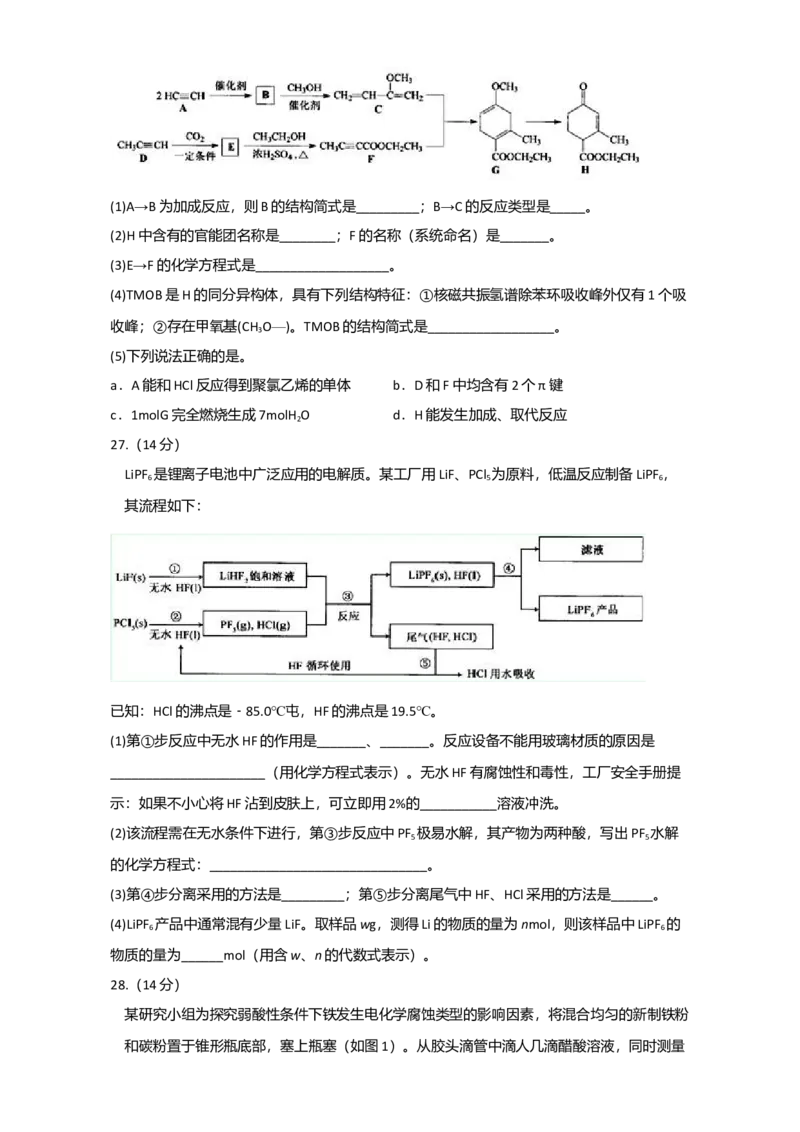
13. 室温下,在0.2mol/LAl (SO ) ,溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随
2 4 2
NaOH溶液体积变化曲线如下图,下列有关说法正确的是
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:
Al3++3OH- Al(OH)
3
B.a-b段,溶液pH增大,A13+浓度不变
C.b-c段,加入的OH-主要用于生成AI(OH) 沉淀
3
D.d点时,Al(OH) 沉淀开始溶解
3
第Ⅱ卷(非选择题 共180分)
25.(14分)Na、Cu、O、Si、S、Cl是常见的六种元素。
(l)Na位于元素周期表第___周期第____族;S的基态原子核外有____个未成对电子;Si的基态
原子核外电子排布式为___________
(2)用“>”或“<”填空:
第一电离能 离子半径 熔点 酸性
Si_____S O2-_____Na+ NaCl_____Si H SO ____HCl O
2 4 4
(3)CuCl(s)与O 反应生成CuCl (s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗
2 2
1molCuCl(s),放热44.4kJ,该反应的热化学方程式是___________________。
(4)ClO 常用子水的净化,工业上可用Cl 氧化NaClO 溶液制取ClO 。写出该反应的离子方程式,
2 2 2 2
并标出电子转移的方向和数目_________________。
26.(16分)
Hagemann酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略
去):(1)A→B为加成反应,则B的结构简式是_________;B→C的反应类型是_____。
(2)H中含有的官能团名称是________;F的名称(系统命名)是_______。
(3)E→F的化学方程式是___________________。
(4)TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有1个吸
收峰;②存在甲氧基(CH O—)。TMOB的结构简式是__________________。
3
(5)下列说法正确的是。
a.A能和HCl反应得到聚氯乙烯的单体 b.D和F中均含有2个π键
c.1molG完全燃烧生成7molH O d.H能发生加成、取代反应
2
27.(14分)
LiPF 是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl 为原料,低温反应制备LiPF ,
6 5 6
其流程如下:
已知:HCl的沸点是﹣85.0℃屯,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是_______、_______。反应设备不能用玻璃材质的原因是
______________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提
示:如果不小心将HF沾到皮肤上,可立即用2%的___________溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF 极易水解,其产物为两种酸,写出PF 水解
5 5
的化学方程式:_______________________________。
(3)第④步分离采用的方法是_________;第⑤步分离尾气中HF、HCl采用的方法是______。
(4)LiPF 产品中通常混有少量LiF。取样品wg,测得Li的物质的量为nmol,则该样品中LiPF 的
6 6
物质的量为______mol(用含w、n的代数式表示)。
28.(14分)
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉
和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴人几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
编号 实验目的 碳粉/g 铁粉/g 醋酸/%
① 为以下实验作参照 0.5 2.0 90.0
② 醋酸浓度的影响 0.5 36.0
③ 0.2 2.0 90.0
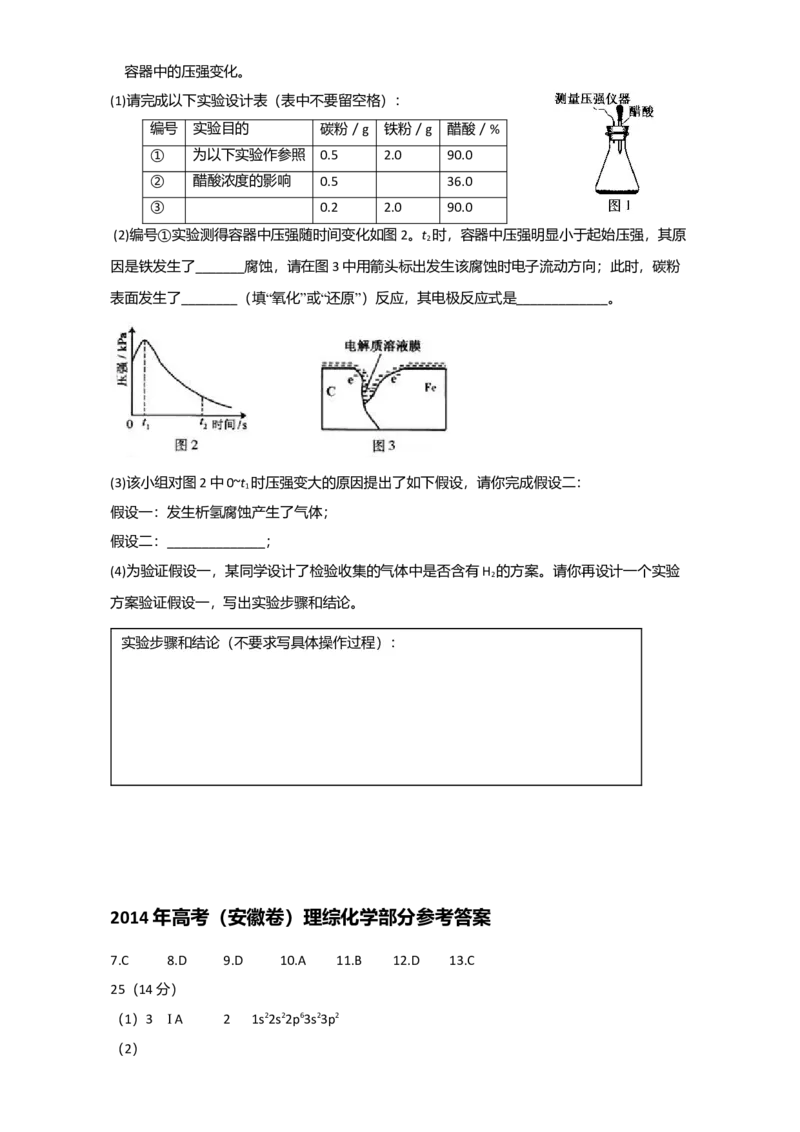
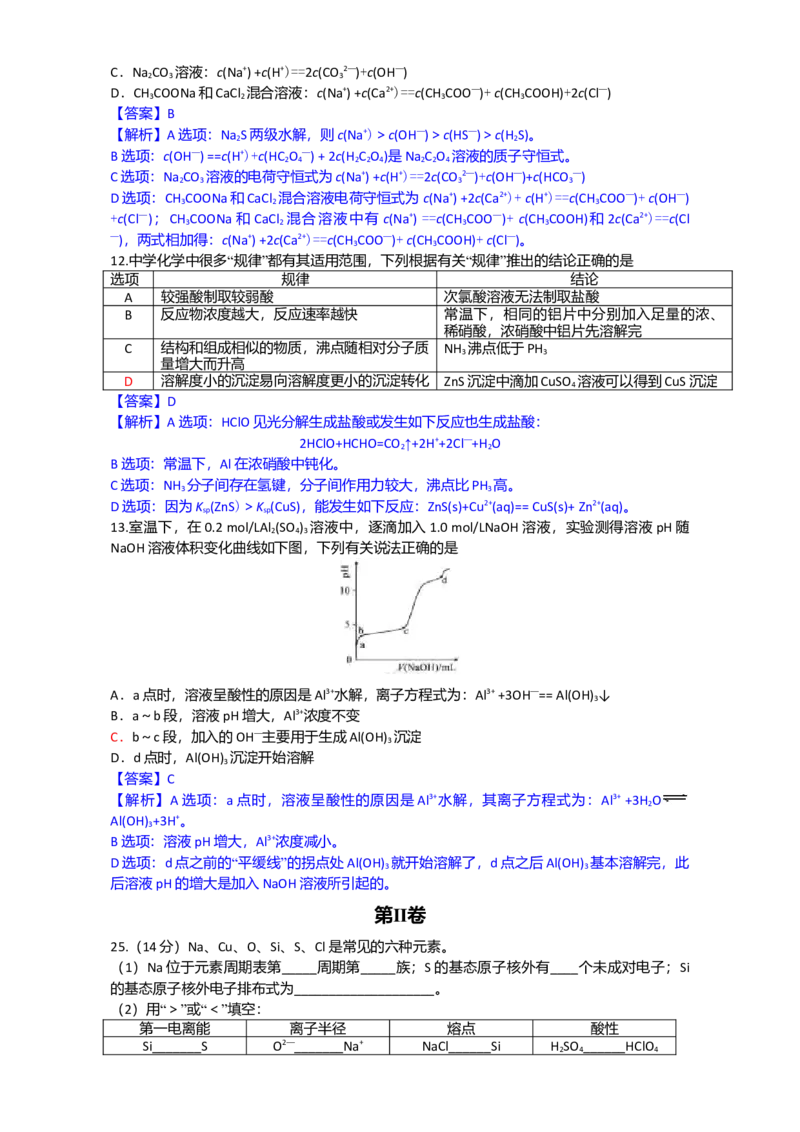
(2)编号①实验测得容器中压强随时间变化如图2。t 时,容器中压强明显小于起始压强,其原
2
因是铁发生了_______腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉
表面发生了________(填“氧化”或“还原”)反应,其电极反应式是_____________。
(3)该小组对图2中0~t 时压强变大的原因提出了如下假设,请你完成假设二:
1
假设一:发生析氢腐蚀产生了气体;
假设二:______________;
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H 的方案。请你再设计一个实验
2
方案验证假设一,写出实验步骤和结论。
实验步骤和结论(不要求写具体操作过程):
2014年高考(安徽卷)理综化学部分参考答案
7.C 8.D 9.D 10.A 11.B 12.D 13.C
25(14分)
(1)3 ⅠA 2 1s22s22p63s23p2
(2)第一电离能 离子半径 熔点 酸性
Si < S O2- > Na+ NaCl < Si H SO < HCl O
2 4 4
(3)4CuCl(s)+O (g)=CuCl (s)+CuO(s) △H=﹣176.6kJ/mol
2 2
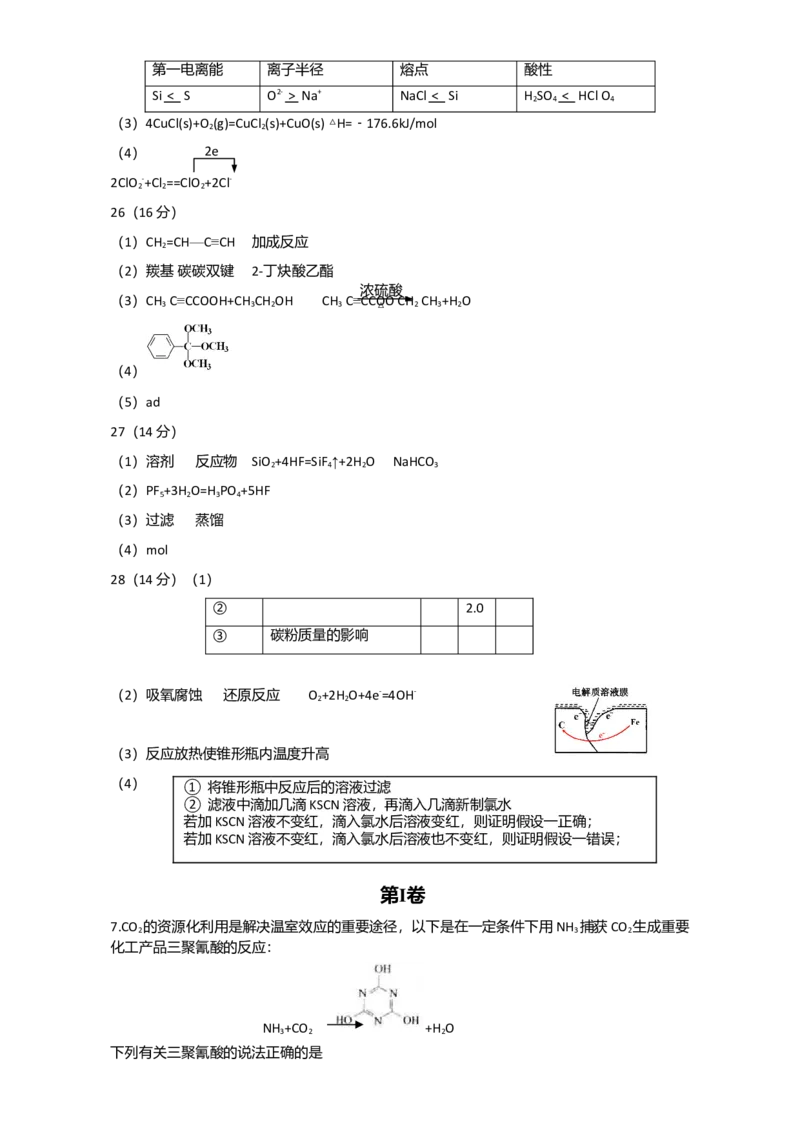
(4) 2e
2ClO -+Cl ==ClO +2Cl-
2 2 2
26(16分)
(1)CH =CH—C≡CH 加成反应
2
(2)羰基 碳碳双键 2-丁炔酸乙酯
浓硫酸
(3)CH C≡CCOOH+CH CH OH CH C≡CCOO CH CH +H O
3 3 2 3 △ 2 3 2
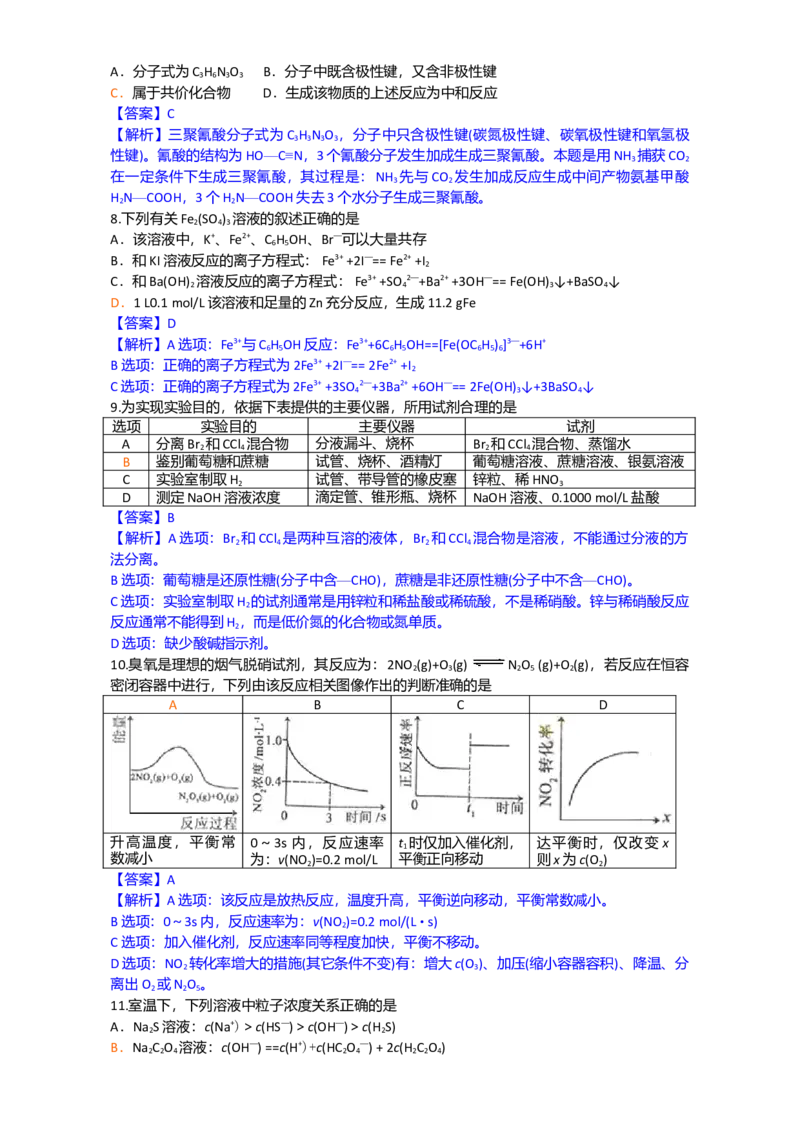
(4)
(5)ad
27(14分)
(1)溶剂 反应物 SiO +4HF=SiF ↑+2H O NaHCO
2 4 2 3
(2)PF +3H O=H PO +5HF
5 2 3 4
(3)过滤 蒸馏
(4)mol
28(14分)(1)
② 2.0
③ 碳粉质量的影响
(2)吸氧腐蚀 还原反应 O +2H O+4e-=4OH-
2 2
(3)反应放热使锥形瓶内温度升高
(4) ① 将锥形瓶中反应后的溶液过滤
② 滤液中滴加几滴KSCN溶液,再滴入几滴新制氯水
若加KSCN溶液不变红,滴入氯水后溶液变红,则证明假设一正确;
若加KSCN溶液不变红,滴入氯水后溶液也不变红,则证明假设一错误;
2014年安徽高考理综化学试题解析
第Ⅰ卷
7.CO 的资源化利用是解决温室效应的重要途径,以下是在一定条件下用NH 捕获CO 生成重要
2 3 2
化工产品三聚氰酸的反应:
NH +CO +H O
3 2 2
下列有关三聚氰酸的说法正确的是A.分子式为C H N O B.分子中既含极性键,又含非极性键
3 6 3 3
C.属于共价化合物 D.生成该物质的上述反应为中和反应
【答案】C
【解析】三聚氰酸分子式为C H N O ,分子中只含极性键(碳氮极性键、碳氧极性键和氧氢极
3 3 3 3
性键)。氰酸的结构为HO—C≡N,3个氰酸分子发生加成生成三聚氰酸。本题是用NH 捕获CO
3 2
在一定条件下生成三聚氰酸,其过程是:NH 先与CO 发生加成反应生成中间产物氨基甲酸
3 2
H N—COOH,3个H N—COOH失去3个水分子生成三聚氰酸。
2 2
8.下列有关Fe (SO ) 溶液的叙述正确的是
2 4 3
A.该溶液中,K+、Fe2+、C H OH、Br—可以大量共存
6 5
B.和KI溶液反应的离子方程式: Fe3+ +2I—== Fe2+ +I
2
C.和Ba(OH) 溶液反应的离子方程式: Fe3+ +SO 2—+Ba2+ +3OH—== Fe(OH) ↓+BaSO ↓
2 4 3 4
D.1 L0.1 mol/L该溶液和足量的Zn充分反应,生成11.2 gFe
【答案】D
【解析】A选项:Fe3+与C H OH反应:Fe3++6C H OH==[Fe(OC H ) ]3—+6H+
6 5 6 5 6 5 6
B选项:正确的离子方程式为2Fe3+ +2I—== 2Fe2+ +I
2
C选项:正确的离子方程式为2Fe3+ +3SO 2—+3Ba2+ +6OH—== 2Fe(OH) ↓+3BaSO ↓
4 3 4
9.为实现实验目的,依据下表提供的主要仪器,所用试剂合理的是
选项 实验目的 主要仪器 试剂
A 分离Br 和CCl 混合物 分液漏斗、烧杯 Br 和CCl 混合物、蒸馏水
2 4 2 4
B 鉴别葡萄糖和蔗糖 试管、烧杯、酒精灯 葡萄糖溶液、蔗糖溶液、银氨溶液
C 实验室制取H 试管、带导管的橡皮塞 锌粒、稀HNO
2 3
D 测定NaOH溶液浓度 滴定管、锥形瓶、烧杯 NaOH溶液、0.1000 mol/L盐酸
【答案】B
【解析】A选项:Br 和CCl 是两种互溶的液体,Br 和CCl 混合物是溶液,不能通过分液的方
2 4 2 4
法分离。
B选项:葡萄糖是还原性糖(分子中含—CHO),蔗糖是非还原性糖(分子中不含—CHO)。
C选项:实验室制取H 的试剂通常是用锌粒和稀盐酸或稀硫酸,不是稀硝酸。锌与稀硝酸反应
2
反应通常不能得到H ,而是低价氮的化合物或氮单质。
2
D选项:缺少酸碱指示剂。
10.臭氧是理想的烟气脱硝试剂,其反应为:2NO (g)+O (g) N O (g)+O (g),若反应在恒容
2 3 2 5 2
密闭容器中进行,下列由该反应相关图像作出的判断准确的是
A B C D
升高温度,平衡常 0~3s 内,反应速率 t 时仅加入催化剂, 达平衡时,仅改变 x
1
数减小 为:v(NO )=0.2 mol/L 平衡正向移动 则x为c(O )
2 2
【答案】A
【解析】A选项:该反应是放热反应,温度升高,平衡逆向移动,平衡常数减小。
B选项:0~3s内,反应速率为:v(NO )=0.2 mol/(L·s)
2
C 选项:加入催化剂,反应速率同等程度加快,平衡不移动。
D选项:NO 转化率增大的措施(其它条件不变)有:增大c(O )、加压(缩小容器容积)、降温、分
2 3
离出O 或N O 。
2 2 5
11.室温下,下列溶液中粒子浓度关系正确的是
A.Na S溶液:c(Na+)>c(HS—)>c(OH—)>c(H S)
2 2
B.Na C O 溶液:c(OH—) ==c(H+)+c(HC O —) + 2c(H C O )
2 2 4 2 4 2 2 4C.Na CO 溶液:c(Na+) +c(H+)==2c(CO 2—)+c(OH—)
2 3 3
D.CH COONa和CaCl 混合溶液:c(Na+) +c(Ca2+)==c(CH COO—)+ c(CH COOH)+2c(Cl—)
3 2 3 3
【答案】B
【解析】A选项:Na S两级水解,则c(Na+)>c(OH—)>c(HS—)>c(H S)。
2 2
B选项:c(OH—) ==c(H+)+c(HC O —) + 2c(H C O )是Na C O 溶液的质子守恒式。
2 4 2 2 4 2 2 4
C选项:Na CO 溶液的电荷守恒式为c(Na+) +c(H+)==2c(CO 2—)+c(OH—)+c(HCO —)
2 3 3 3
D选项:CH COONa和CaCl 混合溶液电荷守恒式为c(Na+) +2c(Ca2+)+ c(H+)==c(CH COO—)+ c(OH—)
3 2 3
+c(Cl—);CH COONa 和 CaCl 混合溶液中有 c(Na+) ==c(CH COO—)+ c(CH COOH)和 2c(Ca2+)==c(Cl
3 2 3 3
—),两式相加得:c(Na+) +2c(Ca2+)==c(CH COO—)+ c(CH COOH)+ c(Cl—)。
3 3
12.中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论正确的是
选项 规律 结论
A 较强酸制取较弱酸 次氯酸溶液无法制取盐酸
B 反应物浓度越大,反应速率越快 常温下,相同的铝片中分别加入足量的浓、
稀硝酸,浓硝酸中铝片先溶解完
C 结构和组成相似的物质,沸点随相对分子质 NH 沸点低于PH
3 3
量增大而升高
D 溶解度小的沉淀易向溶解度更小的沉淀转化 ZnS沉淀中滴加CuSO 溶液可以得到CuS沉淀
4
【答案】D
【解析】A 选项:HClO见光分解生成盐酸或发生如下反应也生成盐酸:
2HClO+HCHO=CO ↑+2H++2Cl—+H O
2 2
B选项:常温下,Al在浓硝酸中钝化。
C选项:NH 分子间存在氢键,分子间作用力较大,沸点比PH 高。
3 3
D选项:因为K (ZnS)>K (CuS),能发生如下反应:ZnS(s)+Cu2+(aq)== CuS(s)+ Zn2+(aq)。
sp sp
13.室温下,在0.2 mol/LAl (SO ) 溶液中,逐滴加入1.0 mol/LNaOH溶液,实验测得溶液pH随
2 4 3
NaOH溶液体积变化曲线如下图,下列有关说法正确的是
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:Al3+ +3OH—== Al(OH) ↓
3
B.a~b段,溶液pH增大,Al3+浓度不变
C.b~c段,加入的OH—主要用于生成Al(OH) 沉淀
3
D.d点时,Al(OH) 沉淀开始溶解
3
【答案】C
【解析】A选项:a点时,溶液呈酸性的原因是Al3+水解,其离子方程式为:Al3+ +3H O
2
Al(OH) +3H+。
3
B选项:溶液pH增大,Al3+浓度减小。
D选项:d点之前的“平缓线”的拐点处Al(OH) 就开始溶解了,d点之后Al(OH) 基本溶解完,此
3 3
后溶液pH的增大是加入NaOH溶液所引起的。
第Ⅱ卷
25.(14分)Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第_____周期第_____族;S的基态原子核外有____个未成对电子;Si
的基态原子核外电子排布式为____________________。
(2)用“>”或“<”填空:
第一电离能 离子半径 熔点 酸性
Si_______S O2—_______Na+ NaCl______Si H SO ______HClO
2 4 4(3)CuCl(s)与O 反应生成CuCl (s)和一种黑色固体。在25、101kPa下,已知该反应每消耗1
2 2
mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是___________________________。
(4)ClO 常用于水的净化,工业上可用Cl 氧化NaClO 溶液制取ClO 。写出该反应的离子方程
2 2 2 2
式,并标出电子转移的方向和数目____________________________________。
【答案】(1)三 IA 2 1s22s22p63s23p2
(2)
< > < <
(3)4CuCl(s)+O (g)==2CuCl (s)+2CuO(s) △H=—177.6 kJ/mol
2 2
(4) 2e—
2ClO — + Cl ==ClO +2Cl—
2 2 2
26.(16分)
Hagemann酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):
OCH
催化剂 CH OH
2CH≡CH B 催化 3 剂 3 OCH O
CH =CH—C=CH 3
2 2
A C
CH 3 CH 3
CH 3 C≡CH 一定 C 条 O 2 件 E CH 浓 3 C H H 2 2 S O O H 4 CH 3 C≡CCOOCH 2 CH 3 CH C 3 OOCH 2 CH C 3 OOCH 2
D G
F H
(1)A → B为加成反应,则B的结构简式是______________;B C的反应类型是_____。
(2)H中含有的官能团名称是____________;F的名称(系统命名)__________________。
(3)E → F的化学方程式是__________________________________________________。
(4)TMOB是H的同分异构体,具有下列结构特征:①核磁共振氢谱除苯环吸收峰外仅有 1
个吸收峰;②存在甲氧基(CH O—)。TMOB的结构简式是____________________。
3
(5)下列说法正确的是________________。
a.A能和HCl反应得到聚氯乙烯的单体 b.D和F中均含有2个π键
c.1 mol G 完全燃烧生成7 molH O d.H能发生加成、取代反应
2
【答案】(16分)(1)CH =CH—C≡CH 加成
2
(2)碳碳双键 羰基 酯基 2-丁炔酸乙酯
浓H SO
2 4
(3)CH C≡CCOOH+CH CH OH △ CH C≡CCOOCH CH +H O
3 3 2 3 2 3 2
(4) OCH
3
—C—OCH
3
OCH (5)ad
3
【解析】合成路线中涉及了多个加成反应:
A B:
催化剂
2CH≡CH CH =CH—C≡CH
2
B C:
OCH
催化剂 3
CH 2 =CH—C≡CH+ CH 3 OH CH 2 =CH—C=CH 2
D E:
一定条件
CH C≡CH+O=C=O CH C≡C—COOH
3 3
E F是酯化反应。C和F生成 G是烯炔加成成环(环加成):
CH CH COO CH OCH
3 2 2 3
C C—OCH
3
CH
C CH 3
COOCH
2
CH
3CH CH
3 2
G H是在HI作用下先生成烯醇,烯醇重排生成H:
OCH 3 OH O
HI
CH 3 无水乙醚 CH 3 分子重排 CH 3
COOCH 2 COOCH 2 COOCH 2
CH 3 CH 3 CH 3
第(4)题H分子中有10个碳原子3个氧原子不饱和度Ω=4,而TMOB分子中含有苯环
(Ω=4)且核磁共振氢谱只有1个吸收峰就是CH O—中氢的吸收峰,除去苯环的6个碳原子,还
3
有4个碳原子和3个氧原子,所以HMOB分子中还含有3个—OCH 。HMOB的结构:
3
OCH
3
—C—OCH
3
OCH
3
第(5)题b选项:F分子中含1个—C≡C—和1个酯基,分子中含3个π键。
c选项:G的分子式为C H O 即完全燃烧生成8 mol H O。
11 16 3 2
27.(14分)
LiPF 是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF ,其
6 6
流程如下:
滤液
① LiHF 2 ④
LiF(s) 无水HF(l) 饱和溶液 LiPF 6 (s)、HF(l)
③ LiPF 6 产品
反应
② 尾 气 (HF ,
PCl 5 (s) 无水HF(l) PF 5 (g)、HCl(g) HCl)
⑤
HF循环使用
HCl用水吸收
已知:HCl的沸点是—85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是____________、_____________。反应设备不能用玻璃
材质的原因是________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全
手册提示:如果不小心将HF沾到皮肤上,可立即用2%的_______溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF 极易水解,其产物为两种酸,写出
5
PF 水解的化学方程式:________________________________________。
5
(3)第④步分离采用的方法是_______;第⑤步分离尾气中HF、HCl采用的方法是____
________。
(4)LiPF 产品中通常混有少量LiF。取样品w g,测得Li的物质的量为n mol,则该样品中
6
LiPF 的物质的量为_______mol(用含w、n的代数式表示)。
6
【答案】(14分)
(1)反应物 溶剂 SiO +4HF==SiF ↑+2H O NaHCO
2 4 2 3
(2)PF +4H O==H PO +5HF
5 2 3 4
(3)过滤 冷凝
(4)(w—26n)/126
【解析】题给的生产流程除了用水吸收HCl外,其它流程均是在非水状态下进行的。因此LiHF
2
的饱和溶液是LiF(s)溶于无水HF(l)中所得到的溶液,这里无水HF(l)不仅是反应物而且是溶剂。
分离LiPF (s)和HF(l)的混合物最佳方法应是蒸馏,但第④步题给分离后的“滤液”暗示分离的方
6
法是过滤,第⑤步分离尾气中HF、HCl应是根据其沸点通过冷却液化分离出 HF,然后用水吸
收HCl。
(4)根据质量守恒,有:152 g·mol—1n(LiPF )+26 g·mol—1n(LiF)==w g
6根据Li守恒,有:n(LiPF )+n(LiF)==n mol
6
解得:n(LiPF )=(w—26n)/126
6
28.(14分)
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和
碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几 滴
醋酸溶液,同时测量容器中压强变化。
(1)请完成以下实验设计表(表中不要留空格):
编号 实验目的 碳粉/g 铁粉/g 醋酸/%
① 为以下实验作参考 0.5 2.0 90
② 醋酸浓度的影响 0.5 36
③ 0.2 2.0 90
(2)编号①实验测得容器中压强随时间变化如图2。t 时,容器 中
2
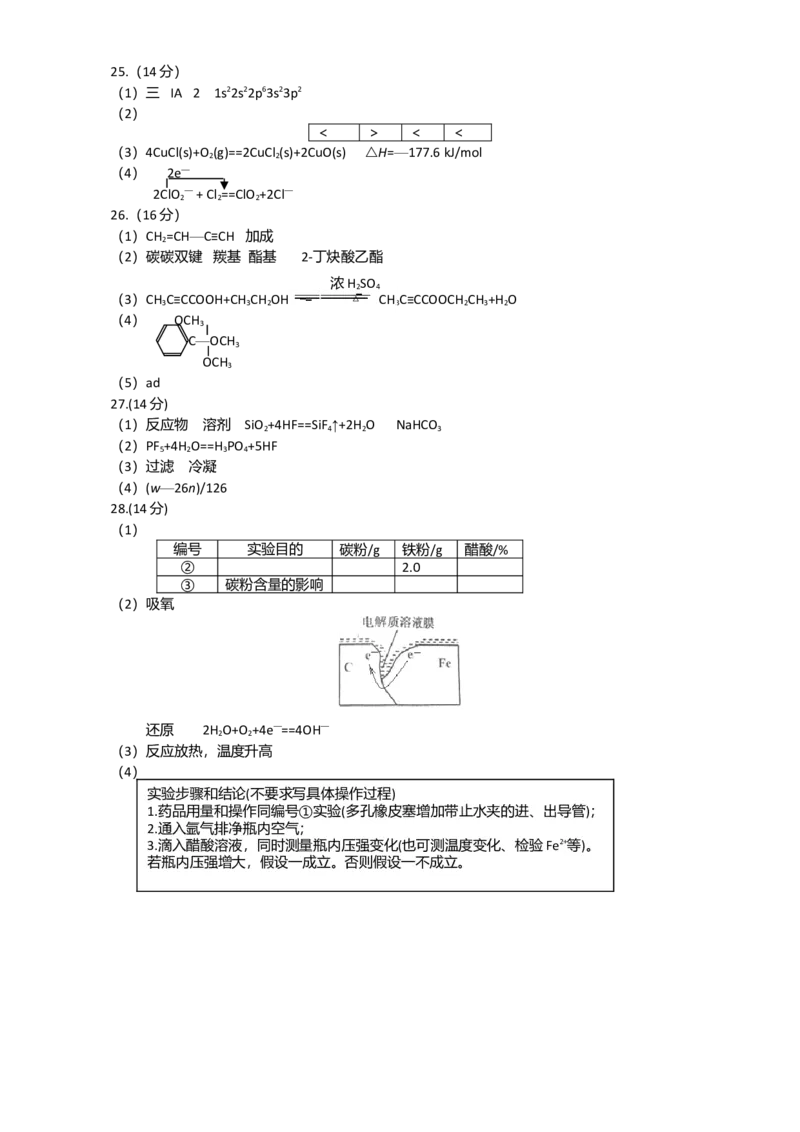
压强明显小于起始压强,其原因是铁发生了_______腐蚀,请在 图
3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了_________(填“氧化”或
“还原”)反应,其电极反应式是_____________________________。
(3)该小组对图2中0~t 时压强变大的原因提出了如下假设,请你完成假设二:
1
假设一:发生析氢腐蚀产生了气体;
假设二:______________________;
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有 H 的方案。请你再设计一个
2
实验方案验证假设一,写出实验步骤和结论。
实验步骤和结论(不要求写具体操作过程)
【答案】(1)
编号 实验目的 碳粉/g 铁粉/g 醋酸/%
② 2.0
③ 碳粉含量的影响
(2)吸氧
还原 2H O+O +4e—==4OH—
2 2
(3)反应放热,温度升高
(4)
实验步骤和结论(不要求写具体操作过程)
1.药品用量和操作同编号①实验(多孔橡皮塞增加带止水夹的进、出导管);
2.通入氩气排净瓶内空气;
3.滴入醋酸溶液,同时测量瓶内压强变化(也可测温度变化、检验Fe2+等)。
若瓶内压强增大,假2设01一4成年立理。否综则化假学设一试不题成第立。Ⅱ卷答案25.(14分)
(1)三 IA 2 1s22s22p63s23p2
(2)
< > < <
(3)4CuCl(s)+O (g)==2CuCl (s)+2CuO(s) △H=—177.6 kJ/mol
2 2
(4) 2e—
2ClO — + Cl ==ClO +2Cl—
2 2 2
26.(16分)
(1)CH =CH—C≡CH 加成
2
(2)碳碳双键 羰基 酯基 2-丁炔酸乙酯
浓H SO
2 4
(3)CH C≡CCOOH+CH CH OH △ CH C≡CCOOCH CH +H O
3 3 2 3 2 3 2
(4) OCH
3
—C—OCH
3
OCH
3
(5)ad
27.(14分)
(1)反应物 溶剂 SiO +4HF==SiF ↑+2H O NaHCO
2 4 2 3
(2)PF +4H O==H PO +5HF
5 2 3 4
(3)过滤 冷凝
(4)(w—26n)/126
28.(14分)
(1)
编号 实验目的 碳粉/g 铁粉/g 醋酸/%
② 2.0
③ 碳粉含量的影响
(2)吸氧
还原 2H O+O +4e—==4OH—
2 2
(3)反应放热,温度升高
(4)
实验步骤和结论(不要求写具体操作过程)
1.药品用量和操作同编号①实验(多孔橡皮塞增加带止水夹的进、出导管);
2.通入氩气排净瓶内空气;
3.滴入醋酸溶液,同时测量瓶内压强变化(也可测温度变化、检验Fe2+等)。
若瓶内压强增大,假设一成立。否则假设一不成立。