文档内容
2023年高考化学试卷(新课标)
一、选择题:本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.(6分)化学在文物的研究和修复中有重要作用。下列说法错误的是( )
A.竹简的成分之一纤维素属于天然高分子
B.龟甲的成分之一羟基磷灰石属于无机物
C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
D.古壁画颜料中所用的铁红,其成分为Fe O
2 3
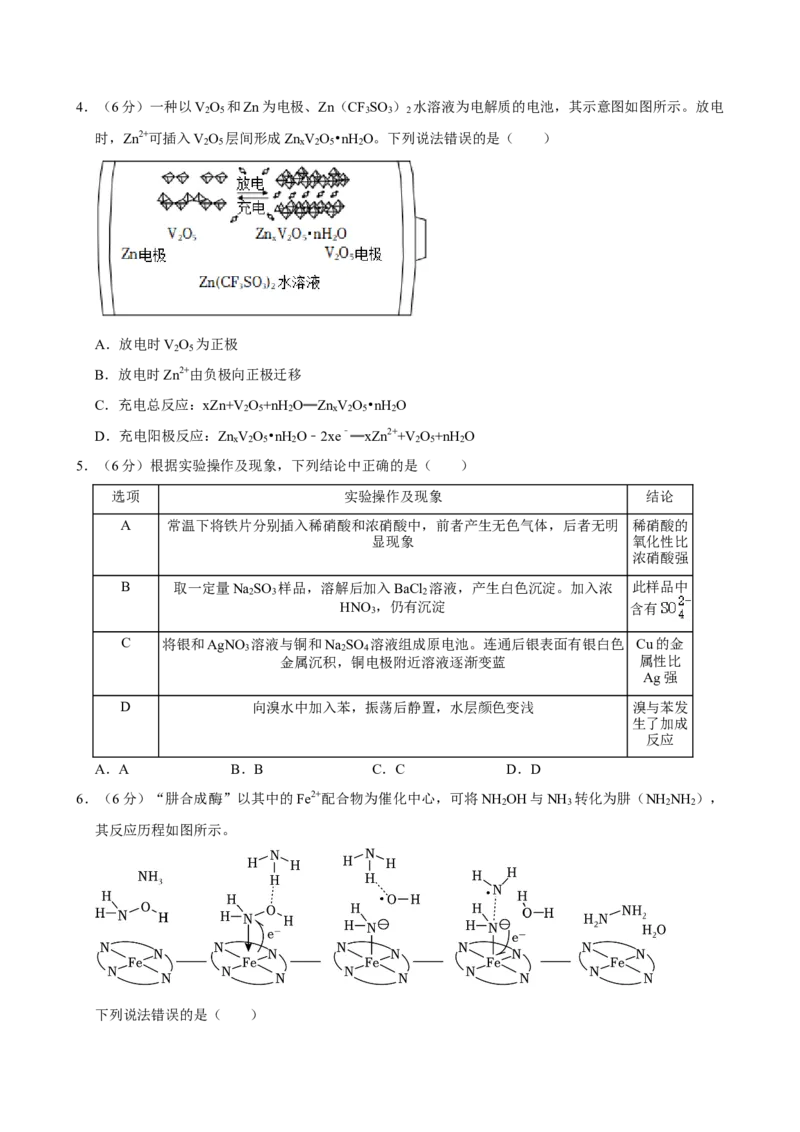
2.(6分)光学性能优良的高分子材料聚碳酸异山梨醇酯可由如图反应制备。
下列说法错误的是( )
A.该高分子材料可降解
B.异山梨醇分子中有3个手性碳
C.反应式中化合物X为甲醇
D.该聚合反应为缩聚反应
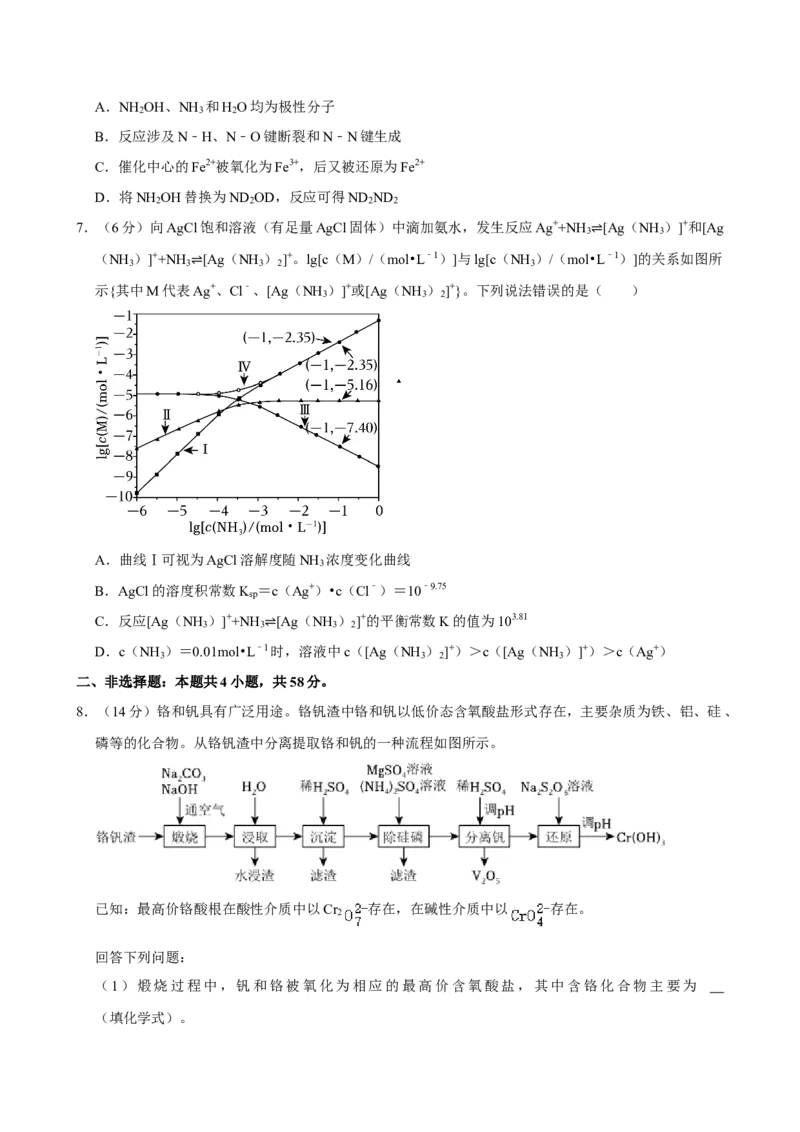
3.(6分)一种可吸附甲醇的材料,其化学式为[C(NH ) ] [B(OCH ) ] Cl,部分晶体结构如图所示,
2 3 4 3 4 3
其中[C(NH ) ]+为平面结构。
2 3
下列说法正确的是( )
A.该晶体中存在N﹣H…O氢键
B.基态原子的第一电离能:C<N<O
C.基态原子未成对电子数:B<C<O<N
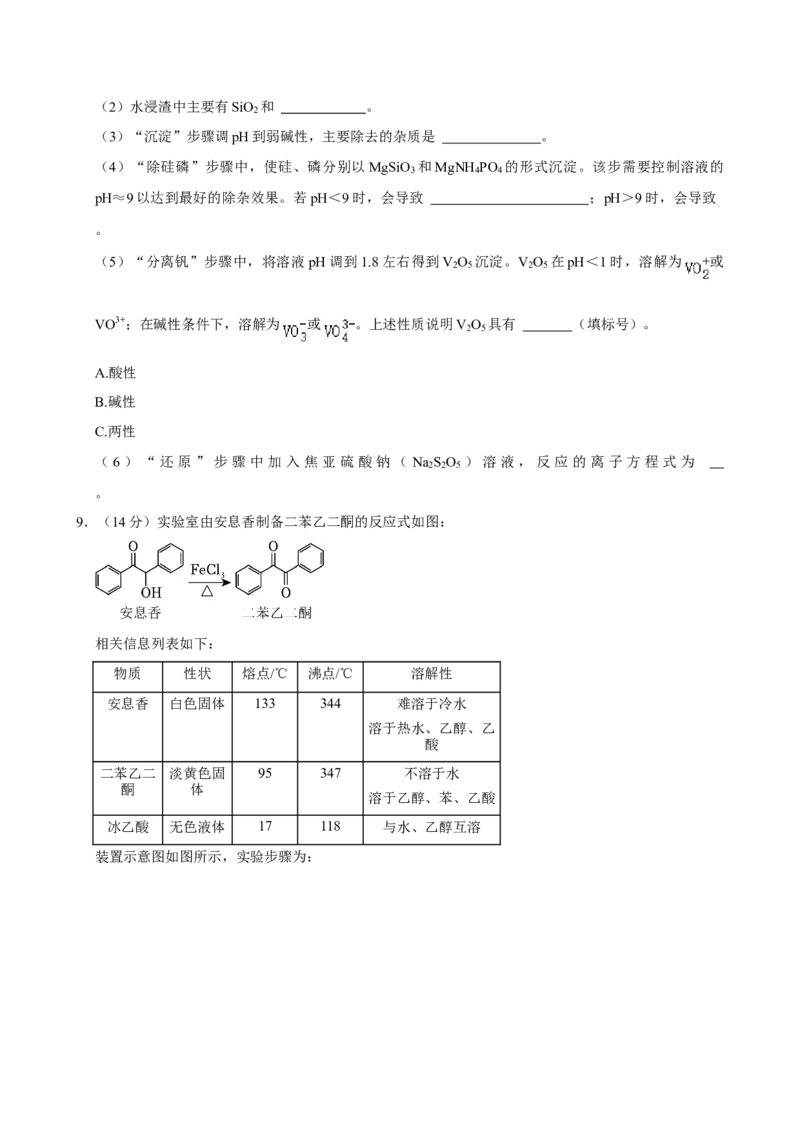
D.晶体中B、N和O原子轨道的杂化类型相同4.(6分)一种以V O 和Zn为电极、Zn(CF SO ) 水溶液为电解质的电池,其示意图如图所示。放电
2 5 3 3 2
时,Zn2+可插入V O 层间形成Zn V O •nH O。下列说法错误的是( )
2 5 x 2 5 2
A.放电时V O 为正极
2 5
B.放电时Zn2+由负极向正极迁移
C.充电总反应:xZn+V O +nH O═Zn V O •nH O
2 5 2 x 2 5 2
D.充电阳极反应:Zn V O •nH O﹣2xe﹣═xZn2++V O +nH O
x 2 5 2 2 5 2
5.(6分)根据实验操作及现象,下列结论中正确的是( )
选项 实验操作及现象 结论
A 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明 稀硝酸的
显现象 氧化性比
浓硝酸强
B 取一定量Na SO 样品,溶解后加入BaCl 溶液,产生白色沉淀。加入浓 此样品中
2 3 2
HNO ,仍有沉淀 含有
3
C 将银和AgNO 溶液与铜和Na SO 溶液组成原电池。连通后银表面有银白色 Cu的金
3 2 4
金属沉积,铜电极附近溶液逐渐变蓝 属性比
Ag强
D 向溴水中加入苯,振荡后静置,水层颜色变浅 溴与苯发
生了加成
反应
A.A B.B C.C D.D
6.(6分)“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH OH与NH 转化为肼(NH NH ),
2 3 2 2
其反应历程如图所示。
下列说法错误的是( )A.NH OH、NH 和H O均为极性分子
2 3 2
B.反应涉及N﹣H、N﹣O键断裂和N﹣N键生成
C.催化中心的Fe2+被氧化为Fe3+,后又被还原为Fe2+
D.将NH OH替换为ND OD,反应可得ND ND
2 2 2 2
7.(6分)向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应Ag++NH [Ag(NH )]+和[Ag
3 3
(NH )]++NH [Ag(NH ) ]+。lg[c(M)/(mol•L﹣1)]与lg[c(NH )/(mol•⇌L﹣1)]的关系如图所
3 3 3 2 3
示{其中M代表⇌Ag+、Cl﹣、[Ag(NH )]+或[Ag(NH ) ]+}。下列说法错误的是( )
3 3 2
A.曲线Ⅰ可视为AgCl溶解度随NH 浓度变化曲线
3
B.AgCl的溶度积常数K =c(Ag+)•c(Cl﹣)=10﹣9.75
sp
C.反应[Ag(NH )]++NH [Ag(NH ) ]+的平衡常数K的值为103.81
3 3 3 2
D.c(NH )=0.01mol•L﹣1⇌时,溶液中c([Ag(NH ) ]+)>c([Ag(NH )]+)>c(Ag+)
3 3 2 3
二、非选择题:本题共4小题,共58分。
8.(14分)铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅、
磷等的化合物。从铬钒渣中分离提取铬和钒的一种流程如图所示。
已知:最高价铬酸根在酸性介质中以Cr 存在,在碱性介质中以 存在。
2
回答下列问题:
(1)煅烧过程中,钒和铬被氧化为相应的最高价含氧酸盐,其中含铬化合物主要为
(填化学式)。(2)水浸渣中主要有SiO 和 。
2
(3)“沉淀”步骤调pH到弱碱性,主要除去的杂质是 。
(4)“除硅磷”步骤中,使硅、磷分别以MgSiO 和MgNH PO 的形式沉淀。该步需要控制溶液的
3 4 4
pH≈9以达到最好的除杂效果。若pH<9时,会导致 ;pH>9时,会导致
。
(5)“分离钒”步骤中,将溶液pH调到1.8左右得到V O 沉淀。V O 在pH<1时,溶解为 或
2 5 2 5
VO3+;在碱性条件下,溶解为 或 。上述性质说明V O 具有 (填标号)。
2 5
A.酸性
B.碱性
C.两性
(6)“还原”步骤中加入焦亚硫酸钠( Na S O )溶液,反应的离子方程式为
2 2 5
。
9.(14分)实验室由安息香制备二苯乙二酮的反应式如图:
相关信息列表如下:
物质 性状 熔点/℃ 沸点/℃ 溶解性
安息香 白色固体 133 344 难溶于冷水
溶于热水、乙醇、乙
酸
二苯乙二 淡黄色固 95 347 不溶于水
酮 体
溶于乙醇、苯、乙酸
冰乙酸 无色液体 17 118 与水、乙醇互溶
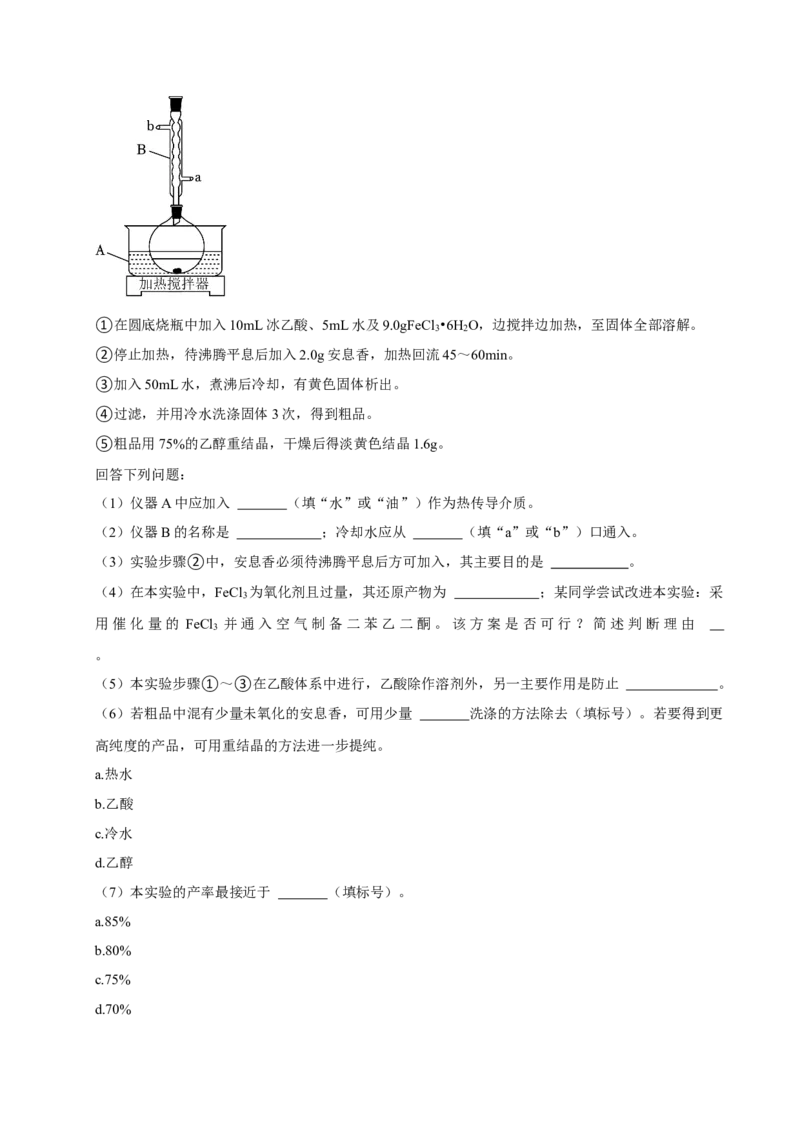
装置示意图如图所示,实验步骤为:①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0gFeCl •6H O,边搅拌边加热,至固体全部溶解。
3 2
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:
(1)仪器A中应加入 (填“水”或“油”)作为热传导介质。
(2)仪器B的名称是 ;冷却水应从 (填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是 。
(4)在本实验中,FeCl 为氧化剂且过量,其还原产物为 ;某同学尝试改进本实验:采
3
用催化量的 FeCl 并通入空气制备二苯乙二酮。该方案是否可行?简述判断理由
3
。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是防止 。
(6)若粗品中混有少量未氧化的安息香,可用少量 洗涤的方法除去(填标号)。若要得到更
高纯度的产品,可用重结晶的方法进一步提纯。
a.热水
b.乙酸
c.冷水
d.乙醇
(7)本实验的产率最接近于 (填标号)。
a.85%
b.80%
c.75%
d.70%10.(15分)氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
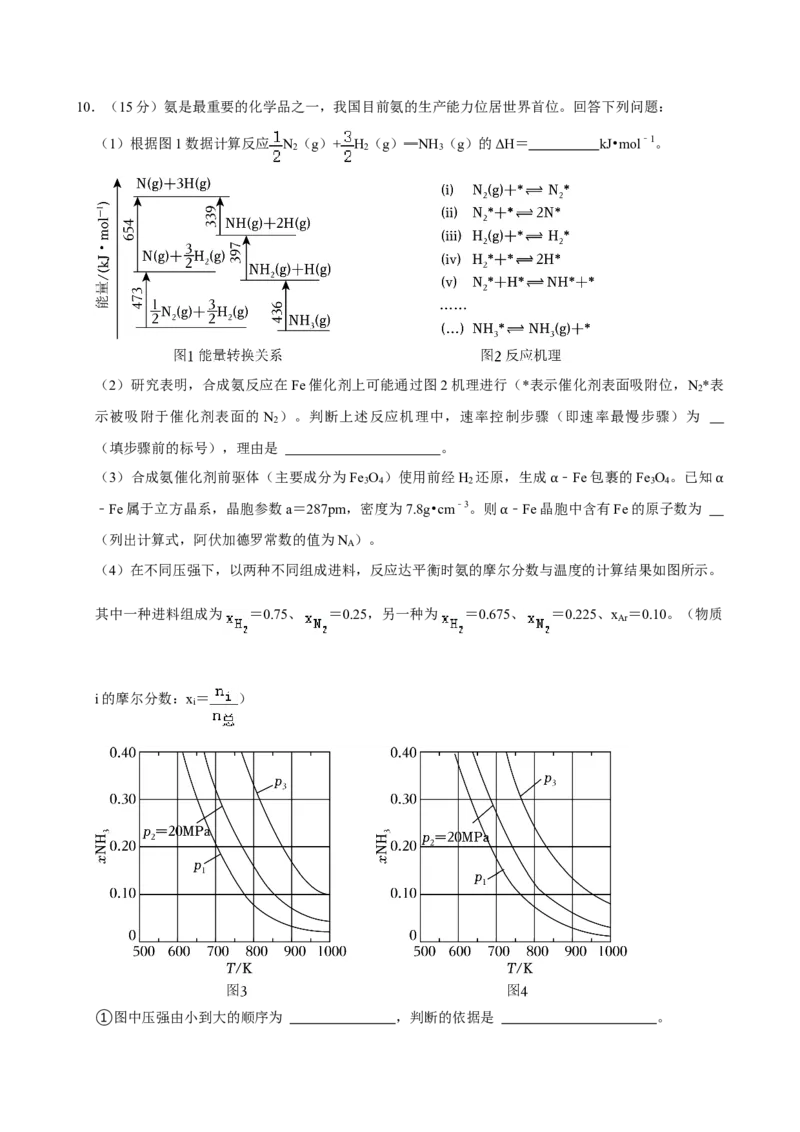
(1)根据图1数据计算反应 N (g)+ H (g)═NH (g)的ΔH= kJ•mol﹣1。
2 2 3
(2)研究表明,合成氨反应在Fe催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,N *表
2
示被吸附于催化剂表面的 N )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
2
(填步骤前的标号),理由是 。
(3)合成氨催化剂前驱体(主要成分为Fe O )使用前经H 还原,生成 ﹣Fe包裹的Fe O 。已知
3 4 2 3 4
﹣Fe属于立方晶系,晶胞参数a=287pm,密度为7.8g•cm﹣3。则 ﹣Fe晶α胞中含有Fe的原子数为 α
(列出计算式,阿伏加德罗常数的值为N )。 α
A
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如图所示。
其中一种进料组成为 =0.75、 =0.25,另一种为 =0.675、 =0.225、x =0.10。(物质
Ar
i的摩尔分数:x= )
i
①图中压强由小到大的顺序为 ,判断的依据是 。②进料组成中含有惰性气体Ar的图是 。
③图3中,当p =20MPa、 =0.20时,氮的转化率 = 。该温度时,反应 N
2 2
α
(g)+ H (g) NH (g)的平衡常数K = MPa﹣1(化为最简式)。
2 3 p
⇌
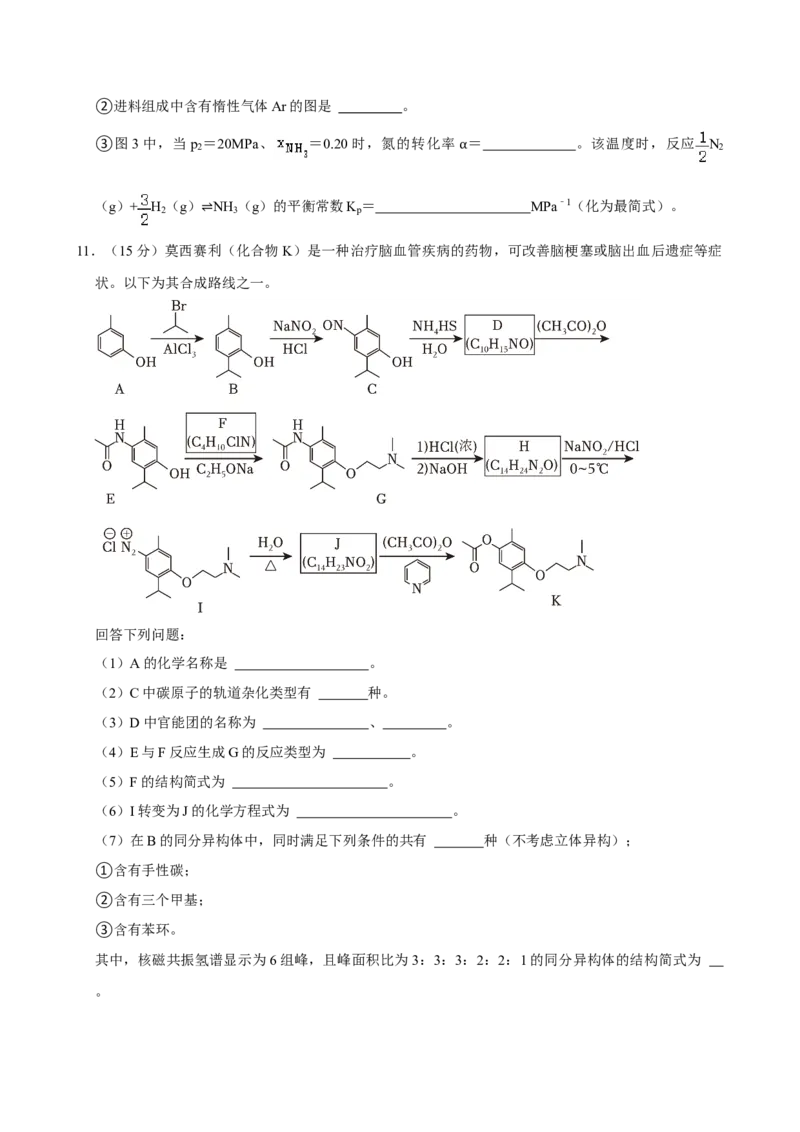
11.(15分)莫西赛利(化合物K)是一种治疗脑血管疾病的药物,可改善脑梗塞或脑出血后遗症等症
状。以下为其合成路线之一。
回答下列问题:
(1)A的化学名称是 。
(2)C中碳原子的轨道杂化类型有 种。
(3)D中官能团的名称为 、 。
(4)E与F反应生成G的反应类型为 。
(5)F的结构简式为 。
(6)I转变为J的化学方程式为 。
(7)在B的同分异构体中,同时满足下列条件的共有 种(不考虑立体异构);
①含有手性碳;
②含有三个甲基;
③含有苯环。
其中,核磁共振氢谱显示为6组峰,且峰面积比为3:3:3:2:2:1的同分异构体的结构简式为
。