文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
专题 20 工艺流程图题
考点01 物质制备类
考点02 废物的处理和回收
考点03 核心反应分析和流程评价
考点01 物质制备类
1.(2025·黑龙江大庆·中考真题)工业上用重晶石(主要成分为硫酸钡)制备碳酸钡的工艺流程如图所示。
下列说法错误的是
A.为了使焙烧更充分可将重晶石粉碎
B.反应1的化学方程式为BaSO+4C BaS+4X↑,则物质X的化学式为CO
4 2
C.操作1、操作2均用到的玻璃仪器有漏斗、烧杯、玻璃棒
D.反应2的基本反应类型为复分解反应
2.(2025·贵州·中考真题)碳酸锂( )是制备新能源汽车电池的重要原料。利用锂辉石(成分为 、
、 )制备 的流程如下:
已知 难溶于水,不与稀 反应; 。下列说法不正确的是
A.操作1、2是过滤,滤渣1是
B.滤液1中的溶质含有 、 、
C.加热分解 的温度比 低
D.若把 溶液换成 溶液,获得的产品更多
3.(2025·四川成都·中考真题)成都盛产蛇纹石,利用蛇纹石生产氢氧化镁的工艺如图。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【资料信息】
1.蛇纹石的主要成分为MgO和 ,含少量 、 等。
2. 难溶于水,不与稀硫酸反应。
3.部分金属离子形成氢氧化物沉淀的pH范围如下表。
金属离子
开始沉淀的pH 2.3 3.5 9.4
沉淀完全的pH 3.2 4.6 12.4
(1)“粉碎”的目的是 。
(2)“酸浸”后,滤液中阳离子有 和 (填符号),滤渣1的主要成分是 。
(3)“碱洗”时,适宜的pH范围为 。
(4)“沉镁”的化学方程式为 。
(5)“洗涤”时,证明氢氧化镁已洗净的方法是 。
4.(2025·河北·中考真题)高纯氧化钙是一种重要的化工原料。如图所示为小组同学以某工厂废渣(主要
成分为 ,含少量 和 )为原料,在实验室制备高纯氧化钙的实验方案。
请回答下列问题:
(1)氧化钙的化学式为 。
(2)将废渣粉碎为细小颗粒的目的是 。
(3)步骤②中过滤时玻璃棒的作用是 。
(4)步骤③中反应的化学方程式为 (写一个即可)。
(5)以相同质量的废渣为原料,仅将步骤②中的石灰水换为氢氧化钠溶液,会使产品的产量
(填“提高”“不变”或“降低”)。
5.(2025·四川泸州·中考真题)碘单质 微溶于水,广泛用于医药染料等方面。 的一种制备方法如下
图所示。回答相关问题:
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)“沉碘富集”反应的化学方程式为 ,该反应的类型为 。
(2)“置换1”沉淀与铁粉反应的化学方程式为 ,反应后分离出“Ag和Fe”的操作名称是 ,
若用化学方法进一步提纯,得到纯净的Ag所需试剂是 (填符号)。
(3)“置换2”所剩“溶液2”中,含有的阴离了主要是
6.(2025·广东深圳·中考真题)铜具有重要战略价值。古代以黄铜矿(其主要成分为 )为原料,运用
火法炼铜工艺得到铜。现代在火法炼铜工艺的基础上发展出闪速炼铜工艺。对比二者原理如图:
(1)“闪速炼铜”速率远快于“火法炼铜”,由此可知, 炼铜需要将黄铜矿颗粒粉末研磨得
更细。
(2)火法炼铜中,持续向 中鼓入空气并维持高温状态,这说明反应是 (吸收/放出)热量,
反应的化学方程式 。
(3)反应生成的 可用于工业制造一种酸,请写出这种酸 (化学式); 可被石灰乳吸收,
请说明其吸收效果优于石灰水的原因: 。
(4)火法炼铜中,炉渣 是由2种物质化合生成的,请写出沙子提供的物质 (填化学
式)。
(5)对比火法炼铜,闪速炼铜的优势有 (填序号)。
a.高温更少,节约能源 b.原料更少,节省成本 c.无污染
7.(2025·四川广元·中考真题)硫酸亚铁广泛应用于医学、农业等领域。某工厂利用菱铁矿【主要成分是
碳酸亚铁( ),还含有少量的氧化铁( )和二氧化硅( )】为原料制备硫酸亚铁的工艺流程如图
所示。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)上述流程中,粉碎和 都能加快反应速率。
(2)反应器Ⅰ中碳酸亚铁与稀硫酸发生复分解反应的化学方程式为 。
(3)该工厂配制质量分数为19.6%的稀硫酸10吨,需质量分数为98%的浓硫酸 吨。
(4)溶液甲中的溶质有 、 (填化学式)和 。
8.(2025·江苏苏州·中考真题)以闪锌矿[主要成分 ,少量 、 (硫化镉)]为原料制备硫酸锌
的流程如下:
(1)“焙烧”时,金属硫化物(ZnS、FeS和CdS)与氧气反应均转化为金属氧化物和 。写出 与
高温反应的化学方程式: 。
(2)①“酸浸”时发生反应的基本类型为 。
②“酸浸”所得滤液中阳离子有 、 、 和 (填离子符号)。
(3)“除铁”时发生反应:
反应Ⅰ
反应Ⅱ
①除铁所得“滤渣2”的用途有 (写一种)。
②铁元素化合价在反应Ⅰ和反应Ⅱ前后的变化情况分别为 (填字母)。
A.升高降低 B.升高不变 C.不变降低 D.降低升高
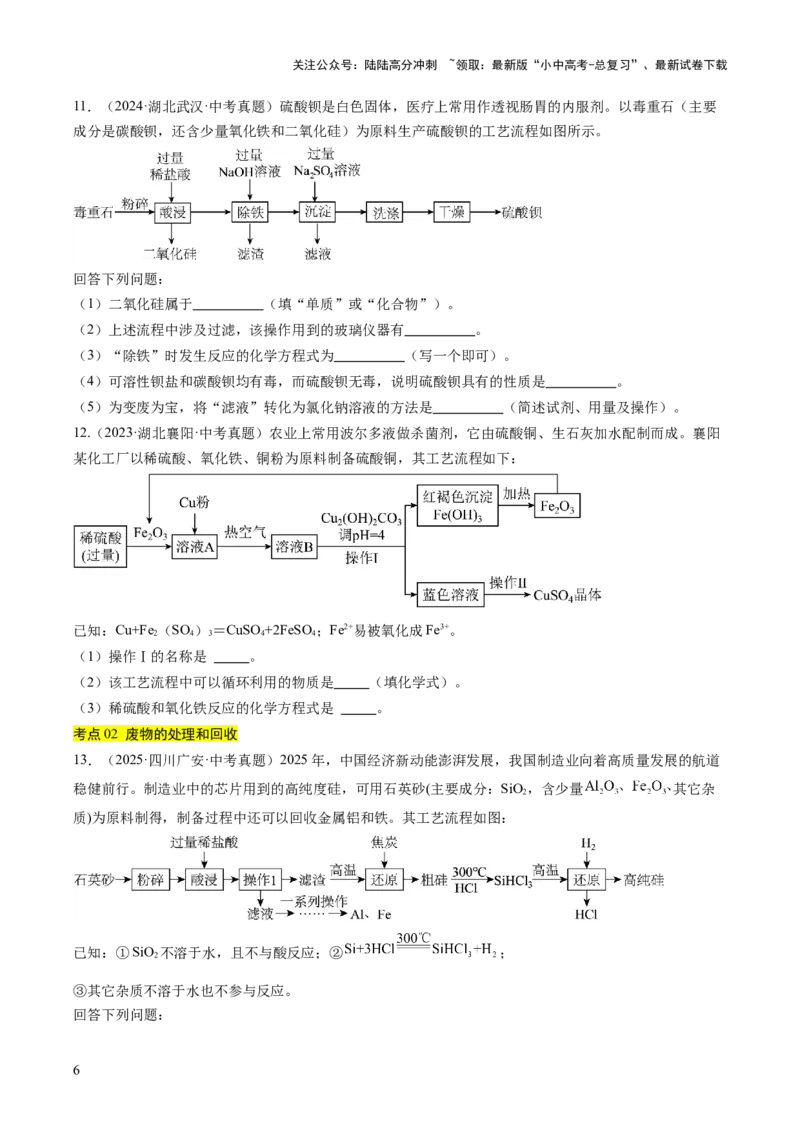
(4)“除镉过滤”前需先测定溶液中 浓度,计算所需锌粉质量的理论值 。如图所示的
是实际参加反应锌的质量与理论值之比 分别为1.2和1.0时,除镉率随时间的变化。
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①金属活动性: (填“>”或“<”)
②除镉率接近100%时, 的原因是 。
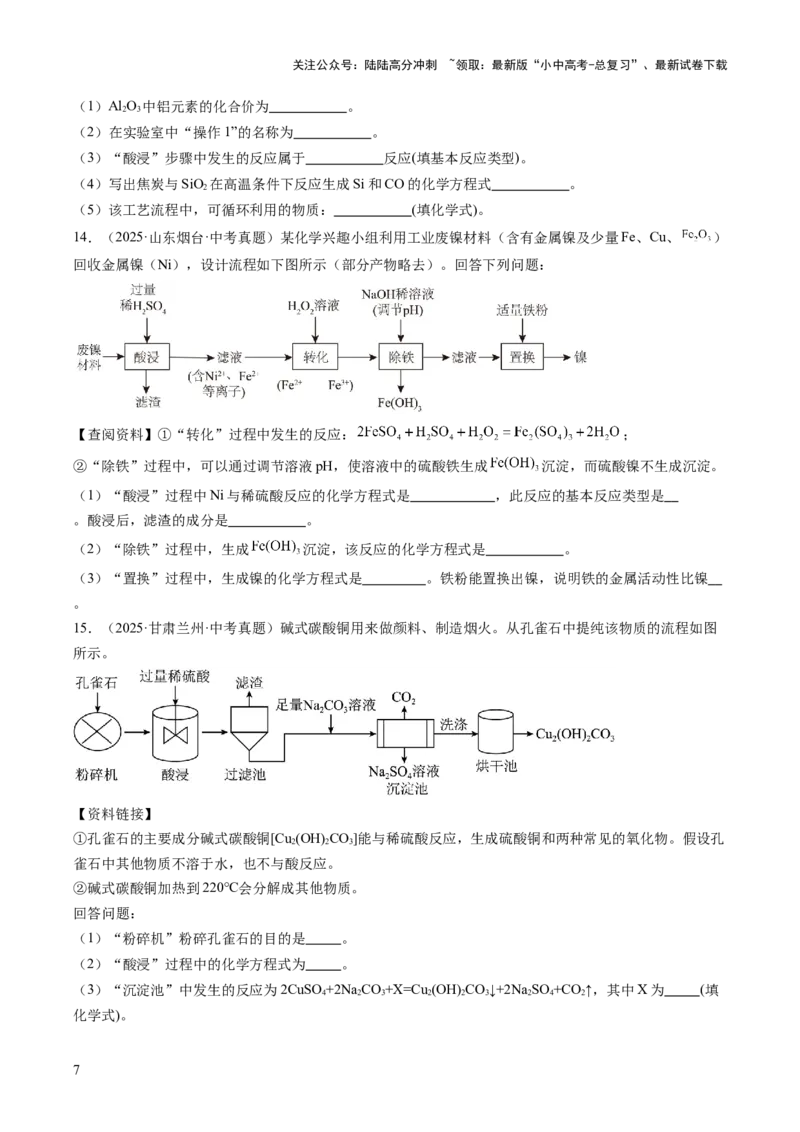
9.(2025·四川遂宁·中考真题)氧化铁红(Fe O)是常见的含铁颜料。工业上可利用硫酸亚铁、氨水、
2 3
空气等物质制取氧化铁红,主要流程如图所示:
已知:“合成”时发生的主要反应为4FeSO +O +6H O 4FeOOH↓+4H SO ;氨水溶液呈碱性。
4 2 2 2 4
(1)FeSO 中铁元素的化合价为 。
4
(2)“操作a”的名称是 。
(3)“合成”过程中不断加入氨水,溶液的pH仍然保持基本不变的原因是 。
(4)若向硫酸亚铁溶液中加入一定量的锌和铜,充分反应后过滤,得到无色滤液和滤渣,则滤渣中一定
有的固体是 。
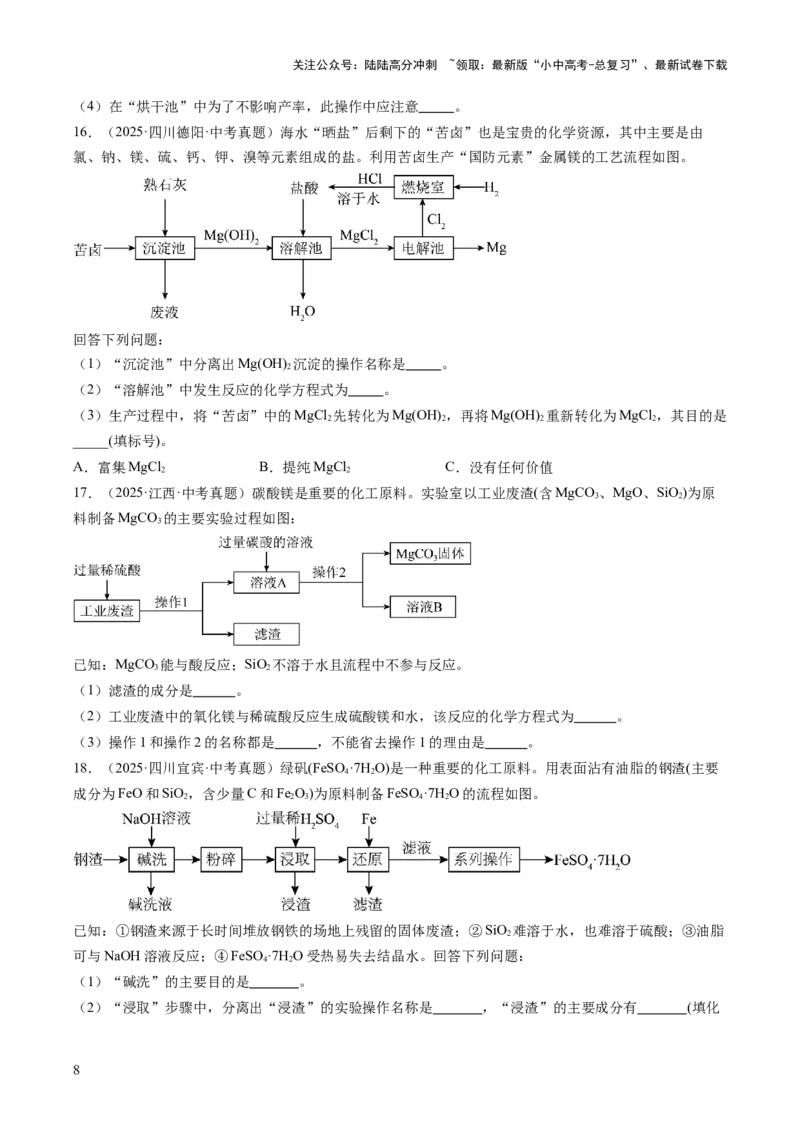
10.(2024·新疆·中考真题)硫酸亚铁广泛应用于医学、农业等领域,可利用菱铁矿进行制备。菱铁矿的
主要成分是碳酸亚铁( ),还含有少量的二氧化硅( )和氧化铁(Fe O)。以菱铁矿为原料制备硫酸
2 3
亚铁的工艺流程如图所示。
回答下列问题:
(1)硫酸亚铁可为人体补充铁元素,在医学上可用于治疗 (填病症名称)。
(2)菱铁矿属于 (填“纯净物”或“混合物”)。
(3)Fe O 中铁元素的化合价为 ,其中铁元素与氧元素的质量比为 。
2 3
(4)由此流程可推知 的性质有______(填字母)。
A.难溶于水 B.化学性质很活泼 C.不能与稀硫酸反应
(5)溶液甲中,属于盐类的两种溶质为 (填化学式)。
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
11.(2024·湖北武汉·中考真题)硫酸钡是白色固体,医疗上常用作透视肠胃的内服剂。以毒重石(主要
成分是碳酸钡,还含少量氧化铁和二氧化硅)为原料生产硫酸钡的工艺流程如图所示。
回答下列问题:
(1)二氧化硅属于 (填“单质”或“化合物”)。
(2)上述流程中涉及过滤,该操作用到的玻璃仪器有 。
(3)“除铁”时发生反应的化学方程式为 (写一个即可)。
(4)可溶性钡盐和碳酸钡均有毒,而硫酸钡无毒,说明硫酸钡具有的性质是 。
(5)为变废为宝,将“滤液”转化为氯化钠溶液的方法是 (简述试剂、用量及操作)。
12.(2023·湖北襄阳·中考真题)农业上常用波尔多液做杀菌剂,它由硫酸铜、生石灰加水配制而成。襄阳
某化工厂以稀硫酸、氧化铁、铜粉为原料制备硫酸铜,其工艺流程如下:
已知:Cu+Fe (SO )=CuSO +2FeSO;Fe2+易被氧化成Fe3+。
2 4 3 4 4
(1)操作Ⅰ的名称是 。
(2)该工艺流程中可以循环利用的物质是 (填化学式)。
(3)稀硫酸和氧化铁反应的化学方程式是 。
考点02 废物的处理和回收
13.(2025·四川广安·中考真题)2025年,中国经济新动能澎湃发展,我国制造业向着高质量发展的航道
稳健前行。制造业中的芯片用到的高纯度硅,可用石英砂(主要成分:SiO,含少量 其它杂
2
质)为原料制得,制备过程中还可以回收金属铝和铁。其工艺流程如图:
已知:①SiO 不溶于水,且不与酸反应;② ;
2
③其它杂质不溶于水也不参与反应。
回答下列问题:
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)Al O 中铝元素的化合价为 。
2 3
(2)在实验室中“操作1”的名称为 。
(3)“酸浸”步骤中发生的反应属于 反应(填基本反应类型)。
(4)写出焦炭与SiO 在高温条件下反应生成Si和CO的化学方程式 。
2
(5)该工艺流程中,可循环利用的物质: (填化学式)。
14.(2025·山东烟台·中考真题)某化学兴趣小组利用工业废镍材料(含有金属镍及少量Fe、Cu、 )
回收金属镍(Ni),设计流程如下图所示(部分产物略去)。回答下列问题:
【查阅资料】①“转化”过程中发生的反应: ;
②“除铁”过程中,可以通过调节溶液pH,使溶液中的硫酸铁生成 沉淀,而硫酸镍不生成沉淀。
(1)“酸浸”过程中Ni与稀硫酸反应的化学方程式是 ,此反应的基本反应类型是
。酸浸后,滤渣的成分是 。
(2)“除铁”过程中,生成 沉淀,该反应的化学方程式是 。
(3)“置换”过程中,生成镍的化学方程式是 。铁粉能置换出镍,说明铁的金属活动性比镍
。
15.(2025·甘肃兰州·中考真题)碱式碳酸铜用来做颜料、制造烟火。从孔雀石中提纯该物质的流程如图
所示。
【资料链接】
①孔雀石的主要成分碱式碳酸铜[Cu (OH) CO]能与稀硫酸反应,生成硫酸铜和两种常见的氧化物。假设孔
2 2 3
雀石中其他物质不溶于水,也不与酸反应。
②碱式碳酸铜加热到220℃会分解成其他物质。
回答问题:
(1)“粉碎机”粉碎孔雀石的目的是 。
(2)“酸浸”过程中的化学方程式为 。
(3)“沉淀池”中发生的反应为2CuSO +2Na CO+X=Cu (OH) CO↓+2Na SO +CO ↑,其中X为 (填
4 2 3 2 2 3 2 4 2
化学式)。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)在“烘干池”中为了不影响产率,此操作中应注意 。
16.(2025·四川德阳·中考真题)海水“晒盐”后剩下的“苦卤”也是宝贵的化学资源,其中主要是由
氯、钠、镁、硫、钙、钾、溴等元素组成的盐。利用苦卤生产“国防元素”金属镁的工艺流程如图。
回答下列问题:
(1)“沉淀池”中分离出Mg(OH) 沉淀的操作名称是 。
2
(2)“溶解池”中发生反应的化学方程式为 。
(3)生产过程中,将“苦卤”中的MgCl 先转化为Mg(OH) ,再将Mg(OH) 重新转化为MgCl ,其目的是
2 2 2 2
_____(填标号)。
A.富集MgCl B.提纯MgCl C.没有任何价值
2 2
17.(2025·江西·中考真题)碳酸镁是重要的化工原料。实验室以工业废渣(含MgCO 、MgO、SiO)为原
3 2
料制备MgCO 的主要实验过程如图:
3
已知:MgCO 能与酸反应;SiO 不溶于水且流程中不参与反应。
3 2
(1)滤渣的成分是 。
(2)工业废渣中的氧化镁与稀硫酸反应生成硫酸镁和水,该反应的化学方程式为 。
(3)操作1和操作2的名称都是 ,不能省去操作1的理由是 。
18.(2025·四川宜宾·中考真题)绿矾(FeSO ·7H O)是一种重要的化工原料。用表面沾有油脂的钢渣(主要
4 2
成分为FeO和SiO,含少量C和Fe O)为原料制备FeSO ·7H O的流程如图。
2 2 3 4 2
已知:①钢渣来源于长时间堆放钢铁的场地上残留的固体废渣;②SiO 难溶于水,也难溶于硫酸;③油脂
2
可与NaOH溶液反应;④FeSO ·7H O受热易失去结晶水。回答下列问题:
4 2
(1)“碱洗”的主要目的是 。
(2)“浸取”步骤中,分离出“浸渣”的实验操作名称是 ,“浸渣”的主要成分有 (填化
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
学式)。
(3)若“滤液”中有FeSO 而没有Fe (SO ),则“还原”步骤发生反应的化学方程式是 、
4 2 4 3
。
(4)“系列操作”过程涉及干燥。干燥时需控制温度低于30℃,原因是 。
(5)用10.64t含铁量50%的钢渣,并在“还原”步骤中加入0.3t铁粉,最终得到27.8tFeSO ·7H O固体,
4 2
则“还原”步骤得到的“滤渣”为 t。(FeSO ·7H O的相对分子质量为278)
4 2
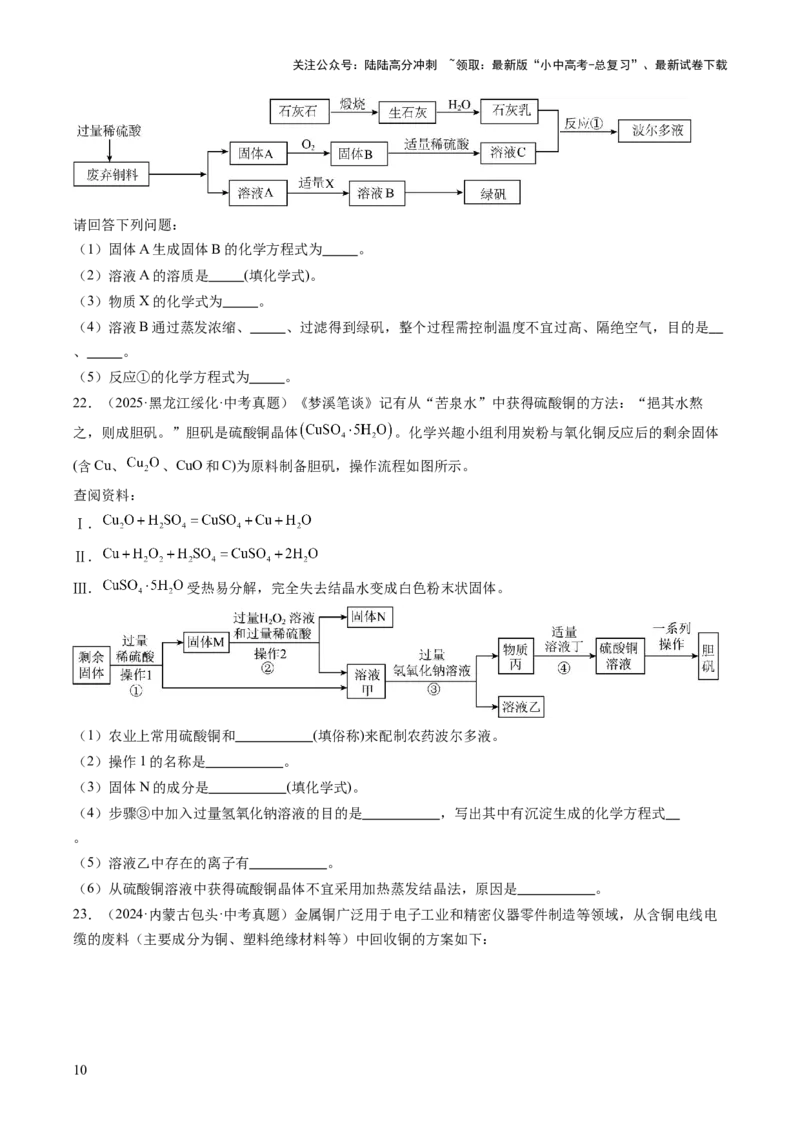
19.(2025·广西·中考真题)废旧电池的回收利用可有效避免环境污染和资源浪费。从废锌镍电池负极片
(主要成分为ZnO、Zn、铜网等)中回收ZnO的一种流程如图所示。
回答下列问题:
(1)“酸溶”前,将负极片变成固体粉末的目的是 。
(2)铜块能制成铜网是利用了铜的 (填“延展性”或“导热性”)。
(3)将“酸洗”和“酸溶”后的溶液混合的目的是 。
(4)“沉锌”时主要发生反应的化学方程式是NaCO+ZnCl =ZnCO ↓+2NaCl,该反应属于
2 3 2 3
___________(填字母序号)。
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(5)若过滤后未洗涤沉淀,沉淀表面会附着杂质,杂质的主要成分是 。
(6)铜的金属活动性比锌的 (填“强”或“弱”),结合流程说明依据: 。
20.(2025·云南·中考真题)现代绘画的红色颜料已很少使用赭石,而是通过化学方法制备) 。例如
可用废铁丝(主要含铁和少量氧化铁,其余杂质不参与反应)制得,其工艺流程如图所示。
(1)“酸浸”过程中,可加快化学反应速率的方法有 (任填一种)。
(2)“酸浸”过程中,加入过量稀盐酸的目的是 。
(3)Fe(OH) 高温焙烧得到两种氧化物,化学方程式为 。
3
(4)流程中的两次过滤均不能省略,其中“过滤1”不能省略的原因是 。
21.(2025·黑龙江大庆·中考真题)“波尔多液”具有杀菌作用,常作为农药使用。某化工厂利用废弃铜
料(只含铜和铁)和石灰石制备“波尔多液”,同时得到副产品绿矾(FeSO ·7H O),工艺流程如图所示(部分
4 2
反应条件和产物已略去)。
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请回答下列问题:
(1)固体A生成固体B的化学方程式为 。
(2)溶液A的溶质是 (填化学式)。
(3)物质X的化学式为 。
(4)溶液B通过蒸发浓缩、 、过滤得到绿矾,整个过程需控制温度不宜过高、隔绝空气,目的是
、 。
(5)反应①的化学方程式为 。
22.(2025·黑龙江绥化·中考真题)《梦溪笔谈》记有从“苦泉水”中获得硫酸铜的方法:“挹其水熬
之,则成胆矾。”胆矾是硫酸铜晶体 。化学兴趣小组利用炭粉与氧化铜反应后的剩余固体
(含Cu、 、CuO和C)为原料制备胆矾,操作流程如图所示。
查阅资料:
Ⅰ.
Ⅱ.
Ⅲ. 受热易分解,完全失去结晶水变成白色粉末状固体。
(1)农业上常用硫酸铜和 (填俗称)来配制农药波尔多液。
(2)操作1的名称是 。
(3)固体N的成分是 (填化学式)。
(4)步骤③中加入过量氢氧化钠溶液的目的是 ,写出其中有沉淀生成的化学方程式
。
(5)溶液乙中存在的离子有 。
(6)从硫酸铜溶液中获得硫酸铜晶体不宜采用加热蒸发结晶法,原因是 。
23.(2024·内蒙古包头·中考真题)金属铜广泛用于电子工业和精密仪器零件制造等领域,从含铜电线电
缆的废料(主要成分为铜、塑料绝缘材料等)中回收铜的方案如下:
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
回答下列问题:
(1)浅绿色溶液中的溶质是 (写化学式)。
(2)黑色固体与稀硫酸反应的化学方程式为 。
(3)写出从 和 的混合物中得到 的一种方法 。
(4)上述方案中可能造成空气污染的原因是 。
24.(2023·四川绵阳·中考真题)某油脂厂废弃的催化剂含金属Ni、Al、Fe及其氧化物。采用如下工艺流程
回收其中的镍制备硫酸镍晶体:
回答下列问题:
(1)滤饼是 (填“纯净物”或“混合物”); 的名称为偏铝酸钠,它所属物质类别是
。
(2)步骤③中 的作用是将 转化为 。
(3)步骤④生成 的化学方程式为 ,所属基本反应类型为 。
(4)步骤⑤需要进行的操作为:蒸发浓缩、冷却结晶、 、洗涤。所得硫酸镍晶体是含结晶水
的化合物,化学式为 ,其中结晶水的质量分数是 (计算结果精确到0.1%)。
(5)已知铁能与硫酸镍溶液发生置换反应,则Ni、Al、Fe三种金属在溶液中的活动性由强到弱的顺序为
。
考点03 核心反应分析和流程评价
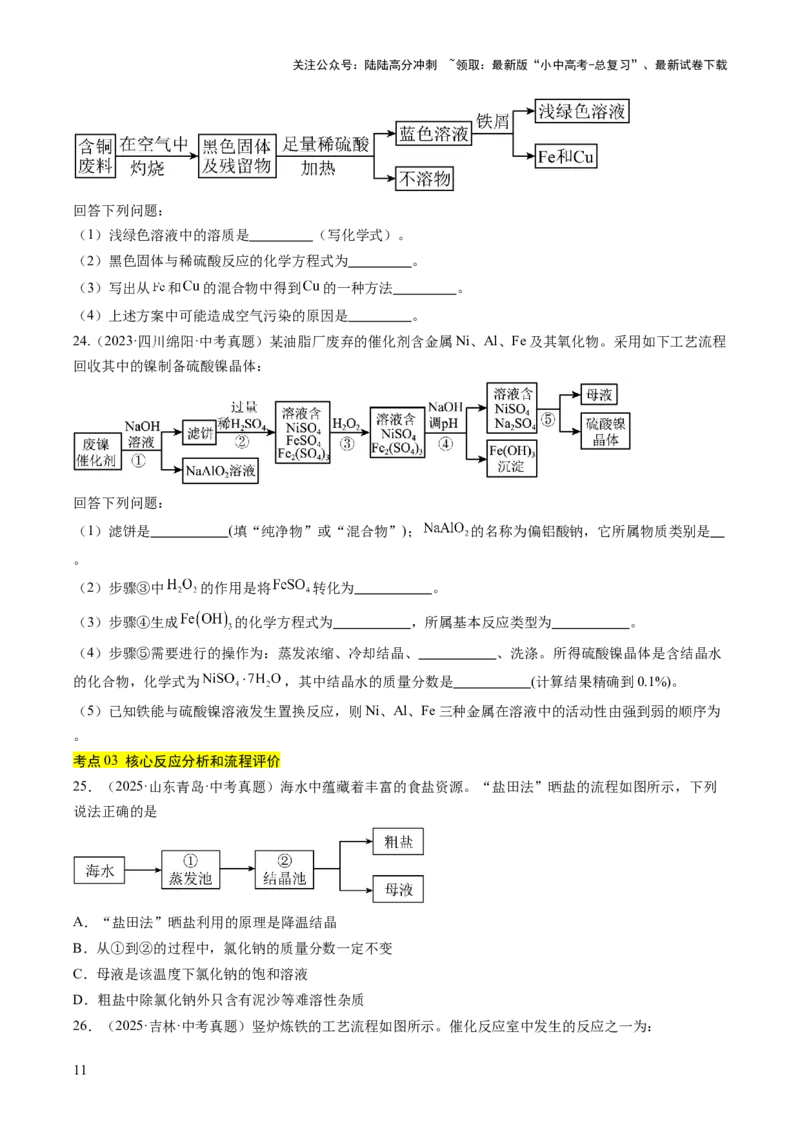
25.(2025·山东青岛·中考真题)海水中蕴藏着丰富的食盐资源。“盐田法”晒盐的流程如图所示,下列
说法正确的是
A.“盐田法”晒盐利用的原理是降温结晶
B.从①到②的过程中,氯化钠的质量分数一定不变
C.母液是该温度下氯化钠的饱和溶液
D.粗盐中除氯化钠外只含有泥沙等难溶性杂质
26.(2025·吉林·中考真题)竖炉炼铁的工艺流程如图所示。催化反应室中发生的反应之一为:
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
。下列分析正确的是
A.赤铁矿石粉碎后可以增加铁元素的含量
B.原料是赤铁矿石、天然气、高温尾气
C.合成气中X的化学式为
D.赤铁矿石和天然气的主要成分都属于化合物
30.(2025·江苏连云港·中考真题)工业上生产CaCl ·2H O的主要流程示意图如题图所示。下列说法正确
2 2
的是
A.石灰石的主要成分是Ca(OH)
2
B.粉碎可以增大反应物间的接触面积
C.反应器中加入的稀盐酸可用稀硫酸代替
D.流程中用于分离提纯的设备有搅拌器和过滤器
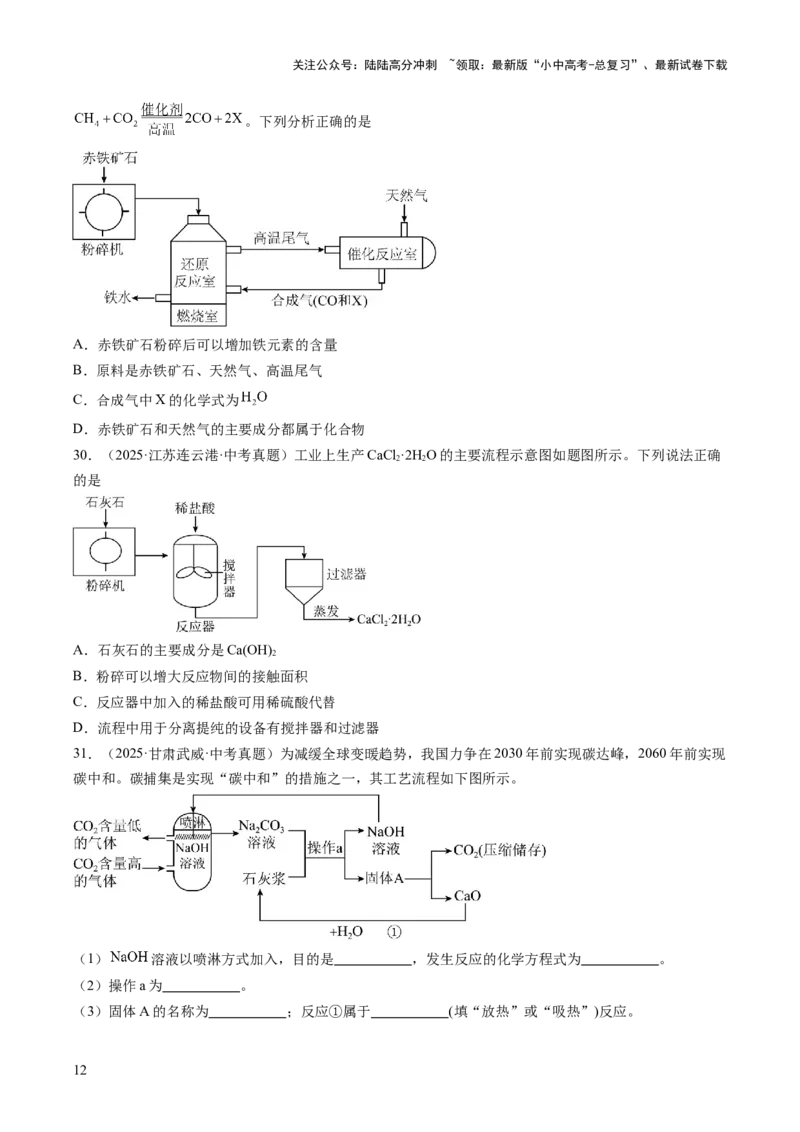
31.(2025·甘肃武威·中考真题)为减缓全球变暖趋势,我国力争在2030年前实现碳达峰,2060年前实现
碳中和。碳捕集是实现“碳中和”的措施之一,其工艺流程如下图所示。
(1) 溶液以喷淋方式加入,目的是 ,发生反应的化学方程式为 。
(2)操作a为 。
(3)固体A的名称为 ;反应①属于 (填“放热”或“吸热”)反应。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)该流程中除了 外,还可循环利用的物质是 。
(5)践行低碳行动的有效措施有 (写一种即可)。
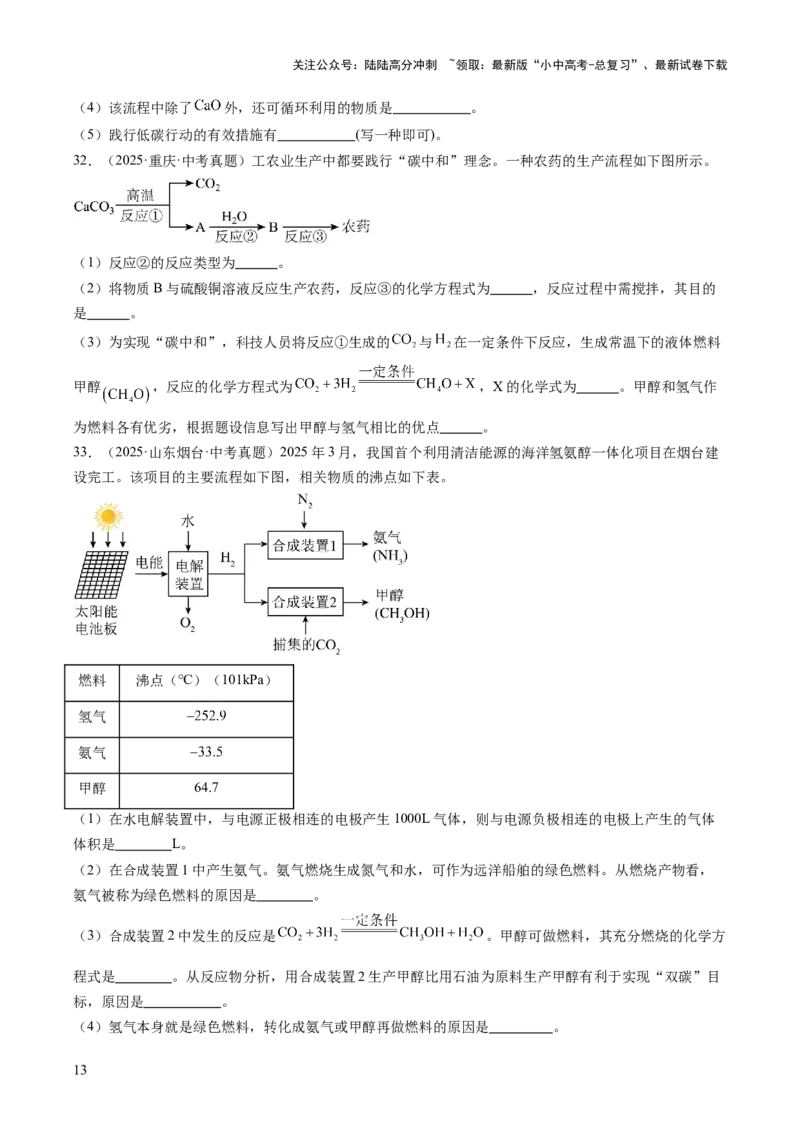
32.(2025·重庆·中考真题)工农业生产中都要践行“碳中和”理念。一种农药的生产流程如下图所示。
(1)反应②的反应类型为 。
(2)将物质B与硫酸铜溶液反应生产农药,反应③的化学方程式为 ,反应过程中需搅拌,其目的
是 。
(3)为实现“碳中和”,科技人员将反应①生成的 与 在一定条件下反应,生成常温下的液体燃料
甲醇 ,反应的化学方程式为 ,X的化学式为 。甲醇和氢气作
为燃料各有优劣,根据题设信息写出甲醇与氢气相比的优点 。
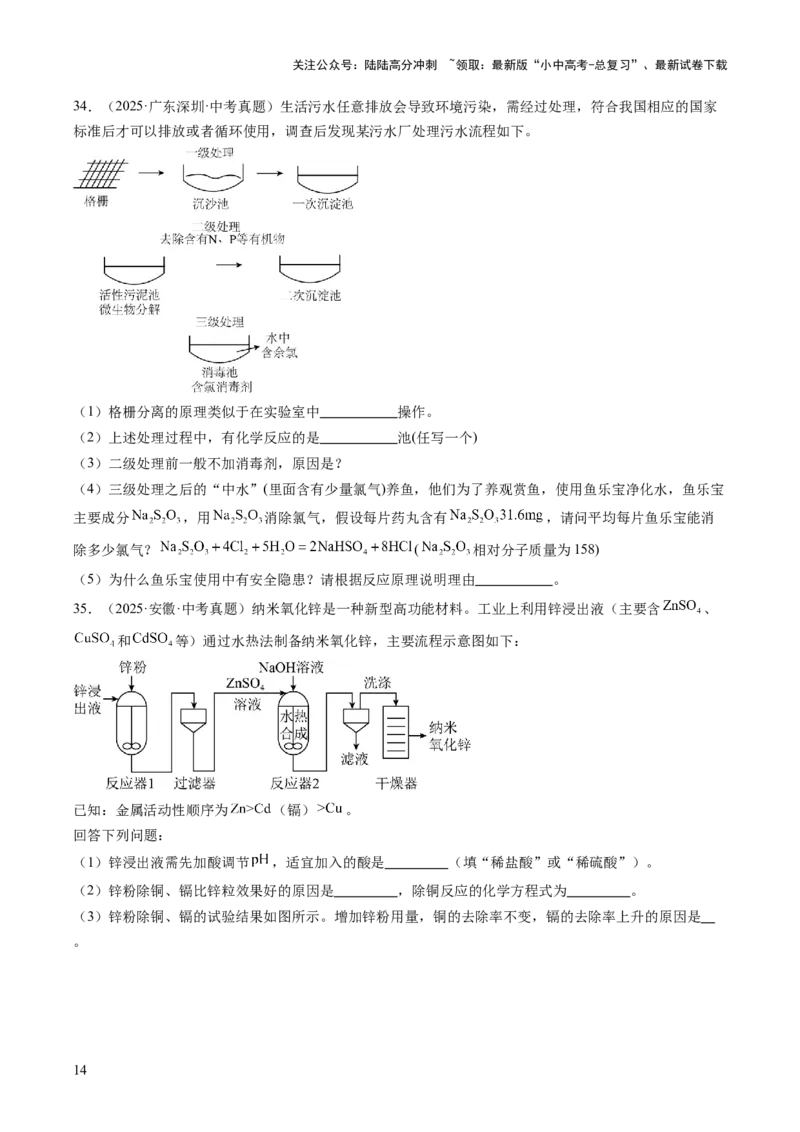
33.(2025·山东烟台·中考真题)2025年3月,我国首个利用清洁能源的海洋氢氨醇一体化项目在烟台建
设完工。该项目的主要流程如下图,相关物质的沸点如下表。
燃料 沸点(°C)(101kPa)
氢气
氨气
甲醇 64.7
(1)在水电解装置中,与电源正极相连的电极产生1000L气体,则与电源负极相连的电极上产生的气体
体积是 L。
(2)在合成装置1中产生氨气。氨气燃烧生成氮气和水,可作为远洋船舶的绿色燃料。从燃烧产物看,
氨气被称为绿色燃料的原因是 。
(3)合成装置2中发生的反应是 。甲醇可做燃料,其充分燃烧的化学方
程式是 。从反应物分析,用合成装置2生产甲醇比用石油为原料生产甲醇有利于实现“双碳”目
标,原因是 。
(4)氢气本身就是绿色燃料,转化成氨气或甲醇再做燃料的原因是 。
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
34.(2025·广东深圳·中考真题)生活污水任意排放会导致环境污染,需经过处理,符合我国相应的国家
标准后才可以排放或者循环使用,调查后发现某污水厂处理污水流程如下。
(1)格栅分离的原理类似于在实验室中 操作。
(2)上述处理过程中,有化学反应的是 池(任写一个)
(3)二级处理前一般不加消毒剂,原因是?
(4)三级处理之后的“中水”(里面含有少量氯气)养鱼,他们为了养观赏鱼,使用鱼乐宝净化水,鱼乐宝
主要成分 ,用 消除氯气,假设每片药丸含有 ,请问平均每片鱼乐宝能消
除多少氯气? ( 相对分子质量为158)
(5)为什么鱼乐宝使用中有安全隐患?请根据反应原理说明理由 。
35.(2025·安徽·中考真题)纳米氧化锌是一种新型高功能材料。工业上利用锌浸出液(主要含 、
和 等)通过水热法制备纳米氧化锌,主要流程示意图如下:
已知:金属活动性顺序为 (镉) 。
回答下列问题:
(1)锌浸出液需先加酸调节 ,适宜加入的酸是 (填“稀盐酸”或“稀硫酸”)。
(2)锌粉除铜、镉比锌粒效果好的原因是 ,除铜反应的化学方程式为 。
(3)锌粉除铜、镉的试验结果如图所示。增加锌粉用量,铜的去除率不变,镉的去除率上升的原因是
。
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(4)水热合成后,“反应器2”中的混合物经 (填操作名称)、洗涤、干燥得到产品。
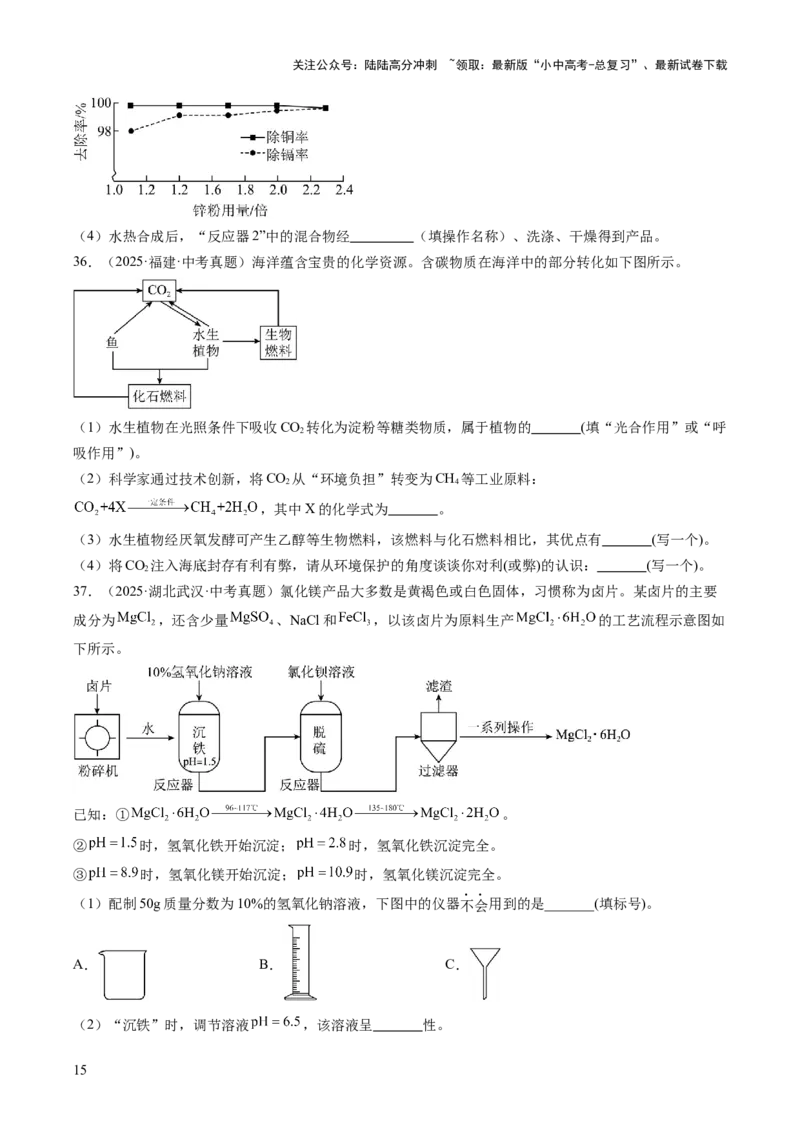
36.(2025·福建·中考真题)海洋蕴含宝贵的化学资源。含碳物质在海洋中的部分转化如下图所示。
(1)水生植物在光照条件下吸收CO 转化为淀粉等糖类物质,属于植物的 (填“光合作用”或“呼
2
吸作用”)。
(2)科学家通过技术创新,将CO 从“环境负担”转变为CH 等工业原料:
2 4
,其中X的化学式为 。
(3)水生植物经厌氧发酵可产生乙醇等生物燃料,该燃料与化石燃料相比,其优点有 (写一个)。
(4)将CO 注入海底封存有利有弊,请从环境保护的角度谈谈你对利(或弊)的认识: (写一个)。
2
37.(2025·湖北武汉·中考真题)氯化镁产品大多数是黄褐色或白色固体,习惯称为卤片。某卤片的主要
成分为 ,还含少量 、NaCl和 ,以该卤片为原料生产 的工艺流程示意图如
下所示。
已知:① 。
② 时,氢氧化铁开始沉淀; 时,氢氧化铁沉淀完全。
③ 时,氢氧化镁开始沉淀; 时,氢氧化镁沉淀完全。
(1)配制50g质量分数为10%的氢氧化钠溶液,下图中的仪器不会用到的是_______(填标号)。
A. B. C.
(2)“沉铁”时,调节溶液 ,该溶液呈 性。
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)加入适量氯化钡溶液可实现“脱硫”,反应的化学方程式为 。
(4)“滤渣”的成分为 。
(5)为制备 ,“一系列操作”中宜采用降温结晶,而不宜采用蒸发结晶,其原因是
(答两点)。
38.(2025·湖南·中考真题)以白云石(主要成分为 和 )为原料制备 的主要流程如图
1所示(部分产物略去),回答下列问题。
(1)为使白云石反应更充分,煅烧前可对白云石采取的措施是 。
(2) 产品的纯度受煅烧窑中煅烧温度的影响, 纯度与煅烧温度的关系如图2所示,煅
烧白云石最佳温度是 ℃。
(3)反应器中 发生化合反应的化学方程式是 。
39.(2024·山西·中考真题)我国是世界上锌冶炼最早的国家。明代宋应星所著的《天工开物》中有关
“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤装载入一泥罐内……然后逐层用煤炭饼
(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”此工艺过程分解
模拟如图。(已知:Zn的冶炼温度为904℃,Zn的沸点为906℃。)请结合图文信息,分析思考,解决问
题:
(1)装入原料器之前,将炉甘石敲碎的目的是 。
(2)高温炉内,碳酸锌(ZnCO)在高温条件下与煤的主要成分发生反应生成Zn和CO,反应的化学方程式
3
为 。该反应生成物中碳元素的化合价为 价。
(3)冷凝器中发生的变化属于 。
(4)我国古代冶锌晚于铁和铜,结合已知信息,分析说明其中的原因是 。
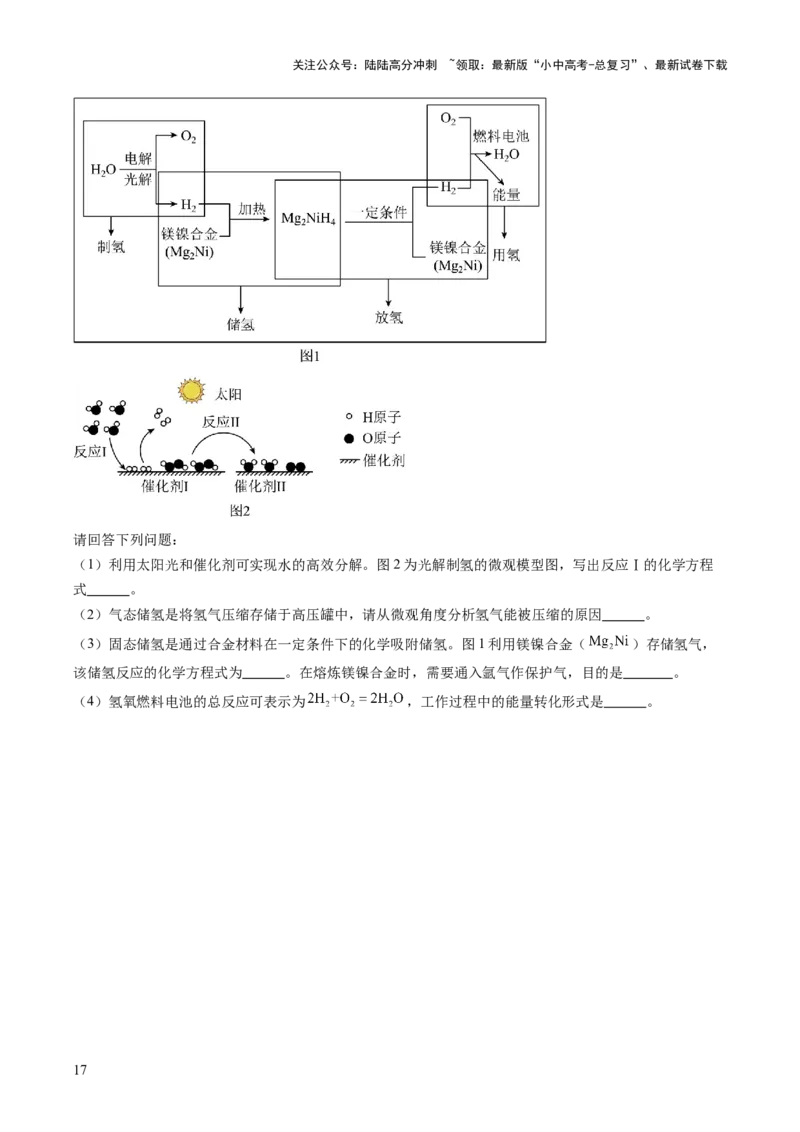
40.(2023·山东潍坊·中考真题)氢能助力“神舟十六”邀游太空,氢氧燃料电池技术在航海、航空航天等
方面发展迅速,图1是氢气的制取、储存、释放和应用的流程图。
16关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请回答下列问题:
(1)利用太阳光和催化剂可实现水的高效分解。图2为光解制氢的微观模型图,写出反应Ⅰ的化学方程
式 。
(2)气态储氢是将氢气压缩存储于高压罐中,请从微观角度分析氢气能被压缩的原因 。
(3)固态储氢是通过合金材料在一定条件下的化学吸附储氢。图1利用镁镍合金( )存储氢气,
该储氢反应的化学方程式为 。在熔炼镁镍合金时,需要通入氩气作保护气,目的是 。
(4)氢氧燃料电池的总反应可表示为 ,工作过程中的能量转化形式是 。
17