文档内容
2024~2025 学年第一学期高三年级期初学情调研测试
化学试题
2024.9
(考试时间:75分钟满分: 100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Co-59
单项选择题:本题包括10小题,每小题3分,共计30分。每小题只有一个选项符合题意。
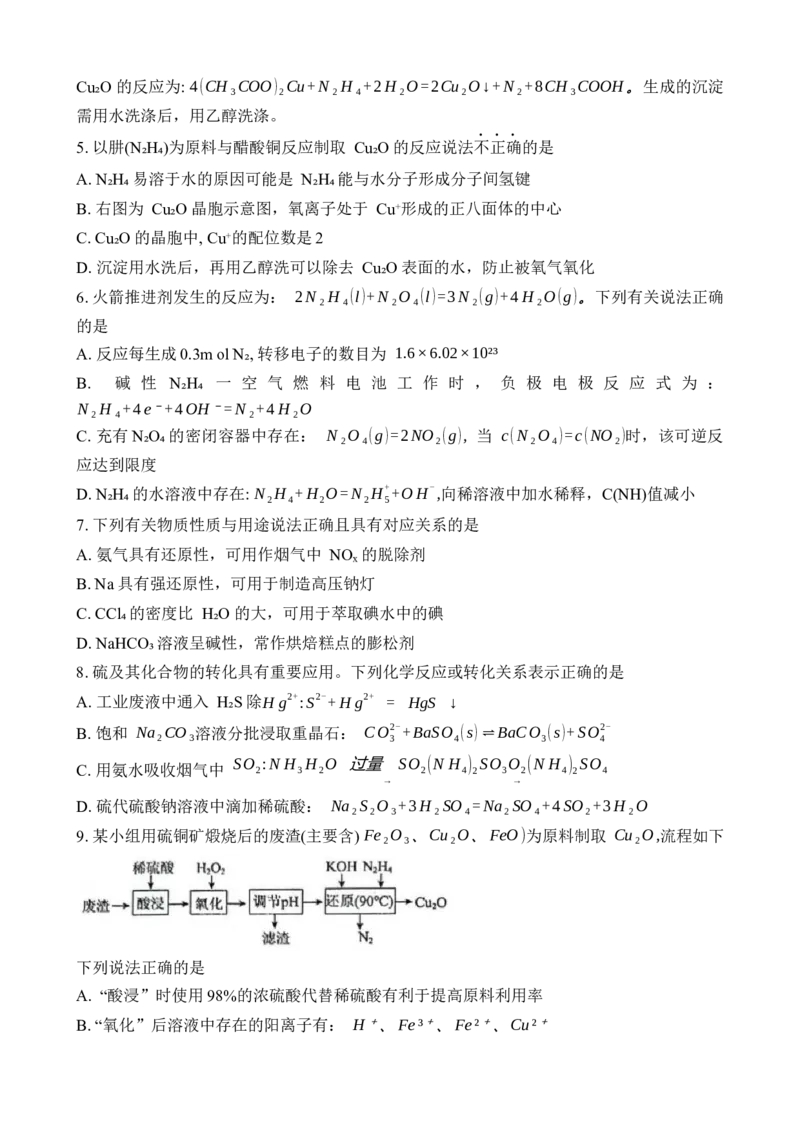
1. 我国提出2030年碳达峰、2060年碳中和的目标。下列关于CO₂的说法不正确是
A. CO₂固态易升华 B. CO₂是酸性氧化物
C. CO₂属于非电解质 D. CO₂为极性分子
2. 检验微量砷的原理为 AsH₃+12AgNO₃+3H₂O=As₂O₃↓+12HNO₃+12Ag↓∘AsH₃常温下
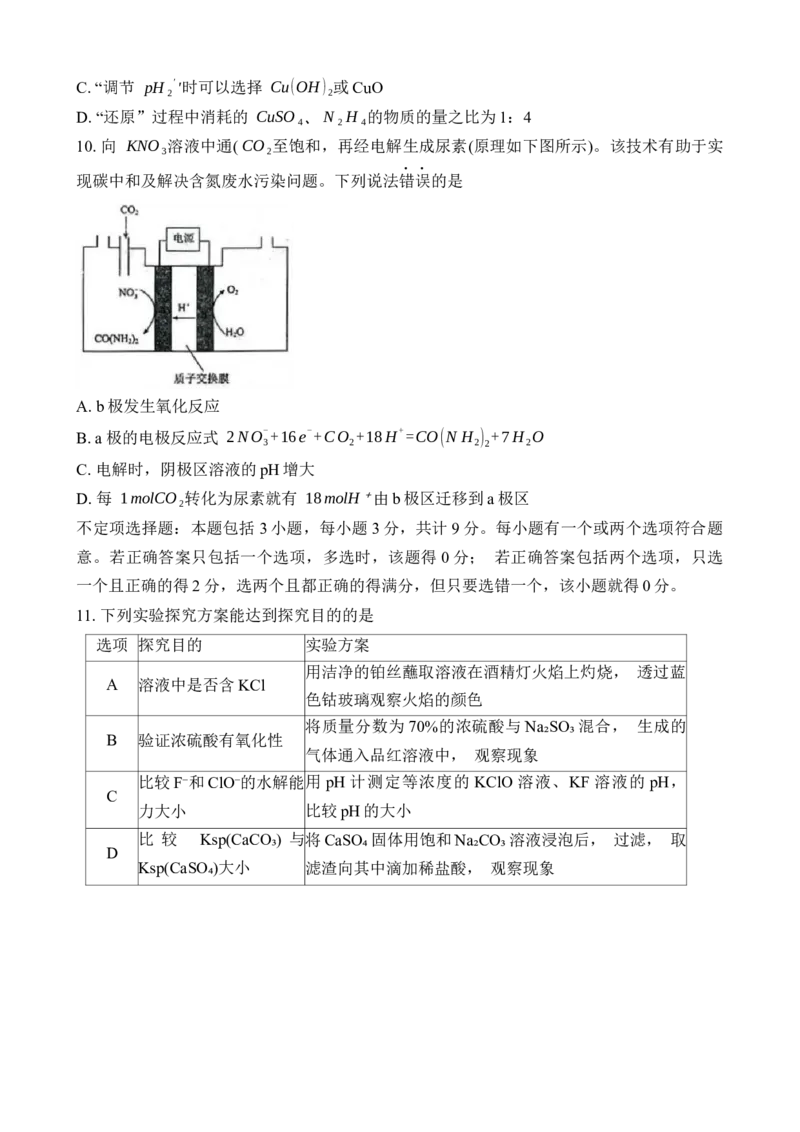
为无色气体。下列说法正确的是
A. 基态O原子的轨道表示式为: B. NO₃的空间构型为平面三角形
C. 固态 AsH₃属于共价晶体 D. HNO₃既含离子键又含共价键
3. 二氧化氯(ClO₂)是一种黄绿色气体,在水中的溶解度约为Cl₂的5倍,其水溶液在较高温度
与光照下会生成ClO₂与ClO₃。ClO₂是一种极易爆炸的强氧化性气体,实验室制备 ClO₂的反
应为 2NaClO₃+SO₂+H₂SO₄=2ClO₂+2NaHSO₄。下列有关实验室制备( ClO₂的实验原理和
装置不能达到实验目的的是
A. 用装置甲获取 SO₂ B. 用装置乙制备 ClO₂
C. 用装置丙吸收( ClO₂ D. 用装置丁处理尾气
4. 铵明矾 [NH₄Al(SO₄)₂⋅12H₂O]是常用的食品添加剂。下列判断正确的是
A. 第一电离能: I₁(N)c(H+)+c(HCO-)+c(H CO )
3 2 3
c(SO2-)
8
B. 反应 PbSO +CO2- ⇌PbCO +SO2-正向进行,需满足 4 > ×106
4 3 3 4 c(CO2-) 37
3
C. “脱硫”后上层清液中:
2c(CO2)+2c(SO2-)+c(HCO-)+c(OH-)=c(Na+)+c(H+)+2c(Pb2)
3 4 3
D. 加热 Pb(NO₃)₂溶液能得到1 Pb(NO₃)₂固体
13. 甲醇-水催化重整可获得 H₂.其主要反应为:
反应I CH₃OH(g)+H₂O(g)=CO₂(g)+3H₂(g)△H=49.4kJ⋅mol⁻
反应Ⅱ CO₂(g)+H₂(g)=CO(g)+H₂O(g)△H=41.2kJ⋅mol⁻¹
在 1.0×10⁵Pa、n (H₂O):n (CH₃OH)=6;5时,若仅考虑上述反应,平衡时 CO 的选择性、
始 始
CH₃OH的转化率和H₂的产率随温度的变化如图所示。
提示:
下列说法正确的是
n(H O)
2
A. 一定温度下,增大 可提高CO 的选
n(CH OH)
3
择性
B. 平衡时 CH₃OH 的转化率与 H₂O的转化率相等
C. 图中曲线②表示平衡时H₂产率随温度的变化
D. 一定温度下,降低体系压强,反应 I 的平衡常
数不变
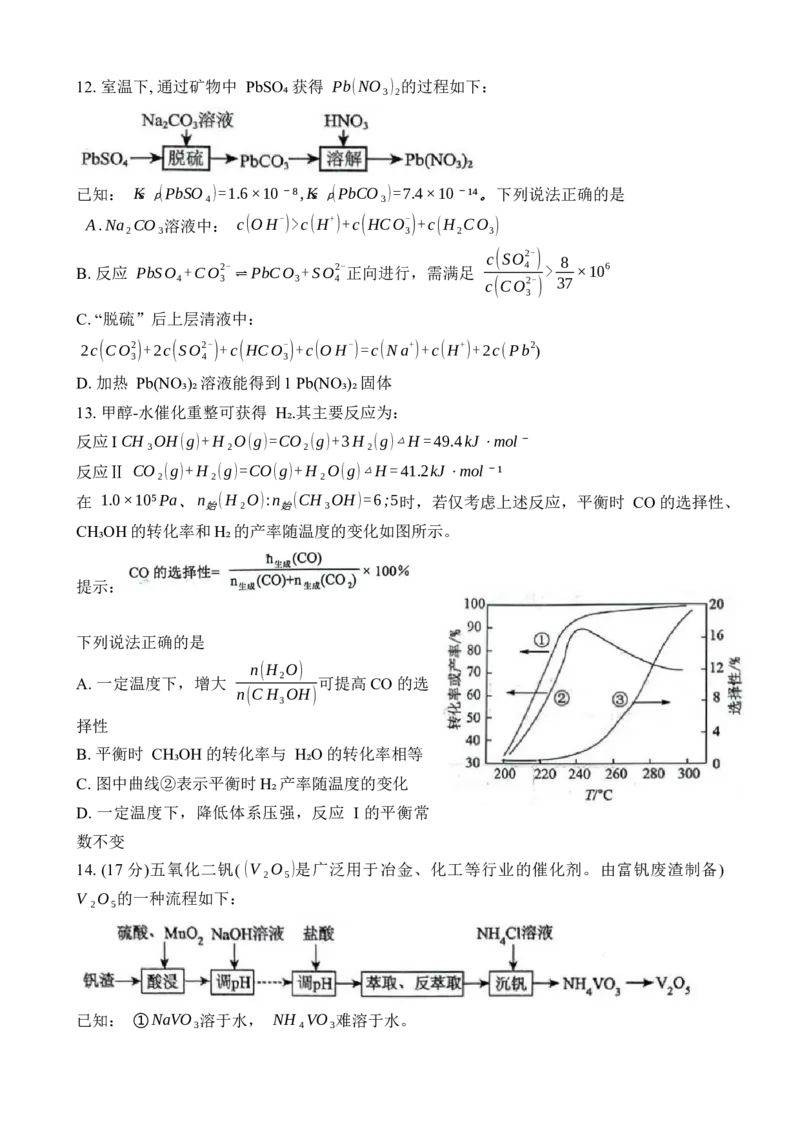
14. (17 分)五氧化二钒( (V ₂O₅)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备)
V ₂O₅的一种流程如下:
已知: ①NaVO₃溶于水, NH₄VO₃难溶于水。②部分含钒(五价)物质在水溶液中的主要存在形式:
pH <1.0 1.0~4.0 4.0~6.0 6.0~8.5 8.5~13.0 >13.0
主要存在形式 vo+ V₂O₅ 多钒酸根 vo- 多钒酸根 vo3-
2 3 4
备注 多钒酸盐在水中溶解度较小
(1)写出基态 V 原子的价层电子排布式 ▲ 。
(2)“酸浸”时, MnO₂将VO⁺转化为 V O+的离子反应方程式为 ▲ 。
2
(3)通过“调pH、萃取、反萃取”等过程,可制得1 NaVO₃溶液。
已知 V O- 能被有机萃取剂(简称 ROH)萃取,其萃取原理可表示为:
3
V O- (水层)+ROH(有机层) RVO₃(有机层)+OH⁻(水层)。
3
反萃取中, V O- 反萃取率⇌随着pH的升高呈现先增大后减小的趋势,其原因是 ▲ 。
3
(4)“沉钒”时, 向pH为8的 NaVO₃溶液中加入过量的 NH₄Cl溶液,析出 NH₄VO₃沉淀。加
入过量的NH₄Cl溶液的目的是 ▲ 。
(5)NH₄VO₃在空气中灼烧得 V₂O₅。写出该反应的化学方程
式 ▲ 。
(6)V ₂O₅可溶于强酸强碱。不同 pH、不同钒元素浓度时,
+5价 V 存在形态如图所示。
①将 0.01molV₂O₅溶解在 200mL 烧碱溶液中,剩余溶液的.
c(OH⁻)=0.01mol⋅L⁻¹,反应的离子方程式为 ▲ 。
②V O4-具有对称结构,其结构式可表示为 ▲ 。
2 7
15.(14分)钴及其化合物用途广泛。如: LiCoO₂做锂电池的正
极材料; 草酸钴可用于催化剂 (Co₃O₄)制备。
Ⅰ.利用 Li₂CO₃制备锂电池的正极材料 LiCoO₂,以某锂云母矿石(主要成分为 Li₂O,还有
Al₂O₃、 Fe₂O₃、MnO、MgF₂等杂质)制备 Li₂CO₃.
已知:①有关沉淀数据如下表(“完全沉淀”时金属离子浓度 ≤1.0×10⁻⁵mol⋅L⁻¹)。
沉淀 Al(OH)₃ Fe(OH)₂ Fc(OH)₃ Co(OH)₂ Mn(OH)₂ Mg(OH)₂
恰好完全沉淀时pH 5.2 8.8 3.2 9.4 9.8 11.1
②部分物质的溶解度曲线见题15 图-1。利用锂云母矿石制备 Li₂CO₃步骤如下:
(1)酸浸。向锂云母矿石中加入30%硫酸,加热至90℃,实验室模拟装置如题15图-2所示。
烧杯中试剂的作用是 ▲ 。
(2)调pH。向酸浸后的溶液中加入NaOH 溶液,调节pH约为6,过滤。再向滤液中继续滴加
氢氧化钠溶液调pH>12,过滤,此时的滤渣主要成分为 ▲ 。分两次调节pH的主要原因
是 ▲ 。
(3)沉锂。将已经除杂的溶液蒸发浓缩,向浓缩后的滤液中加入稍过量饱和 Na₂CO₃溶液,加
热煮沸,趁热过滤,将滤渣洗涤烘干,得 Li₂CO₃固体。浓缩液中离子浓度过大将在产品中
引入 ▲ 杂质(填化学式)。
(4)Li₂CO₃和Co₃O₄混合后,在空气中高温加热可以制备锂电池的正极材料 LiCoO₂,写出反
应方程式 ▲ 。
Ⅱ. 将 CoC₂O₄⋅2H₂O热分解制备催化剂 Co₃O₄.
(5)为确定由 CoC₂O₄⋅2H₂O获得 Co₃O₄的最佳煅烧温
度, 准确称取4.575g的 CoC₂O₄⋅2H₂O样品,在空气中加
热,固体样品的剩余质量随温度的变化如题 15图-3所示
(已知385℃以上残留固体均为金属氧化物)。则煅烧的最
佳温度 ▲ (写出计算过程)。
16. (16分) 硒是人体所需微量元素之一,也是一种重要的工业原料。
工业上从铜阳极泥(含有 Se、Au、Ag、Cu、CuSe、Ag₂Se 等)中提取硒的过程如下:
(1)“焙烧”时, Ag₂Se 与O₂反应每消耗1molO₂,转移电子的物质的量为 ▲ 。
(2)甲酸还原H₂ScO₃反应的化学方程式为 ▲ 。
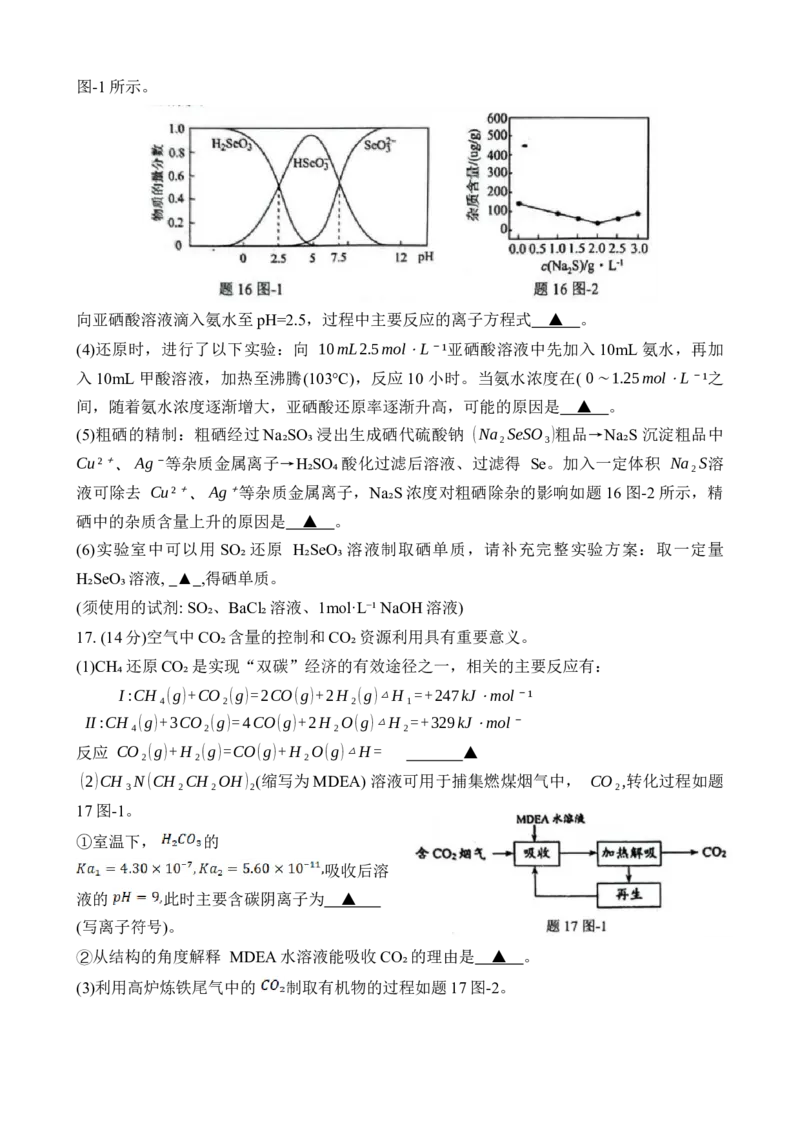
(3)常温下, H₂ScO₃电离平衡体系中含 Se(+4 价)微粒的物质的量分数与 pH的关系如题16图-1所示。
向亚硒酸溶液滴入氨水至pH=2.5,过程中主要反应的离子方程式 ▲ 。
(4)还原时,进行了以下实验:向 10mL2.5mol⋅L⁻¹亚硒酸溶液中先加入10mL 氨水,再加
入10mL 甲酸溶液,加热至沸腾(103℃),反应10 小时。当氨水浓度在( 0∼1.25mol⋅L⁻¹之
间,随着氨水浓度逐渐增大,亚硒酸还原率逐渐升高,可能的原因是 ▲ 。
(5)粗硒的精制:粗硒经过Na₂SO₃浸出生成硒代硫酸钠 (Na₂SeSO₃)粗品→Na₂S 沉淀粗品中
Cu²⁺、Ag⁻等杂质金属离子→H₂SO₄酸化过滤后溶液、过滤得 Se。加入一定体积 Na₂S溶
液可除去 Cu²⁺、Ag⁺等杂质金属离子,Na₂S浓度对粗硒除杂的影响如题 16图-2所示,精
硒中的杂质含量上升的原因是 ▲ 。
(6)实验室中可以用 SO₂ 还原 H₂SeO₃ 溶液制取硒单质,请补充完整实验方案:取一定量
H₂SeO₃溶液, ▲ ,得硒单质。
(须使用的试剂: SO₂、BaCl₂溶液、1mol·L⁻¹ NaOH溶液)
17. (14分)空气中CO₂含量的控制和CO₂资源利用具有重要意义。
(1)CH₄还原CO₂是实现“双碳”经济的有效途径之一,相关的主要反应有:
I:CH₄(g)+CO₂(g)=2CO(g)+2H₂(g)△H₁=+247kJ⋅mol⁻¹
II:CH₄(g)+3CO₂(g)=4CO(g)+2H₂O(g)△H₂=+329kJ⋅mol⁻
反应 CO₂(g)+H₂(g)=CO(g)+H₂O(g)△H= ▲
(2)CH₃N(CH₂CH₂OH)₂(缩写为MDEA) 溶液可用于捕集燃煤烟气中, CO₂,转化过程如题
17图-1。
①室温下, 的
吸收后溶
液的 此时主要含碳阴离子为 ▲
(写离子符号)。
②从结构的角度解释 MDEA 水溶液能吸收CO₂的理由是 ▲ 。
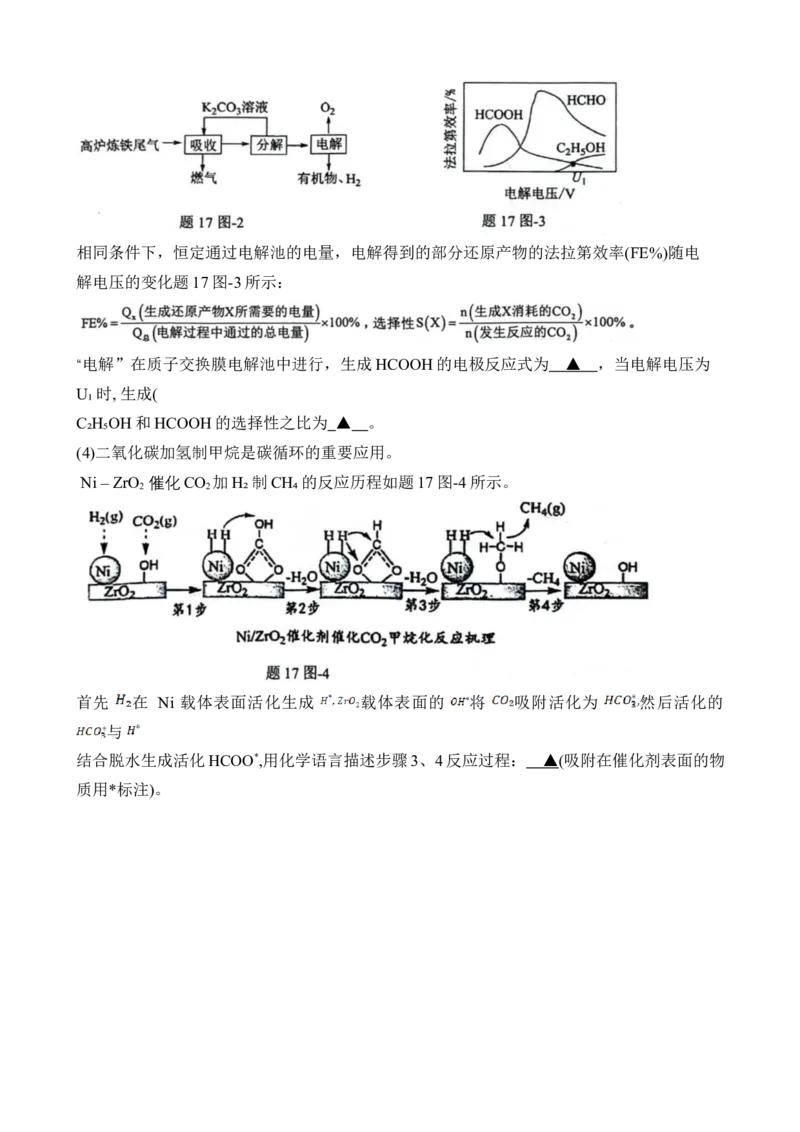
(3)利用高炉炼铁尾气中的 制取有机物的过程如题17图-2。相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电
解电压的变化题17图-3所示:
“电解”在质子交换膜电解池中进行,生成HCOOH的电极反应式为 ▲ ,当电解电压为
U₁时, 生成(
C₂H₅OH和HCOOH的选择性之比为 ▲ 。
(4)二氧化碳加氢制甲烷是碳循环的重要应用。
Ni – ZrO 催化CO 加H₂制CH₄的反应历程如题17图-4所示。
2 2
首先 在 Ni 载体表面活化生成 载体表面的 将 吸附活化为 然后活化的
与
结合脱水生成活化HCOO*,用化学语言描述步骤3、4反应过程: ▲(吸附在催化剂表面的物
质用*标注)。