文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
精练 10 工艺流程题
知识点回顾(时间:5分钟)
知识点一、工艺流程题
1、工艺流程图题的实质
工艺流程图题的实质是以流程图的形式给出工业生产或实验步骤等相关信息的一类题目。
2、工艺流程图题的特点
(1)涉及知识点比较广
工艺流程图只是出题时给出信息的一种方式,根据所给的信息可以涉及初中化学很多知识点,如:
化学用语、实验操作、质量守恒、化学计算、物质的转化与制备、检验与鉴别、分离与除杂、方案
评价等。
(2)取材范围主要涉及物质生产制备、分离提纯、成分推断、资源和废物利用等
(3)起点比较高、落点可高可低,工艺流程一般涉及实际工业生产或比较复杂的化学实验,有我们熟
悉的知识,也涉及没有学过的知识,起点是比较高的。但是落点可高可低,如落点比较低的题一般
重点考查化学式、离子符号、化学方程式的书写、质量守恒的简单运用以及一些实验操作问题;落
点比较高的题涉及用己有的知识和提供的知识进行化学反应的分析、物质推断、化学计算、方案评
价等等,要求比较高,难度比较大。
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
知识点二、工艺流程题解题思路
1、阅读题干,抓住生产或实验目的不论是生产还是实验都是有目的的,通过读题,弄清生产或实
验的目的。
2、分析流程图,弄清操作和原理
流程图的实质是生产或实验的步骤,分析每一步用到了什么操作,起什么作用,涉及到哪些物质,
发生了哪些反应,生成了哪些物质,如何一步一步达到生产或实验目的的。分析过程注意以下几点:
(1)“三线”:“进线”、“出线”和“回头线”“进线”即箭头指向的线,一般是原料或参加反应的
反应物:“出线”即箭头指出的线,一般是反应生成的生成物;“回头线"即从后一步骤指出,指向前面
步骤的线,一般是循环或重复利用的物质。
(2)几个重要操作:①搅拌、粉碎:搅拌混合均匀、充分反应;粉碎增大接触面,使反应更快更充分;②
煅烧、焙烧:是高温分解或在高温下与氧气等反应;
③过滤、蒸发结品:是主要的两个物质分析操作。
3、结合分析得到的信息,回答题目的问题。
抓住了目的,分析清楚了流程图,根据所学的知识就能解决题目的问题
【题型一】海水资源的开发利用
[例题1] (2023•威远县校级一模)海水中含有氯化钠、氯化镁等可溶性盐,利用海水制取
金属镁的流程如图所示:
下表是某品牌不同碱的价格:
试剂 NaOH Ca(OH) Ba(OH) KOH
2 2
价格(元/吨) 2400 850 5300 5500
下列有关制取金属镁的说法错误的是( )
A.试剂X最好选择表格中的KOH
B.经历步骤Ⅰ和步骤Ⅱ两步转化,其目的之一是富集海水中的MgCl
2
C.不能直接用氯化镁溶液通电制取镁
D.制取过程中某些元素的化合价变化了
[例题2] (2023•章丘区一模)(1)我国科学家侯德榜在氨碱法的基础上创立了更为先进
的联合制碱法(侯氏制碱法),其生产流程如图2:
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①制碱原理为向饱和 NaCl 溶液中通入足量 NH 和 CO 生成 NaHCO 晶体和 NH Cl,
3 2 3 4
(NaCl+NH +CO +H O=NaHCO +NH Cl);NaHCO 加热分解即制得纯碱。请写出NaHCO 热分
3 2 2 3 4 3 3
解的化学方程式为 。
②饱和NaCl溶液中通入足量NH 和CO 后,先析出的NaHCO 晶体的原因是 (填序
3 2 3
号)。
A.溶剂质量减少
B.相同温度下,NaHCO 溶解度小于NH Cl
3 4
C.相同反应时间,生成NaHCO 的质量大于NH Cl质量
3 4
③ 向 饱 和 食 盐 水 中 先 通 入 氨 气 再 通 二 氧 化 碳 的 原 因 是
。
(2)工业制取的纯碱样品中常含有少量氯化钠杂质,现取11g该样品将其放入干净的烧杯中,缓
缓滴入溶质质量分数为7.3%的稀盐酸,生成气体的质量与滴入稀盐酸的质量关系如图3所示。试
回答下列问题:
①当滴入稀盐酸溶液80g时(即图中A点),烧杯中溶液里含有的阳离子为 (写离子
符号)。
②当滴入稀盐酸溶液100g时(即图中B点),恰好完全反应,试通过计算,求纯碱样品中碳酸
钠的质量分数(计算结果精确至0.1%)。
【题型二】生产制备流程
[例题3] (2023•工业园区校级二模)科学工作者研发了一种SUNCAT系统,借助该系统利
用如图所示的原理可持续合成氨。下列说法正确的是( )
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.该系统中只有Li、O的化合价发生了改变
B.涉及的反应类型只有化合反应和分解反应
C.理论上,每合成68gNH ,就需要消耗56gN
3 2
D.理论上,每消耗28gN ,需额外补充42gLi
2
[例题4] (2023春•江岸区校级月考)某化学兴趣小组的同学在学习侯德榜为纯碱和氮肥工
业技术的发展做出的杰出贡献后,将所学的相关知识整理如下,请你和他们一起完善学习笔
记。
【资料卡片】
粗盐水中主要含有CaCl 、MgCl ,Na SO 及泥沙等杂质,通常状况下,NH 的溶解度远大于CO
2 2 2 4 3 2
的溶解度。侯氏制碱法主要原理是在饱和食盐水中通入氨气和二氧化碳,生成氯化铵和碳酸氢钠
的过程。请回答下列问题:
(1)X的化学式是 。
(2)除去粗盐中杂质Na
2
SO
4
的反应的化学方程式是
。
(3)滤液中一定有的溶质有 (填化学式)
(4)该流程中可循环利用物质为 。(除H
2
O外,填化学式)
(5)下列学习笔记中,你认为错误的有 (填字母)。
A.海水晒盐遵循质量守恒定律
B.粗盐提纯时要使用Na CO 溶液,其作用是仅除去氯化钙杂质
2 3
C.上述流程中共涉及四种基本反应类型
D.碱厂与氨厂联合后,用NH Cl代替氨水做化肥,便于运输和储存
4
E.若向饱和食盐水中先通入CO 后通入NH ,会导致NaHCO 产量减少
2 3 3
【题型三】分离提纯流程
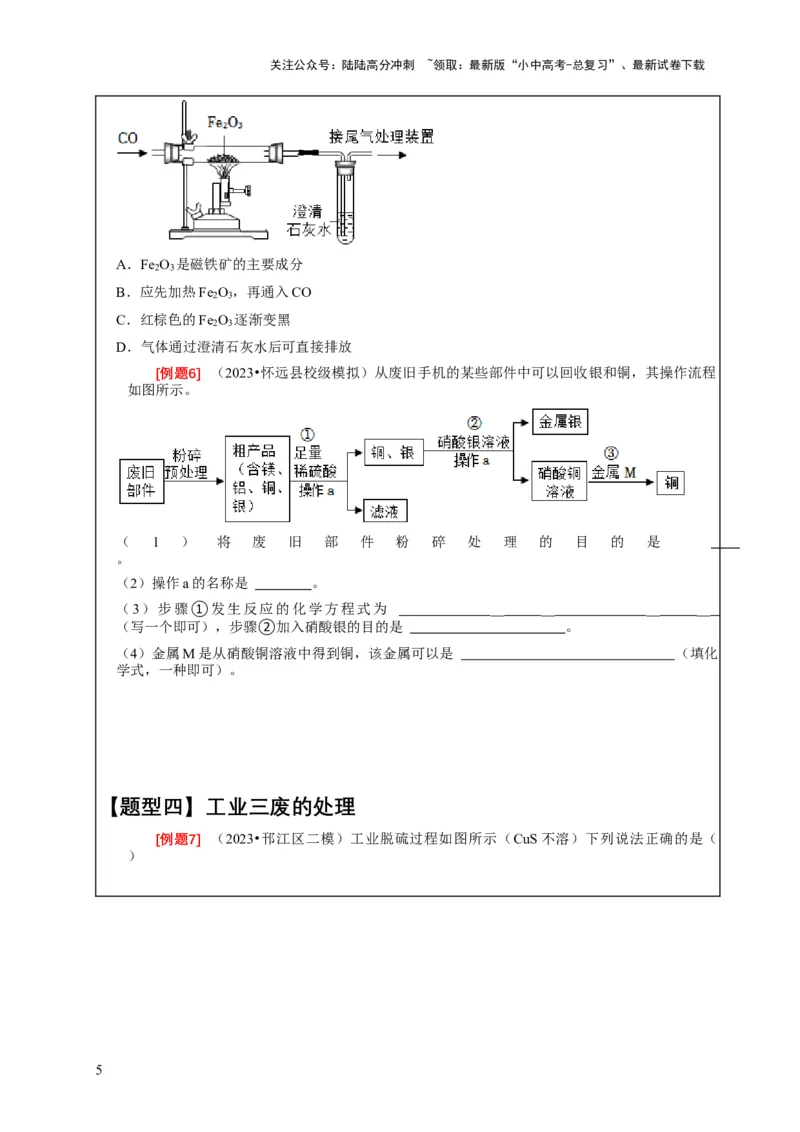
[例题5] (2023•皇姑区三模)实验室用如图所示装置进行模拟炼铁实验。下列说法正确的
是( )
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.Fe O 是磁铁矿的主要成分
2 3
B.应先加热Fe O ,再通入CO
2 3
C.红棕色的Fe O 逐渐变黑
2 3
D.气体通过澄清石灰水后可直接排放
[例题6] (2023•怀远县校级模拟)从废旧手机的某些部件中可以回收银和铜,其操作流程
如图所示。
( 1 ) 将 废 旧 部 件 粉 碎 处 理 的 目 的 是
。
(2)操作a的名称是 。
(3)步骤①发生反应的化学方程式为
(写一个即可),步骤②加入硝酸银的目的是 。
(4)金属M是从硝酸铜溶液中得到铜,该金属可以是 (填化
学式,一种即可)。
【题型四】工业三废的处理
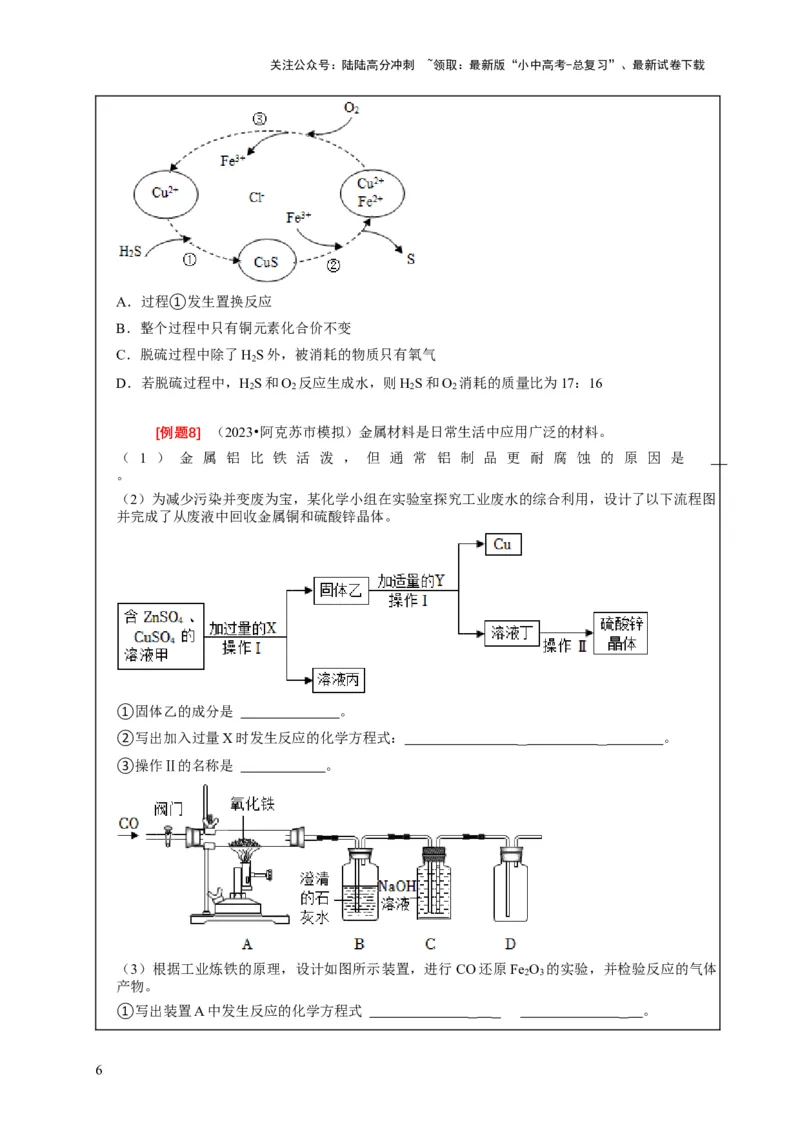
[例题7] (2023•邗江区二模)工业脱硫过程如图所示(CuS不溶)下列说法正确的是(
)
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.过程①发生置换反应
B.整个过程中只有铜元素化合价不变
C.脱硫过程中除了H S外,被消耗的物质只有氧气
2
D.若脱硫过程中,H S和O 反应生成水,则H S和O 消耗的质量比为17:16
2 2 2 2
[例题8] (2023•阿克苏市模拟)金属材料是日常生活中应用广泛的材料。
( 1 ) 金 属 铝 比 铁 活 泼 , 但 通 常 铝 制 品 更 耐 腐 蚀 的 原 因 是
。
(2)为减少污染并变废为宝,某化学小组在实验室探究工业废水的综合利用,设计了以下流程图
并完成了从废液中回收金属铜和硫酸锌晶体。
①固体乙的成分是 。
②写出加入过量X时发生反应的化学方程式: 。
③操作Ⅱ的名称是 。
(3)根据工业炼铁的原理,设计如图所示装置,进行CO还原Fe O 的实验,并检验反应的气体
2 3
产物。
①写出装置A中发生反应的化学方程式 。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
②B装置中的实验现象是什么 。
③ 某 同 学 认 为 该 装 置 不 需 要 补 充 尾 气 处 理 装 置 , 其 理 由 是 什 么
。
(4)现有20g含Fe O 80%的赤铁矿石,加入到150g稀盐酸中,恰好完全反应(铁矿石中的杂质
2 3
都不溶于水,且不与稀盐酸反应),求稀盐酸中溶质的质量分数。
难度:★★★ 建议时间:25分钟
1. (2023•鼓楼区校级三模)海水是一种重要的自然资源,镁被誉为海洋里宝贵的“国
防元素”。从海水或卤水(含氯化镁)中提取镁的主要步骤如下。下列有关说法不正确的是(
)
A.操作A的名称是过滤
B.加入的试剂B可以是氯化钙
C.步骤②发生的化学反应的基本类型属于复分解反应
D.步骤①→步骤②是为了将MgCl 聚集起来,获得比较纯净的MgCl
2 2
2. (2023•西山区一模)明代宋应星著的《天工开物》中有关“火法”冶炼金属锌的记
载:“炉甘石(注:主要成分碳酸锌)十斤,装载入一泥罐内,然后逐层用煤炭饼垫盛,其底
铺薪,发火煅红,冷淀,毁罐取出,即倭铅也。”下列有关叙述错误的是( )
A.该过程利用了“煤炭饼”的还原性
B.“火法”炼锌的反应属于置换反应
C.“倭铅”是指铅和锌的合金
D.“泥封”的目的是隔绝空气
3. (2023•让胡路区校级模拟)黄铁矿的主要成分为二硫化亚铁(FeS ),工业上可利
2
用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
下列说法错误的是( )
A.反应②不是置换反应,反应③④为化合反应
B.反应①中各元素的化合价均发生了改变
C.该工业生产过程产生的废气中的SO 可以用熟石灰溶液吸收
2
D.欲配制19.6%的稀硫酸,实验操作是向100克98%的浓硫酸中加入400克蒸馏水并不断用玻
璃棒搅拌
4. (2023•洪泽区模拟)CuCl 是重要的化工原料。工业上常采用将Cu与稀盐酸在持续
2
通入空气的条件下反应,FeCl 具有催化作用。反应原理如图所示。下列说法正确的是
3
( )
A.该实验说明Cu能与稀盐酸发生置换反应
B.参加反应的O 、HCl分子个数比为1:4
2
C.该反应过程中需要持续添加FeCl 溶液
3
D.该过程中只有铜、氧元素化合价发生改变
5. (2023•青羊区校级模拟)为保障航天员在空间站的生命和健康,科学家们研制出最
新的环境控制和生命保障系统,部分循环过程如图。下列说法不正确的是( )
通电
A.水电解系统发生的反应:2H O 2H ↑+O ↑
2 2 2
¯
❑
B.X的化学式为CO
2
C.图中所示的物质转化中可实现O 的再生
2
D.图示的物质转化中,电解的水与生成的水质量相等
6. (2023•杏花岭区校级一模)炼铁厂以赤铁矿、焦炭、石灰石、空气等为主要原料来
炼铁,主要反应过程如图所示:
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
请根据图示及所学知识判断下列说法错误的是( )
A.工业炼铁的设备是高炉
B.焦炭的作用是提供热量和制取一氧化碳
C.生铁属于混合物
高温
D.生成铁的主要反应是:CO+Fe O Fe+CO
2 3 2
¯
❑
7. (2023•永州模拟)某化工厂与相邻的化肥厂联合设计了以下制备(NH ) SO 的工
4 2 4
艺流程。已知(NH ) SO 受热不稳定。下列说法错误的是( )
4 2 4
A.进入沉淀池选用CaSO 悬浊液而不是溶液,目的是提高产量
4
B.操作②为加热蒸发
C.沉淀池里发生的主要化学反应为:CO +H O+2NH +CaSO ═CaCO ↓+(NH ) SO
2 2 3 4 3 4 2 4
D.该工艺流程中可循环使用的物质为气体Y
8. (2023•广陵区一模)近年来,研究人员提出利用含硫物质循环实现太阳能的转化与
存储,部分循环过程如图所示。下列说法不正确的是( )
A.该过程中能量转化的形式至少有四种
B.反应Ⅰ中每生成64g的SO ,同时生成32gO
2 2
催化剂
C.反应Ⅱ的化学方程式为3SO +2H O 2H SO +S↓
2 2 2 4
¯
❑
D.该过程可实现H SO 、SO 等物质的循环使用
2 4 2
9. (2023•东西湖区模拟)我国是全球规模最大的禽蛋生产国和消费国。对蛋壳(主要
成分为碳酸钙)中的钙源进行回收利用,可以变废为宝。蛋壳高温煅烧法制备乳酸钙的工艺流
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
程如图。
已知乳酸是一种有机酸,具有酸的通性;乳酸钙易溶于水,难溶于乙醇,更易被人体吸收。
下列说法中不正确的是( )
A.碳酸钙难溶于水,但生活中也可用作人体补钙剂
B.乳酸钙在水中溶解度随温度升高而降低
C.在反应液中加灰分可使其pH上升
D.与水相比,用无水乙醇洗涤粗产品,可以提高产品的产率
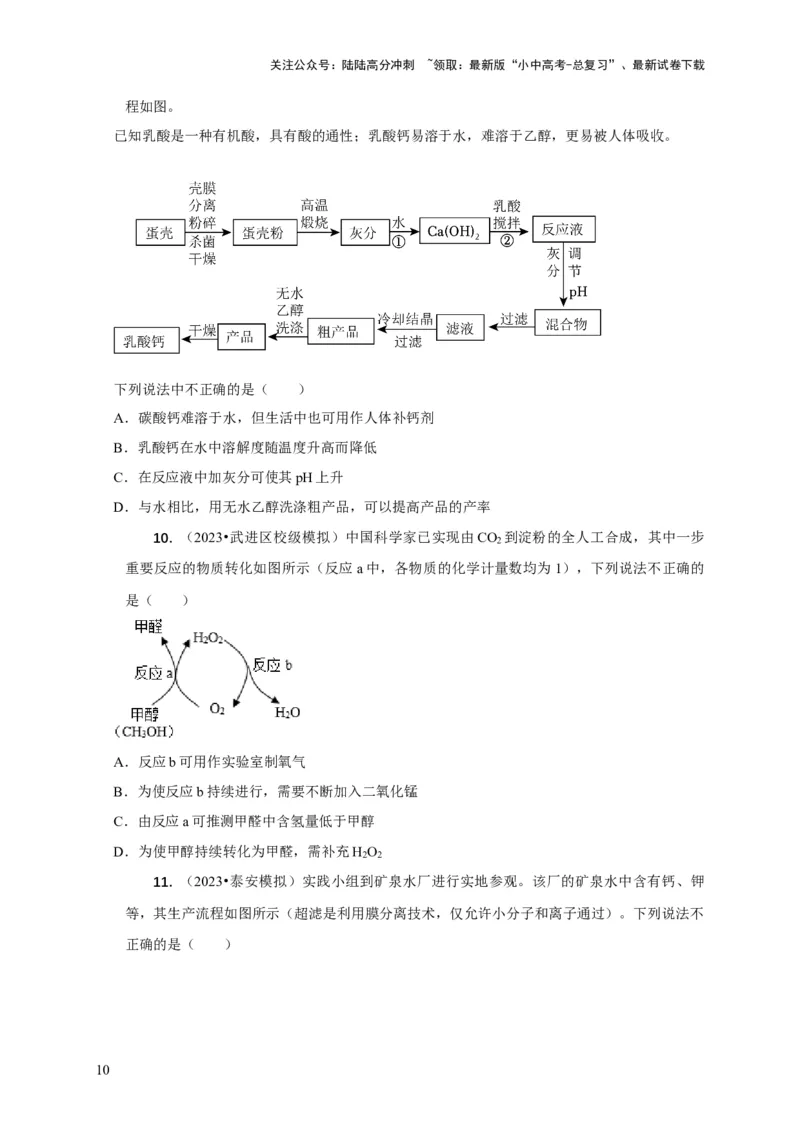
10. (2023•武进区校级模拟)中国科学家已实现由CO 到淀粉的全人工合成,其中一步
2
重要反应的物质转化如图所示(反应a中,各物质的化学计量数均为1),下列说法不正确的
是( )
A.反应b可用作实验室制氧气
B.为使反应b持续进行,需要不断加入二氧化锰
C.由反应a可推测甲醛中含氢量低于甲醇
D.为使甲醇持续转化为甲醛,需补充H O
2 2
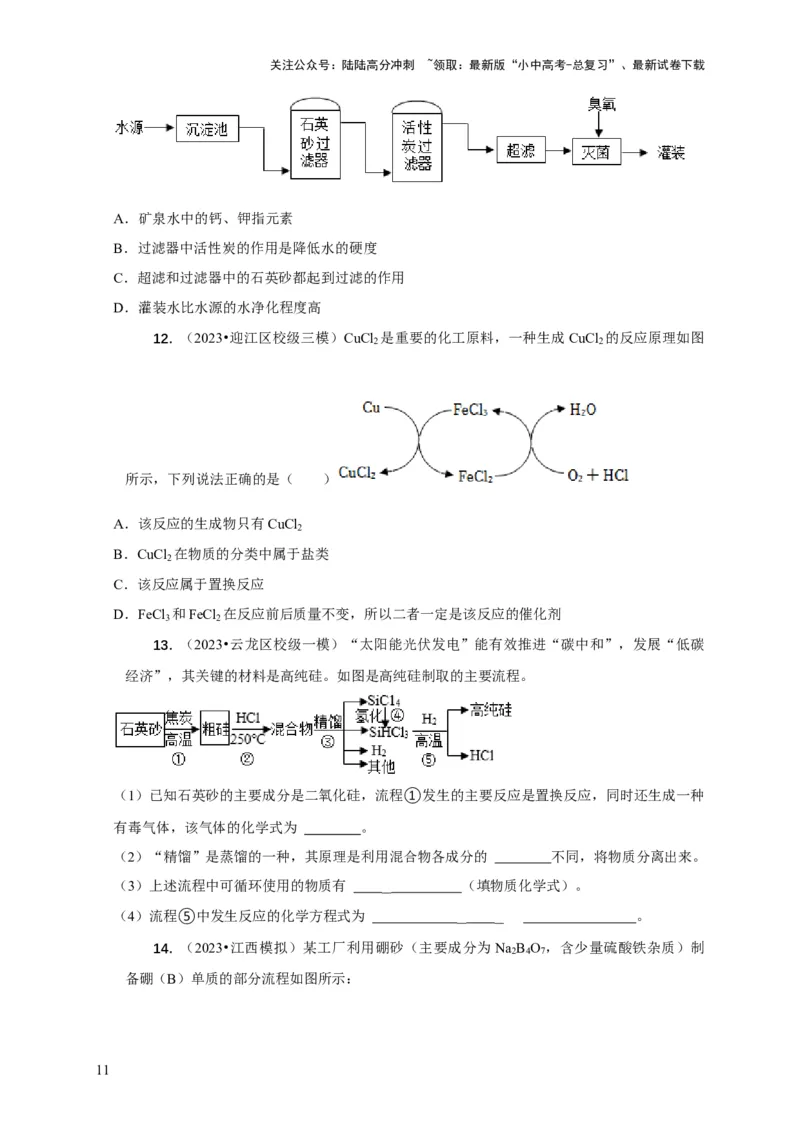
11. (2023•泰安模拟)实践小组到矿泉水厂进行实地参观。该厂的矿泉水中含有钙、钾
等,其生产流程如图所示(超滤是利用膜分离技术,仅允许小分子和离子通过)。下列说法不
正确的是( )
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.矿泉水中的钙、钾指元素
B.过滤器中活性炭的作用是降低水的硬度
C.超滤和过滤器中的石英砂都起到过滤的作用
D.灌装水比水源的水净化程度高
12. (2023•迎江区校级三模)CuCl 是重要的化工原料,一种生成CuCl 的反应原理如图
2 2
所示,下列说法正确的是( )
A.该反应的生成物只有CuCl
2
B.CuCl 在物质的分类中属于盐类
2
C.该反应属于置换反应
D.FeCl 和FeCl 在反应前后质量不变,所以二者一定是该反应的催化剂
3 2
13. (2023•云龙区校级一模)“太阳能光伏发电”能有效推进“碳中和”,发展“低碳
经济”,其关键的材料是高纯硅。如图是高纯硅制取的主要流程。
(1)已知石英砂的主要成分是二氧化硅,流程①发生的主要反应是置换反应,同时还生成一种
有毒气体,该气体的化学式为 。
(2)“精馏”是蒸馏的一种,其原理是利用混合物各成分的 不同,将物质分离出来。
(3)上述流程中可循环使用的物质有 (填物质化学式)。
(4)流程⑤中发生反应的化学方程式为 。
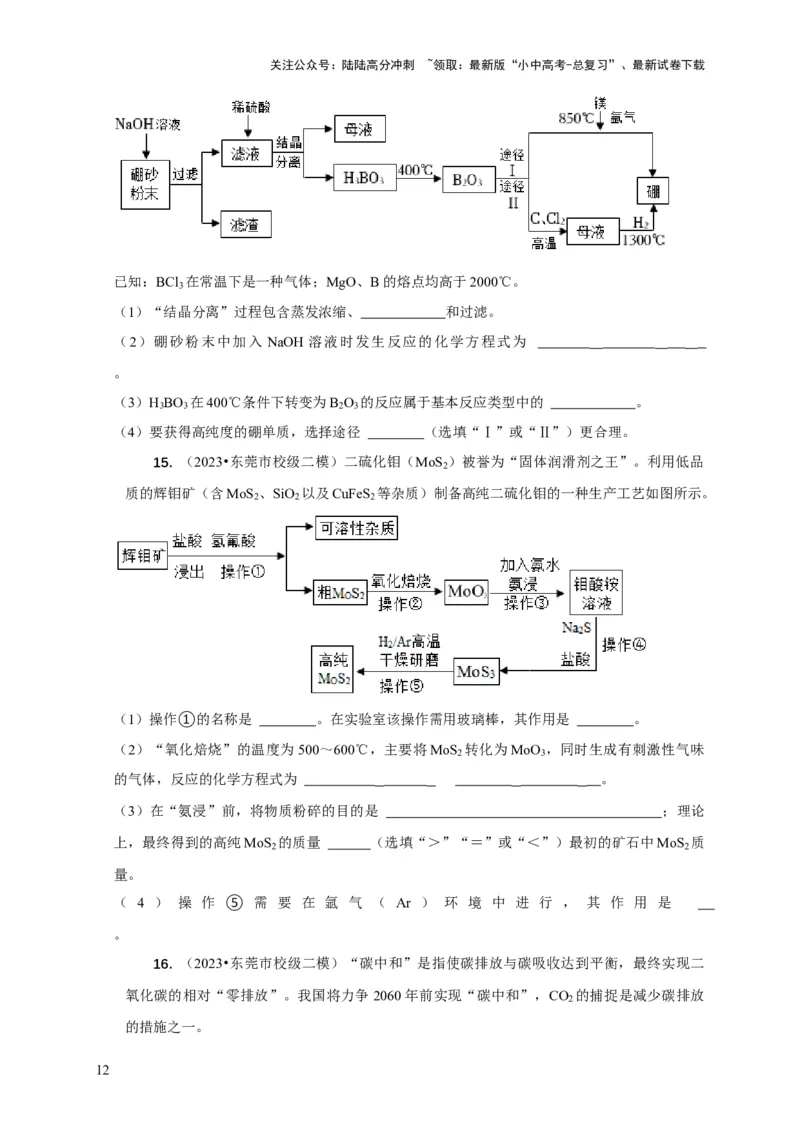
14. (2023•江西模拟)某工厂利用硼砂(主要成分为Na B O ,含少量硫酸铁杂质)制
2 4 7
备硼(B)单质的部分流程如图所示:
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
已知:BCl 在常温下是一种气体;MgO、B的熔点均高于2000℃。
3
(1)“结晶分离”过程包含蒸发浓缩、 和过滤。
(2)硼砂粉末中加入 NaOH 溶液时发生反应的化学方程式为
。
(3)H BO 在400℃条件下转变为B O 的反应属于基本反应类型中的 。
3 3 2 3
(4)要获得高纯度的硼单质,选择途径 (选填“Ⅰ”或“Ⅱ”)更合理。
15. (2023•东莞市校级二模)二硫化钼(MoS )被誉为“固体润滑剂之王”。利用低品
2
质的辉钼矿(含MoS 、SiO 以及CuFeS 等杂质)制备高纯二硫化钼的一种生产工艺如图所示。
2 2 2
(1)操作①的名称是 。在实验室该操作需用玻璃棒,其作用是 。
(2)“氧化焙烧”的温度为500~600℃,主要将MoS 转化为MoO ,同时生成有刺激性气味
2 3
的气体,反应的化学方程式为 。
(3)在“氨浸”前,将物质粉碎的目的是 ;理论
上,最终得到的高纯MoS 的质量 (选填“>”“=”或“<”)最初的矿石中MoS 质
2 2
量。
( 4 ) 操 作 ⑤ 需 要 在 氩 气 ( Ar ) 环 境 中 进 行 , 其 作 用 是
。
16. (2023•东莞市校级二模)“碳中和”是指使碳排放与碳吸收达到平衡,最终实现二
氧化碳的相对“零排放”。我国将力争 2060年前实现“碳中和”,CO 的捕捉是减少碳排放
2
的措施之一。
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)某工厂为实现“碳中和”目标,设计了一种“捕捉”CO 的方案,流程如图1:
2
①吸收器中,NaOH溶液吸收CO
2
的化学方程式为
。
②分离器中,Na
2
CO
3
参与反应的化学方程式为
。
③澄清石灰水也能与CO 反应,但在工业生产中却不宜直接用澄清石灰水“捕捉”CO ,其原
2 2
因是 。
(2)CaO固体也可以捕捉回收CO 。研究表明草酸钙晶体(CaC O •H O,相对分子质量为
2 2 4 2
146)充分加热分解制得的CaO疏松多孔,具有良好的CO 捕捉性能。现称取mg草酸钙晶体置
2
于氮气流中加热,残留固体质量随温度的变化如图2所示(图中各点对应固体均为纯净物),其
△
中A→B发生反应:CaC O •H O CaC O +H O↑。
2 4 2 2 4 2
¯
❑
①写出C→D反应的化学方程式: 。
②m= 。(写出计算过程)
13