文档内容
(四)挖掘教材实验命题
(选择题1~10题,每小题5分,共50分)
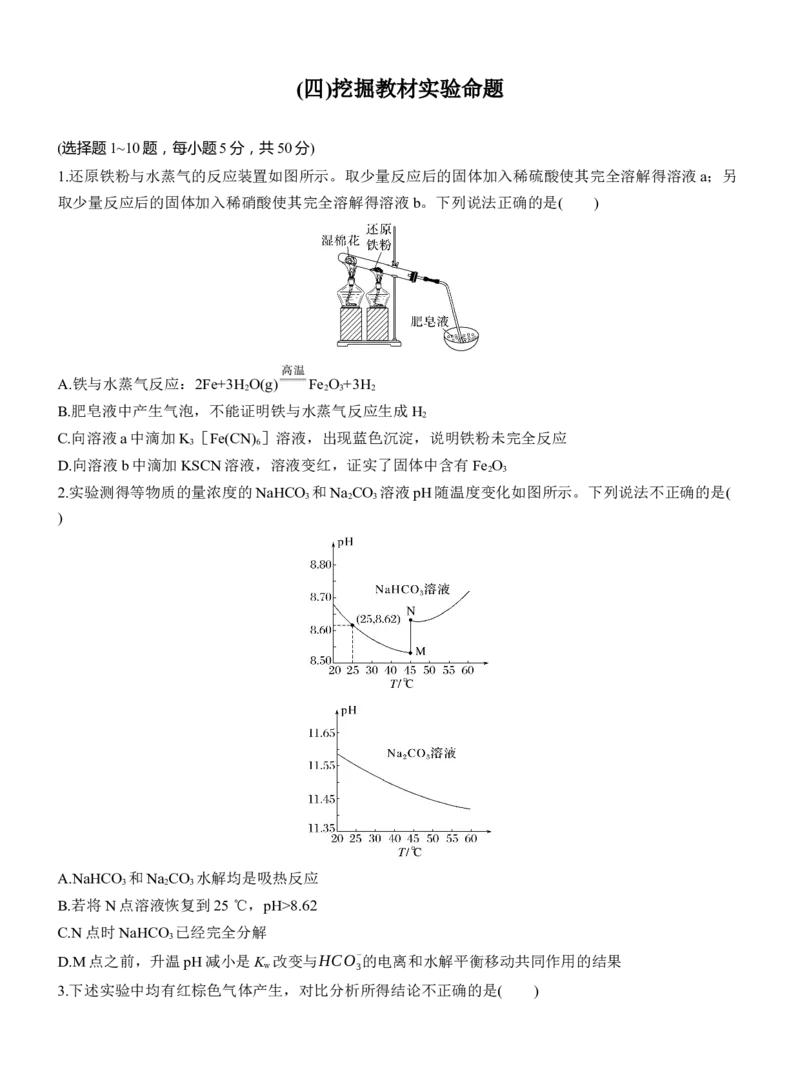
1.还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另
取少量反应后的固体加入稀硝酸使其完全溶解得溶液b。下列说法正确的是( )
A.铁与水蒸气反应:2Fe+3H O(g) Fe O +3H
2 2 3 2
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成H
2
C.向溶液a中滴加K [Fe(CN) ]溶液,出现蓝色沉淀,说明铁粉未完全反应
3 6
D.向溶液b中滴加KSCN溶液,溶液变红,证实了固体中含有Fe O
2 3
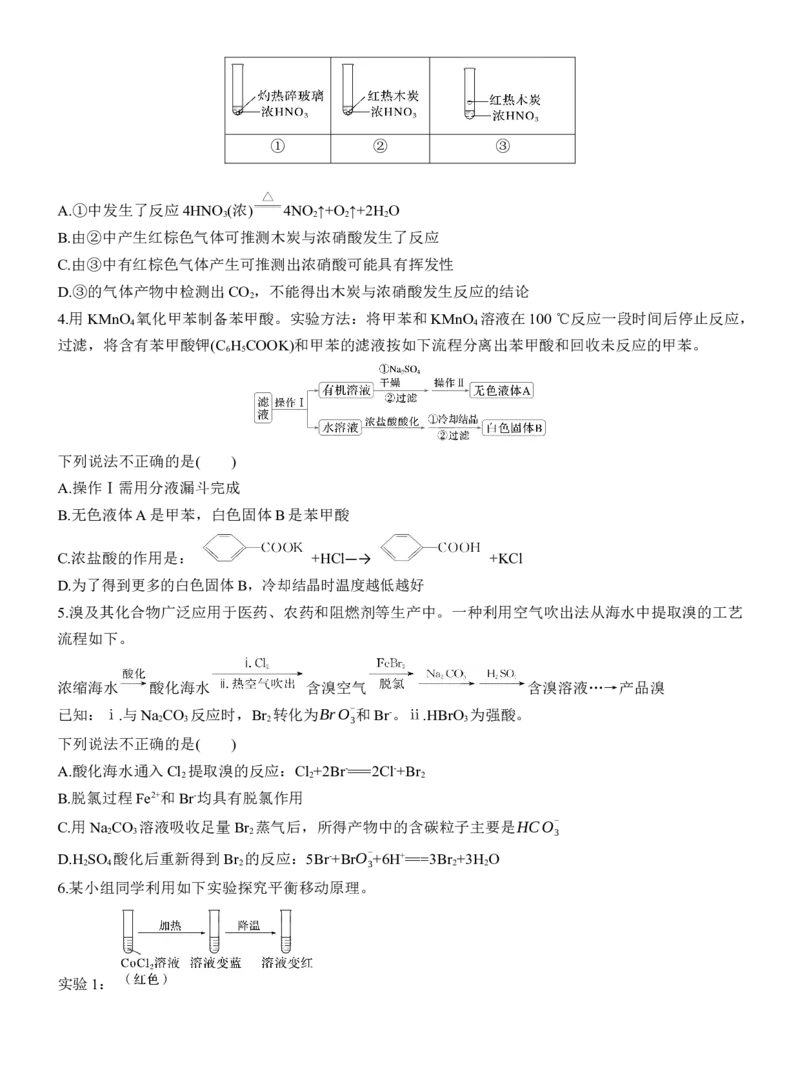
2.实验测得等物质的量浓度的NaHCO 和Na CO 溶液pH随温度变化如图所示。下列说法不正确的是(
3 2 3
)
A.NaHCO 和Na CO 水解均是吸热反应
3 2 3
B.若将N点溶液恢复到25 ℃,pH>8.62
C.N点时NaHCO 已经完全分解
3
D.M点之前,升温pH减小是K
改变与HCO-
的电离和水解平衡移动共同作用的结果
w 3
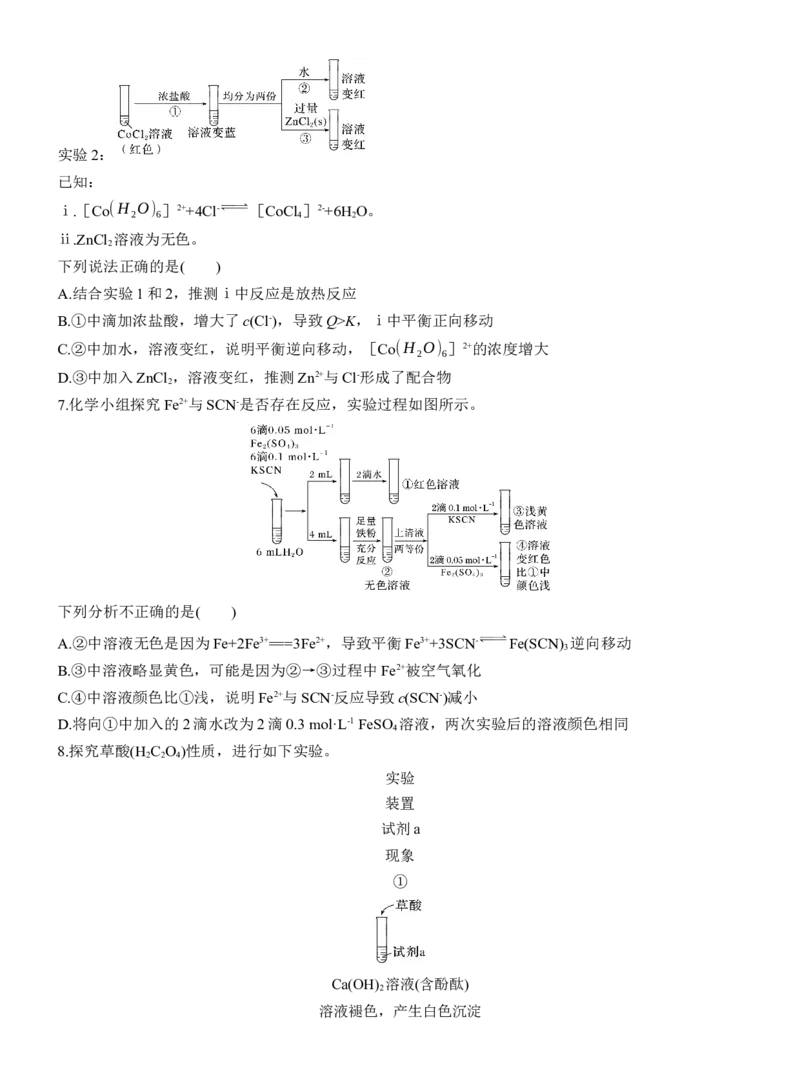
3.下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )① ② ③
A.①中发生了反应4HNO (浓) 4NO ↑+O ↑+2H O
3 2 2 2
B.由②中产生红棕色气体可推测木炭与浓硝酸发生了反应
C.由③中有红棕色气体产生可推测出浓硝酸可能具有挥发性
D.③的气体产物中检测出CO ,不能得出木炭与浓硝酸发生反应的结论
2
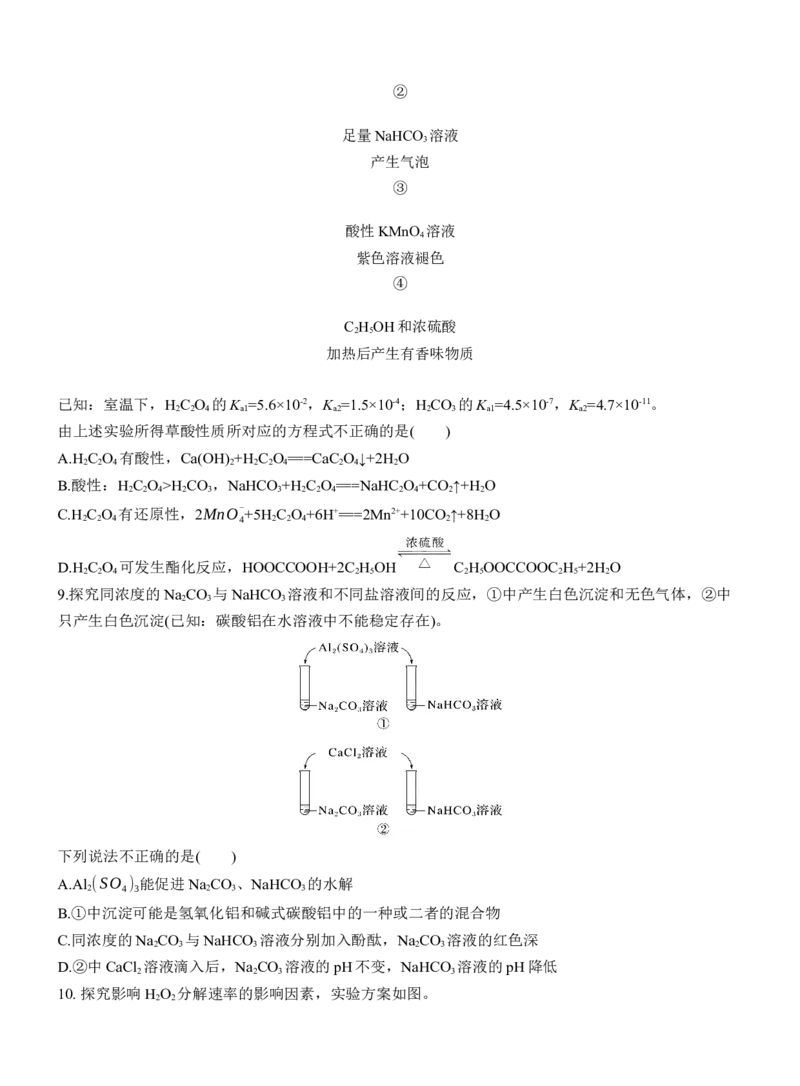
4.用KMnO 氧化甲苯制备苯甲酸。实验方法:将甲苯和KMnO 溶液在100 ℃反应一段时间后停止反应,
4 4
过滤,将含有苯甲酸钾(C H COOK)和甲苯的滤液按如下流程分离出苯甲酸和回收未反应的甲苯。
6 5
下列说法不正确的是( )
A.操作Ⅰ需用分液漏斗完成
B.无色液体A是甲苯,白色固体B是苯甲酸
C.浓盐酸的作用是: +HCl―→ +KCl
D.为了得到更多的白色固体B,冷却结晶时温度越低越好
5.溴及其化合物广泛应用于医药、农药和阻燃剂等生产中。一种利用空气吹出法从海水中提取溴的工艺
流程如下。
浓缩海水 酸化海水 含溴空气 含溴溶液…→产品溴
已知:ⅰ.与Na CO 反应时,Br
转化为BrO-
和Br-。ⅱ.HBrO 为强酸。
2 3 2 3 3
下列说法不正确的是( )
A.酸化海水通入Cl 提取溴的反应:Cl +2Br-===2Cl-+Br
2 2 2
B.脱氯过程Fe2+和Br-均具有脱氯作用
C.用Na CO 溶液吸收足量Br
蒸气后,所得产物中的含碳粒子主要是HCO-
2 3 2 3
D.H SO 酸化后重新得到Br
的反应:5Br-+BrO-
+6H+===3Br +3H O
2 4 2 3 2 2
6.某小组同学利用如下实验探究平衡移动原理。
实验1:实验2:
已知:
ⅰ.[Co(H O) ]2++4Cl- [CoCl ]2-+6H O。
2 6 4 2
ⅱ.ZnCl 溶液为无色。
2
下列说法正确的是( )
A.结合实验1和2,推测ⅰ中反应是放热反应
B.①中滴加浓盐酸,增大了c(Cl-),导致Q>K,ⅰ中平衡正向移动
C.②中加水,溶液变红,说明平衡逆向移动,[Co(H O) ]2+的浓度增大
2 6
D.③中加入ZnCl ,溶液变红,推测Zn2+与Cl-形成了配合物
2
7.化学小组探究Fe2+与SCN-是否存在反应,实验过程如图所示。
下列分析不正确的是( )
A.②中溶液无色是因为Fe+2Fe3+===3Fe2+,导致平衡Fe3++3SCN- Fe(SCN) 逆向移动
3
B.③中溶液略显黄色,可能是因为②→③过程中Fe2+被空气氧化
C.④中溶液颜色比①浅,说明Fe2+与SCN-反应导致c(SCN-)减小
D.将向①中加入的2滴水改为2滴0.3 mol·L-1 FeSO 溶液,两次实验后的溶液颜色相同
4
8.探究草酸(H C O )性质,进行如下实验。
2 2 4
实验
装置
试剂a
现象
①
Ca(OH) 溶液(含酚酞)
2
溶液褪色,产生白色沉淀②
足量NaHCO 溶液
3
产生气泡
③
酸性KMnO 溶液
4
紫色溶液褪色
④
C H OH和浓硫酸
2 5
加热后产生有香味物质
已知:室温下,H C O 的K =5.6×10-2,K =1.5×10-4;H CO 的K =4.5×10-7,K =4.7×10-11。
2 2 4 a1 a2 2 3 a1 a2
由上述实验所得草酸性质所对应的方程式不正确的是( )
A.H C O 有酸性,Ca(OH) +H C O ===CaC O ↓+2H O
2 2 4 2 2 2 4 2 4 2
B.酸性:H C O >H CO ,NaHCO +H C O ===NaHC O +CO ↑+H O
2 2 4 2 3 3 2 2 4 2 4 2 2
C.H C O
有还原性,2MnO-
+5H C O +6H+===2Mn2++10CO ↑+8H O
2 2 4 4 2 2 4 2 2
D.H C O 可发生酯化反应,HOOCCOOH+2C H OH C H OOCCOOC H +2H O
2 2 4 2 5 2 5 2 5 2
9.探究同浓度的Na CO 与NaHCO 溶液和不同盐溶液间的反应,①中产生白色沉淀和无色气体,②中
2 3 3
只产生白色沉淀(已知:碳酸铝在水溶液中不能稳定存在)。
下列说法不正确的是( )
A.Al (SO ) 能促进Na CO 、NaHCO 的水解
2 4 3 2 3 3
B.①中沉淀可能是氢氧化铝和碱式碳酸铝中的一种或二者的混合物
C.同浓度的Na CO 与NaHCO 溶液分别加入酚酞,Na CO 溶液的红色深
2 3 3 2 3
D.②中CaCl 溶液滴入后,Na CO 溶液的pH不变,NaHCO 溶液的pH降低
2 2 3 3
10. 探究影响H O 分解速率的影响因素,实验方案如图。
2 2下列说法不正确的是( )
A.对比①②,可探究FeCl 溶液对H O 分解速率的影响
3 2 2
B.对比②③④,可探究温度对H O 分解速率的影响
2 2
C.H O 是直线形的非极性分子
2 2
D.H O 易溶于水,主要是由于H O 与H O分子之间能形成氢键
2 2 2 2 2答案精析
1.B [Fe与水蒸气反应生成四氧化三铁和氢气,化学方程式为3Fe+4H O(g) Fe O +4H ,故A错误;肥
2 3 4 2
皂液中产生气泡,只能说明有气体生成,但不能说明是氢气,故B正确;若滴加铁氰化钾溶液后出现蓝色
沉淀,说明含有二价铁离子,但不能确定二价铁离子是来自铁粉还是Fe O ,故C错误;若滴加KSCN溶
3 4
液后变红色,说明含三价铁离子,Fe O 也能产生三价铁离子,故D错误。]
3 4
2.C [升高温度部分碳酸氢钠分解为碳酸钠,则将N点溶液恢复到25 ℃,混合液pH>8.62,故B正确;若
N点NaHCO 已经完全分解,则碳酸钠溶液在45 ℃时的pH约为11.45,与碳酸氢钠溶液的pH不符,故C
3
错误;升温,K
增大,同时促进了HCO-
的电离和水解,M点之前,升温pH减小是K
改变与HCO-
的电
w 3 w 3
离和水解平衡移动共同作用的结果,故D正确。]
3.B [浓硝酸受热易分解,故①中发生的反应为4HNO (浓) 4NO ↑+O ↑+2H O,A正确;红热木炭会
3 2 2 2
使浓硝酸受热分解生成二氧化氮、氧气和水,则产生红棕色气体不能表明②中木炭与浓硝酸发生了反应,
B错误;红热木炭可与空气中的氧气反应生成二氧化碳,则③的气体产物中检测出二氧化碳不能说明木炭
一定与浓硝酸发生了反应,D正确。]
4.D [将含有苯甲酸钾(C H COOK)和甲苯的滤液分液得到有机溶液和水溶液,水溶液中加入浓盐酸生成苯
6 5
甲酸,冷却结晶后过滤得到苯甲酸晶体,有机溶液中加入硫酸钠干燥后过滤,然后分液得到甲苯。操作Ⅰ
分离出有机溶液和水溶液,操作方法为分液,需要用分液漏斗完成,故A正确;根据分析可知,无色液体
A为甲苯,白色固体B为苯甲酸,故B正确;根据强酸制取弱酸原理,加入浓盐酸将 转化
成溶解度较小的苯甲酸,发生反应为 +HCl +KCl,故C正确;温度太低
杂质溶解度降低,可析出杂质,导致产物不纯,故D错误。]
5.C [浓缩海水酸化形成酸化海水,通入氯气将溴离子氧化为溴单质,再用热空气吹出生成的单质溴,含
溴空气通过溴化亚铁脱氯,通入碳酸钠吸收Br
转化为BrO- 和Br-,BrO-
和Br-在稀硫酸中发生氧化还原反
2 3 3
应生成溴单质形成含溴溶液,最后得到产品溴。酸化海水通入氯气,氯气与溴离子反应生成Br 和Cl-,A
2
正确;脱氯过程中,亚铁离子和溴离子均能与氯气反应,两者均具有脱氯作用,B正确;用碳酸钠溶液吸
收足量溴蒸气后,发生反应3Br
+3CO2- ===5Br-+BrO-
+3CO ↑,所得产物中的含碳粒子主要为CO ,C错
2 3 3 2 2
误;硫酸酸化后,BrO-
、Br-和氢离子反应生成Br 和水,D正确。]
3 2
6.D [由实验1,降温平衡逆向移动,逆向为放热方向,正向为吸热反应,A错误;①中滴加浓盐酸,增
大了c(Cl-),导致QHC
O-
>H CO ,则反应方程式为
2 2 4 2 4 2 3
2NaHCO +H C O ===Na C O +2CO ↑+2H O,故B项错误;酸性KMnO 溶液具有强氧化性,向酸性
3 2 2 4 2 2 4 2 2 4
KMnO 溶液中加入草酸,溶液褪色,说明草酸将酸性KMnO 溶液还原,体现草酸的还原性,则离子方程
4 4
式为2MnO-
+5H C O +6H+===2Mn2++10CO ↑+8H O,故C项正确;酯具有香味,CH CH OH和浓硫酸中
4 2 2 4 2 2 3 2
加入草酸加热后有香味物质生成,说明有酯生成,所以草酸可以发生酯化反应,对应的化学方程式为
HOOCCOOH+2C H OH C H OOCCOOC H +2H O,故D项正确。]
2 5 2 5 2 5 2
9.D [铝离子水解呈酸性,碳酸根离子和碳酸氢根离子水解呈碱性,硫酸铝能促进碳酸钠和碳酸氢钠的水
解,A正确;①中铝离子水解生成氢氧化铝,也可以与碳酸根离子结合生成碱式碳酸铝沉淀,B正确;同
浓度的碳酸钠和碳酸氢钠溶液中,碳酸根离子水解程度更大,碱性更强,加入酚酞试剂红色更深,C正确;
氯化钙和碳酸钠生成碳酸钙沉淀,碳酸根离子浓度减小,使CO2-
+H O
HCO-
+OH-平衡逆向移动,OH-
3 2 3
浓度减小,pH变小,D错误。]
10.C [H O 的分子结构不对称,为极性分子,C不正确。]
2 2