文档内容
【基础知识】有机物的结构与命名
考点四 研究有机物的一般步骤与方法
【必备知识】
一、研究有机物的基础步骤
二、常见官能团特征反应及有机物的分离提纯
1、常见官能团特征反应
化学方法 可能的官能团名称
①向某烃样品中滴加溴的四氯化碳溶液,红棕色褪去 碳碳双键或碳碳三键
②向某烃样品中滴加酸性KMnO 溶液,紫色褪去 碳碳双键或碳碳三键
4
③向某有机物样品中加入NaOH溶液,并加热、振荡,加入足量稀
碳溴键
硝酸,再加AgNO 溶液,产生淡黄色沉淀
3
④向某有机物样品中加入金属钠,有无色无味气体放出 羟基或羧基
⑤向某有机物样品中加入足量饱和溴水,有白色沉淀产生 酚羟基
⑥向某有机物样品中滴加FeCl 溶液,溶液显紫色 酚羟基
3
⑦将某有机物样品滴加到银氨溶液中,水浴加热,产生光亮的银镜 醛基
⑧将某有机物样品滴加到新制的氢氧化铜中,加热产生砖红色沉淀 醛基
⑨向某有机物样品中滴加NaHCO 溶液,有无色无味气体放出 羧基
3
2、常见有机物的分离提纯
有机物分离常见方法:蒸馏和重结晶、萃取和分液。
写出以下物质除杂时需要添加的试剂
方法 混合物 外加试剂
乙烷(乙烯) 溴的四氯化碳溶液
洗气
乙炔(硫化氢) 氢氧化钠溶液或硫酸铜溶液
乙酸乙酯(乙酸) 饱和碳酸钠溶液
溴苯(溴) 氢氧化钠溶液
分液 硝基苯(硝酸、硫酸) 氢氧化钠溶液
苯(苯甲酸) 氢氧化钠溶液
苯(苯酚) 氢氧化钠溶液
乙醇(水) 生石灰
蒸馏
乙醛(乙酸) 生石灰
三、分析方法:
(1)燃烧法、元素分析法:确定元素组成
(2)红外光谱法:测键种类,确定官能团。
分子中的化学键或官能团可对红外线发生振动吸收,不同的化学键或官能团吸收频率不同。
(3)核磁共振氢谱:确定不同化学环境的氢原子
等效氢种类=吸收峰的 个数 ;每种个数=与吸收峰的面积成 正比 。
(4) 质谱法:
质荷比(分子离子、碎片离子的相对质量与其电荷的比值)最大值即为该有机物的相对分子质量。
其他求相对分子质量的方法:①根据标准状况下气体的密度ρ:M= ρVm 。
②根据气体的相对密度:=D。
m
③根据物质的质量(m)和物质的量(n):M= 。
n
mN
④根据一定质量(m)的物质中微粒数目(N)和阿伏加德罗常数(N ):M= A 。
A N
(5)X射线衍射图:经过计算可获得分子结构的有关数据,如键长、键角等,用于有机化合物晶体结构的测
定
例1、将一定量的有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H O和8.8 g CO ,消耗氧气6.72
2 2
L(标准状况下),则该物质的实验式是_C HO_。
2 6
例2、(2023 全国乙卷)元素分析是有机化合物的表征手段之一。按下图实验装置(部分装置略)对有机化
合物进行C、H元素分析。
回答下列问题:
(1)将装有样品的Pt坩埚和CuO放入石英管中,先___________,而后将已称重的U型管c、d与石英管连
接,检查_______________。依次点燃煤气灯_______________,进行实验。
(2)O 的作用有_______。CuO的作用是_______________(举1例,用化学方程式表示)。
2
(3)c和d中的试剂分别是_______________、_______________(填标号)。
c和d中的试剂不可调换,理由是___________________________。
A.CaCl B.NaCl C.碱石灰(CaO+NaOH) D.NaSO
2 2 3
(4)Pt坩埚中样品CxHyOz反应完全后,应进行操作:___________________。取下c和d管称重。
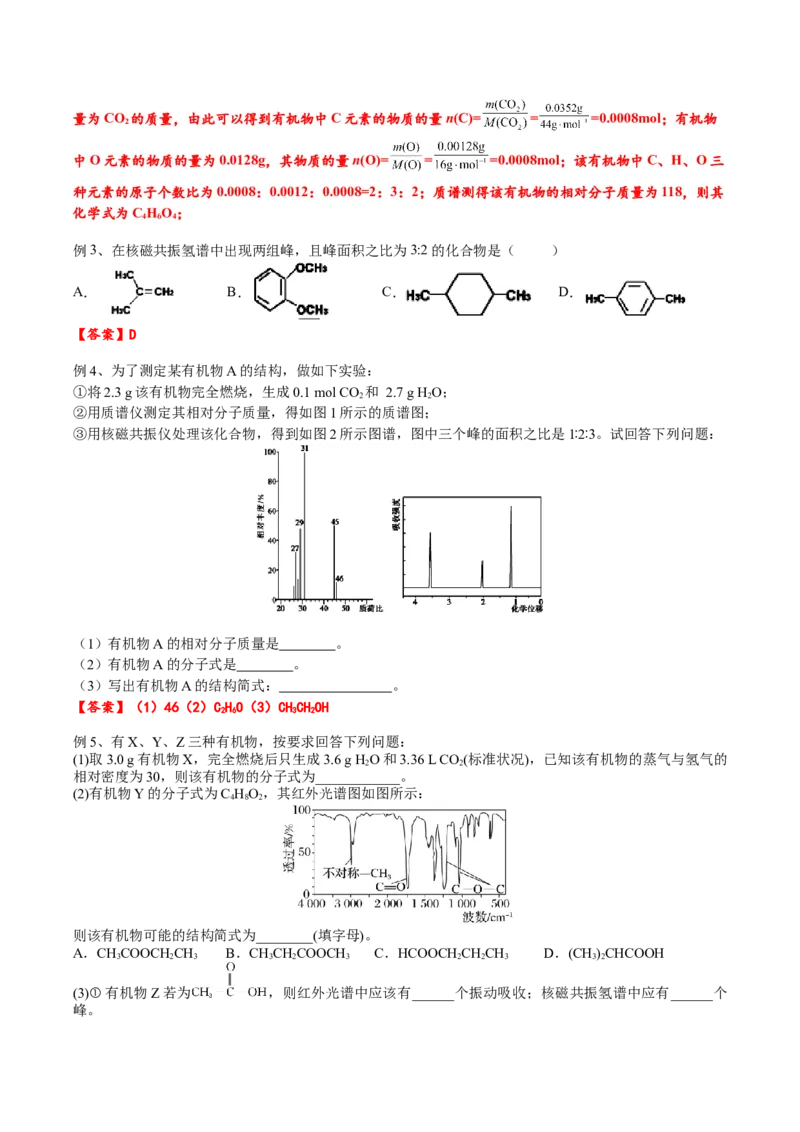
(5)若样品CxHyOz为0.0236g,实验结束后,c管增重0.0108g,d管增重0.0352g。质谱测得该有机物的相
对分子量为118,其分子式为_______________。
【答案】(1)通入一定的O 装置气密性 b、a (2)为实验提供氧化剂、提供气流保证反应产物完
2
全进入到U型管中 CO+CuO Cu+CO (3)A C 碱石灰可以同时吸收水蒸气和二氧化碳
2
(4)继续吹入一定量的O,冷却装置 (5)C HO
2 4 6 4
【解析】(1)实验前,应先通入一定的O 吹空石英管中的杂质气体,保证没有其他产物生成,而后将已
2
U型管c、d与石英管连接,检查装置气密性,随后先点燃b处酒精灯后点燃a处酒精灯,保证当a处发生
反应时产生的CO能被CuO反应生成CO
2
(2)实验中O 的作用有:为实验提供氧化剂、提供气流保证反应产物完全进入到U型管中;CuO的作用
2
是催化a处产生的CO,使CO反应为CO 。
2
(3)有机物燃烧后生成的CO 和HO分别用碱石灰和无水CaCl 吸收,其中c管装有无水CaCl ,d管装
2 2 2 2
有碱石灰,二者不可调换,因为碱石灰能同时吸收水蒸气和二氧化碳,影响最后分子式的确定。
(4)反应完全以后应继续吹入一定量的O,保证石英管中的气体产物完全吹入两U行管中,使装置冷却。
2
(5)c管装有无水CaCl ,用来吸收生成的水蒸气,则增重量为水蒸气的质量,由此可以得到有机物中H
2
元素的物质的量n(H)= = =0.0012mol;d管装有碱石灰,用来吸收生成的CO ,则增重
2量为CO 的质量,由此可以得到有机物中C元素的物质的量n(C)= = =0.0008mol;有机物
2
中O元素的物质的量为0.0128g,其物质的量n(O)= = =0.0008mol;该有机物中C、H、O三
种元素的原子个数比为0.0008:0.0012:0.0008=2:3:2;质谱测得该有机物的相对分子质量为118,则其
化学式为CHO;
4 6 4
例3、在核磁共振氢谱中出现两组峰,且峰面积之比为3:2的化合物是( )
A. B. C. D.
【答案】D
例4、为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO 和 2.7 g H O;
2 2
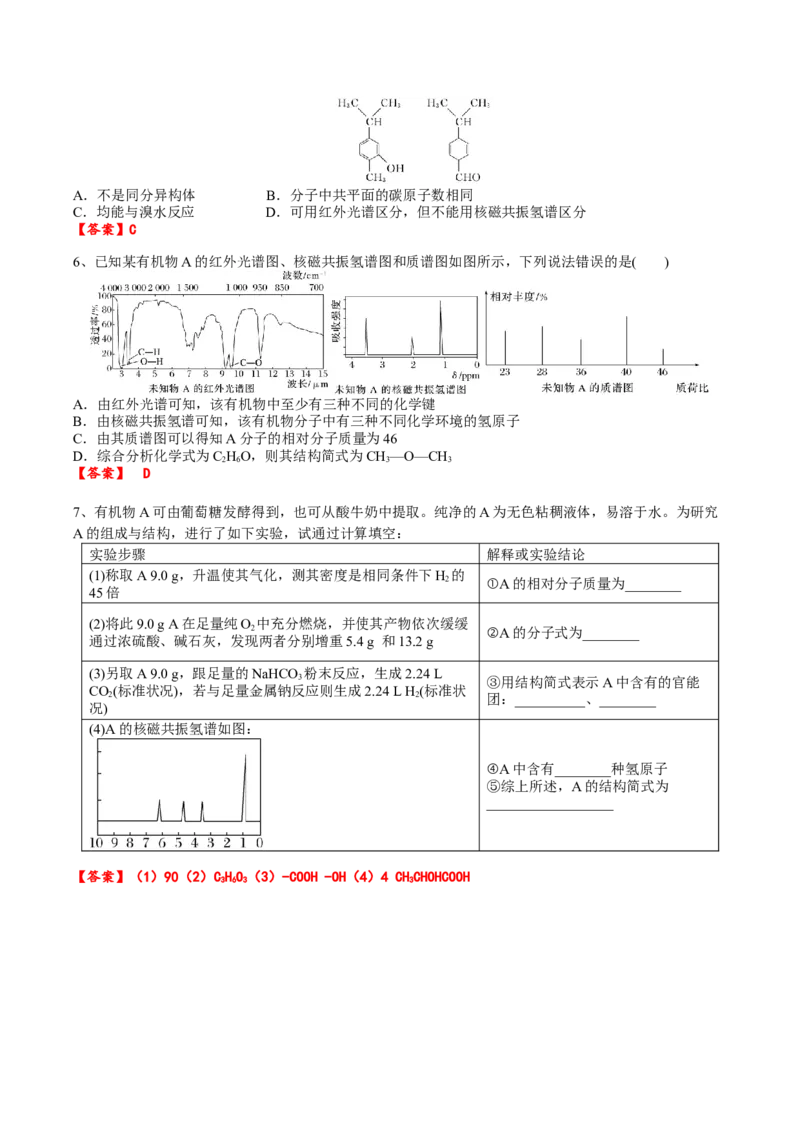
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1∶2∶3。试回答下列问题:
(1)有机物A的相对分子质量是 。
(2)有机物A的分子式是 。
(3)写出有机物A的结构简式: 。
【答案】(1)46(2)CHO(3)CHCHOH
2 6 3 2
例5、有X、Y、Z三种有机物,按要求回答下列问题:
(1)取3.0 g有机物X,完全燃烧后只生成3.6 g H O和3.36 L CO (标准状况),已知该有机物的蒸气与氢气的
2 2
相对密度为30,则该有机物的分子式为____________。
(2)有机物Y的分子式为C HO,其红外光谱图如图所示:
4 8 2
则该有机物可能的结构简式为________(填字母)。
A.CHCOOCH CH B.CHCHCOOCH C.HCOOCH CHCH D.(CH)CHCOOH
3 2 3 3 2 3 2 2 3 3 2
(3)①有机物Z若为 ,则红外光谱中应该有______个振动吸收;核磁共振氢谱中应有______个
峰。②有机物Z若为 ,则红外光谱中应该有_____个振动吸收,核磁共振氢谱中应有______个
峰。
【答案】 (1)CHO (2)AB (3)①5 2 ②3 2
3 8
【易错辨析】
1、有机物完全燃烧后仅生成CO 和HO,则该有机物中一定含有C、H、O三种元素。( )
2 2
2、CHCHOH与CHOCH 互为同分异构体,核磁共振氢谱相同( )
3 2 3 3
3、乙醇是良好的有机溶剂,根据相似相溶原理用乙醇从水溶液中萃取有机物( )
4、用元素分析仪和红外光谱相结合即可确定有机物的结构( )
5、燃烧法可确定有机物的分子结构( )
6、有机化合物 的核磁共振氢谱中会出现三组峰,且峰面积之比为3∶4∶1( )【答案】
1.× 2.× 3.× 4.× 5.× 6.×
【关键能力】
1、下列关于有机物的分离、提纯方法,正确的是( )
A.直接蒸馏乙醇和水的混合物,可以获得无水酒精
B.甲烷中混有乙炔时,可用酸性高锰酸钾溶液洗气
C.用饱和氢氧化钠溶液来除去乙酸乙酯中混有的乙醇和乙酸
D.苯甲酸中混有NaCl时,可用重结晶的方法提纯苯甲酸
【答案】 D
2、为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )
选项 不纯物质 除杂试剂 分离方法
A 苯(甲苯) 酸性KMnO 溶液、NaOH溶液 分液
4
B 溴苯(溴) NaOH溶液 过滤
C 淀粉(葡萄糖) 水 过滤
D 苯(苯酚) 浓溴水 过滤
【答案】 A
3、下列实验中,所采取的分离或提纯方法与对应原理都正确的是( )
选项 实验目的 分离或提纯方法 原理
A 分离溶于水中的碘 乙醇萃取 碘在乙醇中的溶解度较大
B 除去乙醇中的乙酸 加入CaO固体后蒸馏 乙酸转化为难挥发的乙酸钙
C 除去甲烷中的乙烯 通过酸性KMnO 溶液洗气 乙烯与酸性KMnO 溶液反应
4 4
D 除去苯中的苯酚 加入足量浓溴水后过滤 溴与苯酚反应生成三溴苯酚沉淀
【答案】B
4、下列说法正确的是( )
A. 在核磁共振氢谱中有5组吸收峰
B.红外光谱只能确定有机物中所含官能团的种类和数目
C.质谱法不能用于相对分子质量的测定
D.核磁共振氢谱、红外光谱和质谱都可用于分析有机物结构
【答案】 D
5、对下列两种化合物的结构或性质描述正确的是( )A.不是同分异构体 B.分子中共平面的碳原子数相同
C.均能与溴水反应 D.可用红外光谱区分,但不能用核磁共振氢谱区分
【答案】C
6、已知某有机物A的红外光谱图、核磁共振氢谱图和质谱图如图所示,下列说法错误的是( )
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C.由其质谱图可以得知A分子的相对分子质量为46
D.综合分析化学式为C HO,则其结构简式为CH—O—CH
2 6 3 3
【答案】 D
7、有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究
A的组成与结构,进行了如下实验,试通过计算填空:
实验步骤 解释或实验结论
(1)称取A 9.0 g,升温使其气化,测其密度是相同条件下H 的
2 ①A的相对分子质量为________
45倍
(2)将此9.0 g A在足量纯O 中充分燃烧,并使其产物依次缓缓
2 ②A的分子式为________
通过浓硫酸、碱石灰,发现两者分别增重5.4 g 和13.2 g
(3)另取A 9.0 g,跟足量的NaHCO 粉末反应,生成2.24 L
3 ③用结构简式表示A中含有的官能
CO(标准状况),若与足量金属钠反应则生成2.24 L H (标准状
2 2 团:__________、________
况)
(4)A的核磁共振氢谱如图:
④A中含有________种氢原子
⑤综上所述,A的结构简式为
__________________
【答案】(1)90(2)CHO(3)-COOH -OH(4)4 CHCHOHCOOH
3 6 3 39、青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油
醚中可溶解,在水中几乎不溶,熔点为156~157 ℃,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚
沸点为35 ℃。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取
法。乙醚浸取法的主要工艺为
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是____________________________________________。
(2)操作Ⅰ需要的玻璃仪器主要有:烧杯、玻璃棒、____________,操作Ⅱ的名称是
____________________。
(3)操作Ⅲ的主要过程可能是________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
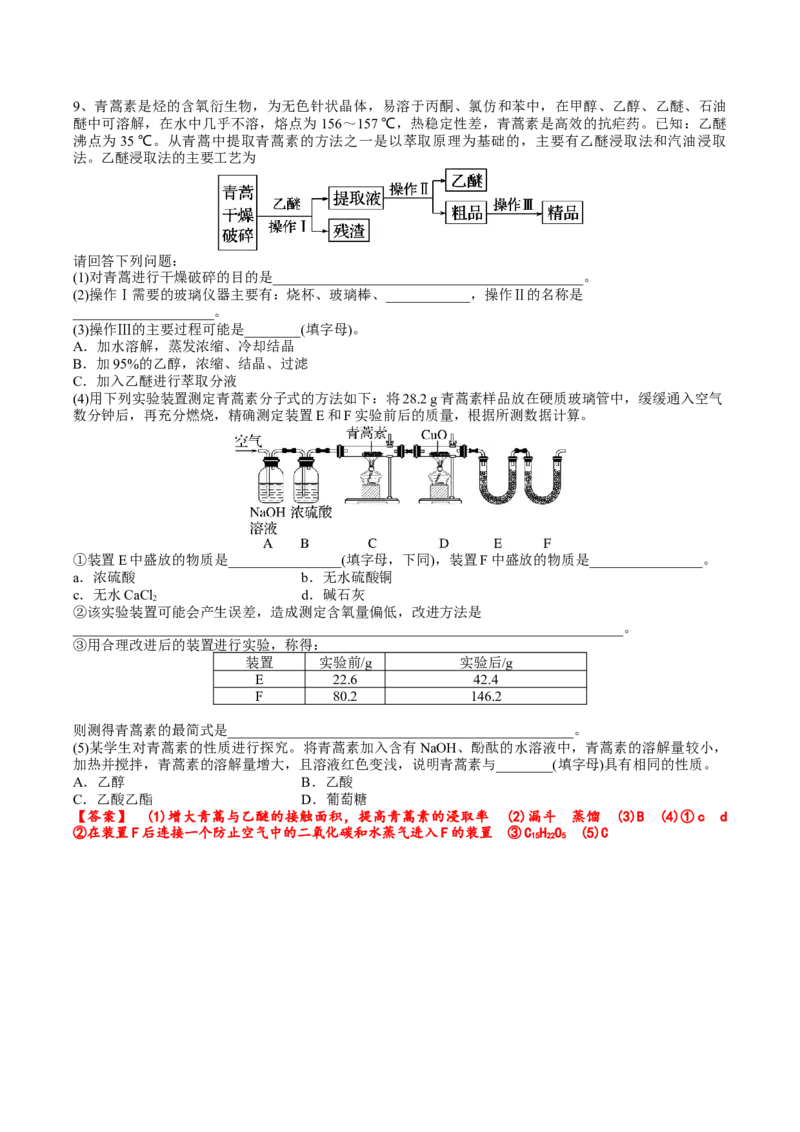
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2 g青蒿素样品放在硬质玻璃管中,缓缓通入空气
数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
①装置E中盛放的物质是________________(填字母,下同),装置F中盛放的物质是________________。
a.浓硫酸 b.无水硫酸铜
c.无水CaCl d.碱石灰
2
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
______________________________________________________________________________。
③用合理改进后的装置进行实验,称得:
装置 实验前/g 实验后/g
E 22.6 42.4
F 80.2 146.2
则测得青蒿素的最简式是_________________________________________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,
加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与________(填字母)具有相同的性质。
A.乙醇 B.乙酸
C.乙酸乙酯 D.葡萄糖
【答案】 (1)增大青蒿与乙醚的接触面积,提高青蒿素的浸取率 (2)漏斗 蒸馏 (3)B (4)①c d
②在装置F后连接一个防止空气中的二氧化碳和水蒸气进入F的装置 ③C H O (5)C
15 22 5