文档内容
第3讲 盐类的水解
[考纲要求]
1.了解盐类水解的原理。
2.了解影响盐类水解程度的主要因素。
3.了解水解常数及有关计算。
4.了解盐类水解的应用。
考点一 盐类的水解
1知识梳理
1.概念:在溶液中盐电离出来的离子跟 产生的H+或OH-结合生成 的反
应。
2.盐类水解的实质
3.盐类水解的特点
(1)水解反应是 反应
(2)水解反应是 反应的逆反应,是 反应
(3)水解反应程度很微弱
4.盐类水解的类型
盐的 是否 水解的 溶液的 溶液
实例
类型 水解 离子 酸碱性 的pH
强酸
NaCl、KNO
3
强碱盐
强酸 NHCl、
4
弱碱盐 Cu(NO)
3 2
弱酸 CHCOONa、
3
强碱盐 NaCO
2 3
5.水解方程式的书写
(1)多元弱酸盐水解:分步进行,以第一步为主,一般只写第一步水解方程式。如NaCO 的水解离子方程式为 。
2 3
(2)多元弱碱盐水解:水解离子方程式一步写完。
如FeCl 的水解离子方程式为 。
3
(3)阴、阳离子相互促进的水解:水解程度较大,书写时要用“===”“↑”“↓”
等。
如NaS溶液与AlCl 溶液混合反应的水解离子方程式为
2 3
________________________________________________________________________。
[思考]
(1)25 ℃时,相同物质的量浓度的下列溶液中:
①NaCl ② NaOH ③ HSO ④(NH ) SO ,其中水的电离程度由大到小顺序
2 4 4 2 4
________________________________________________________________________。
(2)物质的量浓度相同的NaOH溶液与盐酸溶液中,水的电离程度 ;常温下,
pH=5的NHCl溶液与pH=9的CHCOONa溶液中,水的电离程度 。(均填“前者大”
4 3
“后者大”或“相同”)
[判断] (正确的打“√”,错误的打“×”)
(1)酸式盐溶液一定呈酸性( )
(2)能水解的盐溶液一定呈酸性或碱性,不可能呈中性( )
(3)NaCO 溶液显碱性的原因:CO2− +2HO HCO+2OH-( )
2 3 3 2 ⇌ 2 3
(4)向NaAlO 溶液中滴加NaHCO 溶液,有沉淀和气体生成( )
2 3
(5)NaCO 溶液中加入少量Ca(OH)
固体,CO2−
水解程度减小,pH减小( )
2 3 2 3
(6)常温下,pH=11的CHCOONa溶液和pH=3的CHCOOH溶液,水的电离程度相同(
3 3
)
[提醒]
(1)盐类水解的规律可以简记为:,有弱才水解,越弱越水解,谁强显谁性,同强显
中性。
(2)盐类水解方程式书写的一般要求,一般盐类水,解程度很小如NHCl的水解离子方程式为NH+
+HO NH·HO+H+。
4 4 2 ⇌ 3 2
2对点速练
练点一 盐类的水解反应理解判断
1.在盐类发生水解的过程中,正确的说法是( )
A.盐的电离平衡被破坏
B.水的电离程度逐渐增大
C.溶液的pH发生了较大改变
D.水解后溶液一定呈酸性或碱性
2.下列有关盐类水解的叙述中正确的是( )
A.溶液呈中性的盐一定是强酸与强碱生成的盐
B.含有弱酸根离子的盐的水溶液一定呈碱性
C.盐溶液的酸碱性主要取决于形成盐的酸和碱的相对强弱
D.强酸强碱盐的水溶液一定呈中性
3.(1)物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,若它们的pH依次为8、
9、10,则HX、HY、 HZ的酸性由强到弱的排列顺序是 。
(2)室温下 0.1 mol/L的NHCN溶液的pH等于9.32,该溶液中 CN-的水解程度
4
NH+
的水解程度(填“大于”“小于”或“等于”)。
4
规律技巧
弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,溶液显碱性。如NaHCO 溶液中:HC H++C (次
3 O−⇌ O2−
3 3
要),HC +HO HCO+OH-(主要)。
O− 2 ⇌ 2 3
3
②若电离程度大于水解程度,溶液显酸性。如NaHSO 溶液中:HS H++S (主
3 O−⇌ O2−
3 3
要),HS +HO HSO+OH-(次要)。
O− 2 ⇌ 2 3
3
练点二 盐类水解方程式的书写
4.下列反应不属于水解反应或水解方程式不正确的是( )①HCN+HO HO++CN-
2 ⇌ 3
②AlCl+3HO===Al(OH)+3HCl
3 2 3
③NaCO+2HO HCO+2NaOH
2 3 2 ⇌ 2 3
④碳酸氢钠溶液:HC +HO C +HO+
O− 2 ⇌ O2− 3
3 3
⑤NHCl溶于DO中:N +DO NH·DO+H+
4 2 H+ 2 ⇌ 3 2
4
A.①②③④ B.①②③
C.②③⑤ D.全部
5.按要求书写离子方程式
( 1 ) AlCl 溶 液 呈 酸 性
3
________________________________________________________________________。
( 2 ) NaCO 溶 液 呈 碱 性
2 3
________________________________________________________________________、
________________________________________________________________________。
( 3 ) 将 NaHCO 溶 液 与 AlCl 溶 液 混 合
3 3
________________________________________________________________________
________________________________________________________________________。
( 4 ) 实 验 室 制 备 Fe ( OH ) 胶 体
3
________________________________________________________________________。
( 5 ) NaHS 溶 液 呈 碱 性 的 原 因
________________________________________________________________________
________________________________________________________________________。
(6)对于易溶于水的正盐MR 溶液,若pH>7,其原因是
n m
________________________________________________________________________;
若 pH<7 , 其 原 因 是
________________________________________________________________________。
(用离子方程式说明)考点二 影响盐类水解的因素
1知识梳理
1.内因
形成盐对应的酸或碱越 就越易发生水解,当等浓度时,盐溶液的碱性或酸性就越
。
2.外因
(1)温度、浓度
水解程
条件 移动方向 水解产生的离子浓度
度
升高温度
反应 增大
物
减小
浓度
(2)外加物质:
①外加酸碱
水解程度的影响
外加物质
弱酸阴离子 弱碱阳离子
酸
碱
②加能水解的盐
[思考]
以FeCl 水解为例填写下表
3
移动方 H+
条件 pH 现象
向 数
升温 向 颜色
通HCl 向 颜色
加HO 向 颜色
2加NaHCO 向
3
加NHCl 向左 增多 颜色
4
[判断] (正确的打“√”,错误的打“×”)
(1)加热0.1 mol·L-1NaCO 溶液,C 的水解程度和溶液的pH均增大( )
2 3 O2−
3
(2)在滴有酚酞溶液的氨水里,加入NHCl至溶液恰好无色,则此时溶液的pH<7(
4
)
(3)在CHCOONa溶液中加入适量CHCOOH,可使c(Na+)=c(CHCOO-)( )
3 3 3
(4)氯化铵溶液加水稀释时, c(N H+ )的值减小( )
4
c(Cl−
)
(5)降低温度和加水稀释,都会使盐的水解平衡向逆反应方向移动( )
(6)通入适量的HCl气体使FeCl
溶液中c(Fe3+
)增大( )
3
c(Cl−
)
(7)向NaCO 溶液通入CO ,可使水解平衡:C +HO +OH-向正反应方向
2 3 2 O2− 2 ⇌ HCO−
3 3
移动,则溶液pH增大( )
[提醒]
1.稀溶液中,盐的浓度越小,水解程度越大,但由于溶液体积的增大是主要的,故水
解产生的H+或OH-的浓度是减小的,则溶液酸性(或碱性)越弱。
2.相同条件下盐的水解程度
(1)正盐>相应酸式盐,如C > 。
O2− HCO−
3 3
(2)相互促进水解的盐>单独水解的盐>水解相互抑制的盐。如N 的水解:(NH )
H+ 4
4
CO>(NH)SO>(NH)Fe(SO)。
2 3 4 2 4 4 2 4 2
2对点速练
练点一 水解平衡的影响因素及结果
1.在一定条件下,NaCO 溶液中存在水解平衡:C +HO +OH-。下列说法
2 3 O2− 2 ⇌ HCO−
3 3
正确的是( )
A.稀释溶液,促进NaCO 的水解,K增大
2 3 wB.通入CO,平衡向正反应方向移动
2
c(HCO−
)
C.升高温度, 3 减小
c(CO2−
)
3
D.加入NaOH固体,溶液pH减小
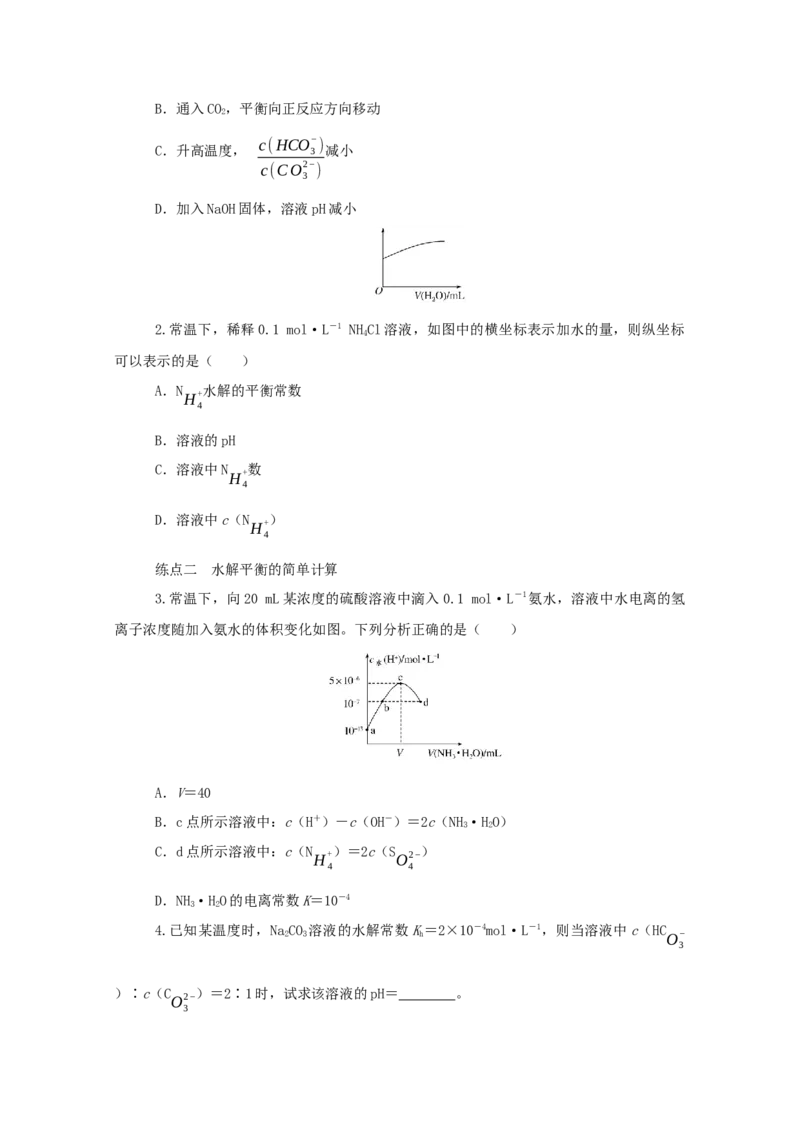
2.常温下,稀释0.1 mol·L-1 NH Cl溶液,如图中的横坐标表示加水的量,则纵坐标
4
可以表示的是( )
A.N 水解的平衡常数
H+
4
B.溶液的pH
C.溶液中N 数
H+
4
D.溶液中c(N )
H+
4
练点二 水解平衡的简单计算
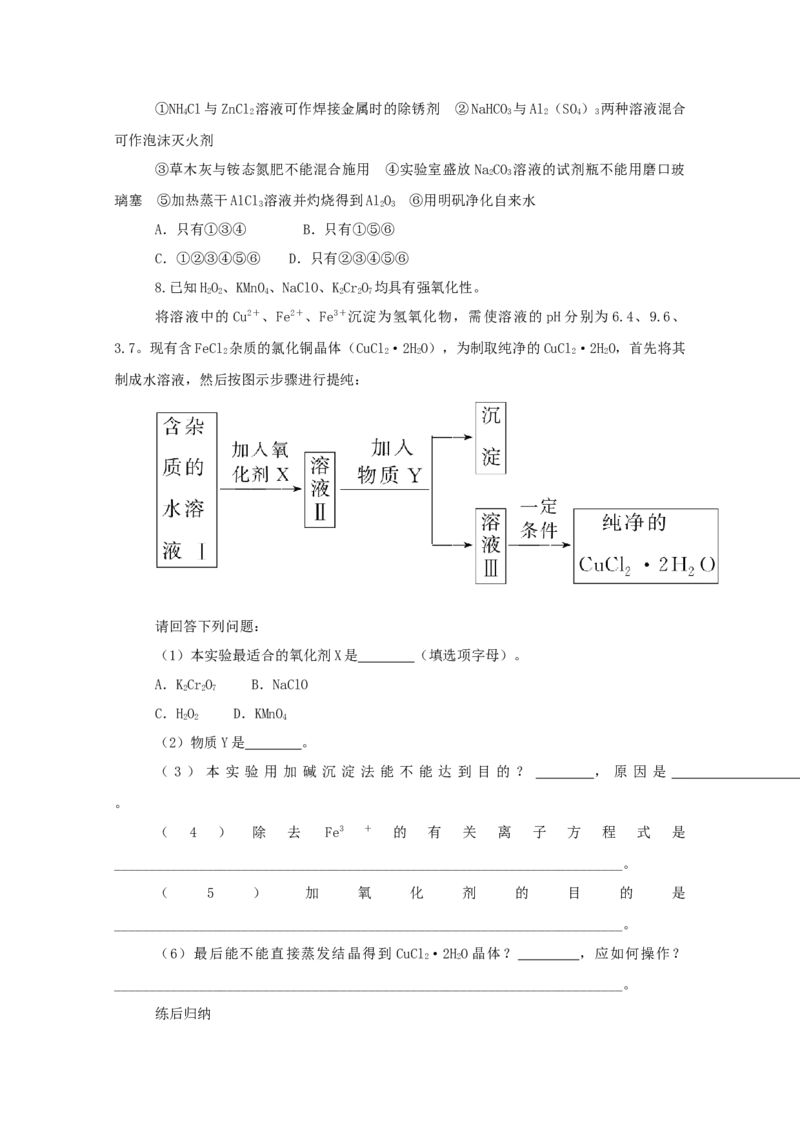
3.常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢
离子浓度随加入氨水的体积变化如图。下列分析正确的是( )
A.V=40
B.c点所示溶液中:c(H+)-c(OH-)=2c(NH·HO)
3 2
C.d点所示溶液中:c(N )=2c(S )
H+ O2−
4 4
D.NH·HO的电离常数K=10-4
3 2
4.已知某温度时,NaCO 溶液的水解常数K=2×10-4mol·L-1,则当溶液中c(HC
2 3 h O−
3
)∶c(C )=2∶1时,试求该溶液的pH= 。
O2−
35.25 ℃时, HS +H+的电离常数K=1× 10-2,则该温度下NaHSO 水解反应的
⇌ O− a 3
3
c(H SO )
平衡常数K h = ,若向 NaHSO 3 溶液中加入少量的 I 2 ,则溶液中 2 3 将
c(HSO−
)
3
(填“增大”“减小”或“不变”)。
方法总结
水解常数与电离常数的关系
MA 表示强碱弱酸盐,则 A-水解的离子方程式为 A-+HO HA+OH-,K=
2 ⇌ h
c(HA)·c(OH− )= c(HA)·c(H+ )·c(OH− )= K w(K
a
为HA的电离常数)由于HA电离出
c(A− ) c(A−)·c(H+ ) K
a
c2 (H+
)
的A-与H+浓度近似相等,平衡时c(HA)又可看成是HA溶液的浓度c,则K= ,c
a
c
(H+)= mol·L-1。
√c·K
a
同理:强酸弱碱盐(如NHCl)的水解常数与弱碱电离常数(K)之间的关系:K=K
4 b h w
K
b
。
练点三 盐类水解的应用
6.下列说法不正确的是( )
A.明矾能水解生成Al(OH) 胶体,可用作净水剂
3
B.水解反应N +HO NH·HO+H+达到平衡后,升高温度平衡逆向移动
H+ 2 ⇌ 3 2
4
C.制备AlCl、FeCl、CuCl 均不能采用将溶液直接蒸干的方法
3 3 2
D.盐类水解反应的逆反应是中和反应
7.下列有关问题与盐的水解有关的是( )①NHCl与ZnCl 溶液可作焊接金属时的除锈剂 ②NaHCO 与Al (SO ) 两种溶液混合
4 2 3 2 4 3
可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用 ④实验室盛放 NaCO 溶液的试剂瓶不能用磨口玻
2 3
璃塞 ⑤加热蒸干AlCl 溶液并灼烧得到AlO ⑥用明矾净化自来水
3 2 3
A.只有①③④ B.只有①⑤⑥
C.①②③④⑤⑥ D.只有②③④⑤⑥
8.已知HO、KMnO、NaClO、KCrO 均具有强氧化性。
2 2 4 2 2 7
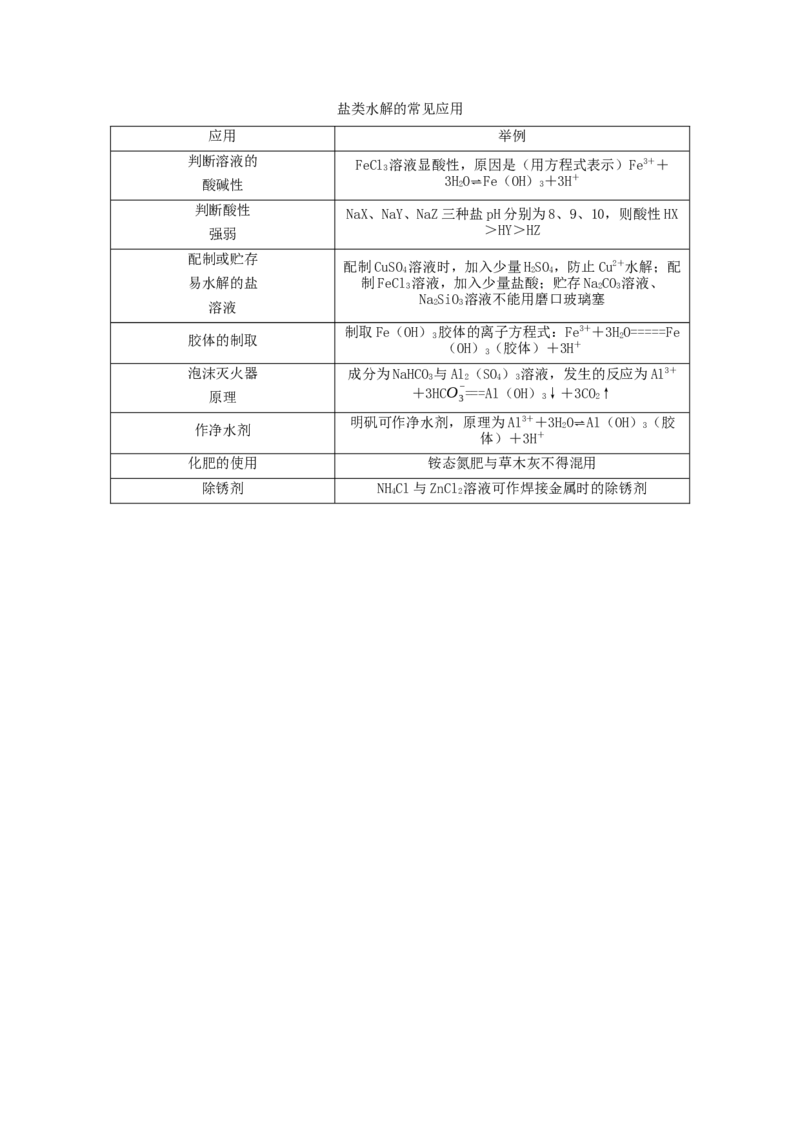
将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需使溶液的pH分别为6.4、9.6、
3.7。现有含FeCl 杂质的氯化铜晶体(CuCl·2HO),为制取纯净的CuCl·2HO,首先将其
2 2 2 2 2
制成水溶液,然后按图示步骤进行提纯:
请回答下列问题:
(1)本实验最适合的氧化剂X是 (填选项字母)。
A.KCrO B.NaClO
2 2 7
C.HO D.KMnO
2 2 4
(2)物质Y是 。
( 3 ) 本 实 验 用 加 碱 沉 淀 法 能 不 能 达 到 目 的 ? , 原 因 是
。
( 4 ) 除 去 Fe3 + 的 有 关 离 子 方 程 式 是
________________________________________________________________________。
( 5 ) 加 氧 化 剂 的 目 的 是
________________________________________________________________________。
(6)最后能不能直接蒸发结晶得到 CuCl·2HO晶体? ,应如何操作?
2 2
________________________________________________________________________。
练后归纳盐类水解的常见应用
应用 举例
判断溶液的 FeCl 溶液显酸性,原因是(用方程式表示)Fe3++
3
酸碱性 3H 2 O ⇌ Fe(OH) 3 +3H+
判断酸性 NaX、NaY、NaZ三种盐pH分别为8、9、10,则酸性HX
强弱 >HY>HZ
配制或贮存
配制CuSO 溶液时,加入少量HSO,防止Cu2+水解;配
4 2 4
易水解的盐 制FeCl 溶液,加入少量盐酸;贮存NaCO 溶液、
3 2 3
NaSiO 溶液不能用磨口玻璃塞
溶液 2 3
制取Fe(OH) 胶体的离子方程式:Fe3++3HO=====Fe
胶体的制取 3 2
(OH)(胶体)+3H+
3
泡沫灭火器 成分为NaHCO 与Al(SO) 溶液,发生的反应为Al3+
3 2 4 3
+3HCO−
===Al(OH)↓+3CO↑
原理 3 3 2
明矾可作净水剂,原理为Al3++3HO Al(OH)(胶
作净水剂 2 ⇌ 3
体)+3H+
化肥的使用 铵态氮肥与草木灰不得混用
除锈剂 NHCl与ZnCl 溶液可作焊接金属时的除锈剂
4 2本讲真题研练
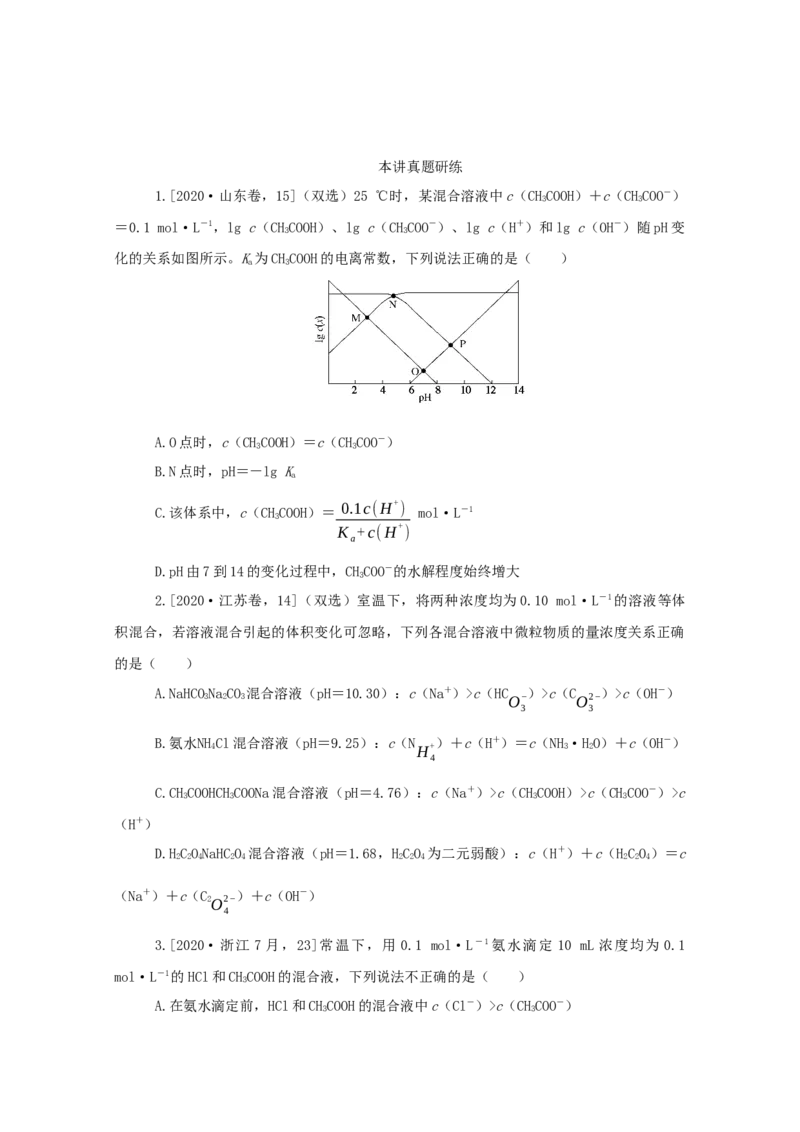
1.[2020·山东卷,15](双选)25 ℃时,某混合溶液中c(CHCOOH)+c(CHCOO-)
3 3
=0.1 mol·L-1,lg c(CHCOOH)、lg c(CHCOO-)、lg c(H+)和lg c(OH-)随pH变
3 3
化的关系如图所示。K为CHCOOH的电离常数,下列说法正确的是( )
a 3
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,pH=-lg K
a
C.该体系中,c(CHCOOH)=
0.1c(H+
) mol·L-1
3
K +c(H+ )
a
D.pH由7到14的变化过程中,CHCOO-的水解程度始终增大
3
2.[2020·江苏卷,14](双选)室温下,将两种浓度均为0.10 mol·L-1的溶液等体
积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确
的是( )
A.NaHCONaCO 混合溶液(pH=10.30):c(Na+)>c(HC )>c(C )>c(OH-)
3 2 3 O− O2−
3 3
B.氨水NHCl混合溶液(pH=9.25):c(N )+c(H+)=c(NH·HO)+c(OH-)
4 H+ 3 2
4
C.CHCOOHCHCOONa混合溶液(pH=4.76):c(Na+)>c(CHCOOH)>c(CHCOO-)>c
3 3 3 3
(H+)
D.HCONaHCO 混合溶液(pH=1.68,HCO 为二元弱酸):c(H+)+c(HCO )=c
2 2 4 2 4 2 2 4 2 2 4
(Na+)+c(C )+c(OH-)
2O2−
4
3.[2020·浙江 7 月,23]常温下,用 0.1 mol·L-1氨水滴定 10 mL 浓度均为 0.1
mol·L-1的HCl和CHCOOH的混合液,下列说法不正确的是( )
3
A.在氨水滴定前,HCl和CHCOOH的混合液中c(Cl-)>c(CHCOO-)
3 3B.当滴入氨水10 mL时,c(N )+c(NH·HO)=c(CHCOO-)+c(CHCOOH)
H+ 3 2 3 3
4
C.当滴入氨水20 mL时,c(CHCOOH)+c(H+)=c(NH·HO)+c(OH-)
3 3 2
D.当溶液呈中性时,氨水滴入量大于20 mL,c(N )c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水解平
3 4 3
衡移动方向不同
5.[2018·北京卷,11]测定0.1 mol·L-1NaSO 溶液先升温再降温过程中的pH,数据
2 3
如下。
时刻 ① ② ③ ④
温
25 30 40 25
度/℃
9.3
pH 9.66 9.52 9.25
7
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色
2
沉淀多。下列说法不正确的是( )
A.NaSO 溶液中存在水解平衡:S +HO HS +OH-
2 3 O2− 2 ⇌ O−
3 3B.④的pH与①不同,是由于S 浓度减小造成的
O2−
3
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D.①与④的K值相等
w
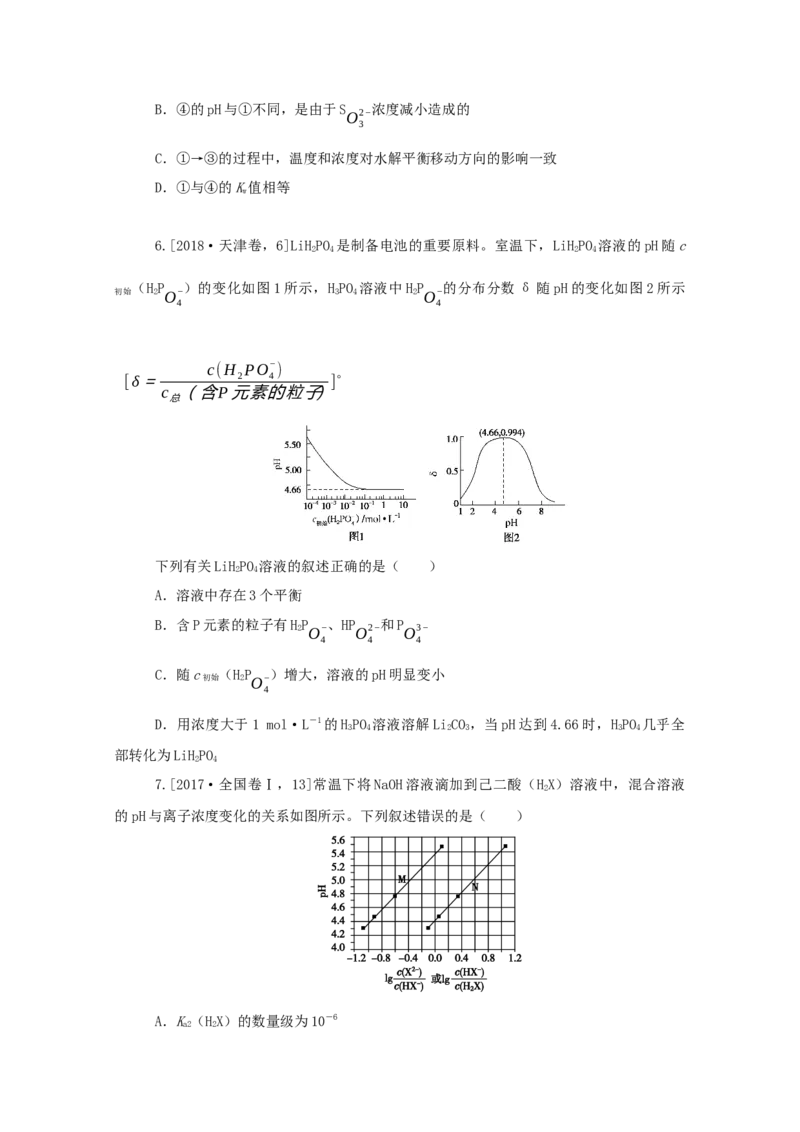
6.[2018·天津卷,6]LiHPO 是制备电池的重要原料。室温下,LiHPO 溶液的pH随c
2 4 2 4
(HP )的变化如图1所示,HPO 溶液中HP 的分布分数δ随pH的变化如图2所示
初始 2 O− 3 4 2 O−
4 4
c(H PO− ) 。
[δ= 2 4 ]
c (含P元素的粒子)
总
下列有关LiHPO 溶液的叙述正确的是( )
2 4
A.溶液中存在3个平衡
B.含P元素的粒子有HP 、HP 和P
2 O− O2− O3−
4 4 4
C.随c (HP )增大,溶液的pH明显变小
初始 2 O−
4
D.用浓度大于1 mol·L-1的HPO 溶液溶解LiCO ,当pH达到4.66时,HPO 几乎全
3 4 2 3 3 4
部转化为LiHPO
2 4
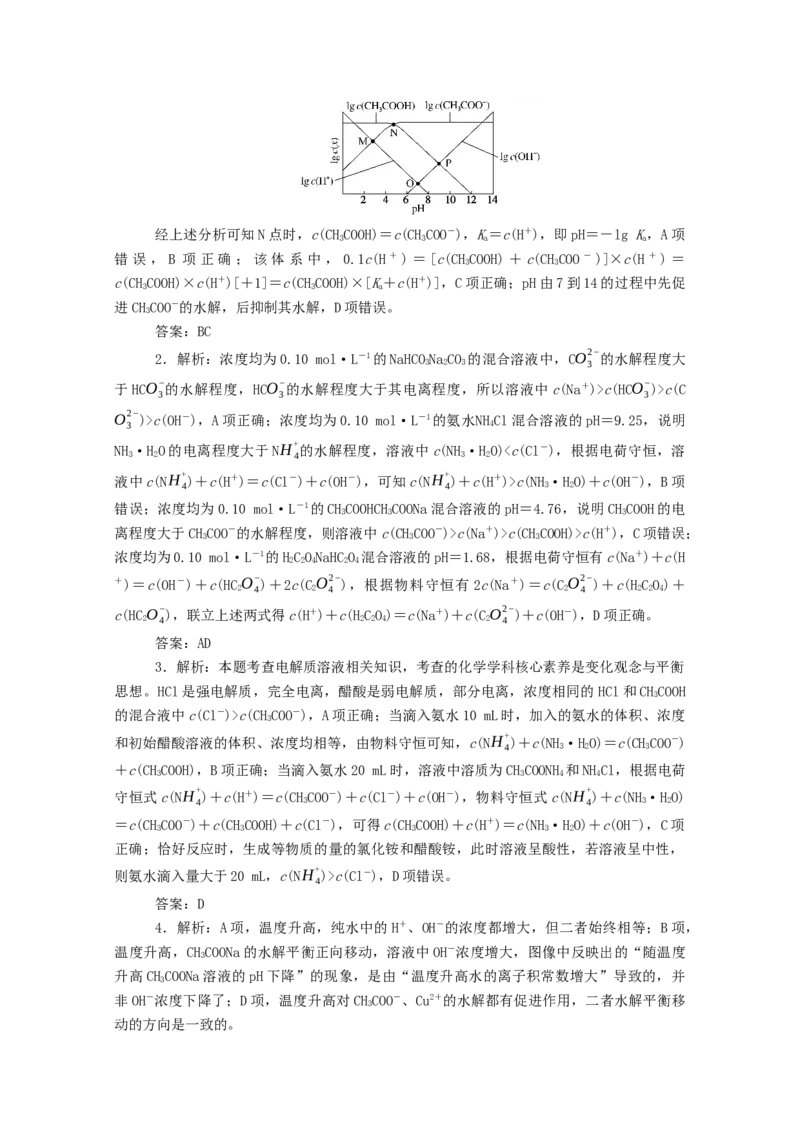
7.[2017·全国卷Ⅰ,13]常温下将NaOH溶液滴加到己二酸(HX)溶液中,混合溶液
2
的pH与离子浓度变化的关系如图所示。下列叙述错误的是( )
A.K(HX)的数量级为10-6
a2 2B.曲线N表示pH与lg c(H X− )的变化关系
c(H X)
2
C.NaHX溶液中c(H+)> c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
第3讲 盐类的水解
考点一
1知识梳理
1.水电离 弱电解质
2.促进
3.(1)可逆 (2)酸碱中和 吸热
4.否 中性 等于7 是 NH+ 、Cu2+ 酸性 小于7 是 CHCOO-、CO2− 碱性
4 3 3
大于7
5.(1)CO2− +HO HCO− +OH- (2)Fe3++3HO Fe(OH) +3H+ (3)2Al3++3S2-+
3 2 ⇌ 3 2 ⇌ 3
6HO===2Al(OH)↓+3HS↑
2 3 2
思考 答案:(1)④>①>②>③ (2)相同 相同
判断 答案:(1)× (2)× (3)× (4)× (5)× (6)×
2对点速练
1.解析:盐类水解是盐电离出的某些离子结合水所电离出的H+或OH-,破坏了水的电
离平衡,促进了水的电离,A错误,B正确;但水解程度是微弱的,故pH改变不大,C错误;
醋酸铵中CHCOO-与NH+
水解程度相同,水解后,溶液仍呈中性,D错误。
3 4
答案:B
2.解析:如果弱酸、弱碱的电离程度相当,生成的盐的水溶液呈中性,如
CHCOONH,A项错误;含有弱酸根离子的盐的水溶液不一定呈碱性,如 NaHSO 溶液呈酸性,B
3 4 3
项错误;强酸强碱盐的水溶液不一定呈中性,例如NaHSO,D项错误。
4
答案:C
3.解析:(1)组成盐的酸根对应的酸越弱,该酸根的水解程度越大,物质的量浓度相
同时该盐溶液的碱性越强,pH越大,则HX、HY、HZ的酸性由强到弱的排列顺序是HX、HY、
HZ。
(2)HCN和NH·HO均是弱电解质,溶液呈碱性,说明CN-的水解程度大于NH+
的水解
3 2 4
程度。
答案:(1)HX、HY、HZ (2)大于
4.解析:①④是电离方程式;②是水解反应方程式,但应用“ ”;③的水解方程式
⇌
错误,应分步进行;⑤应为NH+
+DO NH·HDO+D+。
4 2 ⇌ 3答案:D
5.解析:pH大于7是由于酸根离子水解呈碱性,pH小于7是由于弱碱阳离子水解呈
酸性。
答案:(1)Al3++3HO Al(OH)+3H+
2 ⇌ 3
(2)CO2− +HO HCO− +OH- HCO− +HO HCO+OH-
3 2 ⇌ 3 3 2 ⇌ 2 3
(3)Al3++3HCO−
===Al(OH)↓+3CO↑
3 3 2
(4)Fe3++3HO=====Fe(OH)(胶体)+3H+
2 3
(5)HS-+HO HS+OH-
2 ⇌ 2
(6)Rn-+HO HR(n-1)-+OH-
2 ⇌
Mm++mHO M(OH)+mH+
2 ⇌ m
考点二
1知识梳理
1.弱 强
2.(1)右移 增大 增大 右移 减小 增大 右移 增大 减小 (2)增大 减小
减小 增大 抑制 促进
思考 答案:右 增多 减小 变深 左 增多 减小 变浅 右 增多 增大 变
浅 右 减少 增大 生成红褐色沉淀,放出气体 减小 变浅
判断 答案:(1)√ (2)× (3)√ (4)√ (5)× (6)× (7)×
2对点速练
1.解析:K仅与温度有关,A项错误;CO 通入水中,生成HCO,可以与OH-反应而促
w 2 2 3
c(HCO−
)
3
进平衡正向移动,B项正确;升温,促进NaCO 的水解,平衡正向移动,故 增大,
2 3 c(CO2−
)
3
C项错误;加入NaOH,碱性增强,pH增大,D项错误。
答案:B
2.解析:温度不变,NH+
水解的平衡常数不变,故A项不符合题意;NHCl水解呈酸
4 4
性,加水稀释,水解程度增大,但酸性减弱,溶液的
pH将增大,溶液中NH+
数将减少,c(N
4
H+
)也减小,故B项符合题意,C、D项不符合题意。
4
答案:B
3.解析:(NH)SO 发生水解促进水的电离,因此c点表示硫酸与氨水恰好反应,a点
4 2 4
c (H+)=10-13 mol·L-1,硫酸溶液中c(H+)=0.1 mol·L-1,再根据硫酸溶液的体积和氨
水
水的物质的量浓度可计算出V=20 mL,A项错误;c点表示(NH)SO 溶液,其质子守恒式为
4 2 4
c(H+)-c(OH-)=c(NH·HO),B项错误;因为d点所示溶液呈中性,根据电荷守恒,c(NH)
3 2
=2c(SO2−
),C项正确;因为d点所示的中性溶液体积无法确定,所以不能求出NH·HO的
4 3 2
电离常数,D项错误。
答案:C4.解析:K==2×10-4,
h
又c(HCO− ):c(CO2− )=2:1,则c(OH-)=10-4mol·L-1,结合K=1.0×10-14,可得
3 3 w
c(H+)=10-10mol·L-1。
答案:10
5.解析:K=====1×10-12。由K=得=,加入I 后,HSO被氧化为HSO,c(H+)
h h 2 2 4
增大,c(OH-)减小,K不变,所以增大。
h
答案:1×10-12 增大
6.答案:B
7.解析:①NHCl、ZnCl 均能发生水解,使溶液呈酸性,能与铁锈反应;②NaHCO 与
4 2 3
Al(SO) 发生双水解反应生成Al(OH) 沉淀和CO ,能达到灭火的目的;③草木灰(主要成分
2 4 3 3 2
为KCO)与铵态氮肥(含NH+
)混合时能相互促进水解,从而降低了肥效;④NaCO 溶液中
2 3 4 2 3
NaCO 发生水解:NaCO +HO NaHCO +NaOH,生成的NaOH能与磨口玻璃塞中的SiO 反应生
2 3 2 3 2 ⇌ 3 2
成NaSiO ,NaSiO 具有黏性,瓶塞在较长时间不用后很难被拔出;⑤由于AlCl 水解:AlCl
2 3 2 3 3 3
+3HO Al(OH) +3HCl,加热时HCl大量挥发,促进水解,蒸干并灼烧后最终得AlO ;⑥明
2 ⇌ 3 2 3
矾中Al3+发生水解:Al3++3HO Al(OH)(胶体)+3H+,Al(OH) 胶体能吸附水中悬浮的固体
2 ⇌ 3 3
颗粒物,从而起到净水的作用。
答案:C
8.解析:(1)能把Fe2+氧化为Fe3+,同时又不能引入新的杂质,符合要求的只有
HO 。(2)当CuCl 溶液中混有Fe3+时,可以利用Fe3+的水解:Fe3++3HO Fe(OH) +3H+,加
2 2 2 2 ⇌ 3
入CuO、Cu(OH) 、CuCO 或Cu(OH)CO 与溶液中的H+作用,从而使水解平衡右移,使Fe3+转
2 3 2 2 3
化为Fe(OH) 沉淀而除去。(3)若用加碱法使Fe2+沉淀,同时也必将使Cu2+沉淀。(6)为了抑
3
制CuCl 水解,应在HCl气流中加热蒸发。
2
答案:(1)C
(2)CuO[或Cu(OH) 或CuCO 或Cu(OH)CO]
2 3 2 2 3
(3)不能 加碱的同时也会使Cu2+生成Cu(OH) 沉淀
2
(4)Fe3++3HO Fe(OH) +3H+,CuO+2H+===Cu2++HO[或Cu(OH) +2H+===Cu2++2HO
2 ⇌ 3 2 2 2
等]
(5)将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离
(6)不能 应在HCl气流中加热蒸发
本讲真题研练
1.解析:结合题图可知当pH最小时,溶液呈酸性,溶液中c(CHCOOH)最大,对应lg
3
c(H+)最大,随着pH逐渐增大,当溶液中c(CHCOO-)最大时,对应lg c(OH-)最大。则4条
3
曲线分别对应的lg c(x)如下:经上述分析可知N点时,c(CHCOOH)=c(CHCOO-),K=c(H+),即pH=-lg K,A项
3 3 a a
错误,B 项正确;该体系中, 0.1c(H+)=[c(CHCOOH)+c(CHCOO-)]×c(H+)=
3 3
c(CHCOOH)×c(H+)[+1]=c(CHCOOH)×[K+c(H+)],C项正确;pH由7到14的过程中先促
3 3 a
进CHCOO-的水解,后抑制其水解,D项错误。
3
答案:BC
2.解析:浓度均为0.10 mol·L-1的NaHCONaCO 的混合溶液中,CO2− 的水解程度大
3 2 3 3
于HCO− 的水解程度,HCO− 的水解程度大于其电离程度,所以溶液中c(Na+)>c(HCO−
)>c(C
3 3 3
O2− )>c(OH-),A项正确;浓度均为0.10 mol·L-1的氨水NHCl混合溶液的pH=9.25,说明
3 4
NH·HO的电离程度大于NH+
的水解程度,溶液中c(NH·HO)c(NH·HO)+c(OH-),B项
4 4 3 2
错误;浓度均为0.10 mol·L-1的CHCOOHCHCOONa混合溶液的pH=4.76,说明CHCOOH的电
3 3 3
离程度大于CHCOO-的水解程度,则溶液中c(CHCOO-)>c(Na+)>c(CHCOOH)>c(H+),C项错误;
3 3 3
浓度均为0.10 mol·L-1的HCONaHCO 混合溶液的pH=1.68,根据电荷守恒有c(Na+)+c(H
2 2 4 2 4
+)=c(OH-)+c(HCO− )+2c(CO2− ),根据物料守恒有2c(Na+)=c(CO2−
)+c(HCO)+
2 4 2 4 2 4 2 2 4
c(HCO− ),联立上述两式得c(H+)+c(HCO)=c(Na+)+c(CO2− )+c(OH-),D项正确。
2 4 2 2 4 2 4
答案:AD
3.解析:本题考查电解质溶液相关知识,考查的化学学科核心素养是变化观念与平衡
思想。HCl是强电解质,完全电离,醋酸是弱电解质,部分电离,浓度相同的HCl和CHCOOH
3
的混合液中c(Cl-)>c(CHCOO-),A项正确;当滴入氨水10 mL时,加入的氨水的体积、浓度
3
和初始醋酸溶液的体积、浓度均相等,由物料守恒可知,c(NH+
)+c(NH·HO)=c(CHCOO-)
4 3 2 3
+c(CHCOOH),B项正确;当滴入氨水20 mL时,溶液中溶质为CHCOONH 和NHCl,根据电荷
3 3 4 4
守恒式c(NH+ )+c(H+)=c(CHCOO-)+c(Cl-)+c(OH-),物料守恒式c(NH+
)+c(NH·HO)
4 3 4 3 2
=c(CHCOO-)+c(CHCOOH)+c(Cl-),可得c(CHCOOH)+c(H+)=c(NH·HO)+c(OH-),C项
3 3 3 3 2
正确;恰好反应时,生成等物质的量的氯化铵和醋酸铵,此时溶液呈酸性,若溶液呈中性,
则氨水滴入量大于20
mL,c(NH+
)>c(Cl-),D项错误。
4
答案:D
4.解析:A项,温度升高,纯水中的H+、OH-的浓度都增大,但二者始终相等;B项,
温度升高,CHCOONa的水解平衡正向移动,溶液中OH-浓度增大,图像中反映出的“随温度
3
升高CHCOONa溶液的pH下降”的现象,是由“温度升高水的离子积常数增大”导致的,并
3
非OH-浓度下降了;D项,温度升高对CHCOO-、Cu2+的水解都有促进作用,二者水解平衡移
3
动的方向是一致的。答案:C
5.解析:亚硫酸钠是强碱弱酸盐,存在水解平衡:SO2− +HO HSO− +OH-,A项正确;
3 2 ⇌ 3
①与④的温度相同,但pH不同,主要是由于亚硫酸钠被氧化为硫酸钠,从而导致溶液的碱性
减弱,pH减小,B项正确;①→③的过程中,温度升高使水解平衡正向移动,而
SO2−
浓度逐
3
渐减小,使水解平衡逆向移动,故温度和浓度对水解平衡移动方向的影响不一致,C项错误;
①与④的温度相同,故K相同,D项正确。
w
答案:C
6.解析:LiHPO 溶液中存在HPO− 的电离平衡:HPO− H++HPO2− 、HPO2− H++P
2 4 2 4 2 4⇌ 4 4 ⇌
O3− ,HPO− 的水解平衡:HPO− +HO HPO +OH-, HO的电离平衡:HO H++OH-,溶液
4 2 4 2 4 2 ⇌ 3 4 2 2 ⇌
中存在4个平衡,A项错误;含P元素的粒子有HPO− 、HPO2− 、PO3−
、HPO ,B项错误;根
2 4 4 4 3 4
据图1,随着c
(HPO−
)增大,溶液的pH先逐渐减小后趋向不变,C项错误;根据图2,当
初始 2 4
pH=4.66时,δ=0.994,即HPO−
的分布分数为0.994,故当pH达到4.66时,HPO 几乎全
2 4 3 4
部转化为LiHPO,D项正确。
2 4
答案:D
7.解析:横坐标取0时,曲线M对应pH约为5.4,曲线N对应pH约为4.4,因为是
NaOH滴定HX溶液,所以在酸性较强的溶液中会存在c(HX-)=c(HX),所以曲线N表示pH与
2 2
lg的变化关系,B项正确;=1时,即lg=0,pH=5.4,c(H+)=1×10-5.4 mol·L-1,K =
a2
≈1×10-5.4,A正确;NaHX溶液中,c(HX-)>c(X2-),即<1,lg<0,此时溶液呈酸性,C正确;
D项,当溶液呈中性时,由曲线M可知lg>0,>1,即c(X2-)>c(HX-),错误。
答案:D