文档内容
专项提能特训 12 速率图像与实验探究
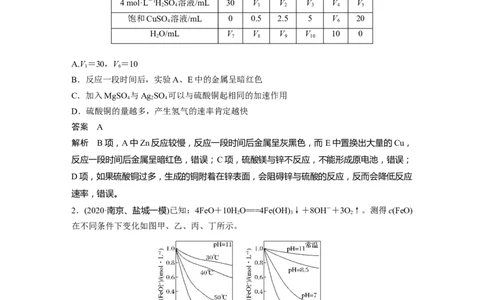
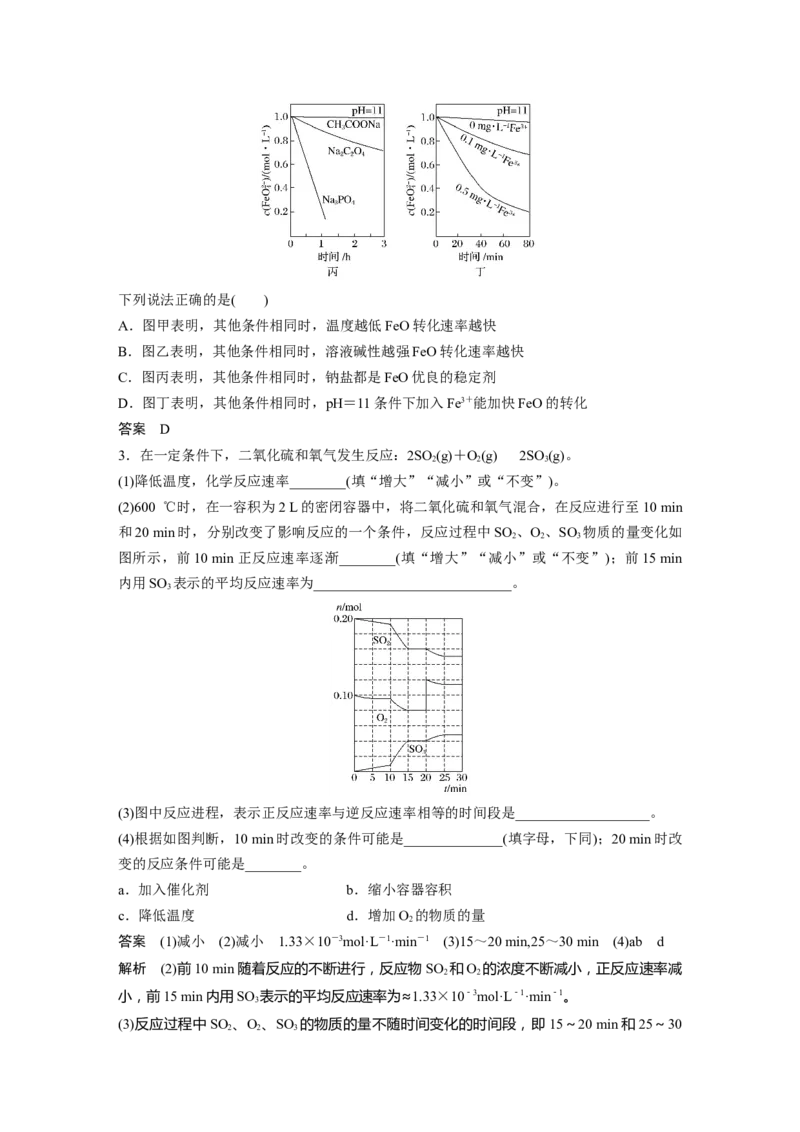
1.为研究硫酸铜的量对锌与稀硫酸反应生成氢气速率的影响,某同学设计了如下一系列实
验。表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录
获得相同体积的气体所需的时间。下列说法正确的是( )
实验
A B C D E F
混合溶液
4 mol·L-1HSO 溶液/mL 30 V V V V V
2 4 1 2 3 4 5
饱和CuSO 溶液/mL 0 0.5 2.5 5 V 20
4 6
HO/mL V V V V 10 0
2 7 8 9 10
A.V=30,V=10
1 6
B.反应一段时间后,实验A、E中的金属呈暗红色
C.加入MgSO 与Ag SO 可以与硫酸铜起相同的加速作用
4 2 4
D.硫酸铜的量越多,产生氢气的速率肯定越快
答案 A
解析 B项,A中Zn反应较慢,反应一段时间后金属呈灰黑色,而 E中置换出大量的Cu,
反应一段时间后金属呈暗红色,错误;C项,硫酸镁与锌不反应,不能形成原电池,错误;
D项,如果硫酸铜过多,生成的铜附着在锌表面,会阻碍锌与硫酸的反应,反而会降低反应
速率,错误。
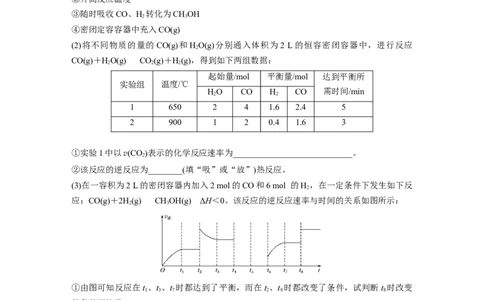
2.(2020·南京、盐城一模)已知:4FeO+10HO===4Fe(OH) ↓+8OH-+3O↑。测得c(FeO)
2 3 2
在不同条件下变化如图甲、乙、丙、丁所示。下列说法正确的是( )
A.图甲表明,其他条件相同时,温度越低FeO转化速率越快
B.图乙表明,其他条件相同时,溶液碱性越强FeO转化速率越快
C.图丙表明,其他条件相同时,钠盐都是FeO优良的稳定剂
D.图丁表明,其他条件相同时,pH=11条件下加入Fe3+能加快FeO的转化
答案 D
3.在一定条件下,二氧化硫和氧气发生反应:2SO (g)+O(g)2SO (g)。
2 2 3
(1)降低温度,化学反应速率________(填“增大”“减小”或“不变”)。
(2)600 ℃时,在一容积为2 L的密闭容器中,将二氧化硫和氧气混合,在反应进行至10 min
和20 min时,分别改变了影响反应的一个条件,反应过程中SO 、O 、SO 物质的量变化如
2 2 3
图所示,前10 min正反应速率逐渐________(填“增大”“减小”或“不变”);前15 min
内用SO 表示的平均反应速率为____________________________。
3
(3)图中反应进程,表示正反应速率与逆反应速率相等的时间段是___________________。
(4)根据如图判断,10 min时改变的条件可能是______________(填字母,下同);20 min时改
变的反应条件可能是________。
a.加入催化剂 b.缩小容器容积
c.降低温度 d.增加O 的物质的量
2
答案 (1)减小 (2)减小 1.33×10-3mol·L-1·min-1 (3)15~20 min,25~30 min (4)ab d
解析 (2)前10 min随着反应的不断进行,反应物SO 和O 的浓度不断减小,正反应速率减
2 2
小,前15 min内用SO 表示的平均反应速率为≈1.33×10-3mol·L-1·min-1。
3
(3)反应过程中SO 、O 、SO 的物质的量不随时间变化的时间段,即 15~20 min和25~30
2 2 3min反应处于平衡状态。(4)10~15 min三条曲线的斜率突然增大,说明反应速率突然加快,
其原因可能是加入催化剂或缩小容器容积。反应进行至 20 min时,曲线发生的变化是O 的
2
物质的量突然增大,平衡发生移动,引起SO 、SO 的物质的量随之发生变化。
2 3
4.煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产
品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为 C(s)+HO(g)CO(g)+H(g) ΔH=+
2 2
131.3 kJ·mol-1。能使化学反应速率加快的措施有____________(填序号)。
①增加C的物质的量
②升高反应温度
③随时吸收CO、H 转化为CHOH
2 3
④密闭定容容器中充入CO(g)
(2)将不同物质的量的CO(g)和HO(g)分别通入体积为2 L的恒容密闭容器中,进行反应
2
CO(g)+HO(g)CO(g)+H(g),得到如下两组数据:
2 2 2
起始量/mol 平衡量/mol 达到平衡所
实验组 温度/℃
HO CO H CO 需时间/min
2 2
1 650 2 4 1.6 2.4 5
2 900 1 2 0.4 1.6 3
①实验1中以v(CO)表示的化学反应速率为____________________________。
2
②该反应的逆反应为________(填“吸”或“放”)热反应。
(3)在一容积为2 L的密闭容器内加入2 mol的CO和6 mol 的H ,在一定条件下发生如下反
2
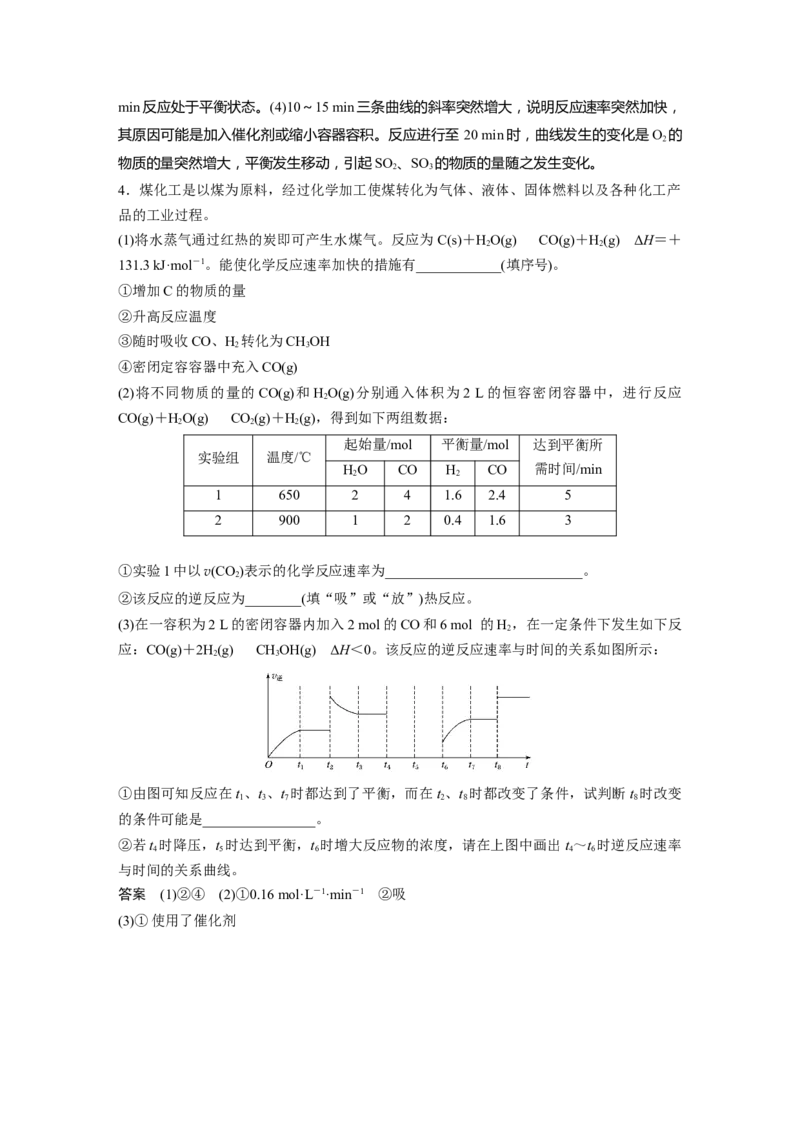
应:CO(g)+2H(g)CHOH(g) ΔH<0。该反应的逆反应速率与时间的关系如图所示:
2 3
①由图可知反应在t 、t 、t 时都达到了平衡,而在t 、t 时都改变了条件,试判断t 时改变
1 3 7 2 8 8
的条件可能是________________。
②若t 时降压,t 时达到平衡,t 时增大反应物的浓度,请在上图中画出t ~t 时逆反应速率
4 5 6 4 6
与时间的关系曲线。
答案 (1)②④ (2)①0.16 mol·L-1·min-1 ②吸
(3)①使用了催化剂②