文档内容
24 沉淀溶解平衡图像的分析
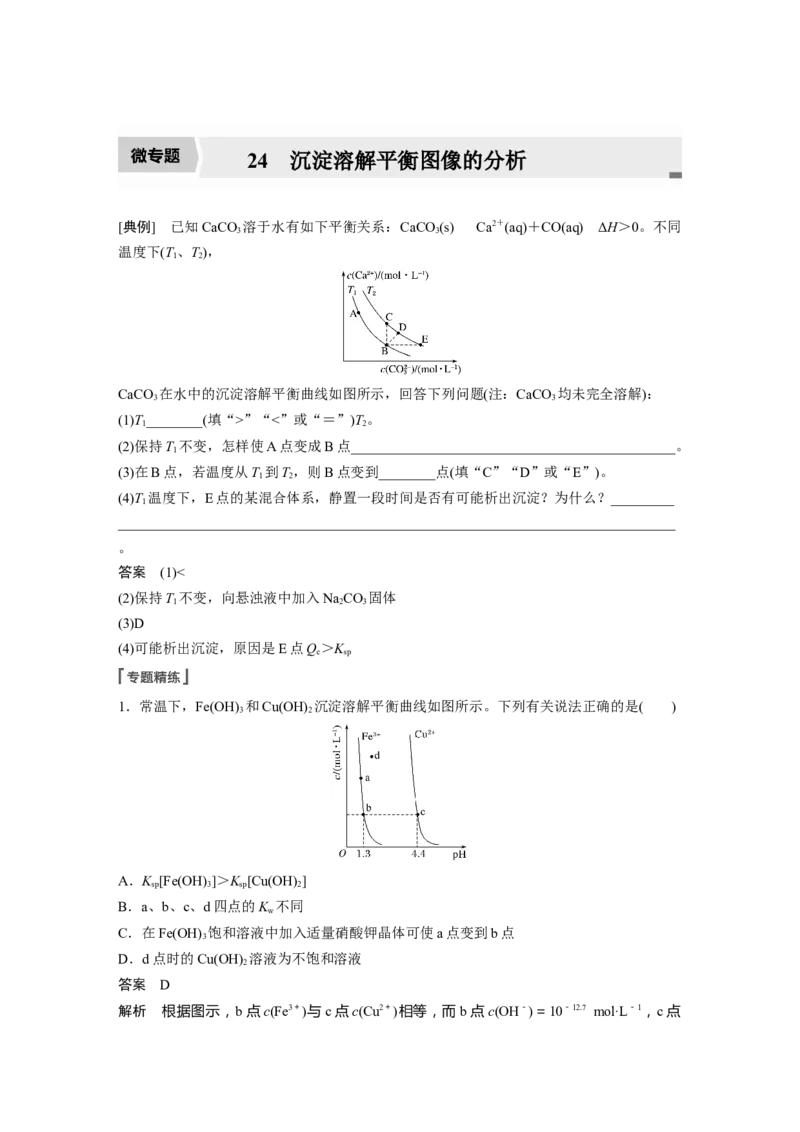
[典例] 已知CaCO 溶于水有如下平衡关系:CaCO (s)Ca2+(aq)+CO(aq) ΔH>0。不同
3 3
温度下(T、T),
1 2
CaCO 在水中的沉淀溶解平衡曲线如图所示,回答下列问题(注:CaCO 均未完全溶解):
3 3
(1)T________(填“>”“<”或“=”)T。
1 2
(2)保持T 不变,怎样使A点变成B点______________________________________________。
1
(3)在B点,若温度从T 到T,则B点变到________点(填“C”“D”或“E”)。
1 2
(4)T 温度下,E点的某混合体系,静置一段时间是否有可能析出沉淀?为什么?_________
1
_______________________________________________________________________________
。
答案 (1)<
(2)保持T 不变,向悬浊液中加入NaCO 固体
1 2 3
(3)D
(4)可能析出沉淀,原因是E点Q>K
c sp
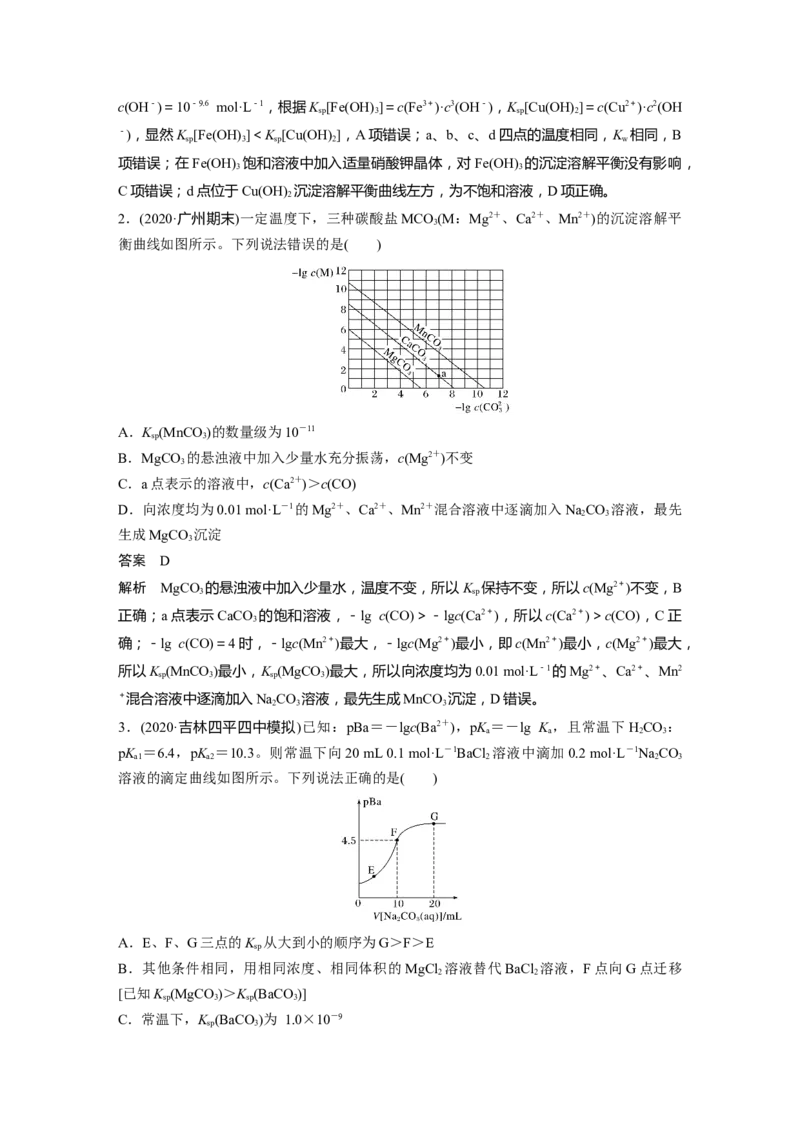
1.常温下,Fe(OH) 和Cu(OH) 沉淀溶解平衡曲线如图所示。下列有关说法正确的是( )
3 2
A.K [Fe(OH) ]>K [Cu(OH) ]
sp 3 sp 2
B.a、b、c、d四点的K 不同
w
C.在Fe(OH) 饱和溶液中加入适量硝酸钾晶体可使a点变到b点
3
D.d点时的Cu(OH) 溶液为不饱和溶液
2
答案 D
解析 根据图示,b点c(Fe3+)与c点c(Cu2+)相等,而b点c(OH-)=10-12.7 mol·L-1,c点c(OH-)=10-9.6 mol·L-1,根据K [Fe(OH) ]=c(Fe3+)·c3(OH-),K [Cu(OH) ]=c(Cu2+)·c2(OH
sp 3 sp 2
-),显然K [Fe(OH) ]<K [Cu(OH) ],A项错误;a、b、c、d四点的温度相同,K 相同,B
sp 3 sp 2 w
项错误;在Fe(OH) 饱和溶液中加入适量硝酸钾晶体,对Fe(OH) 的沉淀溶解平衡没有影响,
3 3
C项错误;d点位于Cu(OH) 沉淀溶解平衡曲线左方,为不饱和溶液,D项正确。
2
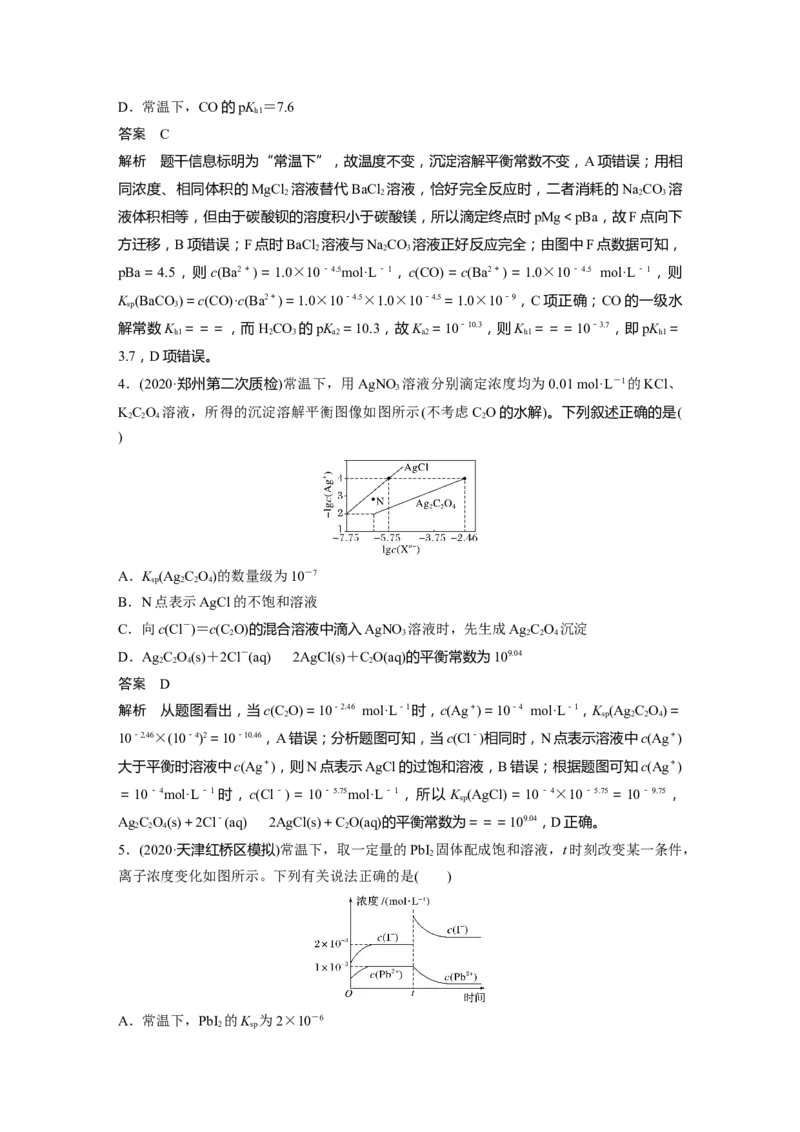
2.(2020·广州期末)一定温度下,三种碳酸盐MCO (M:Mg2+、Ca2+、Mn2+)的沉淀溶解平
3
衡曲线如图所示。下列说法错误的是( )
A.K (MnCO )的数量级为10-11
sp 3
B.MgCO 的悬浊液中加入少量水充分振荡,c(Mg2+)不变
3
C.a点表示的溶液中,c(Ca2+)>c(CO)
D.向浓度均为0.01 mol·L-1的Mg2+、Ca2+、Mn2+混合溶液中逐滴加入NaCO 溶液,最先
2 3
生成MgCO 沉淀
3
答案 D
解析 MgCO 的悬浊液中加入少量水,温度不变,所以K 保持不变,所以c(Mg2+)不变,B
3 sp
正确;a点表示CaCO 的饱和溶液,-lg c(CO)>-lgc(Ca2+),所以c(Ca2+)>c(CO),C正
3
确;-lg c(CO)=4时,-lgc(Mn2+)最大,-lgc(Mg2+)最小,即c(Mn2+)最小,c(Mg2+)最大,
所以K (MnCO )最小,K (MgCO )最大,所以向浓度均为0.01 mol·L-1的Mg2+、Ca2+、Mn2
sp 3 sp 3
+混合溶液中逐滴加入NaCO 溶液,最先生成MnCO 沉淀,D错误。
2 3 3
3.(2020·吉林四平四中模拟)已知:pBa=-lgc(Ba2+),pK =-lg K ,且常温下HCO :
a a 2 3
pK =6.4,pK =10.3。则常温下向20 mL 0.1 mol·L-1BaCl 溶液中滴加0.2 mol·L-1NaCO
a1 a2 2 2 3
溶液的滴定曲线如图所示。下列说法正确的是( )
A.E、F、G三点的K 从大到小的顺序为G>F>E
sp
B.其他条件相同,用相同浓度、相同体积的MgCl 溶液替代BaCl 溶液,F点向G点迁移
2 2
[已知K (MgCO )>K (BaCO)]
sp 3 sp 3
C.常温下,K (BaCO)为 1.0×10-9
sp 3D.常温下,CO的pK =7.6
h1
答案 C
解析 题干信息标明为“常温下”,故温度不变,沉淀溶解平衡常数不变,A项错误;用相
同浓度、相同体积的MgCl 溶液替代BaCl 溶液,恰好完全反应时,二者消耗的NaCO 溶
2 2 2 3
液体积相等,但由于碳酸钡的溶度积小于碳酸镁,所以滴定终点时pMg<pBa,故F点向下
方迁移,B项错误;F点时BaCl 溶液与NaCO 溶液正好反应完全;由图中F点数据可知,
2 2 3
pBa=4.5,则 c(Ba2+)=1.0×10-4.5mol·L-1,c(CO)=c(Ba2+)=1.0×10-4.5 mol·L-1,则
K (BaCO)=c(CO)·c(Ba2+)=1.0×10-4.5×1.0×10-4.5=1.0×10-9,C项正确;CO的一级水
sp 3
解常数K ===,而HCO 的pK =10.3,故K =10-10.3,则K ===10-3.7,即pK =
h1 2 3 a2 a2 h1 h1
3.7,D项错误。
4.(2020·郑州第二次质检)常温下,用AgNO 溶液分别滴定浓度均为0.01 mol·L-1的KCl、
3
KC O 溶液,所得的沉淀溶解平衡图像如图所示(不考虑C O的水解)。下列叙述正确的是(
2 2 4 2
)
A.K (Ag C O)的数量级为10-7
sp 2 2 4
B.N点表示AgCl的不饱和溶液
C.向c(Cl-)=c(C O)的混合溶液中滴入AgNO 溶液时,先生成Ag C O 沉淀
2 3 2 2 4
D.Ag C O(s)+2Cl-(aq)2AgCl(s)+C O(aq)的平衡常数为109.04
2 2 4 2
答案 D
解析 从题图看出,当c(C O)=10-2.46 mol·L-1时,c(Ag+)=10-4 mol·L-1,K (Ag C O)=
2 sp 2 2 4
10-2.46×(10-4)2=10-10.46,A错误;分析题图可知,当c(Cl-)相同时,N点表示溶液中c(Ag+)
大于平衡时溶液中c(Ag+),则N点表示AgCl的过饱和溶液,B错误;根据题图可知c(Ag+)
=10-4mol·L-1时,c(Cl-)=10-5.75mol·L-1,所以 K (AgCl)=10-4×10-5.75=10-9.75,
sp
Ag C O(s)+2Cl-(aq)2AgCl(s)+C O(aq)的平衡常数为===109.04,D正确。
2 2 4 2
5.(2020·天津红桥区模拟)常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某一条件,
2
离子浓度变化如图所示。下列有关说法正确的是( )
A.常温下,PbI 的K 为2×10-6
2 spB.温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,平衡向左移动,Pb2+的浓度减小
2
C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI 的K 增大
2 sp
D.常温下,K (PbS)=8×10-28,向PbI 的悬浊液中加入 NaS溶液,反应 PbI (s)+S2-
sp 2 2 2
(aq)PbS(s)+2I-(aq)的平衡常数为5×1018
答案 D
解析 根据图像知,常温下平衡时溶液中 c(Pb2+)、c(I-)分别是1×10-3mol·L-1、2×10-
3mol·L-1,因此PbI 的K =c(Pb2+)·c2(I-)=4×10-9,A错误;PbI 饱和溶液中存在平衡:
2 sp 2
PbI (s)
2
Pb2+(aq)+2I-(aq),温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,Pb2+浓度增大,
2
平衡逆向移动,最终平衡时Pb2+浓度仍然比原平衡时大,B错误;根据图像知,t时刻改变
的条件是增大I-浓度,温度不变,PbI 的K 不变,C错误;反应PbI (s)+S2-(aq) PbS(s)
2 sp 2
+2I-(aq)的平衡常数K===5×1018,D正确。
(1)分析沉淀溶解平衡图像的三步骤:明确图像中纵、横坐标的含义→理解图像中线上点、
线外点的含义→抓住K 的特点,结合选项分析判断。
sp
(2)沉淀溶解平衡曲线类似于溶解度曲线,曲线上任一点都表示饱和溶液,都是相应温度下
恰好生成沉淀时的离子浓度,同一温度下有相同的K 。
sp