文档内容
专项提能特训 17 四大平衡常数的综合应用
1.已知K(K )、K 、K 、K 分别表示弱酸的电离平衡常数(弱碱的电离平衡常数)、水的离
a b w h sp
子积常数、盐的水解平衡常数、难溶电解质的溶度积常数。通过查阅资料获得温度为 25 ℃
时以下数据:
K =1.0×10-14,K(CHCOOH)=1.8×10-5,
w a 3
K(HSCN)=0.13,K(HF)=4.0×10-4,
a a
K [Mg(OH) ]=1.8×10-11
sp 2
(1)有关上述常数的说法正确的是____________(填字母)。
a.它们都能反映一定条件下对应变化进行的程度
b.所有弱电解质的电离常数和难溶电解质的K 都随温度的升高而增大
sp
c.常温下,CHCOOH在水中的K 大于在饱和CHCOONa溶液中的K
3 a 3 a
d.一定温度下,在CHCOONa溶液中,K =K·K
3 w a h
(2)25 ℃时,1.0 mol·L-1HF溶液的pH约等于____________(已知lg 2≈0.3)。将浓度相等的
HF与NaF溶液等体积混合,判断溶液呈______(填“酸”“碱”或“中”)性,并结合有关
数据解释原因:_________________________________________________________________。
(3)已知CHCOONH 溶液为中性,又知CHCOOH溶液加到NaCO 溶液中有气体放出,现
3 4 3 2 3
有25 ℃时等浓度的四种溶液:
A.NH Cl B.NH SCN
4 4
C.CHCOONH D.NH HCO
3 4 4 3
回答下列问题:
①试推断NH HCO 溶液的pH________(填“>”“<”或“=”)7。
4 3
②将四种溶液按NH浓度由大到小的顺序排列:________(填字母)。
③NH SCN溶液中所有离子浓度由大到小的顺序为____________________。
4
(4)为探究 Mg(OH) 在酸中的溶解性,利用以上数据可以计算出反应: Mg(OH) (s)+
2 2
2CHCOOH(aq)Mg2+(aq)+2CHCOO-(aq)+2HO(l)在 25 ℃时的平衡常数 K=
3 3 2
_________,并据此推断 Mg(OH) ________(填“能”或“不能”)溶解于醋酸。(已知
2
1.83≈5.8)
答案 (1)ad (2)1.7 酸 HF和NaF的浓度相等,K=4.0×10-4,K ==2.5×10-11,故HF
a h
的电离程度大于F-的水解程度,溶液呈酸性 (3)①> ②A>B>C>D ③c(SCN-)>
c(NH)>c(H+)>c(OH-) (4)5.8×107 能
解析 (1)它们都能反映一定条件下对应变化进行的程度,故 a正确;难溶电解质的K 不一
sp
定随温度的升高而增大,故 b错误;K 只随温度变化,故 c错误;由电离平衡常数,
a
K(CHCOOH)=,水的离子积常数K =c(H+)·c(OH-),盐的水解平衡常数K =可知,一定
a 3 w h温度下,在CHCOONa溶液中,K =K·K ,故d正确。
3 w a h
(2)K(HF) = = = 4.0×10 - 4 , 则 1.0 mol·L - 1HF 溶 液 中 氢 离 子 浓 度 为 2.0×
a
10-2 mol·L-1,所以pH=-lg(2.0×10-2)=2-lg2≈1.7,HF和NaF的浓度相等,K=4.0×
a
10-4,K ===2.5×10-11,故HF的电离程度大于F-的水解程度,溶液呈酸性。(3)①因
h
CHCOOH 溶液加到 NaCO 溶液中有气体放出,所以酸性:CHCOOH>HCO ,
3 2 3 3 2 3
CHCOONH 溶液为中性,可得醋酸的酸性和 NH ·H O的碱性一样,所以NH HCO 溶液中
3 4 3 2 4 3
碳酸氢根离子水解程度大于铵根离子的水解程度,则溶液的 pH>7。②NH Cl溶液中Cl-不
4
促进也不抑制NH水解;B、C、D中均相互促进,由K(CHCOOH)=1.8×10-5,K(HSCN)
a 3 a
=0.13,酸性:CHCOOH>HCO 可知,B、C、D中NH水解程度依次增大,则四种溶液
3 2 3
中NH浓度由大到小的顺序排列是A>B>C>D。③由CHCOONH 溶液为中性,K(HSCN)
3 4 a
=0.13>K(CHCOOH)可知,NH SCN溶液呈酸性,所以溶液中所有离子浓度由大到小的顺
a 3 4
序为 c(SCN-)>c(NH)>c(H+)>c(OH-)。(4)Mg(OH) (s)+2CHCOOH(aq)Mg2+(aq)+
2 3
2CHCOO-(aq)+2HO(l)在25 ℃时的平衡常数K====
3 2
≈5.8×107,因K特别大,所以Mg(OH) 能溶解于醋酸。
2
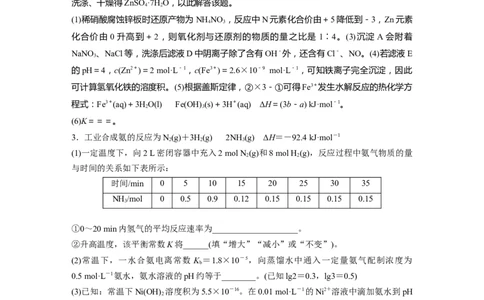
2.制备锌印刷电路板是用稀硝酸腐蚀锌板,产生的废液称“烂板液”。“烂板液”中除含
有硝酸锌外,还含有自来水带入的 Cl-和Fe3+。在实验室里用“烂板液”制取ZnSO·7H O
4 2
的过程如下:
(1)若稀硝酸腐蚀锌板时还原产物为NH NO ,氧化剂与还原剂的物质的量之比是________。
4 3
(2)若步骤①的pH>12,则Zn(OH) 溶解生成偏锌酸钠,写出Zn(OH) 被溶解的离子方程式
2 2
______________________________________________________________________________。
(3)滤液D中除了含有OH-离子外,还含有的阴离子有__________(填离子符号)。
(4)若滤液E的pH=4,c(Zn2+)=2 mol·L-1,c(Fe3+)=2.6×10-9 mol·L-1,能求得的溶度积
是______(填字母)。
A.K [Zn(OH) ]
sp 2
B.K [Zn(OH) ]和K [Fe(OH) ]
sp 2 sp 3
C.K [Fe(OH) ]
sp 3
(5)已知:①Fe(OH) (s)Fe3+(aq)+3OH-(aq) ΔH=a kJ·mol-1
3
②HO(l)H+(aq)+OH-(aq) ΔH=b kJ·mol-1
2
请写出Fe3+发生水解反应的热化学方程式:______________________________________。(6)若Fe(OH) 的溶度积常数为K ,HO的离子积常数为K ,Fe3+发生水解反应的平衡常数
3 sp 2 w
K=______________(用含K 、K 的代数式表示)。
sp w
答案 (1)1∶4 (2)Zn(OH) +2OH-===ZnO+2HO (3)Cl-、NO (4)C (5)Fe3+(aq)+
2 2
3HO(l)Fe(OH) (s)+3H+(aq) ΔH=(3b-a) kJ·mol-1 (6)
2 3
解析 “烂板液”中除含硝酸锌外,还含有自来水带入的Cl-和Fe3+,加入氢氧化钠调节溶
液的pH=8使铁离子、锌离子转化为Fe(OH) 、Zn(OH) 沉淀,过滤分离,滤液C中含有
3 2
NaNO 、NaCl等,沉淀会附着NaNO 、NaCl等,用水洗涤除去,沉淀B用硫酸溶解、控制
3 3
一定pH,Fe(OH) 不溶解,过滤分离得到ZnSO 溶液,再经过蒸发浓缩、冷却结晶、过滤、
3 4
洗涤、干燥得ZnSO·7H O,以此解答该题。
4 2
(1)稀硝酸腐蚀锌板时还原产物为NH NO ,反应中N元素化合价由+5降低到-3,Zn元素
4 3
化合价由 0升高到+2,则氧化剂与还原剂的物质的量之比是 1∶4。(3)沉淀 A会附着
NaNO 、NaCl等,洗涤后滤液D中阴离子除了含有OH-外,还含有Cl-、NO。(4)若滤液E
3
的pH=4,c(Zn2+)=2 mol·L-1,c(Fe3+)=2.6×10-9 mol·L-1,可知铁离子完全沉淀,因此
可计算氢氧化铁的溶度积。(5)根据盖斯定律,②×3-①可得Fe3+发生水解反应的热化学方
程式:Fe3+(aq)+3HO(l)Fe(OH) (s)+3H+(aq) ΔH=(3b-a) kJ·mol-1。
2 3
(6)K===。
3.工业合成氨的反应为N(g)+3H(g)2NH (g) ΔH=-92.4 kJ·mol-1
2 2 3
(1)一定温度下,向2 L密闭容器中充入2 mol N (g)和8 mol H (g),反应过程中氨气物质的量
2 2
与时间的关系如下表所示:
时间/min 0 5 10 15 20 25 30 35
NH /mol 0 0.5 0.9 0.12 0.15 0.15 0.15 0.15
3
①0~20 min内氢气的平均反应速率为____________________。
②升高温度,该平衡常数K将______(填“增大”“减小”或“不变”)。
(2)常温下,一水合氨电离常数 K =1.8×10-5,向蒸馏水中通入一定量氨气配制浓度为
b
0.5 mol·L-1氨水,氨水溶液的pH约等于________。(已知lg2=0.3,lg3=0.5)
(3)已知:常温下Ni(OH) 溶度积为5.5×10-16。在0.01 mol·L-1的Ni2+溶液中滴加氨水到pH
2
=8时,溶液中c(Ni2+)=____________________。
(4)常温下,0.1 mol·L-1氯化铵溶液 pH 约为 5,在该条件下,氯化铵水解常数 K 约为
h
__________________________________。
答案 (1)①5.625×10-3 mol·L-1·min-1 ②减小 (2)11.5 (3)5.5×10-4mol·L-1
(4)1.0×10-9
解析 (1)①v(H )=v(NH )=×=5.625×10-3 mol·L-1·min-1。②合成氨反应的正反应是放热
2 3
反应,升高温度,平衡向逆反应方向移动,平衡常数减小。(2)设0.5 mol·L-1氨水电离出的
c(OH-)为 x,由 NH ·H ONH+OH-可知:K ===1.8×10-5,解得:x≈3.0×10-3
3 2 bmol·L-1,c(H+)== mol·L-1=×10-11 mol·
L-1,pH=-lg(×10-11)=11+lg3=11.5。(3)pH=8时,c(OH-)=1.0×10-6 mol·L-1,由
Ni(OH) (s)Ni2+(aq)+2OH-(aq)可知:c(Ni2+)= mol·L-1=5.5×10-4 mol·L-1。(4)氯化铵
2
溶液中存在水解平衡:NH+HONH ·H O+H+,0.1 mol·L-1氯化铵溶液pH约为5,则
2 3 2
c(H+)=1.0×10-5mol·L-1,则氯化铵水解常数K =≈=1.0×10-9。
h
4.已知K、K、K 、K 分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、
a w sp
难溶电解质的溶度积常数。
(1)已知25 ℃时CHCOONH 呈中性,则该温度下CHCOONH 溶液中水电离的H+浓度为
3 4 3 4
________,溶液中离子浓度大小关系为____________。
(2)NH Cl 溶 液 呈 ______( 填 “ 酸 ” “ 碱 ” 或 “ 中 ” ) 性 , 其 原 因 是
4
______________________(用离子方程式表示)。NaHCO 溶液呈______(填“酸”“碱”或
3
“中”)性,其原因是__(用离子方程式表示)。
(3)已知常温下Fe(OH) 和Mg(OH) 的K 分别为8.0×10-38、1.0×10-11,向浓度均为0.1 mol·L
3 2 sp
-1的FeCl 、MgCl 的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶
3 2
液pH的范围是________。(已知lg2=0.3,离子浓度低于10-5mol·L-1时认为沉淀完全)
答案 (1)1.0×10-7 mol·L-1 c(NH)=c(CHCOO-)>c(OH-)=c(H+) (2)酸 NH+
3
HONH ·H O+H+ 碱 HCO+HOHCO+OH- (3)3.3≤pH<9
2 3 2 2 2 3
解析 (1)CH COOH和NH ·H O电离常数相等,则该温度下CHCOONH 溶液中铵根离子和
3 3 2 3 4
醋酸根离子水解程度相同,导致醋酸铵溶液呈中性;水电离出氢离子的浓度为 1.0×10-7
mol·L-1;水的电离程度很小,溶液中离子浓度大小顺序是c(NH)=c(CHCOO-)>c(OH-)=
3
c(H+)。(2)NH Cl溶液呈酸性,其原因是NH+HONH ·H O+H+;NaHCO 溶液呈碱性,
4 2 3 2 3
其原因是HCO+HOHCO +OH-。(3)≤c(OH-)<, mol·L-1≤c(OH-)< mol·L-1,
2 2 3
2×10-11 mol·L-1≤c(OH-)<1×10-5 mol·L-1, mol·L-1<c(H+)≤ mol·L-1,则3.3≤pH<
9。
5.平衡常数是分析平衡问题的重要依据。回答下列问题。
(1)高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大,但在冰醋酸中却有
一定的差异,以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 HClO HSO HCl HNO
4 2 4 3
K 3.0×10-8 6.3×10-9 1.6×10-9 4.2×10-10
a
从以上表格中的数据判断以下说法中不正确的是______(填字母)。
a.在冰醋酸中这四种酸都没有完全电离
b.在冰醋酸中高氯酸是这四种酸中最强的酸
c.在冰醋酸中硫酸的电离方程式为HSO ===2H++SO
2 4
d.水对于这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱(2)已知:25 ℃时,HA的K=1.0×10-6,则25 ℃时,1 mol·L-1的HA溶液pH=______。
a
(3)在温度为t时,某研究人员测定NH ·H O的电离常数K 为2×10-5,NH的水解常数K 为
3 2 b h
1.5×10-8,则该温度下水的离子积常数K 为________,请判断t______(填“>”“<”或
w
“=”)25 ℃。
(4)化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)CuS(s)+
Mn2+(aq)。
该反应的平衡常数K的数值为__________(保留两位有效数字,CuS和MnS的K 分别为
sp
6.0×10-36、2.0×10-10)。
(5)25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合所得溶液中 c(NH)=
c(Cl-),则溶液显______(填“酸”“碱”或“中”)性;用含a的代数式表示NH ·H O的电
3 2
离常数K =____________。
b
答案 (1)c (2)3 (3)3×10-13 > (4)3.3×1025 (5)中
解析 (1)根据电离平衡常数知,在醋酸中这几种酸都不完全电离,a正确;在醋酸中,高氯
酸的电离平衡常数最大,所以高氯酸的酸性最强,b正确;在冰醋酸中硫酸存在电离平衡,
所以其电离方程式为HSO H++HSO,c错误;这四种酸在水中都完全电离,在冰醋酸
2 4
中电离程度不同,所以水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强
弱,d正确。(2)由c2(H+)=K·c(HA)=1.0×10-6×1=1×10-6,所以c(H+)=10-3 mol·L-1,
a
pH=3。(3)K =K ·K =2×10-5×1.5×10-8=3×10-13,t温度时水的离子积常数大于25 ℃
w b h
时水的离子积常数,水的电离是吸热的,温度越高离子积常数越大,因此温度应高于 25
℃。(4)平衡常数K====≈3.3×1025。(5)根据电荷守恒有c(NH)+c(H+)=c(Cl-)+c(OH
-),由于c(NH)=c(Cl-),故c(H+)=c(OH-),溶液呈中性,故溶液中c(OH-)=10-7 mol·L-
1,溶液中c(NH)=c(Cl-)=×0.01 mol·L-1=0.005 mol·L-1,故混合后溶液中c(NH ·H O)=×a
3 2
mol·L-1-0.005 mol·L-1=(0.5a-0.005) mol·L-1,NH ·H O的电离常数K ==。
3 2 b
6.与K相关的计算:已知 25 ℃时,K [Mg(OH) ]=3.2×10-11,K [Cu(OH) ]=2.2×10-
sp 2 sp 2
20。
(1)25 ℃时,Mg(OH) 的溶解度为____________。
2
(2)向0.02 mol·L-1 MgCl 溶液中加入NaOH固体,要生成Mg(OH) 沉淀,溶液中c(OH-)最
2 2
小为________。
(3)向浓度均为0.02 mol·L-1MgCl 和CuCl 混合液中逐滴加入NaOH溶液,先生成________
2 2
沉淀,当两种沉淀共存时,=____________。
(4)Cu2+的水解平衡常数为:______________________。
(5)25 ℃,已知0.05 mol·L-1 NaA溶液pH=8,求HA的K=________(近似值)。
a
(6)25 ℃时,向a mL 0.1 mol·L-1 NaOH溶液中逐滴加入等浓度的CHCOOH溶液b mL,
3
混合溶液恰好呈中性(体积变化忽略不计),已知 CHCOOH的K =1.75×10-5,求的值
3 a
________。答案 (1)1.16×10-3g (2)4×10-5mol·L-1
(3)Cu(OH) 1.45×109 (4)4.5×10-9 (5)5×10-4 (6)
2
解析 (1)设饱和Mg(OH) 溶液的物质的量浓度为c,则c(Mg2+)·c2(OH-)=4c3=3.2×10-11,
2
c=2×10-4 mol·L-1,假设饱和Mg(OH) 溶液的密度为1 g·mL-1,则100 mL溶液的质量为
2
100 g,含有溶质的质量为2×10-4 mol·L-1×0.1 L×58 g·mol-1=1.16×10-3 g,溶剂的质量
约为100 g,所以其溶解度约为1.16×10-3 g。(2)如果溶液Q>K [Mg(OH) ]就能产生沉淀,
c sp 2
c(OH-)
≥= mol·L-1=4×10-5mol·L-1。(3)Mg(OH) 和Cu(OH) 的溶度积表达式相同,则溶度积常
2 2
数越小的越先产生沉淀,所以先产生的沉淀是 Cu(OH) ,当两种沉淀共存时,===
2
≈1.45×109。(4)K [Cu(OH) ]=c(Cu2+)·c2(OH-)=2.2×10-20,反应Cu2++2HOCu(OH)
sp 2 2 2
+2H+的平衡常数K ====≈4.5×10-9。(5)A-+HOHA+OH-,pH=8,则c(HA)=
h 2
c(OH-)=10-6 mol·L-1,HA的K===5×10-4。(6)溶液呈中性说明c(H+)=10-7 mol·L-
a
1,溶液中c(CHCOO-)=c(Na+)= mol·L-1,醋酸的浓度为mol·L-1,根据平衡常数的计算公
3
式可得:1.75×10-5==,解得=。