文档内容
专项提能特训 16 化工流程中的 K 计算
sp
1.LiTi O 和LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO ,还
4 5 12 4 3
含有少量MgO、SiO 等杂质)来制备,工艺流程如下:
2
回答下列问题:
若“滤液②”中c(Mg2+)=0.02 mol·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+
恰好沉淀完全即溶液中 c(Fe3+)=1.0×10-5 mol·L-1,此时是否有Mg(PO ) 沉淀生成?
3 4 2
___________________________________________________________________(列式计算)。
[已知:FePO 、Mg(PO ) 的K 分别为1.3×10-22、1.0×10-24]
4 3 4 2 sp
答案 否。Fe3+恰好沉淀完全时, c(PO)= mol·L-1=1.3×10-17mol·L-1,c3(Mg2+)·
c2(PO)=0.013×(1.3×10-17)2=1.69×10-40 0
2iii.K (PbSO ) =1.08 ×10-8 ,K (PbCl ) =1.6×10-5
sp 4 sp 2
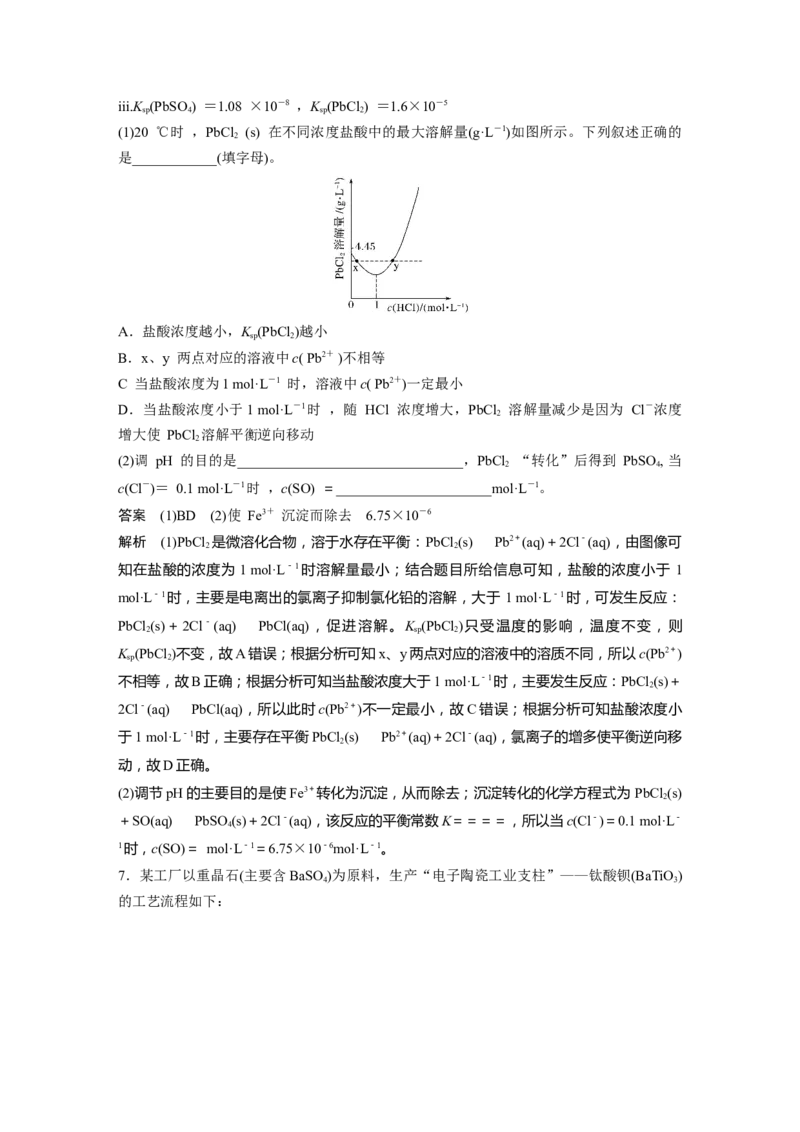
(1)20 ℃时 ,PbCl (s) 在不同浓度盐酸中的最大溶解量(g·L-1)如图所示。下列叙述正确的
2
是____________(填字母)。
A.盐酸浓度越小,K (PbCl )越小
sp 2
B.x、y 两点对应的溶液中c( Pb2+ )不相等
C 当盐酸浓度为1 mol·L-1 时,溶液中c( Pb2+)一定最小
D.当盐酸浓度小于1 mol·L-1时 ,随 HCl 浓度增大,PbCl 溶解量减少是因为 Cl-浓度
2
增大使 PbCl 溶解平衡逆向移动
2
(2)调 pH 的目的是________________________________,PbCl “转化”后得到 PbSO , 当
2 4
c(Cl-)= 0.1 mol·L-1时 ,c(SO) =______________________mol·L-1。
答案 (1)BD (2)使 Fe3+ 沉淀而除去 6.75×10-6
解析 (1)PbCl 是微溶化合物,溶于水存在平衡:PbCl (s)Pb2+(aq)+2Cl-(aq),由图像可
2 2
知在盐酸的浓度为 1 mol·L-1时溶解量最小;结合题目所给信息可知,盐酸的浓度小于 1
mol·L-1时,主要是电离出的氯离子抑制氯化铅的溶解,大于 1 mol·L-1时,可发生反应:
PbCl (s)+2Cl-(aq)PbCl(aq),促进溶解。K (PbCl )只受温度的影响,温度不变,则
2 sp 2
K (PbCl )不变,故A错误;根据分析可知x、y两点对应的溶液中的溶质不同,所以c(Pb2+)
sp 2
不相等,故B正确;根据分析可知当盐酸浓度大于1 mol·L-1时,主要发生反应:PbCl (s)+
2
2Cl-(aq)PbCl(aq),所以此时c(Pb2+)不一定最小,故C错误;根据分析可知盐酸浓度小
于1 mol·L-1时,主要存在平衡PbCl (s)Pb2+(aq)+2Cl-(aq),氯离子的增多使平衡逆向移
2
动,故D正确。
(2)调节pH的主要目的是使Fe3+转化为沉淀,从而除去;沉淀转化的化学方程式为 PbCl (s)
2
+SO(aq)PbSO (s)+2Cl-(aq),该反应的平衡常数K====,所以当c(Cl-)=0.1 mol·L-
4
1时,c(SO)= mol·L-1=6.75×10-6mol·L-1。
7.某工厂以重晶石(主要含BaSO)为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO )
4 3
的工艺流程如下:回答下列问题:
(1)用NaCO 溶液浸泡重晶石(假设杂质不与NaCO 反应),能将BaSO 转化为BaCO ,此反
2 3 2 3 4 3
应的平衡常数K=____________(填写计算结果);若不考虑CO的水解,要使2.33 g BaSO
4
恰好完全转化为BaCO ,则至少需要浓度为1.0 mol·L-1NaCO 溶液______mL。[已知:
3 2 3
K (BaSO)=1.0×10-10,K (BaCO)=5.0×10-9]
sp 4 sp 3
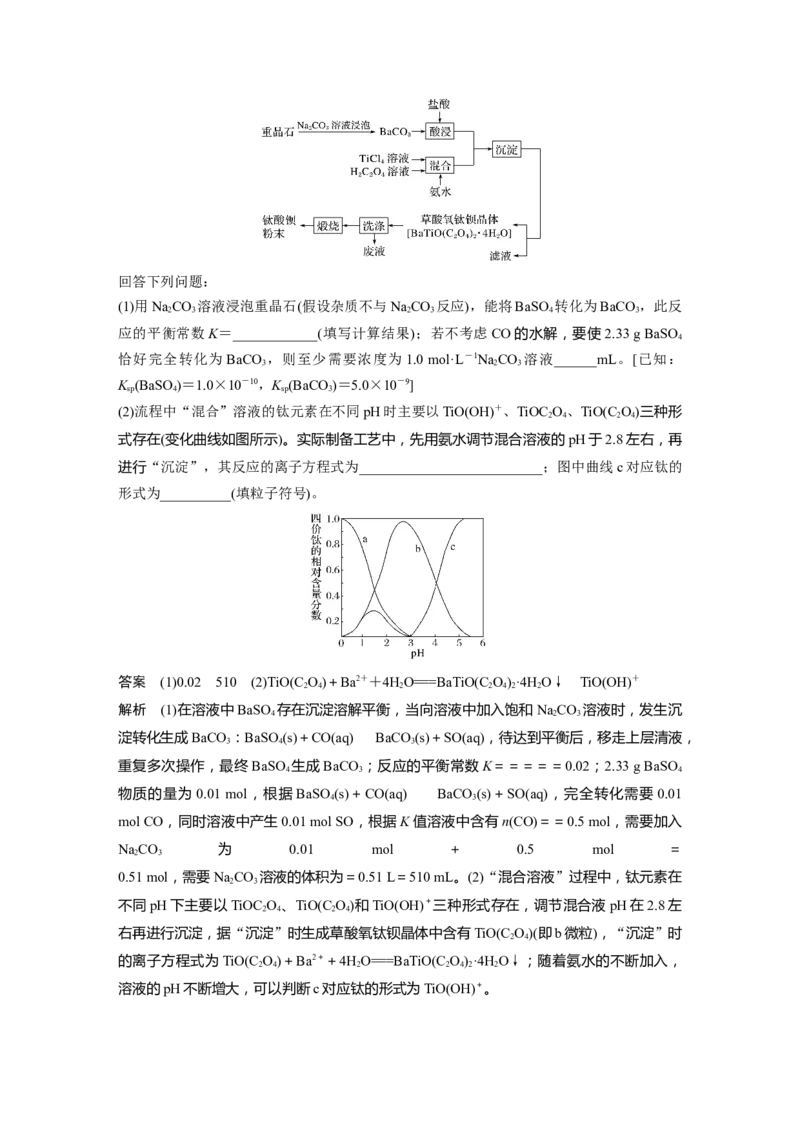
(2)流程中“混合”溶液的钛元素在不同pH时主要以TiO(OH)+、TiOC O、TiO(C O)三种形
2 4 2 4
式存在(变化曲线如图所示)。实际制备工艺中,先用氨水调节混合溶液的pH于2.8左右,再
进行“沉淀”,其反应的离子方程式为__________________________;图中曲线c对应钛的
形式为__________(填粒子符号)。
答案 (1)0.02 510 (2)TiO(C O)+Ba2++4HO===BaTiO(C O)·4H O↓ TiO(OH)+
2 4 2 2 4 2 2
解析 (1)在溶液中BaSO 存在沉淀溶解平衡,当向溶液中加入饱和NaCO 溶液时,发生沉
4 2 3
淀转化生成BaCO :BaSO(s)+CO(aq)BaCO (s)+SO(aq),待达到平衡后,移走上层清液,
3 4 3
重复多次操作,最终BaSO 生成BaCO ;反应的平衡常数K=====0.02;2.33 g BaSO
4 3 4
物质的量为0.01 mol,根据BaSO(s)+CO(aq) BaCO (s)+SO(aq),完全转化需要 0.01
4 3
mol CO,同时溶液中产生0.01 mol SO,根据K值溶液中含有n(CO)==0.5 mol,需要加入
NaCO 为 0.01 mol + 0.5 mol =
2 3
0.51 mol,需要NaCO 溶液的体积为=0.51 L=510 mL。(2)“混合溶液”过程中,钛元素在
2 3
不同pH下主要以TiOC O 、TiO(C O)和TiO(OH)+三种形式存在,调节混合液pH在2.8左
2 4 2 4
右再进行沉淀,据“沉淀”时生成草酸氧钛钡晶体中含有TiO(C O)(即b微粒),“沉淀”时
2 4
的离子方程式为TiO(C O)+Ba2++4HO===BaTiO(C O)·4H O↓;随着氨水的不断加入,
2 4 2 2 4 2 2
溶液的pH不断增大,可以判断c对应钛的形式为TiO(OH)+。