文档内容
角度一 “单膜”电解池
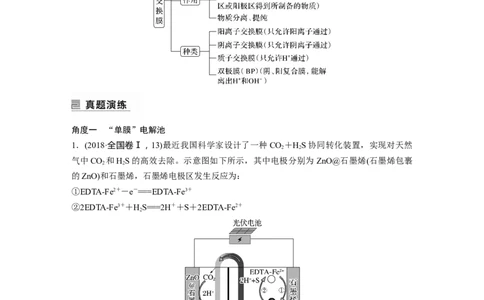
1.(2018·全国卷Ⅰ,13)最近我国科学家设计了一种CO +HS协同转化装置,实现对天然
2 2
气中CO 和HS的高效去除。示意图如下所示,其中电极分别为 ZnO@石墨烯(石墨烯包裹
2 2
的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-===EDTA-Fe3+
②2EDTA-Fe3++HS===2H++S+2EDTA-Fe2+
2
该装置工作时,下列叙述错误的是( )
A.阴极的电极反应:CO+2H++2e-===CO+HO
2 2
B.协同转化总反应:CO+HS===CO+HO+S
2 2 2
C.石墨烯上的电势比ZnO@石墨烯上的低
D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性答案 C
解析 由题中信息可知,石墨烯电极发生氧化反应,为电解池的阳极,则ZnO@石墨烯电极
为阴极。阳极接电源正极,电势高,阴极接电源负极,电势低,故石墨烯上的电势比ZnO@
石墨烯上的高,C项错误;由题图可知,电解时阴极反应式为 CO +2H++2e-===CO+
2
HO,A项正确;将阴、阳两极反应式合并可得总反应式为CO +HS===CO+HO+S,B
2 2 2 2
项正确;Fe3+、Fe2+只能存在于酸性溶液中,D项正确。
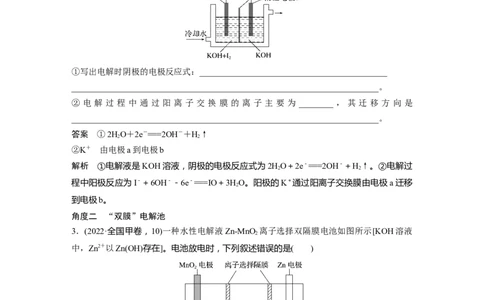
2.[2018·全国卷Ⅲ,27(3)①②]KIO 也可采用“电解法”制备,装置如图所示。
3
①写出电解时阴极的电极反应式:____________________________________________
________________________________________________________________________。
② 电 解 过 程 中 通 过 阳 离 子 交 换 膜 的 离 子 主 要 为 ________ , 其 迁 移 方 向 是
________________________________________________________________________。
答案 ①2HO+2e-===2OH-+H↑
2 2
②K+ 由电极a到电极b
解析 ①电解液是KOH溶液,阴极的电极反应式为2HO+2e-===2OH-+H↑。②电解过
2 2
程中阳极反应为I-+6OH--6e-===IO+3HO。阳极的K+通过阳离子交换膜由电极a迁移
2
到电极b。
角度二 “双膜”电解池
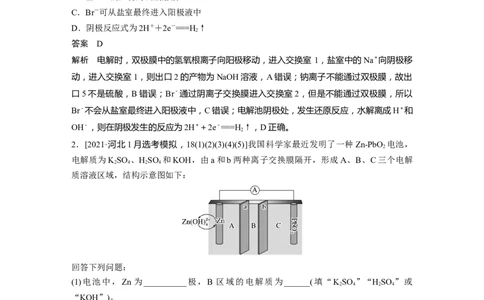
3.(2022·全国甲卷,10)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示[KOH溶液
2
中,Zn2+以Zn(OH)存在]。电池放电时,下列叙述错误的是( )
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO通过隔膜向Ⅱ区迁移
C.MnO 电极反应:MnO +2e-+4H+===Mn2++2HO
2 2 2
D.电池总反应:Zn+4OH-+MnO +4H+===Zn(OH)+Mn2++2HO
2 2
答案 A解析 根据图示的电池结构和题目所给信息可知,Ⅲ区Zn为电池的负极,电极反应为Zn-
2e-+4OH-===Zn(OH),Ⅰ区MnO 为电池的正极,电极反应为MnO +2e-+4H+===Mn2+
2 2
+2HO,K+从Ⅲ区通过隔膜向Ⅱ区迁移,A错误;Ⅰ区的SO通过隔膜向Ⅱ区迁移,B正确;
2
MnO 电极的电极反应式为MnO +2e-+4H+===Mn2++2HO,C正确;电池的总反应为Zn
2 2 2
+4OH-+MnO +4H+===Zn(OH)+Mn2++2HO,D正确。
2 2
角度三 “多膜”电解池
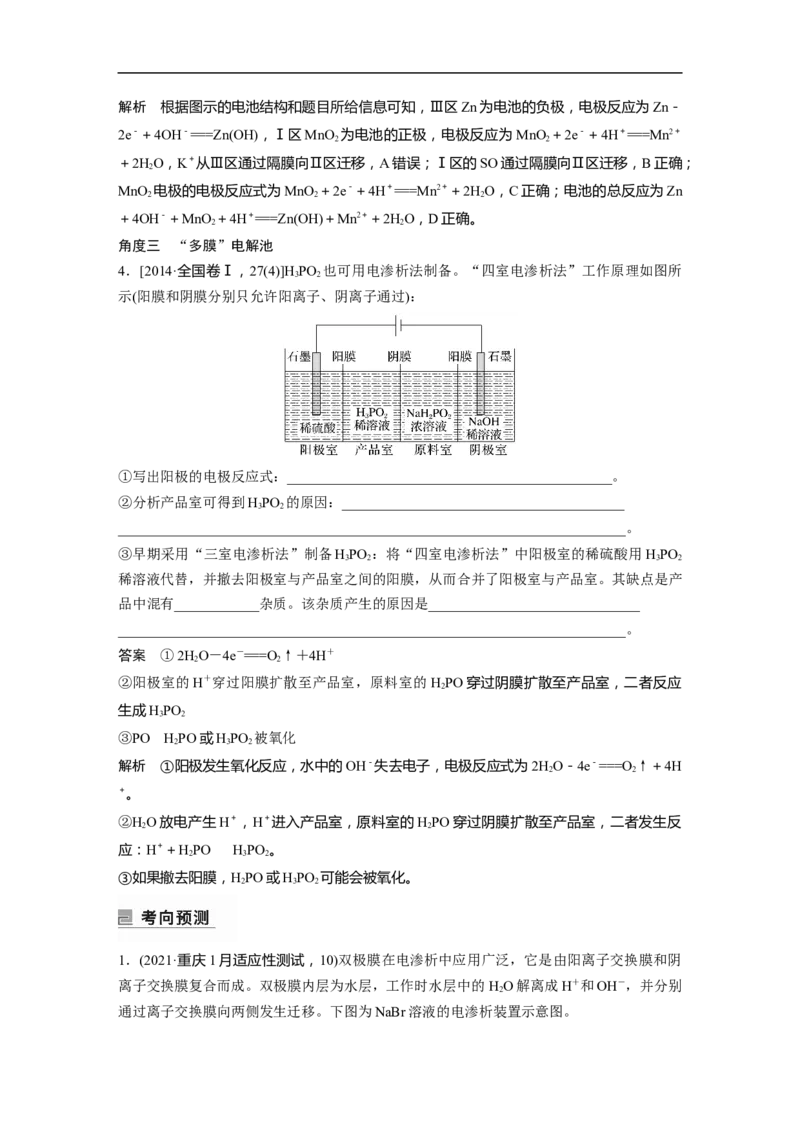
4.[2014·全国卷Ⅰ,27(4)]HPO 也可用电渗析法制备。“四室电渗析法”工作原理如图所
3 2
示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式:______________________________________________。
②分析产品室可得到HPO 的原因:________________________________________
3 2
________________________________________________________________________。
③早期采用“三室电渗析法”制备HPO :将“四室电渗析法”中阳极室的稀硫酸用HPO
3 2 3 2
稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产
品中混有____________杂质。该杂质产生的原因是______________________________
________________________________________________________________________。
答案 ①2HO-4e-===O↑+4H+
2 2
②阳极室的H+穿过阳膜扩散至产品室,原料室的HPO穿过阴膜扩散至产品室,二者反应
2
生成HPO
3 2
③PO HPO或HPO 被氧化
2 3 2
解析 ①阳极发生氧化反应,水中的OH-失去电子,电极反应式为2HO-4e-===O↑+4H
2 2
+。
②HO放电产生H+,H+进入产品室,原料室的HPO穿过阴膜扩散至产品室,二者发生反
2 2
应:H++HPOHPO 。
2 3 2
③如果撤去阳膜,HPO或HPO 可能会被氧化。
2 3 2
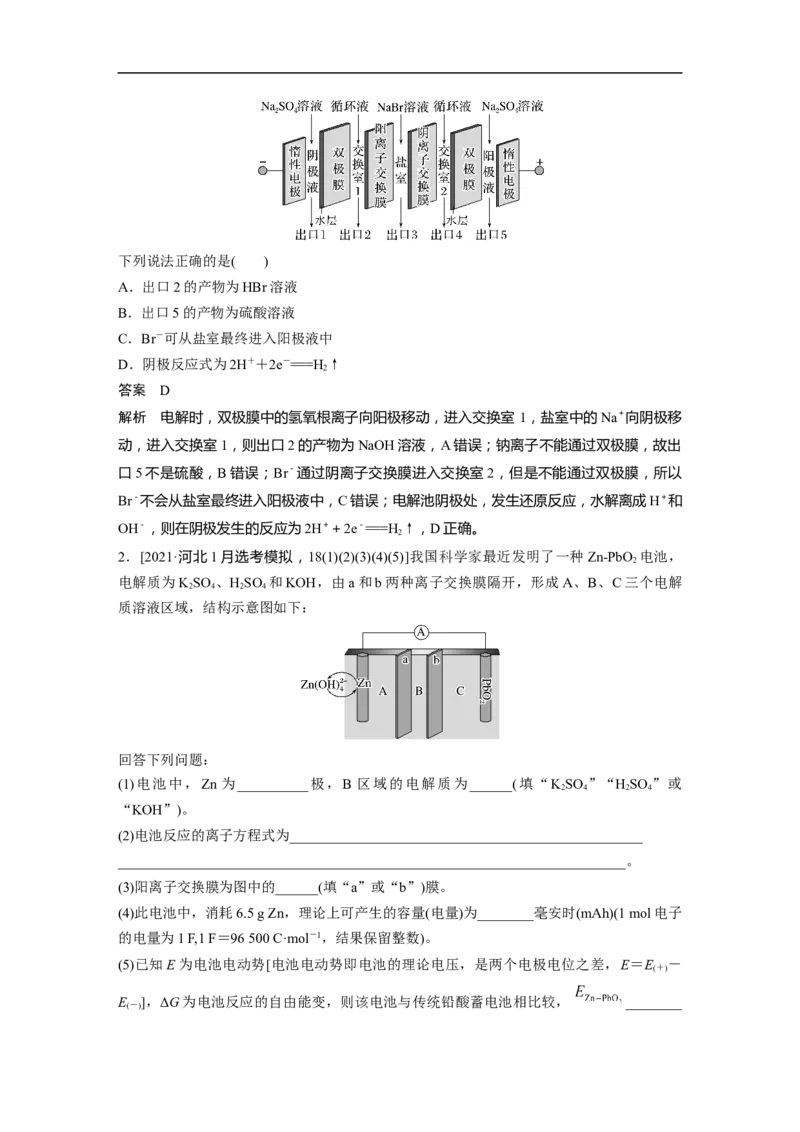
1.(2021·重庆1月适应性测试,10)双极膜在电渗析中应用广泛,它是由阳离子交换膜和阴
离子交换膜复合而成。双极膜内层为水层,工作时水层中的 HO解离成H+和OH-,并分别
2
通过离子交换膜向两侧发生迁移。下图为NaBr溶液的电渗析装置示意图。下列说法正确的是( )
A.出口2的产物为HBr溶液
B.出口5的产物为硫酸溶液
C.Br-可从盐室最终进入阳极液中
D.阴极反应式为2H++2e-===H↑
2
答案 D
解析 电解时,双极膜中的氢氧根离子向阳极移动,进入交换室 1,盐室中的Na+向阴极移
动,进入交换室1,则出口2的产物为NaOH溶液,A错误;钠离子不能通过双极膜,故出
口5不是硫酸,B错误;Br-通过阴离子交换膜进入交换室2,但是不能通过双极膜,所以
Br-不会从盐室最终进入阳极液中,C错误;电解池阴极处,发生还原反应,水解离成H+和
OH-,则在阴极发生的反应为2H++2e-===H↑,D正确。
2
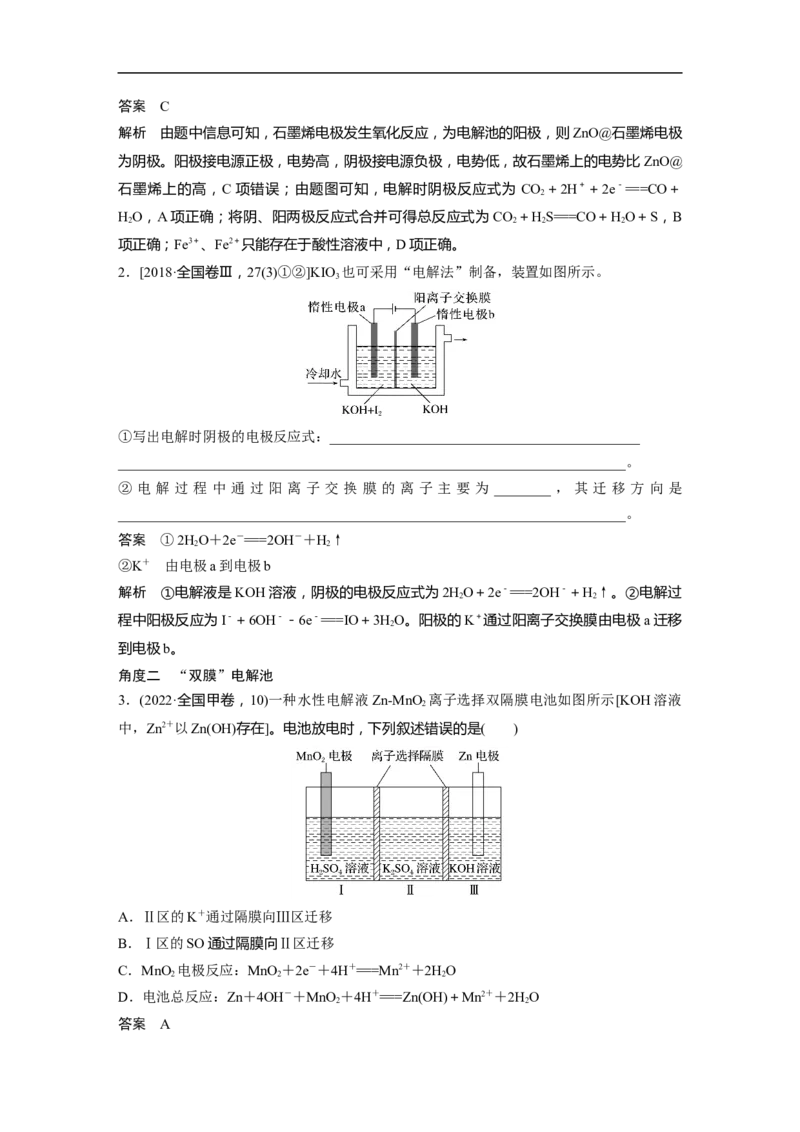
2.[2021·河北1月选考模拟,18(1)(2)(3)(4)(5)]我国科学家最近发明了一种Zn-PbO 电池,
2
电解质为KSO 、HSO 和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解
2 4 2 4
质溶液区域,结构示意图如下:
回答下列问题:
(1)电池中,Zn 为__________极,B 区域的电解质为______(填“KSO ”“HSO ”或
2 4 2 4
“KOH”)。
(2)电池反应的离子方程式为__________________________________________________
________________________________________________________________________。
(3)阳离子交换膜为图中的______(填“a”或“b”)膜。
(4)此电池中,消耗6.5 g Zn,理论上可产生的容量(电量)为________毫安时(mAh)(1 mol电子
的电量为1 F,1 F=96 500 C·mol-1,结果保留整数)。
(5)已知E为电池电动势[电池电动势即电池的理论电压,是两个电极电位之差,E=E -
(+)
E ],ΔG为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较, ________
(-); ____ (填“>”或“<”)。
答案 (1)负 KSO (2)PbO +SO+Zn+2HO===PbSO +Zn(OH) (3)a (4)5 361 (5)>
2 4 2 2 4
<
解析 (1)根据图示可知,Zn电极失去电子生成Zn2+,与溶液中的OH-结合形成Zn(OH),
所以Zn电极为负极;在A区域的电解质为KOH,在B区域的电解质为KSO ,C区域电解
2 4
质为HSO 。(2)负极电极反应式为Zn-2e-+4OH-===Zn(OH),正极的电极反应式为PbO
2 4 2
+2e-+4H++SO===PbSO +2HO,总反应方程式为 PbO +SO+Zn+2HO===PbSO +
4 2 2 2 4
Zn(OH)。(3)A区域是KOH溶液,OH-发生反应生成Zn(OH),为了维持溶液呈电中性,多
余的K+通过交换膜进入到B区域,由于阳离子交换膜只允许阳离子通过,因此a膜为阳离
子交换膜。(4)6.5 g Zn的物质的量是n(Zn)==0.1 mol,则转移电子n(e-)=0.2 mol,1 mol电
子的电量为1 F,1 F=96 500 C·mol-1,转移0.2 mol电子的电量Q=0.2 mol×96 500 C·
mol-1=19 300 C,则理论上可产生的容量(电量)为mAh≈5 361 mAh。(5)由于Zn比Pb活动
性强,正极材料都是 PbO ,所以Zn-PbO 的电势差比Pb-PbO 的电势差大,则 >
2 2 2
;不同电池的电势差越大,电池反应的自由能变就越小,由于Zn-PbO 的电势差比
2
Pb-PbO 的电势差大,所以 < 。
2