文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题06
1.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=11的溶液中:CO Na+、AlO、NO
、
B.无色可使pH试纸变红的溶液中:K+、Na+、MnO SO
、
C.加入Al能放出H 的溶液中:Cl-、HCO SO、NH
2 、
D.由水电离出的c(OH-)=1×10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、CHCOO-
3
答案:A
解析:A.pH=11的溶液,显碱性,该组离子之间不反应,则能够共存,故A正确;
B.MnO B错误;
在水溶液中显紫红色,与无色溶液不符,故
C.加入A1能放出H 的溶液,为酸或强碱溶液,HCO C错误;
2 既能与酸反应又能与碱反应,则不能共存,故
D.由水电离出的c(OH-)=1×10-13mol·L-1的溶液,为酸或碱溶液,酸性溶液CHCOO-会生成
3
醋酸弱电解质,碱溶液中该组离子之间不反应,故D错误;
2.下列离子在对应溶液中能大量共存的是
A.0.1mol·L-1KSCN溶液中:Fe3+、Al3+、NO SO
、
B.0.1mol·L-1HNO 溶液中:Fe2+、Cu2+、Cl-、ClO-
3
C.0.1mol·L-1NaOH溶液中:Na+、K+、SiO S2-
、
D.75%酒精中:Mg2+、H+、Cr O、SO
2
答案:C
解析:A.KSCN溶液中Fe3+与SCN-发生反应,生成一系列红色络合物,不能大量共存,故 A
错误;
B.HNO 溶液中,Fe2+与NO
3 发生氧化还原反应,不能大量共存,故B错误;
C.NaOH溶液中,OH-与Na+、K+、SiO 2-不发生反应,可以大量共存,故C正确;
、S
D.75%酒精中,乙醇与H+、Cr O发生氧化还原反应,不能大量共存,故D错误;
2
3.下列离子反应方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+===Fe2++HO
2
B.漂白粉溶液中通入少量SO :Ca2++2ClO-+SO +HO===CaSO↓+2HClO
2 2 2 3
C.电解饱和食盐水:2Cl-+2H+=====Cl↑+H↑
2 2
D.Al溶于NaOH溶液:2Al+2OH-+2HO===2AlO -+3H↑
2 2 2
答案:D
解析:A.硝酸具有强氧化性,FeO会被氧化成Fe3+,A错误;B.CaSO 和HClO会继续反应
3
生成CaSO,B错误;C.水不可拆,C错误;D.Al和NaOH反应,D正确。
4
4.下列离子方程式正确的是
A.过量SO 通入NaClO溶液中:SO H OClO-HClOHSO
2 2 2
B.向碳酸氢镁溶液中加入过量的NaOH溶液:Mg2++2HCO -=MgCO↓+CO O
+2OH 3 +2H2
C.向含1molFeBr 的溶液中通入标准状况下22.4LCl 时,发生的反应为:2Fe2++2Br-
2 2+2Cl=2Fe3++Br +4Cl-
2 2
D.向NaHSO 溶液中滴入Ba(OH) 溶液至恰好显中性:H++SO+Ba2++OH-=HO+BaSO↓
4 2 2 4
答案:C
解析:A.二氧化硫有还原性,次氯酸根离子有氧化性,两者发生氧化还原反应生成硫酸根离
子和氯离子,A错误;
B.向碳酸氢镁溶液中加入过量的NaOH溶液,应生成氢氧化镁沉淀,B错误;
C.向含1molFeBr 的溶液中通入标准状况下22.4LCl 时,发生的反应为:2Fe2++2Br-+2Cl=
2 2 2
2Fe3++Br +4Cl-,C正确;
2
D.向NaHSO 溶液中滴入Ba(OH) 溶液至恰好显中性,离子方程式为:2H++SO+Ba2++2OH-=
4 2
2HO+BaSO↓,D错误;
2 4
5.下列离子方程式正确的是
A.向NaHSO 溶液中滴加过量Ba(OH) 溶液:2H++SO 2++2OH-=BaSO↓+2H O
4 2 +Ba 4 2
B.用碳酸钠溶液吸收少量二氧化硫:2CO +H O=2HCO -+SO
+SO2 2 3
C.将少量SO 气体通入NaClO溶液中:SO +2ClO-+H O=SO
2 2 2 +2HClO
D.向碳酸氢钠溶液中加入氢氧化钠:HCO -=CO↑+H O
+ OH 2 2
答案:B
解析:A.Ba(OH) 是过量,NaHSO 是少量,系数为1,即离子反应方程式为:H++SO 2+
2 4 +Ba
+OH-=HO+BaSO↓,故A错误;
2 4
B.碳酸钠溶液跟酸反应先生成NaHCO ,故B正确;
3
C.次氯酸具有强氧化性能把SO SO
氧化成 ,故C正确;
D.反应前后电荷不守恒,正确的是:HCO -=H O+CO
+OH 2 ,故D错误。
6.下列离子方程式中,能正确表达反应颜色变化的是
A.向Mg(OH) 浊液中滴加足量FeCl 溶液出现红褐色沉淀:3Mg(OH) +2Fe3+=2Fe(OH) +3Mg2+
2 3 2 3
B.将“84”消毒液和洁厕灵混用会产生黄绿色气体:ClO-+Cl-+H O=Cl ↑+2OH-
2 2
C.将SO 通入溴水中使其褪色:SO +2HO+Br =2H++SO+2HBr
2 2 2 2
D.NaO 在空气中放置后由淡黄色变为白色:2NaO=2Na O+O↑
2 2 2 2 2 2
答案:A
解析:A.由于Fe(OH) 比Mg(OH) 的溶度积更小,所以向Mg(OH) 浊液中滴加足量FeCl 溶液
3 2 2 3
出现红褐色Fe(OH) 沉淀,离子方程式为:3Mg(OH) +2Fe3+=2Fe(OH) +3Mg2+,A正确;
3 2 3
B.“84”消毒液的主要成分为NaClO,洁厕灵的主要成分为盐酸,二者混用会生成 Cl ,离子
2
方程式为:ClO-+Cl-+2H+=Cl↑+H O,B不正确;
2 2
C.HBr为强酸,将SO 通入溴水中使其褪色,离子方程式为:SO +2HO+Br =4H++SO+
2 2 2 2
2Br-,C不正确;
D.NaO 在空气中放置后,会与空气中的水蒸气和二氧化碳反应,从而由淡黄色变为白色,
2 2
而不是发生分解反应,D不正确;
7.25℃时,下列各组离子在指定溶液中一定能大量共存的是A.pH=1的溶液:Ba2+、NO +
、K
B.某无色溶液:Al3+、Na+、HCO
C.能使酚酞变红的溶液:Fe3+、Cl-、I-
D.水电离的c(H+)=1×10-11mol/L的溶液:K+、HCO -
、Cl
答案:A
解析:A.pH=1的溶液呈酸性,这几种离子之间不反应且都和H+不反应,所以能大量共存,
故A正确;
B.Al3+、HCO
发生双水解反应而不能共存,故B错误;
C.能使酚酞试液变红色的溶液呈碱性,能和OH-反应的离子不能大量共存,Fe3+、I-发生氧化
还原反应生成Fe2+和I 而不能大量共存,且OH-和Fe3+反应而不能大量共存,故C错误;
2
D.水电离的c(H+)=1×10-11mol/L的溶液中,水的电离被抑制,溶液呈强酸性或强碱性,H+、
HCO 和HO而不能大量共存,HCO -反应生成碳酸根和HO而不能大量共存,故D错误;
反应生成CO2 2 、OH 2
8.宏观辨识与微观探析是化学学科核心素养之一。下列实验对应的反应方程式书写正确的是
A.NaO 放入水中:NaO+2HO=2Na++2OH-+O↑
2 2 2 2 2 2
B.Fe在Cl 中燃烧:Fe+Cl=====FeCl
2 2 2
C.浓硝酸见光分解:4HNO=====4NO↑+3O↑+2HO
3 2 2
D.盐酸中滴加NaSiO 溶液:2H++SiO HSiO
2 3 = 2 3
答案:D
解析:A.方程式没有配平,氢原子不守恒,A错误;
B.铁在氯气中燃烧生成氯化铁,B错误;
C.浓硝酸分解生成二氧化氮,C错误;
D.强酸制弱酸,盐酸与硅酸钠反应生成硅酸沉淀,D正确;
9.常温时下列各组离子在指定溶液中一定能大量共存的是
A. 0.1mol·L-1的硫酸溶液中:K+、Na+、Cl-、SO
2
B. 中性溶液中:Fe3+、NH、SO、NO
C. 水电离产生的c(OH-)=1×10-12mol·L-1的溶液中:Na+、Al3+、NO -
、Br
D. 澄清透明溶液中:Cu2+、SO、H+、Cl-
答案:D
解析:A.H+和SO
2 会反应生成硫、二氧化硫和水,不能大量共存,A错误;
B.中性溶液中,Fe3+会发生水解生成氢氧化铁沉淀,不能大量共存,B错误;
C.水电离产生的c(OH-)=1×10-12mol·L-1的溶液呈酸性或碱性,Al3+和OH-会反应生成氢氧化
铝沉淀,不能大量共存,C错误;
D.澄清透明溶液中,四种离子相互之间不反应,能大量共存,D正确;
10.下列有关氯气的离子方程式中书写正确的是
A. 向亚硫酸钠溶液中通入少量氯气:SO Cl+HO=SO+2Cl-+2H+
+ 2 2
B. 将氯气通入冷的石灰乳中制取漂白粉:Ca(OH) +Cl=Ca2++Cl-+ClO-+HO
2 2 2C. 将少量氯气通入到碘化亚铁溶液中:2Fe2++Cl=2Fe3++2Cl-
2
D. 食醋和84消毒液混合:Cl-+ClO-+2H+=Cl↑+HO
2 2
答案:B
解析:A.亚硫酸钠溶液中通入少量氯气反应生成氯化钠、硫酸钠和亚硫酸氢钠,离子方程式
为:3SO +H O=SO+2Cl-+2HSO
+Cl2 2 ,故A错误;
B.将氯气通入石灰乳中制取漂白粉,离子方程式:Ca(OH) +Cl=Ca2++Cl-+ClO-+HO,
2 2 2
故B正确;
C.碘化亚铁溶液通入少量氯气,溶液中碘离子还原性大于亚铁离子,氯气只氧化碘离子,离
子方程式为2I-+Cl=2Cl-+I ,故C错误;
2 2
D.将食醋与“84”消毒液混合产生黄绿色气体:2CHCOOH+Cl-+ClO-=
3
Cl↑+H O+2CHCOO-,故D错误;
2 2 3
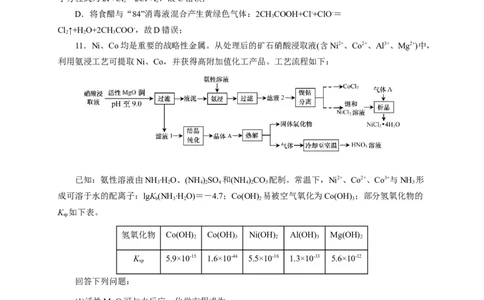
11.Ni、Co均是重要的战略性金属。从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,
利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由NH ∙HO、(NH )SO 和(NH )CO 配制。常温下,Ni2+、Co2+、Co3+与NH 形
3 2 4 2 4 4 2 3 3
成可溶于水的配离子:lgK (NH ∙HO)=-4.7;Co(OH) 易被空气氧化为Co(OH) ;部分氢氧化物的
b 3 2 2 3
K 如下表。
sp
氢氧化物 Co(OH) Co(OH) Ni(OH) Al(OH) Mg(OH)
2 3 2 3 2
K 5.9×10-15 1.6×10-44 5.5×10-16 1.3×10-33 5.6×10-12
sp
回答下列问题:
(1)活性MgO可与水反应,化学方程式为_________________________________________。
(2)常温下,pH=9.9的氨性溶液中,c(NH ∙HO) ___________c(NH) (填“>”“<”或“=”)。
3 2
(3)“氨浸”时,由Co(OH) 转化为[Co(NH )]2+的离子方程式为___________________________。
3 3 6
(4) (NH )CO 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射
4 2 3
图谱中,出现了NH Al(OH) CO 的明锐衍射峰。
4 2 3
①NH Al(OH) CO 属于___________(填“晶体”或“非晶体”)。
4 2 3
②(NH )CO 提高了Ni、Co的浸取速率,其原因是____________________________________。
4 2 3(5)①“析晶”过程中通入的酸性气体A为___________。
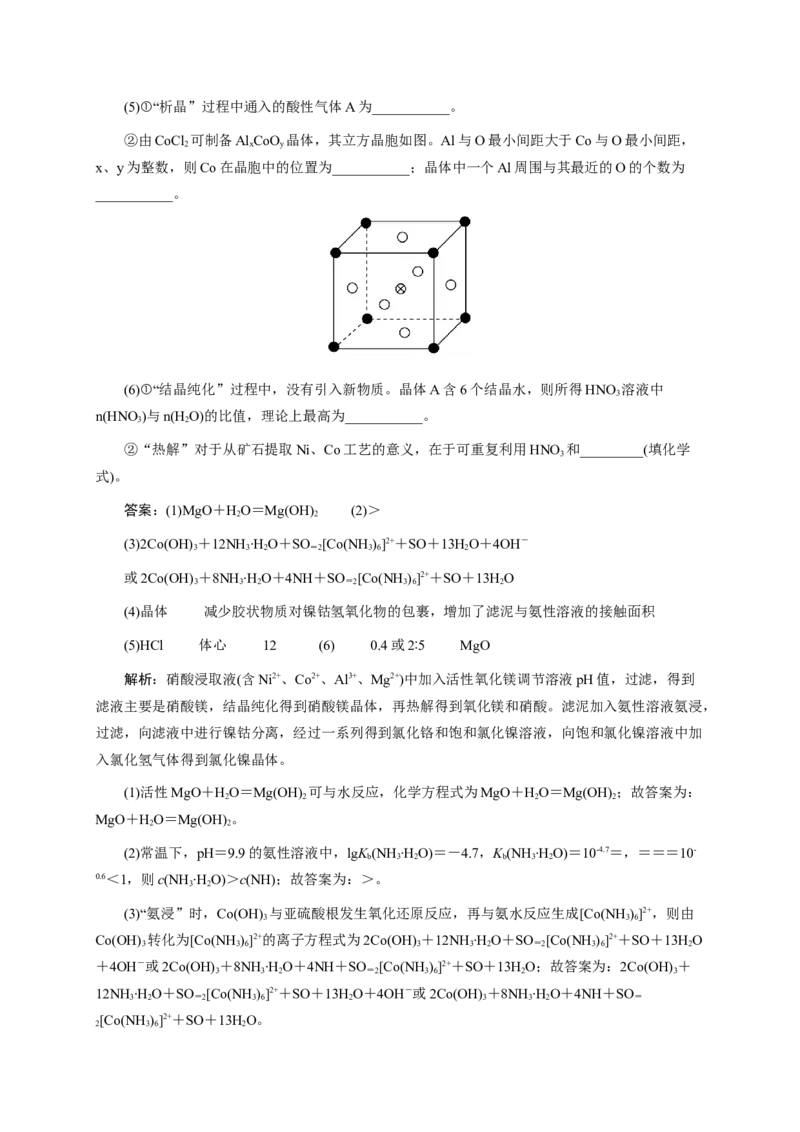
②由CoCl 可制备Al CoO 晶体,其立方晶胞如图。Al与O最小间距大于Co与O最小间距,
2 x y
x、y为整数,则Co在晶胞中的位置为___________;晶体中一个Al周围与其最近的O的个数为
___________。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得HNO 溶液中
3
n(HNO)与n(HO)的比值,理论上最高为___________。
3 2
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO 和_________(填化学
3
式)。
答案:(1)MgO+HO=Mg(OH) (2)>
2 2
(3)2Co(OH) +12NH ∙HO+SO [Co(NH )]2++SO+13HO+4OH-
3 3 2 =2 3 6 2
或2Co(OH) +8NH ∙HO+4NH+SO [Co(NH )]2++SO+13HO
3 3 2 =2 3 6 2
(4)晶体 减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触面积
(5)HCl 体心 12 (6) 0.4或2∶5 MgO
解析:硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中加入活性氧化镁调节溶液pH值,过滤,得到
滤液主要是硝酸镁,结晶纯化得到硝酸镁晶体,再热解得到氧化镁和硝酸。滤泥加入氨性溶液氨浸,
过滤,向滤液中进行镍钴分离,经过一系列得到氯化铬和饱和氯化镍溶液,向饱和氯化镍溶液中加
入氯化氢气体得到氯化镍晶体。
(1)活性MgO+HO=Mg(OH) 可与水反应,化学方程式为MgO+HO=Mg(OH) ;故答案为:
2 2 2 2
MgO+HO=Mg(OH) 。
2 2
(2)常温下,pH=9.9的氨性溶液中,lgK (NH ∙HO)=-4.7,K (NH ∙HO)=10-4.7=,===10-
b 3 2 b 3 2
0.6<1,则c(NH ∙HO)>c(NH);故答案为:>。
3 2
(3)“氨浸”时,Co(OH) 与亚硫酸根发生氧化还原反应,再与氨水反应生成[Co(NH )]2+,则由
3 3 6
Co(OH) 转化为[Co(NH )]2+的离子方程式为2Co(OH) +12NH ∙HO+SO [Co(NH )]2++SO+13HO
3 3 6 3 3 2 =2 3 6 2
+4OH-或2Co(OH) +8NH ∙HO+4NH+SO [Co(NH )]2++SO+13HO;故答案为:2Co(OH) +
3 3 2 =2 3 6 2 3
12NH ∙HO+SO [Co(NH )]2++SO+13HO+4OH-或2Co(OH) +8NH ∙HO+4NH+SO
3 2 =2 3 6 2 3 3 2 =
[Co(NH )]2++SO+13HO。
2 3 6 2(4)(NH )CO 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图
4 2 3
谱中,出现了NH Al(OH) CO 的明锐衍射峰。
4 2 3
①X射线衍射图谱中,出现了NH Al(OH) CO 的明锐衍射峰,则NH Al(OH) CO 属于晶体;故
4 2 3 4 2 3
答案为:晶体。
②根据题意(NH )CO 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物,则(NH )CO
4 2 3 4 2 3
能提高了Ni、Co的浸取速率,其原因是减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性
溶液的接触面积;故答案为:减少胶状物质对镍钴氢氧化物的包裹,增加了滤泥与氨性溶液的接触
面积。
(5)①“析晶”过程中为了防止Ni2+水解,因此通入的酸性气体A为HCl;故答案为:HCl。
②由CoCl 可制备Al CoO 晶体,其立方晶胞如图。x、y为整数,根据图中信息Co、Al都只
2 x y
有一个原子,而氧(白色)原子有3个,Al与O最小间距大于Co与O最小间距,则Al在顶点,因此
Co在晶胞中的位置为体心;晶体中一个Al周围与其最近的O原子,以顶点Al分析,面心的氧原
子一个横截面有4个,三个横截面共12个,因此晶体中一个Al周围与其最近的O的个数为12;故
答案为:体心;12。
(6)①“结晶纯化”过程中,无引新物质入。晶体A含6个结晶水,则晶体A为
Mg(NO)∙6HO,根据Mg(NO)+2HO Mg(OH) +2HNO,Mg(OH) ===MgO+HO,还剩余5
3 2 2 3 2 2 2 3 2 2
个水分子,因此所得HNO 溶液中n(HNO)与n(HO)的比值理论上最高为2∶5;故答案为:0.4或
3 3 2
2∶5。
②“热解”对于从矿石提取Ni、Co工艺的意义,根据前面分析Mg(NO)+2HO Mg(OH)
3 2 2 2
+2HNO,Mg(OH) ===MgO+HO,在于可重复利用HNO 和MgO;故答案为:MgO。
3 2 2 3
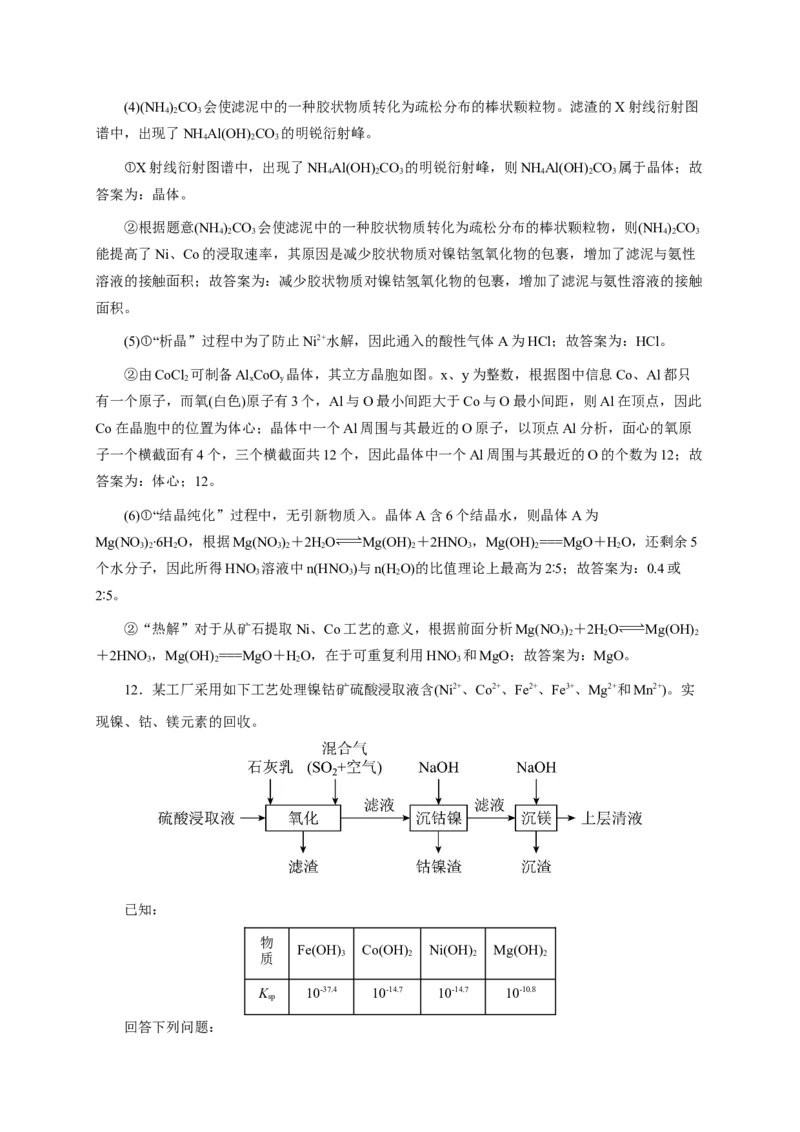
12.某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+)。实
现镍、钴、镁元素的回收。
已知:
物
Fe(OH) Co(OH) Ni(OH) Mg(OH)
质 3 2 2 2
K 10-37.4 10-14.7 10-14.7 10-10.8
sp
回答下列问题:(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为_____________(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H SO ),1mol
2 5
HSO 中过氧键的数目为_______。
2 5
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,该反应的离子方程式为____
2 5 2
____________________(HSO 的电离第一步完全,第二步微弱);滤渣的成分为MnO 、_______(填
2 5 2
化学式)。
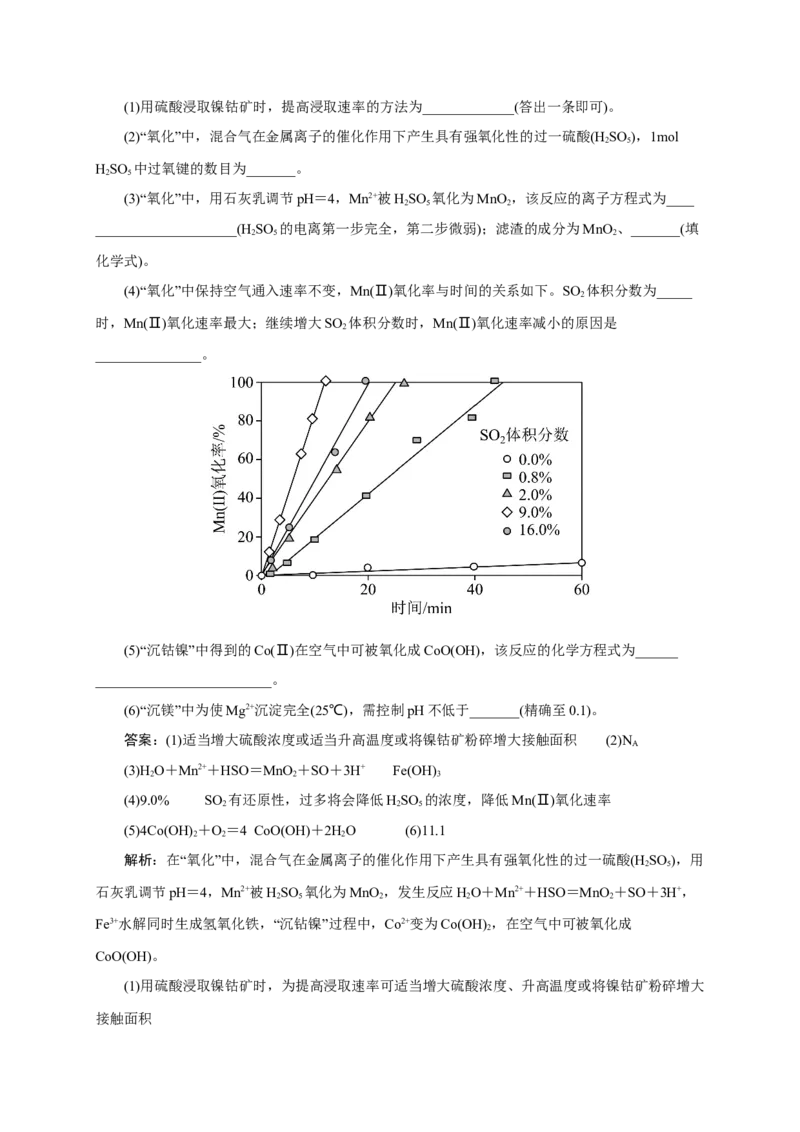
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。SO 体积分数为_____
2
时,Mn(Ⅱ)氧化速率最大;继续增大SO 体积分数时,Mn(Ⅱ)氧化速率减小的原因是
2
_______________。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为______
_________________________。
(6)“沉镁”中为使Mg2+沉淀完全(25℃),需控制pH不低于_______(精确至0.1)。
答案:(1)适当增大硫酸浓度或适当升高温度或将镍钴矿粉碎增大接触面积 (2)N
A
(3)HO+Mn2++HSO=MnO +SO+3H+ Fe(OH)
2 2 3
(4)9.0% SO 有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速率
2 2 5
(5)4Co(OH) +O=4 CoO(OH)+2HO (6)11.1
2 2 2
解析:在“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H SO ),用
2 5
石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,发生反应HO+Mn2++HSO=MnO +SO+3H+,
2 5 2 2 2
Fe3+水解同时生成氢氧化铁,“沉钻镍”过程中,Co2+变为Co(OH) ,在空气中可被氧化成
2
CoO(OH)。
(1)用硫酸浸取镍钴矿时,为提高浸取速率可适当增大硫酸浓度、升高温度或将镍钴矿粉碎增大
接触面积(2) H SO 的结构简式为 ,所以1mol HSO 中过氧键的数目为N
2 5 2 5 A
(3)用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,该反应的离子方程式为:HO+Mn2++
2 5 2 2
HSO=MnO +SO+3H+;氢氧化铁的Ksp=10-37.4,当铁离子完全沉淀时,溶液中c(Fe3+)=10-5mol/L,
2
K [Fe(OH) ]=c(Fe3+)c3(OH-)=10-5×c3(OH-)=10-37.4,c(OH-)=10-10.8mol/L,根据Kw=10-14,pH=
sp 3
3.2,此时溶液的pH=4,则铁离子完全水解,生成氢氧化铁沉淀,故滤渣还有氢氧化铁;
(4)根据图示可知SO 体积分数为0.9%时,Mn(Ⅱ)氧化速率最大;继续增大SO 体积分数时,
2 2
由于SO 有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速率
2 2 5
(5)“沉钻镍”中得到的Co(OH) ,在空气中可被氧化成CoO(OH),该反应的化学方程式为:
2
4Co(OH) +O=4 CoO(OH)+2HO;
2 2 2
(6)Ksp[Mg(OH) ]=10-10.8, 当镁离子完全沉淀时,c(Mg2+)=10-5mol/L,根据Ksp可计算c(OH-)
2
=10-2.9mol/L,根据Kw=10-14,c(H+)=10-11.1mol/L,所以溶液的pH=11.1;