文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题08
1.下列离子方程式书写正确的是
A. 用饱和碳酸钠除去乙酸乙酯中的少量乙酸:2CHCOOH+CO COO-+CO ↑+H O
3 =2CH3 2 2
B. 硫氢化钠溶液与稀硫酸混合有气泡产生:HS-+SO+7H+=2SO↑+4H O
2 2
C. 将碳酸氢钙溶液与过量的澄清石灰水混合:Ca2++HCO -=CaCO ↓+H O
+OH 3 2
D. 向HO 溶液中滴加少量FeCl :2Fe3++H O=O ↑+2H++2Fe2+
2 2 3 2 2 2
答案:C
解析:A.用饱和碳酸钠除去乙酸乙酯中的少量乙酸,根据以少定多原则,其离子方程式应为:
CHCOOH+CO COO-+HCO A项错误;
3 =CH3 ,故
B.稀硫酸没有氧化性,与硫氢化钠溶液混合有气泡产生是因为生成了硫化氢气体,故其离子
方程式为:HS-+H+=H S↑,故B项错误;
2
C.将碳酸氢钙溶液与过量的澄清石灰水混合,根据以少定多原则,碳酸氢根的化学计量数为
1,故其离子方程式为:Ca2++HCO -=CaCO ↓+H O,故C项正确;
+OH 3 2
D.过氧化氢不能还原氧化铁,故该反应不发生,故D项错误。
2.汽车发生剧烈碰撞时,安全气囊中迅速发生反应:10NaN +2KNO=KO+5NaO+16N↑。
3 3 2 2 2
下列说法正确的是
A. 该反应中KNO 是还原剂
3
B. 氧化产物与还原产物的物质的量之比为15∶1
C. 若设计成原电池,KNO 在负极上反应
3
D. 每转移1mole-,可生成2.24LN
2
答案:B
解析:A.KNO 中N元素反应后化合价降低,为氧化剂,NaN 中N元素的化合价由-升高为
3 3
0,是还原剂,故A错误;
B.根据方程式知,叠氮化钠是还原剂、硝酸钾是氧化剂,还原剂和氧化剂的物质的量之比为
10∶2=5∶1,一个叠氮化钠中含有3个N原子,所以被氧化和被还原的N原子的物质的量之比为
15:1,即氧化产物与还原产物的物质的量之比为15:1,故B正确;
C.由选项A分子可知,在该反应中KNO 为氧化剂,则若设计成原电池,KNO 在正极上反应,
3 3
故C错误;
D.由反应可知转移10mol电子生成16mol氮气,则每转移1mol电子,可生成N 为1.6mol,
2
标准状况下N 的体积为35.84L,故D错误;
2
3.下列离子方程式书写正确的是
A.NaHCO 溶液的水解:HCO HO CO HO+
3 + 2 + 3
B. 向Al (SO ) 溶液中滴加NaCO 溶液:2Al3++3CO Al (CO)↓
2 4 3 2 3 = 2 3 3
C. 向Fe (SO ) 溶液中通入足量HS:2Fe3++S2-=2Fe2++S↓
2 4 3 2
D. 向Ca(ClO) 溶液中通入少量SO :Ca2++3ClO-+HO+SO =Cl-+CaSO↓+2HClO
2 2 2 2 4答案:D
解析:A.碳酸氢根离子水解生成碳酸分子和氢氧根离子,水解方程式为:HCO HO
+ 2
HCO+OH-,A错误;
2 3
B.铝离子和碳酸根离子发生双水解,生成氢氧化铝和二氧化碳,离子方程式为:2Al3++3CO
3HO=2Al (CO)↓+3CO↑,B错误;
+ 2 2 3 3 2
C.硫化氢是弱电解质,不能拆,并且三价铁可以把硫离子氧化为单质硫,则离子方程式为:
2Fe3++HS=2Fe2++S↓+2H+,C错误;
2
D.次氯酸根离子有强氧化性,可以将二氧化硫中+4价硫氧化为硫酸根离子,并且二氧化硫少
量,最终应该同时生成次氯酸,则离子方程式为:Ca2++3ClO-+HO+SO =Cl-+CaSO↓+
2 2 4
2HClO,D正确;
4.下列物质中常作耐高温材料的碱性氧化物是
A. K O B. SiO C.Al O D. MgO
2 2 2 3
答案:D
解析:A.KO虽然为碱性氧化物,但其熔点不高,A不符合题意;
2
B.SiO 对应的酸为硅酸,属于酸性氧化物,B不符合题意;
2
C.Al O 为两性氧化物,C不符合题意;
2 3
D.MgO对应的碱为氢氧化镁,属于碱性氧化物,其离子半径较小,晶格能大,熔点高,可作
耐高温材料,D符合题意;
5.关于反应2Fe(CO) +7NO=2FeO+14NO+10CO,下列说法正确的是
5 2 4 2
A. N O 发生氧化反应 B. 生成1molCO ,转移2mol电子
2 4 2
C. 氧化产物与还原产物的物质的量之比为5∶7 D. FeO 可以和Fe反应生成Fe O
2 2 3
答案:D
解析:在反应2Fe(CO) +7NO=2FeO+14NO+10CO 中,Fe由0价升高到+4价,C由+2价
5 2 4 2 2
升高到+4价,N由+4价降低到+2价;电子转移的数目为28e-。
A.NO 中N元素由+4价降低到+2价,化合价降低,得电子发生还原反应,A不正确;
2 4
B.在该反应中,转移电子数目为28e-,则生成1molCO ,转移2.8mol电子,B不正确;
2
C.氧化产物为FeO、CO,还原产物为NO,则氧化产物与还原产物的物质的量之比为
2 2
12:14=6:7,C不正确;
D.FeO 中Fe显+4价,Fe O 中Fe显+3价,则含+4价铁的FeO 和Fe反应,可以生成Fe O,
2 2 3 2 2 3
D正确;
6. 下列反应的离子方程式正确的是
A. Na O 加入到足量的HO中:NaO+HO=2Na++2OH-+O↑
2 2 2 2 2 2 2
B. 少量澄清石灰水与足量Ca(HCO ):Ca2++OH-+HCO CaCO ↓+HO
3 2 = 3 2
C. 过量铁粉加入稀硝酸:Fe+4H++NO Fe3++NO↑+2HO
= 2
D. 水中通入氯气:Cl+HO 2H++Cl-+ClO-
2 2
答案:B解析:A.过氧化钠加水中过氧化钠做氧化剂和还原剂,反应的离子方程式为2NaO+2HO=
2 2 2
4Na++4OH-+O↑,A错误;
2
B.氢氧化钙和碳酸氢钙反应生成碳酸钙和水,反应的离子方程式为Ca2++OH-+HCO
=
CaCO ↓+HO,B正确;
3 2
C.过量的铁和硝酸反应生成硝酸亚铁,离子方程式为:3Fe+8H++2NO Fe3++2NO↑+
=3
4HO,C错误;
2
D.氯气和水反应生成盐酸和次氯酸,次氯酸不能拆成离子形式,离子方程式为:Cl+HO
2 2
H++Cl-+HClO,D错误;
7.下列叙述不涉及氧化还原反应的是
A. 海水提溴 B. 苏打用作食用碱
C. 谷物发酵酿酒 D. 漂白粉久置空气中失效
答案:B
解析:A.海水提溴,是将化合态的溴转化为溴单质再分离出来的过程,涉及氧化还原反应,
故A错误;
B.苏打用作食用碱,是碳酸钠和酸反应的过程,其属于复分解反应,因而不涉及氧化还原反
应,故B正确;
C.谷物发酵酿造食醋的过程为:淀粉水解生成葡萄糖,葡萄糖在酶的作用下生成乙醇,乙醇
氧化生成醋酸的过程,涉及氧化还原反应,故C错误;
D.漂白粉久置与空气中时次氯酸钙与水、二氧化碳反应生成碳酸钙和次氯酸,次氯酸易分解,
分解后生成盐酸和氧气,从而变质,其过程中涉及氧化还原反应,故D错误;
8.下列消毒剂的有效成分属于盐的是
A. 高锰酸钾溶液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
答案:A
解析:A.高锰酸钾溶液的有效成分为KMnO ,其在水溶液中电离出K+和MnO 属于盐,
4 ,故KMnO4
A符合题意;
B.过氧乙酸溶液的有效成分是CHCOOOH,在水溶液中电离出CHCOOO-和H+,即水溶液
3 3
中的阳离子全部为H+,故其属于酸,不合题意;
C.双氧水是由H和O组成的化合物,故其属于氧化物,C不合题意;
D.医用酒精的有效成分为CHCHOH,其属于有机物,不属于盐,D不合题意;
3 2
9.某工业废水中可能含有K+、Ag+、Mg2+、Cu2+、Al3+、NH、Cl-、CO NO SO、I-中的几种,
、 、
且各离子物质的量浓度均为0.2mol/L(忽略水的电离及离子的水解),欲探究废水的组成,进行了如
下实验:
I.取该无色溶液5mL,滴加一滴氨水有沉淀生成,且离子种类增加
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇到空气变为红棕色
IV.向III中所得溶液中加入BaCl 溶液,有白色沉淀生成。
2下列推断不正确的是
A. 溶液中一定不含的阳离子是K+、NH、Cu2+、Ag+
B. III中加入盐酸生成无色气体的离子方程式为:8H++6I-+2NO +2NO↑+4HO
=3I2 2
C. 原溶液除H+和OH-外只含有Mg2+、Al3+、NO SO、I-
、
D. 另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤、洗涤、灼烧沉淀至恒重,
得到固体质量0.8g
答案:C
解析:I.取该无色溶液5 mL,说明一定不含有Cu2+,滴加一滴氨水有沉淀生成,且离子种类
增加,说明增加的是NH,所以原溶液中一定不含NH,可能含有Mg2+、Al3+,不含NH、CO
;
II.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰,说明没有K+;
III.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然
澄清,说明有还原性离子I-与NO +反应生成NO,即溶液中有I-、NO +。
和H ,一定不含有Ag
IV.向III中所得的溶液中加入BaCl 溶液,有白色沉淀生成,说明有SO;
2
综上所述,一定含有的阴离子为NO SO、I-,各离子物质的量浓度均为0.2mol/L,结合电荷守
、
恒可知,溶液中一定有Mg2+和Al3+,且还含有一种-1价的阴离子为Cl-,以此解答。
A.由分析可知,溶液中一定不含的阳离子是K+、NH、Cu2+、Ag+,故A正确;
B.III中加入盐酸,I-与NO +反应生成NO,根据得失电子守恒和电荷守恒配平离子方程式
和H
为:8H++6I-+2NO 3I+2NO↑+4HO,故B正确;
= 2 2
C.由分析可知,原溶液除H+和OH-外只含有Mg2+、Al3+、NO SO、I-、Cl-,故C错误;
、
D.另取100 mL原溶液,加入足量的NaOH溶液,Mg2+、Al3+反应生成Mg(OH) 、NaAlO ,充
2 2
分反应后过滤,洗涤,灼烧沉淀至恒重,根据元素守恒:n(MgO)=n(Mg2+)=cV=0.2 mol/L×0.1
L=0.02 mol,m(MgO)=0.02 mol×40 g/mol=0.8 g,故D正确;
10. 能正确表示下列反应的离子方程式的是
A. 小苏打溶液与过量盐酸混合:CO +=CO↑+H O
+2H 2 2
B. 用铁电极电解饱和食盐水:2C1-+2H O=====Cl↑+H ↑+2OH-
2 2 2
C. Fe(NO ) 溶液中通入足量SO :Fe3++3NO +4H O=Fe2++3NO↑+5SO+8H+
3 3 2 +5SO2 2
D. 硫酸铜溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
3 2 2
答案:C
解析:A.小苏打为碳酸氢钠,离子方程式为:HCO +=CO ↑+H O,故A错误;
+H 2 2
B.铁作阳极时铁失电子,则电解反应为:Fe+2H O=====H↑+Fe(OH) ,故B错误;
2 2 2
C.Fe(NO ) 溶液中通入二氧化硫,溶液显酸性,NO
3 3 表现强氧化性,能将二氧化硫氧化成硫酸根离子,同时二氧化硫也能将
铁离子还原为亚铁离子,离子方程式正确,故C正确;
D.硫酸铜溶液中加入过量氨水,形成配合物:Cu2++4NH·H O=[Cu(NH )]2++4 H O,故D错误;
3 2 3 4 2
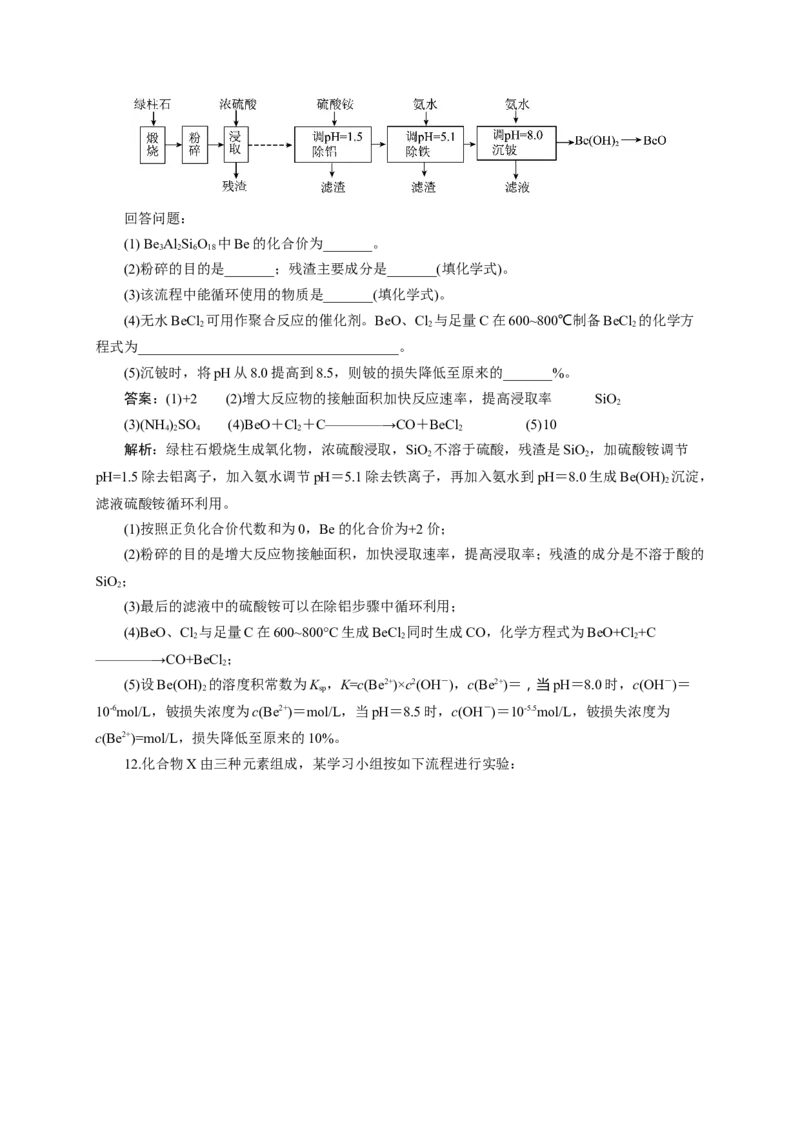
11. 铍的氧化物广泛应用于原子能、航天、电子、陶瓷等领域,是重要的战略物资。利用绿柱
石(主要化学成分为(Be Al Si O ,还含有一定量的FeO和Fe O)生产BeO的一种工艺流程如下。
3 2 6 18 2 3回答问题:
(1) Be Al Si O 中Be的化合价为_______。
3 2 6 18
(2)粉碎的目的是_______;残渣主要成分是_______(填化学式)。
(3)该流程中能循环使用的物质是_______(填化学式)。
(4)无水BeCl 可用作聚合反应的催化剂。BeO、Cl 与足量C在600~800℃制备BeCl 的化学方
2 2 2
程式为_____________________________________。
(5)沉铍时,将pH从8.0提高到8.5,则铍的损失降低至原来的_______%。
答案:(1)+2 (2)增大反应物的接触面积加快反应速率,提高浸取率 SiO
2
(3)(NH )SO (4)BeO+Cl+C————→CO+BeCl (5)10
4 2 4 2 2
解析:绿柱石煅烧生成氧化物,浓硫酸浸取,SiO 不溶于硫酸,残渣是SiO,加硫酸铵调节
2 2
pH=1.5除去铝离子,加入氨水调节pH=5.1除去铁离子,再加入氨水到pH=8.0生成Be(OH) 沉淀,
2
滤液硫酸铵循环利用。
(1)按照正负化合价代数和为0,Be的化合价为+2价;
(2)粉碎的目的是增大反应物接触面积,加快浸取速率,提高浸取率;残渣的成分是不溶于酸的
SiO;
2
(3)最后的滤液中的硫酸铵可以在除铝步骤中循环利用;
(4)BeO、Cl 与足量C在600~800°C生成BeCl 同时生成CO,化学方程式为BeO+Cl +C
2 2 2
————→CO+BeCl ;
2
(5)设Be(OH) 的溶度积常数为K ,K=c(Be2+)×c2(OH-),c(Be2+)=,当pH=8.0时,c(OH-)=
2 sp
10-6mol/L,铍损失浓度为c(Be2+)=mol/L,当pH=8.5时,c(OH-)=10-5.5mol/L,铍损失浓度为
c(Be2+)=mol/L,损失降低至原来的10%。
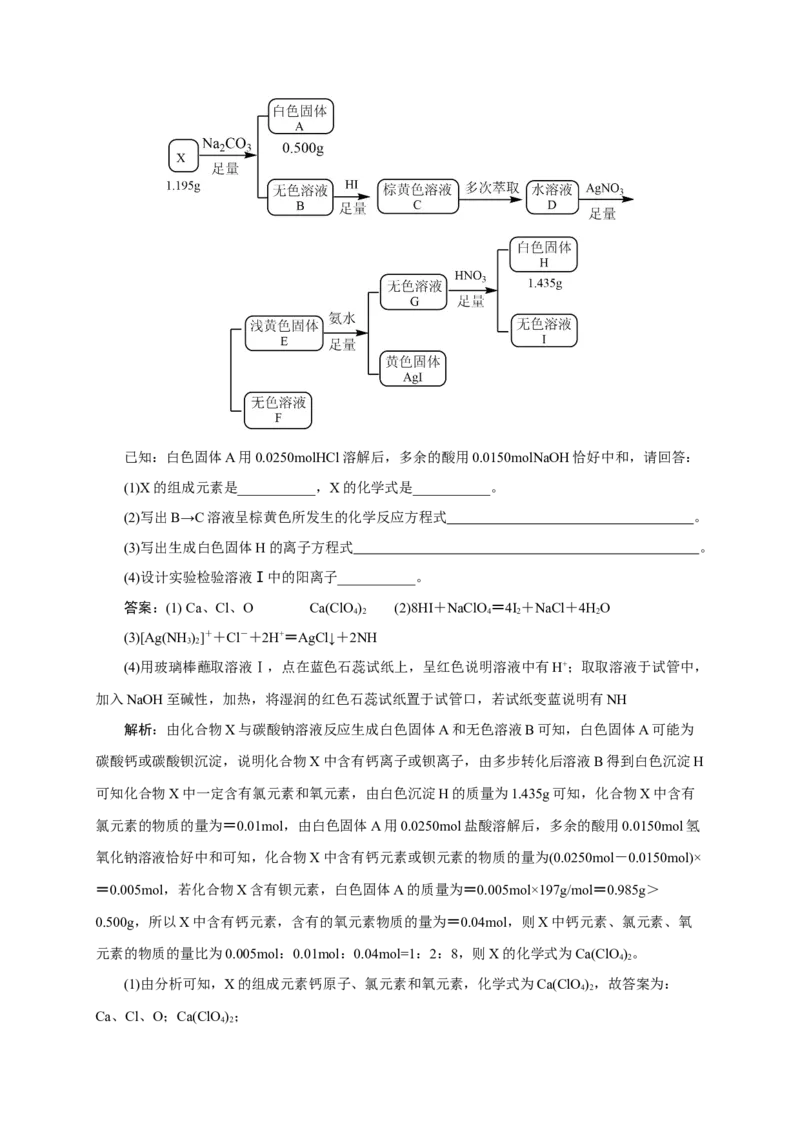
12.化合物X由三种元素组成,某学习小组按如下流程进行实验:已知:白色固体A用0.0250molHCl溶解后,多余的酸用0.0150molNaOH恰好中和,请回答:
(1)X的组成元素是___________,X的化学式是___________。
(2)写出B→C溶液呈棕黄色所发生的化学反应方程式 。
(3)写出生成白色固体H的离子方程式 。
(4)设计实验检验溶液Ⅰ中的阳离子___________。
答案:(1) Ca、Cl、O Ca(ClO ) (2)8HI+NaClO=4I+NaCl+4HO
4 2 4 2 2
(3)[Ag(NH)]++Cl-+2H+=AgCl↓+2NH
3 2
(4)用玻璃棒蘸取溶液Ⅰ,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取取溶液于试管中,
加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH
解析:由化合物X与碳酸钠溶液反应生成白色固体A和无色溶液B可知,白色固体A可能为
碳酸钙或碳酸钡沉淀,说明化合物X中含有钙离子或钡离子,由多步转化后溶液B得到白色沉淀H
可知化合物X中一定含有氯元素和氧元素,由白色沉淀H的质量为1.435g可知,化合物X中含有
氯元素的物质的量为=0.01mol,由白色固体A用0.0250mol盐酸溶解后,多余的酸用0.0150mol氢
氧化钠溶液恰好中和可知,化合物X中含有钙元素或钡元素的物质的量为(0.0250mol-0.0150mol)×
=0.005mol,若化合物X含有钡元素,白色固体A的质量为=0.005mol×197g/mol=0.985g>
0.500g,所以X中含有钙元素,含有的氧元素物质的量为=0.04mol,则X中钙元素、氯元素、氧
元素的物质的量比为0.005mol:0.01mol:0.04mol=1:2:8,则X的化学式为Ca(ClO )。
4 2
(1)由分析可知,X的组成元素钙原子、氯元素和氧元素,化学式为Ca(ClO ),故答案为:
4 2
Ca、Cl、O;Ca(ClO );
4 2(2)由图可知,B→C溶液呈棕黄色所发生的反应为高氯酸钠溶液与氢碘酸反应生成氯化钠、碘
和水,反应的化学反应方程式为8HI+NaClO=4I+NaCl+4HO,故答案为:8HI+NaClO=4I+
4 2 2 4 2
NaCl+4HO;
2
(3)由图可知,生成白色固体H的反应为氯化二氨合银与硝酸溶液反应生成氯化银沉淀和硝酸
铵,反应的离子方程式为[Ag(NH)]++Cl-+2H+=AgCl↓+2NH )]++Cl-+2H+=
3 2 ,故答案为:[Ag(NH3 2
AgCl↓+2NH
;
(4)由图可知,溶液Ⅰ为硝酸和硝酸铵的混合溶液,则检验溶液中氢离子铵根离子的操作为用玻
璃棒蘸取溶液Ⅰ,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取取溶液于试管中,加入NaOH
至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH
,故答案为:用玻璃棒蘸取溶液Ⅰ,点在
H+;取取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸
蓝色石蕊试纸上,呈红色说明溶液中有
置于试管口,若试纸变蓝说明有NH
。