文档内容
第 20 讲 氯气的实验室制法及应用
[复习目标] 掌握实验室制取氯气的原理、装置和操作注意事项。增强设计物质制备实验方
案的绿色环保意识。
1.制取原理
HCl (浓)――――――――――――――――――――→Cl2
完成下列有关反应的离子方程式:
(1)MnO 和浓盐酸: _______________________________________________________
2
________________________________________________________________________。
(2)Ca(ClO) 与浓盐酸: ___________________________________________________。
2
(3)KClO 与浓盐酸: ______________________________________________________。
3
(4)KMnO 与浓盐酸: ____________________________________________________。
4
答案 (1)MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
(2)ClO-+Cl-+2H+===Cl↑+HO
2 2
(3)ClO+5Cl-+6H+===3Cl↑+3HO
2 2
(4)2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO
2 2
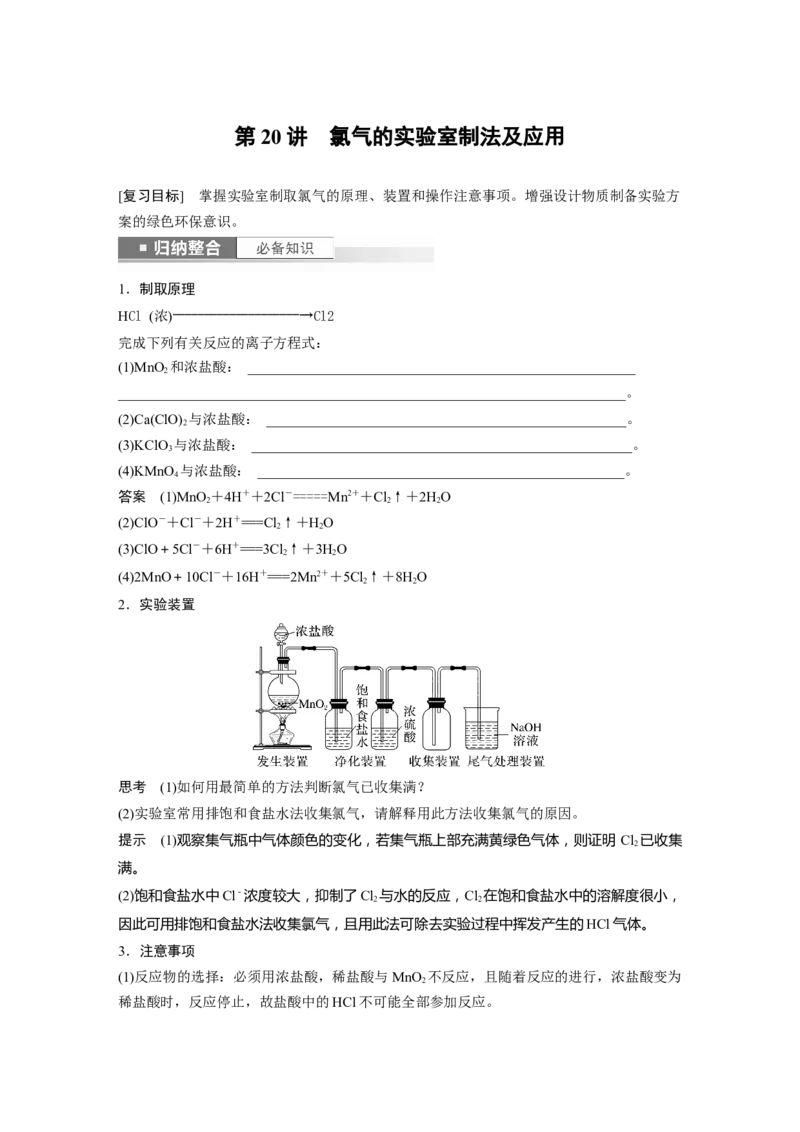
2.实验装置
思考 (1)如何用最简单的方法判断氯气已收集满?
(2)实验室常用排饱和食盐水法收集氯气,请解释用此方法收集氯气的原因。
提示 (1)观察集气瓶中气体颜色的变化,若集气瓶上部充满黄绿色气体,则证明 Cl 已收集
2
满。
(2)饱和食盐水中Cl-浓度较大,抑制了Cl 与水的反应,Cl 在饱和食盐水中的溶解度很小,
2 2
因此可用排饱和食盐水法收集氯气,且用此法可除去实验过程中挥发产生的HCl气体。
3.注意事项
(1)反应物的选择:必须用浓盐酸,稀盐酸与MnO 不反应,且随着反应的进行,浓盐酸变为
2
稀盐酸时,反应停止,故盐酸中的HCl不可能全部参加反应。(2)加热温度:不宜过高,以减少HCl挥发。
(3)实验结束后,先使反应停止并排出残留的Cl 后,再拆卸装置,避免污染空气。
2
(4)尾气处理时,用 NaOH溶液吸收Cl ,不能用澄清石灰水吸收,因为澄清石灰水中含
2
Ca(OH) 的量少,吸收不完全。
2
1.含0.4 mol HCl的浓盐酸与足量的MnO 共热,能得到0.1 mol Cl ( )
2 2
2.用饱和NaHCO 溶液除去Cl 中混有的HCl( )
3 2
3.常用饱和石灰水吸收尾气中的Cl( )
2
4.用干燥的淀粉碘化钾试纸检验Cl 是否收集满( )
2
答案 1.× 2.× 3.× 4.×
1.实验室用MnO 和浓盐酸制Cl 时,有如下操作:①连好装置,检查装置气密性;②缓缓
2 2
加热;③加入MnO 粉末;④从装有浓盐酸的分液漏斗中加入浓盐酸;⑤将多余氯气用
2
NaOH溶液吸收;⑥用向上排空气法收集氯气。顺序排列正确的是( )
A.①②③④⑥⑤ B.③④②①⑥⑤
C.①④③②⑥⑤ D.①③④②⑥⑤
答案 D
解析 制取氯气的正确操作步骤:先连接装置、检查装置气密性,然后装入药品,先向烧瓶
中装入二氧化锰,再向分液漏斗中装入浓盐酸,再加热制取、收集氯气,由于氯气有毒,最
后需要进行尾气吸收,故正确的排序为①③④②⑥⑤。
2.下列方法中,可制得Cl 的正确组合是( )
2
①MnO 和浓盐酸混合共热;②MnO 、NaCl和浓硫酸混合共热;③NaClO和浓盐酸混合;
2 2
④KCr O 和浓盐酸混合;⑤KClO 和浓盐酸混合;⑥KMnO 和浓盐酸混合
2 2 7 3 4
A.①②⑥ B.②④⑥
C.①④⑥ D.①②③④⑤⑥
答案 D
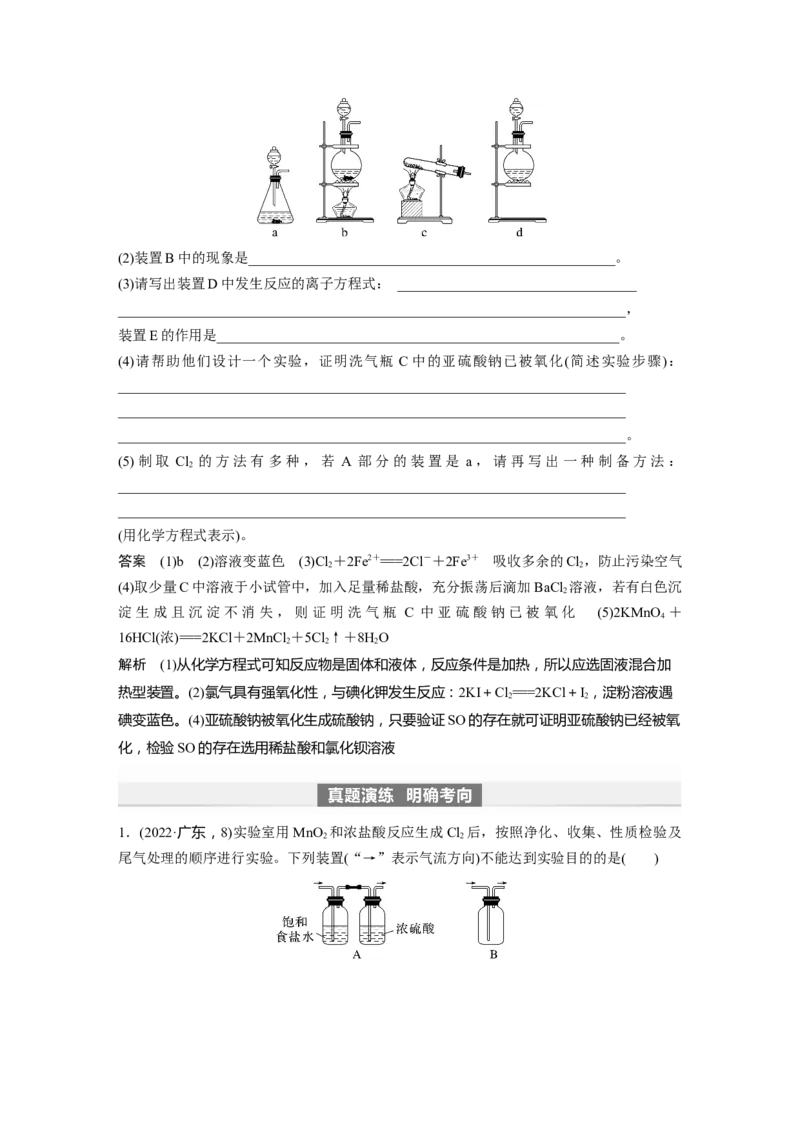
3.某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为
Ca(ClO) +CaCl +2HSO =====2CaSO +2Cl↑+2HO,他们设计如图实验装置制取氯气并
2 2 2 4 4 2 2
验证其性质。请回答下列问题:
(1)该实验中A部分的装置是________(填字母)。(2)装置B中的现象是____________________________________________________。
(3)请写出装置D中发生反应的离子方程式: __________________________________
________________________________________________________________________,
装置E的作用是_________________________________________________________。
(4)请帮助他们设计一个实验,证明洗气瓶 C中的亚硫酸钠已被氧化(简述实验步骤):
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(5)制取 Cl 的方法有多种,若 A 部分的装置是 a,请再写出一种制备方法:
2
________________________________________________________________________
________________________________________________________________________
(用化学方程式表示)。
答案 (1)b (2)溶液变蓝色 (3)Cl +2Fe2+===2Cl-+2Fe3+ 吸收多余的Cl,防止污染空气
2 2
(4)取少量C中溶液于小试管中,加入足量稀盐酸,充分振荡后滴加BaCl 溶液,若有白色沉
2
淀生成且沉淀不消失,则证明洗气瓶 C 中亚硫酸钠已被氧化 (5)2KMnO +
4
16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
2 2 2
解析 (1)从化学方程式可知反应物是固体和液体,反应条件是加热,所以应选固液混合加
热型装置。(2)氯气具有强氧化性,与碘化钾发生反应:2KI+Cl===2KCl+I,淀粉溶液遇
2 2
碘变蓝色。(4)亚硫酸钠被氧化生成硫酸钠,只要验证SO的存在就可证明亚硫酸钠已经被氧
化,检验SO的存在选用稀盐酸和氯化钡溶液
1.(2022·广东,8)实验室用MnO 和浓盐酸反应生成Cl 后,按照净化、收集、性质检验及
2 2
尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )答案 D
解析 浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸
2
干燥,故A不符合题意;氯气的密度大于空气,可用向上排空气法收集,故 B不符合题意;
湿润的红布条褪色,干燥的红布条不褪色,可验证干燥的氯气不具有漂白性,故C不符合
题意;氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,故D符合题意。
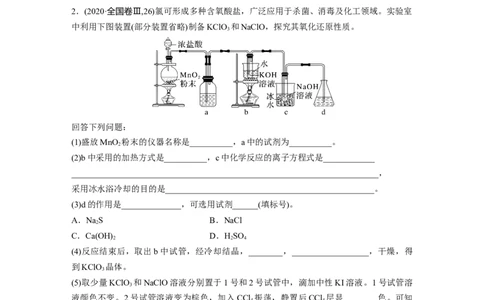
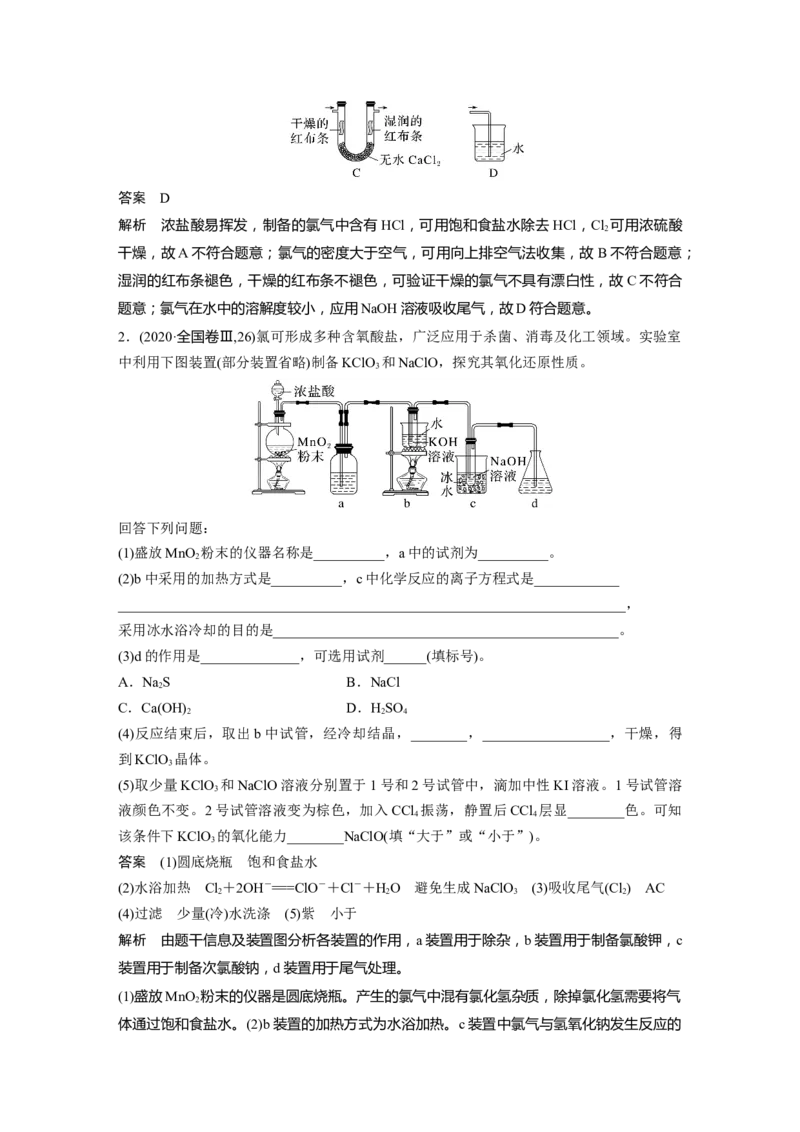
2.(2020·全国卷Ⅲ,26)氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室
中利用下图装置(部分装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是__________,a中的试剂为__________。
2
(2)b中采用的加热方式是__________,c中化学反应的离子方程式是____________
________________________________________________________________________,
采用冰水浴冷却的目的是_________________________________________________。
(3)d的作用是______________,可选用试剂______(填标号)。
A.NaS B.NaCl
2
C.Ca(OH) D.HSO
2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,__________________,干燥,得
到KClO 晶体。
3
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶
3
液颜色不变。2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显________色。可知
4 4
该条件下KClO 的氧化能力________NaClO(填“大于”或“小于”)。
3
答案 (1)圆底烧瓶 饱和食盐水
(2)水浴加热 Cl+2OH-===ClO-+Cl-+HO 避免生成NaClO (3)吸收尾气(Cl ) AC
2 2 3 2
(4)过滤 少量(冷)水洗涤 (5)紫 小于
解析 由题干信息及装置图分析各装置的作用,a装置用于除杂,b装置用于制备氯酸钾,c
装置用于制备次氯酸钠,d装置用于尾气处理。
(1)盛放MnO 粉末的仪器是圆底烧瓶。产生的氯气中混有氯化氢杂质,除掉氯化氢需要将气
2
体通过饱和食盐水。(2)b装置的加热方式为水浴加热。c装置中氯气与氢氧化钠发生反应的离子方程式为Cl +2OH-===ClO-+Cl-+HO。根据b、c装置水浴温度的不同推知,生成
2 2
氯酸盐时需要酒精灯加热,生成次氯酸盐时需要冰水冷却,所以 c中冰水浴的目的是避免氯
酸钠的生成。(3)d是尾气处理装置,吸收氯气可以用硫化钠溶液或氢氧化钙浊液。(4)从溶
液中获得纯净氯酸钾的操作是冷却结晶,过滤,少量冷水洗涤,干燥,此处用少量冷水洗涤
的目的是降低氯酸钾的损耗。(5)碘在四氯化碳中呈紫色;碘在水中的颜色为棕色或褐色,
主要由碘的浓度决定。2号试管中溶液变棕色说明生成I ,1号试管中没有颜色变化,说明
2
没有生成I,由此可以判断氯酸钾的氧化能力小于次氯酸钠的氧化能力。
2
课时精练
1.实验室既可用浓盐酸与MnO 在加热条件下反应制备Cl ,也可用KMnO 与浓盐酸在常
2 2 4
温下反应制备Cl,下列有关说法不正确的是( )
2
A.KMnO 的氧化性比MnO 的强
4 2
B.制备Cl 的整个实验过程中,只需要使用氧化剂与还原剂
2
C.用排气法收集Cl 时,不需要利用其他试剂就能确定集气瓶中已收集满
2
D.制备等质量的Cl,消耗MnO 与KMnO 的物质的量之比为5∶2
2 2 4
答案 B
解析 比较反应的条件即可证明KMnO 的氧化性强于MnO ,A项正确;当整个集气瓶充满
4 2
黄绿色气体时表明已收集满,C项正确。
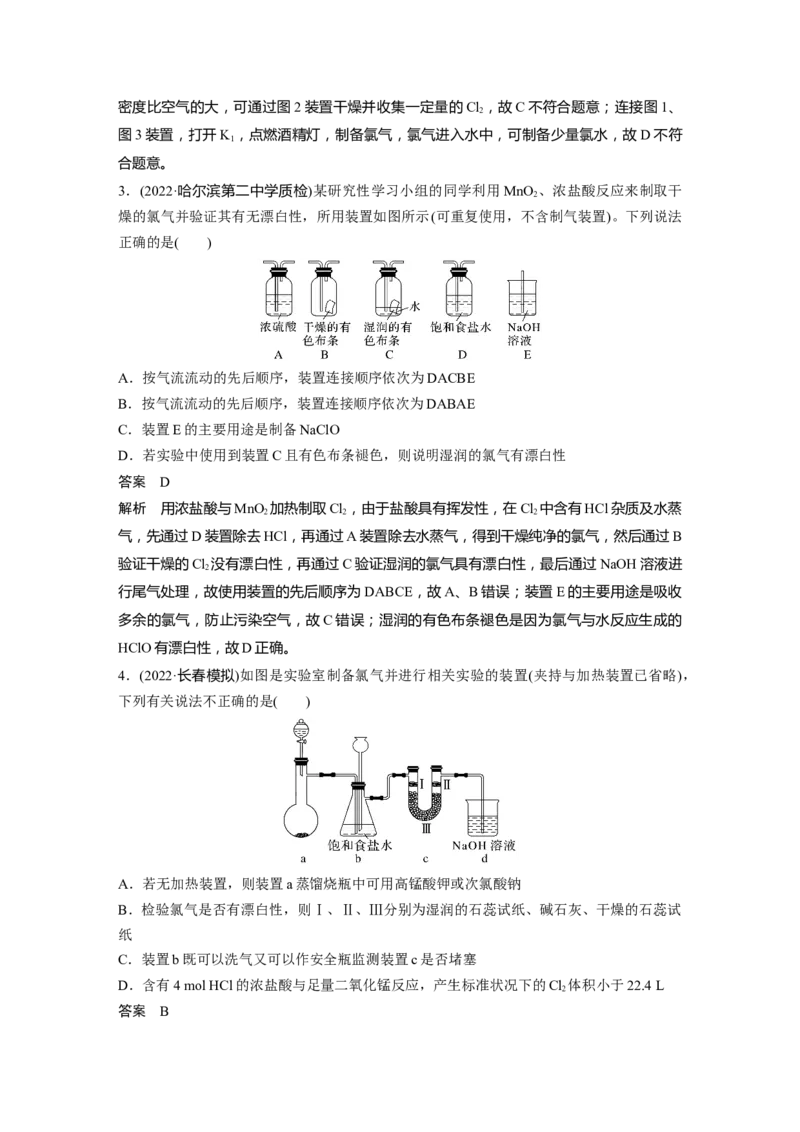
2.实验室中利用MnO 制备干燥的Cl 及少量氯水并收集Cl ,下列图示装置和原理不能达
2 2 2
到实验目的的是( )
A.连接图1、图2装置,向分液漏斗中注水,打开K,关闭K,检查装置气密性
1 2
B.图1装置中,滴加浓盐酸,点燃酒精灯,可制备Cl
2
C.可通过图2装置干燥并收集一定量的Cl
2
D.连接图1、图3装置,打开K,点燃酒精灯,可制备少量氯水
1
答案 A
解析 图1装置中为恒压分液漏斗,注水后无论气密性是否良好,水都能顺利流下,不能检
查装置的气密性,故A符合题意;图1装置中,浓盐酸与二氧化锰在加热的条件下反应可
制备Cl ,故B不符合题意;饱和食盐水除去氯气中的HCl气体,浓硫酸干燥氯气,且氯气
2密度比空气的大,可通过图2装置干燥并收集一定量的Cl ,故C不符合题意;连接图1、
2
图3装置,打开K ,点燃酒精灯,制备氯气,氯气进入水中,可制备少量氯水,故D不符
1
合题意。
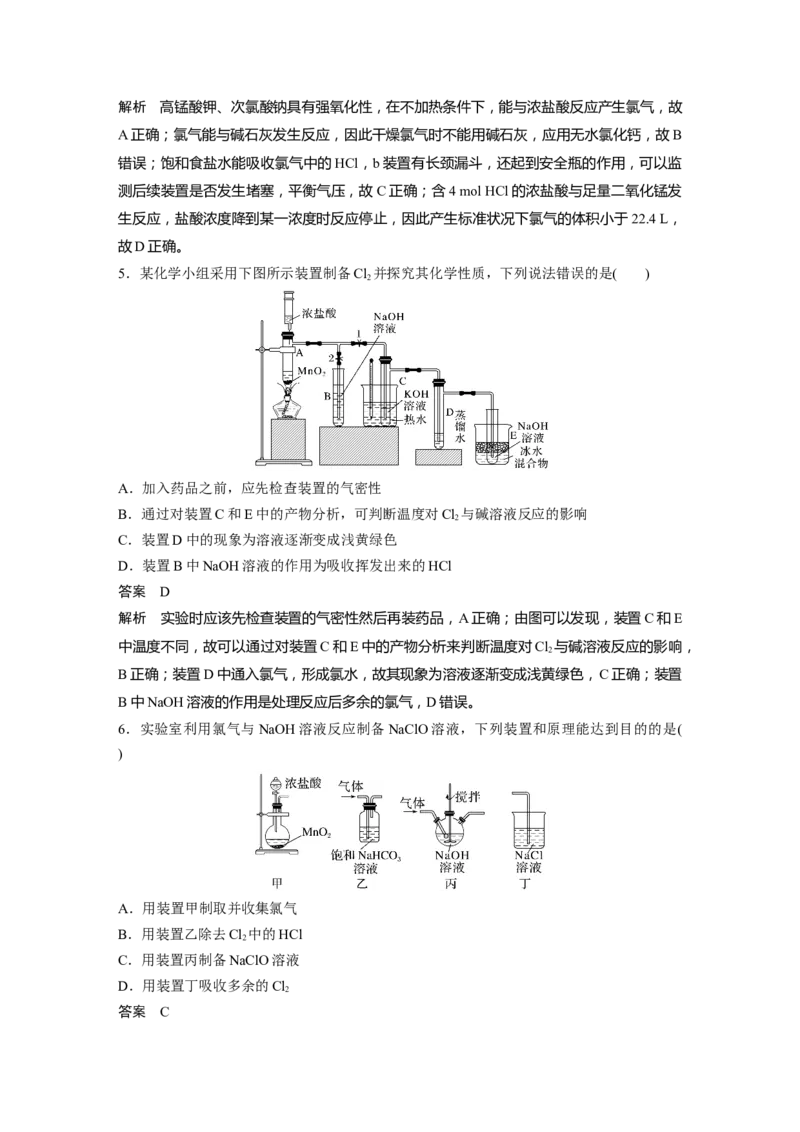
3.(2022·哈尔滨第二中学质检)某研究性学习小组的同学利用MnO 、浓盐酸反应来制取干
2
燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法
正确的是( )
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.若实验中使用到装置C且有色布条褪色,则说明湿润的氯气有漂白性
答案 D
解析 用浓盐酸与MnO 加热制取Cl ,由于盐酸具有挥发性,在Cl 中含有HCl杂质及水蒸
2 2 2
气,先通过D装置除去HCl,再通过A装置除去水蒸气,得到干燥纯净的氯气,然后通过B
验证干燥的Cl 没有漂白性,再通过C验证湿润的氯气具有漂白性,最后通过NaOH溶液进
2
行尾气处理,故使用装置的先后顺序为DABCE,故A、B错误;装置E的主要用途是吸收
多余的氯气,防止污染空气,故C错误;湿润的有色布条褪色是因为氯气与水反应生成的
HClO有漂白性,故D正确。
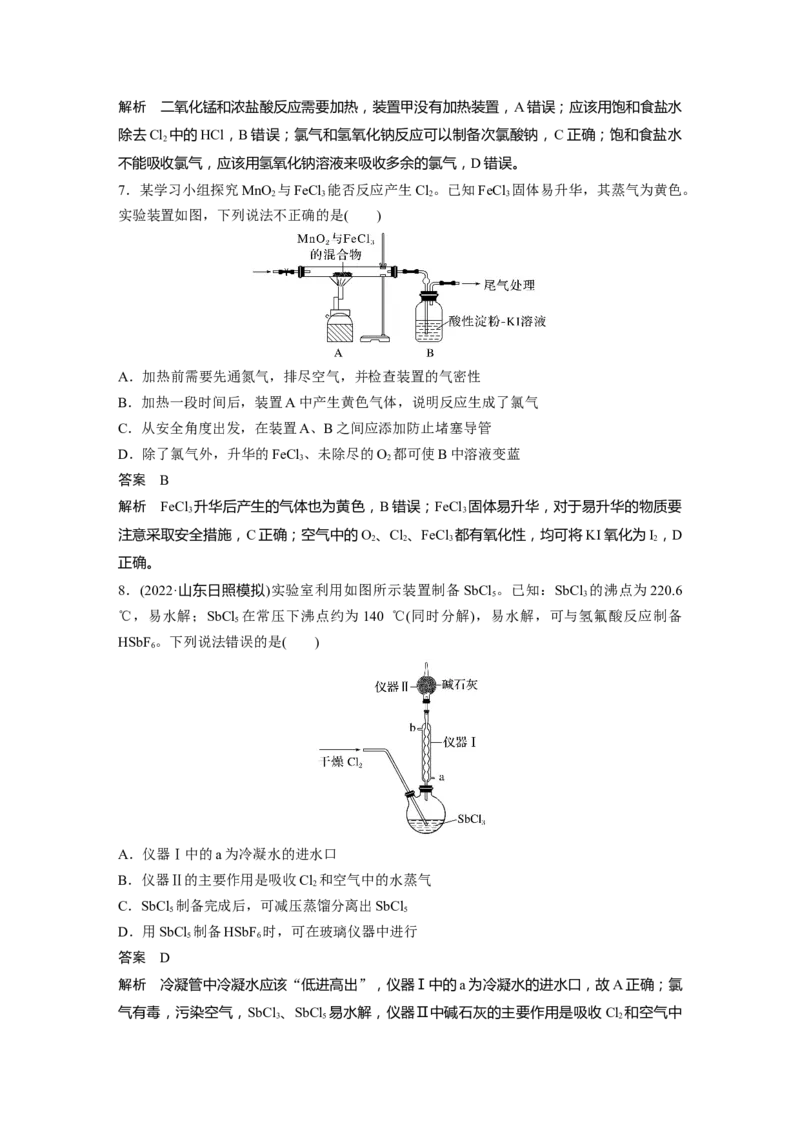
4.(2022·长春模拟)如图是实验室制备氯气并进行相关实验的装置(夹持与加热装置已省略),
下列有关说法不正确的是( )
A.若无加热装置,则装置a蒸馏烧瓶中可用高锰酸钾或次氯酸钠
B.检验氯气是否有漂白性,则Ⅰ、Ⅱ、Ⅲ分别为湿润的石蕊试纸、碱石灰、干燥的石蕊试
纸
C.装置b既可以洗气又可以作安全瓶监测装置c是否堵塞
D.含有4 mol HCl的浓盐酸与足量二氧化锰反应,产生标准状况下的Cl 体积小于22.4 L
2
答案 B解析 高锰酸钾、次氯酸钠具有强氧化性,在不加热条件下,能与浓盐酸反应产生氯气,故
A正确;氯气能与碱石灰发生反应,因此干燥氯气时不能用碱石灰,应用无水氯化钙,故B
错误;饱和食盐水能吸收氯气中的HCl,b装置有长颈漏斗,还起到安全瓶的作用,可以监
测后续装置是否发生堵塞,平衡气压,故C正确;含4 mol HCl的浓盐酸与足量二氧化锰发
生反应,盐酸浓度降到某一浓度时反应停止,因此产生标准状况下氯气的体积小于22.4 L,
故D正确。
5.某化学小组采用下图所示装置制备Cl 并探究其化学性质,下列说法错误的是( )
2
A.加入药品之前,应先检查装置的气密性
B.通过对装置C和E中的产物分析,可判断温度对Cl 与碱溶液反应的影响
2
C.装置D中的现象为溶液逐渐变成浅黄绿色
D.装置B中NaOH溶液的作用为吸收挥发出来的HCl
答案 D
解析 实验时应该先检查装置的气密性然后再装药品,A正确;由图可以发现,装置C和E
中温度不同,故可以通过对装置C和E中的产物分析来判断温度对Cl 与碱溶液反应的影响,
2
B正确;装置D中通入氯气,形成氯水,故其现象为溶液逐渐变成浅黄绿色,C正确;装置
B中NaOH溶液的作用是处理反应后多余的氯气,D错误。
6.实验室利用氯气与NaOH溶液反应制备NaClO溶液,下列装置和原理能达到目的的是(
)
A.用装置甲制取并收集氯气
B.用装置乙除去Cl 中的HCl
2
C.用装置丙制备NaClO溶液
D.用装置丁吸收多余的Cl
2
答案 C解析 二氧化锰和浓盐酸反应需要加热,装置甲没有加热装置,A错误;应该用饱和食盐水
除去Cl 中的HCl,B错误;氯气和氢氧化钠反应可以制备次氯酸钠,C正确;饱和食盐水
2
不能吸收氯气,应该用氢氧化钠溶液来吸收多余的氯气,D错误。
7.某学习小组探究MnO 与FeCl 能否反应产生Cl 。已知FeCl 固体易升华,其蒸气为黄色。
2 3 2 3
实验装置如图,下列说法不正确的是( )
A.加热前需要先通氮气,排尽空气,并检查装置的气密性
B.加热一段时间后,装置A中产生黄色气体,说明反应生成了氯气
C.从安全角度出发,在装置A、B之间应添加防止堵塞导管
D.除了氯气外,升华的FeCl 、未除尽的O 都可使B中溶液变蓝
3 2
答案 B
解析 FeCl 升华后产生的气体也为黄色,B错误;FeCl 固体易升华,对于易升华的物质要
3 3
注意采取安全措施,C正确;空气中的O 、Cl 、FeCl 都有氧化性,均可将KI氧化为I ,D
2 2 3 2
正确。
8.(2022·山东日照模拟)实验室利用如图所示装置制备SbCl 。已知:SbCl 的沸点为220.6
5 3
℃,易水解;SbCl 在常压下沸点约为140 ℃(同时分解),易水解,可与氢氟酸反应制备
5
HSbF 。下列说法错误的是( )
6
A.仪器Ⅰ中的a为冷凝水的进水口
B.仪器Ⅱ的主要作用是吸收Cl 和空气中的水蒸气
2
C.SbCl 制备完成后,可减压蒸馏分离出SbCl
5 5
D.用SbCl 制备HSbF 时,可在玻璃仪器中进行
5 6
答案 D
解析 冷凝管中冷凝水应该“低进高出”,仪器Ⅰ中的a为冷凝水的进水口,故A正确;氯
气有毒,污染空气,SbCl 、SbCl 易水解,仪器Ⅱ中碱石灰的主要作用是吸收Cl 和空气中
3 5 2的水蒸气,故B正确;SbCl 在常压下沸点约为140 ℃(同时分解),比SbCl 的低,为防止
5 3
SbCl 分解,制备完成后应减压蒸馏分离出 SbCl ,故C正确;SbCl 与氢氟酸反应制备
5 5 5
HSbF ,玻璃中的二氧化硅和氢氟酸反应,故D错误。
6
9.实验室测盐酸与亚氯酸钠制备二氧化氯气体的速率,装置如图所示。4 mL 0.2% NaClO
2
溶液预先装入二氧化氯发生器,37.5% HCl溶液装入分液漏斗。开启真空泵抽气,反应开始
后,每隔2 min用注射器取样1 mL,测定NaClO 溶液的浓度。已知ClO 浓度过高时易爆炸。
2 2
下列说法错误的是( )
A.碘化钾吸收瓶中发生的反应为2ClO +10I-+8H+===2Cl-+5I +4HO
2 2 2
B.做实验时整套装置要先抽真空,再加入37.5%HCl溶液,防止ClO 聚集
2
C.分液漏斗作为空气入口,起到搅拌作用
D.实验过程中分液漏斗活塞保持关闭,防止ClO 逸出
2
答案 D
解析 ClO 污染空气,可用酸性KI溶液吸收,A项正确;实验前先打开真空泵,再打开分
2
液漏斗活塞,让盐酸一次性加入发生器,产生的 ClO 快速被抽走,防止聚集爆炸,B项正
2
确;实验过程中,为使真空泵工作顺畅,分液漏斗活塞应保持打开状态,空气从分液漏斗进
入发生器,起到搅拌的作用,C项正确、D项错误。
10.NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,下列说法错误的是( )
2
A.NaClO 的名称是亚氯酸钠
2
B.“尾气吸收”是吸收“电解”过程排出的少量ClO ,此反应的离子方程式为2OH-+
2
HO+2ClO ===2ClO+O↑+2HO
2 2 2 2 2
C.“电解”中阴极反应的主要产物是Cl
2
D.“一系列操作”为蒸发浓缩、趁热过滤、洗涤、干燥
答案 C
解析 电解装置中阴极上ClO 得电子生成ClO,阳极上Cl-失电子生成Cl ,C错误。
2 2
11.(2022·山东枣庄模拟)已知氯气和空气按体积比 1∶3混合通入潮湿的碳酸钠中能生成ClO,且反应放热;不含Cl 的ClO易与水反应生成HClO;ClO在42 ℃以上会分解生成
2 2 2 2
Cl 和O 。设计如图装置(部分夹持装置略)制备HClO,每个虚线框表示一个装置单元,其中
2 2
存在错误的是( )
A.②③⑤ B.①④⑤
C.①②④ D.①③④
答案 D
解析 ①用MnO 和浓盐酸制备氯气需要加热装置,错误;②是将制备的Cl 通入饱和食盐
2 2
水中除去挥发出来的HCl,同时可以控制通入氯气和空气的体积比,并在实验结束后可以将
多余的氯气排出进行尾气处理,正确;③由题干信息可知,制备ClO的反应是放热反应,
2
且ClO在42 ℃以上会分解生成Cl 和O ,则发生装置③需放置在冰水浴中,错误;④为除
2 2 2
去ClO中的Cl 的装置,导管应该长进短出,错误;⑤除去Cl 的ClO通入⑤中进行反应,
2 2 2 2
生成HClO,正确。
12.(2022·湖南岳阳一中模拟)反应2NaClO+C HNO===C NOClNa+NaOH+HO可制备
3 3 3 3 3 3 3 2 2
广谱消毒剂C NOClNa,装置如图所示(夹持装置已略去)。下列说法错误的是( )
3 3 3 2
A.按气流从左至右,装置中导管连接顺序为f→c→d→a→b→e
B.升高温度有利于装置A中产品的生成
C.当加入4 mol NaOH时,消耗氰尿酸(C HNO)的量大于1 mol
3 3 3 3
D.装置D中橡胶管可平衡气压,便于浓盐酸顺利流下
答案 B
解析 A为制取C NOClNa的装置,B为除去氯气中的HCl的装置,C为尾气处理装置,
3 3 3 2
D 为制取氯气装置,所以为完成实验,按气流从左至右,导管连接顺序为f→c→d→a→b→e,A正确;升高温度,氯气和NaOH溶液反应生成NaClO ,生成NaClO
3
的浓度减少,不利于装置A中产品的生成,B错误;由反应方程式:Cl +2NaOH===NaCl
2
+NaClO+HO、2NaClO+C HNO===C NOClNa+NaOH+HO,可得关系式:4NaOH
2 3 3 3 3 3 3 3 2 2
~2NaClO~C HNO ,加入 4 mol NaOH 时,可消耗 1 mol C HNO ,由于产物也生成
3 3 3 3 3 3 3 3
NaOH,则消耗氰尿酸的量大于1 mol,C正确;装置D中浓盐酸和Ca(ClO) 反应生成Cl ,
2 2
由于产生气体,装置D内压强较大,使用橡胶管可平衡气压,便于浓盐酸顺利流下,D正
确。
13.(2022·山西临汾模拟)亚硝酰氯(NOCl)是重要的有机合成试剂,可由NO与Cl 在常温下
2
合成。某学习小组在实验室利用如图装置制备亚硝酰氯。
已知:①亚硝酰氯易水解,能与O 反应;
2
②沸点:NOCl为-5.5 ℃,Cl 为-34 ℃,NO为-152 ℃;
2
③常温下,2NO + Cl===2NOCl、2NO +Cl===2NO Cl。
2 2 2 2
请回答下列问题:
(1)NOCl 中 N 元素的化合价为________;NOCl 水解生成两种酸,其化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)实验所需的NO在A装置中制得,反应的离子方程式为_____________________。
(3)装置B中所盛试剂为________,其作用是__________________________________
________________________________________________________________________。
(4)实验开始时,先关闭 K ,打开 K 、K ,从 a 处通一段时间氩气,其目的是
3 2 4
________________________________________________________________________
________________________________________________________________________。
然后在a处接废气处理装置,关闭K 、K ,打开K ,再打开分液漏斗的活塞,滴加酸性
1 4 3
FeSO 溶液,当观察到D中______________时, 关闭K ,打开K 、K ,通干燥纯净的
4 2 1 4
Cl。
2
(5)为收集产物和分离未反应的两种原料, E、F装置采用不同温度的低温浴槽,其中装置E
的温度(T)区间应控制在__________________________________________________,
装置F 的U形管中收集到的是________。
答案 (1)+3 NOCl+HO===HCl+HNO (2)Fe2++NO+2H+===Fe3++NO↑+HO
2 2 2
(3)水 将NO 转化为NO (4)将E、F装置中的空气排出,防止亚硝酰氯水解和被氧气氧化
2
红棕色气体消失 (5)-34 ℃≤T<-5.5 ℃ Cl
2解析 (1)NOCl中N的非金属性最弱,为正价,O为-2价,Cl为-1价,所以N元素的化
合价为+3价;NOCl水解生成两种酸,分别为盐酸和亚硝酸,其化学方程式为NOCl+
HO===HCl+HNO 。(2)在装置 A中,NaNO 和硫酸酸化的 FeSO 发生氧化还原反应,
2 2 2 4
NaNO 被Fe2+还原为NO,Fe2+被氧化为 Fe3+,反应的离子方程式为 Fe2++ NO+2H+
2
===Fe3++NO↑+HO。(3)装置A中生成了NO,装置A的液面上方有空气,空气中的氧气
2
能将NO氧化为NO ,所以装置B中装有水,可以将NO 转化为NO。(4)亚硝酰氯易水解,
2 2
能与O 反应,实验开始时,先关闭K ,打开K 、K ,从a处通一段时间氩气,其目的是将
2 3 2 4
装置E、F中的空气排出,以免生成的NOCl和空气中的水蒸气、氧气反应。 然后在a处接
废气处理装置,关闭K 、K ,打开K ,再打开分液漏斗的活塞,滴加酸性FeSO 溶液,装
1 4 3 4
置A产生的NO气体进入B中,混有的NO 被B中的水转化为NO,但装置B、C的液面上
2
方有空气,NO会被氧化为NO ,装置D中的空气也能将NO氧化为NO ,所以在D中能观
2 2
察到红棕色的气体,A装置中不断产生的NO将生成的NO 从K 排出,当观察到D中红棕
2 2
色消失时,D中充满了纯净的NO, 此时关闭K ,打开K 、K ,通干燥纯净的Cl 和NO反
2 1 4 2
应。(5)为收集产物NOCl和分离未反应的两种原料NO和Cl ,根据三种物质的沸点,装置
2
E的温度应控制在-34 ℃≤T<-5.5 ℃,可收集NOCl,装置F的温度要低于-34 ℃,可
将未反应的原料氯气冷凝。
14.2022年,新型冠状病毒在全球范围内肆虐,次氯酸钠溶液是常用的环境消毒剂。此外,
次氯酸钠溶液也是常用的漂白剂。某研究性学习小组在实验室制备次氯酸钠溶液,测定其中
NaClO的含量并探究其漂白棉布的效果。回答下列问题:
(一)制备NaClO溶液
(1)装置B的作用是________________;若没有装置B,且D中氢氧化钠不足量,对次氯酸
钠产率的影响是________(填“增大”“减小”或“无影响”)。
(2)装置D中反应的离子方程式为___________________________________________
________________________________________________________________________。
(3)有同学提出三点意见:①装置A中不需要酒精灯;②装置C没有必要;③在装置D后再
连接一个盛有NaOH溶液的尾气处理装置,以降低氯气逸出污染空气的可能性。合理的是
________(填序号)。
(二)测定消毒液中NaClO的含量
步骤①:取制得的消毒液20 mL于锥形瓶中,加足量盐酸酸化,迅速加入过量 KI溶液,盖紧瓶塞并在暗处充分反应。
步骤②:加入淀粉做指示剂,用NaSO 标准溶液滴定至终点,重复滴定操作3次。
2 2 3
(4)步骤①中在暗处反应的原因是___________________________________________。
(5)步骤②中判断滴定终点的现象是_________________________________________
________________________________________________________________________,
已知I +2SO===2I-+SO。平均用去25.00 mL 0.100 0 mol·L-1 Na SO 标准溶液,测得
2 2 4 2 2 3
NaClO的含量为________ g·L-1(结果保留2位小数)。
(三)探究次氯酸钠漂白棉布的效果
已知:棉布用次氯酸钠漂白液漂白会受到一定损伤。织物断裂强度是指织物在被拉断时,所
能承受的最大荷重,单位为kg。
使用次氯酸钠漂白液漂白棉布,不同pH对于漂白的结果如图所示。
(6)漂白速率随pH减小而加快,但酸性条件易产生黄绿色气体,该气体已被实验证明没有漂
白作用,说明起漂白作用的主要是________(填粒子符号);pH最好选择9~11,虽然漂白速
率较慢,但可延长漂白时间达到效果。不宜选择酸性或中性的原因分别是_________
________________________________________________________________________。
答案 (1)除去 HCl气体 减小 (2)Cl +2OH-===Cl-+ClO-+HO (3)②③ (4)防止
2 2
HClO分解 (5)溶液由蓝色变为无色且30 s内不恢复 4.66 (6)HClO 酸性条件易产生氯
气导致环境污染;中性条件下对棉布损伤较大
解析 (1)氯气难溶于饱和食盐水,装置B中饱和食盐水的作用是除去HCl气体,降低Cl 在
2
水中的溶解度;若没有装置B除去Cl 中混有的HCl,D中氢氧化钠不足量,HCl会消耗一
2
定量的氢氧化钠,次氯酸钠的产率减小。(3)①反应需要加热,装置A中不用酒精灯反应难
以进行,不合理;②装置C中浓硫酸用于吸收氯气中的水,没有装置 C不会对实验造成影
响,合理;③氯气有毒会污染环境,在装置D后接一个盛有NaOH溶液的装置,用于尾气
处理,合理。(4)步骤①中NaClO在酸性条件与KI反应生成碘单质和氯化钠,离子方程式为
ClO-+2H++2I-===Cl-+I +HO,ClO-与H+结合形成HClO,见光易分解,所以要在暗
2 2
处进行。(5)淀粉遇碘显蓝色,滴加 NaSO 标准溶液后,发生反应:I +2SO===2I-+
2 2 3 2 2
SO,碘单质被还原,溶液蓝色逐渐变浅,最终完全反应时褪色,滴定消耗NaSO 的物质
4 2 2 3
的量为0.025 L×0.100 0 mol·L-1=0.002 5 mol,根据关系式:ClO-~I ~2SO,n(NaClO)=n(I)=
2 2 2
×0.002 5 mol,NaClO的含量为≈4.66 g·L-1。(6)黄绿色气体为Cl ,无漂白性,NaClO与盐
2
酸反应的离子方程式为ClO-+H+===HClO,pH越小,氢离子浓度越大,平衡向正反应方
向移动,HClO浓度越大,漂白性越强,所以具有漂白性的是HClO。