文档内容
常见的有机化合物作业题
作业题目难度分为3档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目1-3,5-10,14-18题为三星,4,11-13,19-26题为四星。
1.对CH 与Cl 的反应(如图所示)叙述不正确的是( ) ☆☆☆
4 2
A.该反应属于取代反应
B.该反应的条件是光照
C.该反应的生成物有四种
D.该反应的现象是量筒内气体颜色变浅,器壁上有油状液滴,量筒内液面上升
并产生白雾
【解答】
甲烷与氯气(C1 )混合后在光照下可以发生下列反应:CH+Cl CHCl+HCl;
2 4 2 3
CHC1+Cl CHCl+HCl;CHCl+Cl CHCl+HCl;CHCl+Cl CCl+HCl,得到
3 2 2 2 2 2 2 3 3 2 4
的产物中有气态的CHCl和HCl,液态的CHCl、CHCl 和CCl,
3 2 2 3 4
A.甲烷中的氢原子被氯原子取代生成氯代烃,属于取代反应,故 A正确;
B.该反应需光照提供能量,故 B正确;
C.CH 和Cl 在光照下缓慢反应缓慢反应生成了气态的CHCl和HCl,液态的CHCl、
4 2 3 2 2
CHCl 和CCl,共5种,故C错误;
3 4
D.甲烷可以和氯气发生取代反应,生成的产物均无色,所以试管中气体颜色会
变浅,生成的二氯甲烷、三氯甲烷、四氯化碳均是油状的液体,一氯甲烷和HCl
是气体,氯化氢极易溶于水,所以量筒内液面上升并产生白雾,故 D正确。
故选C.
第1页(共16页)2.若甲烷与氯气以物质的量之比 1:3混合,在光照下得到的产物:(1)CHCl
3
(2)CHCl (3)CHCl (4)CCl (5)HCl其中正确的是( ) ☆☆☆
2 2 3 4
A.只有(1)(5) B.只有(3)(5)
C.(1)(2)(3)(5)的混合物 D.(1)(2)(3)(4)(5)的混合物
【解答】
甲烷和氯气在光照下,会发生四步取代反应,而反应进行到哪一步不是由反应物
甲烷和氯气的物质的量之比来决定的,即使甲烷和氯气的物质的量之比是 1:1
的情况,也不会仅生成CHCl,因为一旦生成CHCl后,CHCl分子中的氢原子又
3 3 3
可继续被氯原子取代,直到分子中氢原子都被取代完,因此其产物不是纯净的
CHCl.题设甲烷与氯气以物质的量之比 1:3混合,则四步取代反应都发生,所
3
以得到的是四种氯代烃和氯化氢的混合物。
故选D.
3.将物质的量之比为 1:2 的甲烷和氯气混合后,在强光的照射下充分反应,
生成物中物质的量最大的是( ) ☆☆☆
A.CHCl B.CHCl C.CCl D.HCl
3 2 2 4
【解答】
甲烷在发生取代反应时,除了生成有机物之外,还有氯化氢生成,且有几个氢原
子,就生成几分子氯化氢,所以氯化氢的量最多。
故选D.
4.若要使 2mol CH 完全和 Cl 发生取代反应,且生成的四种氯代物的物质的量
4 2
相同,则所需Cl 的物质的量为( ) ☆☆☆☆
2
A.5mol B.4mol C.3mol D.2mol
第2页(共16页)【解答】
解:2mol 甲烷完全与氯气发生取代反应,若生成相同物质的量的四种取代物,
所以每种取代物的物质的量是 0.5mol,甲烷和氯气的取代反应中,被取代的氢
原子的物质的量与氯气的物质的量相等,
所以生成0.5mol一氯甲烷需要氯气0.5mol氯气,
生成0.5mol二氯甲烷需要氯气1mol,
生成0.5mol三氯甲烷需要氯气1.5mol氯气,
生成0.5mol四氯化碳需要氯气2mol,
所以总共消耗氯气的物质的量=0.5mol+1mol+1.5mol+2mol=5mol。
故选A.
5.甲烷分子是以碳原子为中心的正四面体结构,而不是正方形的平面结构,理
由是( ) ☆☆☆
A.CHCl只有一种结构 B.CHCl 只有一种结构
3 2 2
C.CHCl 只有一种结构 D.CH 中含有4个C﹣H极性键
3 4
【解答】
A、若甲烷是正四面体,则 CHCl只有一种结构,而若甲烷为正方形的平面结构,
3
则CHCl也只有一种结构,故CHCl只有一种结构不能说明甲烷是哪种构型,故
3 3
A错误;
B、若甲烷是正四面体,则CHCl 只有一种结构,而若甲烷为正方形的平面结构,
2 2
则CHCl 有两种结构,而事实是CHCl 只有一种结构,故可以说明甲烷为正四面
2 2 2 2
体结构而非平面结构,故B正确;
C、若甲烷是正四面体,则CHCl 只有一种结构,而若甲烷为正方形的平面结构,
3
则 CHCl 也只有一种结构,故 CHCl 只有一种结构,不鞥说明甲烷为正四面体结
3 3
构而非平面结构,故C错误;
D、无论甲烷为正四面体结构还是平面结构,甲烷中均含4条C﹣H 极性键,故甲
烷中含 4条C﹣H极性键不可以说明甲烷为正四面体结构而非平面结构,故 D错
误。
第3页(共16页)故选B.
6.关于甲烷和乙烯,说法正确的是( ) ☆☆☆
A.甲烷能燃烧,乙烯不能
B.甲烷和乙烯都能使溴水褪色
C.甲烷和乙烯都能使酸性高锰酸钾溶液褪色
D.甲烷和乙烯完全燃烧的产物都是CO 和HO
2 2
【解答】
A.甲烷、乙烯都是仅含有碳和氢两种元素的有机物,都能与氧气反应生成二氧
化碳和水,故A错误;
B.乙烯含有碳碳双键,能与溴发生加成反应,因此能使溴水褪色,而甲烷没有
不饱和键,不能使溴水褪色,故 B错误;
C.乙烯与酸性高锰酸钾反应生成二氧化碳,甲烷没有不饱和键,不能被酸性高
锰酸钾溶液氧化,故C错误;
D.碳和氧反应生成二氧化碳、氢和氧反应生成水,甲烷和乙烯完全燃烧的产物
都是CO 和HO,故D正确。
2 2
故选D.
7.下列反应可制得纯净一氯乙烷的是( ) ☆☆☆
A.乙烯通入浓盐酸中 B.乙烯与氯化氢加成反应
C.乙烷与氯气在光照下反应 D.乙烷通入氯水中
【解答】
A.乙烯和盐酸不反应,所以不能制取一氯乙烷,故A错误;
B.一定条件下,乙烯和 HCl 发生加成反应生成一氯乙烷,没有副产物生成,所
以可以制备较纯净的一氯乙烷,故B正确;
C.光照条件下,氯气和乙烷发生取代反应生成乙烷的多种氯代烃,同时 HCl,
所以不能制备较纯净的一氯乙烷,故C错误;
第4页(共16页)D.乙烷和氯水不反应,所以不能制取一氯乙烷,故D错误。
故选B.
8.由乙烯性质推测丙烯性质,那么丙烯与溴水反应的产物应该是( )
☆☆☆
A.CH﹣CH﹣CHBr B.CH﹣CHBr﹣CHBr
3 2 2 3 2
C.CH﹣CH﹣CHBr D.CH﹣CHBr﹣CH
3 2 3 3
【解答】
乙烯含有碳碳双键与溴水发生加成反应,双键中的一个键断裂,分别在两个碳原
子上各加上一个溴原子生成 1,2﹣二二溴乙烷,根据乙烯和溴的加成反应得,
丙烯和溴的加成反应是丙烯中的碳碳双键断裂,每个双键的碳原子上添加一个溴
原子,生成1,2﹣二溴丙烷。
故选B.
9.除去乙烷中混有的少量乙烯,应采用的简便方法是( ) ☆☆☆
A.将混合气体通过氢氧化钠溶液
B.将混合气体通过溴水
C.将混合气体在催化剂条件下跟氢气反应
D.将混合气体通过酸性KMnO 溶液
4
【解答】
A、乙烯和乙烷与氢氧化钠均不反应,不能除去乙烷中混有的少量乙烯,故 A错
误;
B、乙烯能和溴水加成,而乙烷则不能,将混合气体通过溴水,可以除去乙烷中
混有的少量乙烯,故B正确;
C、将混合气体在催化剂条件下跟氢气反应会使乙烯成为乙烷,达不到除杂目的,
故C错误;
D、乙烯能和高锰酸钾之间发生氧化还原反应,乙烯被氧化为二氧化碳,这样乙
第5页(共16页)烷中混有二氧化碳气体,故 D错误。
故选B.
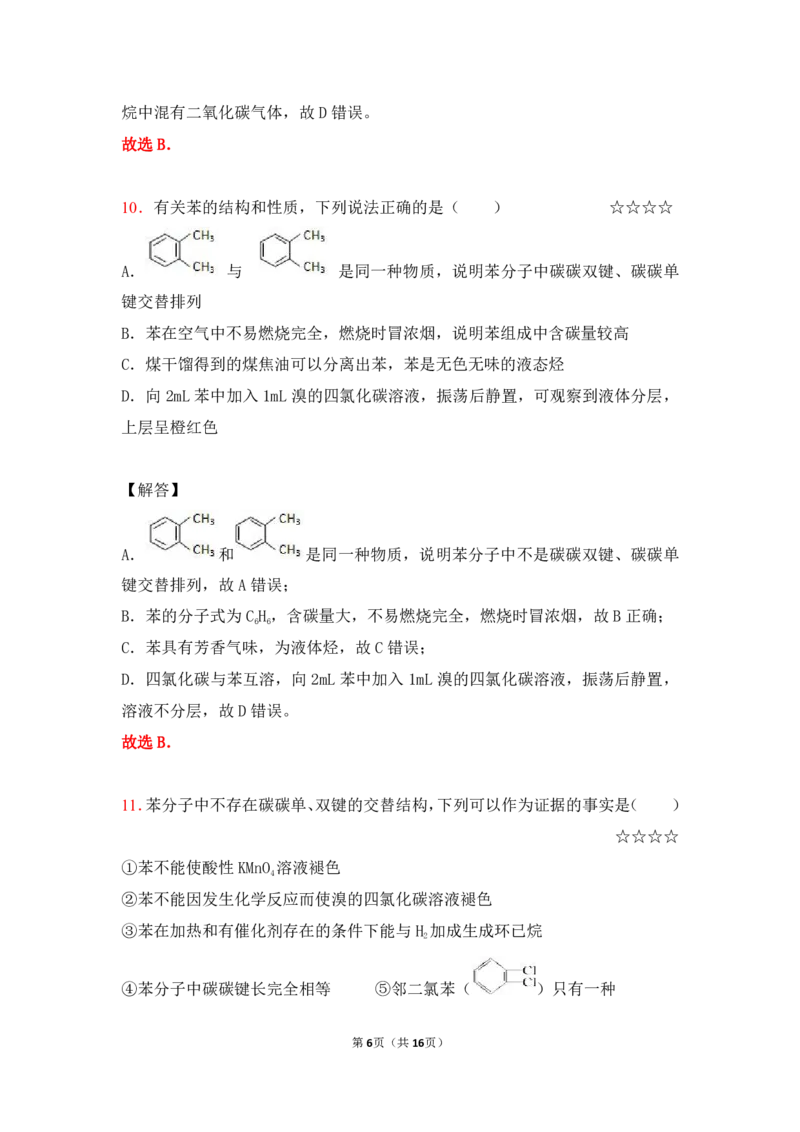
10.有关苯的结构和性质,下列说法正确的是( ) ☆☆☆☆
A. 与 是同一种物质,说明苯分子中碳碳双键、碳碳单
键交替排列
B.苯在空气中不易燃烧完全,燃烧时冒浓烟,说明苯组成中含碳量较高
C.煤干馏得到的煤焦油可以分离出苯,苯是无色无味的液态烃
D.向 2mL 苯中加入 1mL 溴的四氯化碳溶液,振荡后静置,可观察到液体分层,
上层呈橙红色
【解答】
A. 和 是同一种物质,说明苯分子中不是碳碳双键、碳碳单
键交替排列,故A错误;
B.苯的分子式为CH,含碳量大,不易燃烧完全,燃烧时冒浓烟,故B正确;
6 6
C.苯具有芳香气味,为液体烃,故C错误;
D.四氯化碳与苯互溶,向 2mL苯中加入 1mL 溴的四氯化碳溶液,振荡后静置,
溶液不分层,故D错误。
故选B.
11.苯分子中不存在碳碳单、双键的交替结构,下列可以作为证据的事实是( )
☆☆☆☆
①苯不能使酸性KMnO 溶液褪色
4
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色
③苯在加热和有催化剂存在的条件下能与H 加成生成环已烷
2
④苯分子中碳碳键长完全相等 ⑤邻二氯苯( )只有一种
第6页(共16页)⑥间二氯苯( )只有一种.
A.①② B.①⑤ C.③④⑤⑥ D.①②④⑤
【解答】
①苯不能使酸性高锰酸钾溶液褪色,说明苯分子中不含碳碳双键,故①正确;
②苯不能因发生化学反应而使溴的四氯化碳溶液褪色说明不存在双键,说明苯分
子中不存在碳碳单、双键的交替结构,故②正确;
③苯能在一定条件下跟 H 加成生成环己烷,发生加成反应是双键或三键具有的
2
性质,不能证明苯环结构中不存在 C﹣C单键与C=C双键的交替结构,故③错误;
④苯环上碳碳键的键长相等,说明苯环结构中的化学键只有一种,说明苯分子中
不存在碳碳单、双键的交替结构,故④正确;
⑤如果是单双键交替结构,邻二氯苯的结构有两种,一种是两个甲基夹 C﹣C,
另一种是两个甲基夹C=C.邻二氯苯只有一种结构,说明苯环结构中的化学键只
有一种,不存在C﹣C单键与C=C双键的交替结构,故⑤正确;
⑥苯分子中不论是否存在碳碳单、双键的交替结构,间二氯苯只有一种,故⑥错
误。
故选D.
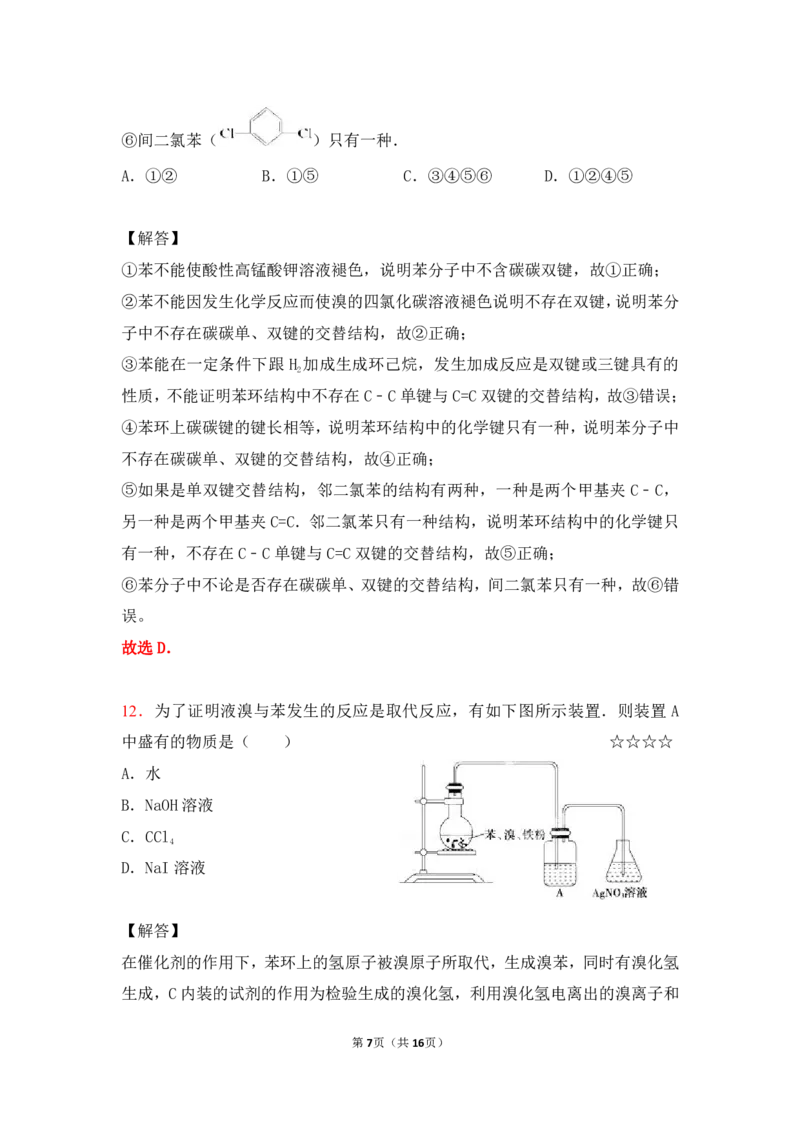
12.为了证明液溴与苯发生的反应是取代反应,有如下图所示装置.则装置 A
中盛有的物质是( ) ☆☆☆☆
A.水
B.NaOH溶液
C.CCl
4
D.NaI溶液
【解答】
在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢
生成,C 内装的试剂的作用为检验生成的溴化氢,利用溴化氢电离出的溴离子和
第7页(共16页)银离子反应,生成淡黄色不溶于硝酸的沉淀溴化银,由此来检验溴和苯发生了取
代反应,但溴会对HBr产生干扰,因此A中液体的作用就是除掉HBr中的Br,
2
A、Br 在水中的溶解度不大,HBr 在水中的溶解度大,故不能除掉 Br ,故 A 错
2 2
误;
B、HBr能与NaOH发生中和反应,故B错误;
C、Br 易溶于CCl,HBr不溶于 CCl,故C正确;
2 4 4
D、HBr在NaI溶液中的溶解度大而被吸收,故D错误。
故选C.
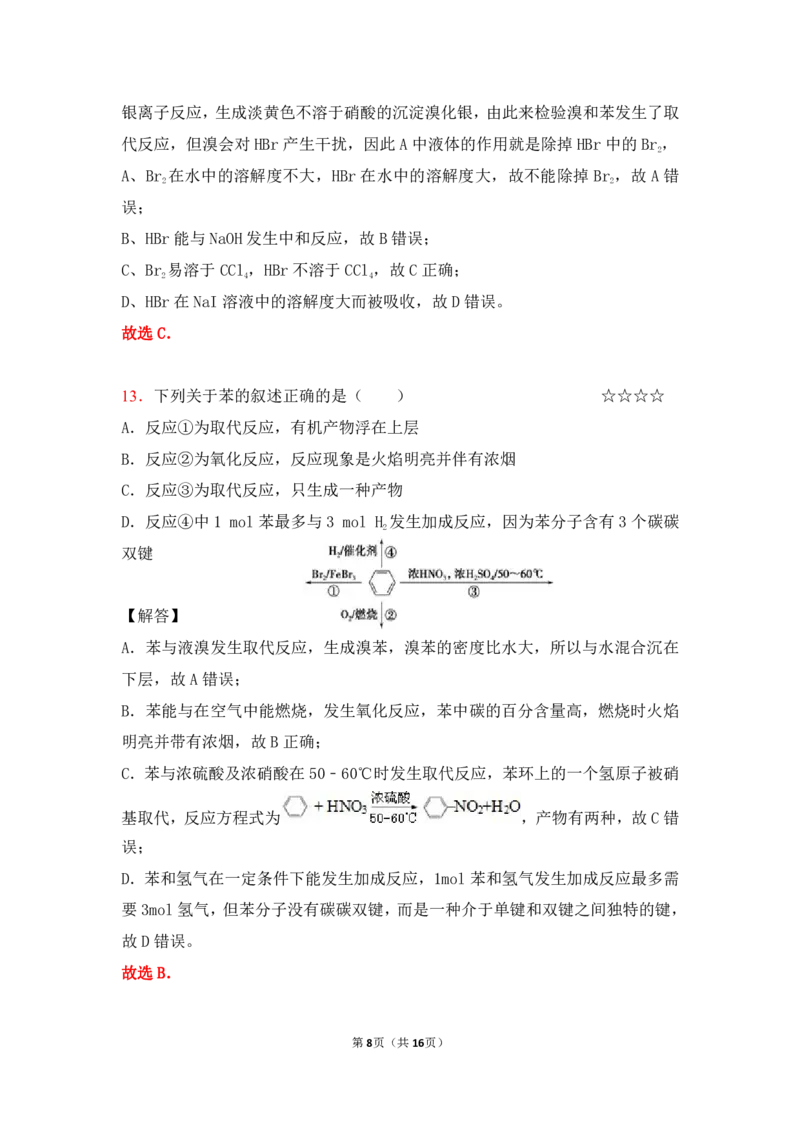
13.下列关于苯的叙述正确的是( ) ☆☆☆☆
A.反应①为取代反应,有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,只生成一种产物
D.反应④中1 mol苯最多与3 mol H 发生加成反应,因为苯分子含有3个碳碳
2
双键
【解答】
A.苯与液溴发生取代反应,生成溴苯,溴苯的密度比水大,所以与水混合沉在
下层,故A错误;
B.苯能与在空气中能燃烧,发生氧化反应,苯中碳的百分含量高,燃烧时火焰
明亮并带有浓烟,故B正确;
C.苯与浓硫酸及浓硝酸在 50﹣60℃时发生取代反应,苯环上的一个氢原子被硝
基取代,反应方程式为 ,产物有两种,故C错
误;
D.苯和氢气在一定条件下能发生加成反应,1mol苯和氢气发生加成反应最多需
要3mol氢气,但苯分子没有碳碳双键,而是一种介于单键和双键之间独特的键,
故D错误。
故选B.
第8页(共16页)14.下列关于乙醇的说法中,不正确的是( ) ☆☆☆
A.乙醇是无色透明、有特殊香味的液体
B.乙醇可以使酸性高锰酸钾溶液褪色
C.乙醇属于烃类物质
D.无水硫酸铜常用于检验乙醇中是否含有水
【解答】
A.乙醇是无色透明、有特殊香味的液体,故A正确;
B.乙醇可以使酸性高锰酸钾溶液氧化使溶液褪色,故 B正确;
C.乙醇中含有C、H、O三种元素,不属于烃,故C错误;
D.无水硫酸铜检验酒精中是否含有水,如有水,生成 CuSO •5HO,固体由白色
4 2
变为蓝色,故D正确。
故选C.
15.下列有关乙醇的物理性质的应用中不正确的是( ) ☆☆☆
A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药中的有效成
分
C.由于乙醇能够以任意比溶解于水,所以酒厂能够勾兑出各种浓度的酒
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法
【解答】
A、乙醇和水互溶,不可以分液,可以采用蒸馏的方法分离,故 A错误;
B、乙醇与中药中的有效成分是互溶的,可用乙醇提取中药中的有效成分,故 B
正确;
C、乙醇可以和不同比例的水混合获得不同浓度的酒精,酒厂能够勾兑出各种浓
度的酒,故C正确;
D、乙醇容易挥发,远远的就可以闻到乙醇的香味,即熟语“酒香不怕巷子深”,
故D正确。
第9页(共16页)故选A.
16.能证明乙醇分子中有一个羟基的事实是( ) ☆☆☆
A.乙醇完全燃烧生成CO 和HO
2 2
B.0.1mol乙醇与足量钠反应生成0.05mol氢气
C.乙醇能溶于水
D.乙醇能脱水
【解答】
乙醇与生成的氢气的物质的量之比为 0.1:0.05=2:1,说明乙醇分子中有一个
活泼的氢原子可被金属钠取代(置换),即乙醇分子中有一个羟基。
故选B.
17.钠与下列物质反应都能够产生氢气:①HO;②CHCOOH;③CHCHOH.从产生
2 3 3 2
氢气的剧烈程度可推断出这三种物质产生 H+的难易程度是(从难到易的顺序)
( ) ☆☆☆
A.①②③ B.②③① C.③①② D.②①③
【解答】
由物质的酸性越强,越容易电离出氢离子,则与钠反应生成氢气的速率就越快,
酸性:CHCOOH>>HO>CHOH,则这三种物质产生H+的难易程度是(从难到易)
3 2 2 5
③①②
故选C.
18.酒后驾车是引发交通事故的重要原因.交警对驾驶员进行呼气酒精检测的原
理是:橙色的KCrO 酸性水溶液遇乙醇迅速生成蓝绿包Cr3+.下列对乙醇的描述
2 2 7
与此测定原理有关的是( ) ☆☆☆
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性
④乙醇是烃的含氧衍生物 ⑤乙醇有刺檄性气味.
第10页(共16页)A.②④⑤ B.②③ C.①③ D.①④
【解答】
①乙醇沸点低,易挥发,若饮酒,呼出的气体中含有酒精,与测定原理有关;
②乙醇密度比水小,可与水以任意比混溶,与测定原理无关;
③乙醇分子中含有羟基,具有还原性,KCrC 具有强氧化性,可以把乙醇迅速氧
2 2 7
化为乙酸蓝绿色的Cr3+,与测定原理有关;
④乙醇可看成是乙烷中的氢原子被羟基取代后的产物,是烃的含氧化合物,与测
定原理无关;
⑤乙醇有刺檄性气味,与测定原理无关;
故对乙醇的描述与此测定原理有关的是①③
故选C.
19.把质量为 mg的铜丝灼烧变黑,立即放入下列物质中,使铜丝变红,而且质
量仍为m g的是( ) ☆☆☆☆
①稀硫酸 ②CHOH ③稀硝酸 ④CO
2 5
A.①② B.②④ C.③④ D.②③
【解答】
①铜丝灼烧成黑色,立即放入硫酸中,CuO与硫酸反应,生成铜盐,铜丝变红,
铜丝质量减少,故①错误;
② 铜 丝 灼 烧 成 黑 色 , 立 即 放 入 CHOH 中 , CuO 与 CHOH 反 应 :
2 5 2 5
CuO+CHOH CHCHO+Cu+HO,反应后铜丝变红,质量保持不变,故②正确;
2 5 3 2
③铜丝灼烧成黑色,立即放入稀硝酸中,CuO、Cu与稀硝酸反应,生成铜盐,铜
丝变红,铜丝质量减少,故③错误;
④铜丝灼烧成黑色,立即放入CO中,CuO与CO反应生成铜和二氧化碳,反应后
铜丝变红,质量保持不变,故④正确。
故选B.
第11页(共16页)20.质量为ag的铜丝,在空气中灼热变黑,趁热放入下列物质中,质量大于ag
的是( ) ☆☆☆☆
A.盐酸 B.CHCOOH C.CHOH D.NaOH
3 2 5
【解答】
A、铜丝灼烧成黑色,立即放入盐酸中,CuO与盐酸反应,生成铜盐,质量减少,
故A错误;
B、铜丝灼烧成黑色,立即放入CHCOOH中,CuO与CHCOOH反应,生成铜盐,质
3 3
量减少,故B错误;
C 、 铜 丝 灼 烧 成 黑 色 , 立 即 放 入 CHOH 中 , CuO 与 CHOH 反 应 :
2 5 2 5
CuO+CHOH CHCHO+Cu+HO,反应前后其质量不变,故C错误;
2 5 3 2
D、铜丝灼烧成黑色,立即放入 NaOH 中,CuO、Cu 与 NaOH 不反应,质量增加,
故D正确。
故选D.
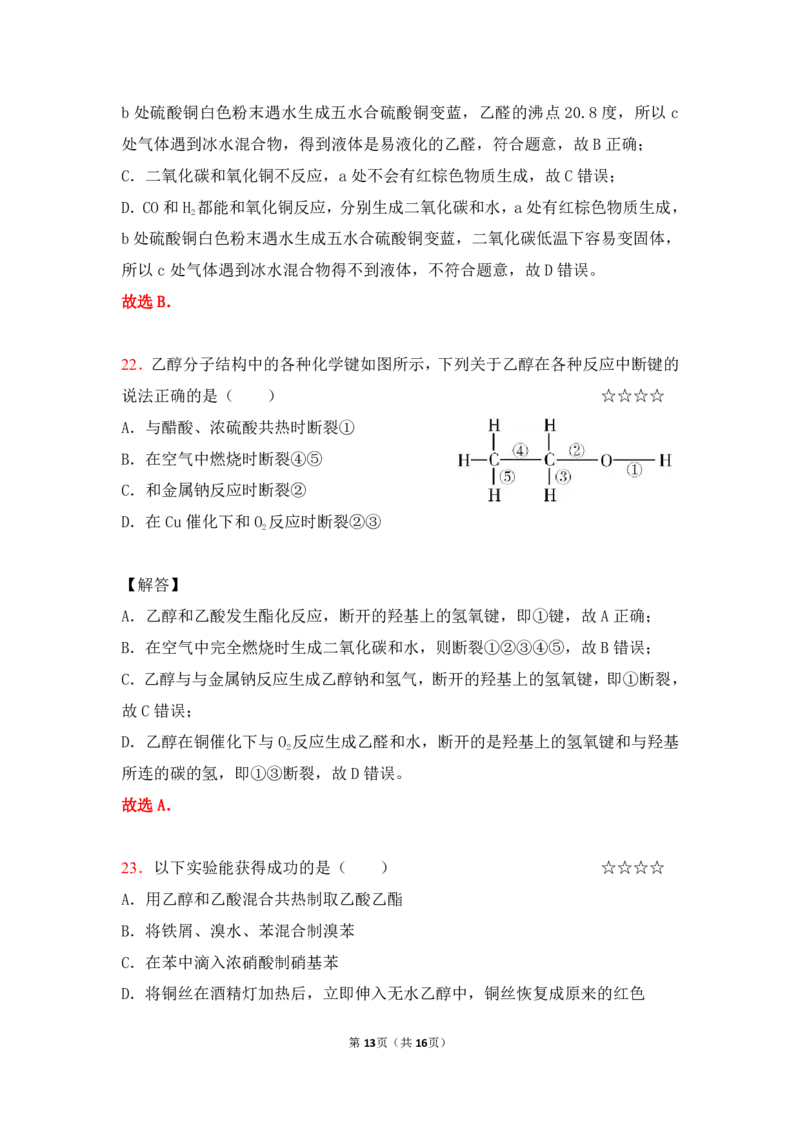
21.按如图装置,持续通入X气体,可以看到a处有红棕色物质生成,b处变蓝,
c处得到液体,则X气体是( ) ☆☆☆☆
A.H B.CHCHOH(气)
2 3 2
C.CO D.CO和H
2 2
【解答】
图示装置,持续通入X气体,可以看到a处有红棕色物质生成,a处放的是氧化
铜,a 处有红棕色物质生成,说明有金属铜生成,b 处是硫酸铜白色粉末,b处
变蓝是硫酸铜白色粉末遇水生成五水合硫酸铜变蓝,c处得到液体是易液化的气
体遇到冰水混合物会变为液体,所以X气体与氧化铜反应生成铜、水和易液化的
气体,
A.氢气与灼热的氧化铜反应H+CuO Cu+HO生成铜和水,a处有红棕色物
2 2
质生成,b处硫酸铜白色粉末遇水生成五水合硫酸铜变蓝,但c处得不到液体,
故A错误;
B.乙醇和氧化铜反应 CHCHOH+CuO CHCHO+Cu+HO,a处有红棕色物质生成,
3 2 3 2
第12页(共16页)b 处硫酸铜白色粉末遇水生成五水合硫酸铜变蓝,乙醛的沸点 20.8 度,所以 c
处气体遇到冰水混合物,得到液体是易液化的乙醛,符合题意,故 B正确;
C.二氧化碳和氧化铜不反应,a处不会有红棕色物质生成,故C错误;
D.CO和H 都能和氧化铜反应,分别生成二氧化碳和水,a处有红棕色物质生成,
2
b处硫酸铜白色粉末遇水生成五水合硫酸铜变蓝,二氧化碳低温下容易变固体,
所以c处气体遇到冰水混合物得不到液体,不符合题意,故 D错误。
故选B.
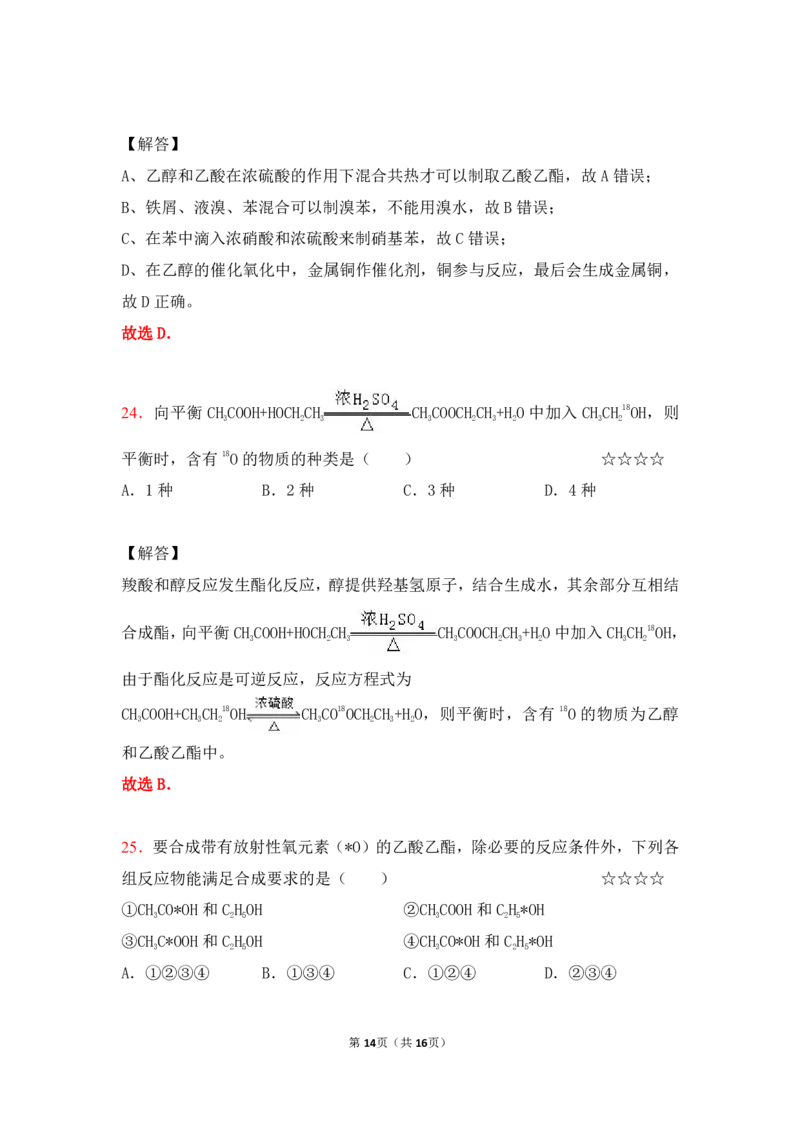
22.乙醇分子结构中的各种化学键如图所示,下列关于乙醇在各种反应中断键的
说法正确的是( ) ☆☆☆☆
A.与醋酸、浓硫酸共热时断裂①
B.在空气中燃烧时断裂④⑤
C.和金属钠反应时断裂②
D.在Cu催化下和O 反应时断裂②③
2
【解答】
A.乙醇和乙酸发生酯化反应,断开的羟基上的氢氧键,即①键,故A正确;
B.在空气中完全燃烧时生成二氧化碳和水,则断裂①②③④⑤,故B错误;
C.乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键,即①断裂,
故C错误;
D.乙醇在铜催化下与O 反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基
2
所连的碳的氢,即①③断裂,故D错误。
故选A.
23.以下实验能获得成功的是( ) ☆☆☆☆
A.用乙醇和乙酸混合共热制取乙酸乙酯
B.将铁屑、溴水、苯混合制溴苯
C.在苯中滴入浓硝酸制硝基苯
D.将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
第13页(共16页)【解答】
A、乙醇和乙酸在浓硫酸的作用下混合共热才可以制取乙酸乙酯,故 A错误;
B、铁屑、液溴、苯混合可以制溴苯,不能用溴水,故 B错误;
C、在苯中滴入浓硝酸和浓硫酸来制硝基苯,故C错误;
D、在乙醇的催化氧化中,金属铜作催化剂,铜参与反应,最后会生成金属铜,
故D正确。
故选D.
24.向平衡 CHCOOH+HOCHCH CHCOOCHCH+HO 中加入 CHCH18OH,则
3 2 3 3 2 3 2 3 2
平衡时,含有18O的物质的种类是( ) ☆☆☆☆
A.1种 B.2种 C.3种 D.4种
【解答】
羧酸和醇反应发生酯化反应,醇提供羟基氢原子,结合生成水,其余部分互相结
合成酯,向平衡CHCOOH+HOCHCH CHCOOCHCH+HO中加入CHCH18OH,
3 2 3 3 2 3 2 3 2
由于酯化反应是可逆反应,反应方程式为
CHCOOH+CHCH18OH CHCO18OCHCH+HO,则平衡时,含有 18O 的物质为乙醇
3 3 2 3 2 3 2
和乙酸乙酯中。
故选B.
25.要合成带有放射性氧元素(*O)的乙酸乙酯,除必要的反应条件外,下列各
组反应物能满足合成要求的是( ) ☆☆☆☆
①CHCO*OH和CHOH ②CHCOOH和CH*OH
3 2 5 3 2 5
③CHC*OOH和CHOH ④CHCO*OH和CH*OH
3 2 5 3 2 5
A.①②③④ B.①③④ C.①②④ D.②③④
第14页(共16页)【解答】
①CHCO*OH和CHOH,酯化反应中,乙酸中的羟基脱去生成了水,所以乙酸乙酯
3 2 5
中不会含有放射性氧元素(*O),故①错误;
②CHCOOH和CH*OH,乙醇在酯化反应中只是失去氢原子,乙醇中的放射性氧元
3 2 5
素(*O)会保留在乙酸乙酯中,故②正确;
③CHC*OOH和CHOH,乙酸中的碳氧双中的放射性氧元素(*O)会保留在乙酸乙
3 2 5
酯中,即生成的乙酸乙酯含含放射性氧元素(*O),故③正确;
④CHCO*OH 和 CH*OH,乙酸的羟基中的放射性氧元素(*O)不会保留在乙酸乙
3 2 5
酯中,但是乙醇中的放射性氧元素(*O)会保留在乙酸乙酯中,即生成的乙酸乙
酯含含放射性氧元素(*O),故④正确。
故选D.
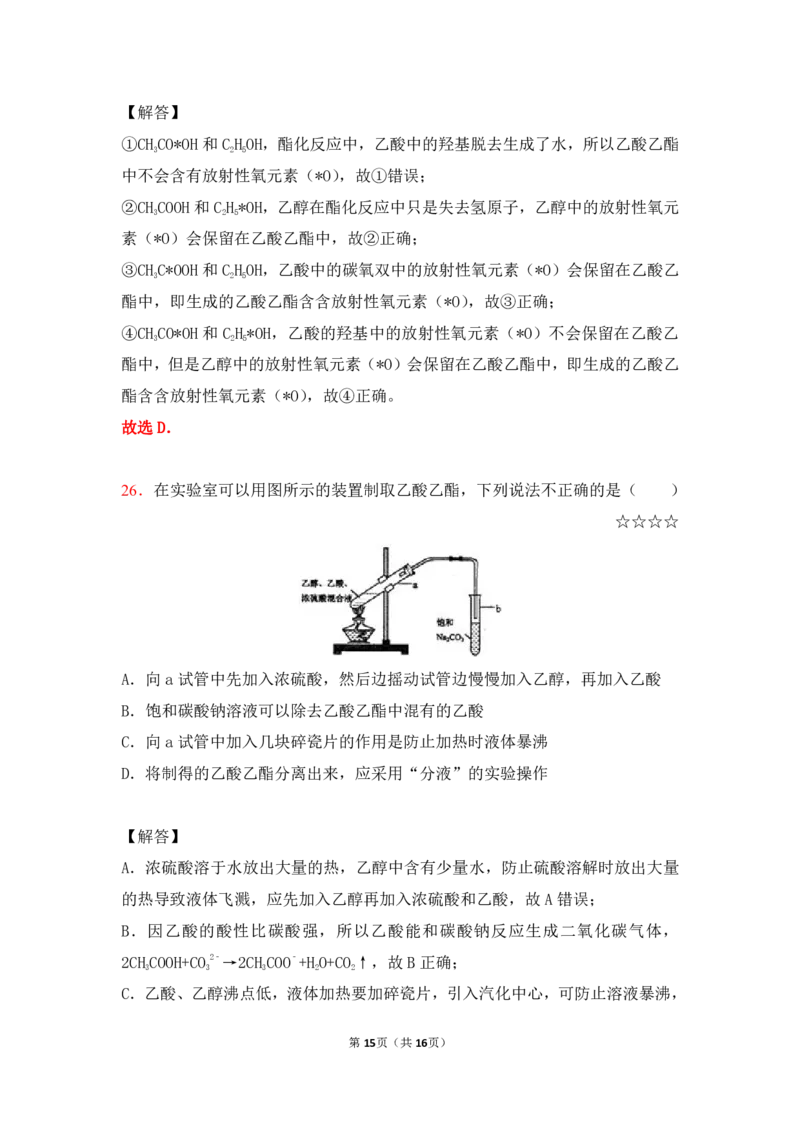
26.在实验室可以用图所示的装置制取乙酸乙酯,下列说法不正确的是( )
☆☆☆☆
A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加入乙酸
B.饱和碳酸钠溶液可以除去乙酸乙酯中混有的乙酸
C.向a试管中加入几块碎瓷片的作用是防止加热时液体暴沸
D.将制得的乙酸乙酯分离出来,应采用“分液”的实验操作
【解答】
A.浓硫酸溶于水放出大量的热,乙醇中含有少量水,防止硫酸溶解时放出大量
的热导致液体飞溅,应先加入乙醇再加入浓硫酸和乙酸,故 A错误;
B.因乙酸的酸性比碳酸强,所以乙酸能和碳酸钠反应生成二氧化碳气体,
2CHCOOH+CO2﹣→2CHCOO﹣+HO+CO↑,故B正确;
3 3 3 2 2
C.乙酸、乙醇沸点低,液体加热要加碎瓷片,引入汽化中心,可防止溶液暴沸,
第15页(共16页)故C正确;
D.试管b中液体混合物分层不互溶,乙酸乙酯在上层,可用分液方法分离,故
D正确。
故选A.
第16页(共16页)