文档内容
备战2024年高考化学考前手感保温训练(新高考卷)
专练15 14道选择题+主观原理题
完卷时间:40分钟
答案速查
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C D D D B C C D B B D B A C
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5
一、选择题(共42分,只有1个正确选项)
1.根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是
材料 组成或结构变化 性质变化与解释
可在铁表面形成一层致密的镍、铬氧化膜,增
A 钢铁 加入适量铬、镍等合金元素
强铁的抗腐蚀性能
通过与硝酸反应,在苯环上 硝基的吸电子作用使三硝基苯酚O-H键极性增
B 苯酚
引入3个硝基 强,羟基上的H更易电离
C 橡胶 在橡胶中添加炭黑 炭黑具有还原性,可增强橡胶的抗老化性能
纤维 用乙酰基取代纤维素上的羟
D 纤维素链上的羟基减少,纤维素吸水能力下降
素 基
A.A B.B C.C D.D
【答案】C
【解析】A.加入铬能使钢铁表面形成致密且紧固的氧化膜,防止内部的铁与氧气接触,加
入镍是使钠铁耐酸,碱腐蚀,A正确;B.苯酚通过与硝酸反应,在苯环上引入3个硝基,
苯环上的亲电取代,硝基的吸电子作用使三硝基苯酚O-H键极性增强,羟基上的H更易电
离,B正确;C.炭黑是最常用的补强填料,在很多橡胶制品中都会加入炭黑来提高制品的
补强性能,更布布耐磨,C错误;D.用乙酰基取代纤维素上的羟基成酯,纤维素链上的羟
基减少,纤维素吸水能力下降,D正确;故选C。
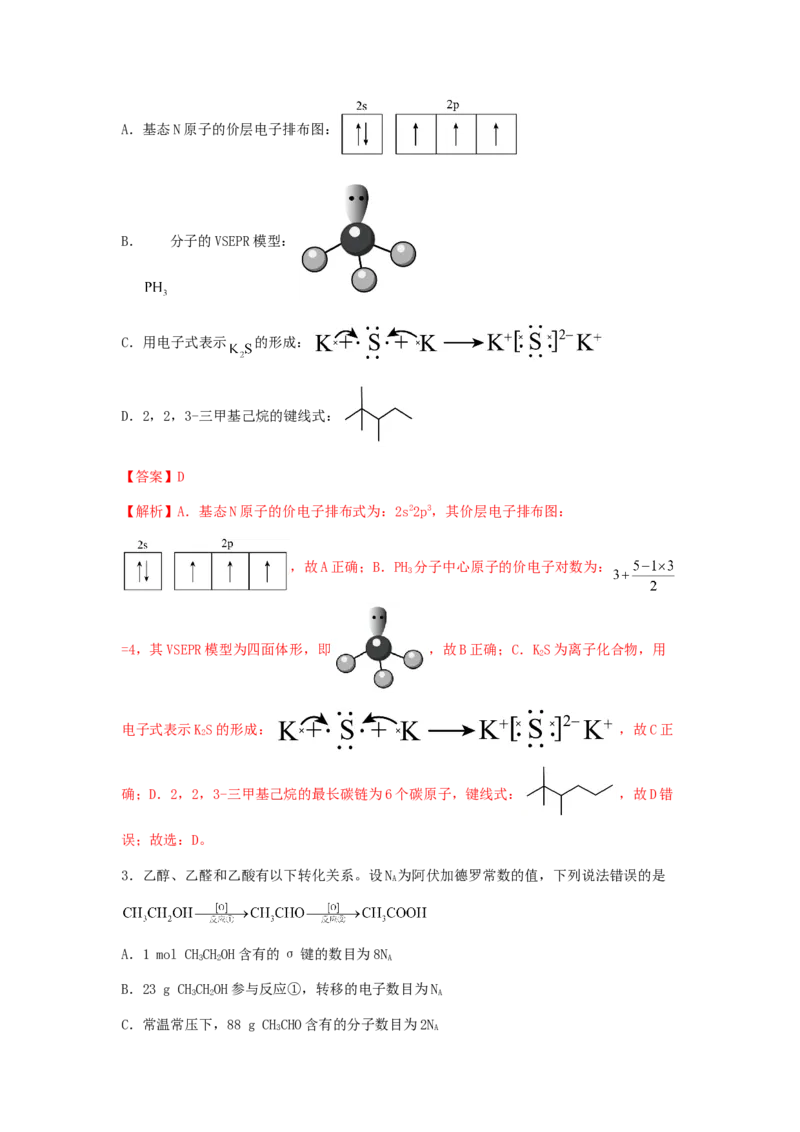
2.下列表示不正确的是A.基态N原子的价层电子排布图:
B. 分子的VSEPR模型:
C.用电子式表示 的形成:
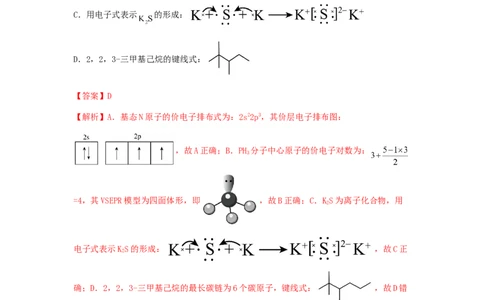
D.2,2,3-三甲基己烷的键线式:
【答案】D
【解析】A.基态N原子的价电子排布式为:2s22p3,其价层电子排布图:
,故A正确;B.PH 分子中心原子的价电子对数为:
3
=4,其VSEPR模型为四面体形,即 ,故B正确;C.KS为离子化合物,用
2
电子式表示KS的形成: ,故C正
2
确;D.2,2,3-三甲基己烷的最长碳链为6个碳原子,键线式: ,故D错
误;故选:D。
3.乙醇、乙醛和乙酸有以下转化关系。设N 为阿伏加德罗常数的值,下列说法错误的是
A
A.1 mol CHCHOH含有的σ键的数目为8N
3 2 A
B.23 g CHCHOH参与反应①,转移的电子数目为N
3 2 A
C.常温常压下,88 g CHCHO含有的分子数目为2N
3 AD.1mol·L-1的CHCOOH溶液中,CHCOOH、CHCOO-的数目之和为N
3 3 3 A
【答案】D
【解析】A.CHCHOH中均为单键,即所有键都是σ键,因此1 mol CHCHOH含有的σ键
3 2 3 2
的数目为8N,故A正确;B.23 g CHCHOH物质的量为0.5mol,反应①中C由-2价上升
A 3 2
到-1价,因此23 g CHCHOH参与反应①,转移的电子数目为N,故B正确;C.88 g
3 2 A
CHCHO物质的量为2mol,因此所含分子数目为2N,故C正确;D.未标明溶液体积,
3 A
CHCOOH、CHCOO-的数目之和无法计算,故D错误;故选D。
3 3
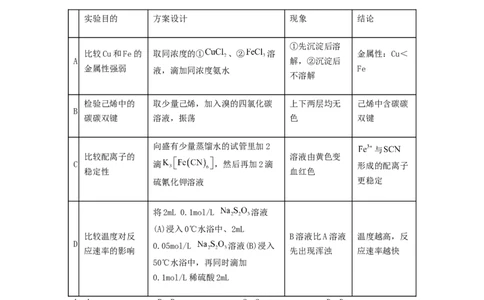
4.根据实验目的设计方案并进行实验,下列有关方案设计、实验现象或结论都正确的是
实验目的 方案设计 现象 结论
①先沉淀后溶
比较Cu和Fe的 取同浓度的① 、② 溶 金属性:Cu<
A 解,②沉淀后
金属性强弱 液,滴加同浓度氨水 Fe
不溶解
检验己烯中的 取少量己烯,加入溴的四氯化碳 上下两层均无 己烯中含碳碳
B
碳碳双键 溶液,振荡 色 双键
向盛有少量蒸馏水的试管里加2
与
比较配离子的 溶液由黄色变
C 滴 ,然后再加2滴 形成的配离子
稳定性 血红色
硫氰化钾溶液 更稳定
将2mL 0.1mol/L 溶液
(A)浸入0℃水浴中、2mL
比较温度对反 B溶液比A溶液 温度越高,反
D 0.05mol/L 溶液(B)浸入
应速率的影响 先出现浑浊 应速率越快
50℃水浴中,再同时滴加
0.1mol/L稀硫酸2mL
A.A B.B C.C D.D
【答案】D
【解析】A.取同浓度的① 、② 溶液,滴加同浓度氨水,CuCl 先生成Cu(OH)
2
沉淀,与氨水继续反应,生成 ,FeCl 生成Fe(OH) 沉淀,该实验不能比
2 3 3
较Fe、Cu金属性的大小,故A错误;B.取少量己烯,加入溴的四氯化碳溶液,振荡,溴
的四氯化碳溶液褪色,溶液不分层,能使溴的四氯化碳溶液褪色的官能团还有碳碳三键等,
该实验也不能说明己烯中含有碳碳双键,故B错误;C.向盛有少量蒸馏水的试管里加2滴,然后再加2滴硫氰化钾溶液,溶液颜色不变,Fe3+与CN-形成的配离子更稳
定,故C错误;D.两份混合溶液体积相同,浓度相同,但温度不同,热水中出现浑浊的时
间短,从而得出升温加可加快化学反应速率,故D正确;故选D。
5.下列化学反应与方程式不相符的是
A.含等物质的量的 和 的溶液混合的离子方程式:
B.铅酸蓄电池充电时的阳极反应:
C.表示 气体燃烧热的热化学方程式:
D.对苯二甲酸与乙二醇合成涤纶:n
【答案】B
【解析】A.含等物质的量的 和 的溶液混合生成 、和 ,
离子方程式: ,故A正确;B.铅酸
蓄电池充电时的阳极反应: ,故B错误;C.在101
kPa时,1 mol纯物质完全燃烧生成指定产物时所放出的热量,叫做该物质的燃烧热,表示
气体燃烧热的热化学方程式:
,故C正确;D.对苯二甲酸与乙二醇合成涤纶是羧基与羟基脱水发生
缩聚反应,化学方程式为:n
,故D正确;故选B。
6. YXEZM 是一种常见的营养强化剂。其中,元素周期表中 与Y、M相邻,基态 原子
4 9 2 4
的价电子排布式nsnnpn,Z的第一电离能大于 的,基态 原子与基态 原子的未成对电
子数相同; 为原子半径最小的元素; 的合金是目前用量最大的金属材料。下列说法正
确的是A.电负性: B.非金属性:
C.简单氢化物的沸点: D.高温下, 的单质与 反应得到
【答案】C
【分析】基态 原子的价电子排布式为nsnnpn,即2s22p2,所以Y是C元素,元素周期表中
与Y、M相邻,Z的第一电离能大于 的,则Z是N元素,基态 原子与基态 原子的未
成对电子数相同,则M为O元素, 为原子半径最小的元素,则X是H元素; 的合金是
目前用量最大的金属材料,则E是Fe元素。
【解析】A.同周期从左到右,元素的电负性逐渐增强,同主族从上到下,元素的电负性逐
渐减小,通常非金属的电负性大于金属,所以电负性:N>H>Fe,A错误;B.同周期从左到
右,元素的非金属性逐渐增强,非金属性:CNH>CH,C正确;D.高
2 2 3 4
温下铁与水蒸气反应得到四氧化三铁,D错误;故选C。
7.物质的结构决定物质的性质。下列性质差异与结构因素匹配正确的是
选项 性质差异 结构因素
A 键角:CH(109°28′)大于NH(107.3°) 中心原子杂化方式
4 3
B 摩氏硬度:金刚石(10) 石英(7) 晶体类型
C 酸性:CFCOOH(pKa=0.23)>CClCOOH(pKa=0.65) 羟基极性
3 3
苯酚的溶解度:高于65℃时(能与水互溶) 室温时
D 电离程度
(9.2g)
A.A B.B C.C D.D
【答案】C
【解析】A.甲烷和氨气的中心原子的杂化方式均为sp3,其键角差异是:氨气的中心原子
N原子上有孤电子对,根据价层电子对互斥理论,孤电子对与σ键的斥力大于σ键之间的
斥力,因此氨气的键角略小于109°28′,A不合题意;B.金刚石和石英均为原子晶体,
由于C-C键的键能小于Si-O,石英的摩氏硬度比金刚石小,B不合题意;C.F电负性较Cl
大,导致-CF 的吸电子效应强于-CCl,羧酸CFCOOH分子中羟基极性增大,则氢离子越易
3 3 3
电离,故酸性:CFCOOH>CClCOOH,C符合题意;D.苯酚和水均为极性分子,苯酚晶体能
3 3
溶于水,苯酚晶体分子间存在氢键,室温下难以被破坏,故苯酚在室温下的溶解度不大,
当温度高于65℃时,苯酚晶体分子间的氢键被破坏,与水分子之间形成了氢键,增大了溶
解度,能与水互溶,即与电离情况无关,D不合题意;故答案为:C。8.实验室进行下列操作时,仪器选用错误的是
Ⅰ.用四氯化碳提取碘水中的碘 Ⅱ.量取一定体积的酸性 溶液
A.分液漏斗 B.酸式滴定管
Ⅲ.灼烧胆矾 Ⅳ.用 固体和水制备少量氧气
C.坩埚 D.启普发生器
A.A B.B C.C D.D
【答案】D
【解析】A.提取碘水中的碘,用四氯化碳萃取,选用分液漏斗,A正确;B.酸性
溶液有强氧化性,选用酸式滴定管,B正确;C.灼烧固体用坩埚,C正确;D. 是粉
末状固体,易从启普发生器的球形容器中掉入底部半球形容器内,且过氧化钠与水反应的
速率太快、反应放热,所以用 固体和水制备少量氧气时不能选用启普发生器装置,D
错误;故答案选D。
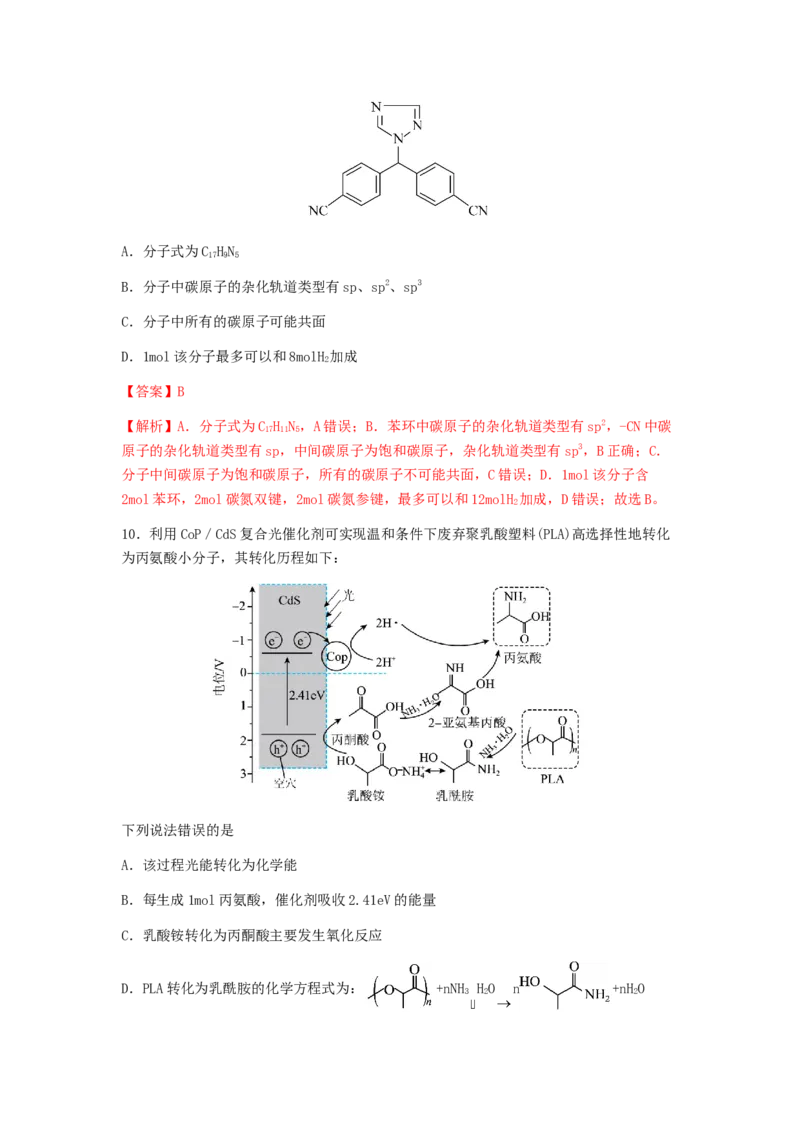
9.药物来曲唑的结构简式如图所示,下列关于来曲唑的叙述正确的是A.分子式为C HN
17 9 5
B.分子中碳原子的杂化轨道类型有sp、sp2、sp3
C.分子中所有的碳原子可能共面
D.1mol该分子最多可以和8molH 加成
2
【答案】B
【解析】A.分子式为C H N,A错误;B.苯环中碳原子的杂化轨道类型有sp2,-CN中碳
17 11 5
原子的杂化轨道类型有sp,中间碳原子为饱和碳原子,杂化轨道类型有sp3,B正确;C.
分子中间碳原子为饱和碳原子,所有的碳原子不可能共面,C错误;D.1mol该分子含
2mol苯环,2mol碳氮双键,2mol碳氮参键,最多可以和12molH 加成,D错误;故选B。
2
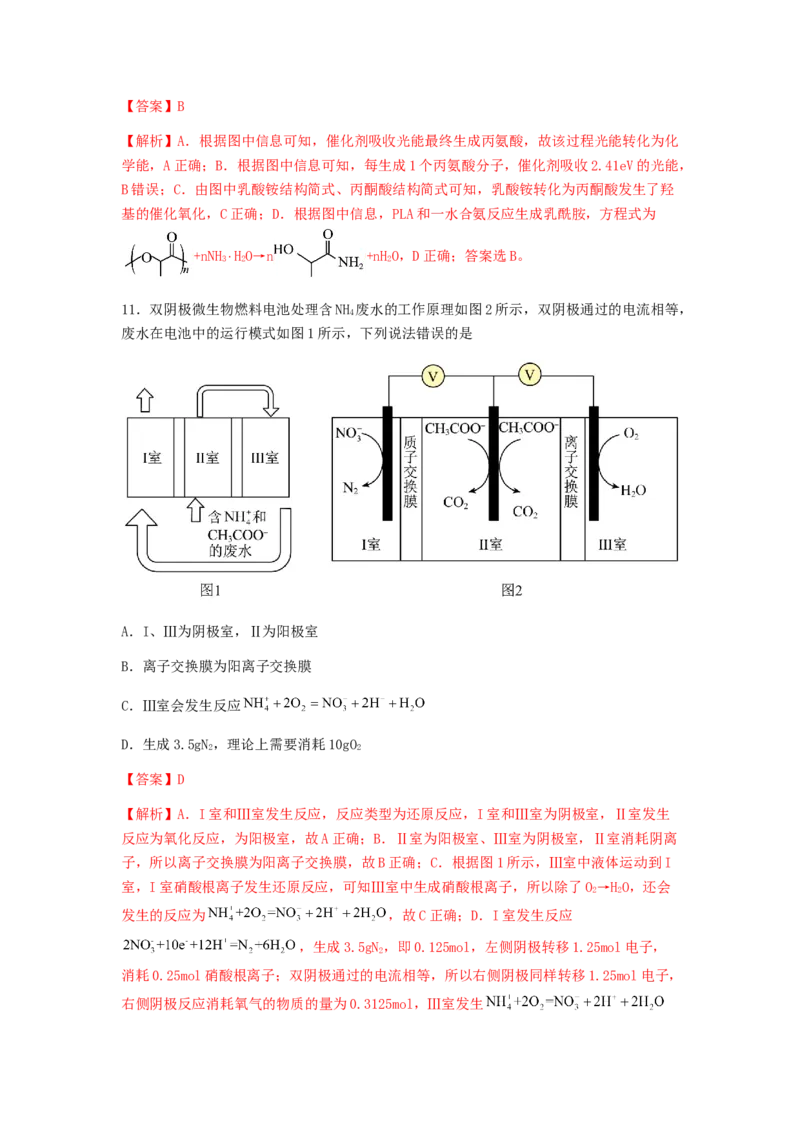
10.利用CoP/CdS复合光催化剂可实现温和条件下废弃聚乳酸塑料(PLA)高选择性地转化
为丙氨酸小分子,其转化历程如下:
下列说法错误的是
A.该过程光能转化为化学能
B.每生成1mol丙氨酸,催化剂吸收2.41eV的能量
C.乳酸铵转化为丙酮酸主要发生氧化反应
D.PLA转化为乳酰胺的化学方程式为: +nNH HO n +nHO
3 2 2【答案】B
【解析】A.根据图中信息可知,催化剂吸收光能最终生成丙氨酸,故该过程光能转化为化
学能,A正确;B.根据图中信息可知,每生成1个丙氨酸分子,催化剂吸收2.41eV的光能,
B错误;C.由图中乳酸铵结构简式、丙酮酸结构简式可知,乳酸铵转化为丙酮酸发生了羟
基的催化氧化,C正确;D.根据图中信息,PLA和一水合氨反应生成乳酰胺,方程式为
+nNH 3⋅H
2
O→n +nH
2
O,D正确;答案选B。
11.双阴极微生物燃料电池处理含NH 废水的工作原理如图2所示,双阴极通过的电流相等,
4
废水在电池中的运行模式如图1所示,下列说法错误的是
A.I、Ⅲ为阴极室,Ⅱ为阳极室
B.离子交换膜为阳离子交换膜
C.Ⅲ室会发生反应
D.生成3.5gN,理论上需要消耗10gO
2 2
【答案】D
【解析】A.I室和Ⅲ室发生反应,反应类型为还原反应,I室和Ⅲ室为阴极室,Ⅱ室发生
反应为氧化反应,为阳极室,故A正确;B.Ⅱ室为阳极室、Ⅲ室为阴极室,Ⅱ室消耗阴离
子,所以离子交换膜为阳离子交换膜,故B正确;C.根据图1所示,Ⅲ室中液体运动到I
室,I室硝酸根离子发生还原反应,可知Ⅲ室中生成硝酸根离子,所以除了O→HO,还会
2 2
发生的反应为 ,故C正确;D.I室发生反应
,生成3.5gN,即0.125mol,左侧阴极转移1.25mol电子,
2
消耗0.25mol硝酸根离子;双阴极通过的电流相等,所以右侧阴极同样转移1.25mol电子,
右侧阴极反应消耗氧气的物质的量为0.3125mol,Ⅲ室发生反应生成0.25mol硝酸根离子消耗0.5mol氧气,理论上需要消耗0.8125molO,即26g,故
2
D错误;答案选D。
12.通过佛尔哈德法可以测定三氯氧磷( )样品中 元素的含量,实验步骤如下:
I.取mg样品于锥形瓶中,加入足量的 溶液,待完全反应后加稀硝酸至溶液显酸性;
II.向锥形瓶中加入0.1000 的 溶液50.00 ,使 完全沉淀;III.向其
中加入2 硝基苯,用力摇动,使沉淀表面被有机物覆盖:
IV.加入指示剂,用c 溶液滴定过量 至终点,记下所用体积为V
。
已知: , 。
下列说法正确的是
A.滴定选用的指示剂为甲基橙
B.硝基苯的作用为防止 转化为
C.若取消步骤III,测定结果偏大
D.本次实验测得 元素的质量分数为
【答案】B
【解析】A.由Ⅰ、Ⅱ、Ⅳ滴定过程溶液始终显酸性,无法用甲基橙作指示剂,A错误;
B.由可知Ksp(AgCl)>Ksp(AgSCN)=2×10-12,硝基苯的作用为防止AgCl转化为AgSCN,B正
确;C.取消步骤Ⅲ,则AgCl转化为AgSCN,所需NHSCN体积V偏大,可知Cl%偏小,C错
4
误;D.Ag+总物质的量为0.1000mol·L-1×50.00mL=5.0×10-3mol,NHSCN的物质的量为
4
cmol·L-1×VmL=cV×10-3mol,设三氯氧磷(POCl)样品中Cl元素的物质的量为x,结合关系
3
式POCl~3Cl-~3AgNO~3Ag+、Ag+~NHSCN可知有x+ cV×10-3=5.0×10-3mol,解得x=(5.0-
3 3 4
cV)×10-3mol,因此三氯氧磷(POCl)样品中Cl元素的质量为(5.0-cV)×10-3mol×35.5g/
3
mol=3.55(5.0-cV) ×10-2g,因此Cl元素的质量分数为 ,D错误;故选B。
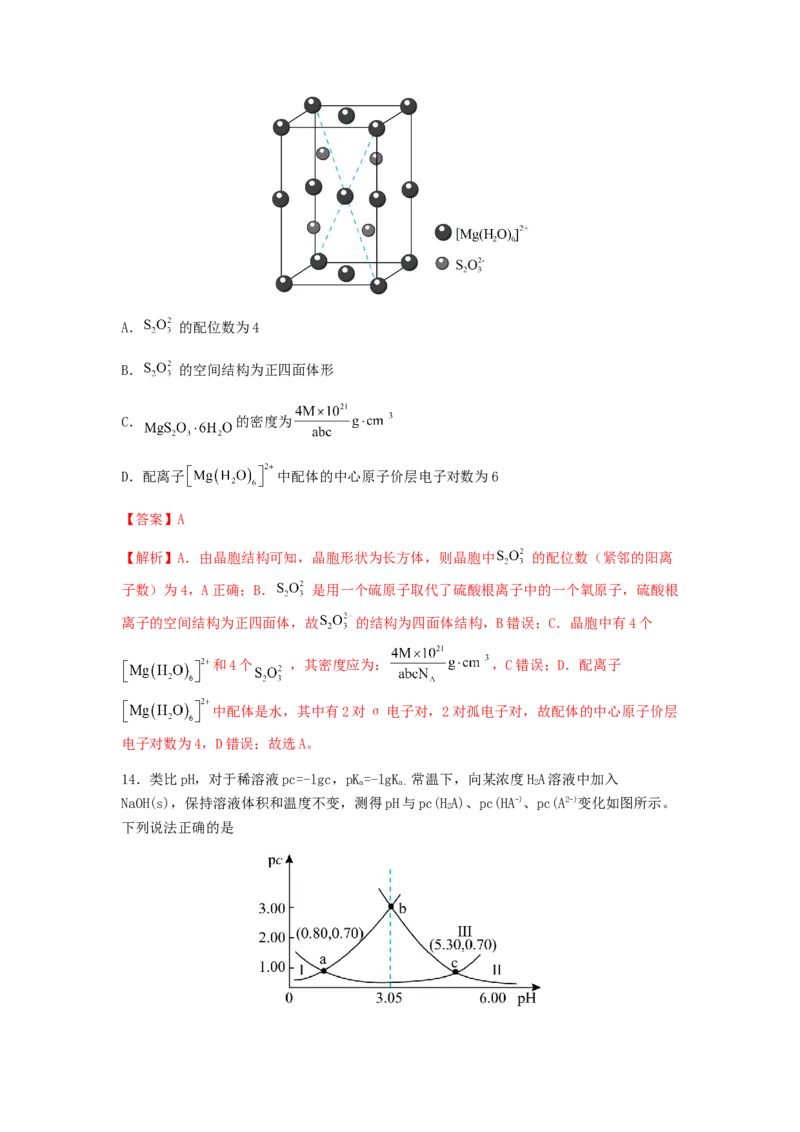
13. (摩尔质量为 )的晶胞形状为长方体,边长分别为a nm、b
nm、c nm,结构如图所示。下列说法正确的是A. 的配位数为4
B. 的空间结构为正四面体形
C. 的密度为
D.配离子 中配体的中心原子价层电子对数为6
【答案】A
【解析】A.由晶胞结构可知,晶胞形状为长方体,则晶胞中 的配位数(紧邻的阳离
子数)为4,A正确;B. 是用一个硫原子取代了硫酸根离子中的一个氧原子,硫酸根
离子的空间结构为正四面体,故 的结构为四面体结构,B错误;C.晶胞中有4个
和4个 ,其密度应为: ,C错误;D.配离子
中配体是水,其中有2对σ电子对,2对孤电子对,故配体的中心原子价层
电子对数为4,D错误;故选A。
14.类比pH,对于稀溶液pc=-lgc,pK=-lgK 常温下,向某浓度HA溶液中加入
a a. 2
NaOH(s),保持溶液体积和温度不变,测得pH与pc(HA)、pc(HA-)、pc(A2-)变化如图所示。
2
下列说法正确的是A.pH=3.05时,c(HA-)>c(A2-)>c(HA)
2
B.K (HA)的数量级为10-6
a1 2
C.c点时,c(Na+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1
D.若醋酸的pK=4.76,则HA-与CHCOO-不能大量共存
a 3
【答案】C
【分析】根据题意和图中信息,随pH增大,c(HA)逐渐减小,c(HA-)先增大后减小,c(A2-)
2
逐渐增大,pM=-lgc(M),则pc(HA)逐渐增大、pc(HA-)先减小后增大、pc(A2-)逐渐减小,
2
即曲线Ⅰ、Ⅱ、Ⅲ分别代表的粒子为HA、A2-、HA-,据此分析解答。
2
【解析】A.曲线Ⅰ、Ⅱ分别代表的粒子为HA、A2-,pH=3.05时,c(A2-)=c(HA),故A错误;
2 2
B.a点,c(HA)=c(HA-),则K = =c(H+)= 10−0.80,则K (HA)的数量级为10-
2 a1 a1 2
1,故B错误;C.c点c(HA-)=c(A2-)=10-0.7,根据电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HA-)
+2c(A2-),c点时,c(Na+)= c(OH-)+3c(HA-)- c(H+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1,
故C正确;D.由c点c(HA-)=c(A2-),K = =c(H+)= 10−5.30,若醋酸的pK=4.76
a2 a
则K=10-4.76> K ,酸性:CHCOOH> HA-,则HA-与CHCOO-能大量共存,故D错误;故选:
a a2 3 3
C。
二、主观题
17.(15分)丙烯是生产塑料、橡胶和纤维三大合成材料的重要基础化工原料。
(1)丙烷经催化脱氢可制丙烯: ,该
反应自发进行的条件是 。下列措施既能提高反应物 的平衡转化率,又能增大生
成 的反应速率的是 (填标号)。
a.升高温度 b.增大压强 c.加入催化剂 d.恒容条件增加 的量
(2)已知丙烷和丙烯的燃烧热分别为 和 ,则丙烷氧化脱氢反应:
(填“ ”“ ”或“
”)。
(3)温度一定时,假定体系内只有反应 发生,反应过程中压强
恒定为 (即 的初始压强),平衡转化率为 ,该反应的平衡常数 为
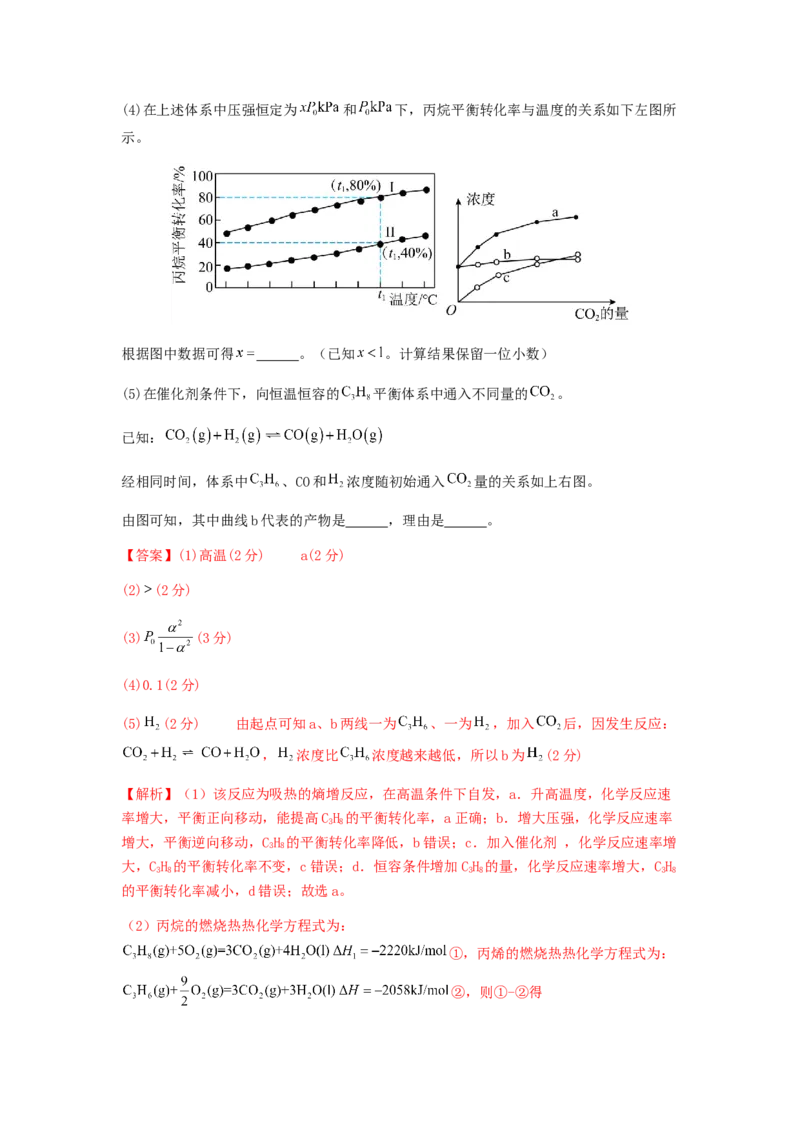
kPa(用平衡分压代替平衡浓度计算,分压 总压 物质的量分数)。(4)在上述体系中压强恒定为 和 下,丙烷平衡转化率与温度的关系如下左图所
示。
根据图中数据可得 。(已知 。计算结果保留一位小数)
(5)在催化剂条件下,向恒温恒容的 平衡体系中通入不同量的 。
已知:
经相同时间,体系中 、CO和 浓度随初始通入 量的关系如上右图。
由图可知,其中曲线b代表的产物是 ,理由是 。
【答案】(1)高温(2分) a(2分)
(2) (2分)
(3) (3分)
(4)0.1(2分)
(5) (2分) 由起点可知a、b两线一为 、一为 ,加入 后,因发生反应:
, 浓度比 浓度越来越低,所以b为 (2分)
【解析】(1)该反应为吸热的熵增反应,在高温条件下自发,a.升高温度,化学反应速
率增大,平衡正向移动,能提高CH 的平衡转化率,a正确;b.增大压强,化学反应速率
3 8
增大,平衡逆向移动,CH 的平衡转化率降低,b错误;c.加入催化剂 ,化学反应速率增
3 8
大,CH 的平衡转化率不变,c错误;d.恒容条件增加CH 的量,化学反应速率增大,CH
3 8 3 8 3 8
的平衡转化率减小,d错误;故选a。
(2)丙烷的燃烧热热化学方程式为:
①,丙烯的燃烧热热化学方程式为:
②,则①-②得-2220+2058=−162kJ⋅mol−1,由于生成液态水
放热更多,所以ΔH
2
>−162kJ⋅mol−1;
(3)假设起始时CH 的物质的量为1mol,则转化的CH 为αmol,生成的CH、H 各为
3 8 3 8 3 6 2
αmol,平衡时CH、CH、H 各为(1-α)mol、αmol、αmol,则p(CH)=p(H)=
3 8 3 6 2 3 6 2
kpa,p(CH)= kpa,K= ;
3 8 p
(4)该反应正向为气体体积增大的方向,加压平衡逆向移动,根据x<1,则p 的压强更大,
0
转化率更小,为40%,xp 的转化率为80%,根据温度不变,平衡常数不变,带入 可
0
得 ,x ;
(5)由图可知,其中曲线b代表的产物是H,由起点可知a、b两线一为CH、一为H,加
2 3 6 2
入CO 后,因发生反应:CO+H CO+HO,H 浓度比CH 浓度越来越低,所以b为H。
2 2 2⇌ 2 2 3 6 2