文档内容
专练 51 实验方案的设计与评价
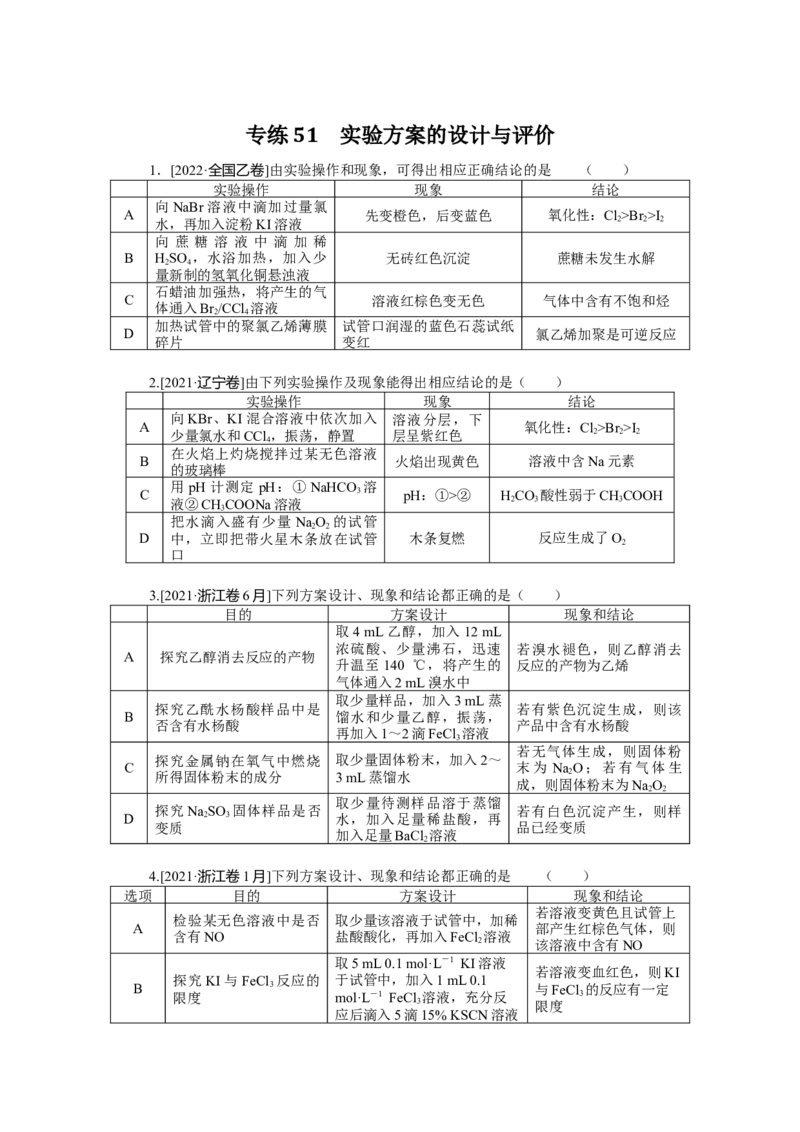
1.[2022·全国乙卷]由实验操作和现象,可得出相应正确结论的是 ( )
实验操作 现象 结论
向NaBr溶液中滴加过量氯
A 先变橙色,后变蓝色 氧化性:Cl>Br >I
水,再加入淀粉KI溶液 2 2 2
向 蔗 糖 溶 液 中 滴 加 稀
B HSO ,水浴加热,加入少 无砖红色沉淀 蔗糖未发生水解
2 4
量新制的氢氧化铜悬浊液
石蜡油加强热,将产生的气
C 溶液红棕色变无色 气体中含有不饱和烃
体通入Br /CCl 溶液
2 4
加热试管中的聚氯乙烯薄膜 试管口润湿的蓝色石蕊试纸
D 氯乙烯加聚是可逆反应
碎片 变红
2.[2021·辽宁卷]由下列实验操作及现象能得出相应结论的是( )
实验操作 现象 结论
向KBr、KI混合溶液中依次加入 溶液分层,下
A 氧化性:Cl>Br >I
少量氯水和CCl ,振荡,静置 层呈紫红色 2 2 2
4
在火焰上灼烧搅拌过某无色溶液
B 火焰出现黄色 溶液中含Na元素
的玻璃棒
用pH计测定 pH:①NaHCO 溶
C 3 pH:①>② HCO 酸性弱于CHCOOH
液②CHCOONa溶液 2 3 3
3
把水滴入盛有少量 NaO 的试管
2 2
D 中,立即把带火星木条放在试管 木条复燃 反应生成了O
2
口
3.[2021·浙江卷6月]下列方案设计、现象和结论都正确的是( )
目的 方案设计 现象和结论
取4 mL乙醇,加入12 mL
浓硫酸、少量沸石,迅速 若溴水褪色,则乙醇消去
A 探究乙醇消去反应的产物
升温至140 ℃,将产生的 反应的产物为乙烯
气体通入2 mL溴水中
取少量样品,加入3 mL蒸
探究乙酰水杨酸样品中是 若有紫色沉淀生成,则该
B 馏水和少量乙醇,振荡,
否含有水杨酸 产品中含有水杨酸
再加入1~2滴FeCl 溶液
3
若无气体生成,则固体粉
探究金属钠在氧气中燃烧 取少量固体粉末,加入2~
C 末为 NaO;若有气体生
所得固体粉末的成分 3 mL蒸馏水 2
成,则固体粉末为NaO
2 2
取少量待测样品溶于蒸馏
探究NaSO 固体样品是否 若有白色沉淀产生,则样
D 2 3 水,加入足量稀盐酸,再
变质 品已经变质
加入足量BaCl 溶液
2
4.[2021·浙江卷1月]下列方案设计、现象和结论都正确的是 ( )
选项 目的 方案设计 现象和结论
若溶液变黄色且试管上
检验某无色溶液中是否 取少量该溶液于试管中,加稀
A 部产生红棕色气体,则
含有NO 盐酸酸化,再加入FeCl 溶液
2 该溶液中含有NO
取5 mL 0.1 mol·L-1 KI溶液
若溶液变血红色,则KI
探究KI与FeCl 反应的 于试管中,加入1 mL 0.1
B 3 与FeCl 的反应有一定
限度 mol·L-1 FeCl 溶液,充分反 3
3 限度
应后滴入5滴15% KSCN溶液取2 mL卤代烃样品于试管
若产生的沉淀为白色,
中,加入5 mL 20%KOH水溶
C 判断某卤代烃中的卤素 则该卤代烃中含有氯元
液混合后加热,再滴加AgNO
3 素
溶液
取2 mL 20%的蔗糖溶液于试
若没有生成砖红色沉
探究蔗糖在酸性水溶液 管中,加入适量稀HSO 后水
D 2 4 淀,则蔗糖在酸性水溶
中的稳定性 浴加热5 min;再加入适量新
液中稳定
制Cu(OH) 悬浊液并加热
2
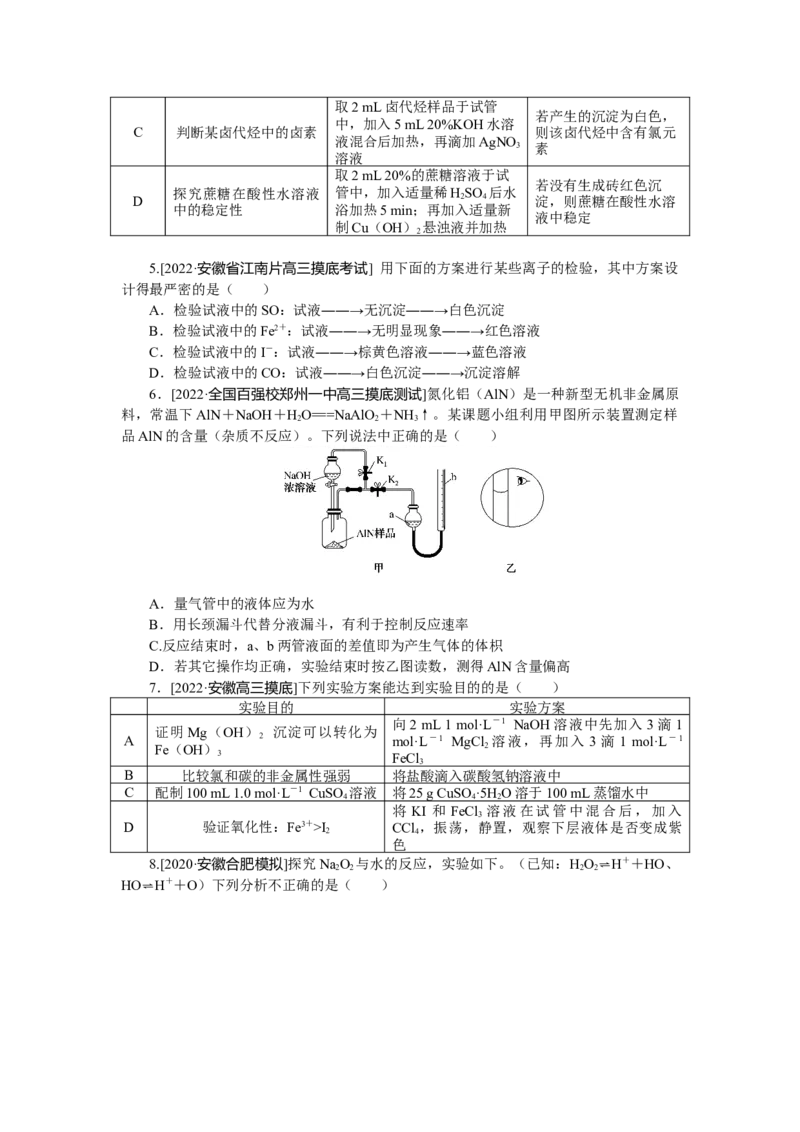
5.[2022·安徽省江南片高三摸底考试] 用下面的方案进行某些离子的检验,其中方案设
计得最严密的是( )
A.检验试液中的SO:试液――→无沉淀――→白色沉淀
B.检验试液中的Fe2+:试液――→无明显现象――→红色溶液
C.检验试液中的I-:试液――→棕黄色溶液――→蓝色溶液
D.检验试液中的CO:试液――→白色沉淀――→沉淀溶解
6.[2022·全国百强校郑州一中高三摸底测试]氮化铝(AlN)是一种新型无机非金属原
料,常温下AlN+NaOH+HO===NaAlO +NH ↑。某课题小组利用甲图所示装置测定样
2 2 3
品AlN的含量(杂质不反应)。下列说法中正确的是( )
A.量气管中的液体应为水
B.用长颈漏斗代替分液漏斗,有利于控制反应速率
C.反应结束时,a、b两管液面的差值即为产生气体的体枳
D.若其它操作均正确,实验结束时按乙图读数,测得AlN含量偏高
7.[2022·安徽高三摸底]下列实验方案能达到实验目的的是( )
实验目的 实验方案
向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1
证明Mg(OH) 沉淀可以转化为
A 2 mol·L-1 MgCl 溶液,再加入 3 滴 1 mol·L-1
Fe(OH) 2
3 FeCl
3
B 比较氯和碳的非金属性强弱 将盐酸滴入碳酸氢钠溶液中
C 配制100 mL 1.0 mol·L-1 CuSO 溶液 将25 g CuSO ·5H O溶于100 mL蒸馏水中
4 4 2
将 KI 和 FeCl 溶液在试管中混合后,加入
3
D 验证氧化性:Fe3+>I CCl ,振荡,静置,观察下层液体是否变成紫
2 4
色
8.[2020·安徽合肥模拟]探究Na
2
O
2
与水的反应,实验如下。(已知:H
2
O 2⇌H++HO、
HO⇌H++O)下列分析不正确的是( )A.①⑤中产生的气体能使带火星的木条复燃
B.①④中均发生了氧化还原反应和复分解反应
C.②⑤中KMnO 与MnO 的作用不同,产生气体的量也不同
4 2
D.通过③能比较酸性:HCl>H O
2 2
9.[2022·辽宁丹东五校联考]下列方案设计、现象和结论都正确的是( )
选项 目的 方案设计 现象和结论
若无气体生成,则固体粉
探究金属钠在氧气中 取少量固体粉末,加入 2~3
A 末为 NaO;若有气体生
受热所得固体的成分 mL蒸馏水 2
成,则固体粉末为NaO
2 2
取5 mL 0.1 mol·L-1 KI 溶液
探究KI与FeCl 3反 于试管中,加入 1 mL 0.1 若溶液变红,则 KI 与
B
应的限度 mol·L-1 FeCl 溶液,充分反 FeCl 的反应有一定限度
3 3
应后滴入几滴KSCN溶液
取少量待测样品溶于蒸馏
探究NaSO 固体样品 若有白色沉淀产生,则样
C 2 3 水,加入足量稀硫酸,再加
是否变质 品已经变质
入足量BaCl 溶液
2
取少量该溶液于试管中,滴
检验某无色溶液中是 不变蓝,证明溶液中无铵
D 加稀氢氧化钠溶液,将湿润
否含有NH 根离子
的红色石蕊试纸放试管口