文档内容
专项训练 反应机理中的过渡态理论(解析版)
一、单选题
1. 选择性催化还原( )是目前最有效且应用最广的除去 的方法,在
催化剂上发生反应的机理如图所示,其中TS表示过渡态。下列说法正确
的是
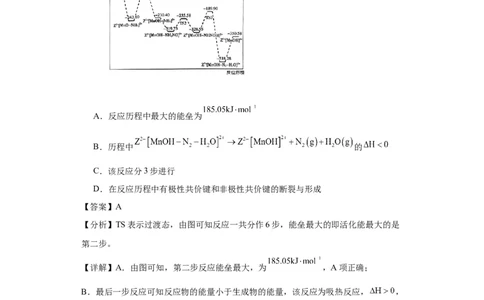
A.反应历程中最大的能垒为
B.历程中 的
C.该反应分3步进行
D.在反应历程中有极性共价键和非极性共价键的断裂与形成
【答案】A
【分析】TS表示过渡态,由图可知反应一共分作6步,能垒最大的即活化能最大的是
第二步。
【详解】A.由图可知,第二步反应能垒最大,为 ,A项正确;
B.最后一步反应可知反应物的能量小于生成物的能量,该反应为吸热反应, ,
B项错误;
C.TS表示过渡态,由图可知反应分6步进行,C项错误;
D.反应历程中没有非极性共价键的断裂,D项错误;
答案选A。
2.科学工作者结合实验与计算机模拟结果,研究了在Pt/SiO 催化剂表面上CO 与H
2 2 2
的反应历程,前三步历程如图所示,其中吸附在Pt/SiO 催化剂表面上的物种用“•”
2
标注,Ts表示过渡态。
资料收集整理【淘宝店铺:向阳百分百】下列有关叙述正确的是
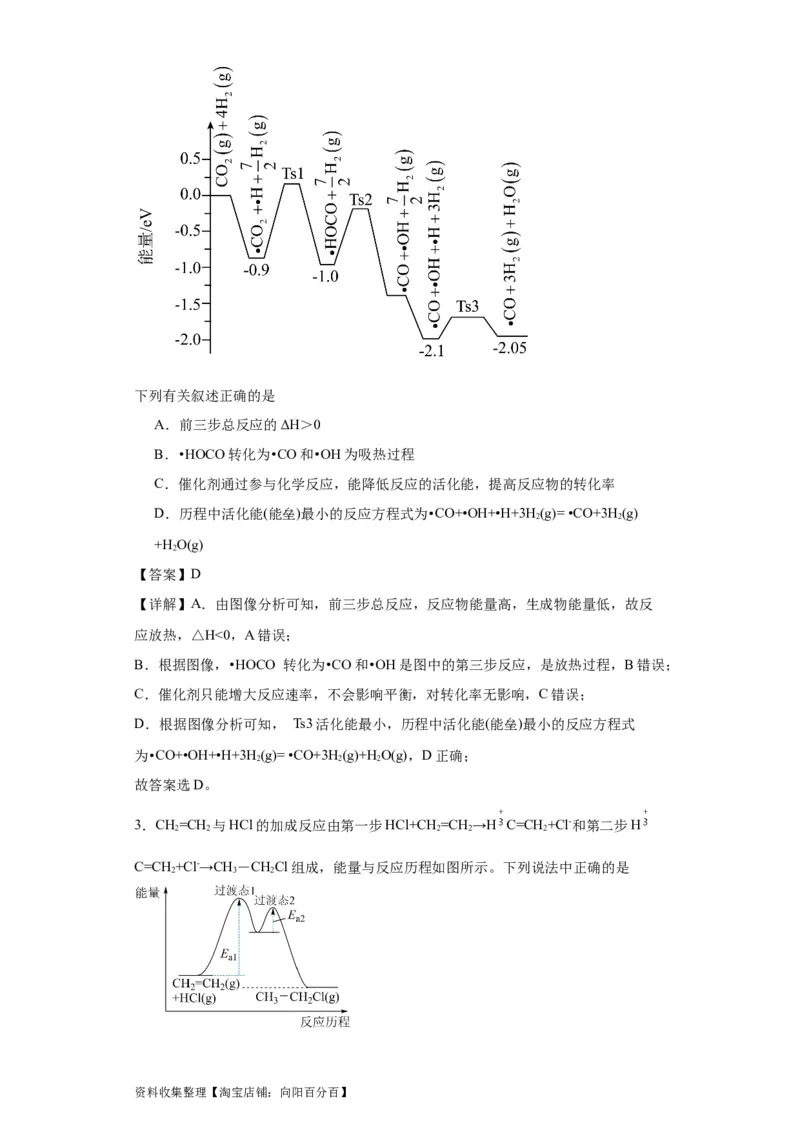
A.前三步总反应的ΔH>0
B.•HOCO转化为•CO和•OH为吸热过程
C.催化剂通过参与化学反应,能降低反应的活化能,提高反应物的转化率
D.历程中活化能(能垒)最小的反应方程式为•CO+•OH+•H+3H (g)= •CO+3H (g)
2 2
+H O(g)
2
【答案】D
【详解】A.由图像分析可知,前三步总反应,反应物能量高,生成物能量低,故反
应放热,△H<0,A错误;
B.根据图像,•HOCO 转化为•CO和•OH是图中的第三步反应,是放热过程,B错误;
C.催化剂只能增大反应速率,不会影响平衡,对转化率无影响,C错误;
D.根据图像分析可知, Ts3活化能最小,历程中活化能(能垒)最小的反应方程式
为•CO+•OH+•H+3H (g)= •CO+3H (g)+HO(g),D正确;
2 2 2
故答案选D。
3.CH=CH 与HCl的加成反应由第一步HCl+CH =CH →H C=CH +Cl-和第二步H
2 2 2 2 2
C=CH +Cl-→CH-CHCl组成,能量与反应历程如图所示。下列说法中正确的是
2 3 2
资料收集整理【淘宝店铺:向阳百分百】A.两步反应均释放能量
B.加入催化剂,E、∆H均减小,反应速率加快
a
C.第二步H C=CH 与Cl-的碰撞100%有效
2
D.过渡态2比过渡态1更稳定
【答案】D
【详解】A.由图可知,第一步反应的反应物的总能量小于生成物的总能量,则第一
步反应为吸热反应,故A错误;
B.催化剂可以降低反应的活化能E,加快反应速率,但不能改变反应的∆H,故B错
a
误;
C.虽然第二步反应速率较快,但H+C=CH 与Cl﹣的碰撞中只有少数碰撞能发生化学
3 2
反应,所以第二步H+C=CH 与Cl﹣的碰撞不是100%有效,故C错误;
3 2
D.物质能量越低越稳定,过渡态2能量较低,则比过渡态1稳定,故D正确;
故选D。
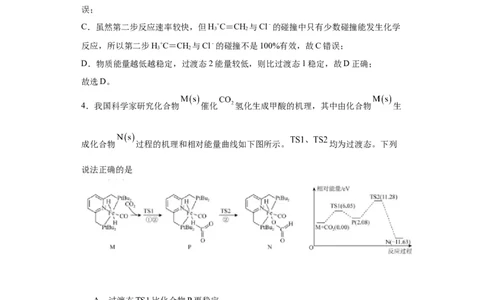
4.我国科学家研究化合物 催化 氢化生成甲酸的机理,其中由化合物 生
成化合物 过程的机理和相对能量曲线如下图所示。 均为过渡态。下列
说法正确的是
A.过渡态TS1比化合物Р更稳定
B.过程M→P为化合物M生成化合物N的决速步骤
C.化合物M催化 氢化生成甲酸的反应过程中一定有 键的生成和断裂
D.由 生成 的热化学方程式:
【答案】C
【详解】A.由图可知,过渡态TS1比P能量高,则P更稳定,选项A错误;
B.由图可知,过程P→TS2为两步反应中活化能较大的反应,为慢反应,即为化合物
资料收集整理【淘宝店铺:向阳百分百】M生成化合物N的决速步骤,选项B错误;
C.化合物M为催化剂,反应前后结构不会改变,比较M、N的结构可知,当Fe-O键
的断裂重新连接氢原子生成M,所以一定有Fe-O键的生成和断裂,选项C正确;
D.图示为一个二氧化碳分子反应过程,能量变化为-11.63eV,所以当有1mol二氧化
碳反应能量变化为-11.63eV×1.6×10-19J/eV×6.02×1023=1.12×106J=1120kJ,则该过程的热
化学方程式为:M(s)+CO (g)=N(s)ΔH=-1120kJmol-1,选项D错误;
2
答案选C。 ⋅
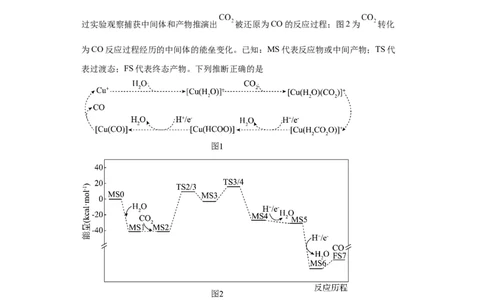
5.在 催化剂和水存在下, 被还原为CO的反应机理示意图如下:图1为通
过实验观察捕获中间体和产物推演出 被还原为CO的反应过程;图2为 转化
为CO反应过程经历的中间体的能垒变化。已知:MS代表反应物或中间产物;TS代
表过渡态;FS代表终态产物。下列推断正确的是
A.由图1可知, 能提高总反应的平衡转化率
B.图1中, 中存在非极性键
C.由图2知,各步反应的 都小于0
D.在图2涉及的反应中, 决定总反应速率
【答案】D
【详解】A.由图1可知, 为催化剂,催化剂不影响平衡,不能提高总反应的平
资料收集整理【淘宝店铺:向阳百分百】衡转化率,A错误;
B. 中存在配位键和极性共价键,不含非极性键,B错误;
C.由图2知,MS →MS 为吸热反应,ΔH>0,C错误;
2 3
D.在多步反应体系中,反应速率最慢的反应决定了反应的总速率,活化能越高,反
应速率越慢,由图2知,MS →MS 活化能最大,反应速率最慢,决定了总反应速率,
2 3
D正确;
故选D。
6.利用计算机技术测得在甲、乙两种催化剂作用下由正丁烷(g)制备1-丁烯(g)的反应
历程如下,其中甲、乙催化剂表面的物种均用*号标注,过渡态均用TS表示,下列说
法中错误的是
A.选用催化剂甲时的最高能垒(活化能 )为1.95eV
B.选用催化剂乙时,相对能量从 的过程为正丁烷的吸附过程
C. 为吸热反应
D.若只从平均反应速率快慢角度考虑,生产中适宜选用催化剂乙
【答案】A
【详解】A.过渡态物质的总能量与反应物总能量的差值为活化能,由图可知,选用
催化剂甲时的最高能垒(活化能 )为选用催化剂甲时的最高能垒(活化能 )为
1.29eV,A项错误;
B.由图可知,选用催化剂乙时,相对能量从 的过程为正丁烷的在催
化剂表面的吸附过程,B项正确;
C.生成物能量高于反应物的能量,则 为吸热反应,C项
正确;
资料收集整理【淘宝店铺:向阳百分百】D.活化能越小反应越快,活化能越大反应越慢,若只从平均反应速率快慢角度考虑,
生产中适宜选用催化剂乙,其反应历程中活化能较小,D项正确。
故选A。
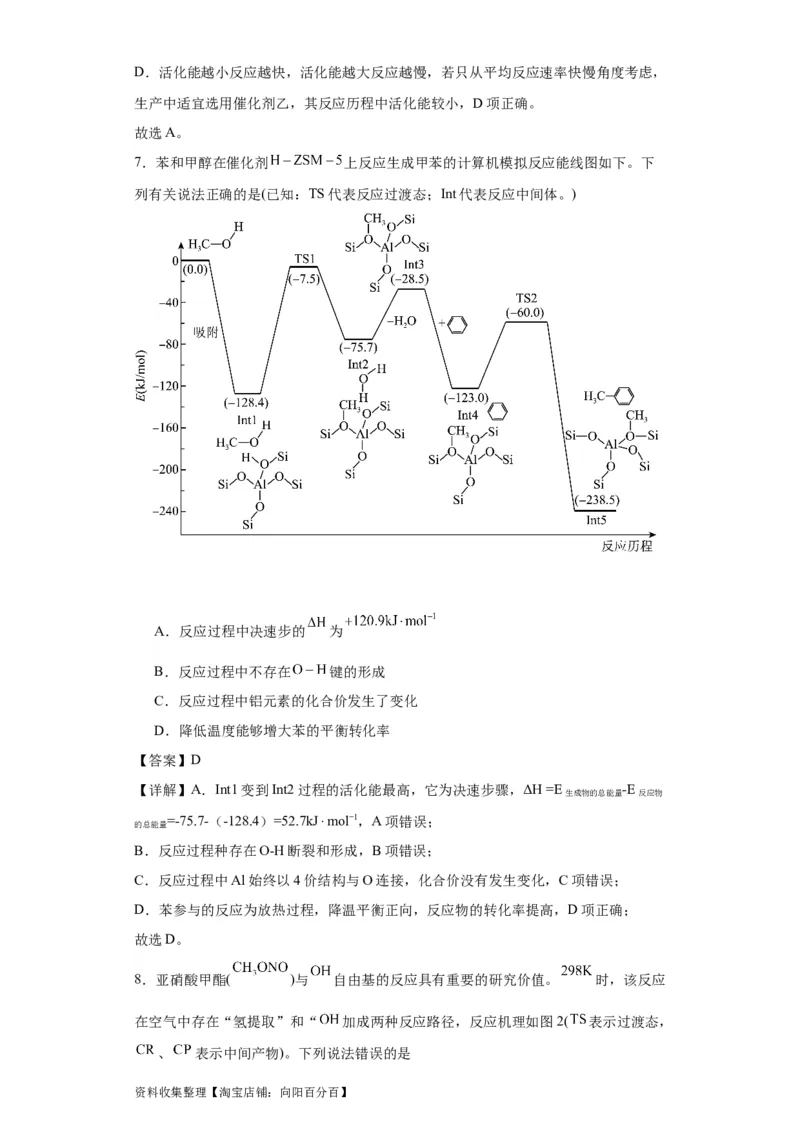
7.苯和甲醇在催化剂 上反应生成甲苯的计算机模拟反应能线图如下。下
列有关说法正确的是(已知:TS代表反应过渡态;Int代表反应中间体。)
A.反应过程中决速步的 为
B.反应过程中不存在 键的形成
C.反应过程中铝元素的化合价发生了变化
D.降低温度能够增大苯的平衡转化率
【答案】D
【详解】A.Int1变到Int2过程的活化能最高,它为决速步骤,ΔH =E -E
生成物的总能量 反应物
=-75.7-(-128.4)=52.7kJ⋅mol−1,A项错误;
的总能量
B.反应过程种存在O-H断裂和形成,B项错误;
C.反应过程中Al始终以4价结构与O连接,化合价没有发生变化,C项错误;
D.苯参与的反应为放热过程,降温平衡正向,反应物的转化率提高,D项正确;
故选D。
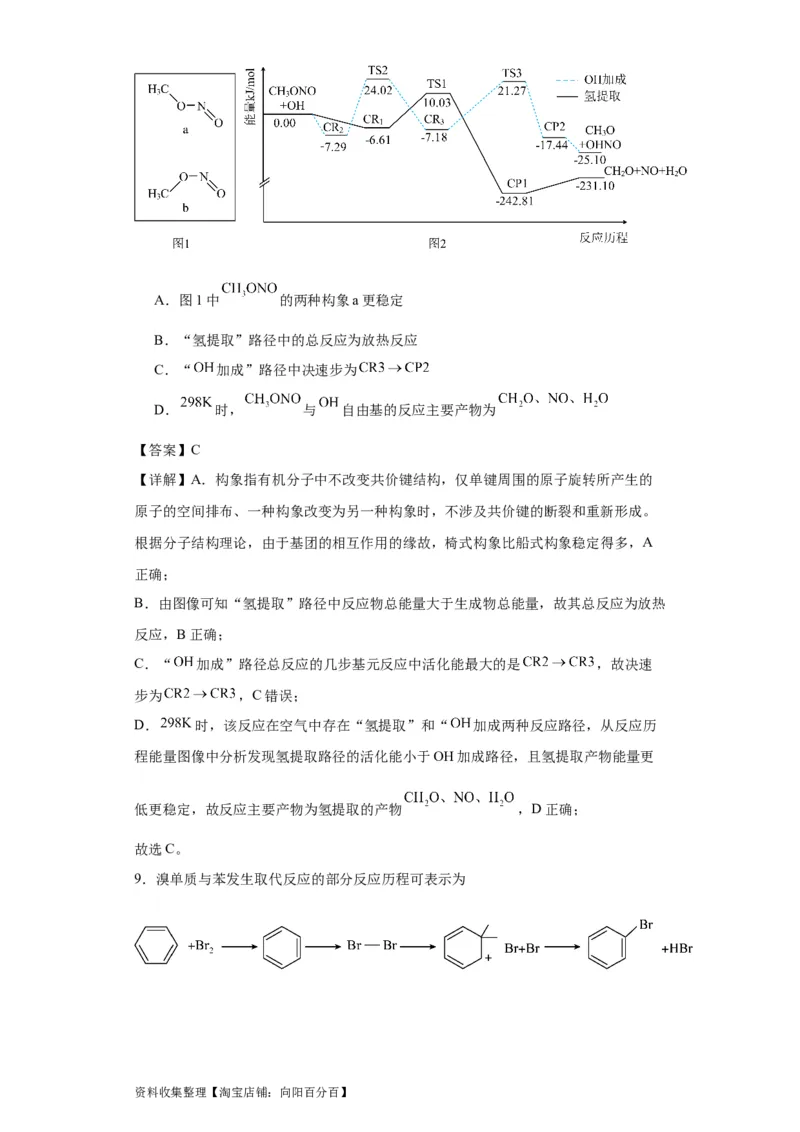
8.亚硝酸甲酯( )与 自由基的反应具有重要的研究价值。 时,该反应
在空气中存在“氢提取”和“ 加成两种反应路径,反应机理如图2( 表示过渡态,
、 表示中间产物)。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.图1中 的两种构象a更稳定
B.“氢提取”路径中的总反应为放热反应
C.“ 加成”路径中决速步为
D. 时, 与 自由基的反应主要产物为
【答案】C
【详解】A.构象指有机分子中不改变共价键结构,仅单键周围的原子旋转所产生的
原子的空间排布、一种构象改变为另一种构象时,不涉及共价键的断裂和重新形成。
根据分子结构理论,由于基团的相互作用的缘故,椅式构象比船式构象稳定得多,A
正确;
B.由图像可知“氢提取”路径中反应物总能量大于生成物总能量,故其总反应为放热
反应,B正确;
C.“ 加成”路径总反应的几步基元反应中活化能最大的是 ,故决速
步为 ,C错误;
D. 时,该反应在空气中存在“氢提取”和“ 加成两种反应路径,从反应历
程能量图像中分析发现氢提取路径的活化能小于OH加成路径,且氢提取产物能量更
低更稳定,故反应主要产物为氢提取的产物 ,D正确;
故选C。
9.溴单质与苯发生取代反应的部分反应历程可表示为
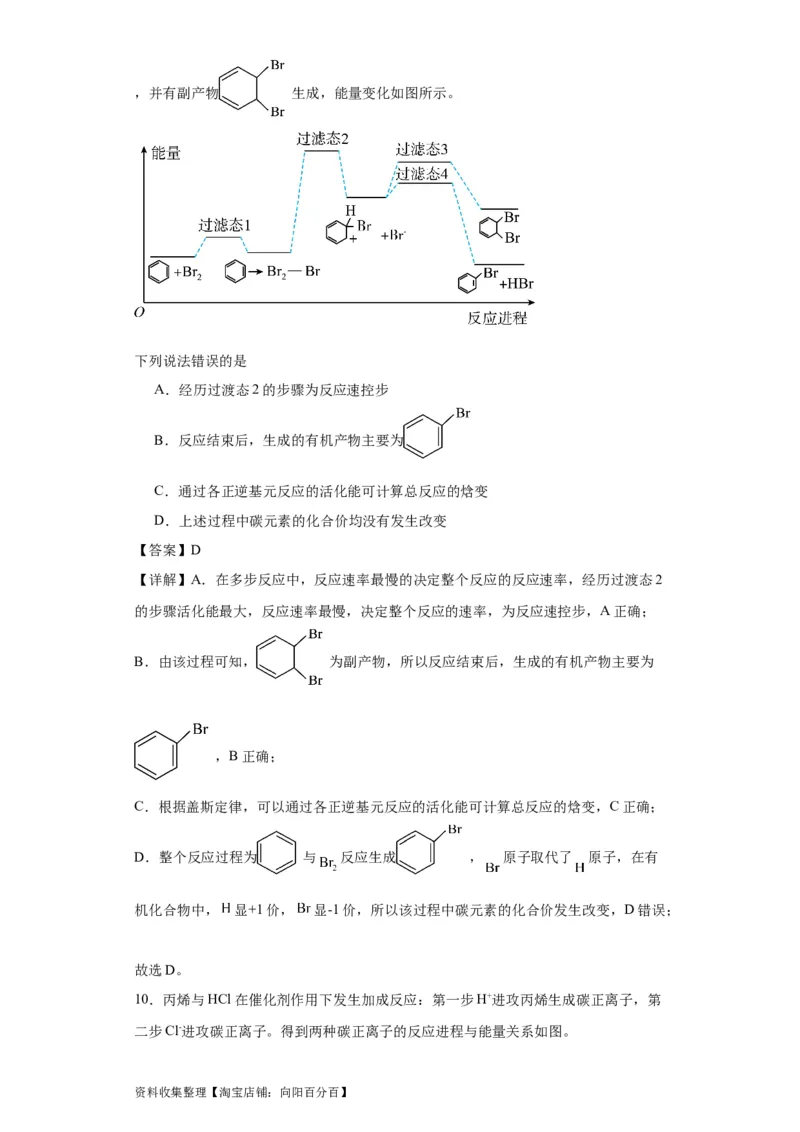
资料收集整理【淘宝店铺:向阳百分百】,并有副产物 生成,能量变化如图所示。
下列说法错误的是
A.经历过渡态2的步骤为反应速控步
B.反应结束后,生成的有机产物主要为
C.通过各正逆基元反应的活化能可计算总反应的焓变
D.上述过程中碳元素的化合价均没有发生改变
【答案】D
【详解】A.在多步反应中,反应速率最慢的决定整个反应的反应速率,经历过渡态2
的步骤活化能最大,反应速率最慢,决定整个反应的速率,为反应速控步,A正确;
B.由该过程可知, 为副产物,所以反应结束后,生成的有机产物主要为
,B正确;
C.根据盖斯定律,可以通过各正逆基元反应的活化能可计算总反应的焓变,C正确;
D.整个反应过程为 与 反应生成 , 原子取代了 原子,在有
机化合物中, 显+1价, 显-1价,所以该过程中碳元素的化合价发生改变,D错误;
故选D。
10.丙烯与HCl在催化剂作用下发生加成反应:第一步H+进攻丙烯生成碳正离子,第
二步Cl-进攻碳正离子。得到两种碳正离子的反应进程与能量关系如图。
资料收集整理【淘宝店铺:向阳百分百】下列说法不正确的是
A.催化剂可以使生成①过程的活化能降低
B.过渡态(Ⅰ)比过渡态(Ⅱ)稳定
C.生成①的过程所需的活化能较高,速率慢
D.丙烯与HCl加成反应主要生成
【答案】B
【详解】A.催化剂可以改变反应历程降低反应所需要的活化能,加快反应速率,故
催化剂可以使生成①过程的活化能降低,A正确;
B.由题干图像可知,过渡态(Ⅱ)能量较低,则比过渡态(Ⅰ)稳定,B错误;
C.由题干图像可知,生成①的过程所需的活化能较高,活化能越高,反应速率越慢,
C正确;
D.活化能越低,反应越易进行,可知丙烯与HCl发生加成反应,主要生成产物
CHCHClCH ,D正确;
3 3
故答案为:B。
11.某反应可有效降低汽车尾气污染物的排放,其反应热 kJ⋅mol-1。一定
条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态)。下列说法
错误的是
A.该化学反应的速率主要由反应②决定
B.三个基元反应中反应②和反应③是放热反应
资料收集整理【淘宝店铺:向阳百分百】C. kJ⋅mol
D.该过程的总反应为2NO+2CO=2CO +N
2 2
【答案】A
【分析】从图中可得出三个热化学方程式:
反应①:2NO=N O △H=+199.2kJ∙mol-1;
2 2 1
反应②:NO+CO=CO +N O △H=-513.5kJ∙mol-1;
2 2 2 2 2
反应③:CO+N O+CO=2CO+N △H=-(∆E-248.3)kJ∙mol-1。
2 2 2 2 3
【详解】A.正反应活化能最小的是反应②,活化能越大反应速率越慢,整个反应由
最慢的一步决定,A错误;
B.由图可知,三个基元反应中,反应②和反应③的反应物总能量大于生成物的总能量,
属于放热反应,B正确;
C.利用盖斯定律,将反应①+②+③得,2NO+2CO=2CO +N △H=+199.2kJ∙mol-1+
2 2
(-513.5kJ∙mol-1)+[ -(∆E-248.3)kJ∙mol-1]= -620.9kJ∙mol-1,则
kJ⋅mol-1,C正确;
D.由C选项中利用盖斯定律所得出的结论,可确定该过程的总反应为
2NO+2CO=2CO +N ,D正确;
2 2
故选A。
12.叔丁基溴在乙醇中反应的能量变化如图所示:
反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)COC H+HBr
2 5 3 3 3 3 2 5
下列说法不正确的是
A.过渡态能量:①>②>③
B.(CH)COC H 可以逆向转化为(CH)CBr,但不会转化为(CH)C=CH
3 3 2 5 3 3 3 2 2
C.若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值增大
4 3
D.向(CH)CBr的乙醇溶液中加入NaOH并适当升温,可以得到较多的
3 3
(CH)C=CH
3 2 2
资料收集整理【淘宝店铺:向阳百分百】【答案】B
【详解】A.由图可知,过渡态能量的大小顺序为①>②>③,故A正确;
B.(CH)COC H 与HBr在一定条件下可以逆向转化为(CH)CBr,即为(CH)CBr和
3 3 2 5 3 3 3 3
C HOH转化为(CH)COC H 的逆过程,该过程需要先转化为(CH)C+Br-和C HOH,
2 5 3 3 2 5 3 3 2 5
(CH)C+Br-和C HOH再转化为(CH)CBr和C HOH,但(CH)C+Br-和C HOH同时也
3 3 2 5 3 3 2 5 3 3 2 5
能转化为(CH)C=CH ,故B错误;
3 2 2
C.氯元素的电负性大于溴元素,则叔丁基氯的能量低于叔丁基溴,(CH)C+Cl-的能量
3 3
高于(CH)C+Br-,所以若将上述反应体系中的叔丁基溴改为叔丁基氯,则E—E 的值
3 3 4 3
增大,故C正确;
D.由图可知,(CH)CBr的乙醇溶液生成(CH)C=CH 过程放出能量相较于生成
3 3 3 2 2
(CH)COC H 低,加入氢氧化钠能与HBr反应使得平衡正向移动,适当升温会使平衡
3 3 2 5
逆向移动,放热越小的反应逆向移动程度更小,因此可以得到较多的(CH)C=CH ,故
3 2 2
D正确;
故选B。
13.我国科学家合成了一种新型Au /MoC材料,实现了低温催化水煤气变换。反应历
15
程如图所示,其中吸附在催化剂表面的物种用“*”标注,TS指过渡态。下列有关说法
不正确的是
A.温度一定时,加压无法提高平衡转化率
B.分子从催化剂表面脱附的过程都是吸热的
C.反应历程中活化能最大的一步为CO*+2HO*→CO*+H O*+OH*+H*
2 2
D.该过程有极性键的断裂和生成
【答案】B
【详解】A.该反应为CO(g)+HO(g) CO(g)+H(g),该反应为等体积反应,
2 2 2
温度一定时加压化学平衡不移动,平衡转化率不变,A正确;
B.从图中可知并不是所有分子从催化剂表面脱附的过程都是吸热的,如
资料收集整理【淘宝店铺:向阳百分百】CO*+H O*+2H*转化为CO+H O*+2H*的过程就是放热的,B错误;
2 2 2 2
C.从图中可知,过渡态TS1的相对能量最大,此时的活化能最大,因此反应历程中
活化能最大的一步为CO*+2HO*→CO*+H O*+OH*+H*,C正确;
2 2
D.该过程中HO中的O-H键断裂,同时也有CO 中C=O键的生成,D正确;
2 2
故答案选B。
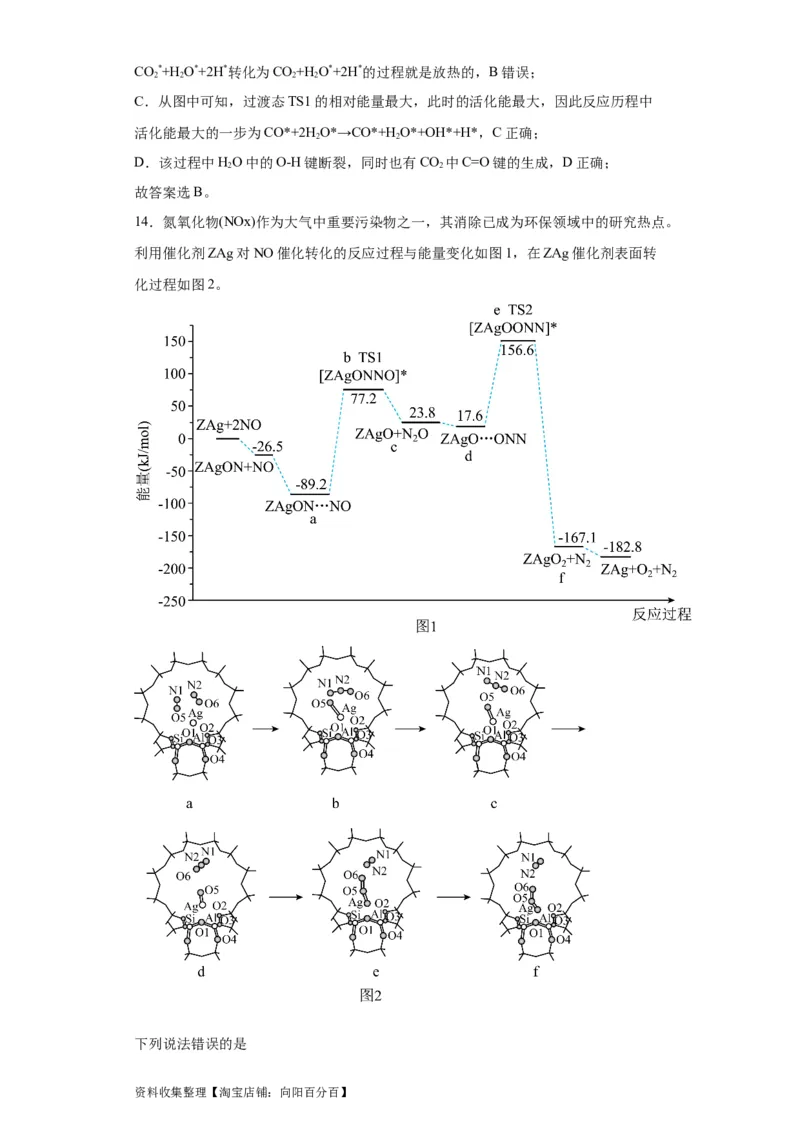
14.氮氧化物(NOx)作为大气中重要污染物之一,其消除已成为环保领域中的研究热点。
利用催化剂ZAg对NO催化转化的反应过程与能量变化如图1,在ZAg催化剂表面转
化过程如图2。
下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.低温下有利于反应过程中NO的转化 B.由a释放 的过程为控速步骤
C.a到b、d到e,都有非极性共价键的生成 D.过渡态d比a稳定
【答案】D
【分析】由图可知,该反应为放热反应。由a到b的能垒为166.4kJ/mol,高于d到e的
能垒139kJ/mol,为反应的决速步骤。
【详解】A.此转化过程为放热反应,降低温度有利于反应正向进行,A正确;
B.由a到b的能垒为166.4kJ/mol,高于由d到e的能垒139kJ/mol,所以由a释放
的过程为控速步骤,B正确;
C.由a到b有氮氮键生成,由d到e有氧氧键生成,都为非极性共价键的生成,C正
确;
D.过渡态d的能量比a的能量高,则d不稳定,D错误;
故选D。
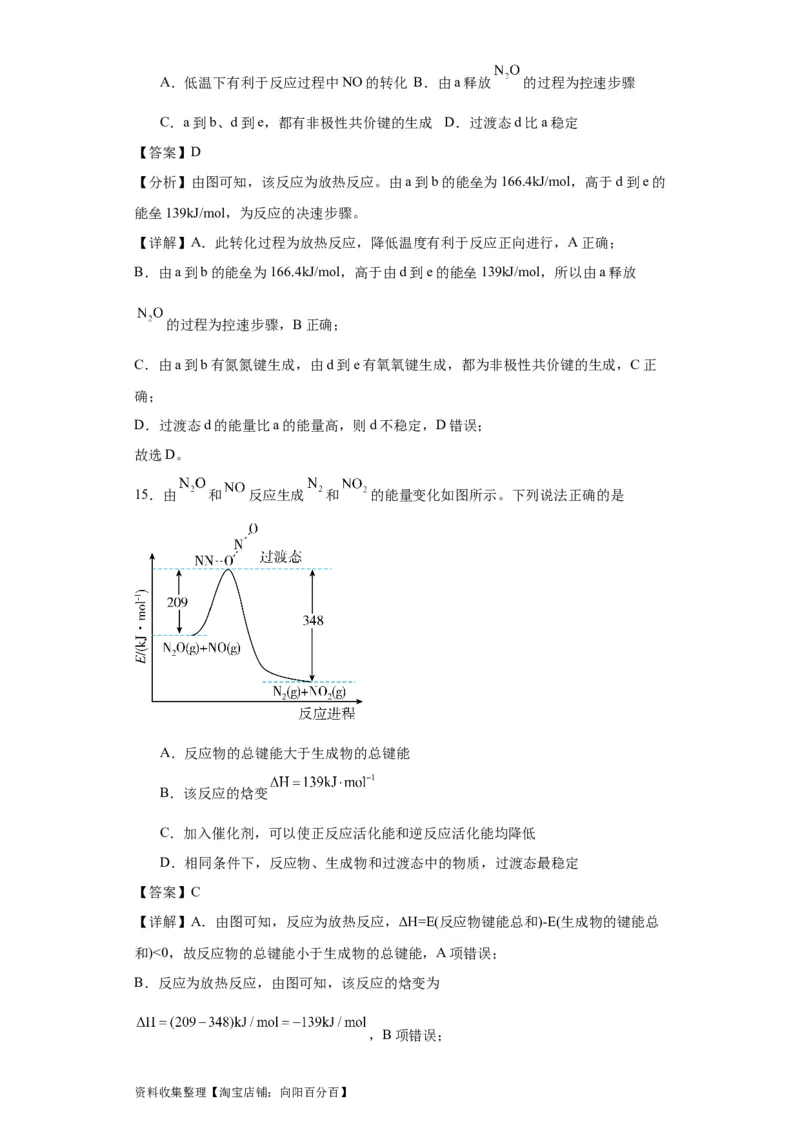
15.由 和 反应生成 和 的能量变化如图所示。下列说法正确的是
A.反应物的总键能大于生成物的总键能
B.该反应的焓变
C.加入催化剂,可以使正反应活化能和逆反应活化能均降低
D.相同条件下,反应物、生成物和过渡态中的物质,过渡态最稳定
【答案】C
【详解】A.由图可知,反应为放热反应,ΔH=E(反应物键能总和)-E(生成物的键能总
和)<0,故反应物的总键能小于生成物的总键能,A项错误;
B.反应为放热反应,由图可知,该反应的焓变为
,B项错误;
资料收集整理【淘宝店铺:向阳百分百】C.加入催化剂改变反应速率但不改变反应焓变,可以使正反应活化能和逆反应活化能
均降低,但两者的差值不变,C项正确;
D.相同条件下,反应物、生成物和过渡态中的物质,过渡态所处能量最高、最不稳
定,D项错误;
故选C。
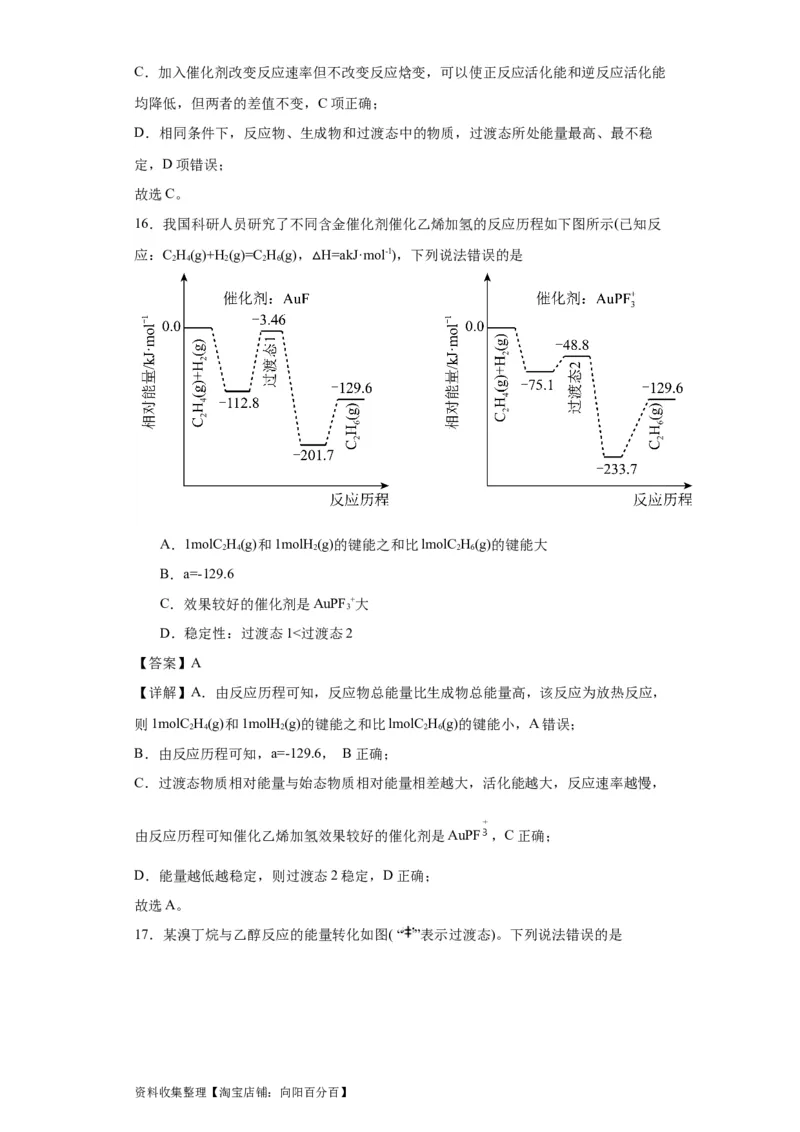
16.我国科研人员研究了不同含金催化剂催化乙烯加氢的反应历程如下图所示(已知反
应:C H(g)+H(g)=C H(g), H=akJ·mol-1),下列说法错误的是
2 4 2 2 6
△
A.1molC H(g)和1molH (g)的键能之和比lmolC H(g)的键能大
2 4 2 2 6
B.a=-129.6
C.效果较好的催化剂是AuPF +大
3
D.稳定性:过渡态1<过渡态2
【答案】A
【详解】A.由反应历程可知,反应物总能量比生成物总能量高,该反应为放热反应,
则1molC H(g)和1molH (g)的键能之和比lmolC H(g)的键能小,A错误;
2 4 2 2 6
B.由反应历程可知,a=-129.6, B正确;
C.过渡态物质相对能量与始态物质相对能量相差越大,活化能越大,反应速率越慢,
由反应历程可知催化乙烯加氢效果较好的催化剂是AuPF ,C正确;
D.能量越低越稳定,则过渡态2稳定,D正确;
故选A。
17.某溴丁烷与乙醇反应的能量转化如图( “ ”表示过渡态)。下列说法错误的是
资料收集整理【淘宝店铺:向阳百分百】A.总反应为取代反应 B.该反应过程中C原子杂化方式有变化
C.加 可以加快该反应的反应速率 D.该过程正逆反应的决速步骤不
同
【答案】C
【详解】A.该溴丁烷与乙醇反应的总反应为
(CH)CBr+CH CHOH→(CH)COCH CH+HBr,此反应类型为取代反应,A正确;
3 3 3 2 3 3 2 3
B.(CH)CBr、CHCHOH中C原子的杂化方式为sp3杂化,(CH)C+碳原子杂化方式
3 3 3 2 3 3
为sp2杂化,B正确;
C.反应物为(CH)CBr与CHCHOH,加入C HONa,对反应物浓度与反应过程中的
3 3 3 2 2 5
过渡态无任何影响,故不能影响反应速率,C错误;
D.正逆反应的决速步骤由反应速率慢的步骤决定,故该过程正逆反应的决速步骤不
同,D正确;
故选C。
18.科学研究人员结合实验与计算机模拟结果,研究了在Pt/SiO 催化剂表面上CO 与
2 2
H 的反应历程,前三步历程如图所示。其中吸附在Pt/SiO 催化剂表面上的物种用
2 2
“•”标注,Ts表示过渡态。下列有关叙述不正确的是
A.•HOCO转化为•CO和•OH为放热过程
B.形成过渡态Ts1的活化能(能垒)为1.15eV
C.前三步总反应的△H<0,总反应的化学反应速率由第一步反应决定
D.历程中活化能最小的反应方程式•CO+•OH+•H+3H(g)=•CO+3H(g)+
2 2
资料收集整理【淘宝店铺:向阳百分百】HO(g)
2
【答案】B
【详解】A.根据图中信息•HOCO转化为•CO和•OH,反应物总能量高于生成物总能
量,因此该过程为放热过程,故A正确;
B.根据Ts1生成的•HOCO,其能量为0.15eV,形成过渡态Ts1的活化能(能垒)为
0.15eV−(−0.9eV)=1.05eV,故B错误;
C.根据前三步总反应分析,反应物总能量大于生成物总能量,因此总反应为放热反应
即△H<0,由于第一步的活化能最大,因此总反应的化学反应速率由第一步反应决定,
故C正确;
D.第三步的活化能最小即历程中活化能最小的反应方程式•CO+•OH+•H+
3H(g)=•CO+3H(g)+HO(g),故D正确。
2 2 2
综上所述,答案为B。
19.乙烯氢化的热化学方程式为C H(g) + H(g) = C H(g) H= akJ·mol-1,使用不同含
2 4 2 2 6
Au催化剂的反应历程如图所示,下列说法正确的是 △
A.1 mol C H(g)的能量大于 1 mol C H(g)与1 mol H (g)具有的能量之和
2 6 2 4 2
B.该反应的焓变: H = -129.6 kJ·mol-1
C.过渡态物质的稳△定性:过渡态1大于过渡态2
D.相应的活化能:催化剂AuF小于催化剂AuPF
【答案】B
【详解】A.由图可知,该反应为放热反应,故1 mol C H(g)的能量小于 1 mol
2 6
C H(g)与1 mol H (g)具有的能量之和,A错误;
2 4 2
B.由图可知C H(g)+H(g)=C H(g) H=生成物能量-反应物能量=-129.6kJ/mol
2 4 2 2 6
-0=-129.6 kJ/mol,B正确; △
C.由图可知,过渡态1的能量大于过渡态2的能量,能量越低越温度,则稳定性:过
渡态1<过渡态2,C错误;;
资料收集整理【淘宝店铺:向阳百分百】D.由图可知,催化剂AuF、催化剂AuPF 的活化能分别为109.34 kJ·mol-1、26.3
kJ·mol-1,则催化剂AuF的活化能大于催化剂AuPF ,D错误;
故选B。
20.如图分别代表溴甲烷和三级溴丁烷发生水解的反应历程。下列说法不正确的是
Ⅰ:
Ⅱ:
A.反应Ⅰ的
B.反应Ⅱ有两个过渡态
C.增加氢氧化钠的浓度并不能使反应Ⅰ和Ⅱ速率都增大
D.反应Ⅰ和Ⅱ都有C-Br键的断裂和C-O键的形成,且生成的两种醇均可被催化
氧化产生C=O键
【答案】D
【详解】A.由题图知,反应Ⅰ中反应物的总能量比生成物的总能量大,所以反应Ⅰ
为放热反应,,A正确;
B.反应Ⅱ有两个过渡态,分别为 和 ,B正确;
C.反应Ⅰ只有1个过渡态,增大反应物浓度,反应Ⅰ的速率加快,对于反应Ⅱ,第一
步反应的活化能比第二步大,所以第一步反应为决速反应,而 只参与第二步反应,
所以增加NaOH浓度,并不能改变反应Ⅱ的速率,C正确;
D. 的羟基碳原子上没有氢原子,不能发生催化氧化,D错误;
故选D。
资料收集整理【淘宝店铺:向阳百分百】