文档内容
专项训练 速率常数的运用(解析版)
一、单选题
1.已知 的速率方程为 (k为速率常数,只与
温度、催化剂有关)。实验测得, 在催化剂X表面反应的变化数据如下:
6
t/min 0 10 20 30 40 50 70
0
0.100 0.080 0.040 0.020 0
下列说法正确的是
A. ,
B. min时,
C.相同条件下,增大 的浓度或催化剂X的表面积,都能加快反应速率
D.保持其他条件不变,若 起始浓度为0.200 mol·L ,当浓度减至一半时共耗
时50 min
【答案】D
【分析】根据表中数据分析,该反应的速率始终不变, 的消耗是匀速的,说明反
应速率与 无关,故速率方程中n=0;
【详解】A.由分析可知,n=0,与 浓度无关,为匀速反应,每10min一氧化二氮
浓度减小0.02 ,则 ,A错误;
B.由分析可知,n=0,与 浓度无关,为匀速反应,t=10min时瞬时速率等于平均
速率 = = ≠ ,B错
误;
资料收集整理【淘宝店铺:向阳百分百】C.速率方程中n=0,反应速率与 的浓度无关,C错误;
D.保持其他条件不变,该反应的反应速率不变,即为 ,若起始
浓度 ,减至一半时所耗时间为 =50min,D正确;
答案选D。
2.室温下,某溶液初始时仅溶有M和N且物质的量浓度相等,同时发生以下两个反
应:① ;② ,反应①的速率可表示为 ,反
应②的速率可表示为 ( 为速率常数)。反应体系中组分 的浓度
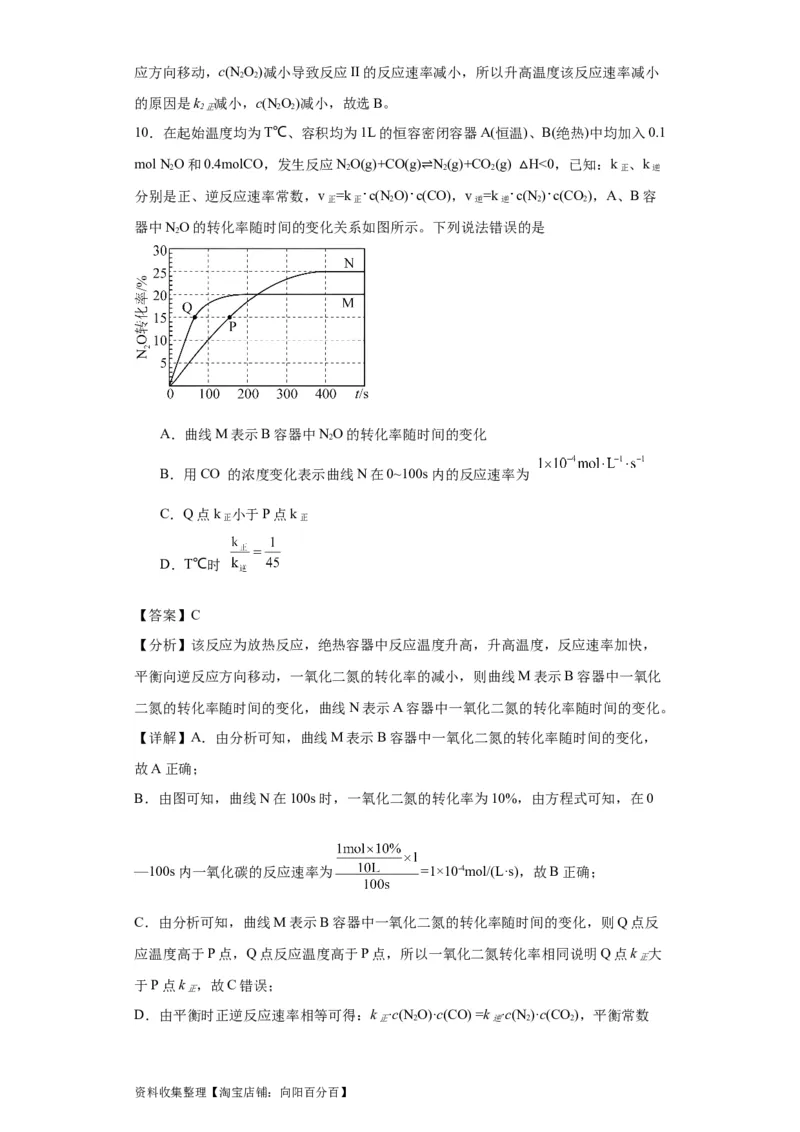
(浓度单位: )随时间(时间单位: )变化情况如图。下列说法不正确的是
A. 时间段内, 的平均反应速率为
B.反应开始后,体系中 和 的浓度之比保持不变
C.
D.如果反应能进行到底,反应结束时 的M转化为
【答案】D
【分析】反应初始时,c(M)=0.5mol L-1,c(Z)=0,反应进程中,c(M)逐渐减小,c(Z)逐
渐增大,反应进行到30min时,c(M)= 0.03mol L-1,c(Z)= 0.125mol L-1
【详解】A.根据图示可知, 时间段内,有如下关系:
资料收集整理【淘宝店铺:向阳百分百】v(Y)= ,故A错误;
B.相同时间内, 和 的浓度之比等于两者平均反应速率之比,因 和 分别是反应
①和反应②的产物,故两者的浓度= = 为定值,故B错误;
C. ,故C错误;
D.反应体系中生成物Y和Z的浓度之比为0.075:0.125=3:5,保持不变,M在反应①、
②中按3:5进行反应,当0.5mol/LM完全反应时,转化Z的M所占的比例为
,故D正确。
答案为D。
3.1,2-二甲基环丙烷的顺反异构体可相互转化: (顺式) (反
式) ,该反应的速率方程为: (顺)和 (反), 和 分别为正、
逆反应速率常数。 ℃时,加入顺式异构体发生反应,两种异构体的质量分数w随时
间t的变化如图所示。下列说法正确的是
A.反应速率: (正) (逆)
B.L点:转化率为50%,Q(浓度商)>K
C.升高温度, 、 增大倍数:
资料收集整理【淘宝店铺:向阳百分百】D. ℃时发生反应,测得 ,则
【答案】C
【详解】A.M和N点反应未达到平衡,则 (正) (逆), (正) (逆),反应过
程中v(正)不断减小,则 (正)> (正),则 (正) (逆),故A错误;
B.L点时,顺1,2-二甲基环丙烷和逆1,2-二甲基环丙烷的质量分数相等,由方程式
(顺式) (反式)可知,此时顺1,2-二甲基环丙烷转化了一半,
转化率为50%,此时反应未达到平衡,平衡正向进行,Q(浓度商)0,为吸热反应,升高温度,K值增大,A正确;
B.由上述分析可知,Ⅰ中NO 的平衡转化率为 ×100%≈66.7%,B正确;
2
C.Ⅰ中平衡时c(O)=0.2 mol·L−1,实验Ⅱ相当于在Ⅰ的基础上再加入NO,平衡会逆
2
向移动,c(O)<0.2 mol·L−1,C正确;
2
D.升高温度,正逆反应速率均加快,反应的 、 均增大,D错误;
故选:D。
8.阿伦尼乌斯经验公式为lnk=lnA (E 为活化能,k为速率常数,R和A为常数),
a
资料收集整理【淘宝店铺:向阳百分百】已知反应 (l) (l),其lnk 和lnk 随温度变化的曲线如图所
正 逆
⇌
示。下列有关该反应的说法不正确的是
A.正反应的活化能大于逆反应的活化能
B.完全燃烧等质量的M(l)、N(l),N(l)放出的热量多
C.选用合适的催化剂能提高 的平衡转化率
D.温度变化对速率常数的影响程度:lnk >lnk
正 逆
【答案】C
【详解】A.根据阿伦尼乌斯经验公式lnk=lnA-EaRT(Ea为活化能)可知,题图中曲线
的斜率代表活化能大小,lnk 的斜率大,活化能大,A正确;
正
B.正反应的活化能大于逆反应的活化能,则该反应为吸热反应,生成物N的能量更
高,完全燃烧等质量的M(l)、N(l),N(l)放出的热量更多,B正确;
C.催化剂只影响化学反应速率,不影响化学平衡,不能改变平衡转化率,C错误;
D.lnk 的斜率大,正反应的活化能大,温度变化对k 的影响程度大于对k 的影响
正 正 逆
程度,D正确;
故选:C。
9.已知升高温度时,速率常数(k)总是增大,因此绝大多数的化学反应速率增大。但是
2NO(g)+O (g) 2NO (g)的速率却随着温度升高而减小,已知该反应历程分两步:
2 2
I.2NO(g) N O⇌(g)(快)ΔH<0,v =k c2(NO)、v =k c(NO);
2 2 1 1正 1正 1逆 1逆 2 2
II.N
2
O
2
(g )+⇌O
2
(g) 2NO
2
(g)(慢) ΔH
2
<0,v
2正
=k
2正
c(N
2
O
2
)c(O
2
)、v
2逆
=k
2逆
c2(NO
2
),试分
析升高温度该反应⇌速率减小的原因是
A.k 增大,c(N O)增大 B.k 减小,c(N O)减小
2正 2 2 2正 2 2
C.k 增大,c(N O)减小 D.k 减小,c(N O)增大
2正 2 2 2正 2 2
【答案】B
【详解】化学反应速率的快慢取决于慢反应,反应II为慢反应,则升高温度,反应速
率减小说明v 减小,所以k 减小;反应I为放热的快反应,升高温度,平衡向逆反
2正 2正
资料收集整理【淘宝店铺:向阳百分百】应方向移动,c(N O)减小导致反应II的反应速率减小,所以升高温度该反应速率减小
2 2
的原因是k 减小,c(N O)减小,故选B。
2正 2 2
10.在起始温度均为T℃、容积均为1L的恒容密闭容器A(恒温)、B(绝热)中均加入0.1
mol NO和0.4molCO,发生反应NO(g)+CO(g) N(g)+CO (g) H<0,已知:k 、k
2 2 2 2 正 逆
分别是正、逆反应速率常数,v =k c(NO) c⇌(CO),v =k c△(N) c(CO),A、B容
正 正 2 逆 逆 2 2
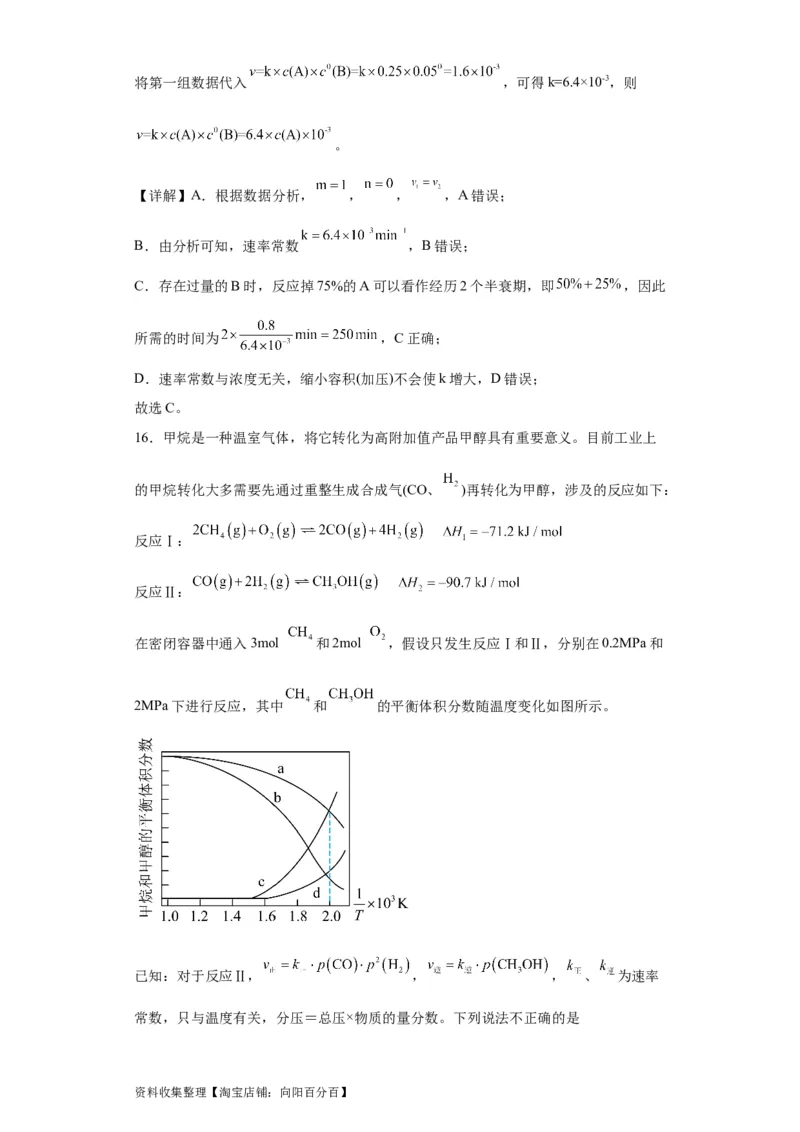
器中NO的转化率随时间的变化关系如图所示。下列说法错误的是
2
A.曲线M表示B容器中NO的转化率随时间的变化
2
B.用CO 的浓度变化表示曲线N在0~100s内的反应速率为
C.Q点k 小于P点k
正 正
D.T℃时
【答案】C
【分析】该反应为放热反应,绝热容器中反应温度升高,升高温度,反应速率加快,
平衡向逆反应方向移动,一氧化二氮的转化率的减小,则曲线M表示B容器中一氧化
二氮的转化率随时间的变化,曲线N表示A容器中一氧化二氮的转化率随时间的变化。
【详解】A.由分析可知,曲线M表示B容器中一氧化二氮的转化率随时间的变化,
故A正确;
B.由图可知,曲线N在100s时,一氧化二氮的转化率为10%,由方程式可知,在0
—100s内一氧化碳的反应速率为 =1×10-4mol/(L·s),故B正确;
C.由分析可知,曲线M表示B容器中一氧化二氮的转化率随时间的变化,则Q点反
应温度高于P点,Q点反应温度高于P点,所以一氧化二氮转化率相同说明Q点k 大
正
于P点k ,故C错误;
正
D.由平衡时正逆反应速率相等可得:k ·c(N O)·c(CO) =k ·c(N )·c(CO),平衡常数
正 2 逆 2 2
资料收集整理【淘宝店铺:向阳百分百】K= = ,由图可知,T℃条件下,容器A平衡时一氧化二氮的转化率
为25%,则平衡时一氧化氮、一氧化碳、二氧化碳、氮气的浓度分别为
=0.075mol/L、 =0.375mol/L、
=0.025mol/L、 =0.025mol/L,反应的平衡常数K= =
= ,故D正确;
故选C。
11.某温度下,在金表面发生反应: ,其速率方程式为
(k为速率常数)。反应过程中, 与S(催化剂)及时间关系如图所示。
已知 (半衰期)为反应物消耗一半所用的时间,下列叙述错误的是
A. ,Ⅰ条件下
B.其他条件相同,S(催化剂)越大,k越大
C.其他条件相同, 增大,反应速率不变
D.该温度下,当S(催化剂) , 时, 为
资料收集整理【淘宝店铺:向阳百分百】【答案】A
【详解】A.根据如所示,Ⅰ和Ⅲ条件相同,起始浓度不同,但反应速率相同,说明
反应速率与起始浓度无关,所以 , ,A错误;
B.对比Ⅰ、Ⅱ和Ⅲ,Ⅱ中S(催化剂)越大最大,反应速率越大,k越大,Ⅰ和Ⅲ的
S(催化剂)相同,反应速率相同,k相同,所以在其他条件相同,S(催化剂)越大,k越
大,B正确;
C.由以上分析, 与反应速率无关,C正确;
D.由图可知,在条件Ⅰ,S(催化剂) , 消耗一半
即小号 所用的时间为 ,所以半衰期为 ,D正确;
故选A。
12.在某催化剂作用下,乙炔选择性加成反应C H(g)+H(g) C H(g) ΔH<0。速率方
2 2 2 2 4
程为v =k c(C H)c(H),v =k c(C H)(k 、k 为速率常数⇌,只与温度、催化剂有
正 正 2 2 2 逆 逆 2 4 正 逆
关)。一定温度下,在2L恒容密闭容器中充入1molC H(g)和1molH (g),只发生上述反
2 2 2
应。测得C H 的物质的量如下表所示:
2 4
t/min 0 5 10 15 20
n/mol 0 0.3 0.5 0.6 0.6
下列说法错误的是
A.0~10min内,v(H )=0.025mol・L-1・min-1
2
B.升高温度,k 增大的倍数小于k 增大的倍数
正 逆
C.净反应速率(v -v )由大到小最终等于0
正 逆
D.在上述条件下,15min时2k =15k
逆 正
【答案】D
【详解】A.由表可知,0~10 min内
,A正确;
B.根据平衡状态的特点,平衡时正、逆反应速率相等,则K= 。上述反应的正反
应是放热反应,升高温度,平衡常数减小,而升高温度,速率常数增大,由此推知,k
增大的倍数小于k 增大的倍数,B正确;
正 逆
C.根据表格数据可知,开始正反应速率最大,逆反应速率为0,随着反应进行,净反
资料收集整理【淘宝店铺:向阳百分百】应速率由大到小,最终等于0(平衡),C正确;
D.15 min时达到平衡,c(C H)=0.2 mol/L ,c(H)=0.2 mol/L ,c(C H)=0.3 mol/ L,故
2 2 2 2 4
K= =7.5,15k =2k ,D错误;
逆 正
答案选D。
13.室温下,气体M、N、P、Q之间存在如下转化关系:①M N+P;②M
N+Q,反应①的速率可表示为v=kc(M),反应②的速率可表示为v=kc(M)(k 、k 为
1 1 2 2 1 2
速率常数),在容积为10L的密闭容器中,反应体系中组分M、P的物质的量随时间的
变化如表所示:
时间(min) 0 1 2 3 4 5 6
M(mol) 1.00 0.76 0.56 0.40 0.36 0.36 0.36
P(mol) 0 0.06 0.11 0.15 0.16 0.16 0.16
下列说法正确的是
A.0~3min时间段内,Q的平均反应速率为0.15mol•L-1•min-1
B.反应①的活化能比反应②的活化能低
C.反应过程中P和Q的浓度之比逐渐减小
D.平衡时M生成Q的转化率为48%
【答案】D
【详解】A.由表格数据可知,0~3min时,M的物质的量变化量为0.60mol、P的物质
的量变化量为0.15mol,则反应生成的Q的物质的量为0.60mol—0.15mol=0.45mol,则
Q的平均反应速率为 ,故A错误;
B.由表格数据可知,4min反应达到平衡时,M的物质的量变化量为0.64mol、P的物
质的量变化量为0.16mol,则反应生成的Q的物质的量为0.64mol—0.16mol=0.48mol,
则反应①的反应速率慢于反应②,反应速率越快,活化能越小,则反应①的活化能比
反应②的活化能高,故B错误;
C.由化学反应速率定义可知,反应开始后,体系中P和Q的浓度变化量之比 c(P):
c(Q)=tv :tv =kc(M):kc(M)= k :k,k、k 为定值,所以反应开始后,体系△中P和
1 2 1 2 1 2 1 2
△Q的浓度之比保持不变,故C错误;
D.由表格数据可知,4min反应达到平衡时,M的物质的量变化量为0.64mol、P的物
质的量变化量为0.16mol,则反应生成的Q的物质的量为0.64mol—0.16mol=0.48mol,
资料收集整理【淘宝店铺:向阳百分百】M生成Q的转化率为 ×100%=48%,故D正确;
故选D。
14.乙酸甲酯催化醇解反应方程式为:
,已知
, ,其
中 、 为速率常数, 为物质的量分数。己醇和乙酸甲酯按物质的量之比1∶1投料,
测得348K、338K两个温度下乙酸甲酯转化率 随时间 的变化关系如图所示,下
列说法中错误的是
A.曲线①②中,曲线①对应的 更大
B.升高温度,该醇解平衡向正反应方向移动
C.a、b、c、d四点中, 与 差值最大的是b点
D.338K时,该反应的化学平衡常数为1
【答案】C
【分析】根据图像可知,①曲线的反应速率最快,说明温度高,即曲线①对应温度为
348K,曲线②对应温度为338K;
【详解】A.温度越高,反应速率越快, 值越大,根据分析以及图像可知,曲线①
对应的 更大,故A说法正确;
B.由图可知,温度越高,乙酸甲酯转化率越高,反应正向进行程度变大,说明反应为
吸热反应,故升高温度,该醇解平衡向正反应方向移动,故B说法正确;
资料收集整理【淘宝店铺:向阳百分百】C. 、 是温度的函数,该反应为吸热反应,升高温度,平衡向正反应方向进行,
受温度的影响较大,因此升高温度, 增大程度大于 ,即 - 的值最大的
是曲线①;据图像可知,a点是反应向正方向进行,c点为平衡点,随着反应进行,v
正
逐渐减小,v 逐渐增大,因此四点中, 与 差值最大的是a点,故C说法错误;
逆
D.338K时,令乙酸甲酯的物质的量为1mol,C H OH的物质的量为1mol,则达到平
6 13
衡时,消耗乙酸甲酯、C H OH的物质的量均为1mol×50%=0.5mol,则生成
6 13
CHCOOC H 和甲醇的物质的量为0.5mol,K= ,故D说法正确;
3 6 13
故选C。
15.反应 的速率方程为 (k为速率常数,
其中 ,A、R为常数, 为活化能,T为开氏温度),其半衰期
(反应物消耗一半所需的时间)为 。改变反应物浓度时,反应的瞬时速率如表所示。
下列说法正确的是
0.25 0.5 l 0.5 l
0.05 0.05 0.1 0.1 0.2
1.6 3.2 3.2
A.
B.
C.在过量的B存在时,A剩余25%所需的时间是
D.升温、加入催化剂,缩小容积(加压),均能使k增大,导致反应的瞬时速率加
快
【答案】C
【分析】由第二组和第四组数据,A浓度相同,B浓度不同,速率相等,可知n=0,再
由第一组和第二组数据代入 可得 ,可知m=1;
资料收集整理【淘宝店铺:向阳百分百】将第一组数据代入 ,可得k=6.4×10-3,则
。
【详解】A.根据数据分析, , , ,A错误;
B.由分析可知,速率常数 ,B错误;
C.存在过量的B时,反应掉75%的A可以看作经历2个半衰期,即 ,因此
所需的时间为 ,C正确;
D.速率常数与浓度无关,缩小容积(加压)不会使k增大,D错误;
故选C。
16.甲烷是一种温室气体,将它转化为高附加值产品甲醇具有重要意义。目前工业上
的甲烷转化大多需要先通过重整生成合成气(CO、 )再转化为甲醇,涉及的反应如下:
反应Ⅰ:
反应Ⅱ:
在密闭容器中通入3mol 和2mol ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和
2MPa下进行反应,其中 和 的平衡体积分数随温度变化如图所示。
已知:对于反应Ⅱ, , , 、 为速率
常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
资料收集整理【淘宝店铺:向阳百分百】A.压强为0.2MPa时,表示 和 的曲线分别是b、d
B.混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡
C.在升温的过程中,反应Ⅱ速率常数增大的倍数; >
D.500K,2MPa条件下,若平衡时CO的物质的量为1mol,则 的转化率约为
66.7%
【答案】C
【分析】2个反应均为放热反应,随着温度降低,平衡均正向移动,甲烷含量减小、
甲醇含量增加,故ab为甲烷变化曲线、cd为甲醇含量曲线;反应Ⅰ为气体分子数增大
的反应、反应Ⅱ为分子数减小的反应,相同条件下,增大压强,反应Ⅰ逆向移动、反
应Ⅱ正向移动,使得甲烷含量增加、甲醇含量增大,则bd为0.2Mpa变化曲线、ac为
2Mpa变化曲线;
【详解】A.由分析可知,压强为0.2MPa时,表示 和 的曲线分别是b、
d,A正确;
B.混合气体的平均相对分子质量M= m/n,气体质量不变,但是气体的总物质的量随
反应进行而改变,所以M会发生改变,当M不变时,反应达到平衡,B正确;
C.已知:对于反应Ⅱ, , ,当 时,
即达到化学平衡态,此时 ,因为反应是放热反应,升温 减小,所以升高
温度 变小,所以 增加的倍数更大,C错误;
D.在密闭容器中通入3mol 和2mol ,只发生反应Ⅰ和Ⅱ:
资料收集整理【淘宝店铺:向阳百分百】由图可知,平衡时,甲烷、甲醇量相等,则3-2a=2a-1,a=1mol, 的转化率约为
66.7%,D正确;
答案选C。
17.一氧化氮的氢化还原反应为
,其正反应速率方程为 ,k为速率常数,只受温
度影响。T℃时,实验得到的数据如下表所示:
实验组 NO起始浓度/( 起始浓度/( 起始的正反应速率/(
别 ) ) )
I
II
III
下列说法正确的是
A.平衡常数
B. ,
C.升高温度,k值减小
D.升高温度,该反应的平衡常数K值增大
【答案】B
【详解】A.I组和II组温度相同,故平衡常数一定相同,A错误;
B.II组NO的浓度是I组的2倍,但正反应速率是其4倍,故 ;III组H 的浓度是
2
I组的2倍,正反应速率是其2倍,故 ,B正确;
C.k为速率常数,升高温度反应速率增大,k值增大,C错误;
D.该反应为放热反应,升高温度,该反应的平衡常数K值减小,D错误;
故选B。
18.在起始温度均为T℃、容积均为10L的密闭容器A(恒温)、B(绝热)中均加入
和4molCO,发生反应 。已知:
、 分别是正、逆反应速率常数, ,
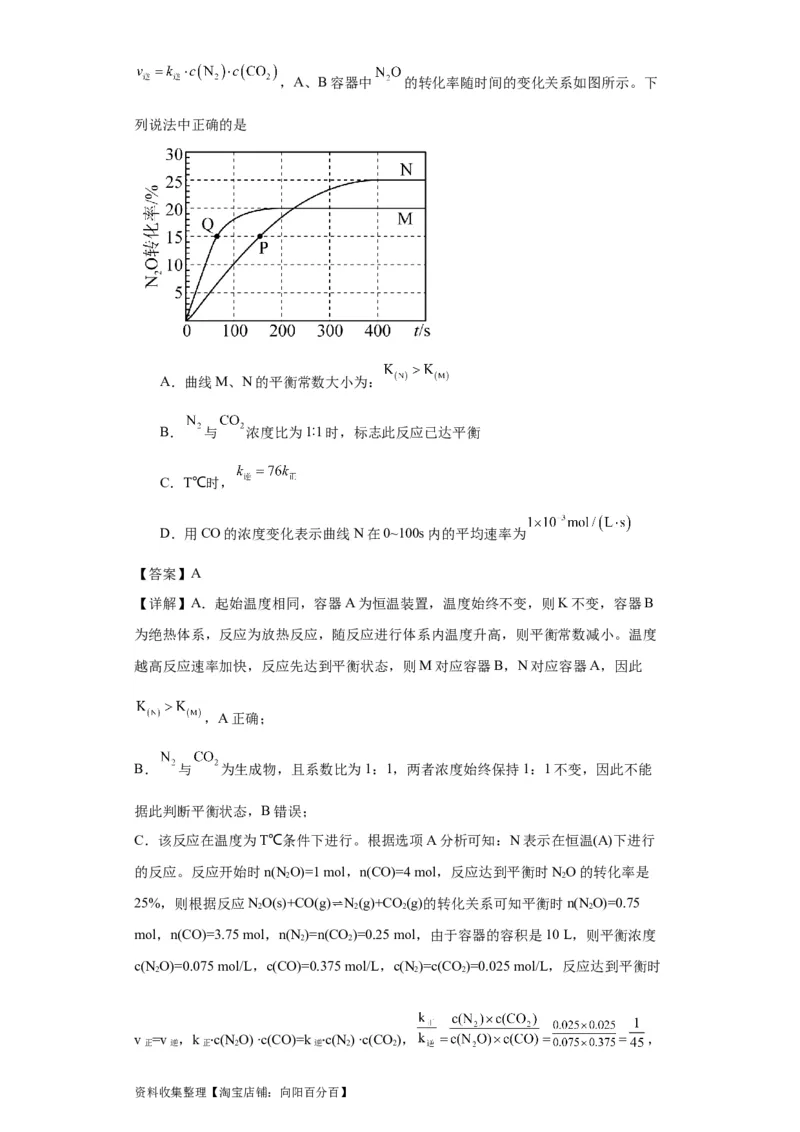
资料收集整理【淘宝店铺:向阳百分百】,A、B容器中 的转化率随时间的变化关系如图所示。下
列说法中正确的是
A.曲线M、N的平衡常数大小为:
B. 与 浓度比为1∶1时,标志此反应已达平衡
C.T℃时,
D.用CO的浓度变化表示曲线N在0~100s内的平均速率为
【答案】A
【详解】A.起始温度相同,容器A为恒温装置,温度始终不变,则K不变,容器B
为绝热体系,反应为放热反应,随反应进行体系内温度升高,则平衡常数减小。温度
越高反应速率加快,反应先达到平衡状态,则M对应容器B,N对应容器A,因此
,A正确;
B. 与 为生成物,且系数比为1:1,两者浓度始终保持1:1不变,因此不能
据此判断平衡状态,B错误;
C.该反应在温度为T℃条件下进行。根据选项A分析可知:N表示在恒温(A)下进行
的反应。反应开始时n(N O)=1 mol,n(CO)=4 mol,反应达到平衡时NO的转化率是
2 2
25%,则根据反应N
2
O(s)+CO(g)⇌N
2
(g)+CO
2
(g)的转化关系可知平衡时n(N
2
O)=0.75
mol,n(CO)=3.75 mol,n(N )=n(CO )=0.25 mol,由于容器的容积是10 L,则平衡浓度
2 2
c(NO)=0.075 mol/L,c(CO)=0.375 mol/L,c(N)=c(CO )=0.025 mol/L,反应达到平衡时
2 2 2
v =v ,k ∙c(NO) ∙c(CO)=k ∙c(N) ∙c(CO), = = = ,
正 逆 正 2 逆 2 2
资料收集整理【淘宝店铺:向阳百分百】C错误;
D.0-100 s时NO的转化率为10 %,NO的反应量为l mol×10% =0.l mol,根据方程式
2 2
中物质反应转化关系可知CO的反应量为0.l mol,则用CO的浓度变化表示曲线N在
0-100 s内的反应速率为v(CO)= =1.0×10-4mol/(L⋅s),D错误;
故选:A。
19.恒温恒容条件下,向密闭容器中加入等物质的量的M和N,发生反应:
,已知该反应的正反应速率 ,其中速率常数满
足关系 (R、A为常数,T为温度, 为反应的活化能)。上述反应在催化剂
Cat1、Cat2作用下的关系如图。下列说法错误的是
A.使用催化剂Cat1时反应的活化能较高
B.平衡时M和N的转化率相等
C.增大N的浓度不影响正反应速率和平衡状态
D.若改为恒容绝热容器,平衡时M的转化率一定降低
【答案】C
【详解】A.从曲线的斜率上可以分析出使用催化剂Cat1时反应的活化能较高,故A
说法正确;
B.反应物的系数相等,投料相等,所以平衡时的转化率也相等,故B说法正确;
C.根据v =kc(M),增大N的浓度不影响正反应速率,但一定会影响平衡状态,故C说
正
法错误;
D.若改为恒容绝热容器,无论反应是吸热反应还是放热反应,平衡时M的转化率一
定降低,故D说法正确;
答案为C。
资料收集整理【淘宝店铺:向阳百分百】二、多选题
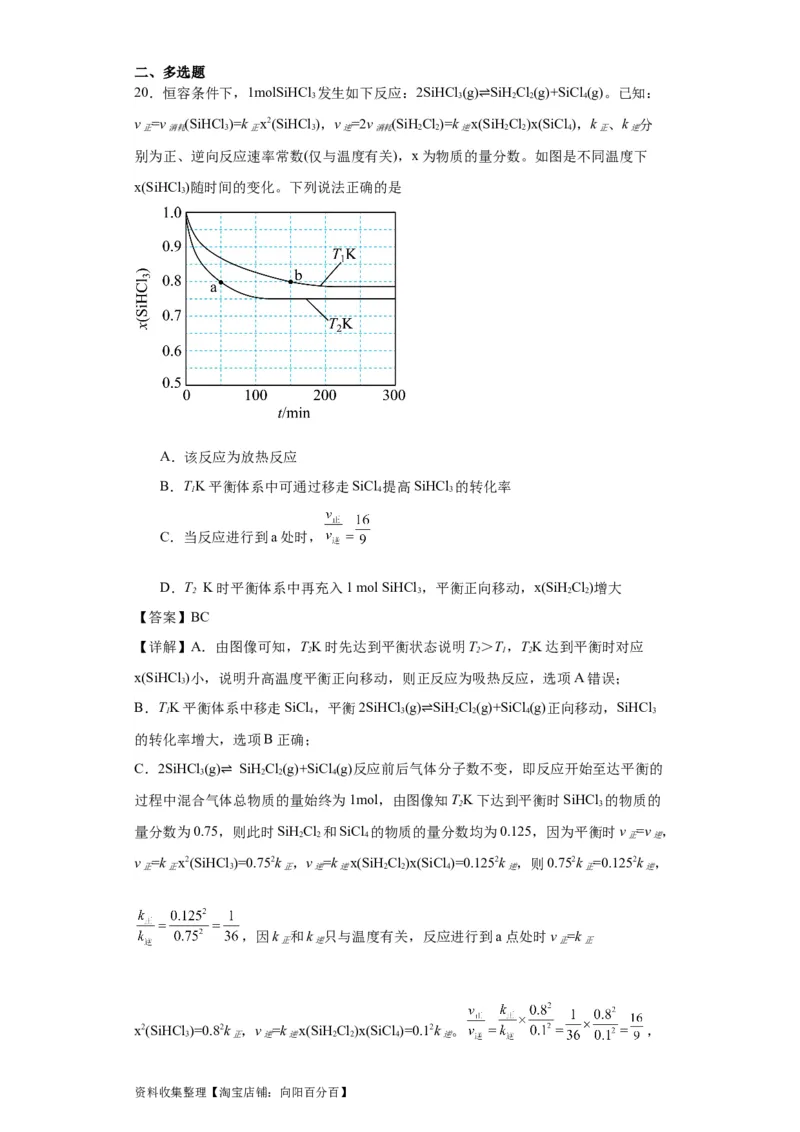
20.恒容条件下,1molSiHCl 发生如下反应:2SiHCl (g) SiHCl(g)+SiCl (g)。已知:
3 3 2 2 4
v =v (SiHCl )=k x2(SiHCl ),v =2v (SiHCl)=k x(⇌SiHCl)x(SiCl ),k 、k 分
正 消耗 3 正 3 逆 消耗 2 2 逆 2 2 4 正 逆
别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下
x(SiHCl )随时间的变化。下列说法正确的是
3
A.该反应为放热反应
B.TK平衡体系中可通过移走SiCl 提高SiHCl 的转化率
1 4 3
C.当反应进行到a处时, =
D.T K时平衡体系中再充入1 mol SiHCl ,平衡正向移动,x(SiHCl)增大
2 3 2 2
【答案】BC
【详解】A.由图像可知,TK时先达到平衡状态说明T>T,TK达到平衡时对应
2 2 1 2
x(SiHCl )小,说明升高温度平衡正向移动,则正反应为吸热反应,选项A错误;
3
B.TK平衡体系中移走SiCl ,平衡2SiHCl (g) SiHCl(g)+SiCl (g)正向移动,SiHCl
1 4 3 2 2 4 3
的转化率增大,选项B正确; ⇌
C.2SiHCl (g) SiHCl(g)+SiCl (g)反应前后气体分子数不变,即反应开始至达平衡的
3 2 2 4
过程中混合气体⇌总物质的量始终为1mol,由图像知TK下达到平衡时SiHCl 的物质的
2 3
量分数为0.75,则此时SiHCl 和SiCl 的物质的量分数均为0.125,因为平衡时v =v ,
2 2 4 正 逆
v =k x2(SiHCl )=0.752k ,v =k x(SiHCl)x(SiCl )=0.1252k ,则0.752k =0.1252k ,
正 正 3 正 逆 逆 2 2 4 逆 正 逆
,因k 和k 只与温度有关,反应进行到a点处时v =k
正 逆 正 正
x2(SiHCl )=0.82k ,v =k x(SiHCl)x(SiCl )=0.12k 。 = = = ,
3 正 逆 逆 2 2 4 逆
资料收集整理【淘宝店铺:向阳百分百】选项C正确;
D.恒容条件下再充入1mol SiHCl ,相当于增大压强,而2SiHCl (g) SiHCl(g)
3 3 2 2
+SiCl (g)反应前后气体分子数不变,所以平衡不移动,x(SiHCl)不变⇌,选项D错误;
4 2 2
答案选BC。
资料收集整理【淘宝店铺:向阳百分百】