文档内容
专题 02 化学计量及其应用
(考试时间:75分钟 试卷满分:100分)
选择题(本题共50小题,每小题2分,共100分。每小题只有一项是符合题目要求的)
1.设N 为阿伏伽德罗常数的值,下列说法不正确的是( )
A
A.30gHCHO和CHCOOH混合物中H原子数为2N
3 A
B.密闭容器中2molSO 和1molO 充分反应后,容器中分子数为2N
2 2 A
C.一定条件下,6.4g铜与过量的氯气反应,转移电子数目为0.2N
A
D.1molH O 中含有共价键的数目为3N
2 2 A
2.设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.18.9g三肽C H NO (相对分子质量:189)中的肽键数目为0.2N
6 11 3 4 A
B.1mol重水比1mol水多N 个质子
A
C.电解精炼铜时,电路中每通过N 个电子时阳极溶解32gCu
A
D.常温常压下,13.6g金刚烷( )中所含C-C键的数目为1.36N
A
3.(2023·浙江省十校联盟高三联考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,11.2LH O 含有的非极性共价键数目为0.5N
2 2 A
B.在1L0.1mol∙L-1CHCOONa溶液中,阴离子的总数等于0.1N
3 A
C.5.6gFe与足量的S反应转移的电子数为0.2N
A
D.1molHOOCCH COOH与足量乙醇在一定条件下反应,生成的酯基的数目为2N
2 A
4.(2023·辽宁省大连市一模)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.0.1 mol/L Na CO 溶液中,含有 的数目为0.2N
2 3 A
B.标准状况下,22.4 L CH 和22.4 L Cl 在光照下充分反应后的分子数为2N
4 2 A
C.1mol CaC 晶体和1molCaH 晶体含有的离子数目均为2N
2 2 A
D.一定条件下,5.6 g Fe与0.1 mol Cl 充分反应,转移的电子数为0.3N
2 A
5.设N 为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A
A.0.1mol的11B中,含有0.6N 个中子
A
B.0℃、101kPa下,0.1mol乙炔和甲醛(HCHO)的混合物中含有 键的数目为0.2N
A
C.将1mol Cl 通入足量水中,所得溶液中Cl 、HClO、Cl-、ClO-三种微粒数目之和为2N
2 2 A
D.常温下,1L0.50 mol·L-1NH Cl溶液与2L0.25 mol·L-1NH Cl溶液所含NH +的物质的量后者小
4 4 4
6.(2023·河南安阳市二模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,生成2.24LO 转移的电子数为0.4N
2 A
B.2L1mol·L-1的氯化铜溶液中H+数目为4N
A
C.常温下,5.6g铁与足量稀硝酸反应转移的电子数为0.3N
AD.2LpH=5的0.05mol·L-1KCr O 溶液中Cr O2-数目为0.1N
2 2 7 2 7 A
7.(2023·浙江省义乌市高三高考适应性考试)设N 为阿伏加德罗常数,下列有关说法正确的是( )
A
A.在25℃时,pH为12的CHCOONa溶液中水电离出的H+数目为0.01N
3 A
B.标准状况下,4.48LSO 和足量O 反应,生成的SO 分子数目为0.2N
2 2 3 A
C.电解精炼粗铜时,阳极质量减少6.4g,外电路中通过电子的数目为0.2N
A
D.13g苯、苯乙烯、聚苯乙烯的混合物中所含氢原子数目为N
A
8.(2023·辽宁省抚顺市普通高中高三模拟)N 表示阿伏加德罗常数的值,下列说法正确的是( )
A
A.1.8g重水(D O)中所含质子数为N
2 A
B.常温下1L pH=13的Ba(OH) 中含有OH-的数目为0.2N
2 A
C.106gNaCO 固体中含有N 个CO2-
2 3 A 3
D.标准状况下,22.4LSO 中含有SO 的分子数为N
3 3 A
9.(2023·河北省衡水市部分重点高中高三二模)已知N 为阿伏加德罗常数的值,下列有关说法正确的
A
是( )
A.在1 mol[Co(NH )Cl]Cl中存在的配位键数目为6N
3 4 2 A
B.34g HO 生成O 转移的电子数一定为2N
2 2 2 A
C.0.1 mol·L-1的NaS溶液中:N(S2-)+ N(HS-)+ N(H S)+=0.1 N
2 2 A
D.16g 14CH 分子所含的电子数目为10N
4 A
10.(2023·福建省福州市普通高中毕业班高三质量检测)设N 为阿伏加德罗常数的值,下列说法正确
A
的是( )
A.32g肼(N H)分子中含σ键数目为5N
2 4 A
B.标准状况下,11.2L SO 所含分子数为0.5N
3 A
C.1mol铜铝合金与足量稀HNO 充分反应,转移的电子数小于2N
3 A
D.室温时,1.0L pH=12的Ba(OH) 溶液中含有的 数目为0.2N
2 A
11.(2023·四川省成都市蓉城名校联盟高三三模)N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.100 mL 2 mol·L−1蔗糖溶液中所含分子数为0.2N
A
B.30 g由乙酸和葡萄糖组成的混合物中含氧原子数为N
A
C.0.1 mol NaHCO 晶体中含阴、阳离子总数为0.3N
3 A
D.浓盐酸分别和KMnO 、KClO 反应制备0.1 mol氯气,转移的电子数均为0.2N
4 3 A
12.(2023·江西省赣州市高三二模)设N 为阿伏伽德罗常数的值,下列说法错误的是( )
A
A.室温下,20gKH固体中所含H-的数目为0.5N
A
B.1L0.01mol·L-1的Ca(HCO ) 溶液中含碳粒子总数为0.02N
3 2 A
C.50g质量分数为46%的乙醇水溶液中含有的氧原子总数为0.5N
A
D.2NH (g) 3H(g)+N(g) ΔH=+akJ·mol-1,若参加反应的NH 数目为2N ,反应会吸收akJ热量
3 2 2 3 A
13.(2023·河北省邢台市九师联盟高三联考)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.17gHO 中含有非极性键的数目为0.5N
2 2 AB.标准状况下,11.2LCHOH含有原子核的数目为3N
3 A
C.1mol·L-1的KCl溶液中含有 的数目为N
A
D.1mol Na O 与足量HO反应,转移电子的数目为2N
2 2 2 A
14.(2023·四川省成都市高三第三次诊断考试)设N 代表阿伏加德罗常数的值。下列说法正确的是
A
( )
A.标准状况下,22.4LCH 中含极性键数目约为13N
4 10 A
B.39gNaO 固体含有离子数约为2N
2 2 A
C.1molNH NO 溶于某稀氨水后所得溶液呈中性,则该溶液中NH +数目为N
4 3 4 A
D.0.5molCl 溶于水后,溶液中的Cl-、ClO-、HClO三者之和为N
2 A
15.(2023·湖北省华大新高考联盟高三二模教学质量测评)设N 为阿佛加德罗常数的值。下列说法正
A
确的是( )
A.标准状况下,22.4L的CH 和CHCl 所含分子数均为N
4 3 A
B.1molSiO 中Si-O键的数目为4N
2 A
C.电解精炼铜时,阳极质量减少32g时,外电路中转移的电子数为N
A
D.F-水解能力弱于NH +则1L1mol·L-1的NH F溶液中,HF和NH +的总数大于N
4 4 4 A
16.(2023·四川省南充市三模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.NaO 作供氧剂时,每生成5.6LO ,转移电子数为0.25N
2 2 2 A
B.工业合成氨时,每反应1molN ,生成的极性共价键数目为6N
2 A
C.电解精炼铜时,阳极质量每减少64g,电路中转移2mol电子
D.明矾净水时,0.1mol/LAl3+形成的Al(OH) 胶粒的数目为0.1N
3 A
17.(2023·山西省晋中市三模)N 表示阿伏加德罗常数的值,下列说法错误的是( )
A
A.1 mol [Cu(NH)]2+中含有σ键数为12N
3 4 A
B.标准状况下,11.2 L HCHO与CH 的混合物中分子数为0.5N
4 A
C.向含1molFeI 的溶液中通入等物质的量的Cl,转移的电子数为2N
2 2 A
D.45g草酸中sp2杂化的C原子个数为N
A
18.(2023·天津市九校高三联考)设N 表示阿伏加德罗常数,下列叙述正确的是( )
A
A.标准状况下,22.4L氮气中含有7N 个中子
A
B.100mL1mol·L-1FeCl 溶液中所含Fe3+的数目为0.1N
3 A
C.标准状况下,22.4LCO 与足量NaO 反应转移的电子数为2N
2 2 2 A
D.3mol单质Fe完全转变为Fe O,失去8N 个电子
3 4 A
19.(2023·山东高三联考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.25℃, 下, 乙烯分子中 键的数目为2.5N
A
B.浓硝酸热分解生成NO 、NO 共 时,转移电子数为0.5N
2 2 4 AC. 溶液中, 和 的离子数目之和为0.01N
A
D. 铁完全发生吸氧腐蚀生成铁锈(Fe O· xHO),在电化学过程中转移的电子数为0.3N
2 3 2 A
20.(2023·河北省石家庄部分重点高中高三联考)N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.0.1mol[Cu(NH )]2+中含有的σ键数为1.2N
3 4 A
B.47g核素 发生裂变反应: ,净产生的中子( )数为2N
A
C.将0.1molCH 与0.1molCl 混合光照,充分反应后,生成的CHCl分子数为0.1N
4 2 3 A
D.0.2g由 和NO 组成的混合气体中含有的电子数为0.1N
2 A
21.(2023·广东省韶关市等4地高三期中考试)设N 为阿伏加德罗常数的数值,下列说法正确的是(
A
)
A.5.6g铁分别与足量氯气和稀硝酸反应,转移的电子数目均为0.3N
A
B.标准状况下,氧原子总数为0.2N 的CO 和NO 的混合气体,其体积为2.24L
A 2 2
C.100g 46%乙醇溶液中所含氧原子数目为N
A
D.常温下,pH=1的盐酸溶液中,由水电离出的H+个数为10-13N
A
22.(2023·河北省高三联考)N 是阿伏加德罗常数的值。下列关于含氮物质的说法错误的是( )
A
A.通常状况下,10.8gN O 中含有的电子数目为5.4N
2 5 A
B.足量铜和1molHNO 反应生成Cu(NO ) 时转移电子数为2N
3 3 2 A
C.1L1mol·L-1NaNO 溶液中NO -和HNO 粒子数目之和为N
2 2 2 A
D.1molN 和4molH 在密闭容器中反应生成NH 分子数目小于2N
2 2 3 A
23.(2023·河南省安阳市高三阶段第一次联考)阿伏加德罗常数的值用N 表示。下列说法中正确的是(
A
)
A.常温常压下,11.2LSO 含有的氧原子数大于N
2 A
B.一定条件下,Ca与O 反应生成7.2gCaO ,转移电子的个数为0.4 N
2 2 A
C.10g质量分数为98%的浓硫酸含有的氢原子数为0.2 N
A
D.0.1mol Na O 和NaO的混合物中含有的离子总数等于0.3 N
2 2 2 A
24.N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.氢原子数为0.6N 的乙醚分子中含有的极性键数为0.8N
A A
B.S 与S 混合物6.4g所含S原子数一定为0.2N
6 8 A
C.10gD16O含有质子数与中子数均为5N
2 A
D.0.1molH 和0.1molI 于密闭容器中充分反应,容器中分子总数为0.2N
2 2 A
25.(2023·河南省重点高中高三9月联考)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.18g重水(D O)中所含的中子数为10N
2 A
B.28gN 与足量的H 充分反应,生成NH 的分子数为2N
2 2 3 AC.电解精炼铜,阳极质量减轻64g时,转移的电子数为2N
A
D.常温下,1LpH=9的醋酸钠溶液中,水电离出的 数目为10-5N
A
26.(2023·江西省五市九校高三第一次联考)设N 代表阿伏加德罗常量的值。下列说法正确的是( )
A
A.100g46%乙醇溶液中含有的氧原子数为4N
A
B.标准状况下,11.2L乙烷和乙烯混合物中含有的氢原子数为2.5N
A
C.2molNO与1molO 在密闭容器中充分反应后,容器中的分子总数为2N
2 A
D.用铜作电极电解饱和NaCl溶液,当电路上通过0.2mole-时,阴、阳两极产生的气体分子总数为
0.2N
A
27.(2023·山东省德州市高三统考)N 为阿伏加德罗常数的值。下列叙述正确的是( )
A
A.标准状况下,11.2L氧气和臭氧混合气体中含氧原子数目为N
A
B.1 mol·L-1CHCOONa溶液中含CHCOOH、CHCOO-总数为N
3 3 3 A
C.一定条件下,1mol氢气与1mol碘单质充分反应后,分子总数为2N
A
D.含0.5mol Cr O2-的酸性溶液与足量HO 反应生成 的过程中转移电子数为4N
2 7 2 2 A
28.(2023·山东省名校联盟高三第一次学业质量联合检测)设N 为阿伏加德罗常数的值。下列说法正
A
确的是( )
A.常温下, 的KOH溶液中OH-的数目为0.1 N
A
B.1 molO 与足量的Na完全反应,转移电子数一定为4 N
2 A
C.11.5g乙醇分子中含有共价键的数目为2 N
A
D.标准状况下,2.24 L 含有的质子数是1.7 N
A
29.(2023·湖南省四大名校名师团队高三模拟)设N 表示阿伏加德罗常数的数值,下列叙述正确的是(
A
)
A.6.2g白磷(分子式为 ,分子结构如图所示( )中所含P-P键的数目为0.15N
A
B.标准状况下,22.4L Cl 参加化学反应时,转移的电子数一定都是2N
2 A
C.标准状况下,0.5N 个CHOH分子所占的体积约为
A 3
D.500mL1mol·L-1氯化铜溶液中的Cu2+数目小于0.5N
A
30.(2023·福建省七地市同三毕业班第一次质量检测)制备NaSO 的反应:2NaS+
2 2 3 2
NaCO+4SO=CO +3 Na SO。设N 为阿伏加德罗常数的值,下列说法正确的是( )
2 3 2 2 2 2 3 A
A.2L0.5mol·L-1NaS溶液中含 的数目为N
2 A
B.5.6LCO (标准状况下)中含电子数目为11N
2 AC.15.8gNa SO 中含非极性共价键的数目为0.1N
2 2 3 A
D.1 mol SO 完全参加反应,转移电子数为N
2 A
31.(2023·福建省泉州市高三模拟)已知:Zn+2HNO+NHNO =N ↑+Zn(NO)+3H O。设N 为阿伏伽德
3 4 3 2 3 2 2 A
罗常数的值,下列说法正确的是( )
A.标准状况下,2.24LH O中含σ键数为0.2N
2 A
B.0.1mol•L-1HNO 溶液中离子总数大于0.2N
3 A
C.若反应中消耗6.5gZn,则该反应转移的电子数为0.2N
A
D.常温下,1LpH=5的NH NO 溶液中含有的H+数目为10-5N
4 3 A
32.(2023·湖南省名校教研联盟高三联考)臭氧法处理含氰废水的主要反应原理为 5O+2CN-
3
+H O=5O+2HCO-+N 。设N 为阿伏加德罗常数的值,下列说法错误的是( )
2 2 3 2 A
A.生成 HCO -转移的电子数目为3N
3 A
B.16gO 和O 的混合物中含有的原子数目为N
3 2 A
C.标准状况下 N 中所含的电子数为14N
2 A
D.2.6g 中含有的σ键的数目为0.1N
A
33.(2023·湖北省武汉市圆创联考)甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反
应制得。N 为阿伏加德罗常数的值。下列有关说法正确的是( )
A
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol甲酸甲酯中含有sp3杂化的原子数目为N
A
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6N
A
34.(2023·重庆市高三二诊考试)氨对水体的污染情况越来越受人们的重视。用次氯酸钠可以脱除水中
的NH ,其反应式为:2NH +3NaClO=N +3NaCl+3HO。设N 为阿伏加德罗常数值,下列说法正确的是
2 3 2 2 A
( )
A.33.6L NH 中所含的σ键数目为4.5N
3 A
B.2L 0.5mol/L NaClO溶液中含有的ClO-数目为N
A
C.若该反应生成27g H O时,转移的电子数为3N
2 A
D.2mol N 与3mol H 在密闭容器中反应生成的NH 分子数为2N
2 2 3 A
35.(2023·辽宁省葫芦岛市协作校高三联考)已知在酸性条件下,硫代硫酸钠会发生歧化反应:
HSO +Na SO=Na SO +SO↑+S↓+H O。设N 为阿伏加德罗常数的值,下列说法正确的是( )
2 4 2 2 3 2 4 2 2 A
A.常温常压下,20gDO中含有的氧原子的数目为N
2 A
B.pH=2的HSO 溶液中,含有的H+数目为0.02N
2 4 A
C.常温下,向100mL18mol•L-1浓硫酸中加入足量的Cu,该过程转移电子的数目为1.8N
A
D.32gSO 与足量的O 充分反应,生成的SO 分子总数为0.5N
2 2 3 A
36.(2023·江西省重点中学联盟高三第二次联考)胍盐是新冠病毒核酸保存液的重要成分之一、胍能吸
收空气中的CO ,且在碱性条件下水解为NH 和尿素[CO(NH)]。设N 为阿佛伽德罗常数的值,下列说法
2 3 2 2 A正确的是( )
A.1mol胍中含有的共用电子对数目为8N
A
B.常温常压下,60g尿素分子中含有C-N键的数目为2N
A
C.22.4L N (标准状况)和足量H 反应,生成NH 分子的数目为2N
2 2 3 A
D.1molCO 和足量NH 合成尿素,转移电子数目为2N
2 3 A
37 . (2023· 福 建 省 宁 德 市 普 通 高 中 高 三 毕 业 班 质 量 检 测 ) 反 应
4NaClO+CH OH+2H SO =4ClO ↑+HCOOH+3H O+2Na SO ,可用于制备绿色消毒剂ClO 。设N 为阿伏加
3 3 2 4 2 2 2 4 2 A
德罗常数的值,下列说法正确的是( )
A. 分子中σ键与π键的数目比为
B.生成1mol ClO 时,转移电子的数目为4N
2 A
C.1L0.1mol·L-1 CHOH溶液中含有的分子数目为0.1N
3 A
D.1molHCOOH与足量CHOH在一定条件下反应,生成的酯基数目为N
3 A
38.(2024·安徽泗县二中高三期中)乙醛是一种重要的有机化工原料,制备原理之一是2CHCHOH+O
3 2 2
2CHCHO+2H O。设阿伏加德罗常数的值为N ,下列有关说法错误的是( )
3 2 A
A.1L1mol•L-1乙醇水溶液中含有氢原子数目为6N
A
B.44g乙醛中所含σ键的数目为6N
A
C.18g冰中含有的氢键数目为2N
A
D.每消耗标准状况下4.48L氧气,转移电子数为0.8N
A
39.(2024·福建龙岩高三联考)我国科研工作者开发了一种空腔串联反应器,其原理如图所示。设 N
A
为阿伏加德罗常数的值,下列说法正确的是( )
A.22g CO 通入水中得到的溶液中含有 HCO 分子数为 0.5N
2 2 3 A
B.lmol CH 中所含质子数和中子数均为 10N
4 A
C.途径 2 生成标准状况下 22.4L CH ,反应转移电子数为 8 N
4 A
D.途径 1 所得产物物质的量之比为 l:1,形成共价键数目为 6N
A
40.84消毒液不能和医用酒精混用的原因是4NaClO+CH CHOH=CHCl +HCOONa+2NaOH+H O。设
3 2 3 2
N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1L0.2mol·L-1 NaClO溶液中ClO-数目为0.2N
A
B.23gCHCHOH中含有σ键数目为4N
3 2 A
C.标准状况下,2.24L CHCl 中原子数为0.5N
3 AD.室温下,pH为13的NaOH溶液中OH-数目为0.1N
A
42.(2024·广东佛山高三教学质量检测)海洋碳循环是影响全球气候变化的关键控制环节,下图为海洋
中碳循环的原理图。设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.1L0.1mol·L-1的NaCO 溶液中,CO2-数目为0.1N
2 3 3 A
B.“钙化”时,消耗16.8g NaHCO ,生成2.24LCO
3 2
C.“光合”时,每生成0.1mol (CH O) 转移电子数为0.4 xN
2 x A
D.0.1mol CO 中含有共用电子对数为0.2 N
2 A
42.(2024·重庆沙坪坝高三期中)氨氮是水体的污染物之一,工业上可用次氯酸钠作处理剂,反应方程
式为:2NH +3NaClO =N+3NaClO+3H O。设阿伏加德罗常数的值为N ,下列说法正确的是( )
3 2 2 A
A.1 L 0.1mol/L NaClO 溶液中含有0.1N 个 ClO⁻
A
B.18 g HO 中含有的孤电子对数目为2N
2 A
C.生成11.2 L N,转移的电子数为 3N
2 A
D.0.5 L0.1 mol/L 氨水中含有0.05N NH ·H O
A 3 2
43.(2023·浙江省温州市高三第一次适应性考试)设[aX+bY]为a个X微粒和b个Y微粒组成的一个微
粒集合体,N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.23gC HOH中C—H单键的数目为6N
2 5 A
B.20gND 溶于水形成的氨水溶液中质子数约为10N
3 A
C.常温下,pH=2的磷酸溶液中H+数目为0.01N
A
D.2SO +O 2SO ,则每1mol[2SO +O ]完全反应转移的电子数等于4N
2 2 3 2 2 A
44.(2023·湖北省荆宜三校高三联考)氨法脱硫工艺利用氨水吸收烟气中的SO 生成亚硫酸铵溶液,并
2
在富氧条件下将亚硫酸铵氧化成硫酸铵。关于该工艺说法正确的是(设N 代表阿伏加德罗常数的值) ( )
A
A.0.5mol氨气中氮原子的价层电子对数为2 N
A
B.若将2 molSO 与1molO 置于密闭容器中充分反应,产物的分子数为2 N
2 2 A
C.每氧化1 mol(NH )SO ,转移的电子数为4 N
4 2 3 A
D.0.01 mol·L-1 (NH )SO 溶液中,SO 2-、HSO -与HSO 的数目之和为0.01 N
4 2 3 3 3 2 3 A
45.(2023·天津市高三联考)已知HSO +2NaClO=Na SO +2HClO,设N 表示阿伏加德罗常数的值。下
2 4 2 4 A
列说法正确的是( )
A.0.2molHClO分子中,含有的H-Cl键数目为0.2 N
A
B. 的 溶液中,含有的 数目可能为0.19a N
A
C.14.2g Na SO 中含有的分子数目为0.1 N
2 4 AD. 的硫酸溶液中,含有的氧原子数目为2 N
A
46.设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,N 是阿伏加德罗常数的值。下列说
A
法正确的是( )
A.标准状况下,1个氧分子体积为 cm3
B.1.0 mol CH 与Cl 在光照下反应生成的CH Cl分子数为1.0N
4 2 3 A
C.在反应4Cl +8NaOH=6NaCl+NaClO+NaClO +4H O中,发生1mol电子转移时,生成氧化产物
2 3 2
[ClO+ClO -]的总数为
3
D.92.0 g甘油中含有羟基数为1.0N
A
47.(2023·安徽省卓越县中联盟高三第一次联考)我国科学家实现了二氧化碳到淀粉的合成,其转化过
程示意图如图所示:
已知CHCHOH的结构简式可表示为“ ”。设阿伏加德罗常数的值为N ,下列说法错误的
3 2 A
是( )
A.若太阳能电池将18gHO分解,则该反应转移的电子数为2 N
2 A
B.常温下,16.2g淀粉中含有的氢原子数为N
A
C.2.24LCO 分子中共用电子对数为0.4 N
2 A
D.3.2g CHOH被完全氧化为 时生成的 分子数为0.1 N
3 A
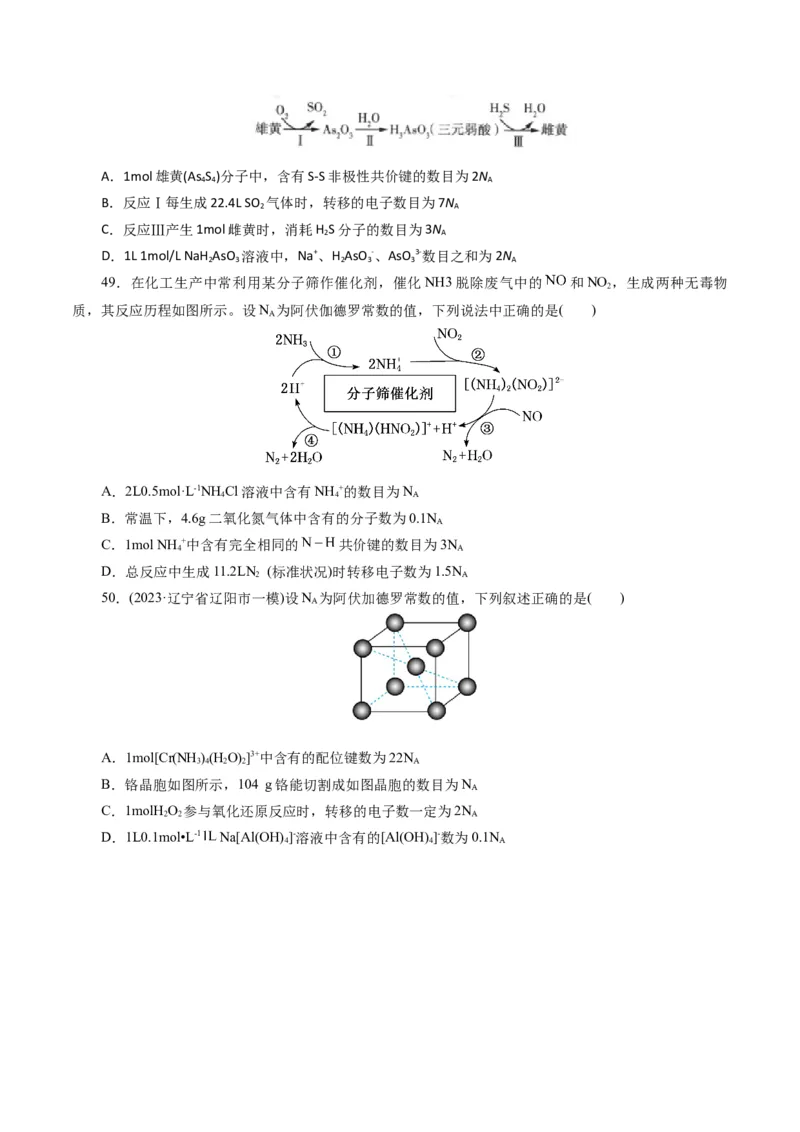
48.(2021·河北高三模拟)雄黄(As S , )与雌黄(As S )在古代均曾入药。二者可发生如图转
4 4 2 3
化;N 表示阿伏伽德罗常数的值,下列说法正确的是( )
AA.1mol雄黄(As S )分子中,含有S-S非极性共价键的数目为2N
4 4 A
B.反应Ⅰ每生成22.4L SO 气体时,转移的电子数目为7N
2 A
C.反应Ⅲ产生1mol雌黄时,消耗H S分子的数目为3N
2 A
D.1L 1mol/L NaH AsO 溶液中,Na+、H AsO -、AsO 3-数目之和为2N
2 3 2 3 3 A
49.在化工生产中常利用某分子筛作催化剂,催化NH3脱除废气中的 和NO ,生成两种无毒物
2
质,其反应历程如图所示。设N 为阿伏伽德罗常数的值,下列说法中正确的是( )
A
A.2L0.5mol·L-1NH Cl溶液中含有NH +的数目为N
4 4 A
B.常温下,4.6g二氧化氮气体中含有的分子数为0.1N
A
C.1mol NH +中含有完全相同的 共价键的数目为3N
4 A
D.总反应中生成11.2LN (标准状况)时转移电子数为1.5N
2 A
50.(2023·辽宁省辽阳市一模)设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.1mol[Cr(NH )(H O) ]3+中含有的配位键数为22N
3 4 2 2 A
B.铬晶胞如图所示,104 g铬能切割成如图晶胞的数目为N
A
C.1molH O 参与氧化还原反应时,转移的电子数一定为2N
2 2 A
D.1L0.1mol•L-1 Na[Al(OH)]-溶液中含有的[Al(OH) ]-数为0.1N
4 4 A