文档内容
专题 03 离子反应
2021年化学高考题
一、单选题
1.(2021·浙江高考真题)不能正确表示下列变化的离子方程式是
CO22H=CO H O
A.碳酸镁与稀盐酸反应: 3 2 2
HSOH O H SO OH
B.亚硫酸氢钠的水解: 3 2 2 3
Zn2OH2H O=Zn(OH) 2 H
C.锌溶于氢氧化钠溶液: 2 4 2
NONH N 2H O
D.亚硝酸钠与氯化铵溶液受热反应: 2 4 2 2
2.(2021·浙江高考真题)下列物质属于弱电解质的是
A.CO B.HO C.HNO D.NaOH
2 2 3
3.(2021·广东)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应
的反应方程式书写正确的是
Na O Na O H O2NaOHO
A. 2 2放入水中: 2 2 2 2
H O(g) 3H O2FeFe O 3H
B. 2 通过灼热铁粉: 2 2 3 2
CuH SO CuSO H
C.铜丝插入热的浓硫酸中: 2 4 4 2
SO KMnO 5SO 2H O2MnO 5SO2 4H 2Mn2
D. 2通入酸性 4溶液中: 2 2 4 4
4.(2021·全国高考真题)下列过程中的化学反应,相应的离子方程式正确的是
CO2CaSO CaCO SO2
A.用碳酸钠溶液处理水垢中的硫酸钙: 3 4 3 4
Fe4H NO Fe3 NO2H O
B.过量铁粉加入稀硝酸中: 3 2Al3 4OH AlO 2H O
C.硫酸铝溶液中滴加少量氢氧化钾溶液: 2 2
Cu2 S2 CuS
D.氯化铜溶液中通入硫化氢:
5.(2021·湖南高考真题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
不能大量共存,因发生反应:
A Na、Al3、Cl、NH
3
H
2
O
Al3 4NH H O=AlO 4NH 2H O
3 2 2 4 2
不能大量共存,因发生反应:
B H、K、S O2、SO2
2 3 4 2H S O2=SSO H O
2 3 2 2
C Na、Fe3、SO2
4
、H
2
O
2
能大量共存,粒子间不反应
D H、Na、Cl、MnO 能大量共存,粒子间不反应
4
A.A B.B C.C D.D
6.(2021·浙江高考真题)下列物质属于强电解质的是
A.KOH B.HPO C.SO D.CHCHO
3 4 3 3
7.(2021·浙江高考真题)下列反应的方程式不正确的是
2
A.石灰石与醋酸反应:CO3 +2CHCOOH=2CHCOO- +CO↑+HO
3 3 2 2
通电
B.铜片上电镀银的总反应(银作阳极,硝酸银溶液作电镀液):Ag(阳极) Ag(阴极)
C.铜与稀硝酸反应:3Cu+2NO3+8H+=3Cu2+ +2NO↑+4HO
2
2
D.明矾溶液中加入少量氢氧化钡溶液:2Al3+ +3SO4 + 3Ba2++6OH-=2Al(OH)↓+ 3BaSO↓
3 42021年化学高考模拟题
一、单选题
1.(2021·九龙坡区·重庆市育才中学高三二模)下列反应的离子方程式正确的是
A.铝和氢氧化钠溶液反应:Al+3OH-=Al(OH)↓
3
SO2
B.向稀HNO 中滴加NaSO 溶液: 3 +2H+=SO↑+HO
3 2 3 2 2
HCO CO2
C.NaHCO 溶液中加足量Ba(OH) 溶液:2 3+Ba2++2OH-=BaCO↓+2HO+ 3
3 2 3 2
D.向CuSO 溶液中加入NaO:2NaO+2Cu2++2HO=4Na++2Cu(OH)↓+O↑
4 2 2 2 2 2 2 2
2.(2021·福建省南安第一中学高三二模)常温下,下列说法正确的是
HCO- SO2- SO2-
A.某溶液中含有 3、 3 、 4 和Na+,若向其中加入NaO,充分反应后,四种离子的
2 2
SO2-
浓度不变的是 4 (忽略反应前后溶液体积的变化)
NH+ SO2-
B.水电离的c (H+)=10-12mol·L—1的溶液中,下列离子能大量共存: 4、Na+、 4 、
水
HCO-
3
C.氢氧化铁溶于HI溶液中的离子方程式为:2Fe(OH)+6H++2I—=2Fe2++I+6HO
3 2 2
SO2-
D.NaHS溶液中,下列离子能大量共存:K+、Al3+、Cl—、 4
3.(2021·重庆第二外国语学校高三三模)下列有关反应的离子方程式正确的是
Sn+Fe3+=Sn4++Fe2+
A.Sn溶于FeCl 溶液:
3
2Ag++H S=Ag S+2H+
B.[Ag(NH)]OH溶液中通入HS: 2 2
3 2 2
C.Cr(OH)(s)中同时加入NaOH溶液和HO 制NaCrO:
3 2 2 2 42Cr(OH) +3H O +4OH-=2CrO2-+8H O
3 2 2 4 2
HSO-+Ba2++OH-=BaSO +H O
D.NHHSO 溶液中加入足量Ba(OH) 溶液: 3 3 2
4 3 2
4.(2021·重庆第二外国语学校高三三模)常温下,下列各组离子在指定溶液中一定能大
量共存的是
2
A.能使紫色石蕊试液变蓝的溶液:Na+、NH4、CO3 、ClO-
B.通入大量二氧化碳的溶液:K+、Ca2+、Cl-、NO3
2
C.含有硝酸钠的溶液:H+、Mg2+、I-、SO4
2
D.室温下,c(OH-)/c(H+)=1的溶液:K+、Fe3+、SO4 、Cl-
5.(2021·重庆市第十一中学校高三二模)下列离子方程式书写正确的是
A.钠投入水中:Na+2HO=Na++2OH-+H↑
2 2
2ClOCO H O2HClOCO2
B.NaClO溶液中通入过量CO: 2 2 3
2
C.沸水中滴入几滴FeCl 饱和溶液:Fe3++3OH-=Fe(OH)(胶体)
3 3
SO Cl 2H O4H2ClSO2
D.饱和氯水中通入SO 至溶液颜色褪去: 2 2 2 4
2
6.(2021·安徽高三一模)下列反应中,现象和方程式都正确的是
浓硫酸
A.向胆矾粉末中加入适量浓硫酸,粉末由白色变成蓝色:CuSO•5HO CuSO+5HO
4 2 4 2
B.Fe加入FeCl 溶液中,溶液由黄色变成浅绿色:Fe+Fe3+=2Fe2+
3
Δ
C.NaO固体在空气中加热后,由白色变为淡黄色:NaO+CO NaCO
2 2 2 2 3
D.向Mg(OH) 悬浊液中滴加足量Fe(SO) 溶液,白色沉淀转化红褐色沉淀:3Mg(OH)(s)
2 2 4 3 2
+2Fe3+=2Fe(OH)(s)+3Mg2+
37.(2021·浙江高三其他模拟)下列有关方程式表示不正确的是
通电
A.用银电极电解AgNO 溶液:4Ag++2HO 4Ag+O↑+4H+
3 2 2
2
B.用重铬酸钾法测定白酒中乙醇的含量:2CrO7 +3CHOH+16H+=4Cr3++3CHCOOH+11HO
2 2 5 3 2
HCO
C.已知酸性:HCO>HCN> 3,则向NaCN溶液中通入少量的CO 时:CN-+CO+HO=HCN+
2 3 2 2 2
HCO
3
HCO
D.碳酸氢钡与少量的氢氧化钠溶液反应:Ba2++OH-+ 3=BaCO↓+HO
3 2
8.(2021·浙江高三其他模拟)下列物质属于电解质,且在熔融态能导电的是
A.硫酸 B.氯化铝 C.生石灰 D.苯酚
9.(2021·阜新市第二高级中学高三其他模拟)常温下,下列各组离子在指定溶液中一定
能大量共存的是
SO2-
A.1.0mol•L-1KNO 溶液:H+、Fe2+、Cl-、 4
3
SO2-
B.透明的溶液:Cu2+、Fe3+、 4 、Cr3+
HCO- SO2-
C.含有大量Ba2+的溶液: 3、Fe3+、SCN-、 4
D.使甲基橙变红的溶液:Na+、Cl-、CHCOO-、Fe2+
3
10.(【一飞冲天】新华中学高三模拟化学.)常温下,下列溶液中各组离子一定能够大量
共存的是
2- -
A.c(H+)/c(OH-)=1.0 ×10-12的溶液: K+、 Na+、CO3 、AlO2
2-
B.水电离出来的c(OH-)=1.0 ×10-13mol/L的溶液: K+、 Cl-、S2- 、SO3
+ 2- 2-
C.使甲基橙变红色的溶液中:Na+、NH4、 SO3 、SO3
2
D.通入足量SO 后的溶液: Na+、 Ba2+、ClO-、CHCOO-
2 311.(2021·吉林东北师大附中高三其他模拟)常温下,下列各组离子在指定溶液中一定能
大量共存的是
+ 2-
A.含有 Fe2+的溶液:K+、NH4 、SO4 、[Fe(CN) ]3 -
6
- +
B.能溶解 Al(OH) 的溶液:Na+ 、F- 、NO3、NH4
3
- 2-
C.含有I- 的溶液:Al3+、H+、MnO4 、SO4
+ -
D.含有 NH4的溶液:Na+、K+、HCO3 、Cl -
12.(2021·青龙满族自治县第一中学高三其他模拟)下列说法不正确的是
2 2
A.用碳酸钠溶液处理锅炉水垢:CaSO(s)+CO3 CaCO(s)+SO4
4 3
B.湿润的淀粉碘化钾试纸遇氯气变蓝:3Cl+I-+3HO=6Cl-+IO3+6H+
2 2
高温
C.铝粉和氧化铁组成的铝热剂用于焊接钢轨:2Al+FeO AlO+2Fe
2 3 2 3
D.用FeCl 溶液“腐蚀”覆铜板:2Fe3++ Cu = 2Fe2++ Cu2+
3
13.(【一飞冲天】8.宝坻一中三模)下列反应的离子方程式表达正确的是
通电
A.用铜电极电解MgCl 溶液:Mg2++2Cl-+2HO H↑+C1↑+Mg(OH)↓
2 2 2 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:CHCOOH+ClO-=HClO+CHCOO-
3 3
MnO C O2
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:2 4 +5 2 4 +16H+=2Mn2+
+10CO↑+8HO
2 2
D.水浴加热银氨溶液与葡萄糖的混合溶液,出现银镜:CHOH(CHOH)CHO+2[Ag(NH)]OH
2 4 3 2
Δ
CHOH(CHOH)COOH+2Ag↓+4NH+HO
2 4 3 2
14.(2021·广东石门中学高三其他模拟)在水溶液中能大量共存的一组离子是 2
A.NH4、Na+、Br-、SO4 B.K+、NH4、OH-、NO3
2 2
C.Fe2+、H+、ClO-、Cl- D.Mg2+、H+、SiO3 、SO3
15.(2021·天津高三一模)下列离子方程式正确的是
SO2-
A.用SO 溶液吸收溴蒸汽:SO+B +2HO= 4 +2Br-+4H+
2 2 r2 2
B.FeO溶于足量稀硝酸:FeO+2H+=Fe2++HO
2
C.用醋酸溶解水垢中的碳酸钙:CaCO+2H+=Ca2++CO↑+HO
3 2 2
D.腐蚀印刷线路板的反应:Fe3++Cu=Fe2++Cu2+
16.(2021·天津南开区·南开中学高三三模)下列离子方程式书写正确的是
A.用碳酸氢钠溶液检验水杨酸中的羧基: +2 → +2HO+2CO↑
2 2
HCO-
3
MnO- C O2-
B.用高锰酸钾标准溶液滴定草酸:2 4+16H++5 2 4 =2Mn2++10CO↑+8HO
2 2
通电
C.电解饱和食盐水:2Cl-+2H+ Cl↑+H↑
2 2
Δ
D.向NHHSO 溶液中加过量NaOH溶液并加热:NH+ +HSO- +2OH- NH↑+SO2- +2HO
4 3 4 3 3 3 2
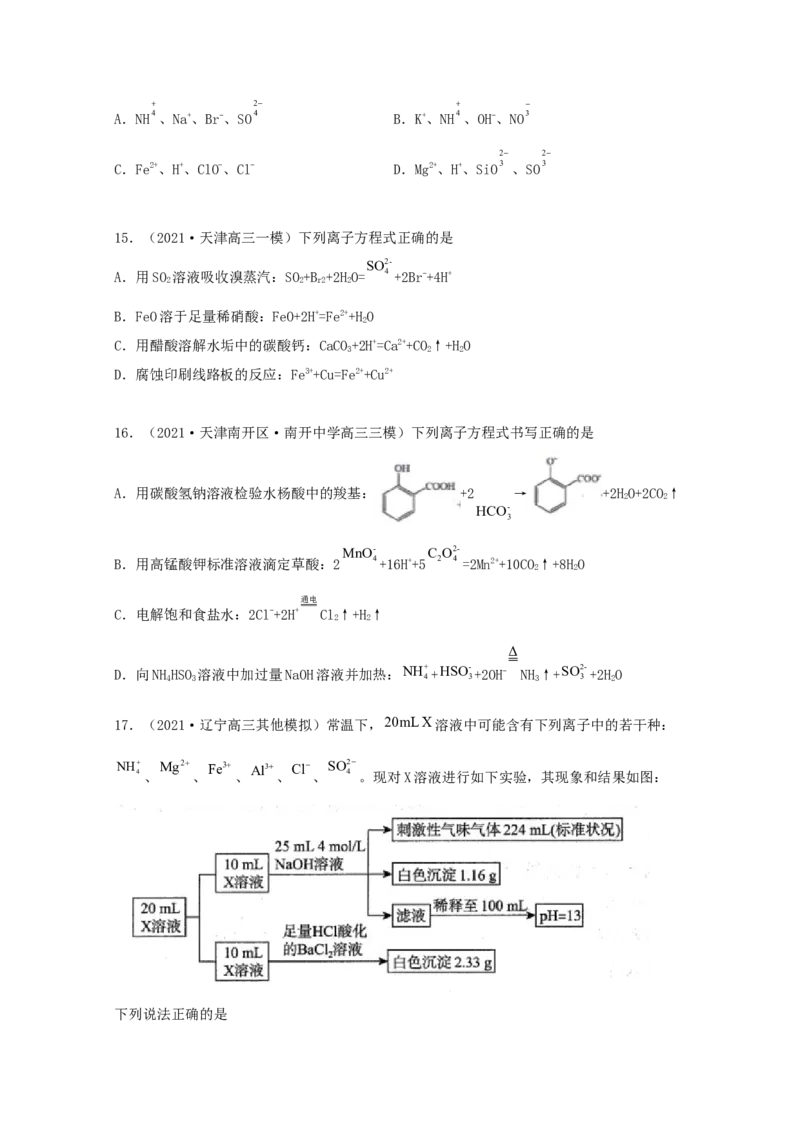
17.(2021·辽宁高三其他模拟)常温下,20mL X溶液中可能含有下列离子中的若干种:
NH
4
、
Mg2
、
Fe3
、
Al3
、
Cl
、
SO2
4
。现对X溶液进行如下实验,其现象和结果如图:
下列说法正确的是pH7
A.X溶液的
Mg2 Al3 NH Cl
B.X溶液中一定含有 、 、 4,不能确定是否含有
Cl c
Cl-
6.0molL1
C.X溶液中一定含有 ,且 为
CO
D.向滤液中通入足量的 2气体,可得白色沉淀,将沉淀过滤、洗涤、灼烧至恒重,可得
0.78g
固体
18.(2021·四川德阳市·高三二模)对于下列实验,能正确描述其反应的离子方程式是
SO2-
A.将少量SO 通入次氯酸钠溶液中:ClO-+SO+HO=Cl-+ 4 +2H+
2 2 2
CO2- SO2-
B.向含CaSO 的水垢中滴入饱和NaCO 溶液:CaSO(s)+ 3 (aq) 4 (aq)+CaCO(s)
4 2 3 4 3
电解
C.用铁电极电解饱和MgCl 溶液:Mg2++2C1-+2HO Mg(OH)↓+Cl↑+H↑
2 2 2 2 2
SO2- NH+
D.向(NH)Fe(SO) 溶液中加入含等物质的量溶质的Ba(OH) 溶液:Ba2++ 4 + 4+OH-
4 2 4 2 2
=BaSO↓+NH·HO
4 3 2
19.(2021·梅州市梅江区梅州中学高三其他模拟)下列反应方程式书写不正确的是
A.用氢氟酸雕刻玻璃:SiO+4HF=SiF↑+2HO
2 4 2
电解
B.工业上用电解法制镁:MgCl(熔融) Mg+Cl↑
2 2
C.向H18O中投入NaO 固体:2H18O+2NaO=4Na++4OH-+18O↑
2 2 2 2 2 2 2
D.氢氧化亚铁暴露于空气中:4Fe(OH)+O+2HO=4Fe(OH)
2 2 2 3
20.(2021·四川高三一模)下列指定反应的离子方程式正确的是
NH+
A.0.1mol/LAgNO 溶液中加入过量氨水:Ag++NH·HO=AgOH↓+ 4
3 3 2NO-
B.NO 通入水中制硝酸:2NO+HO=2H++ 3+NO
2 2 2
C O2-
C.NaOH溶液与过量HCO 溶液反应:HCO+2OH-= 2 4 +2HO
2 2 4 2 2 4 2
D.KOH溶液溶解Al(OH) 固体:Al(OH)+OH-=[Al(OH)]-
3 3 4
21.(2021·重庆市长寿中学校高三其他模拟)下列有关离子方程式的书写正确的是
NH+
A.向饱和NaCl溶液中依次通人足量NH 与CO:Na++NH+CO+HO=NaHCO↓+ 4
3 2 3 2 2 3
B.向BaCl 溶液中通入SO:Ba2++SO+2HO=BaSO↓+2H+
2 2 2 2 3
通电
C.电解MgCl 溶液:2Cl-+2HO Cl↑+H↑+2OH-
2 2 2 2
S O2-
D.NaSO 溶液与硝酸溶液混合: 2 3 +2H+=S↓+SO↑+HO
2 2 3 2 2
22.(2021·福建省福州第一中学)下列离子方程式书写正确的是
A.氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++HO
2
B.向KClO溶液中滴加浓盐酸:ClO-+Cl-+2H+=Cl↑+HO
2 2
C.向Ca(ClO) 溶液中通入少量SO:Ca2++SO+HO+2ClO-=CaSO↓+2HClO
2 2 2 2 3
HCO
D.向Mg(HCO) 溶液中滴加足量NaOH溶液:Mg2++ 3+OH-=MgCO↓+HO
3 2 3 2
23.(2021·广东金山中学高三三模)下列反应的离子方程式表达不正确的是
SO2-
A.将SO 通入酸性FeCl 溶液中:SO+2Fe3++2HO=2Fe2++ 4 +4H+
2 3 2 2
B.某消毒液的主要成分为NaClO,加白醋可增强消毒效果:
CH COOH+ClO-=HClO+CH COO-
3 3
C.向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色:
2MnO-+5C O2-+16H+=2Mn2++10CO +8H O
4 2 4 2 2
Ba2++2HCO-+2OH-=BaCO +CO2-+2H O
D.向碳酸氢钡溶液中加入过量氢氧化钾溶液: 3 3 3 224.(2021·西藏昌都市第一高级中学高三其他模拟)下列有关说法正确的是
A.少量Ca(OH) 溶液和NaHCO 溶液反应的离子方程式:Ca2++OH-+HCO3=CaCO↓+HO
2 3 3 2
B.Fe2+与HO 在酸性溶液中反应的离子方程式:2Fe2++HO+2H+=2Fe3++2HO
2 2 2 2 2
2
C.pH=2的溶液中可能大量存在Na+、NH4、SiO3
D.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
SO2- NH+
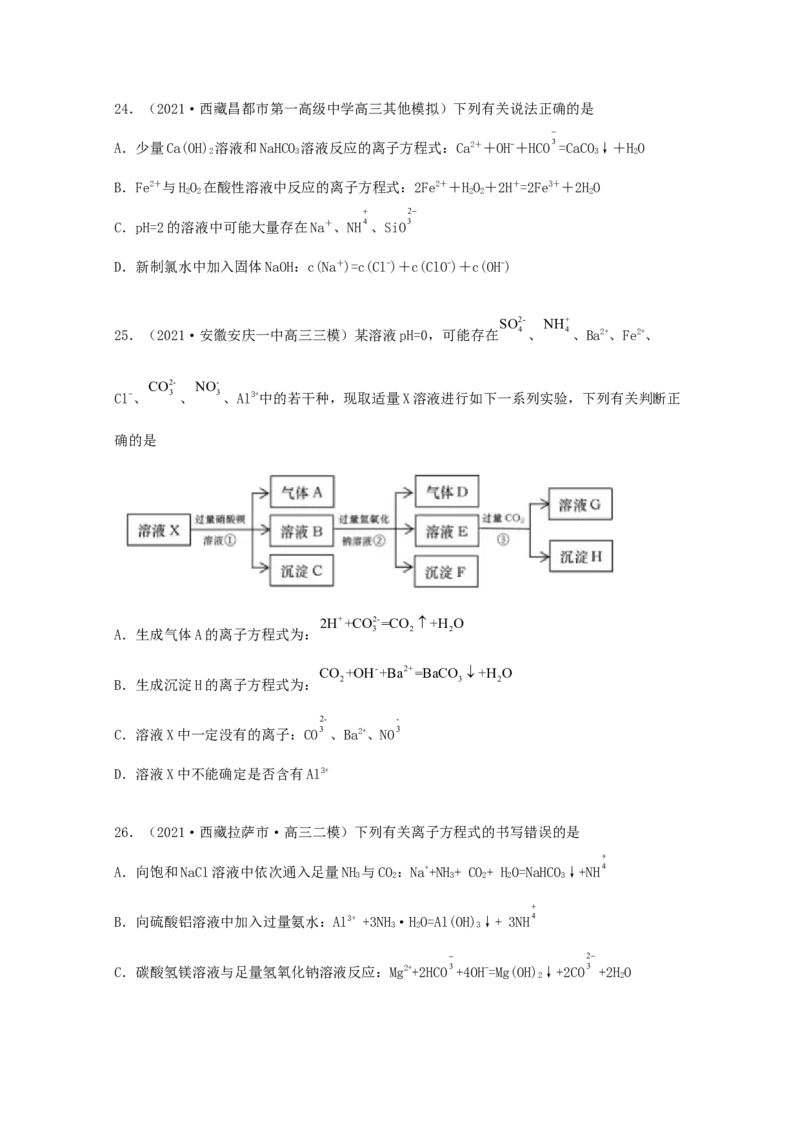
25.(2021·安徽安庆一中高三三模)某溶液pH=0,可能存在 4 、 4、Ba2+、Fe2+、
CO2- NO-
Cl-、 3 、 3、Al3+中的若干种,现取适量X溶液进行如下一系列实验,下列有关判断正
确的是
2H++CO2-=CO +H O
A.生成气体A的离子方程式为: 3 2 2
CO +OH-+Ba2+=BaCO +H O
B.生成沉淀H的离子方程式为: 2 3 2
2- -
C.溶液X中一定没有的离子:CO3 、Ba2+、NO3
D.溶液X中不能确定是否含有Al3+
26.(2021·西藏拉萨市·高三二模)下列有关离子方程式的书写错误的是
A.向饱和NaCl溶液中依次通入足量NH 与CO:Na++NH+ CO+ HO=NaHCO↓+NH4
3 2 3 2 2 3
B.向硫酸铝溶液中加入过量氨水:Al3+ +3NH·HO=Al(OH)↓+ 3NH4
3 2 3
2
C.碳酸氢镁溶液与足量氢氧化钠溶液反应:Mg2++2HCO3+4OH-=Mg(OH)↓+2CO3 +2HO
2 2 2
D.草酸与足量酸性高锰酸钾溶液反应:2MnO4+5CO4 + 16H+=2Mn2++10CO↑+8HO
2 2 2
27.(2021·惠来县第一中学高三月考)下列离子方程式正确的是
A.用HO 从酸化的海带灰浸出液中提取碘:2I-+HO+2H+=I+2HO
2 2 2 2 2 2
B.向碳酸氨铵溶液中加入过量的NaOH溶液:NH4+OH-= NH·HO
3 2
2
C.向饱和的碳酸钠溶液中通入足量的二氧化碳:CO +CO3 +HO= 2HCO3
2 2
D.过量SO 通入NaClO溶液中:SO +HO+ClO-= HClO+HSO3
2 2 2
28.(2021·湖北武汉市·汉阳一中高三三模)下列指定反应的离子方程式正确的是
A.NaO 与H18O反应:2NaO+2H18O=4Na++4OH- +18O↑
2 2 2 2 2 2 2
B.向次氯酸钠溶液中通入少量的CO:ClO—+CO+HO=HClO+HCO3
2 2 2
C.FeCl 溶液中加过量NaS溶液:S2- + 2Fe3+ =S↓+2Fe2+
3 2
D.向Fe(OH) 胶体中加入HI溶液:Fe(OH)+3H+ =Fe3+ +3HO
3 3 2
29.(2021·福建厦门外国语学校高三其他模拟)下列反应的离子方程式正确的是
A.用CuSO 溶液除去电石气中的少量硫化氢:Cu2++S2-=CuS↓
4
2-
B.向NaClO溶液中通入少量SO:ClO-+SO+HO=SO4 +C1-+2H+
2 2 2
C.向稀AgNO 溶液中加入过量稀氨水:Ag++2NH·HO=[Ag(NH)]++2HO
3 3 2 3 2 2
2
D.向苯酚钠溶液中通入少量CO:CO+HO+2 →CO +2
2 2 2 3
30.(2021·广东石门中学高三其他模拟)下列离子方程式错误的是
SO +3C1O-+H O=SO2-+Cl-+2HClO
A.少量SO 气体通入次氯酸钠溶液中: 2 2 4
2
Fe3++2OH-=FeOH
B.向NHFe(SO) 饱和溶液中滴加几滴NaOH溶液: 3
4 4 2
Fe O +6H+=2Fe3++3H O
C.氧化铁溶于HI溶液: 2 3 2
SiO2-+2H O+2CO =2HCO-+H SiO
D.向硅酸钠水溶液中通入过量CO 气体: 3 2 2 3 2 3
231.(2021·哈尔滨市·黑龙江实验中学高三其他模拟)对于下列实验,能正确描述其反应
的离子方程式是
2
A.HCO 具有还原性:2MnO4+5CO4 +16H+=2Mn2++10CO↑+8HO
2 2 4 2 2 2
B.用铝粉和NaOH溶液反应制取少量H:Al+2OH-=AlO2+H↑
2 2
2
C.KClO碱性溶液与Fe(OH) 反应:3ClO-+2Fe(OH)=2FeO4 +3Cl-+4H++HO
3 3 2
D.同浓度同体积NHHSO 溶液与NaOH溶液混合:H++OH-=HO
4 4 2
32.(2021·天津高三二模)下列离子方程式正确的是
Na S O H SO S O22H SSO H O
A. 2 2 3与稀 2 4混合: 2 3 2 2
HCOOH CO H O
B.碳酸氢钠溶液中加入氢氧化钠溶液: 3 2 2
FeOH FeOH 3H Fe33H O
C.向 3中加入氢碘酸溶液: 3 2
3Cu8H 2NO 3Cu2 2NO4H O
D.铜和浓硝酸反应: 3 2
33.(2021·辽宁高三三模)下列关于离子共存或离子方程式书写正确的是
2
A.某无色溶液中可能大量存在:H+、NH4、Cl-、CrO7
2
B.常温下,c(NH4)=c(Cl-)的NHCl和NH•HO的混合溶液中能大量存在:Fe3+、Cl-、NO3、
4 3 2
Al3+
C.向酸性KMnO 溶液中滴加HO:2MnO4+5HO+6H+=2Mn2++5O↑+8HO
4 2 2 2 2 2 2
通电
D.用惰性电极电解MgCl 水溶液:2Cl-+2HO 2OH-+Cl↑+H↑
2 2 2 2
34.(2021·广东茂名市·高三二模)化学与生活关系密切,解释下列应用的离子方程式正
确的是
选项 应用 解释(离子方程式)A 淀粉—KI溶液(稀硫酸酸化)检验碘盐中含KIO 5I-+IO -+6H+=3I +3H O
3 3 2 2
B 电解饱和食盐水制氢气和氯气 2Cl-+2H+=Cl +H
2 2
C 醋酸用于除去水垢 2H++CaCO =Ca2++CO +H O
3 2 2
D 氯化铁用于蚀刻铜板 Fe3++Cu=Cu2++Fe2+
A.A B.B C.C D.D
35.(2021·北京海淀区·人大附中高三三模)下列解释实验现象的离子方程式不正确的是
Cl +2OH-= Cl-+ClO-+H O
A.新制氯水中滴加NaOH溶液后,黄绿色褪去: 2 2
CO2+H O HCO+OH-
B.向NaCO 溶液中滴加酚酞溶液,溶液变红: 3 2 3
2 3
C.向Mg(OH) 悬浊液中滴加FeCl 溶液,生成红褐色沉淀:
2 3
3Mg(OH) +2 Fe3+=2Fe(OH) +3Mg2+
2 3
2S O2+4H+=SO2+3S+2H O
D.向NaSO 溶液中加入稀硫酸,溶液浑浊: 2 3 4 2
2 2 3
36.(2021·天津河西区·高三三模)下列能正确描述其变化的是
A.碳酸氢钠的电离:NaHCO
噲垐��
Na++HCO3
3
B.NO 通入水中制硝酸:2NO+HO=2H++NO3
2 2 2
C.向HO 溶液中滴加FeCl 溶液:2Fe3++HO=O↑+2H++2Fe2+
2 2 3 2 2 2
噲垐��
D.硬质酸钠溶液显碱性:C H COO-+HO C H COOH+OH-
17 35 2 17 35
37.(2021·天津滨海新区·高三三模)下列离子方程式中正确的是
-
A.NaHCO 溶液与少量Ba(OH) 溶液混合:HCO3+ Ba2++OH-= BaCO↓+HO
3 2 3 2
B.CaO投入稀硫酸中:CaO+2H+=Ca2++HO
2
- SO2-
C.向稀硝酸中加入少量FeS:FeS+4H++3NO3=Fe3++ 4 +3NO↑+2HO
2
SO2-
D.SO 通入过量 NaClO溶液: HO+ SO+ClO-= 4 +2H++Cl-
2 2 238.(2021·湖南高三其他模拟)下列离子方程式能用于解释相应实验且书写正确的是
选项 实验 离子方程式
A FeS溶于足量稀硝酸 FeS+2H+=Fe2++HS↑
2
Δ
向沸水中滴加饱和FeCl 溶液并加热,得到红褐
B 3 Fe3++3HO Fe(OH)(胶体)+3H+
色液体 2 3
向NHHCO 溶液中加入过量Ba(OH) 稀溶液,有白
C 4 3 2 OH-+HCO+Ba2+=BaCO+HO
色沉淀产生 3 3 2
向KMnO 溶液(墨绿色)中加入适量醋酸,溶液变
D 2 4 3MnO24H 2MnO MnO 2H O
为紫色且有黑色沉淀生成 4 4 2 2
A.A B.B C.C D.D
39.(2021·江西高三二模)硫酸盐气溶胶作为PM2.5的主要构成成分,科学家最近发现了
一种“水分子桥”催化促进硫酸盐形成的化学机制如图所示,下列说法不正确的是
A.该机制可以解决SO 的空气污染问题
2
B.“水桥”的形成与氢键有关
C.HSO3与NO 间发生的总反应的离子方程式:HSO3+2NO+HO=2HNO+HSO4
2 2 2 2
D.电子传递可以促进HSO3中O—H键的解离,进而形成中间体SO3
40.(2021·北京房山区·高三二模)下列解释实验事实的化学方程式正确的是
A.Na和Cl形成NaCl的过程:
B.用FeCl 溶液“腐蚀”覆铜板:Fe3++ Cu = Fe2+ + Cu2+
3电解
C.用石墨电极电解CuCl 溶液:2Cl-+2H+ H↑+Cl↑
2 2 2
D.“84消毒液”中加少量醋增强漂白性:ClO-+H+= HClO
41.(2021·广东珠海市·高三二模)下列关于离子共存或者离子反应的说法正确的是
0.1molL1CuSO K NH NO CO2
A. 4溶液可能大量存在: 、 4、 3、 3
CO OH HCO
B.用NaOH溶液吸收过量CO: 2 3
2
0.1molL1 K SO2 -
C. 氯化亚铁溶液:Na+、 、 4 、MnO4
Fe(OH) 3H Fe3 3H O
D.氢氧化铁和碘化氢溶液反应: 3 2
42.(2021·辽宁高三其他模拟)某溶液中只可能含有
Na、NH、Fe2、Al3、Cl、SO2、CO2、AlO 0.1molL1
4 4 3 2 中的几种离子,各离子浓度均为 。
某同学进行了如下实验:
下列说法正确的是
A.无法确定原溶液中是否含有Na
NH、Fe2、Cl、SO2
B.原溶液中肯定存在的离子为 4 4
BaSO BaCO Al(OH)
C.沉淀A为 4,沉淀C为 3和 3
NH、Al3 Ba2
D.滤液X中大量存在的阳离子有 4 和
43.(2021·湖北高三二模)下列离子方程式书写不正确的是2-
A.将过量SO 气体通入NaClO溶液中:SO+HO+ClO-=SO4 +Cl-+2H+
2 2 2
B.标准状况下将112 mL氯气通入10 mL 1 mol·L-1溴化亚铁溶液中:2Fe2++4Br-
+3Cl=2Br+2Fe3++6Cl-
2 2
-
C.向FeSO 溶液中滴加NaHCO 溶液和稀氨水,产生大量白色沉淀:Fe2++HCO3
4 3
+
+NH·HO=FeCO↓+NH4+HO
3 2 3 2
2-
D.向明矾溶液中滴加Ba(OH) 溶液,使沉淀的物质的量最大时:2Al3++ 3SO4 + 3Ba2++6OH- =
2
2Al(OH)↓+3BaSO↓
3 4
44.(2021·云南曲靖市·高三二模)下列实验的反应原理用离子方程式表示正确的是
SO Na CO SO CO2 SO2 CO
A.少量 2通入 2 3溶液中: 2 3 3 2
电解
2Cl-+2HO Cl↑+H↑+2OH-
B.用惰性电极电解氯化镁溶液: 2 2 2
KAlSO
C.向 4 2溶液中加入足量Ba(OH) 溶液:
2
Al3 SO2Ba2 3OH BaSO Al(OH)
4 4 3
CuH O 2H Cu2 2H O
D.用双氧水和稀硫酸处理铜印刷电路板: 2 2 2
45.(2021·广东高三其他模拟)常温下,下列各组离子在指定溶液中一定能大量共存的是
A.
c OH- =110-13molL-1
的溶液中:
Mg2 、K
、
SO2
4
、
NO
3
Na Cu2 HCO NO
B.使甲基橙呈红色的溶液: 、 、 3、 3
0.1molL1 KNO H Na SO2 S2
C. 的 3溶液: 、 、 4 、
D.
0.1molL1
的
BaCl
2溶液:
H
、
Na
、
Cl
、
SO2
4
46.(2021·广东高三其他模拟)下列指定反应的离子方程式正确的是
SO 2OH-+SO =SO2-+H O
A.用氨水吸收少量的 2气体: 2 3 2
B.
FeCl
3溶液与Cu的反应:
Cu+Fe3+=Cu2++Fe2+
NH N 3ClO-+2NH =N 3Cl-+3H O
C.加入NaClO将污水中的 3氧化成 2: 3 2 2
NaHCO Ba(OH) HCO-+Ba2++OH-=BaCO H O
D. 3溶液中加入少量 2溶液: 3 3 2
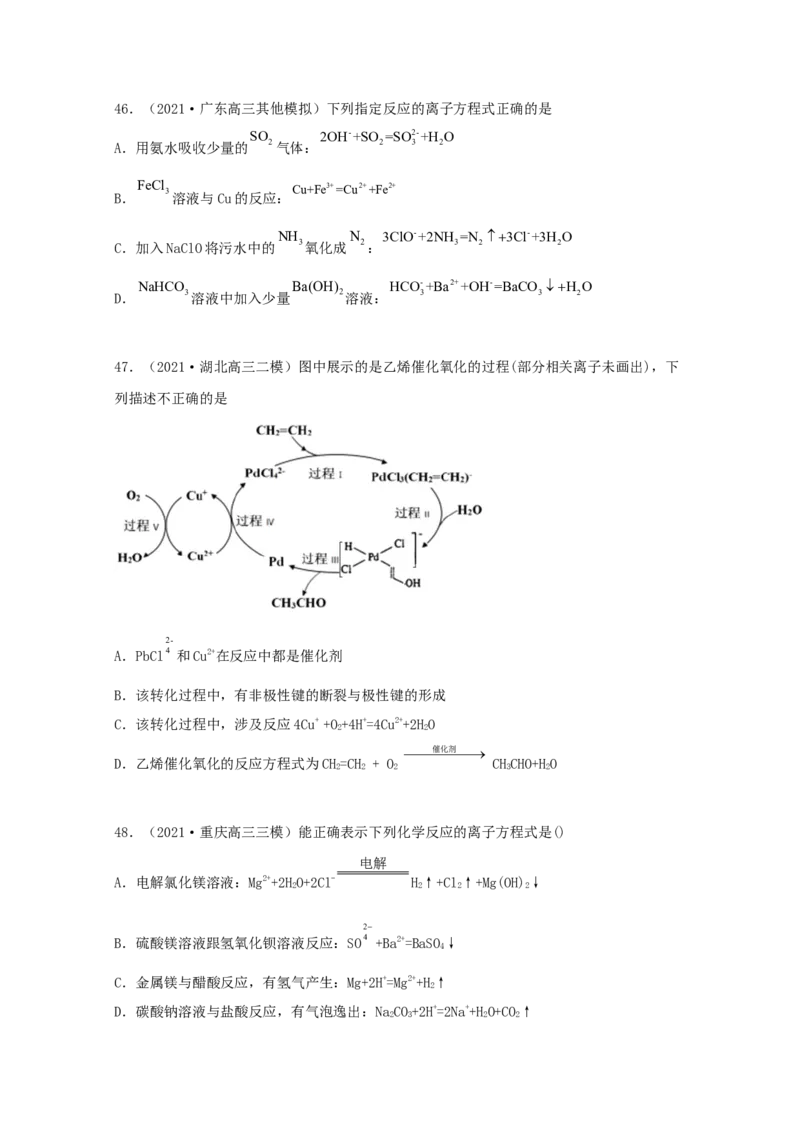
47.(2021·湖北高三二模)图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下
列描述不正确的是
2-
A.PbCl4 和Cu2+在反应中都是催化剂
B.该转化过程中,有非极性键的断裂与极性键的形成
C.该转化过程中,涉及反应4Cu+ +O+4H+=4Cu2++2HO
2 2
催化剂
D.乙烯催化氧化的反应方程式为CH=CH + O CHCHO+HO
2 2 2 3 2
48.(2021·重庆高三三模)能正确表示下列化学反应的离子方程式是()
电解
A.电解氯化镁溶液:Mg2++2HO+2Cl- H↑+Cl↑+Mg(OH)↓
2 2 2 2
2
B.硫酸镁溶液跟氢氧化钡溶液反应:SO4 +Ba2+=BaSO↓
4
C.金属镁与醋酸反应,有氢气产生:Mg+2H+=Mg2++H↑
2
D.碳酸钠溶液与盐酸反应,有气泡逸出:NaCO+2H+=2Na++HO+CO↑
2 3 2 249.(2021·天津高三三模)下列化学用语表述不正确的是
电解
Mg2++2Cl- Mg+Cl↑
A.电解MgCl 溶液: 2
2
K Fe(CN) Fe2:2Fe(CN) 3 3Fe2=Fe Fe(CN)
B.使用 3 6 检验 6 3 6 2
Al3 3HCO Al(OH) 3CO
C.泡沫灭火器工作原理: 3 3 2
D. NH 4 Cl 在水中发生水解: NH 4 H 2 O NH 3 H 2 OH
50.(2021·辽宁高三其他模拟)下列各组离子在给定条件下,因发生配合反应而不能大量
共存的一组是
pH2 K Na Cl CO2
A. 的溶液中: 、 、 、 3
B.含大量 Al(OH) 4 的溶液:Cu2、 NO 3 、 Mg2 、Cl
C.含有大量
Fe3
的溶液:
Na
、
NH
4
、
SO2
4
、
CN
SO K Na ClO SO2
D.溶解少量 2气体的溶液: 、 、 、 4