文档内容
专题 03 离子反应
1.下列物质属于弱电解质的是( )
A.KOH B.NH C.HSO D.NH HCO
3 2 3 4 3
【答案】C
【解析】A项,KOH为强碱,在水溶液中完全电离,为强电解质,A不符合题意;B项,NH 自身不能发
3
生电离,为非电解质,B不符合题意;C项,HSO 为二元弱酸,在水溶液不完全电离,为弱电解质,C符合
2 3
题意;D项,NH HCO 为盐,在水溶液中完全电离,为强电解质,D不符合题意;故选C。
4 3
2.下列物质中,属于电解质的是( )
A.Al B.NaCl C.KOH溶液 D.蔗糖溶液
【答案】B
【解析】A项,铝是金属单质,单质既不是电解质也不是非电解质,故A错误;B项,氯化钠是盐,在溶
液中电离能电离出钠离子和氯离子,属于电解质,故B正确;C项,氢氧化钾溶液是混合物,混合物既不是电
解质也不是非电解质,故C错误;D项,蔗糖溶液是混合物,混合物既不是电解质也不是非电解质,故D错
误;故选B。
3.下列物质中,其水溶液能导电,但本身属于非电解质的是( )
A.金属铁 B.SO C.酒精 D.硫酸钡晶体
2
【答案】B
【解析】A项,铁是单质,不溶于水,铁本身能导电,但不是电解质,也不是非电解质,故A错误;B项,
SO 的水溶液能导电,但SO 本身是非电解质,故B正确;C项,酒精的水溶液不能导电,酒精本身是非电解
2 2
质,故C错误;D项,硫酸钡晶体不溶于水,水溶液不导电,但硫酸钡是电解质,故D错误;故选B。
4.下列有关电解质、强电解质、弱电解质的分类正确的是( )
A B C D
电解质 Cu CO NaCl NaOH
2
强电解质 HCl Ba(OH) HClO BaSO
2 4 4
弱电解质 CHCOOH HO Fe(SCN) 氨水
3 2 3
【答案】C
【解析】A项,Cu是金属单质,而不是化合物,因此不属于电解质,A不符合题意;B项,CO 是化合物,
2但其溶于水或受热熔化时都不能发生电离而导电,因此属于非电解质,B不符合题意;C项,物质分类合理,
C符合题意;D项,氨水是混合物,而不是化合物,因此不属于弱电解质,D不符合题意;故选C。
5.下列物质在水溶液中的电离方程式书写正确的是( )
A.NaHCO ===Na++HCO B.Al O===2Al3++3O2-
3 2 3
C.MgCl ===Mg2++Cl D.NaHSO===Na++HSO
2 4
【答案】A
【解析】HCO为多元弱酸的酸式酸根离子,不能拆成H++CO,应写为HCO,故A项正确;Al O 不溶于
2 3
水,在水溶液中不能电离,只有在熔融状态下电离,故B项错误;MgCl ===Mg2++2Cl-,故C项错误;HSO
2
在水溶液里能完全电离成H+与SO,故D项错误。
6.(2022·浙江省温州十校联合体高一期中)下列物质中属于电解质的是( )
A.铁 B.碳酸钠 C.氯水 D.二氧化碳
【答案】B
【解析】A项,铁属于单质,既不是电解质也不是非电解质,A不符合题意;B项,碳酸钠属于盐,在水
溶液中能够导电,是电解质,B符合题意;C项,氯水是混合物,既不是电解质也不是非电解质,C不符合题
意;D项,CO 在水溶液和熔融状态下均不能导电,属于非电解质,D不符合题意;故选B。
2
7.(2022·浙江省新力量联盟高一期中联考)下列物质的水溶液能导电,但属于非电解质的是( )
A.KClO B.HSO C.CO D.氯气
3 2 4 2
【答案】C
【解析】A项,KClO 溶于水电离出离子而导电,属于电解质,A不符合;B项,HSO 溶于水电离出离
3 2 4
子而导电,属于电解质,B不符合;C项,CO 溶于水生成碳酸,碳酸电离出离子而导电,碳酸属于电解质,
2
二氧化碳是非电解质,C符合;D项,氯气是单质,不是电解质也不是非电解质,D不符合;故选C。
8.(2022·陕西高一月考)NH HSO 在水溶液中能电离出NH +、H+、SO 2-。下列对NH HSO 的分类错误的
4 4 4 4 4 4
是( )
A.NH HSO 是盐 B.NH HSO 是酸
4 4 4 4
C.NH HSO 是电解质 D.NH HSO 是化合物
4 4 4 4
【答案】B
【解析】A项,NH HSO 能电离出阴阳离子,是盐,故A正确;B项,NH HSO 电离出的阳离子除了是
4 4 4 4
酸H+,还有NH +,故B错误;C项,NH HSO 是溶于水能导电的化合物是电解质,故C正确;D项,
4 4 4
NH HSO 是化合物,故D正确;故选B。
4 4
9.下列电离方程式中,正确的是( )
A.CaOH==Ca2++2OH B.FeCl ==Fe3++2Cl
2 2C. HSO ==H ++SO 2- D. Al SO ==2Al3++3 SO2-
2 4 2 4 2 4 3 4
【答案】D
【解析】A项应为CaOH==Ca2++2OH ;B项应为FeCl ==Fe2++2Cl;C项应为HSO ==2H++SO 2-。
2 2 2 4 4
10.下列有关反应中不属于离子反应的是( )
A.NaCO 溶液与澄清石灰水的反应 B.氢氧化铜与稀硫酸的反应
2 3
C.锌与氯化铜溶液的反应 D.二氧化碳与生石灰作用生成碳酸钙的反应
【答案】D
【解析】离子反应指的是有离子参加或生成的反应。酸、碱、盐在溶液中相互之间的反应都有离子参加,
活泼金属可以把较不活泼的金属从其盐溶液中置换出来(K、Ca、Na除外),在这些反应中也都有离子参加,因
此这些反应都属于离子反应。二氧化碳与生石灰的反应没有离子参加,不属于离子反应。
11.下列物质在水溶液中的电离方程式正确的是( )
A.氢氧化钡的电离方程式:Ba(OH) =Ba2++2OH-
2
B.硫酸铵的电离方程式:(NH )SO =2NH++SO2-
4 2 4 4 4
C.碳酸钾的电离方程式:KCO=K ++CO 2-
2 3 2 3
D.硫酸氢钾的电离方程式:KHSO=K++HSO -
4 4
【答案】B
【解析】氢氧化钡为二元碱,电离出的离子为 Ba2+、OH-,A错误;硫酸铵完全电离,离子方程式:
(NH )SO =2 NH ++ SO 2-,B正确;碳酸钾的电离方程式:KCO=2K++ CO2-,C错误;硫酸氢钾在水溶液中电
4 2 4 4 4 2 3 3
离出钾离子、硫酸根离子和氢离子,电离方程式:KHSO=K++H++ SO 2-,D错误。
4 4
12.有关电解质的说法正确的是( )
A.NaOH固体溶于水后能导电,所以NaOH是电解质
B.CO 水溶液能够导电,所以CO 是电解质
2 2
C.铜导电性很好,所以铜是电解质
D.FeCl 溶液能够导电,所以FeCl 溶液是电解质
3 3
【答案】A
【解析】A项,NaOH固体溶于水后电离出钠离子和氢氧根离子,离子自由移动可以导电,所以氢氧化钠
是电解质,A正确;B项,CO 溶于水能导电是因为CO 与水反应生成的HCO 为电解质,而CO 为非电解质,
2 2 2 3 2
B错误;C项,铜为单质,单质既不是电解质也不是非电解质,C错误;D项,氯化铁溶液为混合物,混合物
既不是电解质也不是非电解质,D错误;故选A。
13.下列说法正确的是( )
A.NaCl在电流的作用下可以电离出钠离子和氯离子
B.CO 溶于水能导电,CO 属于电解质
2 2C.熔融的NaOH属于电解质
D.HSO 属于电解质,在水溶液和熔融状态下可以导电
2 4
【答案】C
【解析】A项,NaCl在水溶液中自动电离出Na+、Cl−,不需要在电流的作用,故A错误;B项,CO 溶于
2
水生成的 HCO 才能发生电离,CO 属于非电解质,故B错误;C项,熔融的NaOH中存在自由移动的离子,
2 3 2
能导电,属于电解质,故C正确;D项,HSO 属于电解质,在水溶液中可以导电,但是HSO 为共价化合物,
2 4 2 4
在熔融状态下不能导电,故D错误。故选C。
14.(2022·江西省七校高三联考)室温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 KI溶液:Na+、K+、ClO-、OH-
B.使甲基橙呈黄色的溶液:NH +、Ba2+、Cl-、NO -
4 3
C.0.1 mol·L-1 Fe (SO ) 溶液:Cu2+、NH +、NO -、SO 2-
2 4 3 4 3 4
D.与铝反应产生大量氢气的溶液:Na+、K+、CO2-、SO 2-
3 4
【答案】C
【解析】A项,KI中的I-会与ClO-发生氧化反应而不能大量共存,A不符合题意;B项,使甲基橙呈黄色
的溶液显碱性,碱性溶液中NH +不能大量共存,B不符合题意;C项,0.1 mol·L-1 Fe (SO ) 溶液中,Cu2+、
4 2 4 3
NH +、NO -、 SO 2-相互不反应,可以大量共存,C符合题意;D项,与铝反应产生大量氢气的溶液可能是酸
4 3 4
性溶液,也可能是碱性溶液,而酸性溶液中CO2-不能大量共存,D不符合题意;故选C。
3
15.下列离子或分子在指定的分散系中一定能够大量共存的是( )
A.c(H+)=10-13 mol/L的溶液中:NO、SO、K+、Na+
B.含Fe3+的溶液中:Na+、K+、CHCOO-、HCO
3
C.铁与过量稀硫酸反应后的溶液中:AlO、NH、Cl-、NO
D.空气中:SO 、NO、N、NH
2 2 3
【答案】A
【解析】c(H+)=10-13 mol/L的溶液显碱性,离子能大量共存,A正确;Fe3+与HCO发生双水解,不能大
量存在,B错误;AlO在酸性环境中不能大量存在,C错误;SO 和NH 在空气中反应,不能大量共存,NO与
2 3
氧气反应,不能大量共存,D错误。
16.在溶液中加入足量NaO 后仍能大量共存的离子组是( )
2 2
A.NH、Ba2+、Cl-、NO B.K+、AlO、Cl-、SO
C.Ca2+、Mg2+、NO、HCO D.Na+、Cl-、SO、SO
【答案】B
【解析】NaO 与水反应生成氢氧化钠和氧气。在碱性溶液中NH不能大量存在,故A错误;K+、AlO、
2 2
Cl-、SO间不反应也不与氢氧化钠反应,故B正确;碱性溶液中,Mg2+、HCO不能大量存在,分别与OH-反
应生成氢氧化镁沉淀和CO,故C错误;SO具有还原性,能够被生成的氧气氧化,故D错误。17.下列指定反应的离子方程式正确的是( )
A.0.5 mol/L NaHSO 与0.5 mol/L Ba(OH) 混合至溶液呈中性:Ba2++OH-+SO+H+===BaSO ↓+HO
4 2 4 2
B.向NaSiO 溶液中通入过量SO :SiO+HO+SO ===H SiO↓+SO
2 3 2 2 2 2 3
C.向NaCO 溶液中滴加少量稀盐酸:CO+2H+===CO ↑+HO
2 3 2 2
D.NaHCO 溶液中加足量Ba(OH) 溶液:HCO+Ba2++OH-===BaCO ↓+HO
3 2 3 2
【答案】D
【解析】等浓度的NaHSO 与Ba(OH) 混合至溶液呈中性,正确的离子方程式为 2H++SO+Ba2++2OH-
4 2
===2H O+BaSO↓,故 A 不正确;向 NaSiO 溶液中通入过量 SO ,正确的离子方程式为 SiO+2SO +
2 4 2 3 2 2
2HO===H SiO↓+2HSO,故B不正确;向NaCO 溶液中滴加少量稀盐酸,正确的离子方程式为CO+H+
2 2 3 2 3
===HCO,故C不正确;少量NaHCO 定为 1 mol,以此来确定Ba2+和OH-各消耗1 mol,故D正确。
3
18.(2022·山东省济南市长清第一中学月考)某同学设计如下实验方案,以分离KCl和BaCl 两种固体混合
2
物。试回答下列问题:
(1)固体B的化学式为___________。
(2)该方案的明显失误是因某一个步骤设计不当而使分离产物不纯,该步骤是___________(填序号)。
(3)写出KCO 的电离方程式:______________________。
2 3
(4)写出②、④中对应反应的离子方程式:
②_________________________________,④_________________________________。
(5)检验固体B中是否含有氯离子的方法是_________________________________。
【答案】(1)BaCl (2)⑥ (3)K CO=2K++ CO2-
2 2 3 3
(4) Ba2++ CO2-=BaCO ↓ BaCO +2H+=Ba2++H O+CO↑
3 3 3 2 2
(5)取少量固体B,用适量蒸馏水溶解,向其中加入硝酸酸化的AgNO 溶液,若生成白色沉淀,证明其中
3
含Cl-
【解析】分离KCl和BaCl 两种固体混合物,可先溶于水,然后加入过量KCO 使BaCl 转化为A碳酸钡
2 2 3 2
沉淀,过滤后沉淀加入盐酸可生成BaCl 溶液,经⑤蒸发、结晶后可得B固体BaCl ,操作②所得滤液为KCl
2 2
和KCO 的混合物,应加入过量盐酸可得KCl,固体C为KCl;(1)氯化钾和氯化钡溶液中加入碳酸钾溶液可以
2 3
生成碳酸钡沉淀,则沉淀A为BaCO ;过滤后碳酸钡沉淀中加入盐酸可生成BaCl 溶液,经⑤蒸发、结晶后可
3 2
得B固体BaCl ;(2)蒸发结晶前应加入适量稀盐酸,将过量的碳酸钾转化成氯化钾,否则晶体不纯,故答案是
2
⑥;(3)K CO 为强电解质,完全电离,电离方程式为KCO=2K++ CO2-;(4)②加入碳酸钾生成碳酸钡沉淀,
2 3 2 3 3反应的离子方程式为Ba2++ CO2-═BaCO↓,④为碳酸钡和盐酸的反应,离子方程式为BaCO +2H+═Ba2+
3 3 3
+CO ↑+H O。(5)根据分析B固体BaCl ,取少量固体B,用适量蒸馏水溶解,向其中加入硝酸酸化的AgNO 溶
2 2 2 3
液,若生成白色沉淀,证明其中含Cl-。
19.(1)有一种“地康法”制取氯气的反应原理如下所示:
①反应I的离子方程式为________________________________。
②反应II属于____________反应。(填四种基本反应类型之一)
(2)有A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分
别是NO -、SO 2-、Cl-、CO2-中的一种(离子在物质中不重复出现)。
3 4 3
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
请回答下列问题:
①A的化学式为__________,B的化学式为__________ ,C的化学式为____________。
②写出D与足量CHCOOH溶液反应的离子方程式_______________________。
3
③写出A溶液中阴离子的检验方法_____________________________________。
【答案】(1)①CuO+2H+═Cu2++H O ②置换
2
(2)①BaCl AgNO CuSO
2 3 4
②CO2- +2CH COOH═2CH COO-+H O+CO↑
3 3 3 2 2
③取少量A溶液于试管中,向其中加入AgNO 溶液和稀硝酸,若产生白色沉淀,则含有Cl-
3
【解析】(1)①反应I为CuO与HCl反应生成水和氯化铜;②反应II中氧气与氯化铜反应生成氯气和
CuO;(2)给出八种离子,形成四种可溶性物质,这个可以通过一一组合的形式确定可能存在的物质,之后结合
进行实验和颜色限制进行继续排除,从而最终确定。如Ba2+不能和SO 2-、CO2-结合,而只能和NO -、Cl-;
4 3 3
Ag+不能和SO 2-、Cl-、CO2-三种离子结合,而只能和NO -结合,则一定是BaCl 、AgNO.Cu2+不能和CO2-结
4 3 3 2 3 3
合,所以为CuSO ;Na+对应CO2-为NaCO.即四种物质为BaCl 、AgNO、CuSO 、NaCO。①中由于C盐
4 3 2 3 2 3 4 2 3
是蓝色的,所以C为CuSO ;②四支试管加入盐酸,B有沉淀,则B溶液为AgNO;而D生成无色气体,则
4 3
为二氧化碳,即D为NaCO。(1)①反应I为CuO与HCl反应生成水和氯化铜,反应的离子方程式为:
2 3
CuO+2H+═Cu2++H O;②反应II中氧气与氯化铜反应生成氯气和CuO,该反应属于置换反应;(2)①由上述分
2
析可知A为BaCl ;B为AgNO,C为CuSO ;②D为NaCO,与醋酸反应生成二氧化碳气体,反应的离子方
2 3 4 2 3程式为CO2- +2CH COOH═2CH COO-+H O+CO↑;③A为BaCl ,检验氯离子的方法是取少量A溶液于试管
3 3 3 2 2 2
中,向其中加入AgNO 溶液和稀硝酸,若产生白色沉淀,则含有Cl-。
3
20.2023年是第三十一届“世界水日”。为了深人开展珍惜水、爱护水的主题活动,推进水资源的集约
安全利用,某校、化学兴趣小组的同学展开对我市某饮用水源水库水组成问题的研究,他们猜想该水库水中可
能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组实验:
①取适量该水库水于试管中,滴加过量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加过量的NaCO 溶液,又有白色沉淀生成:
2 3
③另取适量该水库水于试管中,滴加足量稀硝酸后再滴加AgNO 溶液,也产生白色沉淀。
3
请根据已有知识和反应事实回答以下问题:
(1)该小组有关大量存在___________ (填写离子符号)的猜想是错误的。
(2)通过实验可初步确定该水库水中___________(填“含有”或“不含有”)大量Ca+、Mg2+;判断依据的离
子方程式有___________。
(3)该水库水中所含阴离子可以确定有___________,理由是___________。
(4)确定实验②中滴加的NaCO 溶液已过量的检验方法是___________。
2 3
【答案】(1)Cu2+
(2)含有 Mg2++2OH-=Mg(OH) ↓,CO2-+Ca2+=CaCO ↓
2 3 3
(3)Cl- Cl-+Ag+=AgCl↓,AgCl不溶于稀硝酸
(4)取适量实验②反应后的上层清液于试管中,滴加足量盐酸,若产生无色气泡(或滴加CaCl 溶液,若产
2
生白色沉淀),证明NaCO 溶液已过量。
2 3
【解析】(1)①取适量该溶液于试管中,滴加足量的NaOH溶液,产生白色沉淀,说明原溶液中含有
Mg2+,没有铜离子,②过滤后取滤液于试管中,滴加足量的NaCO 溶液,又有白色沉淀生成,说明原溶液中
2 3
含有Ca2+,③另取适量该溶液于试管中,滴加足量稀硝酸后再滴加AgNO 溶液,也产生白色沉淀,说明原溶
3
液中含有Cl-,综上:原溶液中含有Ca2+、Mg2+、Cl-;没有Cu2+,则该小组有关大量存在Cu2+的猜想是错误的。
(2)根据①、②的现象,生成的白色沉淀是氢氧化镁和碳酸钙,可确定原溶液中含有Ca2+、Mg2+阳离子,反应
的离子方程式是:Mg2++2OH-=Mg(OH) ↓,CO2-+Ca2+=CaCO ↓;(3)滴加足量稀硝酸后再滴加AgNO 溶液,能
2 3 3 3
产生不溶于稀硝酸的白色沉淀AgCl,溶液中含有的离子是Cl-,原因是:Cl-+Ag+=AgCl↓,AgCl不溶于稀硝
酸;(4)Na CO 溶液能与盐酸反应放出气体,则确定实验②中滴加的NaCO 溶液已过量的检验方法是:取适量
2 3 2 3
实验②反应后的上层清液于试管中,滴加足量盐酸,若产生无色气泡(或滴加CaCl 溶液,若产生白色沉淀),
2
证明NaCO 溶液已过量。
2 31.(2023·天津市八校联考高三期中)下列反应的离子方程式书写正确的是( )
A.已知氧化性Cl>Br >Fe3+,向FeBr 溶液中通入少量的Cl:2Fe2++4Br-+3Cl=2Fe3++2Br +4Cl-
2 2 2 2 2 2
B.向澄清石灰水中加入Ca(HCO ) 溶液:Ca2++OH-+HCO-=CaCO ↓+H O
3 2 3 3 2
C.用醋酸除去水垢:2H++CaCO =Ca2++CO ↑+H O
3 2 2
D.向Ba(OH) 溶液中滴加NaHSO 溶液至混合溶液恰好为中性:Ba2++OH-+H++SO2-=BaSO ↓+H O
2 4 4 4 2
【答案】B
【解析】A项,已知氧化性Cl>Br >Fe3+,则还原性Fe2+>Br-,向FeBr 溶液中通入少量的Cl,发生反
2 2 2 2
应的离子方程式为:2Fe2++Cl=2Fe3++2Cl-,A错误;B项,向澄清石灰水中加入Ca(HCO ) 溶液,发生反应生
2 3 2
成CaCO 和水,离子方程式为:Ca2++OH-+ HCO -=CaCO ↓+H O,B正确;C项,醋酸为弱酸,保留化学式,
3 3 3 2
用醋酸除去水垢,离子方程式为2CHCOOH+CaCO =Ca2++2CH COO-+CO ↑+H O,C错误;D项,向Ba(OH)
3 3 3 2 2 2
溶液中滴加NaHSO 溶液至混合溶液恰好为中性,采用“以少定多”法,可设Ba(OH) 为1mol,需加入
4 2
NaHSO2mol,离子方程式为:Ba2++2OH-+2H++ SO 2-=BaSO ↓+2H O,D错误;故选B。
4 4 4 2
2.(2023·山西省吕梁市高三阶段性测试)宏观辨识和微观探析是化学学科的核心素养之一,下列指定反应
的离子方程式书写正确的是( )
A.向NaAlO 溶液中加入过量稀盐酸:AlO-+H++H O=Al(OH) ↓
2 2 2 3
B.向CaCl 溶液中通入CO:Ca2++H O+CO=CaCO ↓+2H+
2 2 2 2 3
C.KI溶液久置空气中变黄色:4I-+O +2H O=2I +4OH-
2 2 2
D.明矾[KAl(SO)•12H O]溶液中加入过量Ba(OH) 溶液:Al3++SO2-+Ba2++3OH-=Al(OH) ↓+BaSO ↓
4 2 2 2 4 3 4
【答案】C
【解析】A项,向NaAlO 溶液中加入过量稀盐酸AlO-+4H+ =Al3++2H O,故A错误;B项,碳酸的酸性
2 2 2
弱于盐酸,所以CO 与CaCl 溶液不反应,故B错误;C项,KI溶液久置空气中变黄色,由于碘离子被氧化成
2 2
碘单质:4I-+O +2H O=2I +4OH-,故C正确;D项,明矾KAl(SO )•12H O溶液中加入过量Ba(OH) 溶液,离
2 2 2 4 2 2 2
子方程式为:Al3++2SO2-+Ba2++4OH-=AlO -+2BaSO ↓+2H O,故D错误;故选C。
4 2 4 2
3.(2023·湖北省荆宜三校高三联考)下列反应的离子方程式书写错误的是( )
A.长期放置的 溶液出现黄色:4I-+O +2H O=2I +4OH-
2 2 2
B.饱和NaCO 溶液中通入过量CO:2Na++CO 2-+CO +H O=2NaHCO ↓
2 3 2 3 2 2 3
C.将少量溴水滴入过量NaSO 溶液中:Br +H O+SO 2-=2 Br-+2H++SO2-
2 3 2 2 3 4
D.向酸性KMnO 溶液中滴加HO 溶液:2MnO -+5H O+6H+=2Mn2++5O ↑+8H O
4 2 2 4 2 2 2 2
【答案】C【解析】A项,长期放置的KI溶液出现黄色,是空气中的氧气将碘离子氧化:4I-+O +2H O=2I +4OH-,A
2 2 2
正确;B项,饱和NaCO 溶液中通入过量CO 会生成碳酸氢钠:2Na++CO 2-+CO +H O=2NaHCO ↓,B正确;
2 3 2 3 2 2 3
C项,少量的溴水不能将所有的亚硫酸根氧化成硫酸根,故为Br +H O+3SO 2-=2 2Br-+2HSO -+SO2-,C错误;
2 2 3 3 4
D项,向酸性KMnO 溶液中滴加HO 溶液生成氧气:2MnO -+5H O+6H+=2Mn2++5O ↑+8H O,D正确;故选
4 2 2 4 2 2 2 2
C。
4.(2022·浙江省温州十校联合体高一期中)将Ba(OH) 溶液分为两等份放入烧杯中,分别向其中滴入
2
HSO 和NaHSO 溶液,两份溶液导电能力随滴入溶液体积变化的曲线如图。下列分析不正确的是( )
2 4 4
A.曲线②代表滴加NaHSO 溶液的变化曲线
4
B.b点之前,溶液中发生的离子反应方程式为Ba2++2OH-+2H++SO2-=BaSO ↓+2H O
4 4 2
C.a、c两点对应的溶液均为中性
D.曲线①说明浓度相同的稀硫酸导电能力强于稀Ba(OH) 溶液
2
【答案】B
【解析】Ba(OH) 溶液和HSO 、NaHSO 溶液反应方程式分别为HSO +Ba(OH) =BaSO ↓+2H O、
2 2 4 4 2 4 2 4 2
NaHSO+Ba(OH) =BaSO ↓+NaOH+HO,2NaHSO+Ba(OH) =BaSO ↓+Na SO +2H O,溶液导电能力与离子浓度
4 2 4 2 4 2 4 2 4 2
成正比,根据图知,曲线①在a点溶液导电能力接近0,说明该点溶液离子浓度最小,应该为Ba(OH) 溶液和
2
HSO 的反应,则曲线②为Ba(OH) 溶液和NaHSO 溶液的反应。A项,根据上述分析可知,曲线②代表滴加
2 4 2 4
NaHSO 溶液的变化曲线,A正确;B项,根据图知,a点为Ba(OH) 溶液和HSO 恰好反应,则b点溶液溶质
4 2 2 4
为NaOH,b点溶液中加入NaHSO 溶液时,实际上是酸碱中和反应,离子方程式为H++OH-=H O,B错误;C
4 2
项,a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;c点②中溶质为NaSO 溶液和水,都呈中性,C
2 4
正确;D项,曲线①中a点之前溶质为Ba(OH) ,过了a点后溶质为HSO ,浓度相同HSO 对应的点纵坐标更
2 2 4 2 4
大,导电能力更强,D正确;故选B。
5.(2022·河南省高三模拟预测)下列过程中的化学反应对应的离子方程式正确的是( )
A.用K[Fe(CN) ]溶液检测FeCl 溶液中的Fe2+:2[Fe(CN) ]3-+3Fe2+=Fe [Fe(CN) ]↓
3 6 2 6 3 6 2
B.向稀硫酸中加入少量金属铜:Cu +2H+= Cu 2++H ↑
2
C.用醋酸溶液处理水垢中的氢氧化镁:Mg(OH) +2H+= Mg2++2H O
2 2D.向(NH )Al(SO ) 溶液中滴加过量Ba(OH) 溶液:NH ++Al3++2SO2-+2Ba2++4OH-=2Al(OH) ↓+2BaSO ↓+
4 4 2 2 4 4 3 4
NH ·H O
3 2
【答案】A
【解析】A项,Fe2+与[Fe(CN) ]3-反应生成难溶物Fe [Fe(CN) ],A项正确;B项,铜与稀硫酸不反应,B
6 3 6 2
项错误;C项,醋酸是弱电解质,应写分子式,C项错误;D项,Ba(OH) 溶液过量时Al3+应转化为AlO-,D
2 2
项错误;故选A。
6.(2022·浙江省诸暨市教育研究中心高三选考诊断性考试)下列反应的离子方程式正确的是( )
A.碳酸氢铵溶液中滴加过量澄清石灰水:Ca(OH) +2HCO-=CaCO +2H O+ CO 2-
2 3 3 2 3
B.过量苯酚溶液与碳酸钠溶液反应:2 +CO →2 +H O+CO↑
2 2
C.印刷电路板反应原理:Fe3++Cu=Fe2++Cu2+
D.Mg(HCO ) 溶液与足量烧碱溶液反应:Mg2++2HCO-+4OH-=Mg(OH) ↓+2H O+2 CO2-
3 2 3 2 2 3
【答案】D
【解析】A项,向碳酸氢铵溶液中加入足量的澄清石灰水,设NH HCO 的物质的量为1mol则
4 3
1molNH +和1molHCO -,需要消耗2molOH-和1molCa2+,故离子方程式为:NH ++Ca2++2OH-+HCO-
4 3 4 3
=CaCO ↓+H O+NH ·H O,A错误;B项,酸性:HCO>苯酚>HCO-无论碳酸钠是否过量,苯酚溶液与碳酸钠
3 2 3 2 2 3 3
溶液反应都生成苯酚钠和碳酸氢钠,离子方程式为 +CO 2-→HCO -+ ,B错误;C项,
3 3
腐蚀印刷电路板生成氯化亚铁和氯化铜,离子方程式为:2Fe3++Cu=2Fe2++Cu2+,C错误;D项,Mg (HCO ) 溶
3 2
波与足量NaOH溶液反应生成氢氧化镁沉淀,其离子方程式为:Mg2++2HCO-+4OH-
3
=Mg(OH) ↓+2H O+2CO2-,D正确;故选D。
2 2 3
7.(2022·浙江省余姚市高三选考适应性考试)能正确表示下列变化的离子方程式是( )
A.KHSO 溶液中滴入Ba(OH) 溶液至中性:H++ SO 2-+Ba2++OH- = BaSO↓+H O
4 2 4 4 2
B.CuC1 溶液与过量氨水反应:Cu2++2NH ·H O=Cu(OH) ↓+2NH+
2 3 2 2 4
C.KMnO 溶液滴入KOH溶液中微热,得到透明的绿色溶液KMnO :4 MnO-+4OH- 4 MnO2-
4 2 4 4 4
+O ↑+2H O
2 2
D.NH Al(SO ) 溶液中滴入少量NaOH溶液: NH ++OHˉ= NH·H O
4 4 2 4 3 2
【答案】C
【解析】A项,KHSO 溶液中滴入Ba(OH) 溶液至中性,反应生成硫酸钡沉淀、硫酸钾和水,反应的离子
4 2
方程式为:2H++ SO 2-+Ba2++2OH- = BaSO↓+2H O,A错误;B项,CuC1 溶液与过量氨水反应生成四氨合硫酸
4 4 2 2铜和水,反应的离子方程式为:Cu2++4NH ·H O=[Cu(NH )]2++4H O,B错误;C项,KMnO 溶液滴入KOH
3 2 3 4 2 4
溶液中微热,得到透明的绿色溶液KMnO ,同时生成氧气和水,反应的离子方程式为:4 MnO-+4OH-
2 4 4
4MnO 2-+O ↑+2H O,C正确;D项,NH Al(SO ) 溶液中滴入少量NaOH溶液,氢氧根离子先与铝离子反应生
4 2 2 4 4 2
成氢氧化铝,反应的离子方程式为: Al3++3OHˉ= Al(OH) ↓,D错误;故选C。
3
8.(2022·河北省衡水市场高三化学调研)下列离子方程式书写不正确的是( )
A.向一定体积明矾溶液中滴加Ba(OH) 溶液,使硫酸根离子浓度降低到最小时:Al3++2SO2-+2Ba2++4OH-
2 4
=2BaSO ↓+AlO -+2H O
4 2 2
B.在硫酸酸化的KMnO 溶液中滴入双氧水,溶液褪色:2KMnO +5H O+6H+=2Mn2++5O ↑+8H O
4 4 2 2 2 2
C.向碘化亚铁溶液中滴加少量稀硝酸:2NO -+ 3Fe2++4H+=3Fe3++2NO↑+2HO
3 2
D.已知酸性的强弱:HCO>HCN>HCO -,则向NaCN溶液中通入少量CO 时,CN-
2 3 3 2
+CO +H O=HCN+HCO-
2 2 3
【答案】C
【解析】A项,向明矾溶液中滴加Ba(OH) 溶液,使硫酸根离子浓度降低到最小时,依据KAl (SO ) 组成
2 4 2
可知若2单位SO 2-完全反应需要2个单位Ba(OH) ,即提供4个单位OH-此时1个单位Al3+完全转化为AlO-,
4 2 2
A正确;B项,在硫酸酸化的KMnO 溶液中滴入双氧水,溶液褪色,此时KMnO 作氧化剂,HO 作还原剂,
4 4 2 2
根据电子得失数目相等,其离子方程式为2KMnO +5H O+6H+=2Mn2++5O ↑+8H O,B正确;C项,还原性I-
4 2 2 2 2
>Fe2+,向碘化亚铁溶液中滴加少量稀硝酸,I-与稀硝酸发生氧化还原反应,而不是Fe2+,离子方程式为:2NO -
3
+6I-+8H+=3I +2NO↑+4HO,C错误;D项,因为酸性的强弱顺序:HCO>HCN>HCO -,则向NaCN溶液中
2 2 2 3 3
通入少量的CO 时应该生成HCN和HCO -,离子方程式为:CN-+CO +H O=HCN+HCO-,D正确;故选C。
2 3 2 2 3
9.(2022·湖南省五市十校教研教改共同体高三联考)宏观辨识和微观探析是化学学科核心素养之一,下列
物质性质实验对应的反应方程式书写不正确的是( )
A.NaO 放入水中:2NaO+2H O= 4NaOH+O↑
2 2 2 2 2 2
B.向苯酚钠溶液中通入少量CO:C HONa+H O+CO→C HOH+NaHCO
2 6 5 2 2 6 5 3
C.用碳酸钠溶液处理水垢中的硫酸钙:CaSO+CO 2- CaCO + SO 2--
4 3 3 4
D.向0.1mol·L-1NaAlO 溶液中加入NaHCO 溶液:AlO-+HCO-+H O=Al(OH) ↓+CO ↑
2 3 2 3 2 3 2
【答案】D
【解析】A项,过氧化钠与水反应生成氢氧化钠和氧气,反应的化学方程式为2NaO+2H O=
2 2 2
4NaOH+O ↑,故A正确;B项,苯酚钠溶液与少量二氧化碳反应生成苯酚和碳酸氢钠,反应的化学方程式为
2
C HONa+H O+CO→C HOH+NaHCO,故B正确;C项,硫酸钙的溶度积大于碳酸钙的溶度积,水垢中的硫
6 5 2 2 6 5 3
酸钙能与碳酸钠溶液反应生成碳酸钙和硫酸钠,转化的离子方程式为CaSO+CO 2- CaCO + SO 2-- ,故C
4 3 3 4
正确;D项,偏铝酸钠溶液与碳酸氢钠溶液反应生成氢氧化铝沉淀和碳酸钠,反应的离子方程式为AlO-
2+HCO-+H O=Al(OH) ↓+CO 2-,故D错误;故选D。
3 2 3 3
10.(2022·上海市控江中学高三月考)少量氯水滴加到含NaI和NaSO 混合溶液中,下列离子方程式不正
2 3
确的是( )
A.Cl+ SO 2-+ H O =2Cl- + SO 2-+ 2H+
2 3 2 4
B.Cl+2I-=2Cl- + I
2 2
C.2Cl+2I- + SO 2-+H O=4Cl- +I + SO 2-+ 2H+
2 3 2 2 4
D.Cl+3 SO 2-+H O=2Cl-+ SO 2-+ 2 HSO -
2 3 2 4 3
【答案】B
【解析】A项,向NaSO 、NaI的混合溶液中滴加少量氯水,首先氧化亚硫酸根离子,若只氧化亚硫酸根
2 3
离子,反应的离子方程式可以为:SO 2-+Cl+H O═SO2-+2H++2Cl-,A正确;B项,向NaSO 、NaI的混合溶液
3 2 2 4 2 3
中滴加少量氯水,首先氧化亚硫酸根离子,不可能只发生2I-+Cl=2Cl-+I ,B不正确;C项,向NaSO 、NaI的
2 2 2 3
混合溶液中滴加少量氯水,首先氧化亚硫酸根离子,若亚硫酸根离子完全反应后,氯气剩余,可以再氧化碘离
子,可能发生2Cl+2I-+ SO 2-+H O=4Cl-+ SO 2-+2H++I ,C正确;D项,向NaSO 、NaI的混合溶液中滴加少量
2 3 2 4 2 2 3
氯水,首先氧化亚硫酸根离子,若反应后NaSO 过量,则可能发生Cl+3 SO 2-+H O=2Cl-+ SO 2-+2 HSO -,D
2 3 2 3 2 4 3
正确。故选B。
11.(2022·山东省胶州市教育体育局教学研究室高三期中)某溶液只含有 、 、SO 2-、CO2-、 中的
4 3
几种。取样,滴加KSCN溶液后显血红色。下列有关该溶液的说法错误的是( )
A.一定存在的离子为 、SO 2- B.一定不存在的离子为CO2-、
4 3
C.不能确定的离子为 、SO 2- D.需要经过焰色试验确定是否含有
4
【答案】C
【解析】取样,滴加KSCN溶液后显血红色,则溶液中一定存在Fe3+溶液中一-定不存在与Fe3+反应的
CO2-、I-;根据溶液电中性可知,溶液中一定存在SO 2-,不能确定是否含有钾离子,是否含有K+离子需要经
3 4
过焰色反应。A项,溶液中一定存在Fe3+、SO 2-,A正确;B项,溶液中一定存在Fe3+,溶液中一定不存在与
4
Fe3+反应的CO2-、I-,B正确;C项,溶液中一定含有SO 2-, C错误;D项,无法确定是否含有钾离子,若确
3 4
定是否含有K+离子需要经过焰色反应,D正确;故选 C。
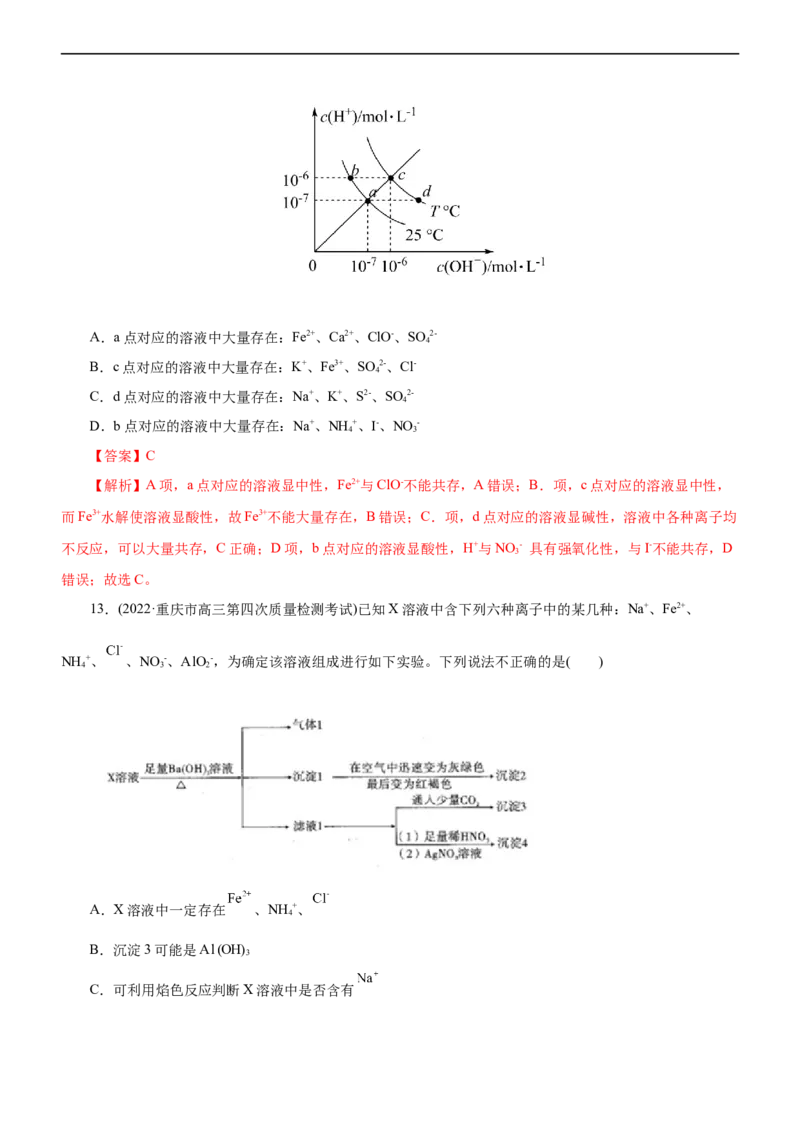
12.(2022·江西省赣州市十六县市十七校高三联考)在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关
系。下列关于离子共存的说法中正确的是( )A.a点对应的溶液中大量存在:Fe2+、Ca2+、ClO-、SO 2-
4
B.c点对应的溶液中大量存在:K+、Fe3+、SO 2-、Cl-
4
C.d点对应的溶液中大量存在:Na+、K+、S2-、SO 2-
4
D.b点对应的溶液中大量存在:Na+、NH +、I-、NO -
4 3
【答案】C
【解析】A项,a点对应的溶液显中性,Fe2+与ClO-不能共存,A错误;B.项,c点对应的溶液显中性,
而Fe3+水解使溶液显酸性,故Fe3+不能大量存在,B错误;C.项,d点对应的溶液显碱性,溶液中各种离子均
不反应,可以大量共存,C正确;D项,b点对应的溶液显酸性,H+与NO - 具有强氧化性,与I-不能共存,D
3
错误;故选C。
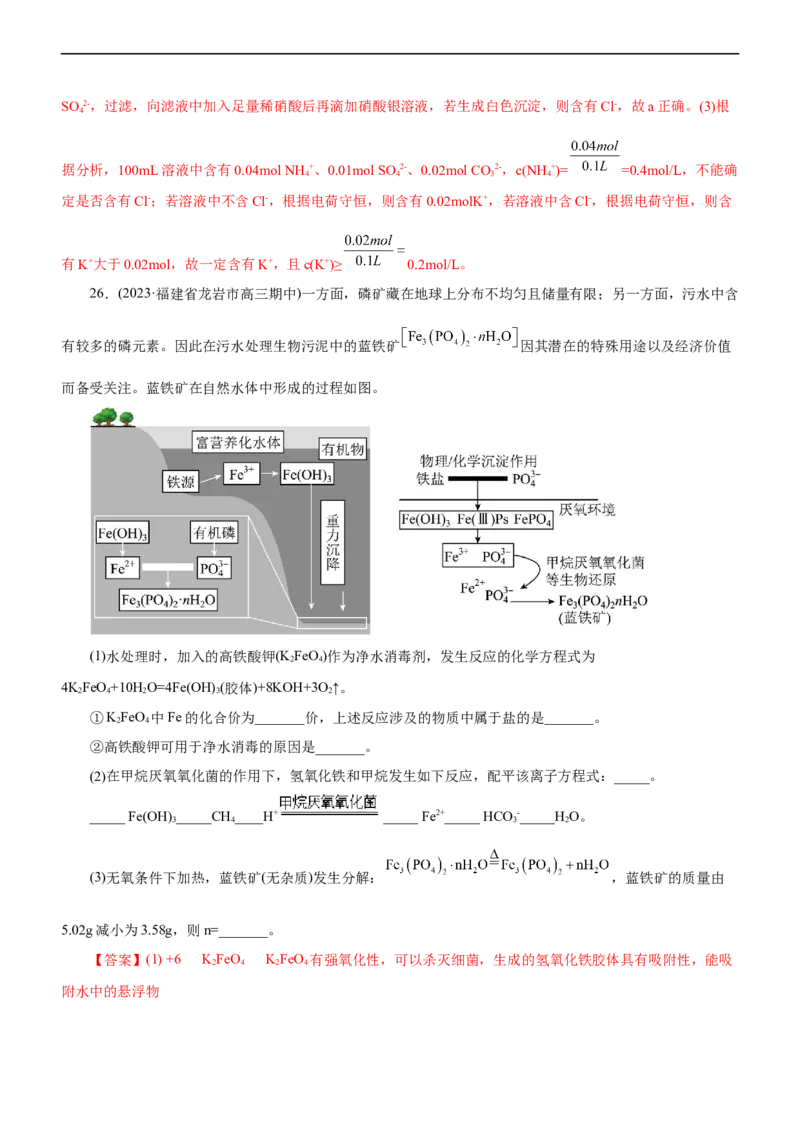
13.(2022·重庆市高三第四次质量检测考试)已知X溶液中含下列六种离子中的某几种:Na+、Fe2+、
NH +、 、NO -、A lO -,为确定该溶液组成进行如下实验。下列说法不正确的是( )
4 3 2
A.X溶液中一定存在 、NH +、
4
B.沉淀3可能是A l (OH)
3
C.可利用焰色反应判断X溶液中是否含有D.无法确定X溶液中是否含有NO -
3
【答案】B
【解析】加碱并加热产生气体,说明X溶液有NH +;加碱出现沉淀,且沉淀迅速变灰绿色,最后变红褐
4
色沉淀,所以沉淀2为Fe(OH) ,沉淀1为Fe(OH) ,说明X溶液中有Fe2+;NH +及Fe2+存在的情况下,A lO -不
3 2 4 2
会存在;硝酸及硝酸银加入出现沉淀,是用以证明卤素离子(Cl-、Br-、I-)的方法,再根据题干信息,说明X溶
液中有Cl-。A项,根据题干实验现象描述及分析,描述正确,不符题意;B项,根据分析,X溶液中不存在A
lO -,所以最终沉淀不会有Al(OH) 成分,描述错误,符合题意;C项,Na+的检验手段是焰色反应,观察灼烧
2 3
药品对应焰色,证明X溶液中是否有Na+,描述正确,不符题意;D项,以上几步实验操作,未能测定出气体
或沉底中有NO -,描述正确,不符题意;故选B。
3
14.(2022·山东省威海市文登区教育教学研究培训中心高三期中)某水溶液中只可能含有下列离子中的若干
种:K+、Mg2+、Ca2+、Ba2+、NH +、Cl−、NO -、SO 2-和CO2-。现每次取10 mL进行实验:
4 3 4 3
①第一份加入足量NaOH后加热,收集到气体1.12L(标准状况下)。
②第二份加入足量BaCl 溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g。下列说法错
2
误的是( )
A.原溶液中一定不含有Mg2+、Ba2+、Ca2+
B.无法确定原溶液中是否含有Cl−和NO -
3
C.原溶液中一定含有SO 2-和CO2-,且浓度分别为1.00 mol·L−1、2.00 mol·L−1
4 3
D.要判断原溶液中是否含有K+,需再做焰色试验确定
【答案】D
【解析】根据实验①现象可知气体为氨气,则含有NH +,且铵根的物质的量为
4
,该溶液中不含Mg2+;根据实验②现象判断,该溶液中含有SO 2-和CO2-,干燥后
4 3
剩余2.33g为BaSO 质量,计算出硫酸根的物质的量为: ,碳酸根的物质的量为:
4
;由于SO 2-和CO2-与Ca2+、Ba2+不共存,则溶液中一定不含有Ca2+、Ba2+;由溶
4 3
液呈电中性,已知一定存在的阳离子的物质的量为0.05×1=0.05mol,阴离子为0.01mol×2+0.02mol×2=0.06mol,则一定存在K+,Cl−、NO -不能确定。 A项,依据以上分析可知,原溶液中一
3
定不含有Mg2+、Ba2+、Ca2+,故A正确;B项,依据以上分析可知,无法确定原溶液中是否含有Cl−和NO -,
3
故B正确;C项,原溶液中一定含有SO 2-和CO2-,且浓度分别为 、
4 3
,故C正确;D项,由溶液呈电中性,已知一定存在的阳离子的物质的量为
0.05×1=0.05mol,阴离子为0.01mol×2+0.02mol×2=0.06mol,则一定存在K+,故D错误;故选D。
15.(2022·辽宁省大连八中高三期中)溶液X中含有下表离子中的某5种,且其浓度均为 (不考
虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有
变化。下列叙述不正确的是( )
阳离子 阴离子
、Fe3+、 、Fe2+、Mg2+、Al3+ OH-、NO -、HCO -、CO2-、SO 2-、Cl-
3 3 3 4
A.X溶液中含有2种阳离子和3种阴离子
B.X溶液中不可能含有HCO -或CO2-
3 3
C.生成的无色气体是NO
D.根据电荷守恒,原溶液中一定含
【答案】D
【解析】根据共存,OH-不能与Fe3+、Al3+、Fe2+、Ca2+、Mg2+、HCO -大量共存;HCO -不能与OH-、Fe3+、
3 3
Al3+大量共存;CO2-不能与Fe3+、Al3+、Fe2+、Ca2+、Mg2+大量共存;向X溶液中加入足量的稀盐酸,阴离子种
3
类没有发生改变,说明X溶液中含有Cl-,加入稀盐酸有无色气体产生,该气体不能是CO,气体如果是
2
CO,则X溶液中含有CO2-或HCO -,X溶液与足量的稀盐酸反应,导致阴离子种类减少,因此无色气体为
2 3 3
NO,X溶液中含有NO -,NO -在酸中具有强氧化性,转化成NO,X溶液中应含有还原性离子,即Fe2+,X溶
3 3
液中有5种离子,X溶液中离子浓度均为0.1mol/L,溶液呈电中性,另外两种为Mg2+和SO 2-。A项,含有的
4
离子是NO -、Fe2+、Cl-、Mg2+、SO 2-,三种阴离子和两种阳离子,故A说法正确;B项,X溶液中一定不含有
3 4
HCO -或CO2-,故B说法正确;C项,无色气体为NO,故C说法正确;D项,X溶液中有SO 2-,能与Ca2+反
3 3 4
应生成硫酸钙沉淀,因此X溶液中一定不含有Ca2+,故D说法错误;故选D。
16.(2022·江苏省海安市高三期中考试)以菱镁矿(主要成分为MgCO ,含少量FeCO)为原料制备高纯氧化
3 3
镁的实验流程如图,下列说法不正确的是( )A.酸溶时适当增大硫酸浓度可提高反应速率
B.MgCO 与稀硫酸反应的离子方程式为CO2-+2H+= CO↑+H O
3 3 2 2
C.“氧化”后的溶液中大量存在Mg2+、Fe3+、H+、SO 2-
4
D.滤渣2的主要成分是Fe(OH)
3
【答案】B
【解析】菱镁矿的主要成分为MgCO ,少量FeCO 及部分难溶于酸的杂质,加硫酸时MgCO 和FeCO 溶
3 3 3 3
解得到MgSO 和FeSO 的混合溶液,过滤,滤去不溶于酸的杂质,向滤液中加双氧水,氧化Fe2+生成Fe3+,再
4 4
加氨水调pH至4,使Fe3+完全沉淀,过滤掉Fe(OH) 沉淀,将滤液(MgSO 溶液)经一系列转化得到MgSO ,再
3 4 4
与碳在高温煅烧下得到MgO。A项,矿石粉碎可以增大矿石与酸液的接触面积,可以加快反应的速率、增大
酸的浓度,也可以加快反应速率,故A正确;B项,MgCO 为难溶性盐,离子方程式中不能拆写,故B错误;
3
C项,向滤液中加双氧水,氧化Fe2+生成Fe3+,故“氧化”后的溶液中大量存在Mg2+、Fe3+、H+、SO 2-,故C
4
正确;D项,加入氨水调节溶液pH为4,Fe3+完全转化为Fe(OH) 沉淀,滤渣2的成分是Fe(OH) ,故D正确;
3 3
故选B。
17.(2022·江西省景德镇一模)无色溶液中可能含有Na+、K+、NH +、Ca2+、Cu2+、SO 2-、SO 2-、Cl-、Br-、
4 4 3
CO2-中的若干种,离子的物质的量浓度都为0.1 mol/L。往该溶液中加入过量的BaCl 和盐酸的混合溶液,无白
3 2
色沉淀生成。某同学另取少量原溶液,设计并完成如图所示实验,则下列关于原溶液的判断正确的是( )
A.无法确定原溶液中是否存在Cl-
B.肯定存在的离子是SO 2-、Br-,是否存在Na+、K+需要通过焰色反应来确定
3
C.肯定不存在的离子是Ca2+、Cu2+、SO 2-、CO2-,是否含NH +另需实验验证
4 3 4
D.若步骤中Ba(NO ) 和HNO 的混合溶液改用BaCl 和盐酸的混合溶液,则对溶液中离子的判断无影响
3 2 3 2
【答案】D【解析】无色溶液中一定不含蓝色Cu2+,往该溶液中加入过量的BaCl 和盐酸的混合溶液,无白色沉淀生
2
成,无SO 2-,加足量氯水,无气体,则无CO2-,溶液加四氯化碳分液,下层橙色,则有Br-,上层加硝酸钡和
4 3
稀硝酸有白色沉淀,有SO 2-,无Mg2+,溶液中一定含阳离子,且离子浓度都为0.1 mol/L,根据电荷守恒,一
3
定含有NH +、Na+、 K+,一定不存在Cl-,滤液中加硝酸酸化的硝酸银有白色沉淀,是过程中加氯水时引入的
4
氯离子,结合溶液为电中性来解答。A项,根据题目中浓度都相等,利用电荷守恒可以判断出是否有氯离子,
A错误;B项,肯定存在的离子是SO 2-、Br-、NH +、Na+、K+,B错误;C项,根据电荷守恒可以判断出溶液
3 4
中有NH +离子,C错误;D项,注意检验是否有SO 2-,根据BaSO 不溶于酸的特点进行判断,溶液中已含有
4 4 4
Cl-,所以对溶液中Cl-的判断无影响,D正确;故选D。
18.(2022·江苏省连云港市高三期中)Na CO 和NaHCO 混合溶液具有控制酸碱平衡的作用。室温下,通
2 3 3
过下列实验探究一定浓度的NaCO 和NaHCO 混合溶液的性质。
2 3 3
实验1:向混合溶液中滴几滴酚酞,溶液显红色;
实验2:向实验1所得溶液中滴加几滴稀盐酸,溶液红色变浅;
实验3:向混合溶液中通入过量的CO,无明显现象;
2
实验4:向实验3所得溶液中滴加少量Ba(OH) 溶液,产生白色沉淀。
2
下列有关说法正确的是( )
A.实验1中溶液显红色的主要原因是:CO2-+2H O HCO+2OH-
3 2 2 3
B.实验2中溶液红色变浅的原因是:HCO -+ H+= H O+CO↑
3 2 2
C.实验3中无明显现象说明没有发生化学反应
D.实验4中产生白色沉淀的原因是:2 HCO-+Ba2++2OH- = 2H O + CO 2-+BaCO ↓
3 2 3 3
【答案】D
【解析】A项,实验1中溶液显红色的主要原因是碳酸钠水解能力强:CO2-+H O HCO -+OH-,故
3 2 3
A错误;B项,实验2中溶液红色变浅的原因是碳酸钠更易与酸反应:CO2-+ H+= HCO -,故B错误;C项,试
3 3
验3中发生了反应CO+ Na CO+H O=2NaHCO ,故C错误;D项,实验4中氢氧化钡和碳酸氢钠反应的离子
2 2 3 2 3
方程为2 HCO-+Ba2++2OH- = 2H O + CO 2-+BaCO ↓,故D正确;故选D。
3 2 3 3
19.(2022·福建师大附中高三期中)某无色溶液中可能含有Na+、K+、NH +、Mg2+、Cu2+、SO 2-、SO 2-、
4 4 3
Cl-、Br-、CO2-中的若干种,离子浓度均为0.1 mol·L-1,往溶液中加入过量的BaCl 和盐酸的混合溶液,无白色
3 2
沉淀生成。某同学另取少量原溶液,设计并完成如下实验:则关于原溶液的判断正确的是( )
A.无法确定原溶液中是否存在Cl-
B.肯定存在的离子是SO 2-、Br-,是否存在Na+、K+需要通过焰色反应来确定
3
C.若把Ba(NO ) 和HNO 溶液改为BaCl 和盐酸的混合溶液,则对溶液中离子的判断无影响
3 2 3 2
D.肯定不存在的离子是Mg2+、Cu2+、SO 2-、CO2-,是否含NH 另需实验验证
4 3
【答案】C
【解析】无色溶液中一定不含Cu2+,往该溶液中加入过量的BaCl 和盐酸的混合溶液,无白色沉淀生成,
2
无SO 2-,加足量氯水,无气体,则无CO2-,溶液加四氯化碳分液,下层橙色,则有Br-,上层加硝酸钡和稀硝
4 3
酸有白色沉淀,有SO 2-,无Mg2+,溶液中一定含阳离子,且离子浓度都为0.1mol·L-1,根据电荷守恒,一定
3
含有NH +、Na+、K+,一定不存在Cl-,滤液中加硝酸酸化的硝酸银有白色沉淀,是过程中加氯水时引入的氯
4
离子。A项,由以上分析可知一定不存在Cl-,故A错误;B项,肯定存在的离子为:SO 2-、Br-,离子浓度都
3
为0.1mol·L-1,根据溶液电中性可知原溶液中有Na+、K+,无需用焰色反应检验,故B错误;C项,加入
Ba(NO ) 和HNO 溶液目的是检验硫酸根离子,若改用BaCl 和盐酸的混合溶液,对溶液中离子的判断无影响,
3 2 3 2
故C正确;D项,肯定不存在的离子是Mg2+、Cu2+、SO 2-、CO2-,一定含NH +,故D错误;故选C。
4 3 4
20.(2022·江苏省如皋市高三期中调研)实验室利用废弃旧电池的铜帽(主要成分为锌铜合金)回收Cu并制
备ZnCl 的部分实验过程如图所示。下列说法正确的是( )
2
A.“溶解”时Cu发生反应的离子方程式为Cu+HO+2HCl=Cu2++2HO+2Cl-
2 2 2
B.因为升高温度可以加快反应速率,所以“溶解”时适宜使用高温
C.“调节pH=2”后,溶液中大量存在的离子有Cu2+、Zn2+、H+、Cl-
D.将ZnCl 溶液加热蒸干即可获得无水ZnCl
2 2
【答案】C
【解析】废弃旧电池的铜帽(主要成分为锌铜合金)回收Cu并制备ZnCl 的部分实验过程中,先加入双氧水、
2
稀盐酸,Zn转化为ZnCl,Cu转化为CuCl ,所得溶液中存在大量Zn2+、Cu2+、Cl-、H+,向溶液中加入适量
2 2
NaOH溶液调节pH=2,此时溶液中含有大量Zn2+、Cu2+、Na+、Cl-、H+,再加入锌粉将Cu2+置换为Cu,过滤得
到Cu,所得滤液中主要成分为NaCl、ZnCl,经过一系列操作后得到无水ZnCl。A项,HCl为易溶强酸,离
2 2
子方程式中应拆分,因此“溶解”时Cu发生反应的离子方程式为Cu+HO+2H+=Cu2++2HO,故A错误;
2 2 2
B项,升高温度能够加快化学反应速率,但双氧水受热易分解、盐酸受热易挥发,因此溶解过程中需在适宜的温度下进行反应,故B错误;C项, “调节pH=2”后,溶液中大量存在的离子有Cu2+、Zn2+、H+、Cl-,故C
正确;D项,ZnCl 为强酸弱碱盐,加热能够促进Zn2+水解,因此需要在HCl的气氛中进行加热蒸干方可得到
2
无水ZnCl,故D错误;故选C。
2
21.(2022·山东省滕州市高三期中联考)某溶液中只可能含有K+、NH +、Fe2+、Al3+、Cl−、SO 2-、CO2-、
4 4 3
[Al(OH) ]-中的若干种离子,离子浓度均为0.1mol/L,已知:稀HNO 可与Fe2+发生氧化还原反应产生NO气体,
4 3
Fe2+被氧化为 ,某同学进行了如下实验,下列说法正确的是( )
A.无法确定原试液中是否含有Al3+、、Cl−
B.滤液X中大量存在的阳离子有NH +、Fe2+和Ba2+
4
C.确定某溶液中存在的离子为NH +、Fe2+、Cl−、SO 2-
4 4
D.无法确定沉淀C的成分
【答案】C
【解析】加入过量稀硫酸无明显现象,说明无CO2-、[Al(OH) ]-;加入过量Ba(NO ) 有气体生成,说明有
3 4 3 2
Fe2+存在,且被氧化,沉淀为硫酸钡,说明有SO 2-存在;加入过量NaOH有气体生成,说明存在NH +,气体
4 4
为氨气,沉淀B为氢氧化铁沉淀;滤液中通入少量CO 产生沉淀,先与OH-、Ba2+反应,沉淀C中一定含碳酸
2
钡;因为存在离子浓度均为0.1mol/L,根据溶液呈电中性,只能含有NH +、Fe2+、Cl−、SO 2-才能保证电荷守恒,
4 4
K+、Al3+不能存在。A项,溶液中一定含有Cl-,一定不含Al3+,故A错误;B项,加入过量Ba(NO ) 溶液,溶
3 2
液中的H+、Fe2+与NO -发生氧化还原反应,Fe2+被氧化为Fe3+,因此滤液X中大量存在的阳离子有NH +、
3 4
Fe3+和Ba2+,故B错误;C项,原溶液中存在的离子为Cl-,故C正确;D项,排除Al3+、[Al(OH) ]-存在的可能,
4
所以向滤液中通入少量CO 产生的沉淀C为碳酸钡,故D错误;故选C。
2
22.(2022·山东省泰安教育发展中心高三期中联考)某学习兴趣小组拟对溶液A的成分进行分析,溶液A
中可能含有如下离子:Na+、NH +、Ba2+、Mg2+、SO 2-、 SO 2-、Cl-、OH-,设计并完成了如下的试验,下列说
4 4 3
法不正确的是( )A.气体E的体积是224mL
B.气体F能使湿润的红色石蕊试纸变蓝
C.溶液A中一定存在Na+、NH +、 SO 2-、 SO 2-
4 4 3
D.溶液A中可能存在Cl-,且c(Na+)≤0.20 mol·L-1
【答案】D
【解析】溶液A加入过量氯化钡溶液生成沉淀B质量为4.50g沉淀,且沉淀部分溶解于稀盐酸,说明原来
有SO 2-,则原溶液中没有Mg2+、Ba2+,沉淀没有完全溶解,说明原溶液中有SO 2-,且BaSO 的质量为2.33g,
3 4 4
则说明原溶液中 SO 2-的物质的量为0.01mol,BaSO 的质量为450g-2.33g=2.17g,则SO 2-的物质的量为
4 3 3
0.01mol,溶液加入NaOH溶液生成448mL气体,为氨气, ,说明含有
0.02molNH +,则阴离子的电荷总数为2n(SO 2-+2n( SO 2-)=2×0.01mol+2×0.01mol=0.04mol,则阳离子的电荷总
4 3 4
数为n NH+=0.02mol,0.04mol>0.02mol根据电荷守恒溶液中肯定存在其它阳离子,故存在Na+。A项,盐酸足
4
量时:BaSO+2HCl=BaCl +H O+SO ,BaSO 的质量为450g-2.33g=2.17g,气体E为二氧化硫,其物质的量为:
3 2 2 2 3
0.1mol,体积是224mL,A正确;B项,溶液加入NaOH溶液生成448mL气体,F为氨气,能使湿润的红色石
蕊试纸变蓝,B正确;C项,溶液A中一定存在Na+、NH +、SO 2-、SO 2-,C正确;D项,溶液A中可能存在
4 4 3
Cl-,则阴离子的电荷总数为: +n(Cl-),阳离子的电荷
总数为:n(NH )+n(Na+)=0.02mol+n(Na+),根据电荷守恒: ,则
,则 ,c(Na+) 0.20 mol ,D错误;故选D。
23.已知还原性:SO>I-。向含a mol KI和a mol K SO 的混合液中通入b mol Cl 充分反应(不考虑Cl 与
2 3 2 2
I 之间的反应)。下列说法不正确的是( )
2
A.当a≥b时,发生的离子反应为SO+Cl+HO===SO+2H++2Cl-
2 2
B.当5a=4b时,发生的离子反应为4SO+2I-+5Cl+4HO===4SO+I+8H++10Cl-
2 2 2C.当a≤b≤a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol
D.当a