文档内容
备战2025年高考化学【二轮·突破提升】专题复习讲义
专题06 氧化还原反应概念、规律及应用
讲义包含四部分:把握命题方向►精选高考真题►高效解题策略►各地最新模拟
氧化还原反应是高考的必考内容,从考查内容上看:
(1)借助STSE型试题判断指定反应是否是氧化还原反应;
(2)氧化还原反应中电子的转移数目在N 题目中是命题的热点;
A
(3)物质氧化性、还原性的强弱常与离子方程式正误判断融合考查;
(4)在工艺流程题中常常涉及陌生氧化还原方程式的书写;
(5)在工艺流程题、综合实验题中涉及氧化还原反应的综合计算;
预测2025年高考仍可能在选择题中结合生产、生活,考查氧化还原反应的判断、氧化还原反应的概念
及相互关系、简单计算等,应予以关注。
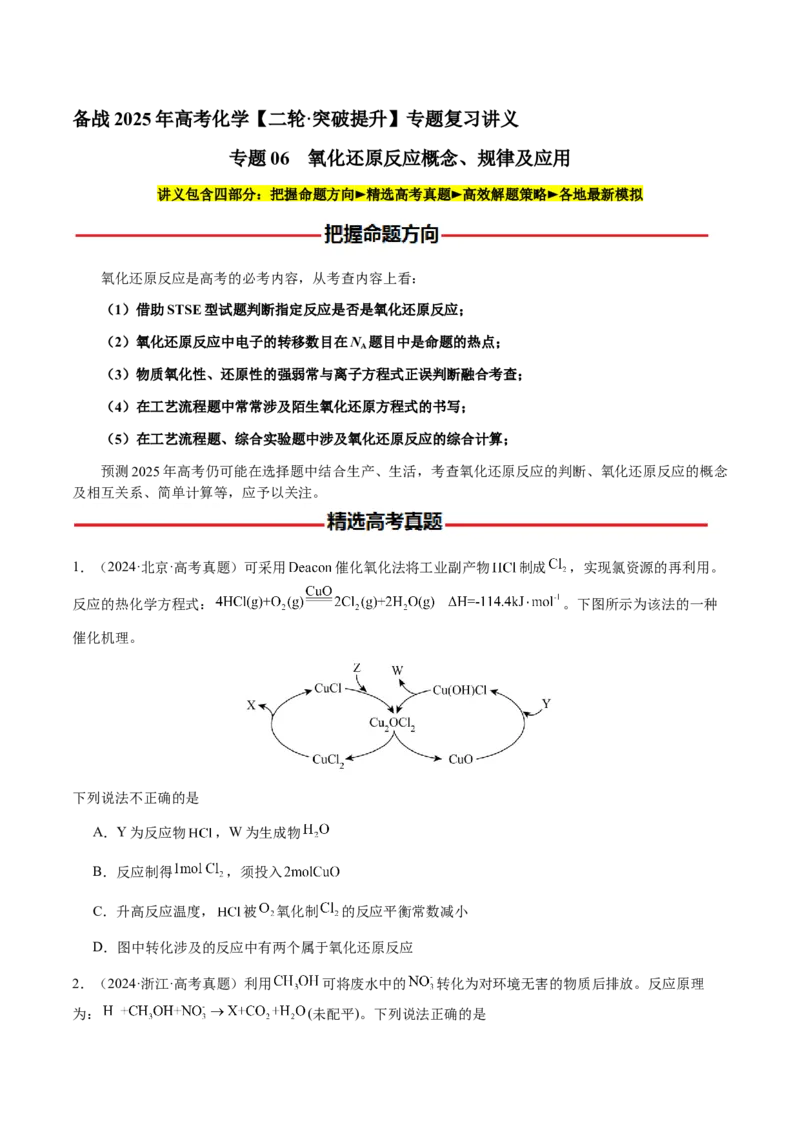
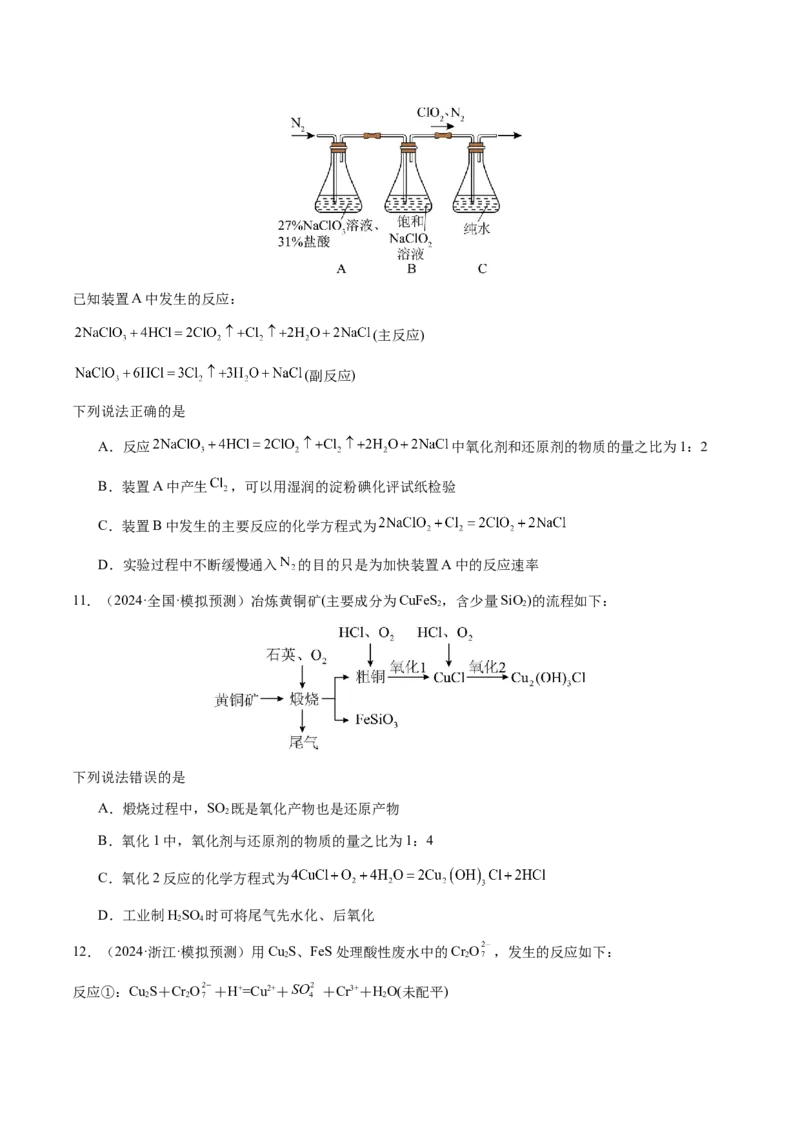
1.(2024·北京·高考真题)可采用 催化氧化法将工业副产物 制成 ,实现氯资源的再利用。
反应的热化学方程式: 。下图所示为该法的一种
催化机理。
下列说法不正确的是
A.Y为反应物 ,W为生成物
B.反应制得 ,须投入
C.升高反应温度, 被 氧化制 的反应平衡常数减小
D.图中转化涉及的反应中有两个属于氧化还原反应
2.(2024·浙江·高考真题)利用 可将废水中的 转化为对环境无害的物质后排放。反应原理
为: (未配平)。下列说法正确的是A.X表示
B.可用 替换
C.氧化剂与还原剂物质的量之比为
D.若生成标准状况下的 气体 ,则反应转移的电子数为 ( 表示阿伏加德罗常数的值)
3.(2024·河北·高考真题)超氧化钾 可用作潜水或宇航装置的 吸收剂和供氧剂,反应为
, 为阿伏加德罗常数的值。下列说法正确的是
A. 中 键的数目为
B. 晶体中离子的数目为
C. 溶液中 的数目为
D.该反应中每转移 电子生成 的数目为
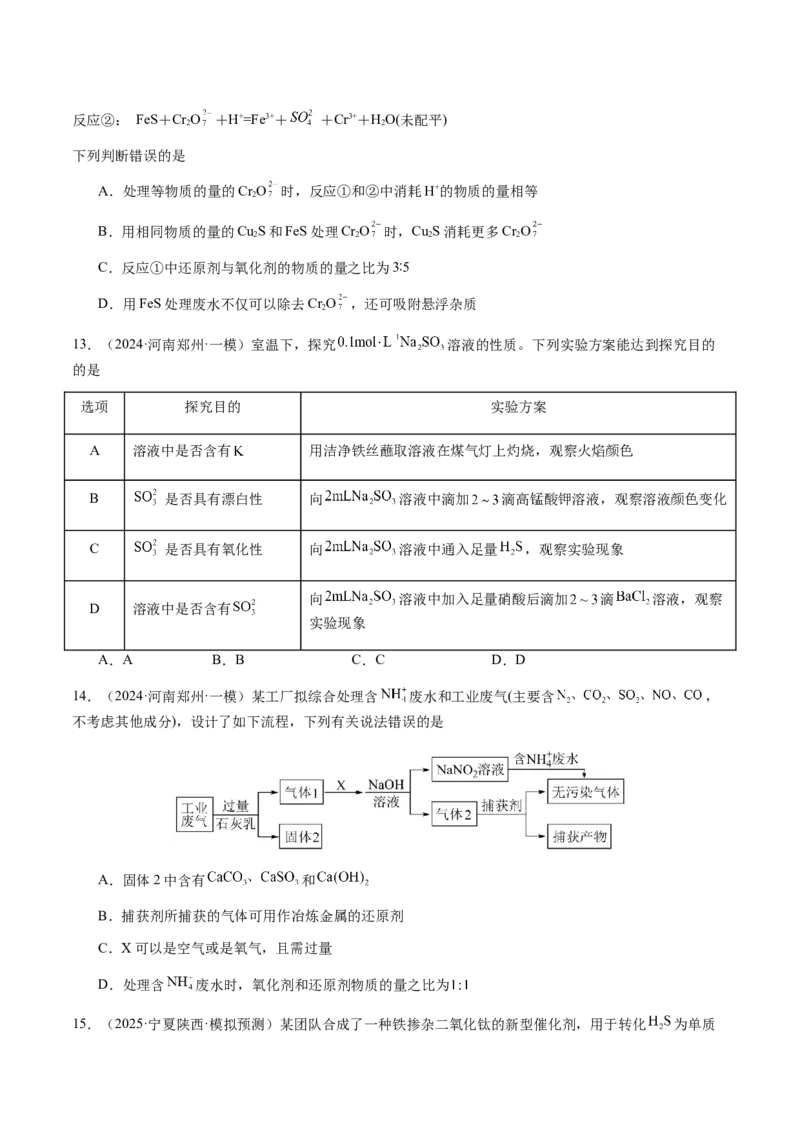
4.(2024·吉林·高考真题)某工厂利用铜屑脱除锌浸出液中的 并制备 ,流程如下“脱氯”步骤仅
元素化合价发生改变。下列说法正确的是
锌浸出液中相关成分(其他成分无干扰)
离子
浓度 145 0.03 1
A.“浸铜”时应加入足量 ,确保铜屑溶解完全
B.“浸铜”反应:
C.“脱氯”反应:
D.脱氯液净化后电解,可在阳极得到
5.(2024·吉林·高考真题) 分解的“碘钟”反应美轮美奂。将一定浓度的三种溶液(① 溶液;②
淀粉、丙二酸和 混合溶液;③ 、稀硫酸混合溶液)混合,溶液颜色在无色和蓝色之间来回振
荡,周期性变色;几分钟后,稳定为蓝色。下列说法错误的是A.无色→蓝色:生成 B.蓝色→无色: 转化为化合态
C. 起漂白作用 D.淀粉作指示剂
6.(2024·浙江·高考真题)汽车尾气中的 和 在催化剂作用下发生反应:
,下列说法不正确的是( 为阿伏加德罗常数的值)
A.生成 转移电子的数目为 B.催化剂降低 与 反应的活化能
C. 是氧化剂, 是还原剂 D. 既是氧化产物又是还原产物
7.(2023·福建·高考真题)稀有气体氙的氟化物 与 溶液反应剧烈,与水反应则较为温和,反
应式如下:
与水反应 与 溶液反应
i.
ii.
iii. iv.
下列说法错误的是
A. 具有平面三角形结构 B. 的还原性比 强
C.反应i~iv中有3个氧化还原反应 D.反应iv每生成 ,转移 电子
8.(2023·重庆·高考真题)已知反应: , 为阿伏加德罗常数的值,若
消耗 (标准状况) ,下列叙述错误的是
A.转移的电子数为 B.生成的 质量为
C.生成的氧化产物分子数为 D.生成的 含有孤电子对数为
9.(2023·北京·高考真题)离子化合物 和 与水的反应分别为①
;② 。下列说法正确的是
A. 中均有非极性共价键
B.①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为D.当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
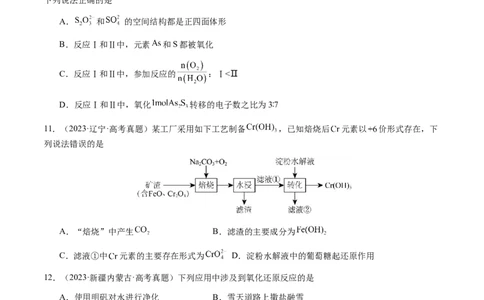
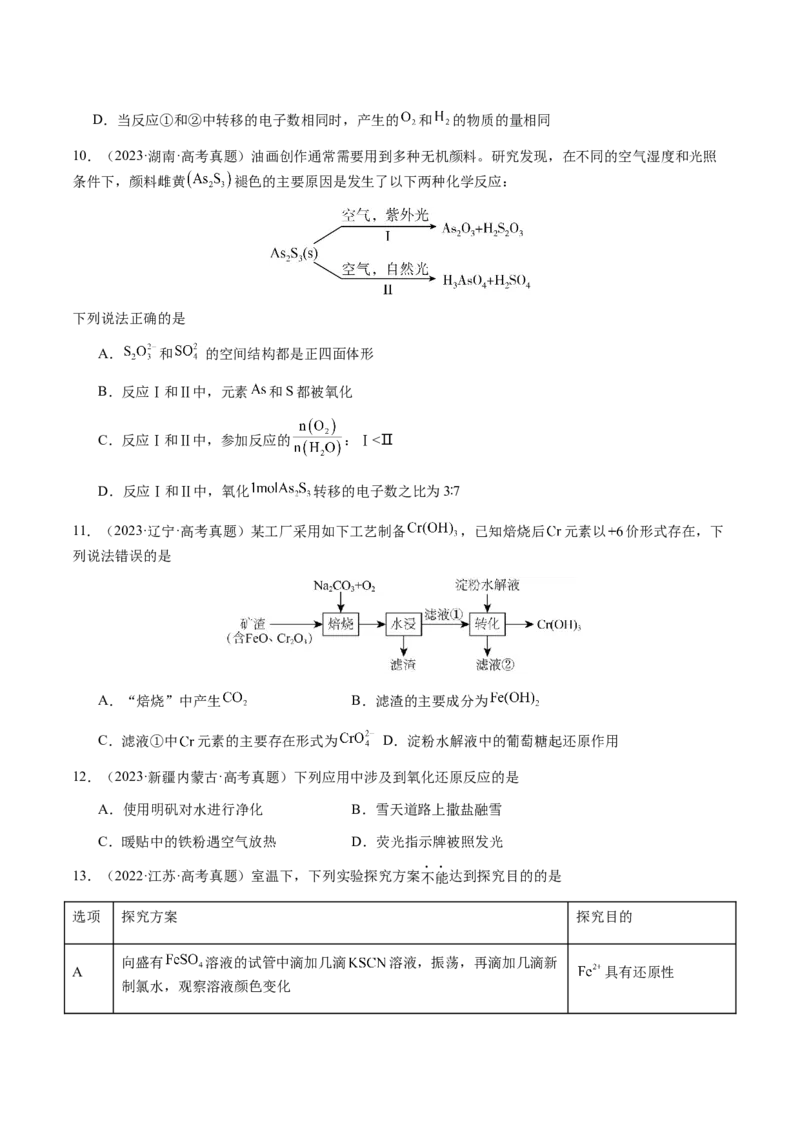
10.(2023·湖南·高考真题)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照
条件下,颜料雌黄 褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A. 和 的空间结构都是正四面体形
B.反应Ⅰ和Ⅱ中,元素 和S都被氧化
C.反应Ⅰ和Ⅱ中,参加反应的 :Ⅰ<Ⅱ
D.反应Ⅰ和Ⅱ中,氧化 转移的电子数之比为3∶7
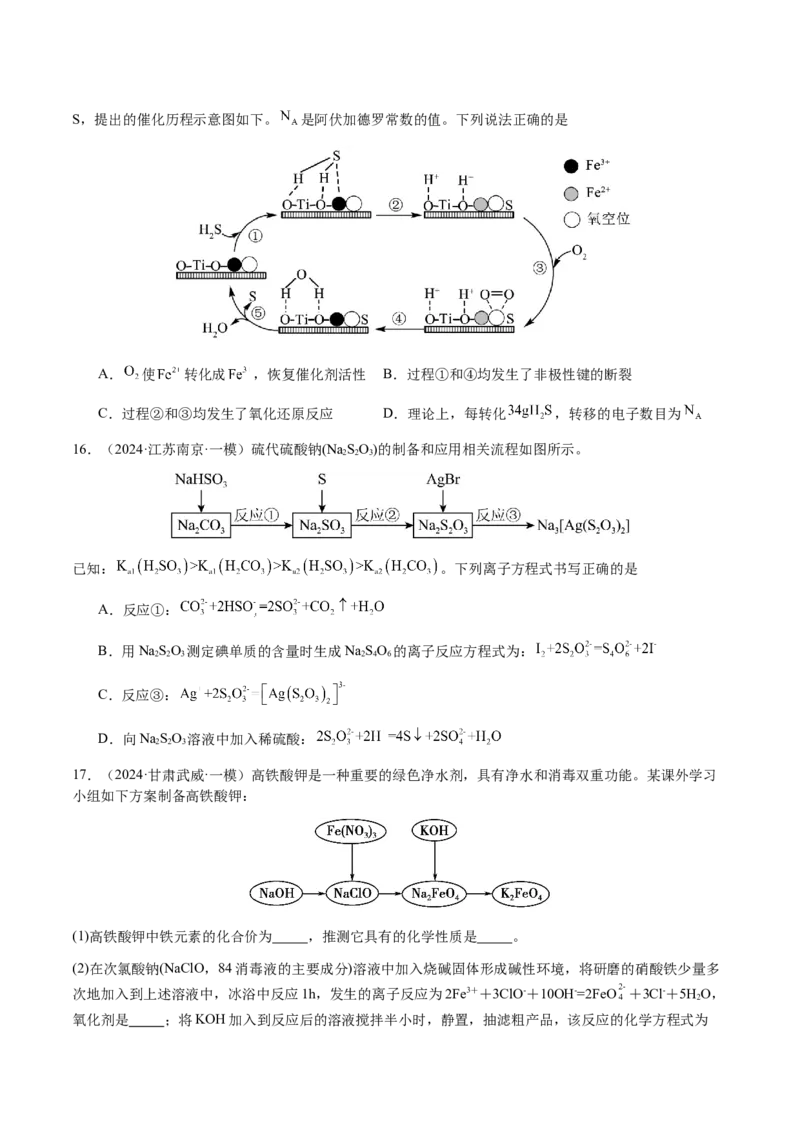
11.(2023·辽宁·高考真题)某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下
列说法错误的是
A.“焙烧”中产生 B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为 D.淀粉水解液中的葡萄糖起还原作用
12.(2023·新疆内蒙古·高考真题)下列应用中涉及到氧化还原反应的是
A.使用明矾对水进行净化 B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热 D.荧光指示牌被照发光
13.(2022·江苏·高考真题)室温下,下列实验探究方案不能达到探究目的的是
选项 探究方案 探究目的
向盛有 溶液的试管中滴加几滴 溶液,振荡,再滴加几滴新
A 具有还原性
制氯水,观察溶液颜色变化向盛有 水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察
B 具有漂白性
溶液颜色变化
C 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 的氧化性比 的强
D 用pH计测量醋酸、盐酸的pH,比较溶液pH大小 是弱电解质
A.A B.B C.C D.D
14.(2022·山东·高考真题)实验室制备 过程为:①高温下在熔融强碱性介质中用 氧化
制备 ;②水溶后冷却,调溶液 至弱碱性, 歧化生成 和 ;③减压
过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得 。下列说法正确的是
A.①中用瓷坩埚作反应器
B.①中用 作强碱性介质
C.②中 只体现氧化性
D. 转化为 的理论转化率约为66.7%
15.(2022·山东·高考真题)古医典富载化学知识,下述之物见其氧化性者为
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳( ):“色黄,以苦酒(醋)洗刷则白”
16.(2022·浙江·高考真题)关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
17.(2022·湖南·高考真题)为探究 的性质,进行了如下实验( 和 溶液浓度均为
)。实
操作与现象
验
① 在 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。
在 溶液中滴加2滴 溶液,变红褐色;
②
再滴加 溶液,产生蓝色沉淀。
在 溶液中滴加2滴 溶液,变红褐色;
③
将上述混合液分成两份,一份滴加 溶液,无蓝色沉淀生成;
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A.实验①说明加热促进 水解反应
B.实验②说明 既发生了水解反应,又发生了还原反应
C.实验③说明 发生了水解反应,但没有发生还原反应
D.整个实验说明 对 的水解反应无影响,但对还原反应有影响
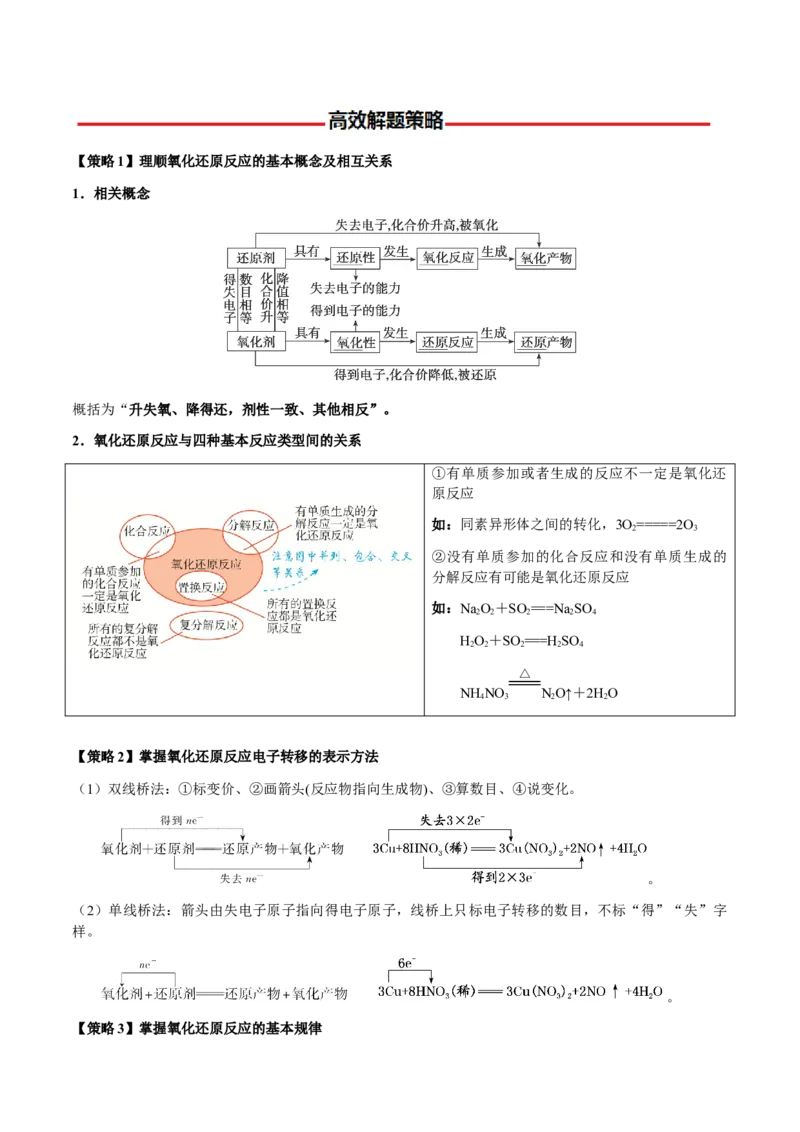
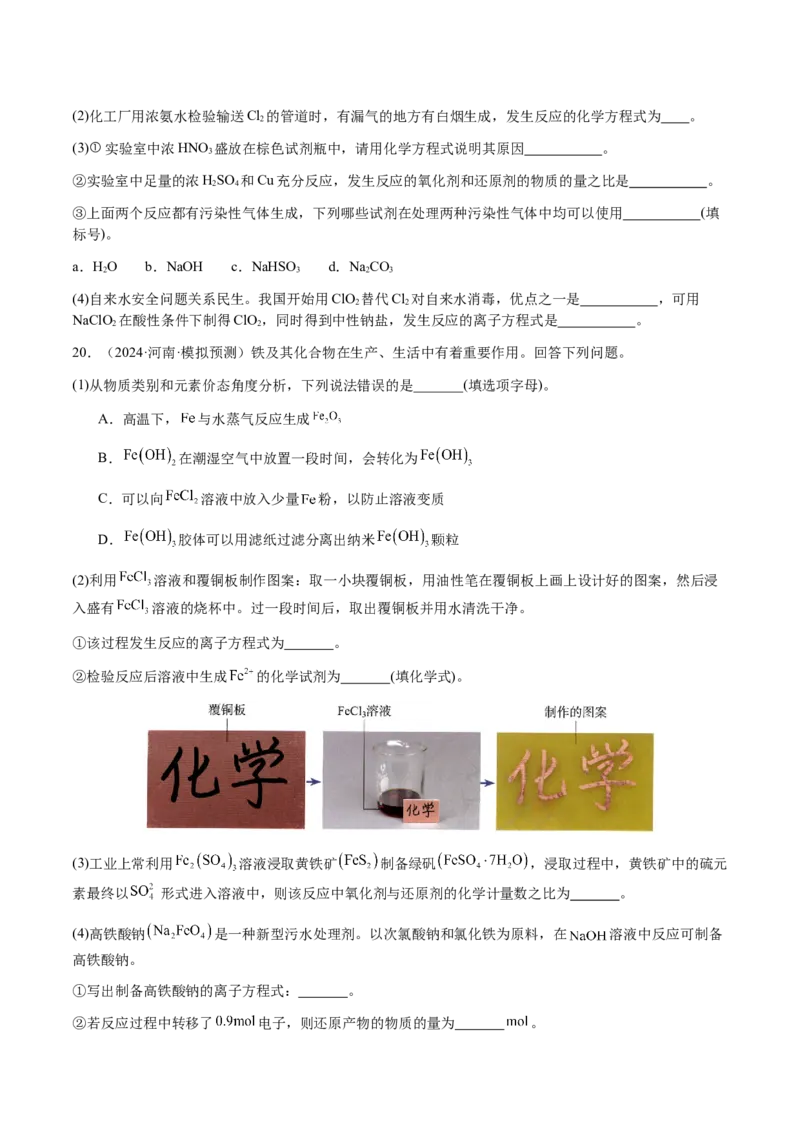
18.(2022·湖南·高考真题)科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋
中的 转化为 进入大气层,反应过程如图所示。
下列说法正确的是
A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
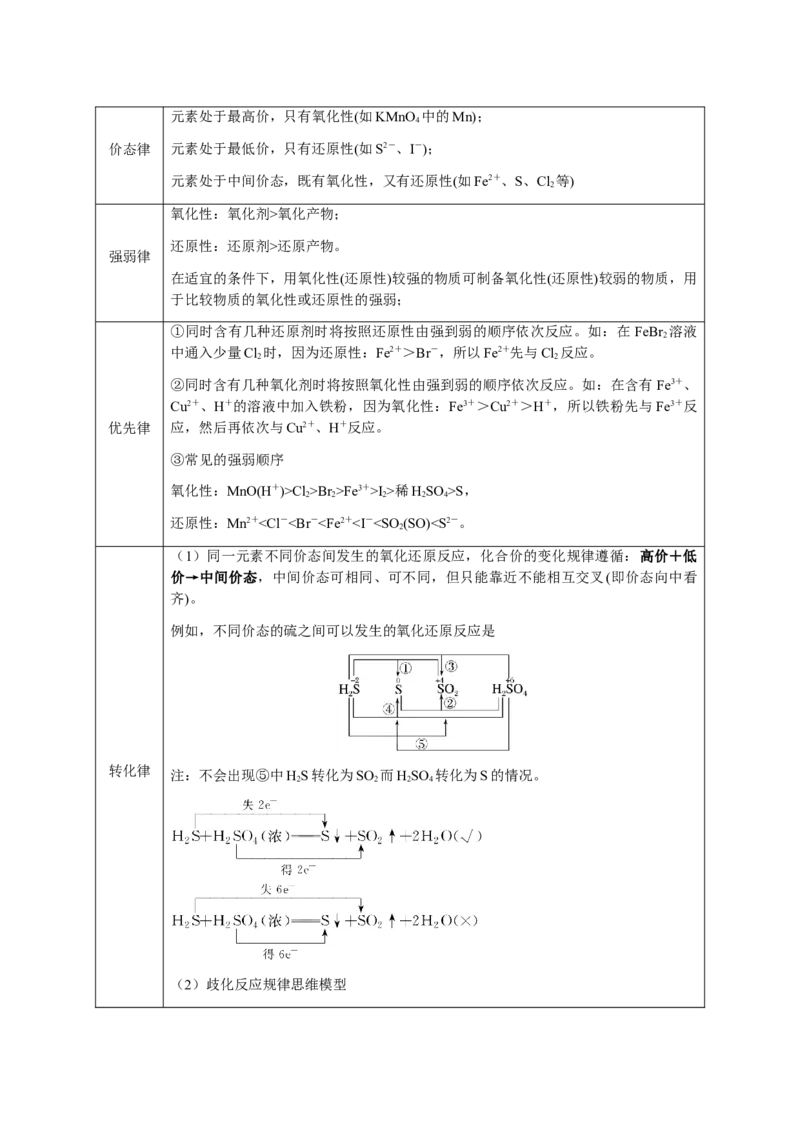
D.过程Ⅰ→Ⅲ的总反应为【策略1】理顺氧化还原反应的基本概念及相互关系
1.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
2.氧化还原反应与四种基本反应类型间的关系
①有单质参加或者生成的反应不一定是氧化还
原反应
如:同素异形体之间的转化,3O=====2O
2 3
②没有单质参加的化合反应和没有单质生成的
分解反应有可能是氧化还原反应
如:NaO+SO ===Na SO
2 2 2 2 4
HO+SO ===H SO
2 2 2 2 4
△
NH NO NO↑+2HO
4 3 2 2
【策略2】掌握氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价、②画箭头(反应物指向生成物)、③算数目、④说变化。
。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”“失”字
样。
。
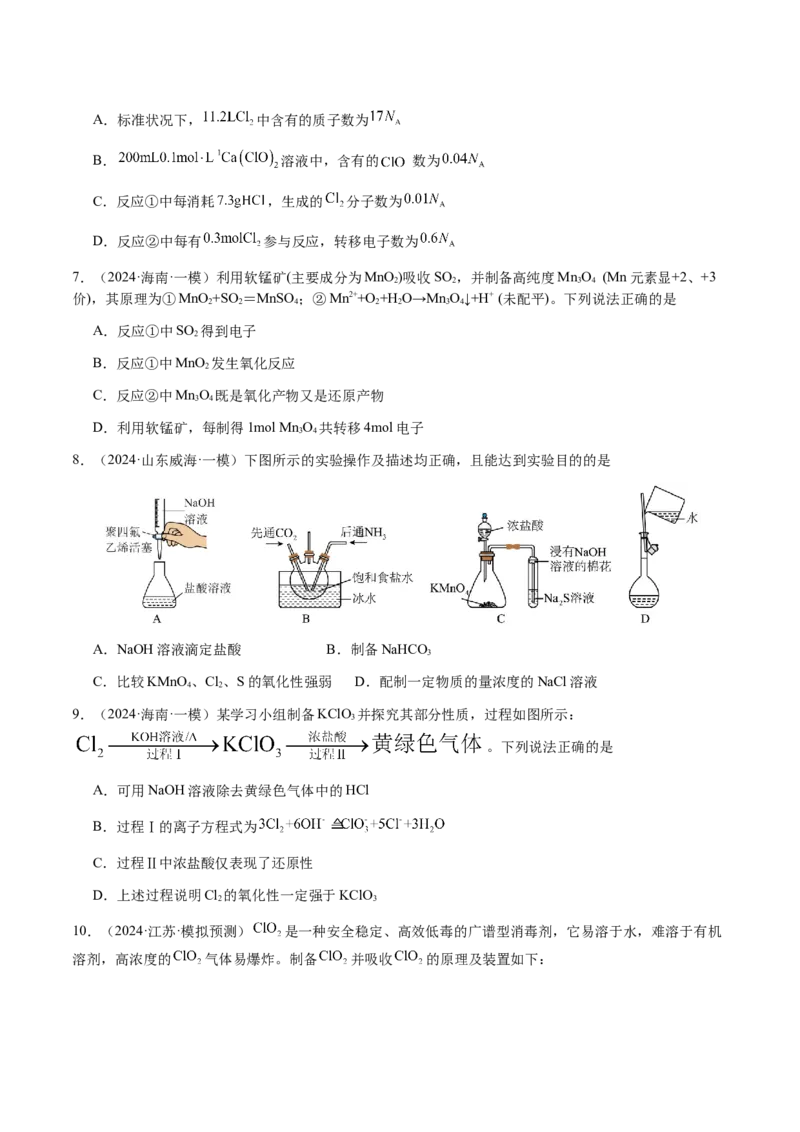
【策略3】掌握氧化还原反应的基本规律元素处于最高价,只有氧化性(如KMnO 中的Mn);
4
价态律 元素处于最低价,只有还原性(如S2-、I-);
元素处于中间价态,既有氧化性,又有还原性(如Fe2+、S、Cl 等)
2
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
强弱律
在适宜的条件下,用氧化性(还原性)较强的物质可制备氧化性(还原性)较弱的物质,用
于比较物质的氧化性或还原性的强弱;
①同时含有几种还原剂时将按照还原性由强到弱的顺序依次反应。如:在 FeBr 溶液
2
中通入少量Cl 时,因为还原性:Fe2+>Br-,所以Fe2+先与Cl 反应。
2 2
②同时含有几种氧化剂时将按照氧化性由强到弱的顺序依次反应。如:在含有 Fe3+、
Cu2+、H+的溶液中加入铁粉,因为氧化性:Fe3+>Cu2+>H+,所以铁粉先与Fe3+反
优先律 应,然后再依次与Cu2+、H+反应。
③常见的强弱顺序
氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀HSO >S,
2 2 2 2 4
还原性:Mn2+