文档内容
专题 09 化学反应速率与化学平衡
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·浙江省部分校高三开学摸底考试)下列说法正确的是( )
A.相同温度和压强下,熵值:1 mol C(s,金刚石)>1 mol C(s,石墨)
B.Ca(g)→Ca2+(g)+2e- ΔH小于0
C.NH NO 溶于水,ΔH>0,ΔS<0
4 3
D.分子间氢键数量:1 molHO(g) <1 molHO(l) <1 molHO(s)
2 2 2
2.(2023·浙江省普通高校招生高三选考模拟)关于反应CO(g)+3H(g) CHOH(g) +HO(l) ΔH<
2 2 3 2
0,下列说法不正确的是( )
A.该反应在低温条件下可以自发进行
B.向反应容器中加入正催化剂,不会改变反应自发进行的临界温度
C.恒容条件下,通入He和Ar组成的混合气体,不会改变反应的速率
D.恒压条件下,可通入过量的CO 气体可以提高H 转化率并增加生成物CHOH的浓度
2 2 3
3.(2023·浙江省温州市高三第一次适应性考试)T℃,反应CaCO (s) CaO(s)+ CO (g),在密闭容器
3 2
中达到平衡时的体积为100mL。已知密度:CaO(s):3.35 g· cm-3、CaCO (s):2.93 g· cm-3。下列有关说法正确
3
的是( )
A.恒温、恒容,体系中再加入56g CaO(s),平衡不移动
B.恒温、恒压,体系中再加入100g CaCO (s),平衡不移动
3
C.恒温,压缩容器体积,平衡后,反应速率加快
D.恒温、恒压,体系中通入一定量N,平衡正向移动,建立新的平衡状态
2
4.(2022·上海市徐汇中学高三期中)在一密闭容器中,进行如下反应:CO(g)+H(g) CO(g)+
2 2
HO(g),能判断该反应是否达到化学平衡状态的依据是( )
2
A.混合气体的密度保持不变 B.容器内的总压不随时间变化
C.V (H )=V (H O) D.C(CO)=C(CO)
正 2 逆 2 2
5.(2022·河北安平中学高三期中)已知凡气体分子总数增多的反应一定是熵增大的反应。一定条件下,下
列反应不能自发进行的是( )
A.2O(g)=3O(g) ΔH<0 B.2CO(g)=2C(s)+O (g) ΔH>0
3 2 2
C.N(g)+3H(g) 2NH (g) ΔH<0 D.CaCO (s)=CaO(s)+CO (g) ΔH>0
2 2 3 3 2
6.(2022•浙江省五校高三联考)在一容积不变,绝热的密闭容器中发生可逆反应:2X(s) Y(g)
+Z(g),以下不能说明该反应达到化学平衡状态的是( )A.混合气体的密度不再变化 B.反应容器中Y的质量分数不变
C.该反应的化学平衡常数不变 D.容器中混合气体的平均相对分子量不变
7.(2022·湖北省“荆、襄、宜“地七校联盟高三联考)某反应的反应机理可以分成如下两步,下列说法正
确的是( )
第一步反应 第二步反应
反应机理
NO +CO=NO+CO (快反
2NO =NO+NO (慢反应) 3 2 2
2 3 应)
A.第一步反应的活化能高于第二步反应的活化能
B.该反应的总反应方程式为NO+CO =NO+CO
2 2
C.该反应的速率主要由第二步反应决定
D.加入合适的催化剂既可以加快反应速率,又可以提高NO 的转化率
2
8.(2022·江苏省泰州市高三阶段性测试)NH 、NH Cl、NO、NO 、HNO 等是氮重要的化合物,NO 与
3 4 2 3 2
NO 能相互转化,热化学方程式为NO(g) 2NO (g) H=+57kJ•mol-1。对于反应NO(g)
2 4 2 4 2 2 4
2NO (g) H=+57kJ•mol-1,下列有关说法正确的是( ) △
2
A.升高△体系温度正反应速率增大,逆反应速率减小
B.若容器体积不变,密度不变时说明该反应建立化学平衡
C.其它条件不变,向平衡后的容器中再加入少量NO,新平衡后 的值不变
2 4
D.增大体系的压强能提高NO 的反应速率和平衡转化率
2 4
9.(2022·河南省名校联盟高三毕业班阶段测试)我国科技工作者研究利用 (氢型
分子筛)为载体,以CO 和氢气为原料合成绿色燃料甲醚。一定条件下发生反应:2CO(g)+6H(g)
2 2 2
CHOCH (g)+3HO(g) H=-123.8kJ·mol-1。下列叙述正确的是( )
3 3 2 1
A.恒容时,升高温度△,CO
2
的平衡转化率增大
B.恒容恒温时,及时分离出甲醚,平衡右移,反应速率增大
C.恒容恒温时,增大c(CO),反应物转化率均增大
2
D. 是该反应的催化剂,可加快反应速率
10.(2022·江苏省常州市部分重点中学高三期中)氨是化肥生产工业的重要原料。传统的Haber—Bosch法
目前仍是合成氨的主要方式,反应原理为N(g)+3H(g) 2NH (g),其生产条件需要高温高压。近来电催
2 2 3
化氮气合成氨因节能、环境友好等优势,受到广泛关注,下列有关Haber-Bosch法合成氨反应的说法正确的是(
)
A.该反应的ΔH>0、ΔS<0B.将氨气及时液化分离可加快化学反应速率
C.当2v(H ) =3v(NH ) 时,反应达到平衡状态
2 正 3 逆
D.提高体系的压强可增大反应的化学平衡常数
11.(2022·山东省实验中学高三第二次诊断考试)人体内的血红蛋白(Hb)可与O 结合,更易与CO结合使人
2
体中毒,涉及原理如下:
①
②
③
下列说法错误的是( )
A. 的数值范围是>1
B.反应①、②在一定温度下均可能自发进行
C.刚从平原到高原时,人体血液中c(HbO )将降低,使人体因缺氧而不适
2
D.将CO中毒的人转至高压氧仓中治疗,反应③平衡逆向移动而缓解症状
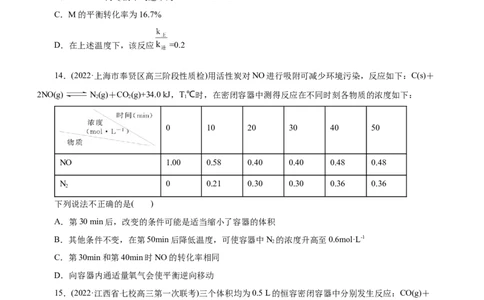
12.(2022·上海市虹口区高三期末学生学习能力诊断测试)T℃,体积均为1L的甲、乙、丙容器中发生反
应:2X(g)+Y(g) 3Z(s) ΔH<0, 。t 时刻容器中X、Y与Z的物质的量如下表,下列说法正确的
1
是( )
X Y Z
甲
乙
丙
A.甲容器中
B.乙容器若降低温度,达到平衡时c(X)可能为2 mol·L-1
C.乙、丙容器达到平衡后,X的浓度不相等
D.若丙容器中X的体积分数不变,则该反应已达平衡
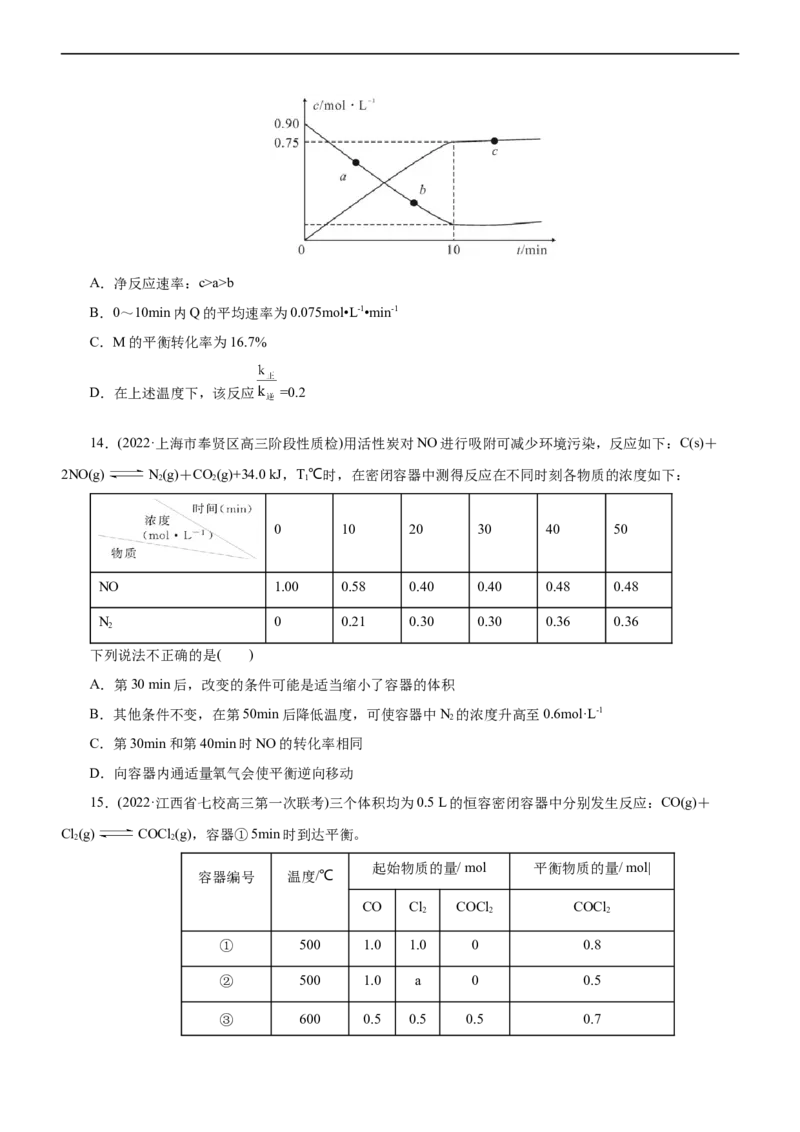
13.(2022·湖北省公安县等六县教学研究中心高三上学期质检考试)在一定温度下,在刚性密闭容器中充入
一定量M发生反应:M(g) Q(g)+E(s),测得M、Q的浓度与时间关系如图所示。已知:生成Q净反应速
率v=v -v =k •c(M)-v •c(Q)。下列说法正确的是( )
正 逆 正 逆A.净反应速率:c>a>b
B.0~10min内Q的平均速率为0.075mol•L-1•min-1
C.M的平衡转化率为16.7%
D.在上述温度下,该反应 =0.2
14.(2022·上海市奉贤区高三阶段性质检)用活性炭对NO进行吸附可减少环境污染,反应如下:C(s)+
2NO(g) N(g)+CO(g)+34.0 kJ,T℃时,在密闭容器中测得反应在不同时刻各物质的浓度如下:
2 2 1
0 10 20 30 40 50
NO 1.00 0.58 0.40 0.40 0.48 0.48
N 0 0.21 0.30 0.30 0.36 0.36
2
下列说法不正确的是( )
A.第30 min后,改变的条件可能是适当缩小了容器的体积
B.其他条件不变,在第50min后降低温度,可使容器中N 的浓度升高至0.6mol·L-1
2
C.第30min和第40min时NO的转化率相同
D.向容器内通适量氧气会使平衡逆向移动
15.(2022·江西省七校高三第一次联考)三个体积均为0.5 L的恒容密闭容器中分别发生反应:CO(g)+
Cl(g) COCl (g),容器①5min时到达平衡。
2 2
起始物质的量/ mol 平衡物质的量/ mol|
容器编号 温度/℃
CO Cl COCl COCl
2 2 2
① 500 1.0 1.0 0 0.8
② 500 1.0 a 0 0.5
③ 600 0.5 0.5 0.5 0.7下列说法正确的是( )
A.该反应正反应方向为吸热反应
B.容器①中前5min的平均反应速率v(Cl )=0.16 mol·L-1·min-1
2
C.a=0.55
D.若起始时向容器①加入CO 0.8 mol、Cl 0.8 mol,达到平衡时CO转化率大于80%
2
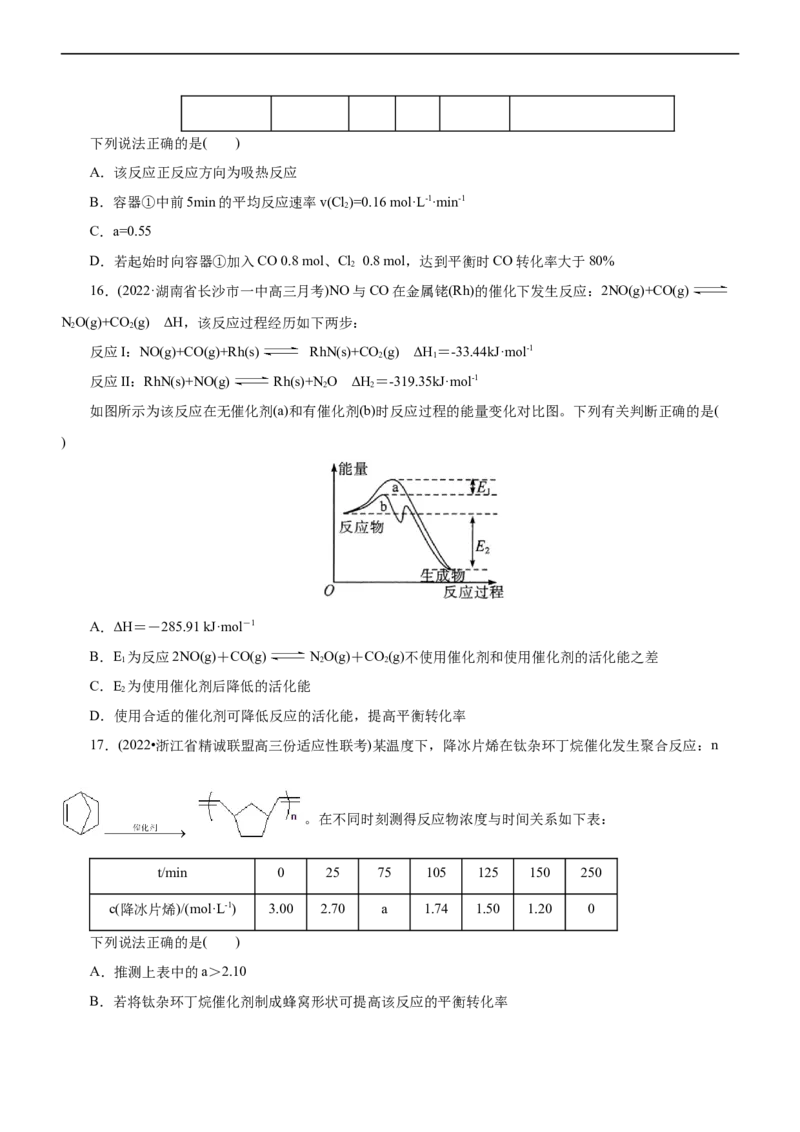
16.(2022·湖南省长沙市一中高三月考)NO与CO在金属铑(Rh)的催化下发生反应:2NO(g)+CO(g)
NO(g)+CO(g) ΔH,该反应过程经历如下两步:
2 2
反应I:NO(g)+CO(g)+Rh(s) RhN(s)+CO (g) ΔH=-33.44kJ·mol-1
2 1
反应II:RhN(s)+NO(g) Rh(s)+NO ΔH=-319.35kJ·mol-1
2 2
如图所示为该反应在无催化剂(a)和有催化剂(b)时反应过程的能量变化对比图。下列有关判断正确的是(
)
A.ΔH=-285.91 kJ·mol-1
B.E 为反应2NO(g)+CO(g) NO(g)+CO(g)不使用催化剂和使用催化剂的活化能之差
1 2 2
C.E 为使用催化剂后降低的活化能
2
D.使用合适的催化剂可降低反应的活化能,提高平衡转化率
17.(2022•浙江省精诚联盟高三份适应性联考)某温度下,降冰片烯在钛杂环丁烷催化发生聚合反应:n
。在不同时刻测得反应物浓度与时间关系如下表:
t/min 0 25 75 105 125 150 250
c(降冰片烯)/(mol·L-1) 3.00 2.70 a 1.74 1.50 1.20 0
下列说法正确的是( )
A.推测上表中的a>2.10
B.若将钛杂环丁烷催化剂制成蜂窝形状可提高该反应的平衡转化率C.105-155min,生成聚降冰片烯的平均速率为0.012mol·L-1·min-1
D.其他条件相同时,若将降冰片烯起始浓度减少为1.5mol/L,则该反应速率不变
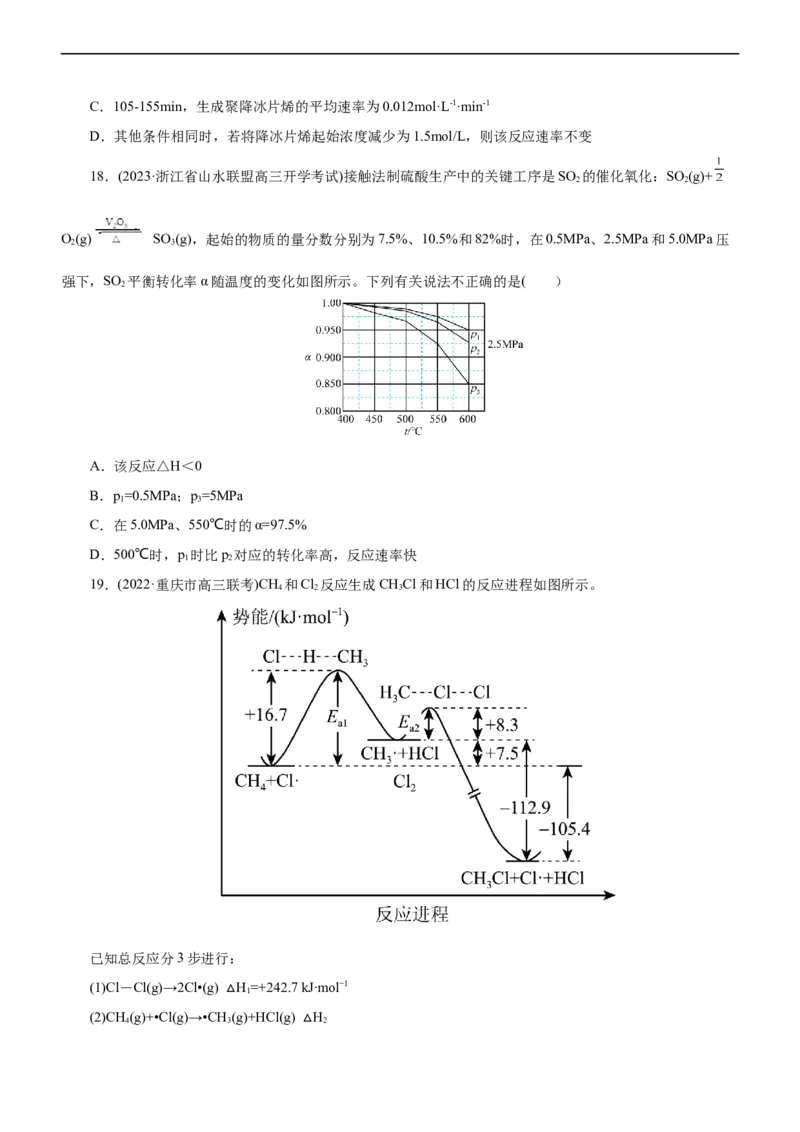
18.(2023·浙江省山水联盟高三开学考试)接触法制硫酸生产中的关键工序是SO 的催化氧化:SO (g)+
2 2
O(g) SO (g),起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和5.0MPa压
2 3
强下,SO 平衡转化率α随温度的变化如图所示。下列有关说法不正确的是( )
2
A.该反应△H<0
B.p=0.5MPa;p=5MPa
1 3
C.在5.0MPa、550℃时的α=97.5%
D.500℃时,p 时比p 对应的转化率高,反应速率快
1 2
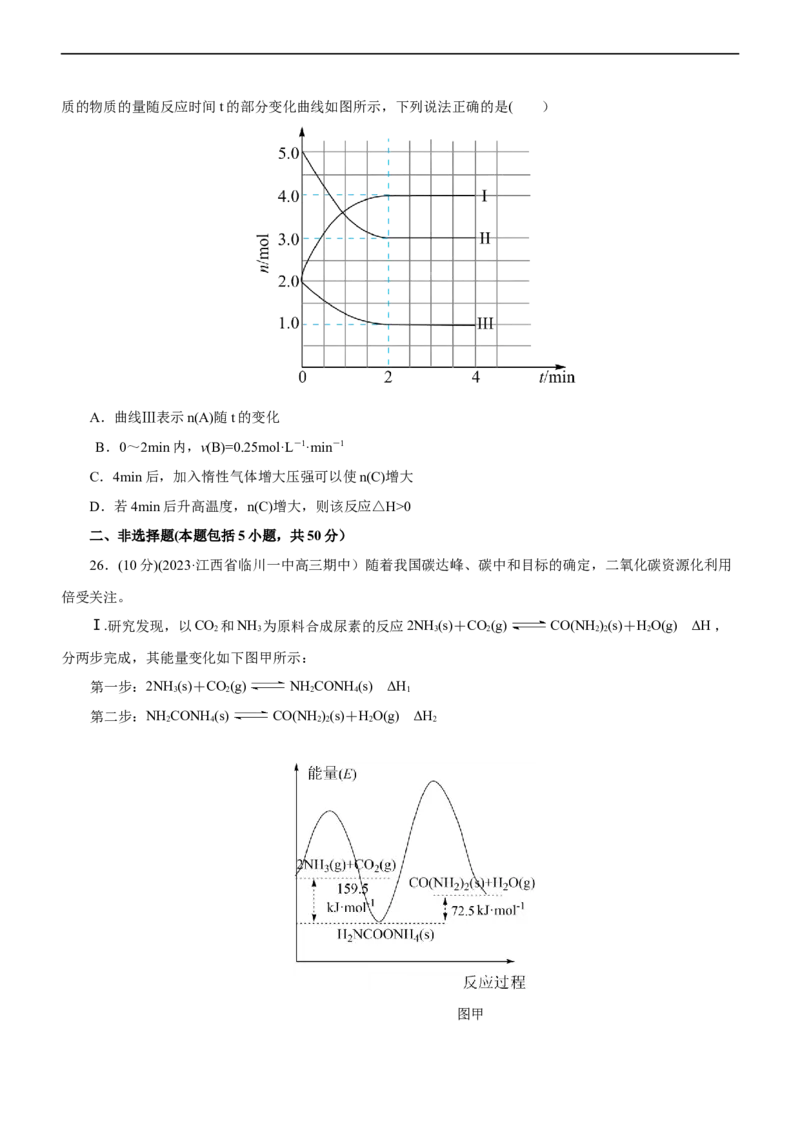
19.(2022·重庆市高三联考)CH 和Cl 反应生成CHCl和HCl的反应进程如图所示。
4 2 3
已知总反应分3步进行:
(1)Cl-Cl(g)→2Cl•(g) H=+242.7 kJ∙mol−1
1
(2)CH
4
(g)+•Cl(g)→•CH△3 (g)+HCl(g) H
2
△(3)•CH (g)+Cl-Cl(g)→CH Cl(g)+•Cl(g) H
3 3 3
下列有关说法正确的是( ) △
A.△H<0
2
B.第2步的反应速率小于第3步的反应速率
C.根据上述信息,反应中只有C-H键的断裂和C-Cl键的形成
D.CH(g)+Cl (g)→CH Cl(g)+HCl(g) H=−112.9 kJ∙mol−1
4 2 3
20.(2023·河北省邢台市五校高三第二△次联考)一定温度下,向2L恒容容器中充入1.0molA和1.0molB,
发生反应A(g)+B(g) C(g),经过一段时间后达到平衡。反应过程中测定的部分数据如表,下列说法正确
的是( )
0 5 15 25 35
1.0 0.85 0.81 0.80 0.80
A.前5s的平均反应速率
B.反应进行到25s时,反应刚好达到平衡状态
C.温度不变,起始向容器中充入0.4molA、0.4molB和0.1molC,达平衡前
D.保持温度不变,起始时向容器中充入2.0molC,达平衡时,C的转化率大于80%
21.(2023·安徽省卓越县中联盟高三第一次联考)一定温度下,在 恒容密闭容器中投入1 mol CO (g)与
2
4 mol H (g)制备CHOH(g),不考虑副反应,其物质的量随时间变化的关系如图所示:
2 3
下列说法中正确的是( )
A.该反应的化学方程式为CO(g)+3H(g) CHOH(g) +HO(g)
2 2 3 2
B.0~30min内,用H 表示的平均反应速率为0.05 mol·L-1·min-1
2
C.逆反应速率:a点大于b点
D.故选的平衡转化率是50%22.(2023·江苏省徐州市第七中学高三期中)CH 与CO 催化重整可以同时利用两种温室气体,其工艺过
4 2
程中涉及如下反应:
反应I:CH(g)+CO (g) 2CO(g)+2H(g) ΔH =247.4kJ·mol-1
4 2 2 1
反应Ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH =41.2kJ·mol-1
2 2 2 2
反应Ⅲ:CH(g)+ O(g) CO(g)+2H(g) ΔH =-35.6 kJ·mol-1
4 2 2 3
一定条件下,向体积为VL的密闭容器中通入CH、CO 各1.0mol及少量O,测得不同温度下反应平衡时
4 2 2
各产物产量如图所示。下列说法正确的是( )
A.图中曲线b表示H 的平衡产量随温度的变化曲线
2
B.1100K时,CH 与CO 的转化率分别为95%、90%,反应I的平衡常数
4 2
C.反应CO(g)+3H(g) CH(g)+HO(g) ΔH=206.2kJ·mol-1
2 4 2
D.若选用其它催化剂可能使平衡时HO的产量随着温度升高而增加
2
23.(2023·江苏省南通市高三期中)甲烷催化双重整制备合成气(CO和H)包括了水蒸气重整(反应I)和二
2
氧化碳重整(反应Ⅱ)两个反应。在P=3.2×106pa下,向密闭容器中按n(CH)∶n(H O)∶n(CO)=5∶4∶2通入混
4 2 2
合气,发生反应:(E 表示反应中基元反应的最大活化能)
a
反应I:CH(g) + HO(g) =CO(g) + 3H (g) ΔH = +206.2kJ·mol-1E = 240.1kJ·mol-1
4 2 2 1 a1
反应Ⅱ:CH(g) + CO (g) =2CO(g) + 2H (g) ΔH = +247.0kJ·mol-1 E = 577.6kJ·mol-1
4 2 2 2 a2
副反应:CH(g) =C(s) + 2H (g)
4 2
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是( )A.CO(g) + H O(g) = CO (g) + H(g) ΔH = +40.8kJ·mol-1
2 2 2
B.图中曲线X表示平衡时CH 的体积分数随温度的变化
4
C.其他条件不变,550~900℃范围内升高温度,平衡时n(H )/n(CO) 比值不断增大
2
D.温度过高,由于副反应发生,会导致甲烷双重整反应速率迅速下降
24.(2023·广东省百校高三联考)某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:
反应I:2X(g)+Y(g) 2Q(g) ΔH <0
1
反应II:M(g)+N(g) Q(g) ΔH >0
2
如图是部分组分浓度随时间变化曲线,平衡时M、N浓度相等。该温度下,下列说法不正确的是( )
A.初始浓度:c(M)= c(N)
B.活化能一定有:反应I>反应II
C.反应I的平衡常数:
D.平衡时的转化率:
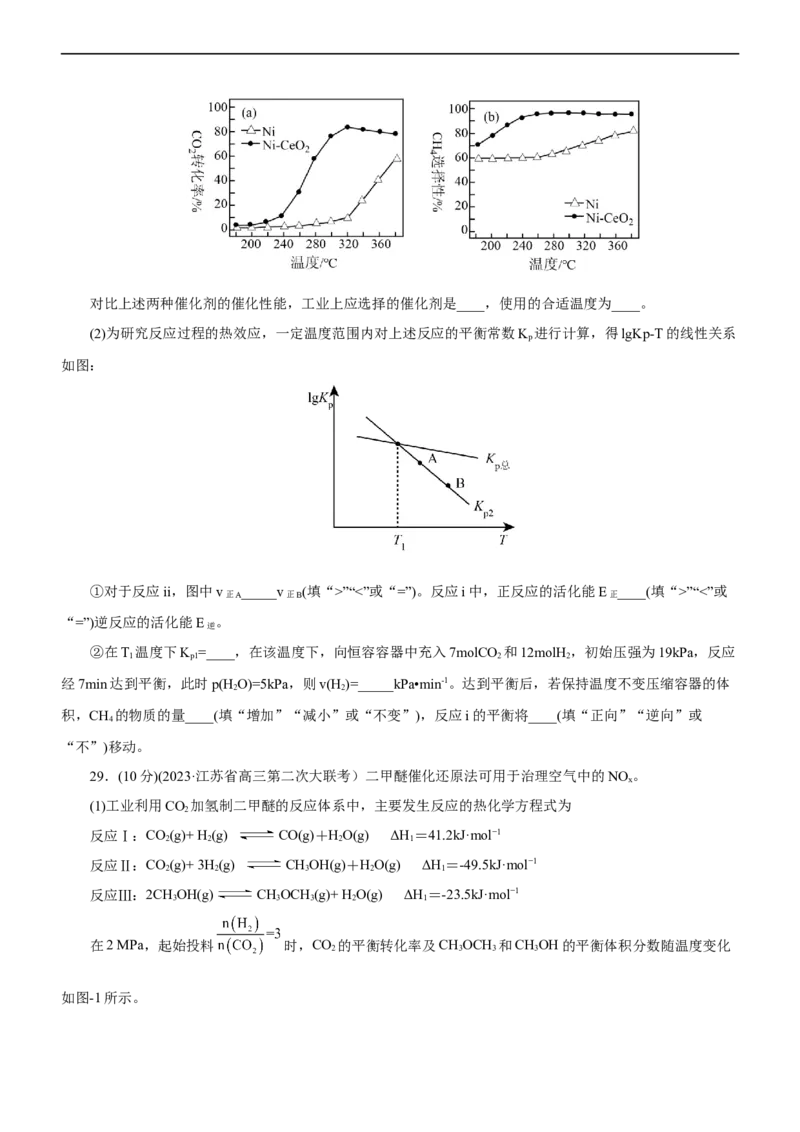
25.(2023·广东省茂名市电白区高三联考)在2L恒容密闭容器中发生反应2A(g)+B(s) 2C(g),各物
2质的物质的量随反应时间t的部分变化曲线如图所示,下列说法正确的是( )
A.曲线Ⅲ表示n(A)随t的变化
B.0~2min内,v(B)=0.25mol·L-1·min-1
C.4min后,加入惰性气体增大压强可以使n(C)增大
D.若4min后升高温度,n(C)增大,则该反应△H>0
二、非选择题(本题包括5小题,共50分)
26.(10分)(2023·江西省临川一中高三期中)随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用
倍受关注。
Ⅰ.研究发现,以CO 和NH 为原料合成尿素的反应2NH (s)+CO(g) CO(NH)(s)+HO(g) ΔH ,
2 3 3 2 2 2 2
分两步完成,其能量变化如下图甲所示:
第一步:2NH (s)+CO(g) NH CONH (s) ΔH
3 2 2 4 1
第二步:NH CONH (s) CO(NH)(s)+HO(g) ΔH
2 4 2 2 2 2
图甲(1)合成尿素的决速反应是_________反应(填“第一步”或“第二步”)。
(2)已知合成尿素2NH (s)+CO(g) CO(NH)(s)+HO(g) ΔH 的活化能Ea(逆)为 ,则该
3 2 2 2 2
反应的活化能Ea(正)为_________ 该反应在_________(填“高温”、“低温”、“任意温度”)下可自
发进行。
Ⅱ.以CO 和CH 催化重整制备合成气发生反应:CH(g)+CO(g) 2CO(g)+ H (g)。
2 4 4 2 2
(3)在一定条件下,在密闭容器中通入一定量的CH 和CO,CH 的平衡转化率随温度、压强的变化关系如
4 2 4
下图乙所示。
①若反应在恒温、恒压密闭容器中进行,下列叙述能说明反应达到平衡状态的是_________(填序号)。
A.容器中混合气体的密度保持不变 B.容器内CO与H 的物质的量之比保持不变
2
C.反应速率: D.断裂 同时断裂 键
②由图乙可知,压强P_________P(填“>”、“<”或“=”,下同);压强为P 时,对应温度下Y点速率
1 2 2
_________ 。
③若在Y点时对反应容器升温的同时扩大容器体积使体系压强减小,重新达到新的平衡状态时,可能是
图中:A、B、C、D、E点中的_________点。
(4)一定温度下,向容积不变的密闭容器中通入总压强为PkPa的等物质的量的CH 和CO 以及一定量的水
4 2
蒸气(水蒸气不参与反应),达到平衡后总压强为1.48PkPa,CH 的转化率为60%,则该温度下的
4
_________(用含P的代数式表示,只列计算表达式;用平衡分压代替平衡浓度,已知气体分压 气体总压 气
体的物质的量分数)。27.(10分)(2023·湖北省黄冈市高三期中质量抽测)二氧化碳甲烷化助力我国2060年前实现“碳中和”,
其中涉及的主要反应如下:
反应Ⅰ:CO₂(g)+4H₂(g) CH₄(g)+2H₂O(g) H=-164.7kJ·mol⁻¹
反应Ⅱ:CO₂(g)+H₂(g) CO(g)+H₂O(g) H△=+41.2kJ·mol⁻¹
回答下列问题: △
(1)由热化学方程式可知,反应Ⅰ属于反应_______(填写序号)
A.高温自发 B.低温自发 C.恒自发 D.恒不自发
(2)动力学研究:在多个1L恒容密闭装置中,分别充入1molCO₂和 发生上述反应Ⅰ,在不同温度
下反应到10分钟时,测得H₂转化率与温度关系如图1所示。已知该反应的速率方程为 ,
,其中 、 为速率常数,只受温度影响。
①图1中,至a点的H₂平均反应速率为_______ 。
②图1中,v(a)逆_______v(c)逆(填“>”、“=”或“<”)。
③图1中c点的 对应的是图2中的_______点。
④图1中a点的v正,v逆与a点的K(平衡常数)、Q(浓度商)的关系是 ______。
(3)热动力学研究:向10L的恒压密闭装置中充入5mol CO₂和20mol H₂,在不同温度下同时发生上述反应
Ⅰ和反应Ⅱ,得到平衡时各含碳物质的物质的量n(X)与温度T的关系如下图所示。①当反应Ⅰ和反应Ⅱ均达到化学平衡状态时,维持温度不变,压缩装置体积,则反应Ⅱ的平衡移动方向是
_______(填序号)。
A.正向移动 B.逆向移动 C.
不移动 D.无法确定
②曲线Z表示的是_______ (填写含碳元素物质的化学式)的物质的量与温度的关系,简述其在温度段500K
~800K物质的量增大的原因_______。
③800K时,反应Ⅱ的平衡常数为_______(计算结果保留两位有效数字)。
28.(10分)(2023·山东省日照市高三期中联考)将CO 转化为高附加值碳基燃料,可有效减少碳的排放。
2
在催化剂作用下CO 甲烷化的总反应为: CO(g)+2H(g) CH(g)+ H O(g) H K ,该反应分两步
2 2 2 4 2 总 p总
△
完成,反应过程如下:
i.CO (g)+H(g) CO(g)+HO(g) H K
2 2 2 1 p1
△
ii.CO(g)+H (g) CO(g)+ CH(g) H K
2 2 4 2 p2
△
回答下列问题:
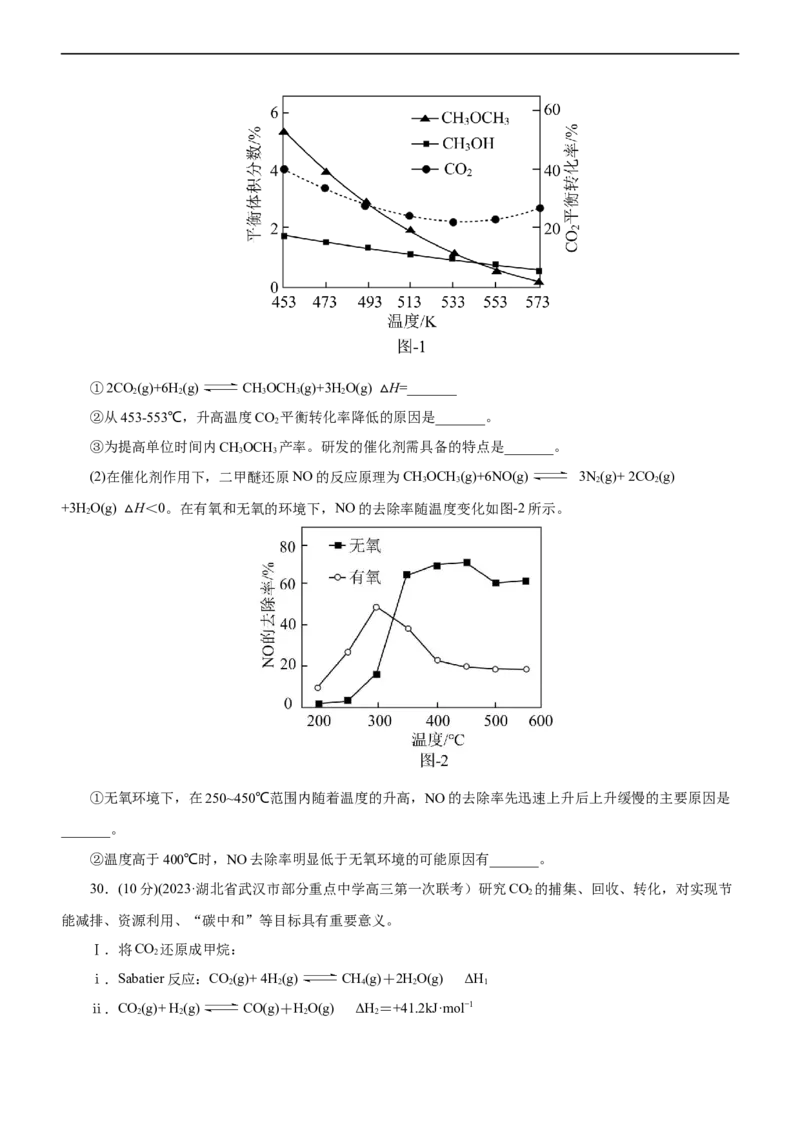
(1)催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO 转化率和
2 2
生成CH 选择性随温度的变化如图所示。
4对比上述两种催化剂的催化性能,工业上应选择的催化剂是____,使用的合适温度为____。
(2)为研究反应过程的热效应,一定温度范围内对上述反应的平衡常数K 进行计算,得lgKp-T的线性关系
p
如图:
①对于反应ii,图中v _____v (填“>”“<”或“=”)。反应i中,正反应的活化能E ____(填“>”“<”或
正A 正B 正
“=”)逆反应的活化能E 。
逆
②在T 温度下K =____,在该温度下,向恒容容器中充入7molCO 和12molH ,初始压强为19kPa,反应
1 p1 2 2
经7min达到平衡,此时p(H O)=5kPa,则v(H )=_____kPa•min-1。达到平衡后,若保持温度不变压缩容器的体
2 2
积,CH 的物质的量____(填“增加”“减小”或“不变”),反应i的平衡将____(填“正向”“逆向”或
4
“不”)移动。
29.(10分)(2023·江苏省高三第二次大联考)二甲醚催化还原法可用于治理空气中的NO 。
x
(1)工业利用CO 加氢制二甲醚的反应体系中,主要发生反应的热化学方程式为
2
反应Ⅰ:CO(g)+ H (g) CO(g)+HO(g) ΔH =41.2kJ·mol−1
2 2 2 1
反应Ⅱ:CO(g)+ 3H (g) CHOH(g)+HO(g) ΔH =-49.5kJ·mol−1
2 2 3 2 1
反应Ⅲ:2CHOH(g) CHOCH (g)+ H O(g) ΔH =-23.5kJ·mol−1
3 3 3 2 1
在2 MPa,起始投料 时,CO 的平衡转化率及CHOCH 和CHOH的平衡体积分数随温度变化
2 3 3 3
如图-1所示。①2CO(g)+6H(g) CHOCH (g)+3HO(g) H=_______
2 2 3 3 2
②从453-553℃,升高温度CO 平衡转化率降低的△原因是_______。
2
③为提高单位时间内CHOCH 产率。研发的催化剂需具备的特点是_______。
3 3
(2)在催化剂作用下,二甲醚还原NO的反应原理为CHOCH (g)+6NO(g) 3N(g)+ 2CO(g)
3 3 2 2
+3H O(g) H<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
2
△
①无氧环境下,在250~450℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
_______。
②温度高于400℃时,NO去除率明显低于无氧环境的可能原因有_______。
30.(10分)(2023·湖北省武汉市部分重点中学高三第一次联考)研究CO 的捕集、回收、转化,对实现节
2
能减排、资源利用、“碳中和”等目标具有重要意义。
Ⅰ.将CO 还原成甲烷:
2
ⅰ.Sabatier反应:CO(g)+ 4H (g) CH(g)+2HO(g) ΔH
2 2 4 2 1
ⅱ.CO(g)+ H (g) CO(g)+HO(g) ΔH =+41.2kJ·mol−1
2 2 2 2ⅲ.CO(g)+ 3H (g) CH(g)+HO(g) ΔH =-206.1kJ·mol−1
2 4 2 3
(1) ΔH =________。
1
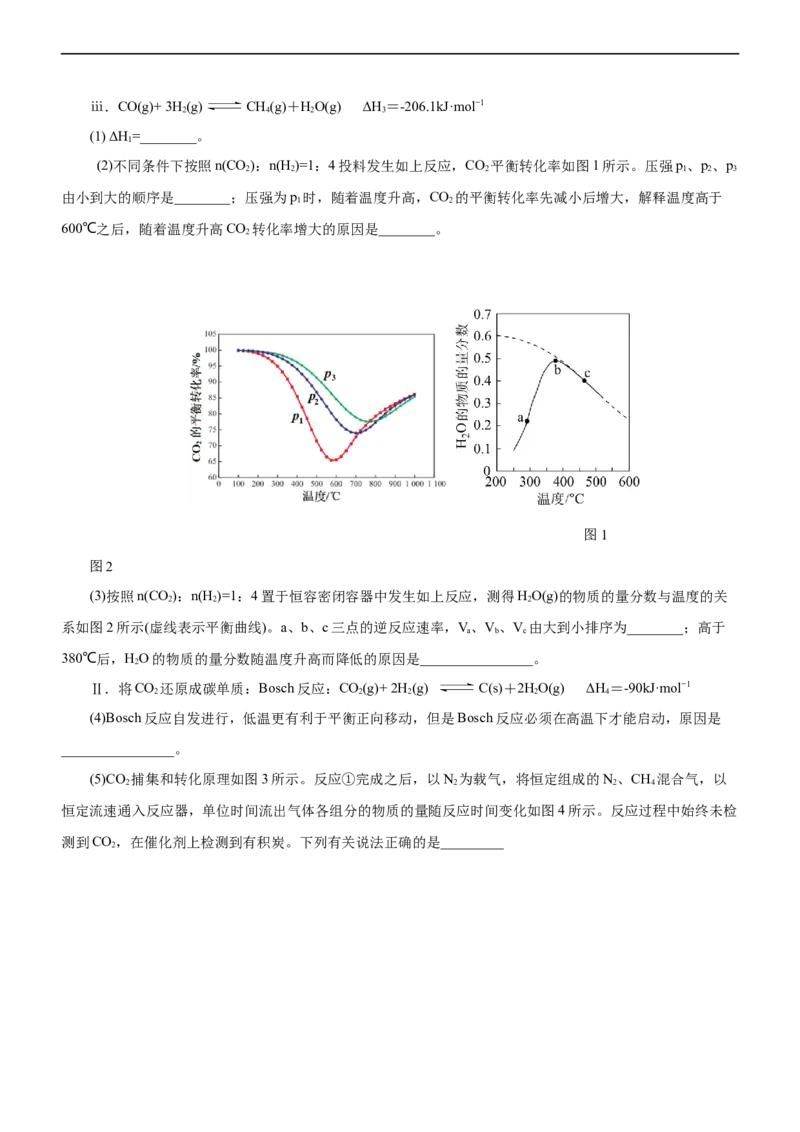
(2)不同条件下按照n(CO):n(H )=1:4投料发生如上反应,CO 平衡转化率如图1所示。压强p、p、p
2 2 2 1 2 3
由小到大的顺序是________;压强为p 时,随着温度升高,CO 的平衡转化率先减小后增大,解释温度高于
1 2
600℃之后,随着温度升高CO 转化率增大的原因是________。
2
图1
图2
(3)按照n(CO):n(H )=1:4置于恒容密闭容器中发生如上反应,测得HO(g)的物质的量分数与温度的关
2 2 2
系如图2所示(虚线表示平衡曲线)。a、b、c三点的逆反应速率,V、V、V 由大到小排序为________;高于
a b c
380℃后,HO的物质的量分数随温度升高而降低的原因是________________。
2
Ⅱ.将CO 还原成碳单质:Bosch反应:CO(g)+ 2H (g) C(s)+2HO(g) ΔH =-90kJ·mol−1
2 2 2 2 4
(4)Bosch反应自发进行,低温更有利于平衡正向移动,但是Bosch反应必须在高温下才能启动,原因是
________________。
(5)CO 捕集和转化原理如图3所示。反应①完成之后,以N 为载气,将恒定组成的N、CH 混合气,以
2 2 2 4
恒定流速通入反应器,单位时间流出气体各组分的物质的量随反应时间变化如图4所示。反应过程中始终未检
测到CO,在催化剂上检测到有积炭。下列有关说法正确的是_________
2a.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+CO+2H
2 3 3 4 2
b.t- t ,n(H )比n(CO)多,且生成的H 速率不变,推测有副反应CH C+2H
1 3 2 2 4 2
c.t 时刻,副反应生成H 的速率大于反应②生成H 的速率
2 2 2
d.t 之后,生成CO的速率为0,是因为反应②不再发生
3