文档内容
专题 09 化学反应速率与化学平衡
1.下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2
D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
2.(2023·江西省九江市十校高三联考)某温度下,反应2CH=CH (g)+HO(g) CHCHOH(g)在密闭
2 2 2 3 2
容器中达到平衡,下列说法正确的是( )
A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时CHCHOH(g)的浓度增大
3 2
C.恒压下,充入一定量的N,平衡向逆反应方向移动
2
D.恒容下,充入一定量的CH=CH (g),CH=CH (g)的平衡转化率增大
2 2 2 2
3.(2022·湖北省部分学校高三质量检测)反应进行的方向是化学反应原理的三个重要组成部分之一、下列
说法中正确的是( )
A. , 的反应一定可以自发进行
B.根据反应的自发性可以预测该反应发生的快慢
C.可逆反应正向进行时,正反应具有自发性, 一定小于零
D.常温下,反应C(s)+ CO (g) 2CO(g)不能自发进行,该反应的ΔH>0
2
4.(2022•浙江省温州市高三适应性测试)一定条件下,向一带活塞、有钒触媒的密闭容器中充入2molSO
2
和1molO ,发生反应:2SO (g)+O(g) 2SO(g) ΔH=-198.0kJ·mol−1,则下列说法正确的是( )
2 2 2 3
A.该反应的逆方向低温自发
B.若容器绝热,则化学反应速率会越来越快
C.保持温度不变,达到平衡后,充入2molN ,SO 的转化率将减小
2 2
D.n(SO )/n(O)不变,则该可逆反应已达到平衡状态
2 2
5.(2023届·浙江省十校联盟高三10月月考)含 的废水常用MnS(s)作沉淀剂,原理为Cu2+(aq)+
MnS(s) CuS(s)+Mn2+(aq)。一定温度下,下列有关该反应的推理正确的是( )
A.该反应达到平衡时,c(Cu2+)=c(Mn2+)B.平衡体系中加入少量CuS(s)后,c(Mn2+)变小
C.平衡体系中加入少量CuCl(s)后, 变大
2
D.该反应平衡常数:
6.(2022·安徽省皖江名校高三第四次联考)在PdCl -CuCl 做催化剂和适宜的温度条件下,用O 将HCl氧
2 2 2
化为Cl:4HCl(g)+O (g)=2HO(g)+2Cl (g) ΔH<0,下列有关说法不正确的是( )
2 2 2 2
A.降低温度,可提高Cl 产率
2
B.提高 ,该反应的平衡常数增大
C.若断开1molH-Cl键的阿时有1molH-O键断开,则表明该反应达到平衡状态
D.该反应的平衡常数表达式
7.(2022·山东省高三第三次联考)在容积为2L的密闭容器中进行如下反应:A(s)+2B(g) 3C(g)
+nD(g),开始时A为4mol,B为6mol;5min末时测得C的物质的量为3mol,用D表示的化学反应速率v(D)
为0.1 mol/(L·min)。下列说法错误的是( )
A.前5min内用A表示的化学反应速率v(A)为0.1mol/(L·min)
B.化学方程式中n值为1
C.反应达到平衡时3v (B)=2v (C)
正 逆
D.此反应在两种不同情况下的速率分别表示为:①v(B)=6 mol/(L·min),②v(D)=4.5 mol/(L·min),其中
反应速率快的是②
8.以反应 5HC O+2MnO -+6H+ = 10CO↑+ 2Mn2+ + 8H O 为例探究“外界条件对化学反应速率的影
2 2 4 4 2 2
响”。实验时,分别量取 H2C2O 溶液和酸性 KMnO 溶液,迅速混合并开始计时,通过测定溶液褪色所需时
4 4
间来判断反应的快慢。
下列说法不正确的是( )A.实验①、 ②、 ③所加的HC O 溶液均要过量
2 2 4
B.若实验①测得 KMnO 溶液的褪色时间为 40 s,则这段时间内平均反应速率 v(KMnO)= 2. 5×10-4
4 4
mol/L/s
C.实验①和实验②是探究浓度对化学反应速率的影响,实验②和③是探究温度对化学反应速率的影响
D.实验①和②起初反应均很慢,过了一会儿速率突然增大,可能是生成的 Mn2+对反应起催化作用
9.(2023·湘豫名校联考一轮复习诊断考试)某温度下,将2mol H 和2molI 充入密闭的刚性容器中发生反
2 2
应H(g)+I(g) 2HI(g),该反应的v-t图象如图所示,t 时刻测定容器内HI的物质的量为1mol,t 时刻保
2 2 1 2
持等温等容,抽走0.5mol HI。下列有关叙述正确的是( )
A.该温度下H(g)+I(g) 2HI(g)的平衡常数
2 2
B.反应过程中,可以利用气体的总压强保持不变来判断是否达到平衡
C.t 时刻,抽取HI的瞬间,v′(逆)在图象上的变化应该是c点
2
D.t 时刻,抽取HI后达到平衡后H 的百分含量减少
2 2
10.(2023·河北省部分学校高三联考)高炉炼铁中的一个反应为FeO(s)+CO(g) Fe(s)+CO (g) ΔH>
2
0,在1100℃下,若CO起始浓度为1.2mol/L,10min后达到平衡时 的体积分数为 ,下列说法错误的是(
)
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为v(CO)=0.02 mol·L-1·min-1
C.达到平衡后,若增大c(CO),则达到新平衡时, 增大
2
D.测得某时刻c(CO)=0.8mol/L,则此时
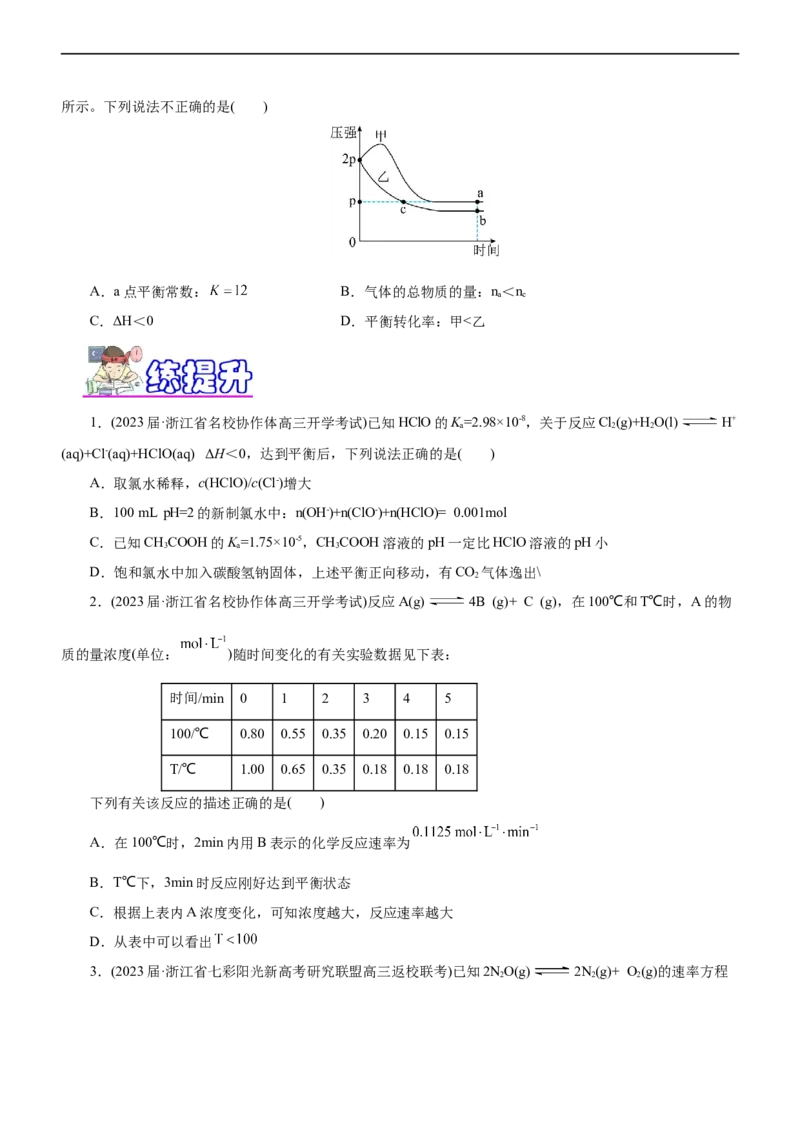
11.(2023·江西省九江市十校高三联考)向体积均为1L的两恒容容器中分别充入2molX和1molY发生反应:
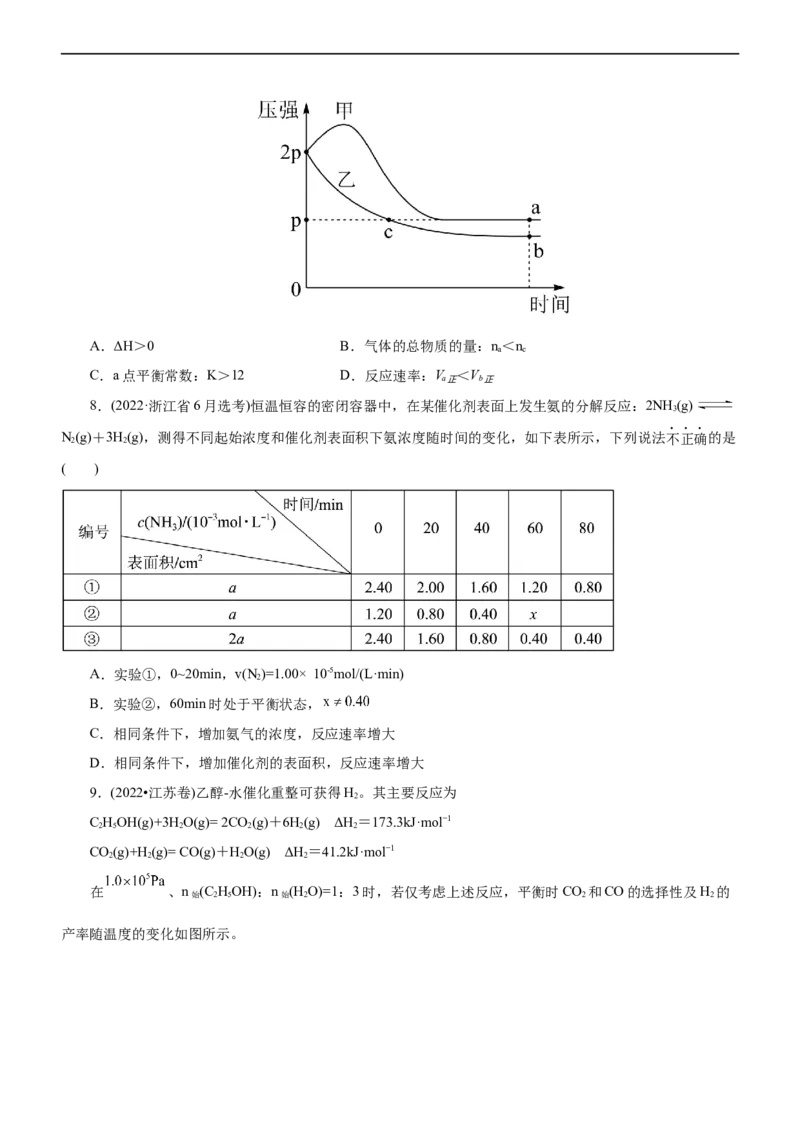
2X(g)+Y(g) Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法不正确的是( )
A.a点平衡常数: B.气体的总物质的量:n<n
a c
C.ΔH<0 D.平衡转化率:甲<乙
1.(2023届·浙江省名校协作体高三开学考试)已知HClO的K=2.98×10-8,关于反应Cl(g)+H O(l) H+
a 2 2
(aq)+Cl-(aq)+HClO(aq) ΔH<0,达到平衡后,下列说法正确的是( )
A.取氯水稀释,c(HClO)/c(Cl-)增大
B.100 mL pH=2的新制氯水中:n(OH-)+n(ClO-)+n(HClO)= 0.001mol
C.已知CHCOOH的K=1.75×10-5,CHCOOH溶液的pH一定比HClO溶液的pH小
3 a 3
D.饱和氯水中加入碳酸氢钠固体,上述平衡正向移动,有CO 气体逸出\
2
2.(2023届·浙江省名校协作体高三开学考试)反应A(g) 4B (g)+ C (g),在100℃和T℃时,A的物
质的量浓度(单位: )随时间变化的有关实验数据见下表:
时间/min 0 1 2 3 4 5
100/℃ 0.80 0.55 0.35 0.20 0.15 0.15
T/℃ 1.00 0.65 0.35 0.18 0.18 0.18
下列有关该反应的描述正确的是( )
A.在100℃时,2min内用B表示的化学反应速率为
B.T℃下,3min时反应刚好达到平衡状态
C.根据上表内A浓度变化,可知浓度越大,反应速率越大
D.从表中可以看出
3.(2023届·浙江省七彩阳光新高考研究联盟高三返校联考)已知2NO(g) 2N(g)+ O(g)的速率方程
2 2 2为 (k为速率常数,只与温度、催化剂有关)。实验测得,NO在催化剂X表面反应的变化数据如
2
下:
2
t/min 0 10 30 40 50 60 70
0
0.100 0.080 0.040 0.020 0
下列说法正确的是( )
A.t=10min时,v(N O)= 2.0×10-3 mol·L-1·min-1
2
B.速率方程中n=1,表格中c>c=c
1 2 3
C.相同条件下,增加NO的浓度或催化剂X的表面积,都能加快反应速率
2
D.保持其他条件不变,若起始浓度为 ,当减至一半时共耗时70min
4.(2023届·浙江省普通高校招生高三选考模拟)将xmolH S气体平均分成两份,分别通入容器A、容器
2
B(容积均为1L),其中一容器为绝热环境,另一容器为25℃恒温环境,在容器内均发生:2HS(g) 2H(g)
2 2
+S (g) ΔH>0 (25℃),相关数据如下表:
2
时间/min 0 10 20 30 40 50 60
容器A 0 0.8 1.5 2 2.3 2.4 2.4
容器B 0 1 1.8 2.5 3 3 3
下列说法正确的是( )
A.根据上表信息,可推算出x=3
B.容器A为25℃恒温环境,容器B为绝热环境
C.1~60min内,25℃恒温环境反应速率可表示为v(H S生成)=0.1mol·L-1·min-1
2
D.可通过降低容器的温度,从而加快逆反应的速率,达到抑制HS气体分解的目的
2
5.(2023届·浙江省部分校高三开学摸底考试)甲酸乙酯在OH-存在下发生水解:HCOOC H+OH-
2 5
HCOO-+C HOH,两种反应物的初始浓度均为0.500 mol·L-1,不同温度下测得HCOOC H 的浓度(mol·L-1)随时
2 5 2 5
间变化的数据如表所示。下列有关说法不正确的是( )
t/s 0 120 180 240 330 530 600 700 800
15 ℃ 0.500 0.335 0.291 0.256 0.210 0.156 0.148 0.145 0.145
35 ℃ 0.500 0.325 0.2775 0.238 0.190 … 0.130 0.130 0.130
A.该反应在15 ℃,120 s~180 s区间的v(HCOOC H)为7.33×10-5 mol·L-1·s-1
2 5C.530 s时,表格中35 ℃对应的数据一定是0.130
D.由表中数据可知,温度升高,反应速率加快
D.其他条件不变,提高c(OH-),可使该反应的化学平衡常数增大
6.(2023届·浙江省浙南名校联盟高三上学期第一次联考)某反应A(g)+B(g)→C(g)+D(g)的速率方程为
v=k•cm(A)•cn(B),其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为 。改变反应物浓度时,反应的
瞬时速率如表所示:
c(A)/(mol•L-1) 0.25 0.50 1.00 0.50 1.00 c
1
c(B)/(mol•L-1) 0.050 0.050 0.100 0.100 0.200 c
2
v/(10-3mol•L-1•min-1) 1.6 3.2 v 3.2 v 4.8
1 2
下列说法不正确的是( )
A.上述表格中的c=0.75、v=6.4
1 2
B.该反应的速率常数k=6.4×10-3min-1
C.在过量的B存在时,反应掉93.75%的A所需的时间是500min
D.升温、加入催化剂、缩小容积(加压),使k增大导致反应的瞬时速率加快
7.(2022·河南省部分重点高中高三适应性检测)一氧化氮的氢化还原反应为2NO(g)+2H (g) N(g)
2 2
+2H O(g) H,其正反应速率方程为 ,T℃时,实验得到的一组数据如下表所示:
2
△
实验组 NO起始浓度/ 起始浓度/ 起始时的正反应速率/
别 mol·L-1 mol·L-1 mol·L-1·s-1
Ⅰ
Ⅱ
Ⅲ
下列说法正确的是( )
A.正反应一定为吸热反应 B. ,
C.k的数值为 D.升高温度,k的值减小
8.(2022·辽宁省铁岭市六校高三联考)化学反应进行的方向和限度是化学反应原理所要研究的两个重要问
题,下列有关化学反应进行的方向和限度的说法中不正确的是( )
A.恒温恒容的密闭容器中发生反应mA(g)+nB(g) pC(g),若B是有色物质,A,C均为无色物质,达到平衡后,加入一定量C,体系的颜色会变深
B.一定温度下两个体积相同密闭容器中,分别放有二氧化氮、气态溴,起始时两个容器中气体颜色相同,
若将容器体积压缩至原来的一半,则C >C
NO2 Br2
C.综合考虑反应速率和限度,以及催化剂活性,合成氨一般选择400℃~500℃
D.恒温时,对于反应A(g)+3B(g) 2C(g),起始充入等物质的量的A和B,达到平衡时A的体积分
数为n%,此时若给体系加压为原来的两倍,则A体积分数仍为n%
9.(2023·重庆市南开中学高三模拟)将0.8 mol 放入一个装满O 的恒压密闭容器中,在 、
2
的条件下使之充分反应至t 时刻,此时容器中无S剩余,剩余0.2 mol O。再向该体系中迅速投入 无水
1 2
FeSO 固体,此过程容器与外界未发生气体交换,充分反应至t 时刻。已知此条件下可以发生如下反应:
4 2
S(s)+O(g) SO (g)
2 2
2FeSO (s) Fe O(s)+SO (g)+SO(g) K =8.1×107Pa2
4 2 3 2 3 P2
2SO (g) 2SO (g)+O(g) K =7.2×103Pa
3 2 2 P2
下列说法不正确的是( )
A.t 时刻,容器中气体总物质的量为1.0mol
1
B.t 时刻,容器中S(s)+O(g) SO (g)的分压为
1 2 2
C.起始时,容器中n(O )=1.25mol
2
D.t 时刻,容器中的固体为FeSO 与Fe O 的混合物
2 4 2 3
10.(2022·江苏省常州市八校高三联合调研试题)碳是生命的核心元素,碳及其化合物在工农业生产中有着
广泛的应用。工业上用CO 生产CHOH燃料,其热化学方程式为CO(g)+3H(g) CHOH(g)+H O(g)
2 3 2 2 3 2
H=-49.0kJ·mol-1。燃煤燃烧时生成的CO 用氨的饱和NaCl溶液吸收,可得到NaHCO 等化工产品。CO 会引起
2 3 2
△温室效应,我国力争在2060年前实现“碳中和”。“碳中和”是指企业、团体或个人测算在一定时间内直接或
间接产生的温室气体排放总量,然后通过植物造树造林、节能减排等形式,抵消自身产生的排放量,CO 实现
2
“零排放”。对于反应CO(g)+3H(g) CHOH(g)+H O(g),下列有关说法正确的是( )
2 2 3 2
A.增大 的值,可提高H 的转化率
2
B.升高温度能提高CO 的反应速率和转化率
2
C.达平衡时缩小容器体积, (正)增大, (逆)减小
D.1molCO 和3molH 充分反应时放出的热量为49.0kJ
2 2
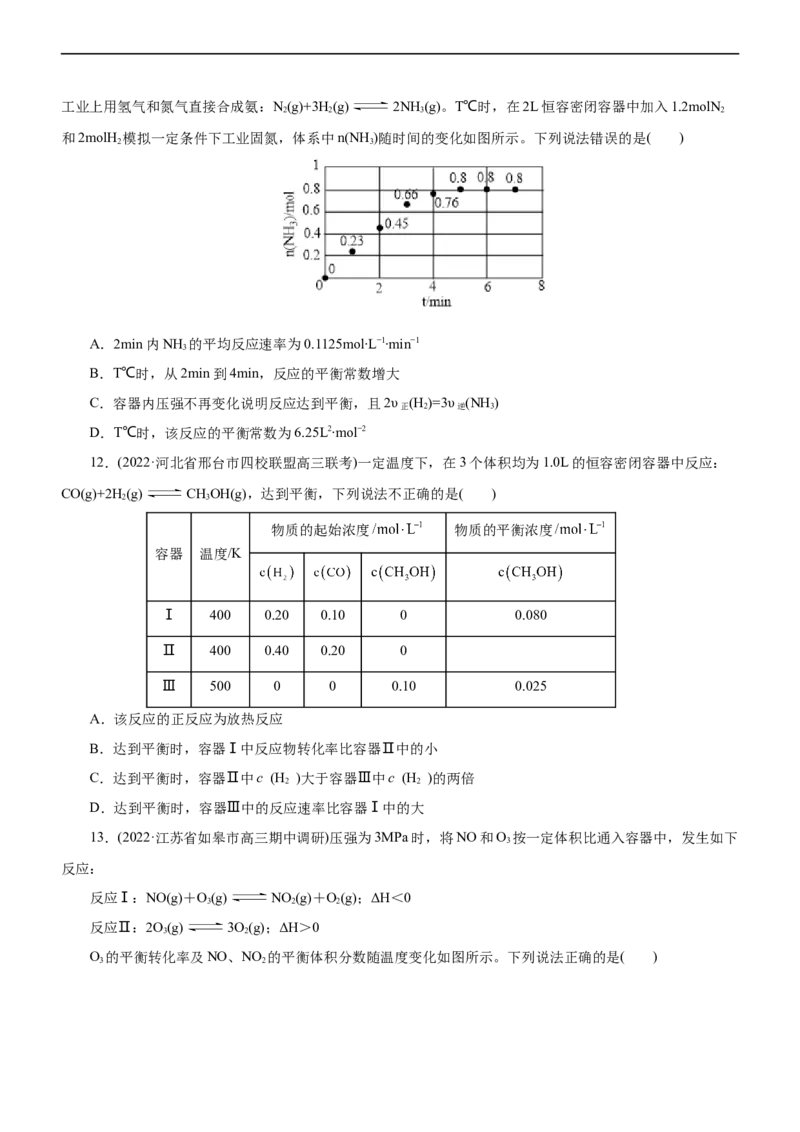
11.(2022·黑龙江省龙东地区四校高三第一次联考)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨:N(g)+3H(g) 2NH (g)。T℃时,在2L恒容密闭容器中加入1.2molN
2 2 3 2
和2molH 模拟一定条件下工业固氮,体系中n(NH )随时间的变化如图所示。下列说法错误的是( )
2 3
A.2min内NH 的平均反应速率为0.1125mol∙L−1∙min−1
3
B.T℃时,从2min到4min,反应的平衡常数增大
C.容器内压强不再变化说明反应达到平衡,且2υ (H )=3υ (NH )
正 2 逆 3
D.T℃时,该反应的平衡常数为6.25L2∙mol−2
12.(2022·河北省邢台市四校联盟高三联考)一定温度下,在3个体积均为1.0L的恒容密闭容器中反应:
CO(g)+2H(g) CHOH(g),达到平衡,下列说法不正确的是( )
2 3
物质的起始浓度 物质的平衡浓度
容器 温度/K
Ⅰ 400 0.20 0.10 0 0.080
Ⅱ 400 0.40 0.20 0
Ⅲ 500 0 0 0.10 0.025
A.该反应的正反应为放热反应
B.达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C.达到平衡时,容器Ⅱ中c (H )大于容器Ⅲ中c (H )的两倍
2 2
D.达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大
13.(2022·江苏省如皋市高三期中调研)压强为3MPa时,将NO和O 按一定体积比通入容器中,发生如下
3
反应:
反应Ⅰ:NO(g)+O(g) NO (g)+O(g);ΔH<0
3 2 2
反应Ⅱ:2O(g) 3O(g);ΔH>0
3 2
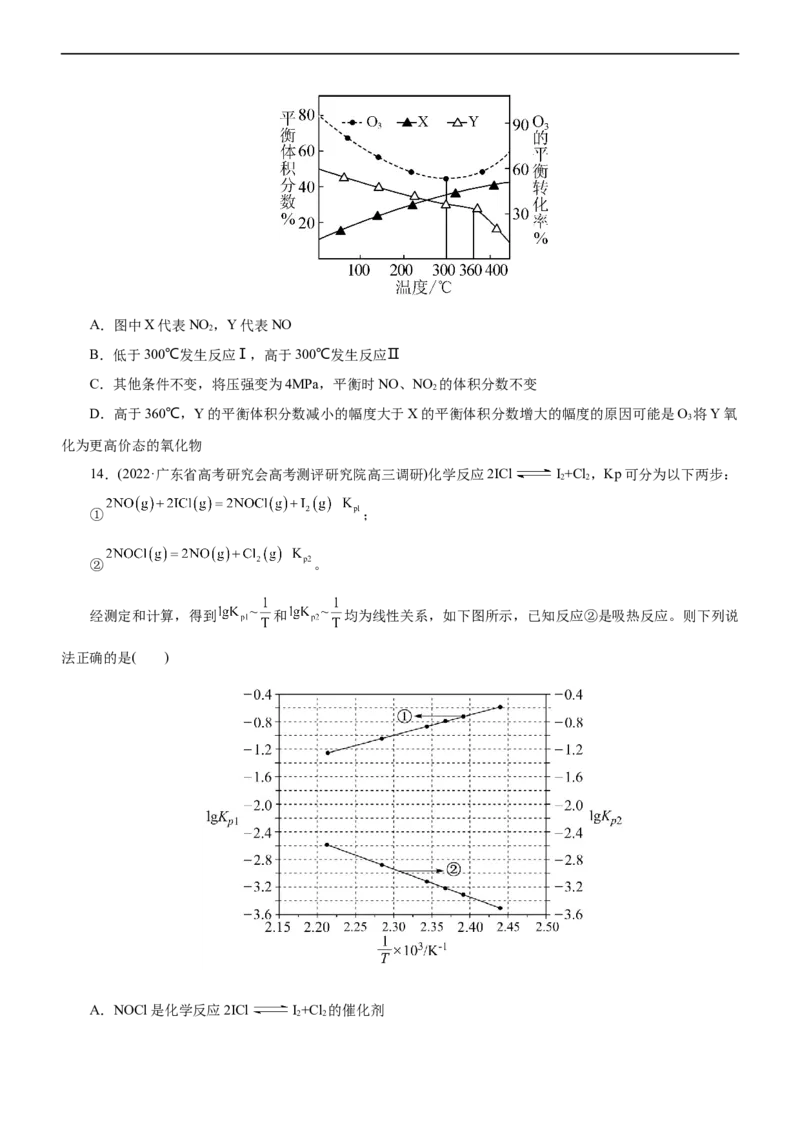
O 的平衡转化率及NO、NO 的平衡体积分数随温度变化如图所示。下列说法正确的是( )
3 2A.图中X代表NO ,Y代表NO
2
B.低于300℃发生反应Ⅰ,高于300℃发生反应Ⅱ
C.其他条件不变,将压强变为4MPa,平衡时NO、NO 的体积分数不变
2
D.高于360℃,Y的平衡体积分数减小的幅度大于X的平衡体积分数增大的幅度的原因可能是O 将Y氧
3
化为更高价态的氧化物
14.(2022·广东省高考研究会高考测评研究院高三调研)化学反应2ICl I+Cl,Kp可分为以下两步:
2 2
① ;
② 。
经测定和计算,得到 和 均为线性关系,如下图所示,已知反应②是吸热反应。则下列说
法正确的是( )
A.NOCl是化学反应2ICl I+Cl 的催化剂
2 2B.图②代表
C.
D.当 时,表明可逆反应2ICl I+Cl 达到了平衡状态
2 2
15.(2022·江苏省百校大联考高三第二次考试)在一定的温度和压强下,将按一定比例混合的CO 和H 通
2 2
过装有催化剂的反应器可得到甲烷。已知:
CO(g)+4H(g)=CH (g)+2HO(g) ΔH=-165kJ·mol-1
2 2 4 2
CO(g)+H(g)=CO(g)+HO(g) ΔH=+41kJ·mol-1
2 2 2
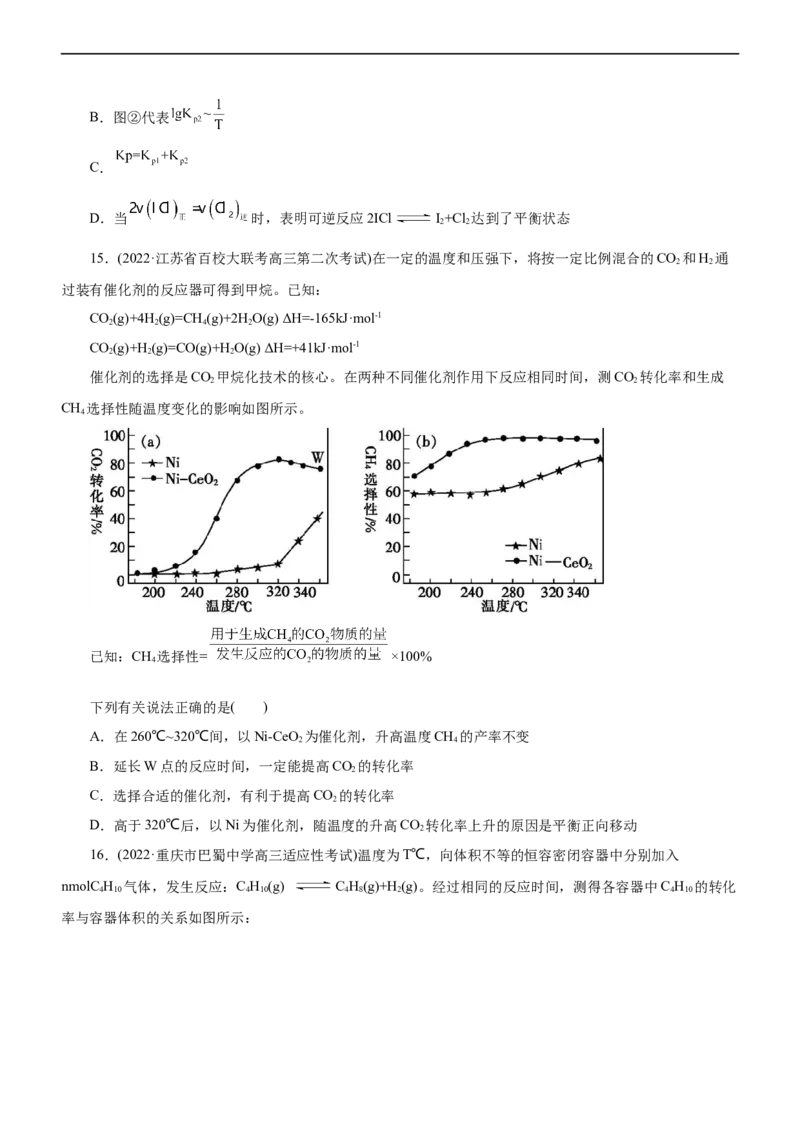
催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测CO 转化率和生成
2 2
CH 选择性随温度变化的影响如图所示。
4
已知:CH 选择性= ×100%
4
下列有关说法正确的是( )
A.在260℃~320℃间,以Ni-CeO 为催化剂,升高温度CH 的产率不变
2 4
B.延长W点的反应时间,一定能提高CO 的转化率
2
C.选择合适的催化剂,有利于提高CO 的转化率
2
D.高于320℃后,以Ni为催化剂,随温度的升高CO 转化率上升的原因是平衡正向移动
2
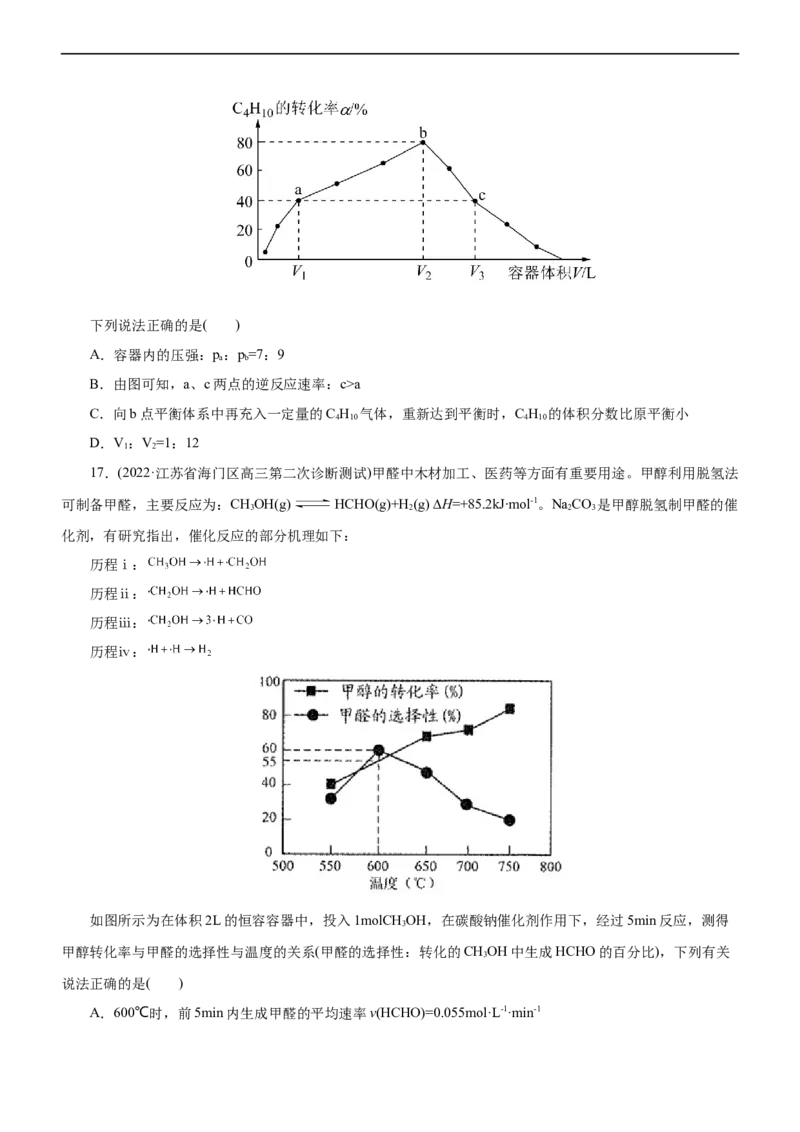
16.(2022·重庆市巴蜀中学高三适应性考试)温度为T℃,向体积不等的恒容密闭容器中分别加入
nmolC H 气体,发生反应:C H (g) C H(g)+H(g)。经过相同的反应时间,测得各容器中C H 的转化
4 10 4 10 4 8 2 4 10
率与容器体积的关系如图所示:下列说法正确的是( )
A.容器内的压强:p:p=7:9
a b
B.由图可知,a、c两点的逆反应速率:c>a
C.向b点平衡体系中再充入一定量的C H 气体,重新达到平衡时,C H 的体积分数比原平衡小
4 10 4 10
D.V:V=1:12
1 2
17.(2022·江苏省海门区高三第二次诊断测试)甲醛中木材加工、医药等方面有重要用途。甲醇利用脱氢法
可制备甲醛,主要反应为:CHOH(g) HCHO(g)+H(g) ∆H=+85.2kJ∙mol-1。NaCO 是甲醇脱氢制甲醛的催
3 2 2 3
化剂,有研究指出,催化反应的部分机理如下:
历程ⅰ:
历程ⅱ:
历程ⅲ:
历程ⅳ:
如图所示为在体积2L的恒容容器中,投入1molCH OH,在碳酸钠催化剂作用下,经过5min反应,测得
3
甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的CHOH中生成HCHO的百分比),下列有关
3
说法正确的是( )
A.600℃时,前5min内生成甲醛的平均速率v(HCHO)=0.055mol·L-1·min-1B.700℃时,反应历程ⅱ的速率小于反应历程ⅲ的速率
C.脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D.反应历程ⅰ的活化能大于CHOH(g) HCHO(g)+H(g)的活化能
3 2
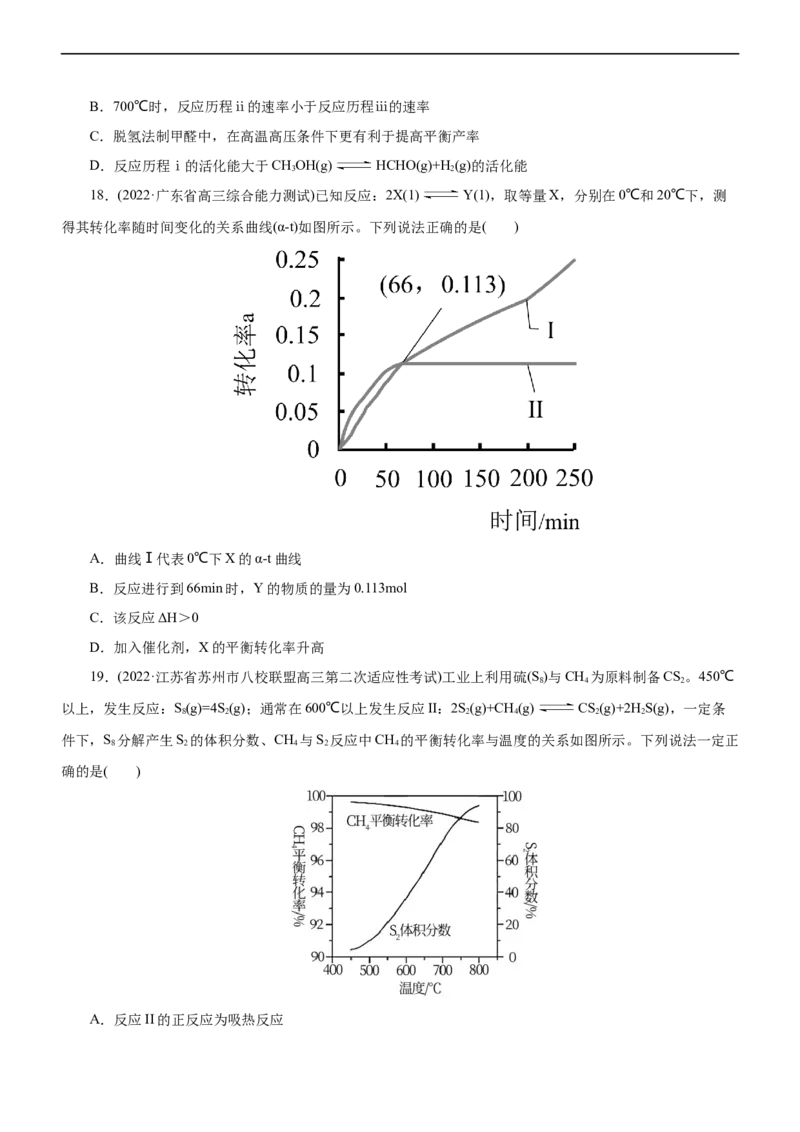
18.(2022·广东省高三综合能力测试)已知反应:2X(1) Y(1),取等量X,分别在0℃和20℃下,测
得其转化率随时间变化的关系曲线(α-t)如图所示。下列说法正确的是( )
A.曲线Ⅰ代表0℃下X的α-t曲线
B.反应进行到66min时,Y的物质的量为0.113mol
C.该反应ΔH>0
D.加入催化剂,X的平衡转化率升高
19.(2022·江苏省苏州市八校联盟高三第二次适应性考试)工业上利用硫(S )与CH 为原料制备CS。450℃
8 4 2
以上,发生反应:S(g)=4S (g);通常在600℃以上发生反应II:2S(g)+CH (g) CS(g)+2HS(g),一定条
8 2 2 4 2 2
件下,S 分解产生S 的体积分数、CH 与S 反应中CH 的平衡转化率与温度的关系如图所示。下列说法一定正
8 2 4 2 4
确的是( )
A.反应II的正反应为吸热反应B.在恒温密闭容器中,反应相同时间,温度越低,CH 的转化率越大
4
C.发生反应II温度不低于600℃的原因是:此温度CH 平衡转化率已很高;低于此温度,S 浓度小,反
4 2
应速率慢
D.某温度下若S 完全分解成S,在密闭容器中,n(S )∶n(CH)=2∶1开始反应,当CS 体积分数为10%
8 2 2 4 2
时,CH 转化率为43%
4
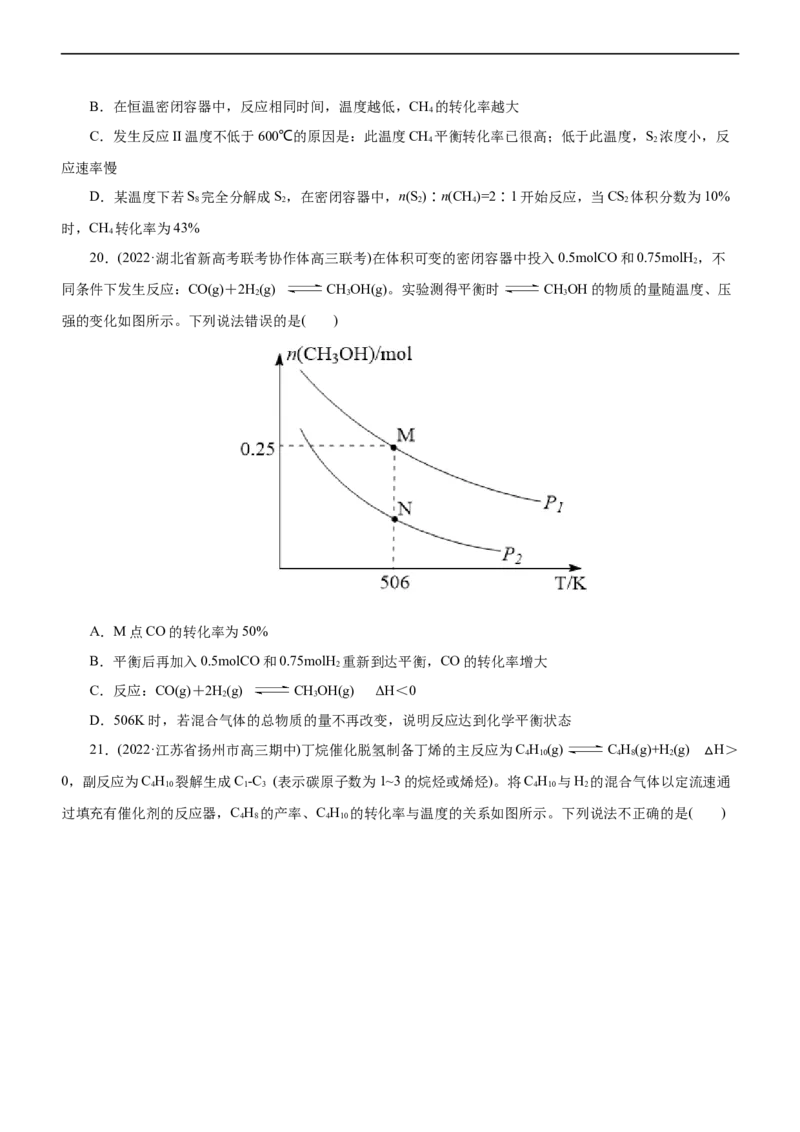
20.(2022·湖北省新高考联考协作体高三联考)在体积可变的密闭容器中投入0.5molCO和0.75molH,不
2
同条件下发生反应:CO(g)+2H(g) CHOH(g)。实验测得平衡时 CHOH的物质的量随温度、压
2 3 3
强的变化如图所示。下列说法错误的是( )
A.M点CO的转化率为50%
B.平衡后再加入0.5molCO和0.75molH 重新到达平衡,CO的转化率增大
2
C.反应:CO(g)+2H(g) CHOH(g) ΔH<0
2 3
D.506K时,若混合气体的总物质的量不再改变,说明反应达到化学平衡状态
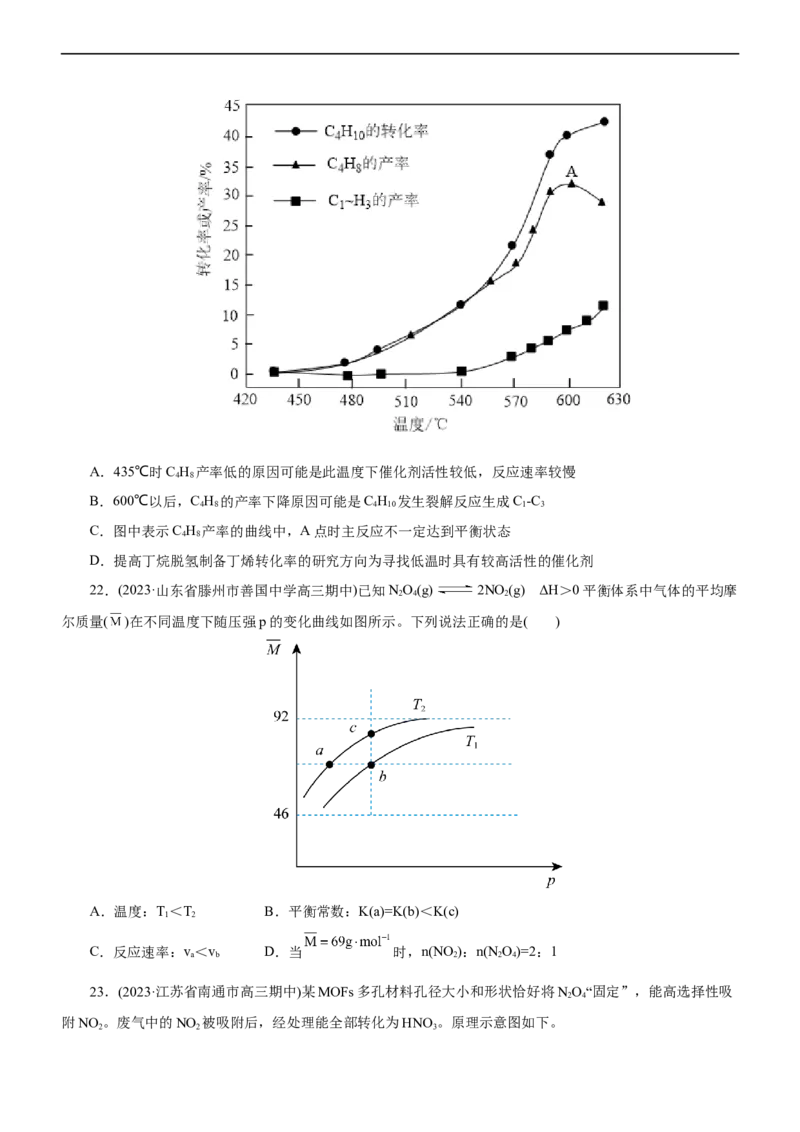
21.(2022·江苏省扬州市高三期中)丁烷催化脱氢制备丁烯的主反应为C H (g) C H(g)+H(g) H>
4 10 4 8 2
0,副反应为C H 裂解生成C -C (表示碳原子数为1~3的烷烃或烯烃)。将C H 与H 的混合气体以定流速△通
4 10 1 3 4 10 2
过填充有催化剂的反应器,C H 的产率、C H 的转化率与温度的关系如图所示。下列说法不正确的是( )
4 8 4 10A.435℃时C H 产率低的原因可能是此温度下催化剂活性较低,反应速率较慢
4 8
B.600℃以后,C H 的产率下降原因可能是C H 发生裂解反应生成C -C
4 8 4 10 1 3
C.图中表示C H 产率的曲线中,A点时主反应不一定达到平衡状态
4 8
D.提高丁烷脱氢制备丁烯转化率的研究方向为寻找低温时具有较高活性的催化剂
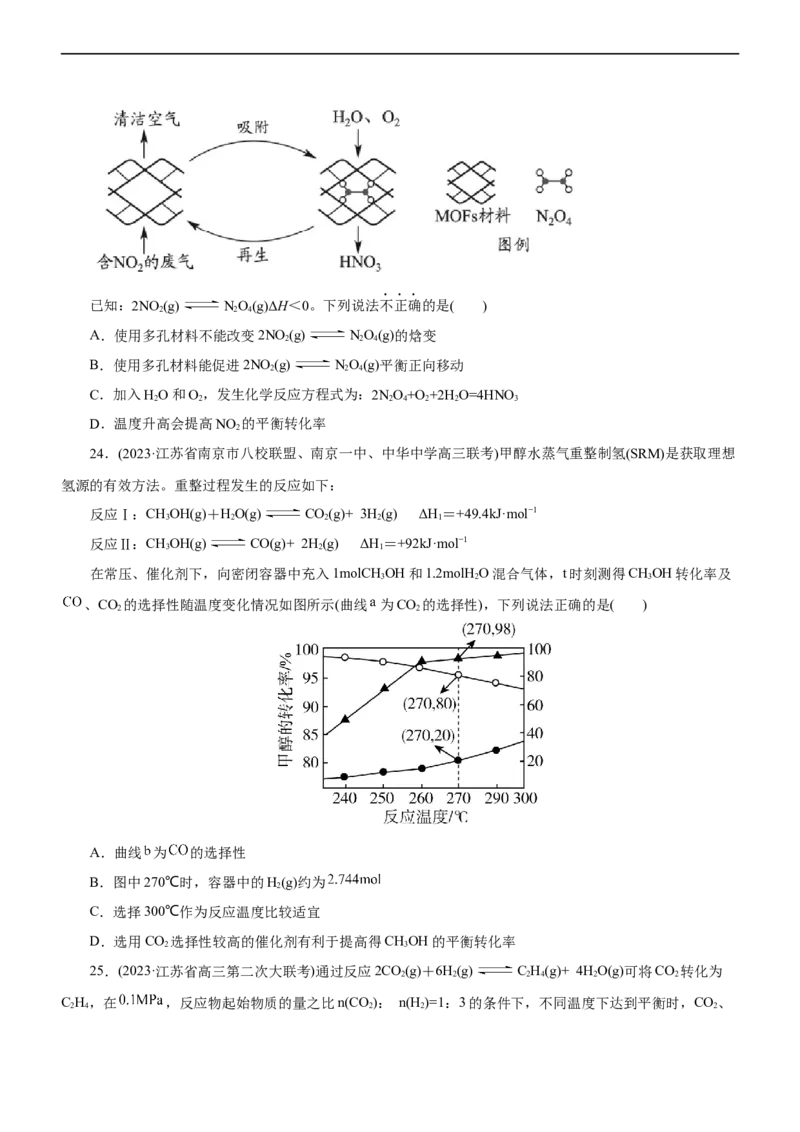
22.(2023·山东省滕州市善国中学高三期中)已知NO(g) 2NO (g) ΔH>0平衡体系中气体的平均摩
2 4 2
尔质量( )在不同温度下随压强p的变化曲线如图所示。下列说法正确的是( )
A.温度:T<T B.平衡常数:K(a)=K(b)<K(c)
1 2
C.反应速率:v<v D.当 时,n(NO ):n(N O)=2:1
a b 2 2 4
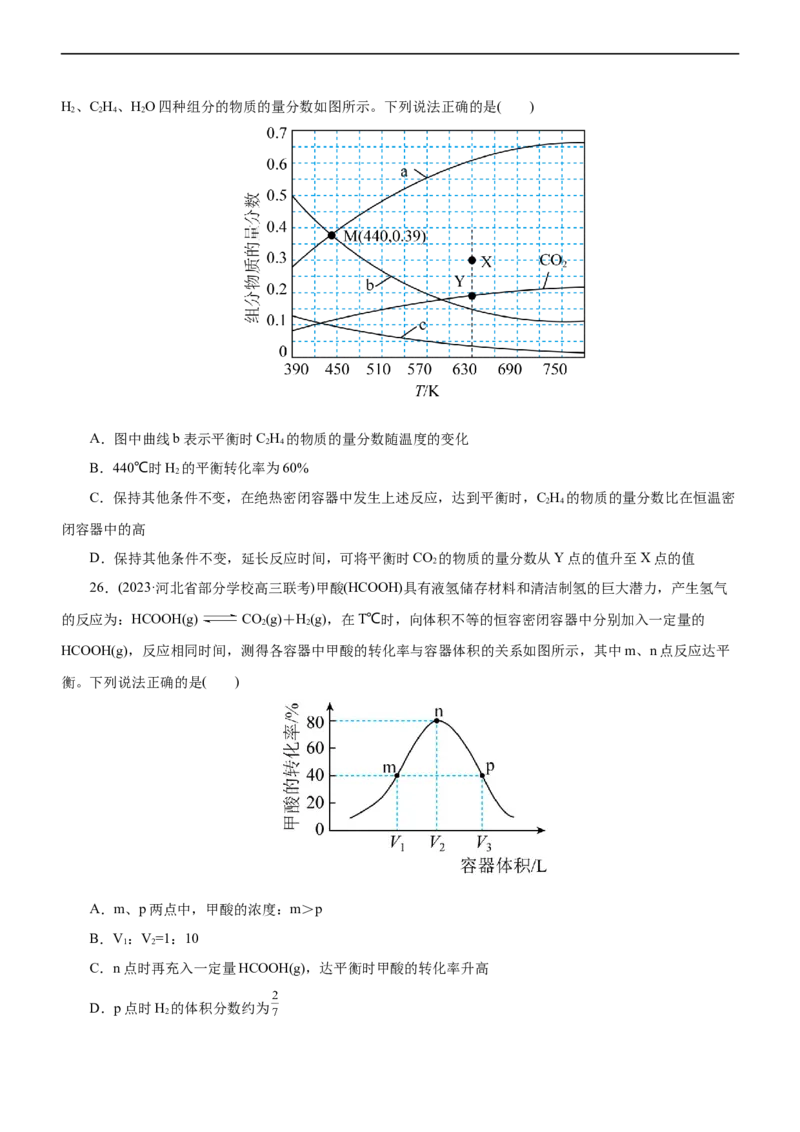
23.(2023·江苏省南通市高三期中)某MOFs多孔材料孔径大小和形状恰好将NO“固定”,能高选择性吸
2 4
附NO 。废气中的NO 被吸附后,经处理能全部转化为HNO。原理示意图如下。
2 2 3已知:2NO (g) NO(g)ΔH<0。下列说法不正确的是( )
2 2 4
A.使用多孔材料不能改变2NO (g) NO(g)的焓变
2 2 4
B.使用多孔材料能促进2NO (g) NO(g)平衡正向移动
2 2 4
C.加入HO和O,发生化学反应方程式为:2NO+O +2H O=4HNO
2 2 2 4 2 2 3
D.温度升高会提高NO 的平衡转化率
2
24.(2023·江苏省南京市八校联盟、南京一中、中华中学高三联考)甲醇水蒸气重整制氢(SRM)是获取理想
氢源的有效方法。重整过程发生的反应如下:
反应Ⅰ:CHOH(g)+HO(g) CO(g)+ 3H(g) ΔH=+49.4kJ·mol−1
3 2 2 2 1
反应Ⅱ:CHOH(g) CO(g)+ 2H(g) ΔH=+92kJ·mol−1
3 2 1
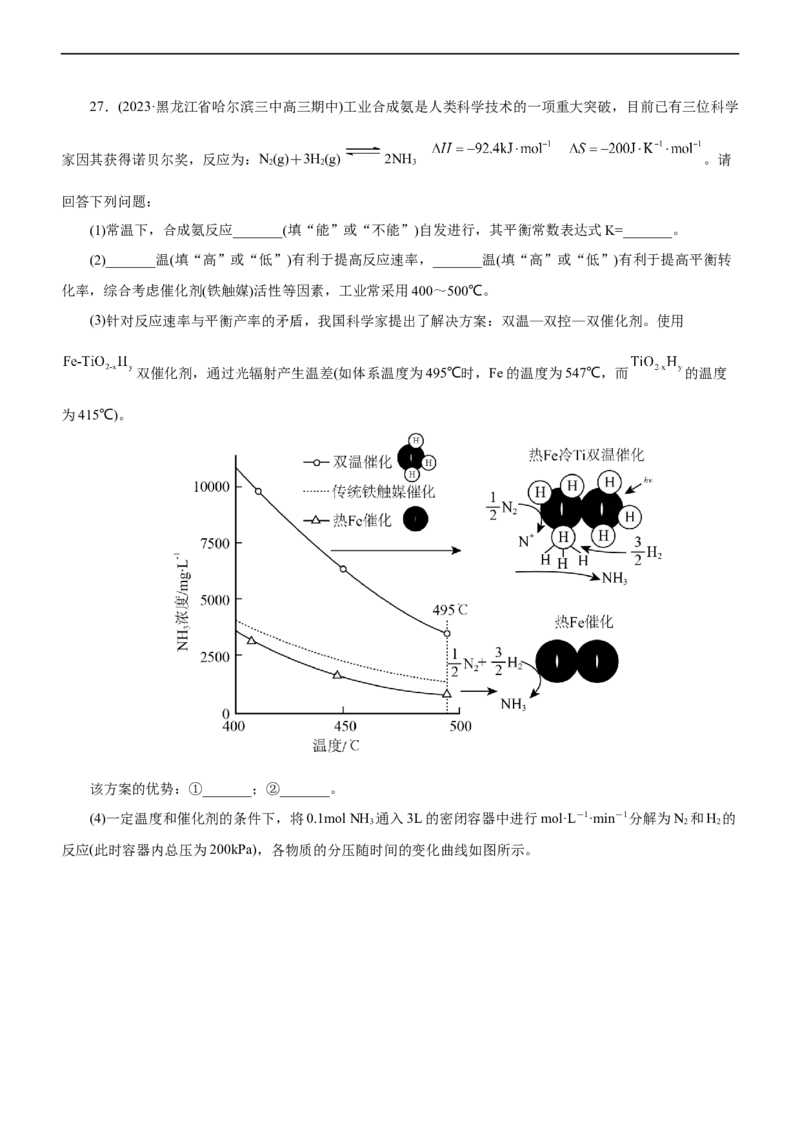
在常压、催化剂下,向密闭容器中充入1molCH OH和1.2molH O混合气体,t时刻测得CHOH转化率及
3 2 3
、CO 的选择性随温度变化情况如图所示(曲线 为CO 的选择性),下列说法正确的是( )
2 2
A.曲线 为 的选择性
B.图中270℃时,容器中的H(g)约为
2
C.选择300℃作为反应温度比较适宜
D.选用CO 选择性较高的催化剂有利于提高得CHOH的平衡转化率
2 3
25.(2023·江苏省高三第二次大联考)通过反应2CO(g)+6H(g) C H(g)+ 4HO(g)可将CO 转化为
2 2 2 4 2 2
C H,在 ,反应物起始物质的量之比n(CO): n(H )=1:3的条件下,不同温度下达到平衡时,CO、
2 4 2 2 2H、C H、HO四种组分的物质的量分数如图所示。下列说法正确的是( )
2 2 4 2
A.图中曲线b表示平衡时C H 的物质的量分数随温度的变化
2 4
B.440℃时H 的平衡转化率为60%
2
C.保持其他条件不变,在绝热密闭容器中发生上述反应,达到平衡时,C H 的物质的量分数比在恒温密
2 4
闭容器中的高
D.保持其他条件不变,延长反应时间,可将平衡时CO 的物质的量分数从Y点的值升至X点的值
2
26.(2023·河北省部分学校高三联考)甲酸(HCOOH)具有液氢储存材料和清洁制氢的巨大潜力,产生氢气
的反应为:HCOOH(g) CO(g)+H(g),在T℃时,向体积不等的恒容密闭容器中分别加入一定量的
2 2
HCOOH(g),反应相同时间,测得各容器中甲酸的转化率与容器体积的关系如图所示,其中m、n点反应达平
衡。下列说法正确的是( )
A.m、p两点中,甲酸的浓度:m>p
B.V:V=1:10
1 2
C.n点时再充入一定量HCOOH(g),达平衡时甲酸的转化率升高
D.p点时H 的体积分数约为
227.(2023·黑龙江省哈尔滨三中高三期中)工业合成氨是人类科学技术的一项重大突破,目前已有三位科学
家因其获得诺贝尔奖,反应为:N(g)+3H(g) 2NH 。请
2 2 3
回答下列问题:
(1)常温下,合成氨反应_______(填“能”或“不能”)自发进行,其平衡常数表达式K=_______。
(2)_______温(填“高”或“低”)有利于提高反应速率,_______温(填“高”或“低”)有利于提高平衡转
化率,综合考虑催化剂(铁触媒)活性等因素,工业常采用400~500℃。
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用
双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而 的温度
为415℃)。
该方案的优势:①_______;②_______。
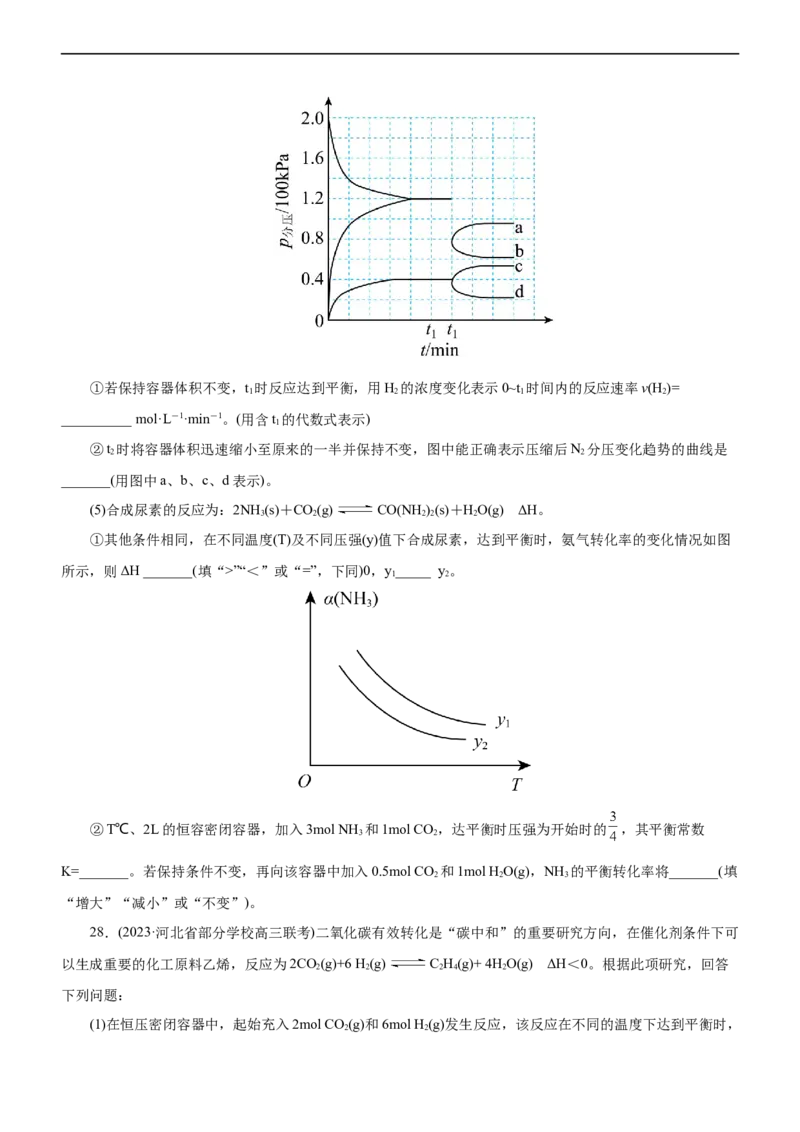
(4)一定温度和催化剂的条件下,将0.1mol NH 通入3L的密闭容器中进行mol·L-1·min-1分解为N 和H 的
3 2 2
反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。①若保持容器体积不变,t 时反应达到平衡,用H 的浓度变化表示0~t 时间内的反应速率v(H )=
1 2 1 2
__________mol·L-1·min-1。(用含t 的代数式表示)
1
②t 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N 分压变化趋势的曲线是
2 2
_______(用图中a、b、c、d表示)。
(5)合成尿素的反应为:2NH (s)+CO(g) CO(NH)(s)+HO(g) ΔH。
3 2 2 2 2
①其他条件相同,在不同温度(T)及不同压强(y)值下合成尿素,达到平衡时,氨气转化率的变化情况如图
所示,则ΔH _______(填“>”“<”或“=”,下同)0,y_____ y 。
1 2
②T℃、2L的恒容密闭容器,加入3mol NH 和1mol CO,达平衡时压强为开始时的 ,其平衡常数
3 2
K=_______。若保持条件不变,再向该容器中加入0.5mol CO 和1mol HO(g),NH 的平衡转化率将_______(填
2 2 3
“增大”“减小”或“不变”)。
28.(2023·河北省部分学校高三联考)二氧化碳有效转化是“碳中和”的重要研究方向,在催化剂条件下可
以生成重要的化工原料乙烯,反应为2CO(g)+6 H (g) C H(g)+ 4H O(g) ΔH<0。根据此项研究,回答
2 2 2 4 2
下列问题:
(1)在恒压密闭容器中,起始充入2mol CO(g)和6mol H(g)发生反应,该反应在不同的温度下达到平衡时,
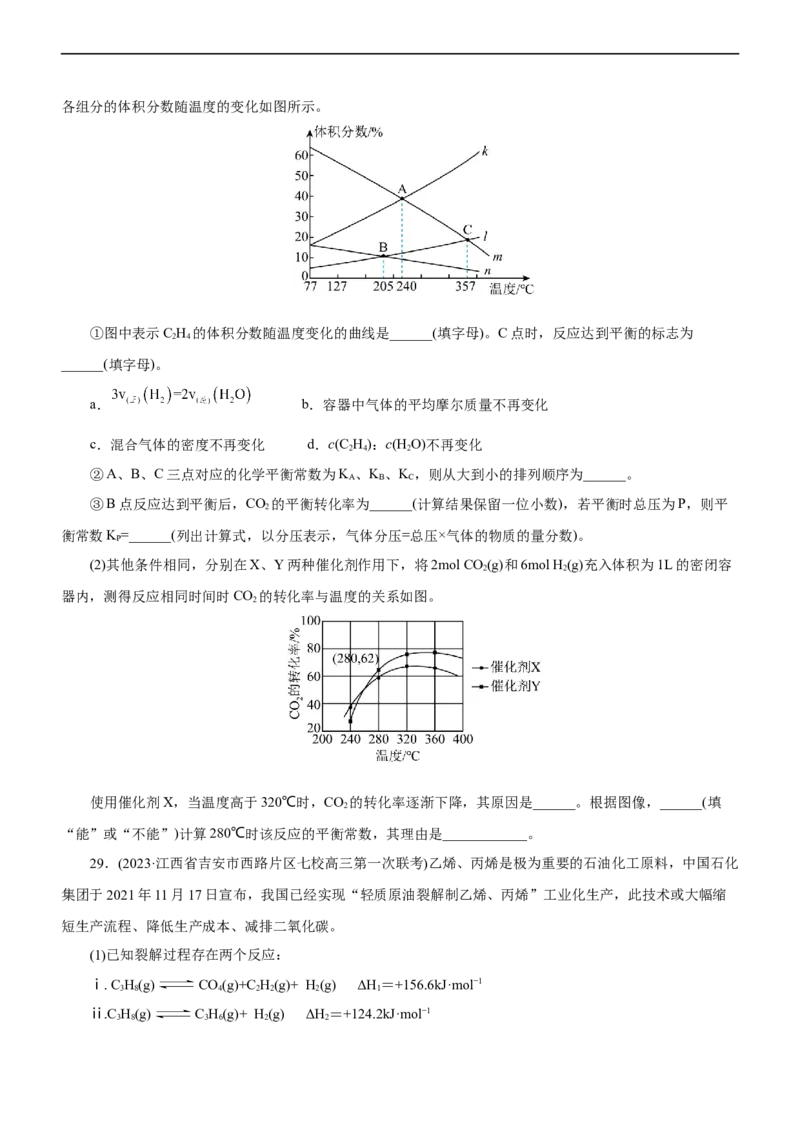
2 2各组分的体积分数随温度的变化如图所示。
①图中表示C H 的体积分数随温度变化的曲线是______(填字母)。C点时,反应达到平衡的标志为
2 4
______(填字母)。
a. b.容器中气体的平均摩尔质量不再变化
c.混合气体的密度不再变化 d.c(C H):c(H O)不再变化
2 4 2
②A、B、C三点对应的化学平衡常数为K 、K 、K ,则从大到小的排列顺序为______。
A B C
③B点反应达到平衡后,CO 的平衡转化率为______(计算结果保留一位小数),若平衡时总压为P,则平
2
衡常数K =______(列出计算式,以分压表示,气体分压=总压×气体的物质的量分数)。
P
(2)其他条件相同,分别在X、Y两种催化剂作用下,将2mol CO(g)和6mol H(g)充入体积为1L的密闭容
2 2
器内,测得反应相同时间时CO 的转化率与温度的关系如图。
2
使用催化剂X,当温度高于320℃时,CO 的转化率逐渐下降,其原因是______。根据图像,______(填
2
“能”或“不能”)计算280℃时该反应的平衡常数,其理由是____________。
29.(2023·江西省吉安市西路片区七校高三第一次联考)乙烯、丙烯是极为重要的石油化工原料,中国石化
集团于2021年11月17日宣布,我国已经实现“轻质原油裂解制乙烯、丙烯”工业化生产,此技术或大幅缩
短生产流程、降低生产成本、减排二氧化碳。
(1)已知裂解过程存在两个反应:
ⅰ. C H(g) CO(g)+C H(g)+ H(g) ΔH=+156.6kJ·mol−1
3 8 4 2 2 2 1
ⅱ.C H(g) C H(g)+ H(g) ΔH=+124.2kJ·mol−1
3 8 3 6 2 2则C H(g) C H(g)+ CH(g) ΔH=_______;下列措施最有可能提高丙烯产率的是_______(填标号)。
3 6 2 2 4
A.减小压强 B.分离出H
2
C.升高温度 D.使用对丙烯高选择性的催化剂
(2)一定条件下,向某密闭容器中通入 的丁烷,控制适当条件使其发生如下反应:C H (g)
4 10
C H(g)+ C H(g) ΔH,测得丁烷的平衡转化率随温度、压强的变化如下图所示:
2 4 2 6
①X表示_______ (填“温度”或“压强”),Y_______Y(填“>”或“<”),该反应为焓_______ (填“增”
1 2
或“减”)反应。
②A点对应的压强为 ,若反应从开始到恰好达到平衡状态所用时间为 ,则v(C H )= _______
4 10
,此温度下平衡常数 _______,A、B、C三点对应的平衡常数 的大小关
系为_______。(K 为用分压表示的平衡常数,分压=总压×物质的量分数)
P
30.(2023·山东省实验中学高三第二次诊断考试))研究氮、碳及其化合物的资源化利用具有重要的意义。
回答下列问题:
(1)已知氢气还原氮气合成氨低温下自发发生。若将2.0 mol N 和6.0molH 通入体积为1L的密闭容器中,
2 2分别在T 和T 温度下进行反应。曲线A表示T 温度下n(H )的变化,曲线B表示T 温度下n(NH )的变化,T
1 2 2 2 1 3 2
温度下反应到a点恰好达到平衡。
①温度T______(填“>”“<”或“=”下同) T 。T 温度下恰好平衡时,曲线B上的点为b(m,n),则
1 2 1
m______12,n_____2;
②T 温度下,若某时刻容器内气体的压强为起始时的80%,则此时v(正)________(填“>”“<”或“=”)v(逆)。
2
(2)以焦炭为原料,在高温下与水蒸气反应可制得水煤气,涉及反应如下:
I.C(s)+HO(g) CO(g)+ H(g) ΔH=+131.3kJ·mol−1 K
2 2 1 1
II.C(s)+2HO(g) CO(g)+ 2H(g) ΔH=+90.3kJ·mol−1 K
2 2 2 1 2
III.CO(g)+ HO(g) CO(g)+H(g) ΔH =-41.0kJ·mol−1 K
2 2 2 3 3
三个反应的平衡常数随温度变化的关系如图所示,则表示K、K 的曲线依次是_______、_______。
1 3
(3) CO 在Cu-ZnO催化下,同时发生以下反应,是解决能源短缺的重要手段。
2
I.CO(g)+3H(g) CHOH(g)+HO(g) ΔH <0
2 2 3 2 1
II.CO(g)+H(g) CO(g)+HO(g) ΔH >0
2 2 2 2
在容积不变的密闭容器中,保持温度不变,充入一定量的CO 和H,起始及达平衡时,容器内各气体的
2 2
物质的量及总压强如下表所示:
CO H CHOH CO HO 总压强/kPa
2 2 3 2
起始/mol 0.5 0.9 0 0 0
平衡/mol 0.3
若容器内反应I、II均达到平衡时, ,反应①的平衡常数K =______(kPa)-2。(用含p的式子表示,
P
分压=总压×气体物质的量分数)31.(2022·上海市杨浦区高三调研)氧硫化碳( ),用于合成除草剂、杀虫剂等,还能作为粮食熏蒸剂。
完成下列填空:
(1) 的结构与二氧化碳类似, 的电子式为:___________; 是___________分子(填“极性”或
“非极性”)。
、CO 分别与HS反应均能制得COS,反应如下:
2 2
反应Ⅰ:CO(g)+HS (g) COS(g)+H(g)+Q
2 2 1
反应Ⅱ:CO(g)+HS (g) COS(g)+HO(g)+Q
2 2 2 2
已知:在相同条件下,
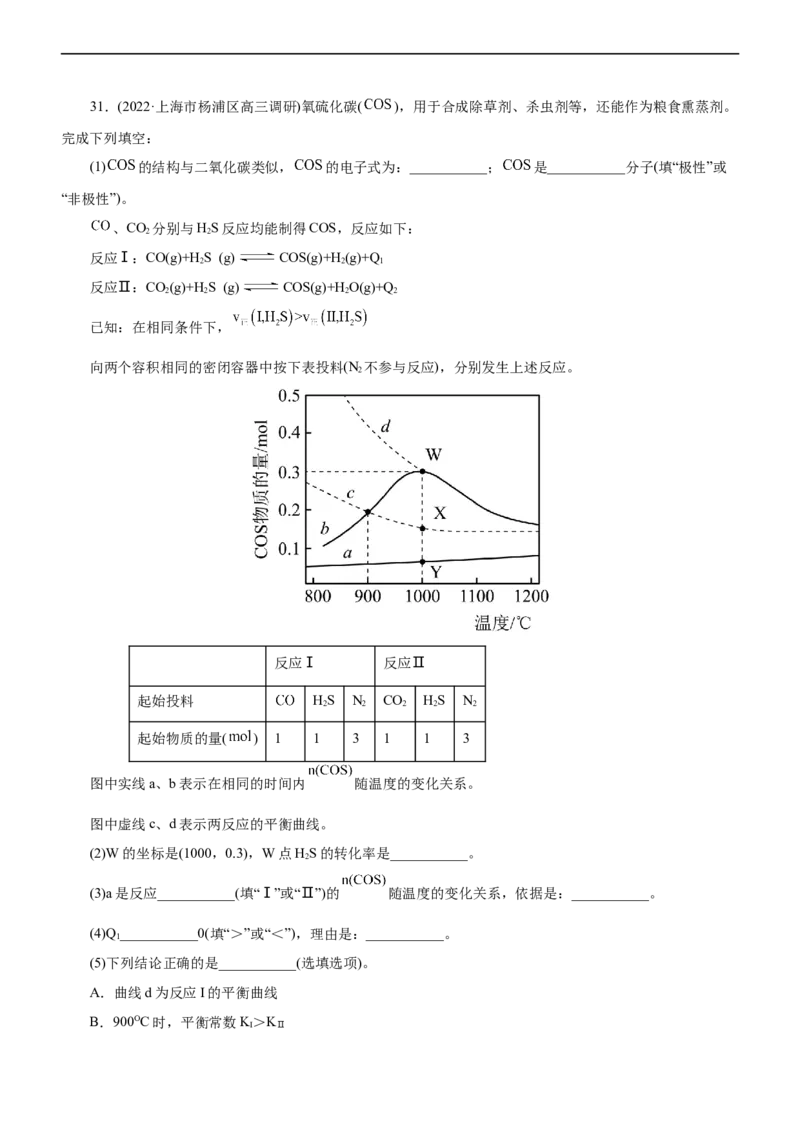
向两个容积相同的密闭容器中按下表投料(N 不参与反应),分别发生上述反应。
2
反应Ⅰ 反应Ⅱ
起始投料 HS N CO HS N
2 2 2 2 2
起始物质的量( ) 1 1 3 1 1 3
图中实线a、b表示在相同的时间内 随温度的变化关系。
图中虚线c、d表示两反应的平衡曲线。
(2)W的坐标是(1000,0.3),W点HS的转化率是___________。
2
(3)a是反应___________(填“Ⅰ”或“Ⅱ”)的 随温度的变化关系,依据是:___________。
(4)Q ___________0(填“>”或“<”),理由是:___________。
1
(5)下列结论正确的是___________(选填选项)。
A.曲线d为反应I的平衡曲线
B.900OC时,平衡常数K>K
I ⅡC.相同条件下,延长反应时间也不能使反应体系中Y点COS的量达到W点
D.恒温恒容下,向W点表示的反应体系中增大n(N),能提高HS的转化率
2 2
32.(2022·山东省青岛市高三期中教学质量检测)CO 是一种主要温室气体,研究CO 的利用对促进低碳社
2 2
会构建具有重要的意义。
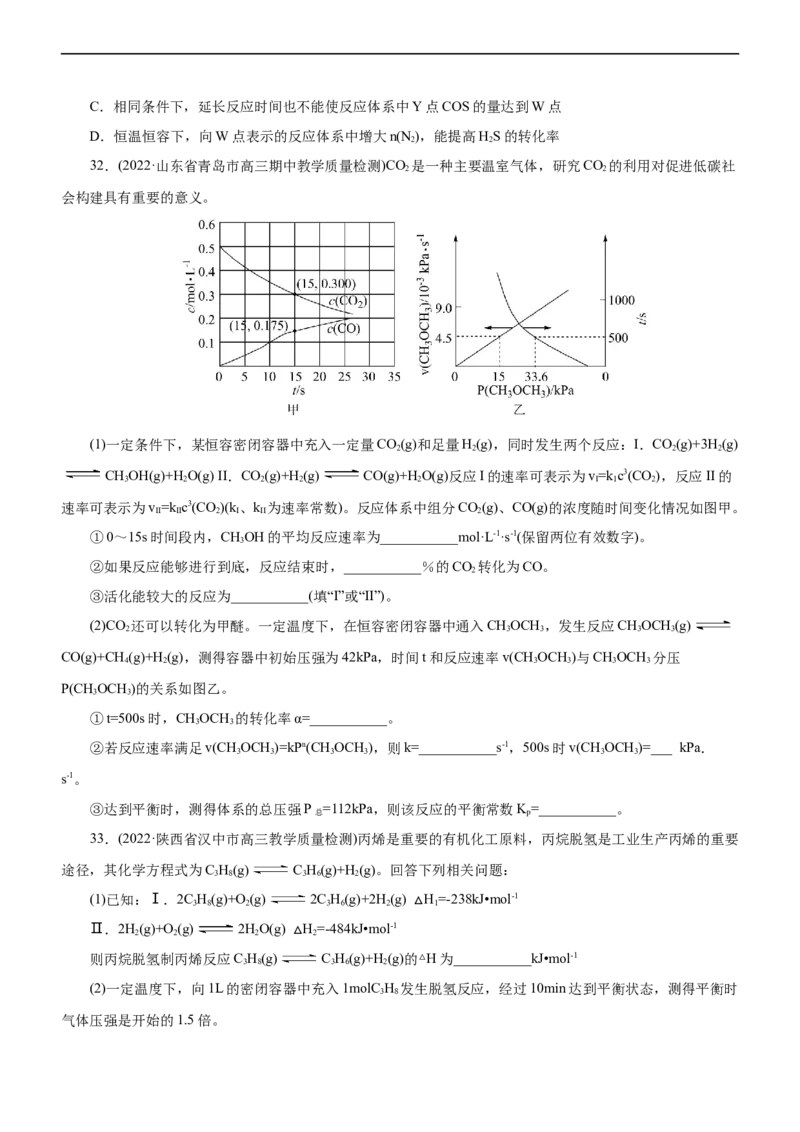
(1)一定条件下,某恒容密闭容器中充入一定量CO(g)和足量H(g),同时发生两个反应:I.CO(g)+3H(g)
2 2 2 2
CHOH(g)+H O(g) II.CO(g)+H(g) CO(g)+HO(g)反应I的速率可表示为v=kc3(CO),反应II的
3 2 2 2 2 I 1 2
速率可表示为v =k c3(CO)(k、k 为速率常数)。反应体系中组分CO(g)、CO(g)的浓度随时间变化情况如图甲。
II II 2 I II 2
①0~15s时间段内,CHOH的平均反应速率为___________mol·L-1·s-1(保留两位有效数字)。
3
②如果反应能够进行到底,反应结束时,___________%的CO 转化为CO。
2
③活化能较大的反应为___________(填“I”或“II”)。
(2)CO 还可以转化为甲醚。一定温度下,在恒容密闭容器中通入CHOCH ,发生反应CHOCH (g)
2 3 3 3 3
CO(g)+CH(g)+H(g),测得容器中初始压强为42kPa,时间t和反应速率v(CHOCH )与CHOCH 分压
4 2 3 3 3 3
P(CH OCH )的关系如图乙。
3 3
①t=500s时,CHOCH 的转化率α=___________。
3 3
②若反应速率满足v(CHOCH )=kPn(CHOCH ),则k=___________s-1,500s时v(CHOCH )=___ kPa.
3 3 3 3 3 3
s-1。
③达到平衡时,测得体系的总压强P =112kPa,则该反应的平衡常数K=___________。
总 p
33.(2022·陕西省汉中市高三教学质量检测)丙烯是重要的有机化工原料,丙烷脱氢是工业生产丙烯的重要
途径,其化学方程式为C H(g) C H(g)+H(g)。回答下列相关问题:
3 8 3 6 2
(1)已知:Ⅰ.2C H(g)+O(g) 2C H(g)+2H(g) H=-238kJ•mol-1
3 8 2 3 6 2 1
Ⅱ.2H 2 (g)+O 2 (g) 2H 2 O(g) H 2 =-484kJ•mol-1 △
则丙烷脱氢制丙烯反应C 3 H 8 (g) △ C 3 H 6 (g)+H 2 (g)的△H为___________kJ•mol-1
(2)一定温度下,向1L的密闭容器中充入1molC H 发生脱氢反应,经过10min达到平衡状态,测得平衡时
3 8
气体压强是开始的1.5倍。①0~10min丙烯的化学反应速率v(C H)=___________mol•L-1•min-1
3 6 。
②下列情况能说明该反应达到平衡状态的是___________。
A.△H不变 B.C H 与H 的物质的量之比保持不变
3 6 2
C.混合气体的总压强不变 D.c(C H) =c(C H)
3 6 正 3 6 逆
③欲提高丙烷转化率,采取的措施是___________(填字母标号)。
A.降低温度 B.升高温度 C.加催化剂 D.及时分离出H
2
④若在恒温、恒压的密闭容器中充入丙烷和氩气发生脱氢反应,起始n(氩气)/n(丙烷)越大,丙烷的平衡转
化率越大,其原因是___________。
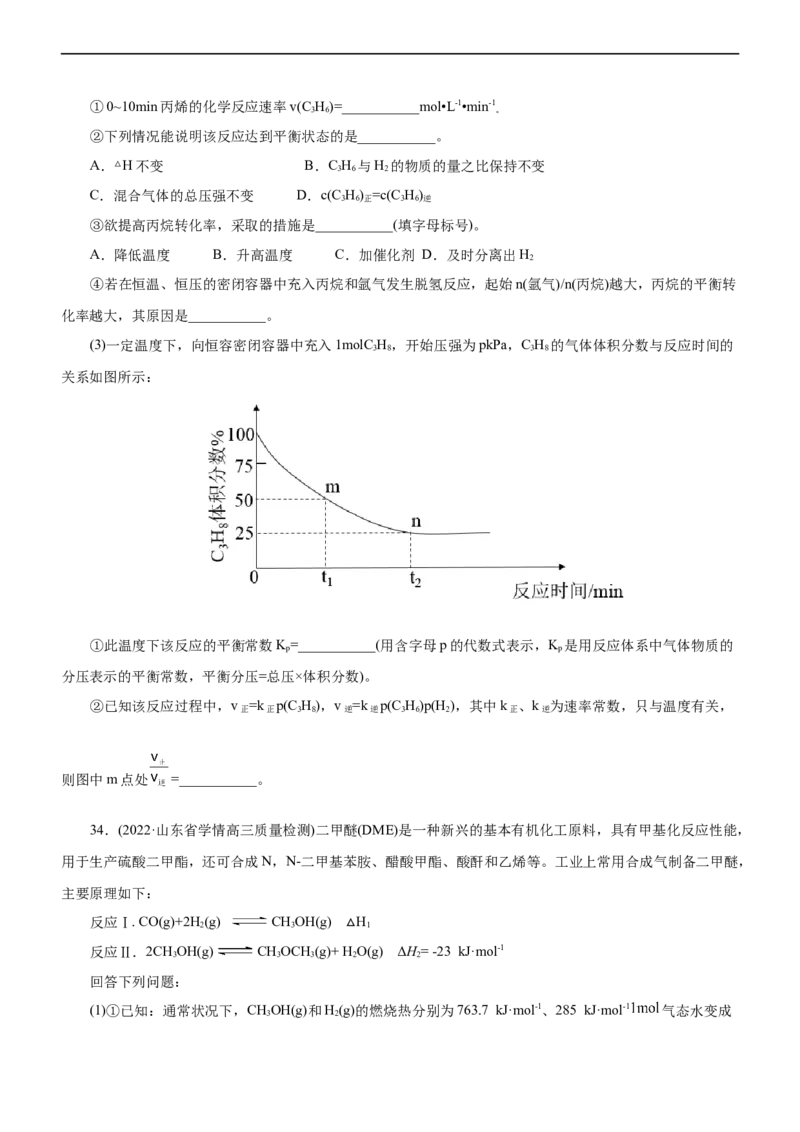
(3)一定温度下,向恒容密闭容器中充入1molC H,开始压强为pkPa,C H 的气体体积分数与反应时间的
3 8 3 8
关系如图所示:
①此温度下该反应的平衡常数K=___________(用含字母p的代数式表示,K 是用反应体系中气体物质的
p p
分压表示的平衡常数,平衡分压=总压×体积分数)。
②已知该反应过程中,v =k p(C H),v =k p(C H)p(H ),其中k 、k 为速率常数,只与温度有关,
正 正 3 8 逆 逆 3 6 2 正 逆
则图中m点处 =___________。
34.(2022·山东省学情高三质量检测)二甲醚(DME)是一种新兴的基本有机化工原料,具有甲基化反应性能,
用于生产硫酸二甲酯,还可合成N,N-二甲基苯胺、醋酸甲酯、酸酐和乙烯等。工业上常用合成气制备二甲醚,
主要原理如下:
反应Ⅰ. CO(g)+2H (g) CHOH(g) H
2 3 1
反应Ⅱ.2CH
3
OH(g) CH
3
OCH
3
(g)+ H△2 O(g) ΔH
2
= -23 kJ·mol-1
回答下列问题:
(1)①已知:通常状况下,CHOH(g)和H(g)的燃烧热分别为763.7 kJ·mol-1、285 kJ·mol-1 气态水变成
3 2液态放出44kJ的热量,则CHOH(g)燃烧热为___________
3
②若有反应Ⅱ活化能Ea(正)为 ,则该反应的活化能Ea (逆)为___________kJ/mol
③反应达平衡后采取下列措施,能提高CHOCH 产率的有__________(填字母代号)。
3 3
A.升高温度 B.增大压强 C.加入CHOH
3
D.移出HO E.使用催化剂
2
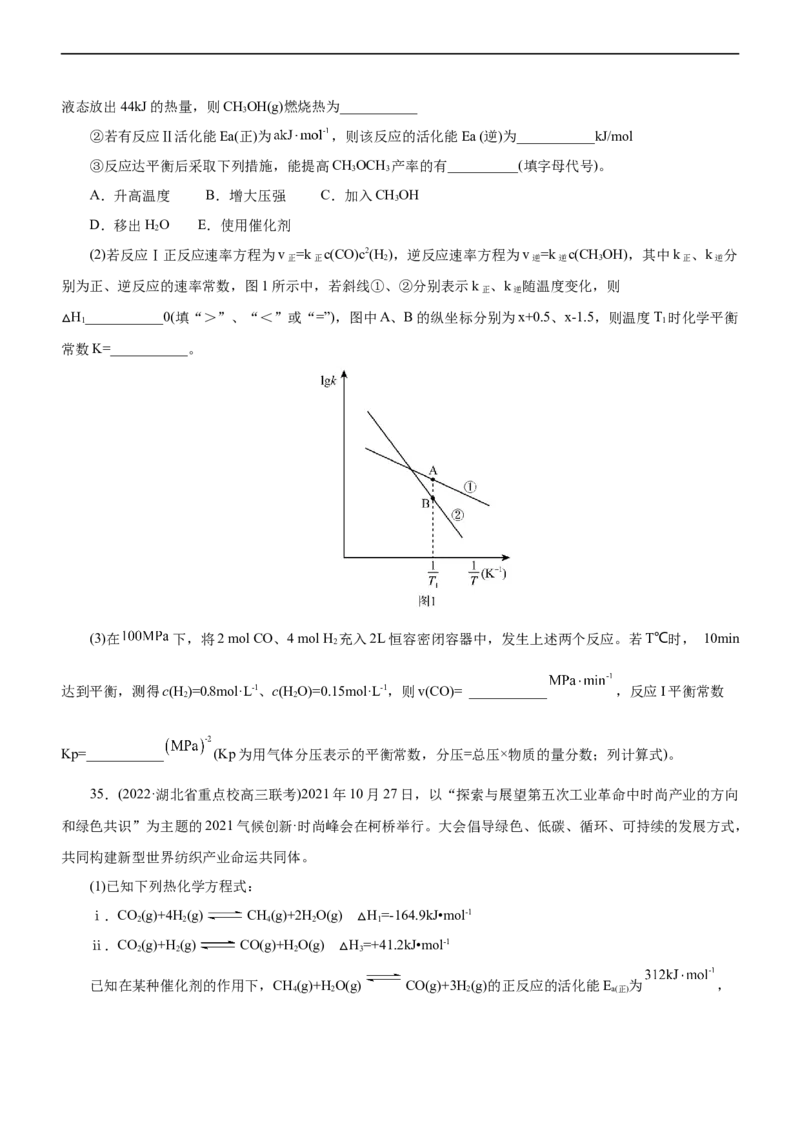
(2)若反应Ⅰ正反应速率方程为v =k c(CO)c2(H ),逆反应速率方程为v =k c(CHOH),其中k 、k 分
正 正 2 逆 逆 3 正 逆
别为正、逆反应的速率常数,图1所示中,若斜线①、②分别表示k 、k 随温度变化,则
正 逆
H___________0(填“>”、“<”或“=”),图中A、B的纵坐标分别为x+0.5、x-1.5,则温度T 时化学平衡
1 1
△常数K=___________。
(3)在 下,将2 mol CO、4 mol H 充入2L恒容密闭容器中,发生上述两个反应。若T℃时, 10min
2
达到平衡,测得c(H )=0.8mol·L-1、c(H O)=0.15mol·L-1,则v(CO)= ___________ ,反应I平衡常数
2 2
Kp=___________ (Kp为用气体分压表示的平衡常数,分压=总压×物质的量分数;列计算式)。
35.(2022·湖北省重点校高三联考)2021年10月27日,以“探索与展望第五次工业革命中时尚产业的方向
和绿色共识”为主题的2021气候创新·时尚峰会在柯桥举行。大会倡导绿色、低碳、循环、可持续的发展方式,
共同构建新型世界纺织产业命运共同体。
(1)已知下列热化学方程式:
ⅰ.CO(g)+4H(g) CH(g)+2HO(g) H=-164.9kJ•mol-1
2 2 4 2 1
ⅱ.CO
2
(g)+H
2
(g) CO(g)+H
2
O(g) H△3 =+41.2kJ•mol-1
△
已知在某种催化剂的作用下,CH(g)+HO(g) CO(g)+3H(g)的正反应的活化能E 为 ,
4 2 2 a(正)则该反应逆反应的活化能E 为___________kJ/mol。
a(逆)
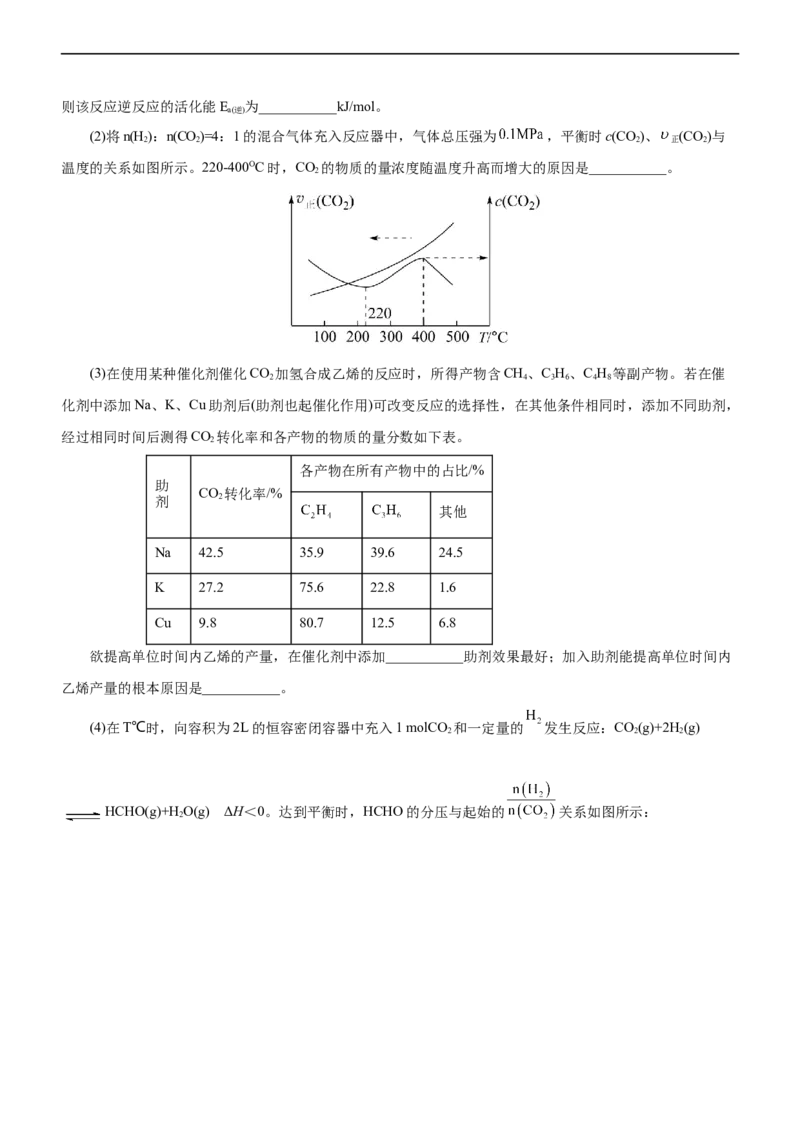
(2)将n(H ):n(CO)=4:1的混合气体充入反应器中,气体总压强为 ,平衡时c(CO)、 (CO)与
2 2 2 正 2
温度的关系如图所示。220-400OC时,CO 的物质的量浓度随温度升高而增大的原因是___________。
2
(3)在使用某种催化剂催化CO 加氢合成乙烯的反应时,所得产物含CH、C H、C H 等副产物。若在催
2 4 3 6 4 8
化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性,在其他条件相同时,添加不同助剂,
经过相同时间后测得CO 转化率和各产物的物质的量分数如下表。
2
各产物在所有产物中的占比/%
助
CO 转化率/%
剂 2
其他
Na 42.5 35.9 39.6 24.5
K 27.2 75.6 22.8 1.6
Cu 9.8 80.7 12.5 6.8
欲提高单位时间内乙烯的产量,在催化剂中添加___________助剂效果最好;加入助剂能提高单位时间内
乙烯产量的根本原因是___________。
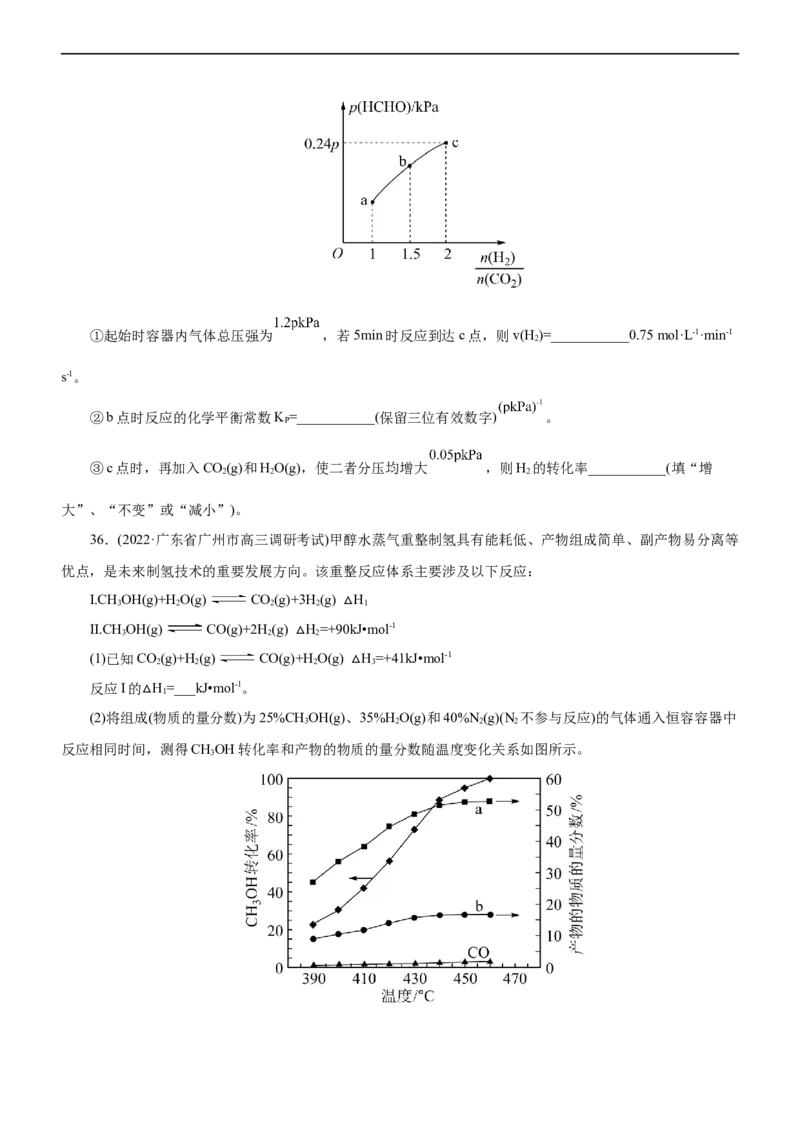
(4)在T℃时,向容积为2L的恒容密闭容器中充入1 molCO 和一定量的 发生反应:CO(g)+2H(g)
2 2 2
HCHO(g)+HO(g) ΔH<0。达到平衡时,HCHO的分压与起始的 关系如图所示:
2①起始时容器内气体总压强为 ,若5min时反应到达c点,则v(H )=___________0.75 mol·L-1·min-1
2
s-1。
②b点时反应的化学平衡常数K =___________(保留三位有效数字) 。
P
③c点时,再加入CO(g)和HO(g),使二者分压均增大 ,则H 的转化率___________(填“增
2 2 2
大”、“不变”或“减小”)。
36.(2022·广东省广州市高三调研考试)甲醇水蒸气重整制氢具有能耗低、产物组成简单、副产物易分离等
优点,是未来制氢技术的重要发展方向。该重整反应体系主要涉及以下反应:
I.CH OH(g)+H O(g) CO(g)+3H(g) H
3 2 2 2 1
II.CH
3
OH(g) CO(g)+2H
2
(g) H
2
=+90△kJ•mol-1
(1)已知CO
2
(g)+H
2
(g) CO(g)+△H
2
O(g) H
3
=+41kJ•mol-1
反应I的 H 1 =___kJ•mol-1。 △
(2)将组成△(物质的量分数)为25%CH
3
OH(g)、35%H
2
O(g)和40%N
2
(g)(N
2
不参与反应)的气体通入恒容容器中
反应相同时间,测得CHOH转化率和产物的物质的量分数随温度变化关系如图所示。
3①曲线a和b分别代表产物___和___。
②下列对甲醇水蒸气重整制氢反应体系的说法合理的有___。
A.增大N 的浓度,反应I、II的正反应速率都增加
2
B.移除CO 能提高CHOH的平衡转化率
2 3
C.升高温度,N 的物质的量分数保持不变
2
D.440℃~460℃时,升高温度,H 的产率增大
2
③反应I活化能小于反应II,结合图中信息解释判断依据___。
(3)一定条件下,向2L的恒容密闭容器中通入1molCH OH(g)和1molH O(g)发生上述反应,达到平衡时,
3 2
容器中CO 为0.8mol,CO为0.1mol,此时H 的浓度为___mol•L-1,反应I的平衡常数K=___(写出计算式)。
2 2
(4)研究发现以铜作催化剂时,反应I经历三步:
①CHOH→HCHO+H ,
3 2
②HCHO+H O→HCOOH+H ,
2 2
③___。
37.(2022·山东省潍坊市高三阶段联考)苯乙烯是一种重要的有机化工原料,可利用乙苯催化脱氢法制备。
实际生产中常在体系中充入一定量的CO,主要反应如下:
2
I.C H (g) C H(g)+H(g) ΔH=+117.6kJ·mol-1;
8 10 8 8 2 1
II.CO (g)+H(g) CO(g)+HO(g) ΔH=+41.2kJ·mol-1。
2 2 2 2
回答下列问题:
(1)一定温度下,向盛放催化剂的10L恒容密闭容器中充入2molC H (g)和1molCO (g)发生反应I和反应
8 10 2
II。20min末达到平衡,C H(g)、HO(g)的体积分数分别为25%和5%。
8 8 2
①0~20min内,用C H 的物质的量浓度变化表示的平均反应速率 (C H )=_______。
8 10 8 10
②起始投料量不变,在不同温度、压强下重复实验,测得H 的平衡体积分数与温度和压强的关系如图所
2
示。由图可知,温度低于T°C时,以反应_______(填“I”或“II”)为主,理由为_______;T°C时,三条曲线
0 1
几乎相交的原因为_______。
(2)催化脱氢过程中发生积碳反应: (g)→8C(s)+4H (g) ΔH=-126kJ·mol-1。积碳反应可
2 3
能导致的后果为_______(写一条即可)。
38.(2022·山东省潍坊市高三阶段联考)氮的氧化物是大气污染物之一,研究氮氧化物的反应机理对缓解环
境污染有重要意义,回答下列问题。
(1)已知:2NO(g)+O (g)=2NO (g) ΔH= -114 kJ·mol-1
2 2 1
C(s) +O (g) =CO (g) ΔH= -393.5 kJ·mol-1
2 2 2
N(g) +O (g) =2NO(g) ΔH= +181 kJ·mol-1
2 2 3
若某反应的平衡常数表达式为 ,请写出此反应的热化学方程式_______。
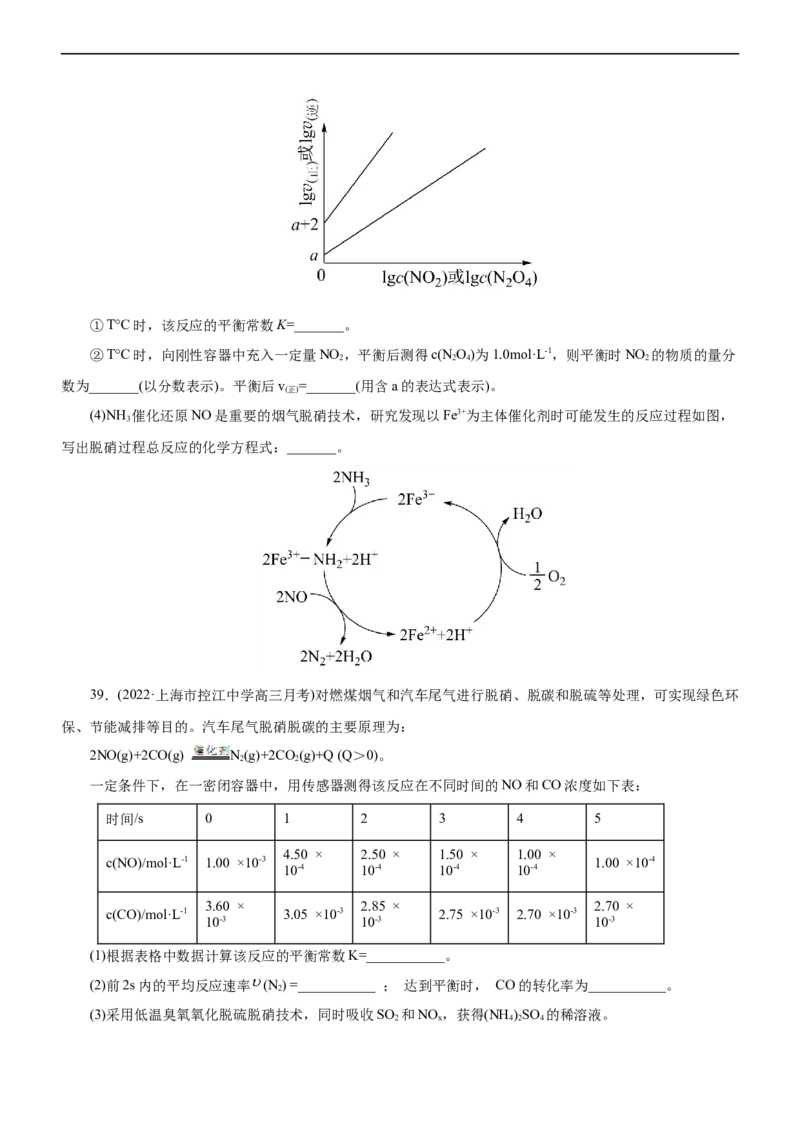
(2)对反应2NO(g)+2CO(g) N(g)+2CO (g) ΔH= -746.5 kJ·mol-1,分别在不同温度、不同催化剂下,保
2 2
持其它初始条件不变,重复实验,在相同时间内测得NO转化率与温度的关系如图所示。
在催化剂乙作用下,图中M点对应的速率(对应温度400°C)v _______v (填“>”、“<”或“=”),温度高于
(正) (逆)
400°C,NO转化率降低的原因可能是_______。
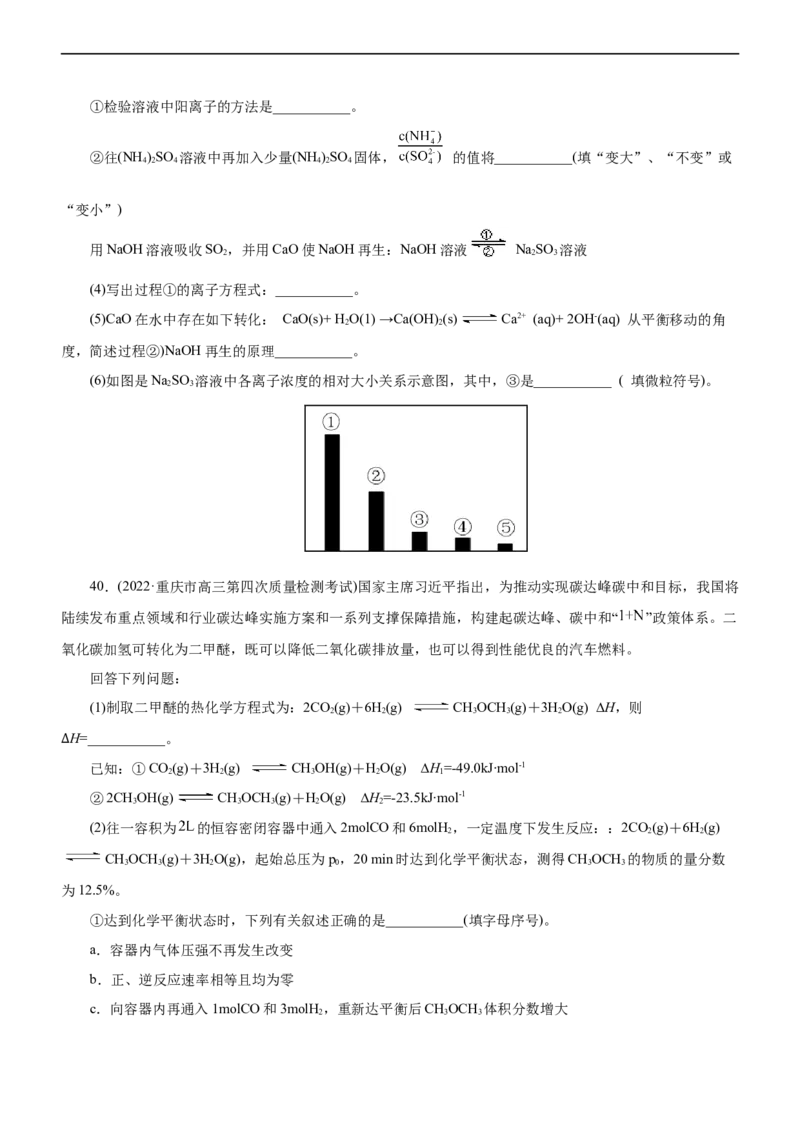
(3)T°C时,存在如下平衡:2NO (g) NO(g)。该反应正逆反应速率与NO 、NO 的浓度关系为:
2 2 4 2 2 4
v =k c2(NO ),v =k c(NO)(k 、k 是速率常数),且lgv ~lgc(NO )与lgv ~lgc(NO)的关系如图所示。
(正) 正 2 (逆) 逆 2 4 正 逆 (正) 2 (逆) 2 4①T°C时,该反应的平衡常数K=_______。
②T°C时,向刚性容器中充入一定量NO ,平衡后测得c(NO)为1.0mol·L-1,则平衡时NO 的物质的量分
2 2 4 2
数为_______(以分数表示)。平衡后v =_______(用含a的表达式表示)。
(正)
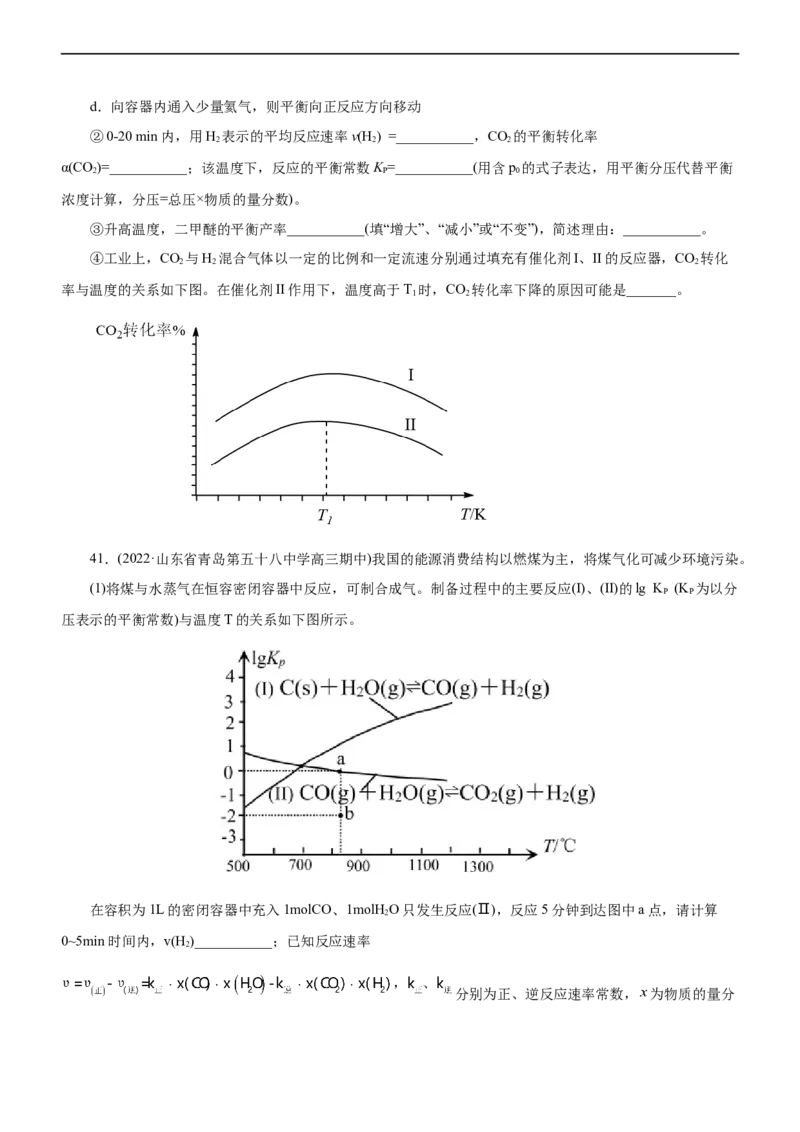
(4)NH 催化还原NO是重要的烟气脱硝技术,研究发现以Fe3+为主体催化剂时可能发生的反应过程如图,
3
写出脱硝过程总反应的化学方程式:_______。
39.(2022·上海市控江中学高三月考)对燃煤烟气和汽车尾气进行脱硝、脱碳和脱硫等处理,可实现绿色环
保、节能减排等目的。汽车尾气脱硝脱碳的主要原理为:
2NO(g)+2CO(g) N(g)+2CO (g)+Q (Q>0)。
2 2
一定条件下,在一密闭容器中,用传感器测得该反应在不同时间的NO和CO浓度如下表:
时间/s 0 1 2 3 4 5
4.50 × 2.50 × 1.50 × 1.00 ×
c(NO)/mol·L-1 1.00 ×10-3 1.00 ×10-4
10-4 10-4 10-4 10-4
3.60 × 2.85 × 2.70 ×
c(CO)/mol·L-1 3.05 ×10-3 2.75 ×10-3 2.70 ×10-3
10-3 10-3 10-3
(1)根据表格中数据计算该反应的平衡常数K=___________。
(2)前2s内的平均反应速率 (N ) =___________ ; 达到平衡时, CO的转化率为___________。
2
(3)采用低温臭氧氧化脱硫脱硝技术,同时吸收SO 和NO ,获得(NH )SO 的稀溶液。
2 x 4 2 4①检验溶液中阳离子的方法是___________。
②往(NH )SO 溶液中再加入少量(NH )SO 固体, 的值将___________(填“变大”、“不变”或
4 2 4 4 2 4
“变小”)
用NaOH溶液吸收SO ,并用CaO使NaOH再生:NaOH溶液 NaSO 溶液
2 2 3
(4)写出过程①的离子方程式:___________。
(5)CaO在水中存在如下转化: CaO(s)+ H O(1) →Ca(OH) (s) Ca2+ (aq)+ 2OH-(aq) 从平衡移动的角
2 2
度,简述过程②)NaOH再生的原理___________。
(6)如图是NaSO 溶液中各离子浓度的相对大小关系示意图,其中,③是___________ ( 填微粒符号)。
2 3
40.(2022·重庆市高三第四次质量检测考试)国家主席习近平指出,为推动实现碳达峰碳中和目标,我国将
陆续发布重点领域和行业碳达峰实施方案和一系列支撑保障措施,构建起碳达峰、碳中和“ ”政策体系。二
氧化碳加氢可转化为二甲醚,既可以降低二氧化碳排放量,也可以得到性能优良的汽车燃料。
回答下列问题:
(1)制取二甲醚的热化学方程式为:2CO(g)+6H(g) CHOCH(g)+3HO(g) ∆H,则
2 2 3 3 2
H=___________。
∆ 已知:①CO 2 (g)+3H 2 (g) CH 3 OH(g)+H 2 O(g) ∆H 1 =-49.0kJ∙mol-1
②2CHOH(g) CHOCH(g)+HO(g) ∆H=-23.5kJ∙mol-1
3 3 3 2 2
(2)往一容积为 的恒容密闭容器中通入2molCO和6molH ,一定温度下发生反应::2CO(g)+6H(g)
2 2 2
CHOCH(g)+3HO(g),起始总压为p,20 min时达到化学平衡状态,测得CHOCH 的物质的量分数
3 3 2 0 3 3
为12.5%。
①达到化学平衡状态时,下列有关叙述正确的是___________(填字母序号)。
a.容器内气体压强不再发生改变
b.正、逆反应速率相等且均为零
c.向容器内再通入1molCO和3molH ,重新达平衡后CHOCH 体积分数增大
2 3 3d.向容器内通入少量氦气,则平衡向正反应方向移动
②0-20 min内,用H 表示的平均反应速率v(H ) =___________,CO 的平衡转化率
2 2 2
α(CO)=___________;该温度下,反应的平衡常数K =___________(用含p 的式子表达,用平衡分压代替平衡
2 P 0
浓度计算,分压=总压×物质的量分数)。
③升高温度,二甲醚的平衡产率___________(填“增大”、“减小”或“不变”),简述理由:___________。
④工业上,CO 与H 混合气体以一定的比例和一定流速分别通过填充有催化剂I、II的反应器,CO 转化
2 2 2
率与温度的关系如下图。在催化剂II作用下,温度高于T 时,CO 转化率下降的原因可能是_______。
1 2
41.(2022·山东省青岛第五十八中学高三期中)我国的能源消费结构以燃煤为主,将煤气化可减少环境污染。
(1)将煤与水蒸气在恒容密闭容器中反应,可制合成气。制备过程中的主要反应(I)、(II)的lg K (K 为以分
P P
压表示的平衡常数)与温度T的关系如下图所示。
在容积为1L的密闭容器中充入1molCO、1molH O只发生反应(Ⅱ),反应5分钟到达图中a点,请计算
2
0~5min时间内,v(H )___________;已知反应速率
2
分别为正、逆反应速率常数, 为物质的量分数, ___________。
(2)煤气化过程中产生的有害气体HS可用足量的NaCO 溶液吸收,该反应的离子方程式为
2 2 3
___________(已知:K (H S)=9.1×10-8,K (H S)=11×10-12;K (H CO )=4.30×10-7,K (H CO)=5.61×10-11)
a1 2 a2 2 a1 2 3 a2 2 3
(3)已知:CO(g)+3HO(g) CO(g)+H(g) H=+ akJ·mol-1
2 2 2 1
2CO (g)+O
2
(g) 2CO
2
(g) H
2
= -b kJ·mol-△1
CH
4
(g)+CO
2
(g) 2CO(g)+2H△2 (g) H
3
=+ckJ·mol-1 (a、b、c均为正值)
则CO
2
(g)+2H
2
O(g) CH
4
(g)+2O
2
(g)△的△H
4
=___________ kJ·mol-1 (用a、b、c表示)。
(4)CO 还可制取CHOH(g)和水蒸气。将1molCO 和3molH 充入0.5L恒容密闭容器中,在两种不同催化
2 3 2 2
剂下发生反应,相同时间内CO 的转化率随温度变化曲线如图3所示:
2
①随温度的升高,CO 的转化率先增大后减小,理由是___________。
2
②已知c点容器内压强为P,在T 温度反应的平衡常数K 为___________(用含P的关系式表示)
5 p
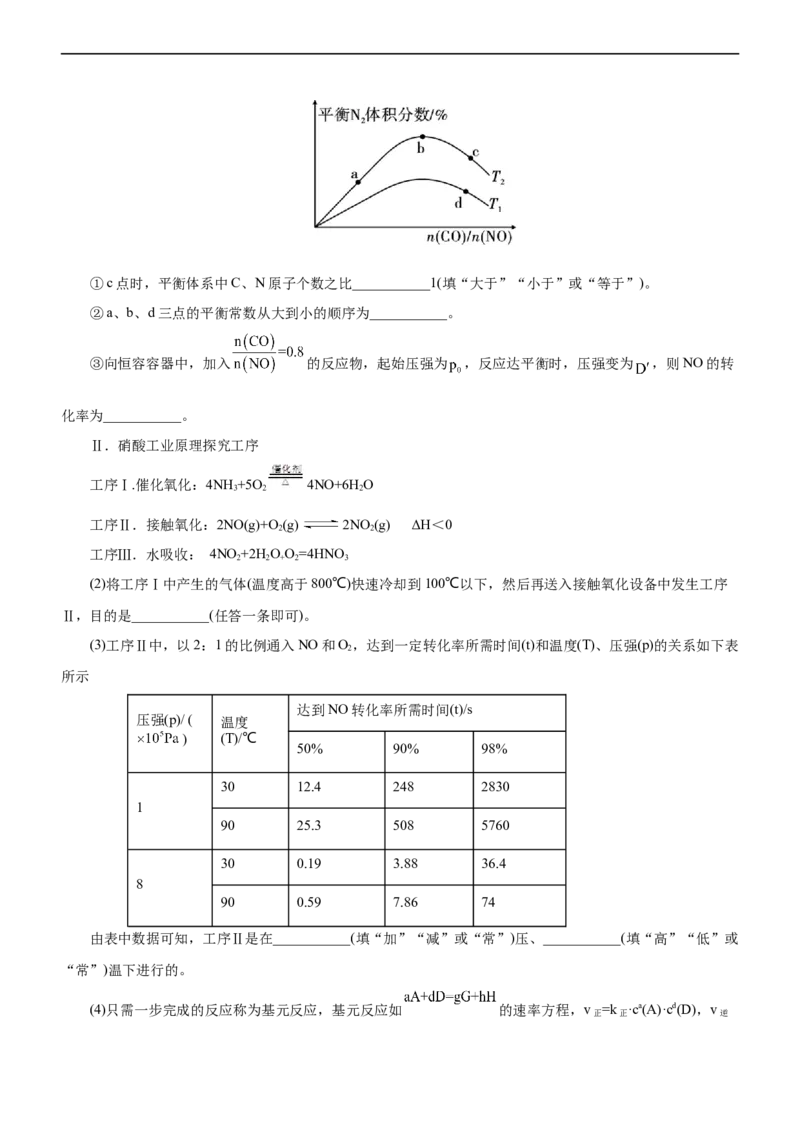
42.(2022·重庆一中高三半期考试)燃油汽车尾气中的NO、CO和硝酸工厂尾气的排放,是大气污染的主
要原因。
Ⅰ.燃油汽车尾气研究
燃油汽车发展史上,有人提出通过反应2NO(g)+2CO(g) N(g)+2CO(g)来处理汽车尾气。
2 2
(1)现将CO和NO按不同比例投入一密闭容器中,发生反应:2NO(g)+2CO(g) N(g)+2CO(g) H=
2 2
△
-746.8kJ•mol-1,反应达到平衡时, 的体积分数随 的变化曲线如图。①c点时,平衡体系中C、N原子个数之比___________1(填“大于”“小于”或“等于”)。
②a、b、d三点的平衡常数从大到小的顺序为___________。
③向恒容容器中,加入 的反应物,起始压强为 ,反应达平衡时,压强变为 ,则NO的转
化率为___________。
Ⅱ.硝酸工业原理探究工序
工序Ⅰ.催化氧化:4NH +5O 4NO+6H O
3 2 2
工序Ⅱ.接触氧化:2NO(g)+O(g) 2NO(g) ΔH<0
2 2
工序Ⅲ.水吸收: 4NO +2H O O=4HNO
2 2 + 2 3
(2)将工序Ⅰ中产生的气体(温度高于800℃)快速冷却到100℃以下,然后再送入接触氧化设备中发生工序
Ⅱ,目的是___________(任答一条即可)。
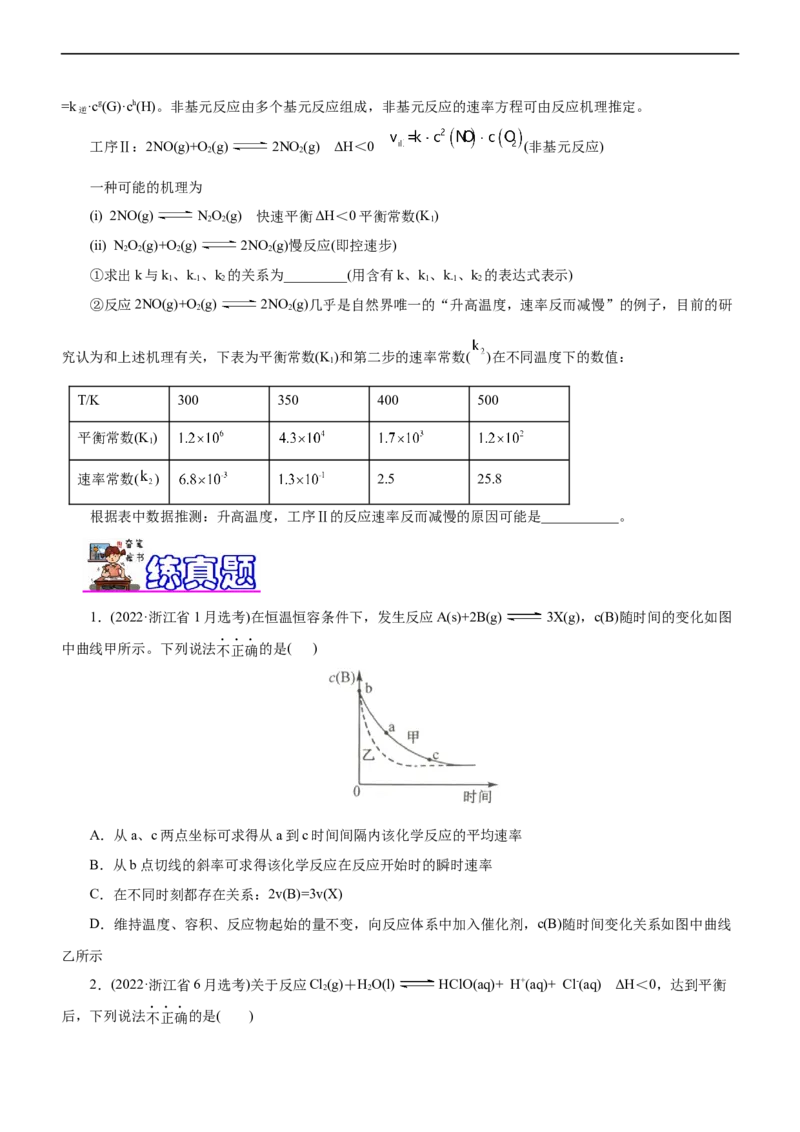
(3)工序Ⅱ中,以2:1的比例通入NO和O,达到一定转化率所需时间(t)和温度(T)、压强(p)的关系如下表
2
所示
达到NO转化率所需时间(t)/s
压强(p)/ ( 温度
) (T)/℃
50% 90% 98%
30 12.4 248 2830
1
90 25.3 508 5760
30 0.19 3.88 36.4
8
90 0.59 7.86 74
由表中数据可知,工序Ⅱ是在___________(填“加”“减”或“常”)压、___________(填“高”“低”或
“常”)温下进行的。
(4)只需一步完成的反应称为基元反应,基元反应如 的速率方程,v =k ·ca(A)·cd(D),v
正 正 逆=k ·cg(G)·ch(H)。非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。
逆
工序Ⅱ:2NO(g)+O(g) 2NO(g) ΔH<0 (非基元反应)
2 2
一种可能的机理为
(i) 2NO(g) NO(g) 快速平衡ΔH<0平衡常数(K )
2 2 1
(ii) NO(g)+O(g) 2NO(g)慢反应(即控速步)
2 2 2 2
①求出k与k、k 、k 的关系为_________(用含有k、k、k 、k 的表达式表示)
1 -1 2 1 -1 2
②反应2NO(g)+O(g) 2NO(g)几乎是自然界唯一的“升高温度,速率反而减慢”的例子,目前的研
2 2
究认为和上述机理有关,下表为平衡常数(K )和第二步的速率常数( )在不同温度下的数值:
1
T/K 300 350 400 500
平衡常数(K )
1
速率常数( ) 2.5 25.8
根据表中数据推测:升高温度,工序Ⅱ的反应速率反而减慢的原因可能是___________。
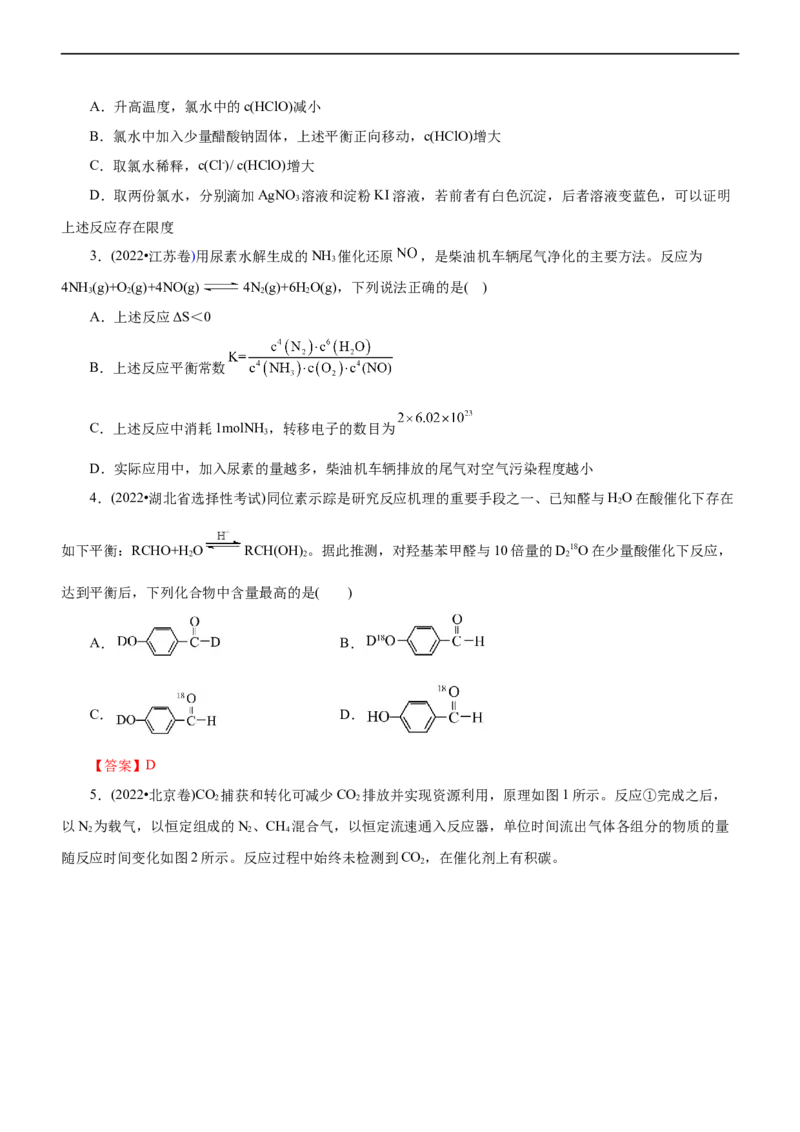
1.(2022·浙江省1月选考)在恒温恒容条件下,发生反应A(s)+2B(g) 3X(g),c(B)随时间的变化如图
中曲线甲所示。下列说法不正确的是( )
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间变化关系如图中曲线
乙所示
2.(2022·浙江省6月选考)关于反应Cl(g)+HO(l) HClO(aq)+ H+(aq)+ Cl-(aq) ΔH<0,达到平衡
2 2
后,下列说法不正确的是( )A.升高温度,氯水中的c(HClO)减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动,c(HClO)增大
C.取氯水稀释,c(Cl-)/ c(HClO)增大
D.取两份氯水,分别滴加AgNO 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明
3
上述反应存在限度
3.(2022•江苏卷)用尿素水解生成的NH 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
3
4NH (g)+O(g)+4NO(g) 4N(g)+6HO(g),下列说法正确的是( )
3 2 2 2
A.上述反应ΔS<0
B.上述反应平衡常数
C.上述反应中消耗1molNH ,转移电子的数目为
3
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
4.(2022•湖北省选择性考试)同位素示踪是研究反应机理的重要手段之一、已知醛与HO在酸催化下存在
2
如下平衡:RCHO+H O RCH(OH)。据此推测,对羟基苯甲醛与10倍量的D18O在少量酸催化下反应,
2 2 2
达到平衡后,下列化合物中含量最高的是( )
A. B.
C. D.
【答案】D
5.(2022•北京卷)CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,
2 2
以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质的量
2 2 4
随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2下列说法不正确的是( )
A.反应①为CaO+CO=CaCO;反应②为CaCO+CH CaO+2CO+2H
2 3 3 4 2
B.t ~ t ,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成 的速率为0,是因为反应②不再发生
3
6.(2022•广东选择性考试)恒容密闭容器中,BaSO(s)+4H(g) BaS(s)+4HO(g)在不同温度下达平
4 2 2
衡时,各组分的物质的量(n)如图所示。下列说法正确的是( )
A.该反应的ΔH<0
B.a为n(H O)随温度的变化曲线
2
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入BaSO,H 的平衡转化率增大
4 2
7.(2022•湖南选择性考试)向体积均为1L的两恒容容器中分别充入 和 发生反应:2X (g)+
Y(g) 2Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。
下列说法正确的是( )A.ΔH>0 B.气体的总物质的量:n<n
a c
C.a点平衡常数:K>12 D.反应速率:V <V
a正 b正
8.(2022·浙江省6月选考)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:2NH (g)
3
N(g)+3H(g),测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确的是
2 2
( )
A.实验①,0~20min,v(N )=1.00× 10-5mol/(L·min)
2
B.实验②,60min时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
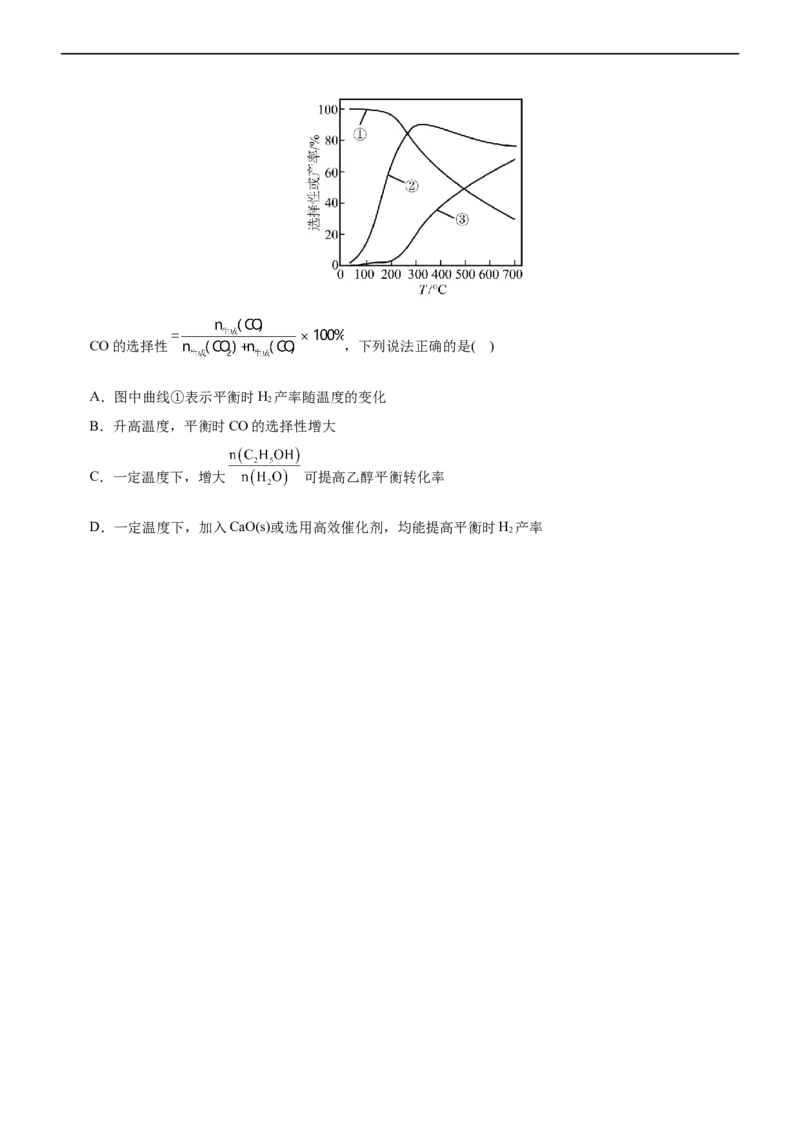
9.(2022•江苏卷)乙醇-水催化重整可获得H。其主要反应为
2
C HOH(g)+3H O(g)= 2CO (g)+6H(g) ΔH =173.3kJ·mol−1
2 5 2 2 2 2
CO(g)+H(g)= CO(g)+HO(g) ΔH =41.2kJ·mol−1
2 2 2 2
在 、n (C HOH):n (H O)=1:3时,若仅考虑上述反应,平衡时CO 和CO的选择性及H 的
始 2 5 始 2 2 2
产率随温度的变化如图所示。CO的选择性 ,下列说法正确的是( )
A.图中曲线①表示平衡时H 产率随温度的变化
2
B.升高温度,平衡时CO的选择性增大
C.一定温度下,增大 可提高乙醇平衡转化率
D.一定温度下,加入CaO(s)或选用高效催化剂,均能提高平衡时H 产率
2